Gerichte genuitschakeling BRAF synergetisch fotothermisch effect remt de groei van levercellen met behulp van nieuw GAL-GNR-siBRAF-nanosysteem
Abstract
Leverkanker is wereldwijd een van de meest voorkomende maligniteiten. De RAF-kinaseremmers zijn effectief bij de behandeling van hepatocellulair carcinoom (HCC); daarom is remming van de BRAF/MEK/ERK-route een nieuwe therapeutische strategie geworden voor nieuwe HCC-therapie. Gerichte specifieke toedieningssystemen voor tumoren vormen echter nog steeds een belangrijk obstakel voor klinische toepassingen. Galactose (GAL) kan zich richten op de asialoglycoproteïnereceptor (ASGPR) die sterk tot expressie wordt gebracht op leverkankercellen. In deze studie hebben we een nieuw multifunctioneel nanomateriaal GAL-GNR-siBRAF ontworpen dat uit drie delen bestaat, GAL als de leverkankergerichte groep, gouden nanostaafjes (GNR) die fotothermisch vermogen bieden onder bijna-infrarood licht, en siRNA dat specifiek BRAF tot zwijgen brengt (siBRAF). ). De nanodrager GAL-GNR-siBRAF vertoonde een hoge siRNA-laadcapaciteit en remde de afbraak van siRNA in serum. Vergeleken met naakte gouden nanostaafjes, bezat GAL-GNR-siBRAF een lagere biotoxiciteit en een hogere werkzaamheid van gene silencing. Behandeling met GAL-GNR-siBRAF verlaagde de expressie van BRAF aanzienlijk en verminderde proliferatie, migratie en invasie van leverkankercellen. Bovendien gaven combinatorische fotothermische effecten en BRAF-knockdown door GAL-GNR-siBRAF effectief aanleiding tot tumorceldood. Daarom ontwikkelde onze studie een nieuw type gericht multifunctioneel nanomateriaal GAL-GNR-siBRAF voor de behandeling van leverkanker, dat ideeën biedt voor de ontwikkeling van nieuwe klinische behandelmethoden.
Inleiding
Hepatocellulair carcinoom (HCC) is een groot wereldwijd gezondheidsprobleem [1]. Het is de zesde meest voorkomende vorm van kanker ter wereld en de derde belangrijkste doodsoorzaak door kanker [2, 3]. De meeste HCC-gevallen komen voor in Oost-Azië en Afrika bezuiden de Sahara. De incidentie is echter gestegen in sommige ontwikkelde landen, waaronder Frankrijk, Groot-Brittannië, Japan en de VS [4]. De standaardbehandeling voor vroege HCC is chirurgische resectie van de tumor. Na de operatie kan de 5-jaarsoverleving variëren van 89 tot 93% [5]. Helaas wordt slechts een klein percentage van de HCC-patiënten (ongeveer 20-30%) in een vroeg stadium gediagnosticeerd; de meeste HCC-patiënten (> 70%) bevinden zich in een vergevorderd stadium en kunnen geen chirurgische resectie ondergaan. Andere behandelingsopties zijn levertransplantatie, transkatheter arteriële chemo-embolisatie (TACE) en systemische chemotherapie [6]. Levertransplantatie wordt echter beperkt door het aanbod en onvolledige TACE-embolisatie kan leiden tot falen van de behandeling, met significante bijwerkingen van systemische chemotherapie en een slechte algehele prognose. Daarom zijn nieuwe behandelmethoden voor hepatocellulair carcinoom klinisch zeer veeleisend [7].
De RAS/RAF-signaleringsroute speelt een essentiële rol bij de ontwikkeling van leverkanker en BRAF is een van de essentiële met kanker geassocieerde genen in deze route. Genetische veranderingen in deze genen resulteren vaak in twee cascade stoornissen. Abnormale activering van de RAS/RAF-signaleringsroute is geassocieerd met een slechte prognose bij kankerpatiënten [8]. BRAF is het meest gemuteerde gen in de RAF-familie, en het richten op de RAS/RAF-route is een nieuwe therapeutische strategie voor de behandeling van HCC [8,9,10]. Aangezien is aangetoond dat de RAF-kinaseremmer sorafenib nuttig is bij de behandeling van HCC, zijn BRAF-mutaties het voorkeursdoelwit geworden voor HCC-therapie [8]. Meer specifiek zijn BRAF-mutaties een wenselijk doelwit geworden voor de behandeling van gevorderd HCC, aangezien de klinische ontwikkeling van de RAF-kinaseremmer sorafenib is gevonden bij HCC-behandeling in Azië, Europa en de VS [11]. Vergeleken met placebo verhoogde sorafenib de algehele overleving, waardoor de mediane algehele overleving van patiënten met gevorderde HCC werd verlengd [12,13,14]. Sorafenib heeft echter een slecht vermogen om tumoren te targeten, wat kan leiden tot nadelige bijwerkingen zoals hoge bloeddruk, haaruitval en misselijkheid [15]. Geneesmiddelen die gericht zijn op leverkanker met een hoge specificiteit en die RAF blokkeren, moeten nog verder worden onderzocht.
De asialoglycoproteïnereceptor (ASGPR), ook bekend als de levergalactosereceptor, is een C-type lectine dat tot expressie wordt gebracht op het sinusoïdale oppervlak van hepatocyten [16]. ASGPR wordt beschouwd als een essentieel doelwit voor levernanostructuren omdat het een belangrijke rol speelt bij de binding, internalisatie en eliminatie van stoffen met terminale galactoseresiduen [17]. Van verschillende monosachariden (galactose, mannose, lactose, N-acetylgalactosamine en siaalzuur) is gemeld dat ze in verschillende mate interageren met ASGPR, en galactose vertoonde een hogere affiniteit voor ASGPR [18]. Omdat ASGPR sterk wordt blootgesteld aan het oppervlak van hepatische parenchymale cellen [19], heeft de receptor een sterke affiniteit voor galactose en gegalactosyleerde prodrugs of afgiftesystemen die zich op de lever richten. Galactose-nanodeeltjes [20], galactose-micellen [21] en galactose-liposomen [22] zijn geïdentificeerd als medicijnsystemen die zich op de lever richten, die specifiek gericht zijn op hepatocellulaire carcinoïde cellen.
Gouden nanostaafjes (GNR) zijn staafvormige gouden nanodeeltjes die aanzienlijke voordelen hebben als nanodragers [23]. Gouden nanostaafjes (GNR) hebben een uitstekende biocompatibiliteit en kunnen worden gebruikt voor stabiele afgifte van siRNA [24]; ze hebben een groot specifiek oppervlak, wat flexibele modificatie van specifieke tumor-targeting adapters mogelijk maakt [25]; gelokaliseerde oppervlakteplasmonresonantie (LSPR) heeft een hoge fotothermische conversie-efficiëntie onder nabij-infraroodlichtbestraling en is een uitstekend fotothermisch antitumormateriaal geworden [26]. De maximale fotothermische efficiëntie kan worden bereikt door de beeldverhouding van de gouden nanostaafjes (GNR) aan te passen. De in vitro en in vivo toxiciteit van gouden nanodeeltjes hangt af van hun grootte, oppervlaktelading en oppervlaktecoating [27]. Cetyltrimethylammoniumbromide (CTAB) is echter een essentieel actief middel bij de synthese van gouden nanostaafjes, die duidelijke cytotoxiciteit heeft en biologische toepassingen beperkt [28].
RNA-interferentie (RNAi) is een veelbelovende benadering van kankerbehandeling geworden omdat het doelgenen effectief uitschakelt of tot zwijgen brengt door klein interfererend RNA (siRNA) [29]. Onlangs zijn siRNA-moleculen de proeffase bij de mens ingegaan en worden ze beschouwd als veelbelovende manieren om meerdere gemuteerde genkankers en tumoren te behandelen [30]. De toepassing van siRNA staat echter nog steeds voor enorme uitdagingen zoals seruminstabiliteit (afbraak door nucleasen in de extracellulaire omgeving) en off-target effecten [31]. Bovendien zijn siRNA's negatief geladen, waardoor ze niet kunnen binden aan negatief geladen celmembranen [32]. Vanwege deze kenmerken is het onwaarschijnlijk dat siRNA zelf rechtstreeks aan cellen wordt afgeleverd. De stabiliteit van siRNA kan worden verbeterd door chemische modificatie van siRNA of door siRNA-laders in beschermende dragermaterialen te plaatsen [33].
In deze studie hebben we nieuw een multifunctionele nanocarrier GAL-GNR-siBRAF gebouwd. Het systeem maakt gebruik van gouden nanostaafjes met optisch warmtegenererend vermogen als de binnenkern en extern gemodificeerde GAL (d-galactose) met specifieke targeting van levertumoren. Dit systeem verminderde de biologische toxiciteit van CTAB op het oppervlak van gouden nanostaafjes en vertoonde een hoge siRNA-laadcapaciteit en kan worden gebruikt om het BRAF-gen bij leverkanker effectief tot zwijgen te brengen. De toepassing van GAL-GNR-siBRAF verminderde proliferatie, invasie en migratie van leverkankercellen aanzienlijk. Bovendien induceerde de GAL-GNR-siBRAF gelijktijdig gen-uitschakeling van BRAF en fotothermische effecten die synergetische werkzaamheid bereikten bij het doden van tumorcellen, wat een nieuwe manier van denken opleverde voor de ontwikkeling van klinische behandeling van leverkanker.
Materiaal en methoden
Mobiele lijn
De muis hepatocellulaire carcinoom cellijn Hepa1-6 werd gekocht bij de Stem Cell Bank, Chinese Academy of Sciences. Cellen werden gekweekt in DMEM-medium (Life Technologies, Carlsbad, CA) dat 10% FBS bevat bij 37 ° C met 5% CO2 .
Synthese van BRAF-siRNA
De sequentie voor siRNA gericht op het BRAF-gen is 5'-GCUUACUGGAGAGGAGUUACA-3' en werd gesynthetiseerd door Dharmacon, Inc. (Lafayette, CO, VS). Het in de handel verkrijgbare gerichte luciferase-gen siGL2 werd gebruikt als een siRNA voor negatieve controle.
Synthese van CTAB-GNR
In water oplosbare gouden nanostaafjes werden gesynthetiseerd met behulp van een zaadgemedieerde groeiroute [34]. De zaadoplossing werd als volgt vervaardigd:1 mL cetyltrimethylammoniumbromide (CTAB) (0,2 M) (Sinopharm) werd voorzichtig gemengd met 1 mL HAuCl4 (0,5 mM) (Sinopharm). De oplossing geroerd bij 28 °C, grondig gemengd en 0,12 mL koud NaBH4 toegevoegd (0,01 M) (Sinopharm) totdat de verkregen zaadoplossing bruin werd en in reserve bleef. De groeioplossing werd vervolgens als volgt gesynthetiseerd:50 mL CTAB (0,2 M) en 50 mL HAuCl4 (1 mM), 2,5 mL AgNO3 (4 mM) (Sinopharm) werden licht gemengd bij 28 ° C. Na grondig mild mengen werd 670 L ascorbinezuur (0,079 M) toegevoegd wanneer de kleur van de oplossing zal veranderen van donkergeel in kleurloos. Honderdtwintig microliter van de zaadoplossing werd onder zacht roeren bij 28°C toegevoegd en de kleur werd geleidelijk transparant van paars tot paarszwart. Na 24 uur roeren bij constante temperatuur, werd de oplossing 10 min gecentrifugeerd bij 12.000 tpm om extra CTAB te verwijderen en vacuüm gevriesdroogd tot GNR-poeder voor toekomstig gebruik.
Synthese van MUA-PEI en GAL-PEI-MUA
Mercaptoundecaanzuur (MUA; 654 mg) werd opgelost in 30 mL chloroform (CHCl3 ) en vervolgens geïncubeerd met 100 mmol 1-ethyl-3-[3-dimethylaminopropyl] carbodiimide hydrochloride (EDC) en 100 mmol N-hydroxysuccinimide (NHS) gedurende 15 min bij kamertemperatuur. Vervolgens werd 100 mmol polyethyleenimine (PEI) aan de bovenstaande oplossing toegevoegd. Na een reactie van 24 uur bij kamertemperatuur werd een gelijk volume gedeïoniseerd water gebruikt om het in water oplosbare PEI-MUA te extraheren. Dezelfde methode werd gebruikt om de activering van d-galactose in waterige oplossing te voltooien. Vervolgens werd een overmaat geactiveerd d-galactose (500 mmol) toegevoegd aan de bovengenoemde in water oplosbare PEI-MUA-oplossing, en de reactie werd voldoende uitgevoerd bij kamertemperatuur gedurende 24 u om een in water oplosbare GAL-PEI-MUA te verkrijgen complex.
Synthese van GAL-PEI-MUA-GNR (GAL-GNR) en PEI-MUA-GNR (PEI-GNR)
Gevriesdroogd CTAB-GNR-poeder (10 mg) werd gesuspendeerd in 10 mL in water oplosbare PEI-MUA- of GAL-PEI-MUA-complexen. CTAB werd vervangen door Au-S-binding bij 24 uur roeren bij kamertemperatuur. De oplossing werd 15 min bij 12.000 tpm gecentrifugeerd om overtollig supernatant te verwijderen, en het neerslag werd driemaal gewassen met gedestilleerd water. PEI-GNR- of GAL-GNR-poeders werden bereid door vriesdrogen, gewogen en opgelost in niet-ribozymwater, en vervolgens werd het plasmaresonantie-effect waargenomen door een multifunctionele enzymanalysator (Spectra Max M5e, MD, VS).
Transmissie-elektronenmicroscopie
De GNR of GAL-GNR werd gesuspendeerd in gedestilleerd water en de hersuspensie werd op een koperen rooster geplaatst. Nadat de monsters op het kopergaas 30 min grondig aan de lucht waren gedroogd, werd het kopergaas afgebeeld met behulp van een transmissie-elektronenmicroscoop (LIBRA 120, Carl Zeiss, Duitsland).
Ultraviolet-zichtbare analyse
De GNR, PEI-GNR of GAL-GNR werd gesuspendeerd in gedestilleerd water. Het oppervlakte-plasmonresonantie-effect van nanomaterialen in het golflengtebereik van 600 tot 900 nm werd onderzocht met behulp van een multifunctionele microplaatlezer (SpectraMax M5e, MD, VS).
Zeta-potentiaal- en hydrodynamische diameteranalyse
De GNR, PEI-GNR of GAL-GNR werd gesuspendeerd in gedestilleerd water en vervolgens werden de zeta-potentiaal en hydrodynamische diameter van het nanomateriaal gemeten op een Zetasizer Nano ZS.
Nucleaire magnetische resonantieanalyse
Het GAL-GNR gevriesdroogde poeder werd opgelost in zwaar water (99%, Sigma) om een homogene suspensie te maken, en de suspensie werd vervolgens overgebracht naar een NMR-monsterbuis. De samenstelling van GAL-GNR werd bepaald door nucleaire magnetische resonantie (NMR) (Bruker, 600 mhz, Duitsland).
Gelverschuivingstest
GAL-GNR en siBRAF werden gemengd volgens de massaverhouding (0:1, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1). Na 30 min incubatie bij kamertemperatuur werd de DNA-laadbuffer aan het mengsel toegevoegd. Alle monsters werden toegevoegd aan 2% agarosegel die 0, 01% Goldview (Bioshop, VS) bevat en vervolgens gedurende 30 min bij 90 V geëlektroforeerd. De mate van siBRAF-verpakking werd gevisualiseerd op het gelbeeldvormingssysteem.
Stabiliteit van siRNA in serum
Het mengsel van GAL-GNR-siBRAF (6:1) werd geïncubeerd in vers muizenserum bij 37 ° C gedurende respectievelijk 0 uur, 3 uur, 6 uur, 12 uur, 24 uur en 48 uur. De naakte groep siBRAF plus verse muizenserum werd onder dezelfde omstandigheden behandeld. Een gelijk volume 2% natriumdodecylsulfaat (SDS) werd toegevoegd aan de GAL-GNR-siBRAF-oplossing. Na incubatie gedurende 30 min bij kamertemperatuur werd DNA-laadbuffer toegevoegd en werden alle monsters op een 2% agarosegel geladen (die 0,02% Goldview (Bioshop, VS) bevat) en gedurende 30 min bij 90 V geëlektroforeerd. De striphelderheid van de siBRAF werd gevisualiseerd op een gelbeeldvormingssysteem.
Competitive Inhibition Assay van GAL-GNR-siBRAF
2 × 10 5 Hepa1-6-cellen werden 's nachts gekweekt in microplaten met 12 putjes. Vervolgens werden de cellen gedurende 12 uur voorbehandeld met Lactobionzuur en vervolgens gedurende 30 min getransfecteerd met GAL-GNR--siBRAF (Cy3-gelabeld). De intracellulaire fluorescentie-intensiteit werd bepaald met een fluorescentiemicroscoop (schaalbalk =200 m).
Op leverkanker gerichte leveringscapaciteit van GAL-GNR-siBRAF
Eén microgram cy3-gelabeld siBRAF werd gedurende 20 min bij kamertemperatuur geïncubeerd met PEI-GNR (30 g / ml), GAL-GNR (30 g / ml) en vervolgens toegevoegd aan de media van Hepa1-6-cellen. Na incubatie gedurende 30 min werden de cellen driemaal gewassen met 50% FBS en werd de fluorescentie-intensiteit in de cellen gemeten onder een fluorescentiemicroscoop.
Fotothermische effecten
Twintig, 40, 60, 80 en 100 g GAL-GNR en 100 μg GNR gevriesdroogd poeder werden grondig opgelost in 1 mL gedestilleerd water. De oplossing werd toegevoegd aan een plaat met 24 putjes en continu bestraald met 803 nm nabij-infrarood laserbron (2 W/cm 2 ) gedurende 15 min. De temperatuur van elke groep werd de eerste 5 min om de 0,5 min gemeten met een infraroodthermometer en vervolgens werd de temperatuur elke 1 min aangegeven.
MTT-assay
Tweehonderd microliter cellen (3,5 × 10 4 /mL) werd gedurende 24 h gekweekt in microplaten met 96 putjes en vervolgens gekweekt met verschillende concentraties GNR of GAL-GNR (0, 15, 30, 45, 60, 75, 90, 105, 120 g/mL). Na 24 of 48 u incubatie werd 20 L MTT aan het kweeksysteem toegevoegd en nog eens 4 u geïncubeerd. De paarse kristallen werden opgelost in 150 μL DMSO, gevolgd door spectrofotometrische analyse bij 490 nm met behulp van een referentie van 650 nm in een microplaatlezer (SpectraMax M5e, MD, VS).
Calceïne-AM- en PI-kleuringstest
Hepa1-6 cellen (1,5 × 10 5 ) werden overnacht in een 12-wells plaat bewaard en behandeld met PBS, laser, GAL-GNR-siBRAF (30 g/mL:1 g), GAL-GNR-siGL2 (30 g/mL:1 g) + laser of GAL -GNR-siBRAF (30 μg/mL:1 μg) + laser gedurende 4 h, en vervolgens bestraald met nabij-infrarood licht (808 nm, 2 W/cm 2 ) gedurende 15 min. De cytotoxiciteit van GAL-GNR werd gedetecteerd door calceïne-AM (levende cellen) en PI (dode cellen) kleuringsexperimenten. Groene fluorescentie van calceïne-AM en rode fluorescentie van PI werden gefotografeerd onder fluorescentiemicroscopie.
Realtime kwantitatieve PCR
Totaal cellulair RNA werd geëxtraheerd met behulp van Trizol (Trizol-reagens, Invitrogen) en gebruikt als een matrijs voor cDNA-synthese. Q-PCR werd uitgevoerd met behulp van genspecifieke voorwaartse en achterwaartse primers (elk 0, 5 L x 10 μM) in het Stratagene Mx3000P qRT-PCR-systeem (Agilent Technologies, Lexington, MA, VS). SYBR groene PCR MasterMix (Life Technologies) werd gebruikt volgens het schema van de fabrikant. Huishoudgen β-actine werd gebruikt als een interne referentie. De primersequenties waren β-actine:5'AGGGAAATCGTGCGTGACATCAAA-3' (voorwaarts) en 5'ACTCATCGTACTCCTGCTTGCTGA-3' (omgekeerd); BRAF:5'-CAATTGGCTGGGACACGGACAT-3' (vooruit) en 5'-TTGACAACGGAAACCCTGGAAAAG-3' (achteruit). Het verschil in genexpressie werd berekend en weergegeven door 2 −∆∆Ct methode.
Western Blot
Het totale eiwit van Hepa1-6-cellen werd verkregen door RIPA-buffer (Cell signaling, Pickering, Ontario, Canada) en gekwantificeerd door bicinchoninezuur (BCA). Eiwit werd gescheiden in 12% SDS-PAGE en overgebracht naar polyvinylideenfluoride (PVDF). Het huishoudgen β-actine werd gebruikt als een interne referentie om BRAF-eiwitexpressie te detecteren. De eiwitband en interne referentie van het doeleiwit werden gedetecteerd door ECL-chemiluminescentie.
Krastest
De getransfecteerde Hepa1-6 (1,7 × 10 5 /mL) cellen werden overnacht in platen met 12 putjes gezaaid. Cellen die volledig aan de plaat hechtten, werden bekrast met een pipetpunt van 10 L. De cellen werden tweemaal gewassen met PBS en vervangen door medium dat 2% FBS bevatte. Het gemiddelde van de wondlijn werd waargenomen onder een microscoop na 0, 24 en 48 h. Elke krastest werd in drievoud uitgevoerd.
Transwell-assay voor migratie en invasie
Transwell-kamers van acht micrometer (Corning Life Science) werden gebruikt om celmigratie en invasie te beoordelen. Hepa1-6 gesuspendeerd in 200 μL serumvrij medium werd toegevoegd aan de bovenste kamers met een dichtheid van 1,7 × 10 5 ml cellen / putje, en vervolgens werd 500 L medium met 12% FBS toegevoegd aan de onderste kamer. Na incubatie gedurende 24-48 h werden de cellen gedurende 30 min gefixeerd met een 4% paraformaldehyde-oplossing en vervolgens werden de cellen gekleurd met een 1% kristalviolette oplossing gedurende 30 min. Ten slotte werden de cellen gefotografeerd en geteld onder een omgekeerde microscoop. Voor de celinvasie-assay vereisen celinvasie-experimenten ECM-gelcoating en de resterende stappen zijn consistent.
Statistieken
Alle experimenten werden in drievoud uitgevoerd. Gegevens werden uitgedrukt als gemiddelde ± SD en Student's t test (tweezijdig) om het verschil tussen de twee methoden te bepalen. Een one-way ANOVA-test werd gebruikt voor het vergelijken van meerdere groepen. Gegevens werden als statistisch significant beschouwd bij p <0,05 (*p <0,05, **p <0,01, ***p <0,001).
Resultaten
Synthese en karakterisering van Nanocarrier GAL-GNR-siBRAF
We hebben een nieuwe nanodrager GAL-GNR ontworpen die in staat is om klein interfererend RNA (siRNA) aan de levercellen te leveren en tegelijkertijd het fotothermische effect van de gouden nanostaafjes te behouden. De syntheseprocedure van GAL-GNR wordt getoond in Schema 1. Dit op de lever gerichte systeem bevat drie functionele componenten. Ten eerste is het basisdeel van GAL-GNR een GNR-skelet, dat ongeveer 30 nm lang en 10 nm in diameter is, zoals getoond in het TEM-beeld (Fig. 1a) en chemisch geconjugeerde GNR (GAL-GNR) vertoonde geen significante dimensionale verandering en bezat nog steeds een goede dispergeerbaarheid (figuur 1b). De gegevens van de deeltjesgrootte toonden aan dat de gemiddelde grootte van GNR 30,23 nm was, wat consistent was met de resultaten van elektronenmicroscopie, en dat de grootte van GAL-GNR (50 nm) en PEI-GNR (42,35 nm) groter was dan GNR sinds de conjugatie van GAL en PEI verhoogde de hydratatie tussen deeltjes (figuur 1c). Ten tweede werd biologisch toxisch CTAB op het oppervlak van GNR vervangen door positief geladen MUA-PEI dat kan worden geladen met negatief geladen siRNA. De zeta-potentiaalmeting toonde aan dat de oppervlaktelading van GNR toenam van 35,6 tot 42,7 mV of 41,8 mV wanneer de GNR werd gemodificeerd met respectievelijk PEI of GAL-PEI, wat aangeeft dat GAL-GNR een sterk vermogen bezat om siRNA te binden (Fig. 1d). Ten derde hebben we GAL toegepast als een gidsmolecuul om GNR-nanodragers te conjugeren, die kunnen worden gebruikt voor specifieke homing van hepatocellulair carcinoom. UV-Vis-absorptiespectroscopie werd gebruikt om de structuur van gemodificeerde GNR voorlopig te detecteren. De initiële absorptiespectrumgolflengte van ongewijzigde GNR was 763 nm; een verschuiving van 7 nm in golflengte werd aanvankelijk waargenomen met de MUA-PEI-modificatie en een andere verschuiving van 8 nm werd waargenomen aan het einde van de synthese, toen de modificatie van GNR met GAL met succes werd uitgevoerd (figuur 1e). Om GAL in het nanosysteem te bevestigen, werd NMR-beeld gebruikt om de chemische groepen te analyseren. De resultaten toonden aan dat het H-signaal van galactose alleen werd gevonden in het GAL-GNR-spectrum op het NMR-waterstofspectrum, dat δ was:3,60, 3,65, 3,70, 3,78, 3,90, 4,53. NMR-spectra bevestigden de chemische structuur van GAL, waarin GAL met succes werd geconjugeerd aan het GNR-oppervlak (Fig. 1f).
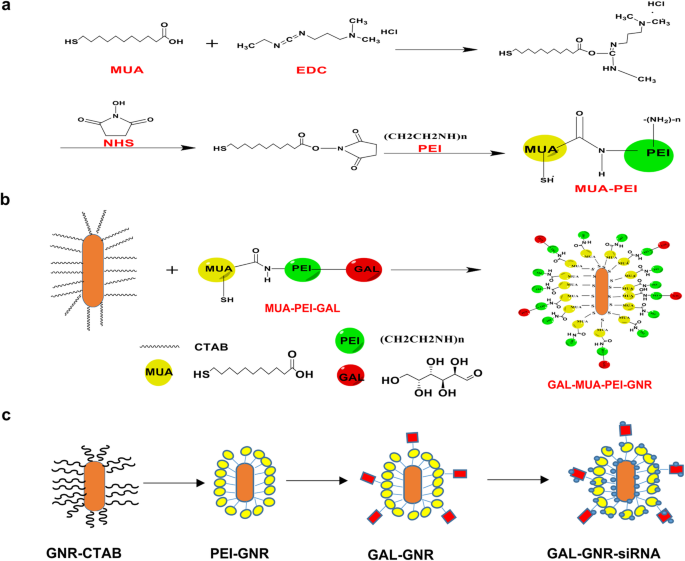
GAL-GNR synthetische procedure. een Het synthetische proces van MUA-PEI. b Activering van d-galactose en chemische reactie met MUA-PEI. c Het uiteindelijke synthetische product van GAL-GNR
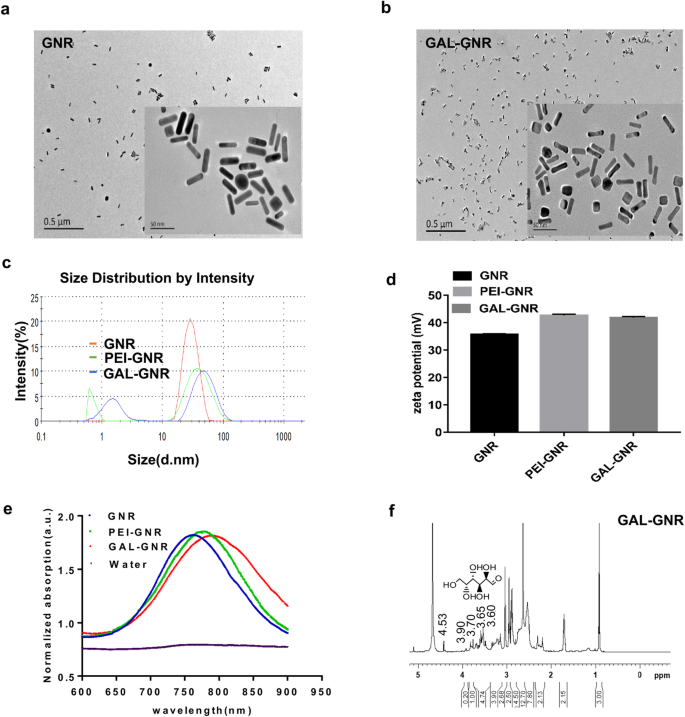
Karakterisering van GNR en GAL-GNR. een TEM-microfoto van GNR (schaal =0,5 m/50 nm). b TEM-microfoto van GAL-GNR (schaal =0,5 m / 50 nm). c Deeltjesgrootteanalyse van verschillende gemodificeerde GNR. d Zeta-potentiaalanalyse van verschillende gemodificeerde GNR (GAL-GNR). e Genormaliseerde UV-Vis-absorptiespectra van verschillende gemodificeerde GNR en water. v NMR-absorptiespectra van GAL-GNR
siRNA-inkapselingsvermogen en stabiliteit van GAL-GNR
Het GAL-GNR nanoskelet werd gemodificeerd door positief geladen PEI, dat kan worden gecombineerd met negatief geladen siRNA door middel van elektrostatische interactie. We gebruikten gel shift-assay om het siRNA-bindend vermogen van GAL-GNR te evalueren. Het vrije siRNA kan langs de doorgang van de gel bewegen, terwijl het gebonden siRNA wordt vertraagd of volledig wordt gestopt. Bovendien zal het gebonden siRNA niet langer effectief binden aan bromide, en dus zal de fluorescentie-intensiteit dienovereenkomstig afnemen. Het resultaat van gelelektroforese toonde aan dat de optimale verhouding voor het verzadigen van GAL-GNR met siBRAF 6:1 (w/w) is (Fig. 2a).
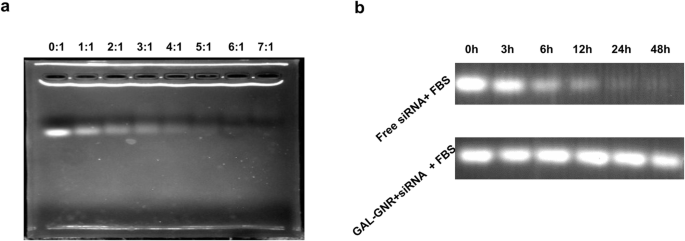
Gel shift-assays. een siRNA-laadcapaciteit van GAL-GNR. Eén microgram siRNA werd in gelijke volumes gemengd met verschillende massaverhoudingen van GAL-GNR. Na incubatie gedurende 30 min werd een gelmigratietest gebruikt om de siRNA-laadcapaciteit van GAL-GNR te beoordelen. b Stabiliteit van siRNA in muizenserum. Eén microgram BARF-siRNA werd geïnoculeerd met de GAL-GNR in een massaverhouding van 1:6 en werd vervolgens toegevoegd aan vers muizenserum. Na reactie van 0, 3, 6, 12, 24 en 48 h bij 37 °C, werd siRNA van GAL-GNR-siBARF geëxtraheerd met 2% SDS en gevisualiseerd met Ethidium Bromide
Naakt siRNA is zeer afbreekbaar, vooral in vivo. Een belangrijke functie van het afgiftesysteem is het beschermen van siRNA tegen afbraak. We hebben dus het beschermende effect van nanocarrier GAL-GNR op siRNA in vers serum getest. In vergelijking met het naakte siRNA werd het gebonden siRNA gedurende langere tijd in serum bewaard. Zoals getoond in Fig. 2b, kon naakt siRNA tot 12 uur in serum voorkomen, terwijl het gebonden siRNA na 48 uur nog steeds overvloedig aanwezig was. Het resultaat toonde aan dat GAL-GNR effectief kan voorkomen dat siRNA wordt afgebroken in serum, waardoor gerichte levering in vivo wordt gegarandeerd.
Cytotoxiciteit van nanomaterialen
Lage biologische toxiciteit is een andere belangrijke eigenschap van nanomaterialen, waardoor ze kunnen worden gebruikt bij de behandeling van kanker. Om de biocompatibiliteit van deze nieuwe GAL-GNR-nanostructuur te evalueren, hebben we de cytotoxiciteit ervan getest. Zoals getoond in Fig. 3, werden dode cellen van Hepa1-6 in de niet-gemodificeerde GNR-behandelde groep aanvankelijk waargenomen bij een lage concentratie van 30 g/ml. Na incubatie met 75 g/mL GNR gedurende 24 h, was het celsterftecijfer tot 56,09% en de mortaliteit nam toe tot 75,5% na incubatie gedurende 48 h. Integendeel, GAL-modificatie verminderde de cytotoxiciteit aanzienlijk. Na 48 h incuberen van GAL-GNR waren meer dan 80% cellen nog in leven, zelfs bij hoge concentratie (105 μg/ml). Deze gegevens suggereerden dat de nanodrager GAL-GNR een hoge biocompatibiliteit had in vergelijking met GNR, wat de veiligheid van de toepassing garandeert.
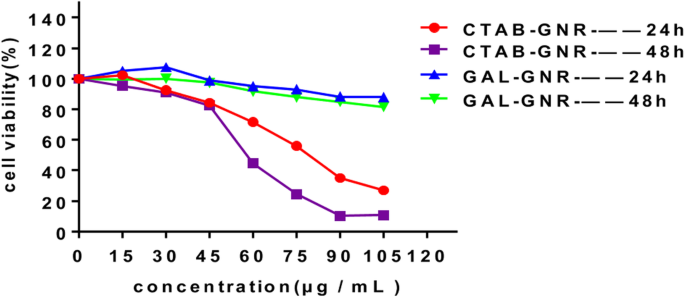
Toxiciteit van GAL-GNR. Hepa1-6-cellen werden gedurende 24 of 48 h bij de aangegeven concentraties behandeld met GNR (CTAB-GNR) of GAL-GNR. De levensvatbaarheid van de cellen werd gemeten met MTT-assay (n =5)
Hepatomacellen-gerichte levering van siRNA en gen-uitschakeling van BRAF in vitro
Het vermogen om siRNA in kankercellen af te geven is een van de belangrijkste functies van nanomaterialen. Om het potentieel van GAL-GNR bij siRNA-afgifte te onderzoeken, hebben we de werkzaamheid van gen-uitschakeling gedetecteerd met behulp van siBRAF geladen door GAL-GNR in Hepa1-6-cellen. Vergeleken met de blanco groep heeft de expressie van BRAF in met GAL-GNR-siGL2 (negatieve controle) getransfecteerde cellen geen verandering, terwijl de met GAL-GNR-siBRAF getransfecteerde cellen een significante afname hadden (Fig. 4a). Bovendien was het silencing-effect dosisafhankelijk, wat gecorreleerd is met de toename van de GAL-GNR-concentratie. De qPCR-resultaten toonden aan dat de ideale getransfecteerde concentratie van GAL-GNR-siBRAF 30 g/ml was, en de silencing-efficiëntie kan oplopen tot 90,29%, wat vergelijkbaar was met de groep van lipofectamine 2000 (positieve controle). Het resultaat van western blot was consistent met qPCR en de eiwitexpressie van BRAF werd neerwaarts gereguleerd na 48 h transfectie (Fig. 4b).
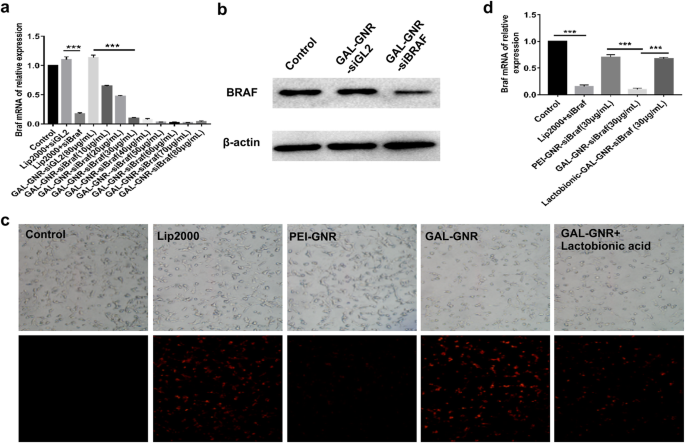
Hepatoomcel-gerichte levering van siRNA en gen-uitschakeling van BRAF in vitro. een Het mRNA van BRAF-expressie na GAL-GNR-siBRAF-transfectie. Hepa1-6-cellen werden gedurende 24 uur getransfecteerd met verschillende concentraties GA-GNR met dezelfde hoeveelheid BRAF-siRNA (1 g). De expressie van BRAF-mRNA werd bepaald met qPCR. De foutbalk vertegenwoordigt de standaarddeviatie van drie experimenten (***p <0,001). b De eiwitexpressie van BRAF in Hepa1-6 na GAL-GNR-siBRAF-transfectie. Hepa1-6-cellen werden gedurende 48 uur getransfecteerd met GAL-GNR-siBRAF, GAL-GNR-siGL2 of PBS, de niveaus van BRAF en β-actine werden bepaald door Western-blot. c en d Op leverkanker gericht leveringsvermogen van GAL-GNR-siBRAF. Eén microgram cy3-gelabeld siBRAF werd gedurende 20 min bij kamertemperatuur geïncubeerd met lip2000, PEI-GNR (30 g/ml), GAL-GNR (30 g/ml) en vervolgens toegevoegd aan de media van Hepa1-6-cellen. Voor een competitieve remmingstest werden Hepa1-6-cellen een nacht voorbehandeld met Lactobionzuur. De intracellulaire fluorescentie-intensiteit werd waargenomen onder de fluorescentiemicroscoop (schaalbalk =200 m), en de mRNA-expressies van BRAF werden gekwantificeerd door q-PCR. De foutbalk vertegenwoordigt de standaarddeviatie van drie experimenten (*p <0,05)
Lactobionzuur is qua structuur vergelijkbaar met GAL en kan competitief worden gecombineerd met de asialoglycoproteïnereceptor (ASGPR) die tot expressie wordt gebracht op het oppervlak van het celmembraan van hepatocellulair carcinoom [35]. Om de specifieke doelgerichtheidsefficiëntie van GAL-GNR te bevestigen, werden Hepa1-6-cellen vooraf geïncubeerd met lactobionzuur en vervolgens getransfecteerd met GAL-GNR-siBRAF. Onbehandelde cellen werden gebruikt als blanco controle en klassiek transfectiereagens lipofectamine 2000 werd gebruikt als positieve controle. Zoals getoond in Fig. 4c, was de rode fluorescentie-intensiteit van GAL-GNR-getransfecteerde cellen vergelijkbaar met de positieve controlegroep, terwijl de fluorescentie-intensiteit van PEI-GNR-getransfecteerde cellen significant verminderd is. Aan de andere kant werden cellen getransfecteerd met alleen GAL-GNR-siBRAF waargenomen sterkere rode fluorescentie van Cy3 dan Hepa1-6-cellen die waren voorbehandeld met lactobionzuur (Fig. 4c), en het resultaat van qPCR was consistent met dat van rode fluorescentieresultaten ( Afb. 4d). Deze resultaten illustreerden verder dat GAL de endocytose van siRNA door Hepa1-6-cellen effectief bevorderde en kan worden toegepast als een gericht deel van HCC.
De impact van GAL-GNR-siBRAF op proliferatie, migratie en invasie van Hepa1-6-cellen
BRAF speelt een belangrijke rol in de MAPK-route, die verantwoordelijk is voor het reguleren van celproliferatie, migratie en invasie [36]. Om de impact van GAL-GNR-siBRAF op hepatocellulaire carcinoomcellen te beoordelen, analyseerden we eerst de celproliferatie door MTT-assays. Zoals getoond in Fig. 5a, was de proliferatie van met GAL-GNR-siBRAF getransfecteerde hepa1-6-cellen significant verminderd in vergelijking met de GAL-GNR-siGL2 (negatieve controle) of PBS-behandelde cellen. Vervolgens hebben we het effect van GAL-GNR-siBRAF op celmigratie onderzocht door middel van scratch- en transwell-assays. Compared with negative control cells, the migration ability of Hepa1-6 cells that transfected with GAL-GNR-siBRAF was evidently reduced (Fig. 5b–d).
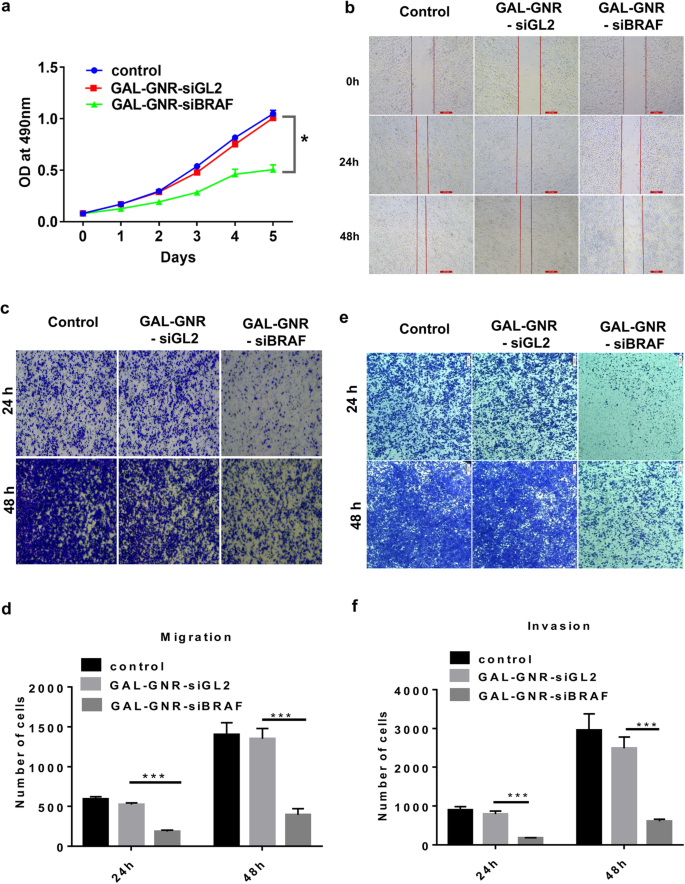
The impact of silencing BRAF gene on Hepa1-6 cells by GAL-GNR-siBRAF. een Proliferation of Hepa1-6 Cells. Hepa1-6 cells were transfected with GAL-GNR-siBRAF, GAL-GNR-siGL2, or PBS, and the cell proliferation was measured by MTT assay (n =5). The error bar represents the standard deviation of three experiments (*p <0,05). b Scratch test of Hepa1-6 cells. Hepa1-6 cells were transfected for 24 h as described above and then scraped with a 10 μL tip. The cell scratch images were taken at different time points (scale bar =200 μm). c en e Migration and invasion of Hepa1-6 cells. Hepa1-6 cells were transfected for 24 h as described above. Cell migration and invasion ability was determined by transwell assay, and imagines were taken at different time points (scale bar =200 μm). d en f Columnar statistical analysis of cell migration and invasive capacity (***p <0.001)
To further investigate the potential of GAL-GNR-siBRAF on the invasion, transwell assays were performed. The results showed that hepa1-6 cells transfected with GAL-GNR-siBRAF haven significantly decreased the invasion of Hepal-6, as compared with GAL-GNR-siGL2 or PBS (Fig. 5e and f). The above results implied that knockdown of BRAF gene using GAL-GNR-siBRAF complexes can effectively reduce migration and invasion of hepatocellular carcinoma cells.
Combination Treatment with Photothermal Effect and Gene Silencing of GAL-GNR-siBRAF
Our previous studies have demonstrated that gold nanomaterials can generate thermal energy under near infrared radiation [37]; this phenomenon is called photothermal effect due to LSPR properties of the GNR. Our results showed that, with the increase of GAL-GNR concentration, the heat production capacity of GAL-GNR was enhanced. When the concentration of GAL-GNR is 100 μg/mL, the temperature quickly rises from 24 to over 60 °C. In addition, there was no significant difference in heat production capacity between GNR and GAL-GNR (Fig. 6a).
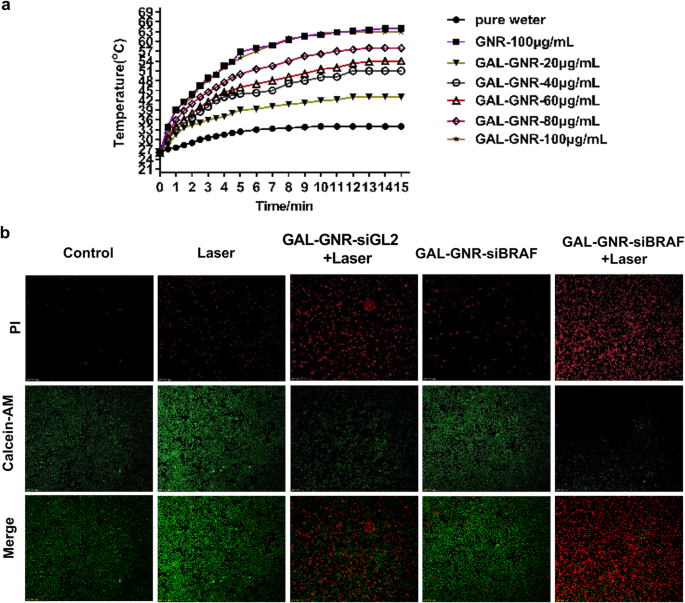
Photothermal effect induced by GAL-GNR and combination treatment of photothermal effect and gene silencing on liver cancer cells. een 803 nm near-infrared laser source (2 W/cm 2 ) was used to irradiate the solution of GNR, GAL-GNR, or distilled water (blank control) for 15 min. The temperature was detected by infrared thermometer at different time point. b Hepa1-6 cells were treated with PBS, laser, GAL-GNR-siBRAF, GAL-GNR-siGL2 + Laser, or GAL-GNR-siBRAF + Laser, respectively. Green fluorescence of calcein AM (live cells) and red fluorescence of PI (dead cells) were observed under fluorescence microscope
The novel nano-system GAL-GNR-siBRAF possesses three individual characteristics:specific targeting of liver cancer, siRNA-based gene silencing of BRAF, and GNR-offered photothermal effects. Thus, we further study the synergistic therapeutic effect of GAL-GNR-siBRAF in anti-tumor treatment. Hepa1-6 cells without GAL-GNR kept higher viability even under near infrared radiation, suggesting laser itself had no significant effect on tumor cells. Once the laser irradiation was carried out on the basis of GAL-GNR-siGL2 treatment, the photothermal effect showed powerful killing ability on Hepa1-6 cells. Although BRAF gene silencing alone induced cell death, the effect was not conclusive. The treatment of cells with the nano-material GAL-GNR-siGL2 plus laser irradiation resulted in much stronger cell-killing ability than BRAF gene silencing individual (Fig. 6b). These data indicates that the BRAF gene silencing and photothermal effect can synergistically increase the potential of killing tumor cells.
Discussion
Difficulties in tumor-targeted delivery are major obstacles in the clinical treatment of tumors. This study demonstrated for the first time that we have developed a novel multifunctional nanocarrier GAL-GNR-siBRAF, and it was provided with many advantages. The modified GAL-GNR not only possessed good biocompatibility but also maintained the LSPR phenomena of GNR skeleton and still has excellent photothermal conversion ability. GNR modified with GAL can home hepatocellular carcinoma cells through ASGPR, which has great potential in targeted molecular therapy of hepatocellular carcinoma. Further studies showed that BRAF gene silencing inhibited the proliferation, migration, and invasion of hepatoma cells. It is worth noting that GAL-GNR-siBRAF shows a stronger cell killing ability in the combination of photothermal effect and gene silencing of BRAF.
RNA interference (RNAi) has attracted much attention due to its crucial role in gene expression and regulation. Using siRNA to knock down sequence-specific genes in cancer cells for gene therapy is an effective and specific targeted gene therapy, and which has become a new therapeutic tool for many diseases including cancer [29, 31]. However, low stability in serum and poor cell uptake limit siRNA in clinical application [38]. On the other hand, siRNA possess negative charge that prevents it from binding negatively charged cell membranes, and siRNA itself is unlikely to be delivered directly into cells [32, 39]. In addition, there are problems associated with low transfection efficiency and poor cell internalization in siRNA therapy [40]. These barriers impede the delivery of siRNA to target cells. To enhance siRNA stability and to strengthen gene silencing efficacy, we synthesized a novel nanocarrier, GAL-GNR-siBRAF, which includes three components (Scheme 1). This nanocarrier has low molecular size (about 30-nm longitude and 10-nm diameter) and good dispersibility (Fig. 1). Additionally, GAL-GNR-siBRAF could effectively load large amount of siRNA at low concentration (Fig. 2a) and protect siRNA degradation from RNase in serum; the siRNA was evidenced by stability for at least two days at 37 °C in the presence of fresh murine serum (Fig. 2b).
Good biocompatibility is essential for nanomaterials used in the field of biotherapy. CTAB is an essential active reagent in the synthesis of gold nanorods although it has apparent cytotoxicity that limits its biological application [41]. In order to reduce the cytotoxicity of the material, we manipulated the GNR by external modification of positive charge PEI and targeting adaptor GAL (d-galactose). Our results showed that, compared with unfunctionalized GNR, GAL-modified GNR has a better biocompatibility. The cell viabilities maintained over 80% even at very high concentrations (105 μg/mL) of GAL-GNR for 48 h (Fig. 3). In addition, the small molecular size and cylindrical shape of the nanorod facilitate its penetration through the cell membrane into the cell [37, 38, 42]. This phenomenon is particularly evident in targeted therapy of cancer cells. Nano-construct modified with the galactose-targeting moieties resulted in high accumulation of GAL-GNR-siBRAF in tumor cells, inducing effective downregulation of BRAF gene expression (Fig. 4). Moreover, according to the competitive inhibition experiments, we found that GAL-GNR entered cells mainly through ASGPR surface receptors of Hepa1-6 cells (Fig. 4c).
It was reported that HCC with high expression of BRAF and RAF1 tends to have rapid proliferation and growth [41, 43, 44]. B-Raf and Raf1 mainly act on the downstream of ERK/MAPK pathway, regulating nuclear factors through cascade amplification. Activation of this pathway accelerates the proliferation and differentiation of HCC cells abnormally [41, 44, 45]. RAF gene can also promote the expression of matrix metalloproteinases (MMPs), which can change the adhesion of tumor cells, degrade extracellular matrix (ECM) and basement membrane, and promote the invasion and metastasis of tumors [44, 45]. BRAF kinase regulates the RAS-RAF-MEK-ERK pathway, which promotes tumor cell proliferation, invasion and metastasis, and allows cell death through apoptosis [5, 46, 47]. In previous work, we found that BRAF gene was highly expressed in Hepa1-6 cells (data were not shown). It is speculated that the knock down of BRAF expression in Hepa1-6 will block the RAS-RAF-MEK-ERK pathway and lead biological changes of Hepa1-6. To verify our hypothesis, we transfected hepatocellular carcinoma cells with GAL-GNR-siBRAF and found that it can restrain the cell proliferation, migration, and invasion significantly (Fig. 5), providing a new strategy for clinical treatment of hepatocellular carcinoma.
Another important advantage of GNR is that it possesses local surface plasmon resonance (LSPR), which can convert absorbed light energy into heat energy under near infrared light irradiation, thereby killing and destroying cells [42]. Then, we explored the light-to-heat conversion ability of GAL-GNR, and the results showed that the modified GAL-GNR can induce heat energy effectively under the irradiation of near infrared light (Fig. 6a). Next, we further investigated the synergistic effects of GAL-GNR-siBRAF. Whereas BRAF gene silencing showed limited cytotoxicity, the treatment of GAL-GNR-siGL2 + laser had a much stronger killing ability on tumor cells. At the same time, the combination of photothermal hyperthermia and BRAF gene silencing could cause more than 85% cell death (Fig. 6b) which indicates that the synergy of GAL-GNR-siBRAF and photothermal effects could be an ideal strategy to inhibit liver cancer.
Conclusion
This study showed that GAL-GNR-siBRAF overcome the obstacle of siRNA degradation, effectively increased the stability of siRNA in serum in vitro. In addition, GAL-GNR-siBRAF can target deliver siRNA to hepatocellular carcinoma cells and knockdown the expression of BRAF and inhibit the cell proliferation, invasion, and migration significantly. More importantly, GAL-GNR-siBRAF, as a new multifunctional nanocarrier, can greatly enhance the ability of killing tumor cells when combined with near-infrared light. In conclusion, GAL-GNR-siBRAF has great potential in treatment of hepatocellular carcinoma and provides new ideas for clinical application of liver cancer.
Beschikbaarheid van gegevens en materialen
All data generated and materials used in this study are included in the manuscript and corresponding additional files.
Afkortingen
- GAL:
-
d-galactose
- GNR:
-
Golden nanorods
- siBRAF:
-
Small interfering RNA specific for BRAF
- HCC:
-
Hepatocellulair carcinoom
- ASGPR:
-
Asialoglycoprotein receptor
- TACE:
-
Transcatheter arterial chemoembolization
- LSPR:
-
Gelokaliseerde oppervlakteplasmonresonantie
- CTAB:
-
cetyltrimethylammonium bromide
- MUA:
-
Mercaptoundecanoic acid
- EDC:
-
1-ethyl-3-[3-dimethylaminopropyl] carbodiimide hydrochloride
- NHS:
-
N-hydroxysuccinimide
- PEI:
-
Polyethyleenimine
- TEM:
-
Transmissie-elektronenmicroscopie
- NMR:
-
Kernmagnetische resonantie
- FBS:
-
Foetaal runderserum
- DMSO:
-
Dimethyl Sulfoxide
- BCA:
-
Bicinchoninic acid
- PVDF:
-
Polyvinylideenfluoride
Nanomaterialen
- Voorbereiding van met ICA geladen mPEG-ICA nanodeeltjes en hun toepassing bij de behandeling van door LPS geïnduceerde H9c2-celbeschadiging
- 131I-getraceerde PLGA-lipide nanodeeltjes als dragers van medicijnafgifte voor de gerichte chemotherapiebehandeling van melanoom
- Een nieuwe methode zonder organisch oplosmiddel voor gerichte nanodrug voor verbeterde werkzaamheid tegen kanker
- Effect van in situ gloeibehandeling op de mobiliteit en morfologie van op TIPS pentaceen gebaseerde organische veldeffecttransistoren
- Effect van schuine hoek gesputterde ITO-elektrode in MAPbI3 perovskiet-zonnecelstructuren
- Bevordering van SH-SY5Y-celgroei door gouden nanodeeltjes gemodificeerd met 6-mercaptopurine en een neuron-penetrerend peptide
- Toxiciteit van PEG-gecoate CoFe2O4-nanodeeltjes met behandelingseffect van curcumine
- Directe groei van op III-nitride nanodraad gebaseerde gele lichtgevende diode op amorf kwarts met behulp van dunne Ti-tussenlaag
- Ronde gouden nanodeeltjes:effect van deeltjesgrootte en concentratie op de wortelgroei van Arabidopsis thaliana
- Effectieve lichtabsorptie met behulp van de dubbelzijdige piramideroosters voor dunne-film silicium zonnecel
- Het apoptose-effect op leverkankercellen van gouden nanodeeltjes gemodificeerd met lithocholzuur



