Hydrothermische synthese van met zilver gedecoreerde nanovlokken van gereduceerd grafeenoxide (rGO) met effectieve fotokatalytische activiteit voor afvalwaterzuivering
Abstract
Grafeenoxide (GO) werd verkregen door middel van de gemodificeerde hummers-methode en gereduceerd grafeenoxide (rGO) werd verkregen door warmtebehandeling toe te passen. Verschillende concentraties (2,5, 5, 7,5 en 10 gew.%) zilver (Ag) werden opgenomen in GO-nanobladen door een hydrothermische benadering toe te passen. Gesynthetiseerde Ag gedecoreerde rGO-fotokatalysator Ag / rGO werd gekarakteriseerd met behulp van röntgendiffractie (XRD) om fasezuiverheid en kristalstructuur te bepalen. XRD-patronen toonden de vorming van GO tot Ag/rGO. Moleculaire trillingen en functionele groepen werden bepaald door middel van Fourier Transform Infrared spectroscopie (FTIR). Optische eigenschappen en een afname in bandgap met insertie van Ag werden bevestigd met UV-Visible (Uv-Vis) spectrofotometer en fotoluminescentie (PL). Elektronische eigenschappen en afwijkingen in koolstofstructuren werden onderzocht door middel van Raman-spectroscopie die het bestaan van karakteristieke banden (D en G) aan het licht bracht. Oppervlaktemorfologie van bereide monsters werd onderzocht met veldemissie scanning elektronenmicroscoop (FESEM). Homogene verdeling, grootte en bolvorm van Ag NP's over rGO-vellen werden verder bevestigd met behulp van een transmissie-elektronenmicroscoop met hoge resolutie (HR-TEM). Kleurafbraak van gedoteerde en niet-gedoteerde monsters werd onderzocht door middel van Uv-Vis-spectra. Experimentele resultaten gaven aan dat de fotokatalytische activiteit van Ag@rGO toenam met een verhoogde doteringsverhouding als gevolg van verminderde recombinatie van elektron-gatparen. Daarom wordt gesuggereerd dat Ag@rGO kan worden gebruikt als een gunstige en superieure fotokatalysator om het milieu en afvalwater te reinigen.
Inleiding
Water op aarde is verwant aan bloed in ons lichaam. Het is een belangrijke grondstof voor overleving en ontwikkeling van alle levende soorten. Hoewel 71% van het aardoppervlak bedekt is met water, wordt slechts 0,03% van het totale water beschouwd als zoet water dat direct door mensen kan worden gebruikt via zoetwatermeren, rivieren en ondiep grondwater [1]. In de afgelopen decennia heeft de ontoereikende beschikbaarheid van schoon drinkwater zich als een niet-aflatend wereldwijd probleem gemanifesteerd. De snelle groei van de wereldbevolking en de industrialisatie hebben geleid tot een toenemende milieuvervuiling, waardoor ongeveer 750 miljoen mensen geen toegang hebben tot schoon water [2, 3]. Waterreservoirs worden herhaaldelijk verontreinigd door verschillende gevaarlijke verontreinigende stoffen die zware metaalionen, kleurstoffen, olie en andere chemicaliën bevatten die vrijkomen uit verschillende leerlooierijen en industrieën die verband houden met textiel, rubber, papier, cosmetica, verven, plastic en voedsel [4]. Volgens het rapport van de Wereldbank wordt 17-20% van de watervervuiling veroorzaakt door de textielindustrie. Jaarlijks worden ~ 1/10 miljoen soorten kleurstoffen geproduceerd in tal van textielprocessen, waarvan methyleenblauw (MB) 10-15% direct vrijkomt in het effluent. Deze verontreinigende stoffen veroorzaken ernstige gezondheidsproblemen zoals kanker, huidirritaties, allergie en leverfunctiestoornissen en zijn ook schadelijk voor het waterleven [4, 5].
Om deze wereldwijde problemen aan te pakken, worden bepaalde conventionele behandelingsbenaderingen zoals ionenuitwisseling, elektrolyse, koolstoffilter, chemische coagulatie, biologische methoden, membraanfiltratie en omgekeerde osmose (RO) gebruikt. Desalniettemin zijn er een reeks nadelen en beperkingen verbonden aan deze technieken, waaronder onbekwaamheid, complexe procedures, hoge slibvorming, hoge implementatie- en operationele kosten en het gebruik van grote hoeveelheden energie [4, 6, 7]. Er moeten dus efficiënte technologieën met bovengenoemde eigenschappen worden ontwikkeld; van dergelijke technieken overwint fotokatalyse maximale tekortkomingen.
Tot op heden heeft fotokatalytische degradatie met behulp van anorganische halfgeleider nanomaterialen enorme wenselijkheid en interesse getoond voor onderzoekers vanwege de uitstekende fysische en chemische eigenschappen zoals lage toxiciteit, elektrochemische stabiliteit, super oxidatieve capaciteit, kosteneffectiviteit en levensvatbaarheid van het milieu [2, 8, 9 ]. Tijdens het fotokatalytische (PC) proces absorberen nanomaterialen meer zichtbare lichtenergie dan door bandgap geïnitieerde excitatie tussen valentie- en geleidingsbanden. Door ladingsscheiding worden elektron-gatparen gegenereerd. Vrije radicalen (OH) oxideren organische verbindingen en breken verontreinigingen af [8, 10].
Aan de andere kant zijn enkele cruciale factoren van vitaal belang om de pc-prestaties te bepalen, met name het oppervlak van de fotokatalysator, aangezien organische verontreinigende stoffen voornamelijk op het oppervlak van de halfgeleider worden afgebroken. Aanwezigheid van robuust lichtabsorptievermogen, snelle grensvlakredoxsnelheid, tussen verschillende nanostructuren; tweedimensionale (2D) nanostructuren hebben de neiging om deze functies efficiënter te bereiken [11,12,13,14]. 2D-nanomaterialen bieden ook elektronentransportkanalen vanwege verminderde knooppunten en korrelgrenzen in tegenstelling tot andere sferische nanokristallen. Snel transport van elektronen vermindert de recombinatiesnelheid en verhoogt de prestatie van pc-degradatie. Dus in deze lijn is grafeenoxide (GO) een geschikte kandidaat om de halfgeleidende pc-efficiëntie te onderschrijven [15,16,17,18].
In de afgelopen decennia kwam grafeen met een enkele atomaire dikke nanosheet, naast CNT's en andere op koolstof gebaseerde nanomaterialen, naar voren als een in het oog springende kandidaat met een breed scala aan veelbelovende relevante eigenschappen, waaronder energieconversie, opslag en katalytische activiteiten [19, 20,21]. In studies met betrekking tot waterbehandeling en distillatie, vanwege een groot aantal gedelokaliseerde elektronen geconjugeerd in sp 2 configuratie van koolstofnetwerk, grafietkool verrijkt het transport van foto-elektronen en verbetert de efficiëntie van de fotoconversie van het systeem aanzienlijk. Bovendien vertoont GO een hoog absorptievermogen van organische materialen in een waterig medium [22, 23]. GO en gereduceerde grafeenoxiden (rGO) zorgen voor PC-reactie en worden vanwege hun smalle bandgap gepromoot als zichtbaar licht actieve halfgeleiderfotokatalysatoren. Desalniettemin is er ruimte voor verbetering, aangezien de fotoconversie slecht bleek te zijn, veroorzaakt door de snelle recombinatie van elektron-gatparen aan het oppervlak.
De efficiëntie van fotoconversie van fotokatalysatoren op basis van GO/rGO kan worden verbeterd door elektron-gat-recombinatie te voorkomen. Om dit doel te bereiken, werden oppervlaktemodificaties goed ontwikkeld met edelmetaalionen, waaronder platina (Pt), palladium (Pd), zilver en gouden nanodeeltjes (NP's). Het zilver van de meest bestudeerde edelmetalen wordt beschouwd als een waarschijnlijke kandidaat voor modificatie van grafeen en zijn analogen voor pc-relevantie vanwege de lage kosten, ongeëvenaarde optische eigenschappen, hogere chemische stabiliteit en niet-toxische aard. Meer immobiliteit van zilveren nanodeeltjes versierd op rGO wordt erkend als verbeterde prestaties, voornamelijk als gevolg van een groter reactief gebied en superieure ladingsscheiding. Unieke elektronenaggregatie- en transporteigenschappen van GO via geconjugeerd schema drijven hete elektronen naar reactieve plaatsen en onderdrukken recombinatie [23]. Dientengevolge wilden we, namens de bovengenoemde voordelen, verschillende verhoudingen van Ag-gehalte (2,5, 5, 7,5, 10) gewichts% synthetiseren met rGO-fotokatalysator via een hydrothermische route om de efficiëntie van de fotokatalysator te onderzoeken en ook bereide monsters zouden worden gekarakteriseerd door middel van verschillende technieken om te bestuderen structurele optische en elektronische eigenschappen.
Methoden
De huidige studie was gericht op het synthetiseren van verschillende concentraties Ag in rGO-nanobladen via een hydrothermale route om de efficiëntie van de fotokatalysator te onderzoeken.
Materialen
Grafiet (99%) en natriumnitraat (NaNO3 ) 99,9% werd verkregen van "Sigma-Aldrich", terwijl zwavelzuur (H2 SO4 , 37%) en fosforzuur (H3 PO4 ) zijn overgenomen van "Analar." Zilver (Ag, 99,8 %), kaliumpermanganaat (KMnO4 , 99% en zoutzuur (HCL) werden verkregen uit "Merck." Alle chemicaliën werden gebruikt zonder verdere zuivering.
Synthese van GO
Gemodificeerde hummers-methode werd toegepast om GO te verkrijgen. Grafiet (5 g) en NaNO3 (2,5 g) werden gemengd in H2 SO4 (108 ml) met 12 ml H3 PO4 . Het mengsel werd gedurende 10 minuten magnetisch in een ijsbad geroerd; verdere filtraatoplossing werd gedurende 2 uur in een moffeloven bij 60°C gedroogd om vocht te verwijderen. Later, KMnO4 (15 g) werd langzaam toegevoegd bij handhaving van een temperatuur tot onder 5°C. Suspensie werd gedurende 2 uur overgebracht naar een ijsbad na krachtig roeren bij 98°C gedurende 60 minuten terwijl continu water werd toegevoegd. Er werd meer gedeïoniseerd water toegevoegd totdat het suspensievolume 400 ml was na 5 minuten H2 O2 (12 ml) werd gemengd. Ten slotte werd de suspensie gecentrifugeerd en herhaaldelijk gewassen met water en het HCL-product werd gedroogd bij 60 ° C en de pH van GO bleek 5,7 te zijn na wassen, zoals geïllustreerd in Fig. 1 [24, 25].
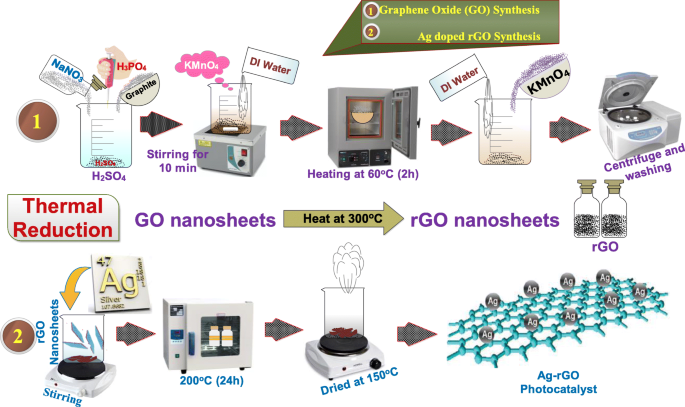
Syntheseproces voor GO en Ag-gedoteerde rGO
Synthese van Ag/rGO
De rGO is geëxtraheerd uit GO door thermische reductie. GO is gereduceerd door het op reductietemperatuur (300 °C) te houden. Een plotselinge verandering in temperatuur veroorzaakt eliminatie van functionele groepen en zuurstofatomen uit koolstofvlakken en afschilfering van GO vindt plaats om rGO te produceren [ 26]. De rGO kan worden beschouwd als chemisch afgeleid grafeen, waarvan de structuur varieerde van één laag tot meerdere lagen [27]. Ag-gedoteerde rGO met verschillende concentratieverhoudingen werd hydrothermisch gesynthetiseerd, met behulp van 800 mg GO-nanosheets opgenomen met (25, 50, 75 en 100 mg) Ag in 80 ml gedeïoniseerd water onder krachtig roeren gedurende 20 min. De oplossing werd vervolgens gecentrifugeerd (30 min) en vervolgens overgebracht naar een met Teflon beklede autoclaaf van 100 ml, afgesloten en verwarmd tot 200 °C (24 u). Het eindproduct werd gedroogd bij ~ 200 °C zoals weergegeven in Fig. 1 [9].
Fotokatalytische activiteit
Fotokatalytische activiteit van bereide producten werd geëvalueerd door de afbraak van synthetisch methyleenblauw (MB) in waterig medium zoals getoond in Fig. 2. Kleurstof (5 mg/500 ml) werd bereid met 10 mg suspensie van fotokatalysator (0,025:1, 0,050:1, 0,075:1 en 0,1:1) onder roeren (5 min) en gedurende 30 min blootgesteld aan het donker om een significante absorptie te bereiken. Een 60 ml bereide oplossing werd onder krachtig roeren overgebracht naar een fotoreactor onder een kwiklamp (400 W en 400-700 nm) die als een zichtbare lichtbron werd gebruikt. Na blootstelling aan licht gedurende gespecificeerde tijdsintervallen (20 min), werd suspensie (3 ml) verzameld om de kleurstofafbraak te bepalen. De concentratie/absorptie van MB werd onderzocht met een UV-Vis-spectrometer; ontkleuringsefficiëntie van de bereide fotokatalysator werd geëvalueerd als:
$$ \mathrm{Degradation}\ \left(\%\right)=\left[1-\left(C/{C}_o\right)\right]\times 100 $$ (1)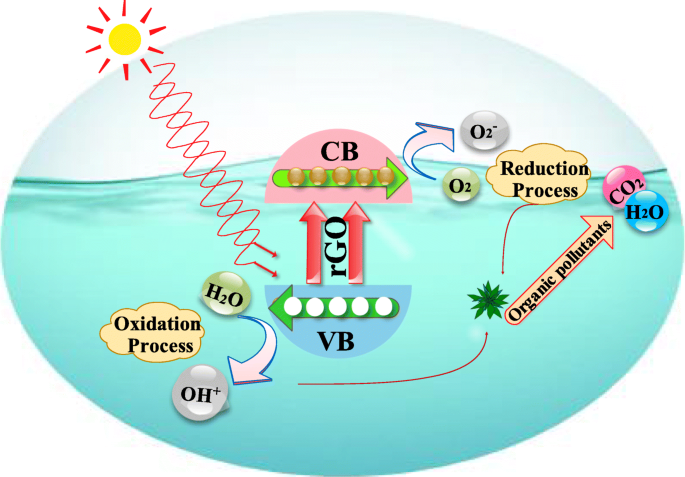
Fotokatalytisch mechanisme voor kleurstofafbraak in aanwezigheid van Ag/rGO
waar C o is de absorptie bij t =0 en C is de absorptie op het moment t (specifiek tijdsinterval) [8, 10].
Het mechanisme van fotokatalytische afbraak van organische moleculen wordt als volgt toegelicht (Fig. 2). Wanneer fotokatalysator (Ag/rGO) wordt bestraald met fotonen met een energie gelijk aan of meer dan de bandgap-energie van PC, dan zullen elektronen (e − ) worden opgewekt door de valentieband (VB)
$$ \mathrm{PC}+ hv\to {e}^{-}\left(\mathrm{CB}\right)+{h}^{+}\left(\mathrm{VB}\right) $$ (2)Gegenereerde elektronen door bestraling kunnen gemakkelijk worden opgevangen door O2 geabsorbeerd molecuul op het oppervlak van fotokatalysator (PC) of opgelost O2 om superoxideradicalen te geven, d.w.z. O2 •−
$$ {e}^{-}+{\mathrm{O}}_2\to {\mathrm{O}}_2^{\bullet -} $$ (3)Dus, O2 •− kan reageren met H2 O om hydroperoxyradicaal te produceren (H2 O • ) en hydroxylradicaal (OH • ), wat invloedrijke oxidatiemiddelen zijn die organische moleculen afbreken:
$$ {\mathrm{O}}_2^{\bullet -}+{\mathrm{H}}_2\mathrm{O}\to {\mathrm{H}\mathrm{O}}_2^{\bullet } +\wiskunde{O} $$ (4)Tegelijkertijd kunnen fotogegenereerde gaten worden opgevangen door hydroxylgroepen aan het oppervlak (H2 O) op het oppervlak van een fotokatalysator om hydroxylradicalen te produceren (OH • ):
$$ {h}^{+}+{\mathrm{OH}}^{-}\to {}^{\bullet}\mathrm{O}{\mathrm{H}}_{\mathrm{ad}} $$ (5) $$ {h}^{+}+{\mathrm{H}}_2\mathrm{O}\to {}^{\bullet}\mathrm{O}\mathrm{H}+{\ wiskunde{H}}^{+} $$ (6)Uiteindelijk zullen organische moleculen worden geoxideerd tot CO2 en H2 O als volgt:
OH + organische moleculen + O2 → producten (CO2 en H2 O) (7)
Tijdelijk kan een lichte recombinatie van positief gat en elektron plaatsvinden, wat de fotokatalytische activiteit van de bereide nanokatalysator [28] zou kunnen verminderen.
Kenmerken van materialen
Kristalstructuur en fase-informatie van GO en Ag@rGO werden onderzocht via XRD, door spectrum Bruker-systeem (XRD, D2 Phaser, VS) uitgerust met monochromatische Cu K-straling met een gemiddelde golflengte van 0,154 nm (5-80 °) met behulp van een scansnelheid van 0,05/min. FTIR Perklin Elmer 3100 spectrometer met een spectraal bereik van 4000–400 cm −1 met een toename van 32 scans en een resolutie van 0,2 cm −1 werd gebruikt om functionele groepen en andere moleculaire trillingen van voorbereide monsters te detecteren. Optische eigenschappen werden vastgelegd met een UV-Vis-spectrofotometer (TECAN oneindig M200PRO) in het bereik van 200-700 nm. Oppervlaktemorfologie en tussenlaagafstand van gesynthetiseerde monsters werden waargenomen met behulp van veldemissie scanning elektronenmicroscoop (FESEM), JSM-6460LV en hoge resolutie transmissie-elektronenmicroscoop (HR-TEM) Philips CM30 en JEOL JEM 2100F. Om GO-, Ag/rGO-vlokken en vibratiemodi te bevestigen, werden Raman-spectra gebruikt op Renishaw in door reflex confocale Raman-microscoop met een golflengte van 532 nm (6 mW) laser. Fotoluminescentiespectra van bereide en gedoteerde monsters werden opgenomen door spectrofluorometer (JASCO, FP -8300).
Resultaten en discussie
De fasestructuur en kristallietgrootte van bereide Ag-ingevoegde rGO-nanobladen werden onderzocht met behulp van XRD-analyse (figuur 3a). Diffractogram van GO toont intense reflectie op ~ 10,27 ° toegeschreven aan (001) vlak met een tussenlaag van 0,80 nm [23, 29, 30]. Bij Ag-doping ontstaat een brede piek bij ~ 25,4 °, wat wordt herkend als de karakteristieke piek van grafeen, geïndexeerd als (002) vlak (JCPDS No # 04-0783) van hexagonaal grafiet, met een d-afstand van 0,34 nm [23, 30,31 ,32]. Peak (001) onthult het grafietpoeder volledig geoxideerd tot GO en (002) peak onderschreef de verwijdering van polykoolwaterstofmatrijs tussen twee lagen rGO [30]. Na Ag-substitutie verschoof de GO-piek (001) naar een hogere waarde naar 2θ bij 25,4 ° met lagere d-afstand duidelijk tot redoxreactie tussen grafeenoxide en zilverionen (Ag-rGO) en d-verschuivingswaarde na reductie veroorzaakt door de verwijdering van zuurstofbevattende groepen die intercaleren tussen lagen gereduceerd grafeenoxide (rGO) zoals zichtbaar in XRD-diffractogram [29, 32]. Gemiddelde kristallietgrootte bepaald door de vergelijking van Scherer:
$$ \mathrm{D}=\frac{\mathrm{k}\lambda }{\beta \cos \uptheta} $$ (8)De kristallietafmetingen blijken respectievelijk ~ 4,85, 11,3, 11,53, 11,6 en 28,3 nm te zijn. In verg. (8) k =0,89, β =FWHM, λ =0,154 nm, en θ =diffractiehoek. Geselecteerde gebiedselektronendiffractie (SAED) in Fig. 3b en c, overeenkomend met XRD-patronen van bereide monsters, vertoont duidelijke ringkenmerken en geeft de hexagonale fase van GO en Ag / rGO aan, gemanifesteerd tot goed gekristalliseerde producten; ook was ringindexering consistent met XRD-patronen.
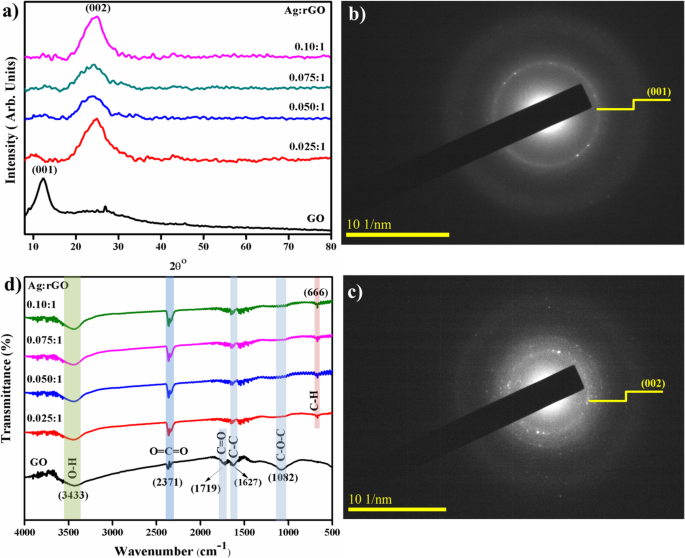
een XRD-patroon. b , c SAED-ringen van bereid en met Ag gedoteerd RGO (b ) 0:1 (c ) 0,010:1. d FTIR-spectra
Fourier-transformatie infrarood (FTIR) spectra van GO en Ag-gedoteerde rGO worden geïllustreerd in Fig. 3d. Waargenomen piek ~ 3433 cm –1 komt overeen met O-H strektrilling [23]. Lage transmissiepieken bij 1719 cm –1 toewijzen aan C =O rektrillingen veroorzaakt door COOH-groepen en de band op 1627 cm −1 toegewezen aan de aromatische C-C-uitrekking [10, 33]. Piek op ~ 2371 cm −1 toegewezen aan COO-groepen [34]. Transmissiepiek (~ 650 cm −1 ) is een vingerafdrukgebied van gehybridiseerde sp 2 koolstofbinding toegewezen als C-H-buigtrilling [35]. Band ~ 1082 cm –1 komt overeen met C-O-C van hydroxyl-strektrillingen, bij doping veranderde de piekwaarde van functionele groepen op het gedoteerde monster enigszins terwijl hun vormen vergelijkbaar blijven [23, 29, 36].
Optische eigenschappen in termen van absorptie en bandgap-analyse van Ag-rGO-fotokatalysator werden onderzocht door middel van Uv-Vis-spectrograaf variërend van 200-700 nm, zoals weergegeven in figuur 4a. Het Uv-Vis-spectrum van GO vertoont kenmerken die pieken rond 230 nm als gevolg van π –π * overgang van aromatische C-C-bindingen duidde op herstel van een uitgebreid geconjugeerd raamwerk van sp 2 koolstof atomen. Een andere schouderpiek waargenomen bij 300 nm toegeschreven aan n –π * overgangen van C=O bindingen [19, 23, 31]. Omgekeerd werden deze twee pieken zwakker in het geval van Ag/rGO overeenkomend met π –π * overgang van aromatische C-C-binding bleek roodverschoven te zijn bij 270 nm, wat de reductie van GO bevestigt en aangeeft dat de elektronenconjugatie van grafeen niet hersteld is [23, 29]. De absorptie in het zichtbare gebied (~ 400 nm) als gevolg van hun oppervlakte-plasmonische resonantie van Ag NP's, is verder bewijs voor als zichtbaar licht actieve fotokatalysator voor het verwijderen van organische lichamen [23, 29, 37]. Bandgap werd berekend met de Tauc-vergelijking; αhν = D (hν − Bijv. ) n door het plotten van (αhν ) 2 vs hν door geëxtrapoleerd van lineaire passingen, werd berekend dat de band 4,10 eV was voor GO en 3,98 tot 3,50 eV voor Ag / rGO, bandgap nam geleidelijk af met hogere doping van Ag NP's duidelijk waargenomen in Fig. 4b [38].
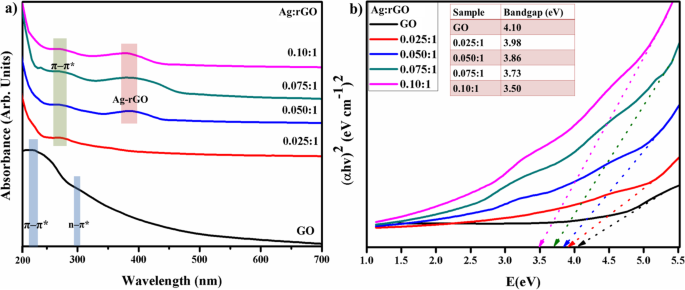
een UV-Vis-spectra van GO en Ag-rGO. b Bandgap vergelijking
De morfologische kenmerken van GO- en Ag-rGO-monsters opgehelderd door FESEM en HR-TEM, getoond in Fig. 5. GO-afbeeldingen (Fig. 5a) tonen enkele lagen microstructuren met rijke rimpels en pluizige morfologie die lijkt op een dun gordijn. Afbeeldingen van Ag@rGO (Fig. 5b-d) tonen gedeeltelijk gevouwen en krullende transparante nanosheets met kleine fluctuaties die essentieel zijn om de thermodynamische stabiliteit van grafeen te doorstaan, vanwege de 2D-kristalstructuur. Nanosheets vertonen extreem schone, zijdeachtige en golvende structuren en deze functie kan belangrijk zijn om aggregatie van rGO-vellen te voorkomen en het oppervlak te behouden om de aanhechting van Ag NP's op grafeenvellen te vergemakkelijken die kunnen worden gevisualiseerd in HR-TEM-afbeeldingen [36]. De bijbehorende HR-TEM-beelden (Fig. 6 a1 -d1 ), vertoont GO een lamellaire en plaatachtige structuur met een schoon oppervlak (Fig. 6a1 ), in Ag-rGO-monster (Fig. 5 b1 ) weinig stapelvouwen vanwege hun vervormingen door een hoge fractie van sp 3 C-O-bindingen [29]. Met toenemende concentratie van Ag NP's (Fig. 6 c1 , d1 ) afbeeldingen onthulden een goed verspreide en homogene verstrooiing van bolvormige Ag NP's op het oppervlak van rGO-platen met een gemiddelde deeltjesgrootte van 10-12 nm [23, 29]. In Afb. 6 d1 met een hogere concentratie (10%) Ag, nam de aggregatie van deeltjes toe, wat duidelijk is voor gedoteerde soorten.

(een -d , een 1 -d 1 ) FESEM- en HR-TEM-beelden van GO en Ag/rGO (a , een 1 ) GA (b , b 1 ) 0,050:1 (c , c 1 ) 0,075:1 en (d , d 1 ) 0,10:1
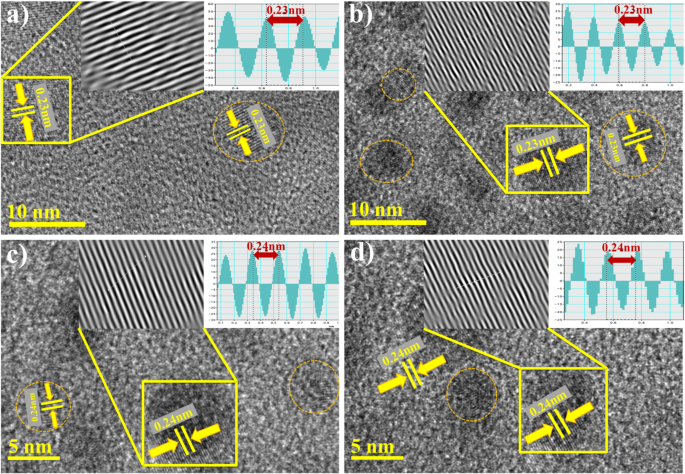
een -d d-afstand van HR-TEM-afbeeldingen van Ag-rGO (a ) 0,025:1 (b ) 0,050:1 (c ) 0,075:1 (d ) 0,10:1
De extreem hoge resolutiebeelden tot 5 en 10 nm d-afstand van Ag / rGO-monsters kunnen duidelijk worden waargenomen in Fig. 6a-d. Omcirkelde gebieden geven de aanwezigheid van Ag NP's aan met een roosterafstand van Ag nanokristal van ongeveer 0,235 nm [23, 29].
Fotoluminescentie (PL) -analyse werd uitgevoerd om de levensduur, overdracht en vangst van een elektron-gatpaar te onderzoeken en de interactie tussen grafeennanostructuren te bestuderen, de invloed ervan op de fotokatalytische respons geïllustreerd in Fig. 7a [39, 40]. Grafiet vertoont geen luminescentie-eigenschappen vanwege de nul-bandgap. Desalniettemin, bij een afname in grootte tot nanoschaal, wordt de bandgap groot, veroorzaakt door het kwantumopsluitingseffect. In nanosheets van GO en rGO veranderden oxidegroepen en koolstofvacatures het grafeen om elke koolstofnanocluster te vormen die halfgeleidend gedrag en luminescentiefenomeen vertoont dat kan worden beïnvloed door de grootte of fractie van ketens en clusters [40, 41]. In PL-spectra waren luminescentiepieken gelokaliseerd op ~ 330, 565 en 608 nm, wat wordt toegeschreven aan de recombinatie van elektron-gatparen in de lokale toestand van sp 2 koolstofclusters geïntegreerd met sp 3 Matrix. Daarom is rGO-luminescentie te wijten aan verdwenen functionele zuurstofgroepen die de percolatie van paden tussen sp 2 vergemakkelijken clusters [40]. Significante piek bij ~ 565 nm sterk afgenomen in het geval van rGO met reductie van GO-oxide functionele groepen die zijn afgenomen en sp 2 koolstofclusters worden gelijktijdig uitgebreid [41].
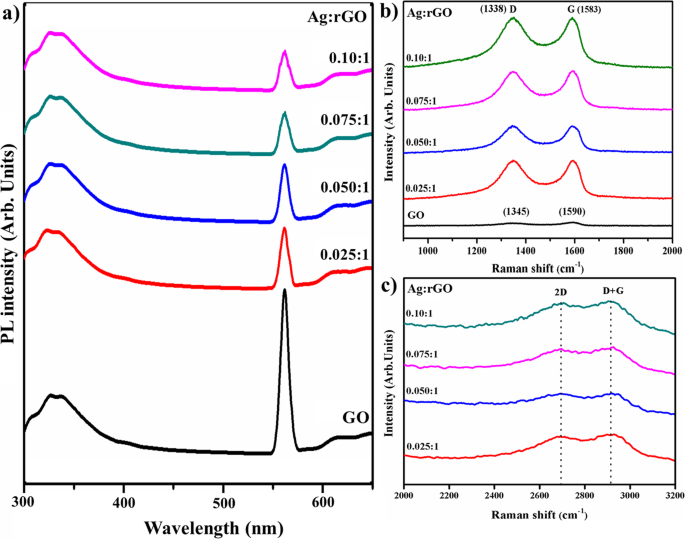
een PL-spectra. b Raman-spectra van bereide monsters. c Zoomgebied van Raman-spectra
Raman-spectroscopie werd ingezet om elektronische en structurele eigenschappen van het controlemonster en Ag@rGO te onderzoeken voor het onderscheiden van geordende en ongeordende koolstofstructuren zoals aangetoond in Fig. 7b, c. In het geval van GO bevinden zich twee banden op ~ 1340 en ~ 1590 cm −1 respectievelijk toegewezen als D- en G-band. De D-band is toegewezen aan de ademhalingsmodus van k punt fononen met A1g symmetrie en band van sp 3 koolstof atomen; G-band suggereert een karakteristieke piek van sp 2 hybride structuur die symmetrie en kristalliseerbaarheid van koolstof onthult en E2g . introduceert fononverstrooiing van koolstofatomen [32, 33, 36]. Bovendien is de D-band duidelijk voor oppervlaktedefecten en ontstaan structurele onvolkomenheden met aangehechte hydroxyl- en epoxidefunctiegroepen met koolstofbasisvlakken [36]. De G-band is alleen Raman-modus in grafeen afkomstig van een conventioneel eerste-orde Raman-verstrooiingsproces en komt overeen met in-plane zone center, dubbel gedegenereerde fonon-modus (transversaal (TO) en longitudinaal (LO) optisch) met E2g symmetrie [42]. In het geval van Ag-rGO Raman-spectrum waargenomen bij 1338 cm −1 (D-band), 1583 cm −1 (G-band) en 2682 cm −1 (2D-band) er is een extra piek gecentreerd op 2900 cm −1 (D + G-band) die stoornis vertegenwoordigt als gevolg van combinatieverstrooiing in Fig. 7b, c [31, 35, 42,43,44,45]. De D- en 2D-modi zijn afkomstig van het tweede-orde dubbele resonantieproces tussen niet-equivalente k-punten in de Brillouin-zone (BZ) van grafeen, aangezien de 2D-band de tweede orde van de D-band aangeeft, wat verwijst naar de boventoon van de D-band met zijn bestaan als gevolg van twee vibratieprocessen van telefoonroosters; desalniettemin is het niet geassocieerd met defecten zoals de D-band in figuur 7c [35, 41]. De variaties in relatieve intensiteiten van de G- en D-band in Raman-spectra van GO tijdens reductie worden meestal aangeduid als een verandering in de elektronische conjugatietoestand. Deze wijziging suggereert een toename van het aantal sp 2 atomaire domeinen na de reductie van GO [46]. De intensiteitsverhouding van de D- tot G-band definieert de mate van wanorde in grafietlagen; ID /IG =0,87 voor een gedoteerd vrij monster (GO), ID /IG =1,15 voor met Ag gedoteerde monsters en een toename van de verhouding duidt op een afname van de gemiddelde grootte van sp 2 koolstofdomeinen na synthese van Ag@rGO, terwijl intensiteitsverhouding tussen 2D en G-band (I2D /IG ) wat 1,69 is, zijn gebruikt om de elektronenconcentratie in rGO te onderzoeken [31, 32, 35, 47].
Ag-nanodeeltjes, wanneer ze zijn gedoteerd in een halfgeleidermateriaal, genereren een contactpotentiaalverschil vanwege hun verschillende werkfuncties. Dit potentiaalverschil wordt de Schottky-barrière genoemd. Zoals getoond in Fig. 8, is de bandbuiging wanneer een contact wordt gevormd na het bereiken van een evenwicht afhankelijk van de relatieve energieën van de werkfuncties van metaal (ϕM ) en de halfgeleidende (ϕB ) componenten. Dit fenomeen kan de efficiëntie van de ladingsscheiding aanzienlijk verbeteren, zodra het de gerichte migratie van fotogegenereerde elektronen van de halfgeleider naar het metaal kan induceren. Met andere woorden, het kan leiden tot het genereren van een effectieve elektronenvangplaats om de elektron-gat-recombinatie te onderdrukken [48].
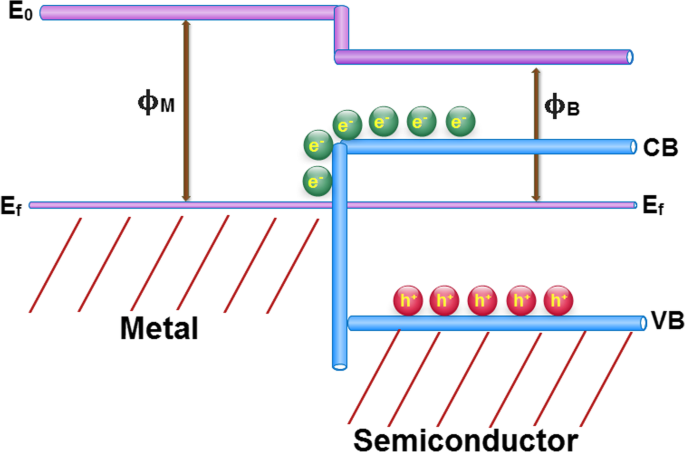
Kwalitatieve elektronische bandstructuur van met Ag versierde nanosheets
De fotokatalytische activiteit van GO- en Ag / rGO-nanobladen trad op vanwege hun hoge oppervlakte en lage bandgap-energie. Ag / rGO vertoont dus een aanzienlijke verbetering in de fotodegradatie van MB en de kleurstof degradeert volledig (figuur 9b) in 120 min. De pseudo-eerste-ordevergelijking kan worden gebruikt om expliciet de fotokatalytische efficiëntie (Fig. 8a) van GO- en Ag / rGO-monsters uit te werken, met behulp van de volgende uitdrukking.
$$ -\mathit{\ln}\left({C}_t/{C}_o\right)=kt $$ (9)waarbij Co de beginconcentratie van de kleurstof is en C t is de concentratie op het moment, k is de schijnbare snelheidsconstante van het afbraakproces die wordt weergegeven in de absorptiegrafiek (Fig. 9a), d.w.z. de waarde van k voor GO is ongeveer 0,1300 min −1 en k neemt buitengewoon toe in het geval van Ag/rGO (0,1300 min −1 tot 0,7459 min −1 ). Figuur 9c onthult compressie van % degradatie in de tijd, GO toont 65% efficiëntie en een geleidelijke toename met dopingconcentratie. Ag/rGO (0.10:1) vertoont een maximaal percentage afbraak tot 100%, wat waarschijnlijk te wijten is aan synergetische effecten van Ag NP's [49, 50]. Ten slotte kan op basis van deze bevindingen in de huidige studie worden gesuggereerd dat Ag/rGO een uitstekend product is dat kan worden gebruikt voor het zuiveren van water uit organische kleurstoffen.
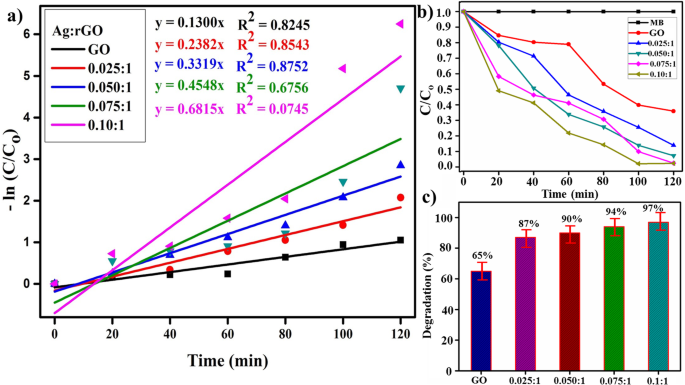
een Plot van -ln (Ct/C0) versus tijdspectra voor kleurstofreductie. b Plot van concentratieverhouding (C/C0 ) versus tijd. c Degradatie (%) vergelijking van alle monsters
Conclusie
GO werd met succes verkregen via de gemodificeerde hummers-methode en rGO werd gesynthetiseerd uit thermische behandeling tijdens het inbrengen van Ag (2,5, 5, 7,5 en 10 wt.%) via hydrothermale route. Volgens het XRD-patroon wijzen piekverschuiving en afname in d-afstand (0,34 tot 0,023 nm) in de richting van redoxreactie van GO na Ag-doping met hexagonale kristalstructuur; gemiddelde toename van de kristallietgrootte (4,85 tot 15,6 nm) met vervanging van Ag wordt waargenomen. FTIR-spectra bevestigde transmissiepiek rond 650 cm −1 wat een vingerafdrukgebied is van gehybridiseerde sp 2 koolstofbinding toegewezen als CH-buigingstrillingen en onthult informatie over andere bijgevoegde functionele groepen. De karakteristieke piek toegeschreven aan π –π * en n –π * bonding en roodverschuiving in pieken. Het onderschrijft de aanwezigheid van Ag zoals opgehelderd met UV-Vis-spectroscopie, een duidelijke afname van de bandgap-energie (4,10 tot 3,50 eV) met een verhoogde dopingverhouding die werd berekend met behulp van de Tauc-vergelijking. Morfologische kenmerken tonen stapellagen van GO en Ag / rGO met een roosterafstand van ~ 0,235 nm, bolvorm en grootte (10-12 nm) van Ag NP's gevisualiseerd door HR-TEM. De koolstofatomen van de lokale staat sp 2 clusters opgenomen met sp 3 matrix, significante piekafname bij rGO en uitgebreide sp 2 koolstofcluster na doping werd bevestigd met PL-spectra. A1g symmetrie in sp 3 koolstofatomen op D-band, sp 2 hybride structuur die symmetrie en kristalliseerbaarheid van koolstof onthult en E2g fonon-verstrooiing van een koolstofatoom introduceert en oppervlaktedefecten werden berekend via Raman-spectra. Fotokatalytische activiteit reageert op Ag/rGO (0,10:1) en degradeert 100% van de MB-concentratie. Deze bevindingen suggereren dat bereide nanokatalysatoren geen gevaarlijk gedrag vertonen bij waterbehandeling en een uitstekende nanokatalysator zijn voor de verwijdering van organische verontreinigende stoffen uit afvalwater.
Beschikbaarheid van gegevens en materialen
Alle gegevens zijn onbeperkt beschikbaar.
Afkortingen
- UV-Vis:
-
Ultraviolette zichtbare spectroscopie
- XRD:
-
Röntgendiffractie
- FTIR:
-
Fourier-transformatie infraroodspectroscopie
- EDS:
-
Energiedispersieve röntgenspectroscopie
- SEM:
-
Scanning elektronenmicroscopie
- TEM:
-
Transmissie-elektronenmicroscopie
- JCPDS:
-
Paritair comité voor poederdiffractienormen
Nanomaterialen
- Verlaag de operationele kosten met effectieve waterbehandelingsprogramma's
- Temperatuurafhankelijke kristallisatie van MoS2-nanovlokken op grafeen-nanobladen voor elektrokatalyse
- Hydrothermische synthese van In2O3 nanodeeltjes hybride tweeling hexagonale schijf ZnO heterostructuren voor verbeterde fotokatalytische activiteiten en stabiliteit
- synergetische effecten van Ag-nanodeeltjes/BiV1-xMoxO4 met verbeterde fotokatalytische activiteit
- One-Pot-synthese van Cu2ZnSnSe4-nanoplaten en hun door zichtbaar licht aangedreven fotokatalytische activiteit
- Eenstaps-kogelfreesvoorbereiding van CL-20/grafeenoxide op nanoschaal voor aanzienlijk kleinere deeltjesgrootte en gevoeligheid
- Op grafeenoxide gebaseerde nanocomposieten versierd met zilveren nanodeeltjes als antibacterieel middel
- De anionische oppervlakteactieve stof/ionische vloeistoffen geïntercaleerd gereduceerd grafeenoxide voor krachtige supercondensatoren
- Een gemakkelijke aanpak voor de bereiding van zinkoxide van nanoformaat in water/glycerol met extreem geconcentreerde zinkbronnen
- Millstone Exfoliation:een True Shear Exfoliation voor grootschalig grafeenoxide met weinig lagen
- Gemakkelijke synthese en verbeterde fotokatalytische activiteit van zichtbaar licht van nieuwe p-Ag3PO4/n-BiFeO3-heterojunctie-composieten voor degradatie van kleurstoffen



