Verbeterde Cocatalyst TiO2/Fe2O3-fotoanodes met patroon voor watersplitsing
Abstract
In deze studie hebben we een heetpersproces gebruikt om de fotokatalytische eigenschappen van TiO2 te verbeteren. /Fe2 O3 bimetaaloxide met een periodieke patroonstructuur op het oppervlak om de fotonabsorptie te verhogen voor fotokatalyse in de zuurstofontwikkelingsreactie voor watersplitsing. De warmgeperste monsters laten zien dat het combineren van de twee metaaloxiden de absorptiebandrand van de elektrode bij verschillende golflengten verbetert. De patroonstructuur die is verkregen met behulp van het heetpersproces verbetert met succes de fotonenabsorptie, wat resulteert in een tweevoudige verbetering in vergelijking met een elektrode met een plat oppervlak.
Inleiding
Fotokatalytische ontleding voor het splitsen van water om zuurstof te produceren is een veel bestudeerd systeem voor het omzetten van lichtenergie [1,2,3,4]. Wanneer fotonen met verschillende golflengten op een halfgeleiderfotokatalysator worden gestraald, beweegt hun energie de elektronen van de valentieband, waardoor ze naar de geleidingsband springen. Een door foto gegenereerd gat wordt gevormd in de valentieband en de aangeslagen elektronen in de geleidingsband ondergaan een reductiereactie met watermoleculen om waterstof te produceren via de zogenaamde waterstofevolutiereactie (HER) [5]. Dit gat domineert de zuurstofproductie via de zogenaamde zuurstofevolutiereactie (OER) [6]. De rand van de geleidingsband van het fotokatalysatormateriaal van de halfgeleider moet zich boven de H + bevinden /H2 energieniveau verlagen. De foto-elektronen in de fotokatalysator kunnen water reduceren tot waterstof. Omdat het oxidatie-reductiepotentiaalverschil van de watersplitsingsreactie echter 1,23 eV is, moet het energieniveau van de valentieband van de fotokatalysator lager zijn dan het oxidatie-energieniveau van O2 /H2 O om water te oxideren tot zuurstof.
Om dit doel te bereiken is de aanpassing van de benodigde energie en de afstemming van het zonnestralingsspectrum van belang [1]. De meeste eerdere studies hebben edele metalen zoals Pt en Au als katalysatoren gebruikt [2, 5,6,7]; deze zijn echter duur en schaars, en daarom zijn er studies uitgevoerd om alternatieve katalytische materialen te vinden. In dit opzicht hebben typische halfgeleidermetaaloxiden veel aandacht getrokken. Overvloedige metaaloxiden zoals titaniumdioxide (TiO2 ) [8, 9], WO3 [10, 11], BiVO4 [12, 13], CuO2 [14, 15] en ijzeroxide (Fe2 O3 ) [16, 17] verbeteren fotonabsorptie door hun n- of p-type halfgeleidereigenschappen en energiekloof matching; daarom vertonen ze een hoge fotokatalytische efficiëntie over een groot golflengtebereik. De fotonenergie van een specifieke golflengte kan de scheiding van elektron-gatparen veroorzaken, waardoor de omzetting van lichtenergie in chemische energie verder wordt bevorderd. TiO2 [18,19,20,21] en Fe2 O3 [22, 23] worden vaak gebruikt voor fotokatalyse omdat ze voordelen bieden zoals eenvoudige bereiding, hoge chemische stabiliteit, lage kosten, niet-toxiciteit en corrosieweerstand; verder de energiekloof van TiO2 (3.2 eV) vertoont een goede overeenkomst met de energiekloof (2.2 eV) van Fe2 O3 [24, 25], zoals weergegeven in Fig. 1a. Dankzij deze eigenschap kan de bimetaalhalfgeleider die wordt gevormd door deze twee metaaloxiden te combineren, meer dan 30% van de bandafstand effectief absorberen. Zonlicht [26] kan het fotokatalytische effect van de elektrode effectief versterken.
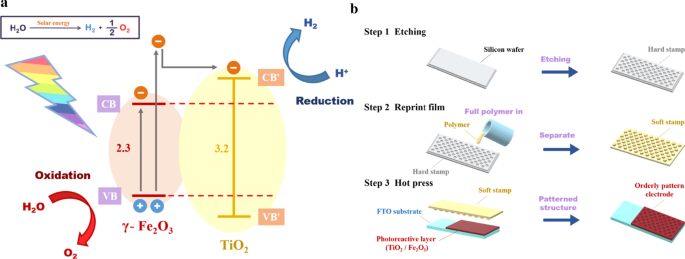
een Water-splitsend reactiemechanisme in TiO2 /Fe2 O3 bimetaal halfgeleidersysteem. b Fabricage van patroon met behulp van een heetpersproces
De dimensionale structuur van het elektrodeoppervlak beïnvloedt ook de foto-elektrochemische eigenschappen. Met name periodieke microstructuren hebben veel belangstelling gewekt op het gebied van optica. Yablonovitch en John beschreven dit concept in 1987 [27]. Ze wilden een medium ontwerpen dat fotonen kan opvangen om het energieverbruik en afval te verminderen. Na meerdere jaren van onderzoek ontdekten ze dat een medium met een bepaalde periodieke structuur op het oppervlak fotonen effectief vangt [28, 29] zonder de intrinsieke chemische eigenschappen van materie te veranderen om de vereiste optische eigenschappen te verkrijgen. Tot dusverre hebben veel onderzoeken naar zonne-energie materialen geselecteerd met periodieke structuren om de absorptie van fotonenenergie te verhogen [30]. Verder, omdat een periodieke microstructuur het reactiegebied van het elektrodeoppervlak drastisch vergroot, zal de verkregen stroomrespons ook aanzienlijk worden verbeterd.
In deze studie hebben we een eenvoudig patroon gefabriceerd met behulp van een heetpersproces op het fotoanode-oppervlak, zoals weergegeven in figuur 1b, en een etsmethode gebruikt om een origineel substraat met een periodieke oppervlaktestructuur te vormen. Het originele substraat wordt opnieuw gevormd door een polymeer om te dienen als een nieuw stempelsubstraat dat vervolgens wordt gebruikt als een mal met de voorbereide laag van de TiO2 /Fe2 O3 cokatalysator. Ten slotte wordt een heetpersproces uitgevoerd om een periodieke microstructuur te verkrijgen. Dit proces verbetert de overdrachtssnelheid van de drager door een verbeterd interfacecontact binnen het cokatalysatormateriaal en verbetert de lichtabsorptie-efficiëntie door extra lichtopsluiting en verstrooiing van de oppervlaktepatronen.
Methoden
Voorbereiding van de Fe2 O3 en TiO2 Poeder
FeCl2 en FeCl3 werden opgelost in gedeïoniseerd water, geroerd om een oplossing te vormen, snel in een natriumhydroxideoplossing gegoten en tenslotte 30 minuten bij 80 ° C geroerd. Nadat de oplossing grondig was gemengd, liet men deze 30 minuten staan totdat het product neersloeg. De bovenlaagoplossing werd verwijderd; het neerslag werd gewassen met aceton, ethanol en gedeïoniseerd water; en het werd 12 uur gedroogd bij 120 °C om Fe3 . te verkrijgen O4 (zwart poeder). Dit poeder werd opgelost in alcohol en 30 min krachtig geroerd om een roodbruine Fe2 te verkrijgen O3 suspensie oplossing. Ten slotte, de neergeslagen Fe2 O3 werd in een kwartsboot geplaatst die op zijn beurt gedurende 3 uur in een sinteroven bij 450 ° C werd geplaatst en vervolgens op natuurlijke wijze afgekoeld tot kamertemperatuur om Fe2 te verkrijgen O3 poeder met een hematietfase. Een TiO2 voorloperoplossing werd verkregen door de toevoeging van tetraethyltitaanzuur aan n-propanol om een voorloperoplossing te bereiden, gevolgd door de toevoeging van zwavelzuur en roeren bij kamertemperatuur, waarbij men deze 2 uur bij 25 °C laat staan om een doorschijnende gel te vormen, in een oven van 50 °C plaatsen, opwarmen en natuurlijk afkoelen tot kamertemperatuur.
Bereiding van de bimetaaloxide-colloïdale oplossing
Ten slotte hebben we 7 gew.% polyvinylalcohol (PVA) bereid, 1 ml gedeïoniseerd water toegevoegd en 30 minuten op een hete plaat bij 120 ° C geplaatst. Vervolgens hebben we de PVA geroerd om het effectief op te lossen in gedeïoniseerd water om oplossing A te verkrijgen. We hebben 20 mg Fe2 bereid O3 poeder en 98 µL TiO2 oplossing om op te lossen in 1 ml N-methyl-2-pyrrolidon (NMP), plaatste het in een ultrasone oscillator, schudde het gedurende 30 minuten om vaste oplossingen te verkrijgen, en plaatste ze gedurende 30 minuten in een ultrasone oscillator om de uiteindelijke halfgeleider te verkrijgen bimetaaloxide colloïdale oplossing.
Voorbereiding van de periodieke structuur op de elektroden
We gebruikten het afdruklithografieproces om de siliciumwafel voor de zachte stempel te fabriceren [31,32,33]. Bovendien hebben we, om de zachte stempel te maken, eerst aceton, ethanol en water gebruikt om de siliciumwafel te trillen na het 20 minuten durende etsproces om het bord te reinigen en vervolgens op een verwarmingsplaat bij 40 ° C te plaatsen om te drogen. Tegelijkertijd werd de epoxyhars geactiveerd en vervolgens plat op het oorspronkelijke substraatoppervlak gelegd totdat het droog was. Na droging werd de epoxyhars van de oorspronkelijke ondergrond afgescheurd om de gewenste zachte stempel te verkrijgen. We hebben 100 µL van de halfgeleider bimetaaloxide colloïdale oplossing aangebracht op de TiO2 filmoppervlak en hield het gedurende 1 uur bij kamertemperatuur totdat de colloïdale oplossing veranderde in een gelei-achtige toestand, en vervolgens voerden we het heetpersproces gedurende 15 minuten uit. Ten slotte werd de fotoanode met patroon gedurende 3 uur in een sinteroven bij 500 ° C in een argonatmosfeer geplaatst om de fotoanode met patroon met een periodieke structuur te verkrijgen. De OER-prestaties van de fotoanode werden onderzocht met behulp van de verbindingsmethode met drie elektroden. Het systeem omvatte de werkelektroden, een tegenelektrode (koolstofstaaf) en een referentie-elektrode (Ag/AgCl) in 1 M KOH als elektrolyt.
Resultaten en discussie
De structuur met oppervlaktepatroon werd geverifieerd zoals weergegeven in figuur 2. Figuur 2a toont een scanning elektronenmicroscoop (SEM) afbeelding van de siliciumwafel als een moedervormsubstraat. Het oppervlak had periodiek opgestelde cirkelvormige gaten, elk met een langwerpige opening van 2 µm. Afbeelding 2b toont een afbeelding van het overeenkomstige omgekeerde patroon op het epoxyharsoppervlak. De epoxyhars repliceerde met succes de hele structuur van het oorspronkelijke patroon van het Si-substraat, dat dienovereenkomstig periodiek gerangschikte cilindrische structuren met een diameter van 2 m vertoonde. Ten slotte hebben we onderzocht of de overeenkomstige periodieke structuur met patroon via het heetpersproces op het elektrodeoppervlak wordt overgebracht. Afbeelding 2c toont het patroon TiO2 /Fe2 O3 fotoanode voor en na bestraling met zichtbaar licht. Deze afbeelding laat zien dat het elektrode-oppervlak er zwart uitziet als het niet verlicht is. Het vertoont echter een merkbare regenboogkleur onder bestraling met zichtbaar licht, wat impliceert dat het invallende licht aanzienlijk wordt opgesloten en vele malen wordt gebroken in de periodieke patroonstructuur. Afbeelding 2d, e toont SEM-afbeeldingen van het oppervlak van een TiO2 . met patroon /Fe2 O3 fotoanode onder verschillende vergrotingen en hoeken. Het oppervlak van de foto-elektrode vertoonde een cyclus die vergelijkbaar was met die van een moederbord van een siliciumwafeltje. De poriegrootte was ongeveer 2 µm, wat bevestigt dat we met succes microstructuren met periodiek patroon op het elektrode-oppervlak hebben gedrukt. Ten slotte presenteert Fig. 2f een dwarsdoorsnede die is geproduceerd door het elektrodeoppervlak te snijden met behulp van een gefocusseerde ionenstraal (FIB). De afbeelding in dwarsdoorsnede toont ook de cirkelvormige gatenvorm van deze periodieke patroonstructuur, met een gatdiepte van 0,642 µm. We hebben ook met succes het anodische aluminiumoxide als stempel gebruikt om een kleiner patroon te fabriceren, en de SEM-afbeeldingen zijn te vinden in aanvullend bestand 1:Fig. S1.

een SEM-afbeelding van siliciumwafel bereid met behulp van de etsmethode. b Zachte stempel gemaakt van siliconenwafel met omgekeerde pilaarstructuur. c Foto's gemaakt met en zonder lichtinstraling. d –e SEM-beeld onder verschillende vergrotingen en hoeken. v Dwarsdoorsnede van het elektrode-oppervlak van TiO2 /Fe2 O3 bestelde fotoanode met patroon
Om de voorgestelde TiO2 . te karakteriseren /Fe2 O3 fotoanode met patroon, voerden we FIB-transmissie-elektronenmicroscoop (TEM) -analyse uit. Afbeelding 3a geeft het resultaat weer van de elementverdelingsanalyse (EDS-toewijzing) van de TiO2 /Fe2 O3 fotoanode met patroon. Fe, Ti en O waren uniform verdeeld in de elektrode en het C-signaal kwam voort uit de PVA- en NMP-bindmiddelen; dit had echter geen invloed op de verdeling van de primaire materialen, namelijk TiO2 en Fe2 O3 . Afbeelding 3b geeft STEM-afbeeldingen weer die zijn verkregen onder verschillende vergrotingen. TiO2 en Fe2 O3 poeders vertoonden korrelige morfologieën. Zoals weergegeven in figuur 3c, zijn de roosterparameters van Fe2 O3 en TiO2 werden door de analyse bepaald op respectievelijk 0,28 en 0,31 nm, wat aangeeft dat het heetpersproces roostervervorming veroorzaakte in zowel Fe2 O3 en TiO2 .
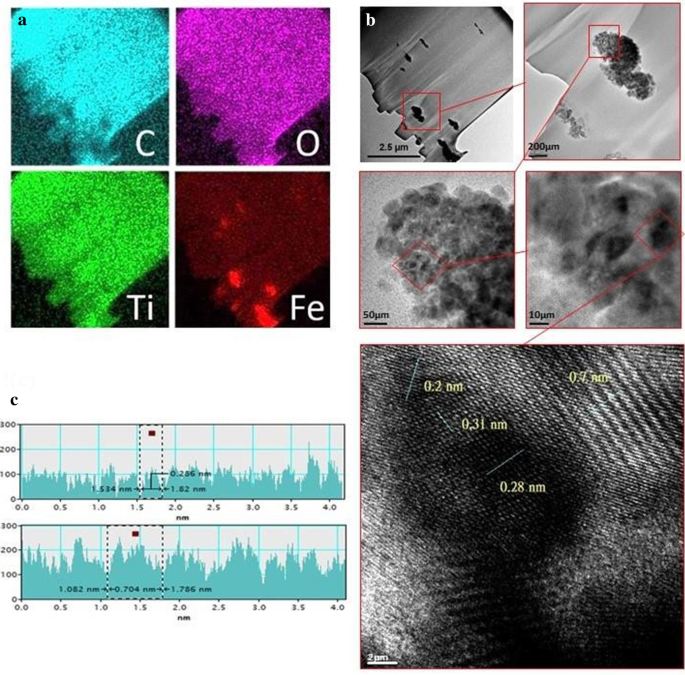
FIB-TEM afbeelding van TiO2 /Fe2 O3 -bestelde fotoanode met patroon met a EDS-toewijzing van C, O, Ti en Fe. b STEM-afbeeldingen met verschillende vergrotingen. c Analyse van Fe2 O3 en TiO2 roosters
Verder hebben we röntgenfoto-elektronspectroscopie (XPS) uitgevoerd om de chemische toestanden van elementen te bepalen. Afbeelding 4 geeft de resultaten weer van de fijne scanspectrumanalyse die is uitgevoerd met XPS voor de zes elementen in de fotoanode, en het volledige XPS-onderzoeksspectrum kan ook worden verkregen in aanvullend bestand 1:Fig. S2. In figuur 4a toont de C 1s-orbitaal signalen die overeenkomen met een enkele C-C-binding en een enkele C-O-binding bij een bindingsenergie van 284,9 eV. In Fig. 4b toont de O 1s-orbitaal een signaal van de C =O dubbele binding bij een bindingsenergie van 532,5 eV, wat bevestigt dat er veel geoxideerde koolstoffen op het elektrodeoppervlak voorkomen en een signaal van de O van de oxiden bij een bindingsenergie van 530 eV. In figuur 4c toont de N 1s-orbitaal signalen van de N-H-binding bij bindingsenergieën van 397,2 en 400 eV. De binding N en metaalionen kunnen het gevolg zijn van de binding tussen N en een kleine hoeveelheid overgangsmetaalelementen wordt ook gezien. In figuur 4d worden Fe 2p2/3- en Fe 2p1/3-signalen gezien bij bindingsenergieën van respectievelijk 711,3 en 724,8 eV, en satellietpieken van Fe 2p2/3 en Fe 2p1/3 worden gezien bij bindingsenergieën van 720 en 731,3 eV, respectievelijk; dit zijn typische Fe2 O3 configuratie signalen. In Fig. 4e worden Ti 2p3/2 en Ti 2p1/2 signalen gezien bij bindingsenergieën van respectievelijk 457,9 en 464,3 eV; deze worden gegenereerd door TiO2 . In Fig. 4f worden Sn 3d3/2 en Sn 3d5/2 signalen gezien bij bindingsenergieën van respectievelijk 285,9 en 495,1 eV; deze worden gegenereerd door de SnO2 substraat.
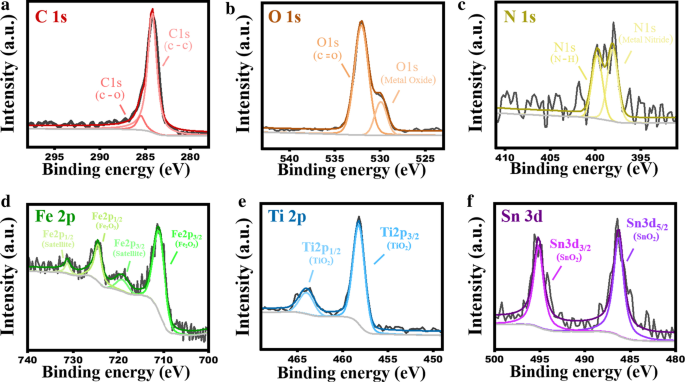
XPS-spectra van TiO2 /Fe2 O3 -bestelde fotoanode met patroon voor a C 1s, b O 1s, c N 1s, d Fe 2p, e Ti 2p en f Sn 3d
Om het effect van patroonstructuren op de lichtabsorptie van de fotoanode aan te tonen, hebben we voor en na het heetpersproces ultraviolet-zichtbare spectroscopie (UV-Vis) uitgevoerd, zoals weergegeven in figuur 5a. Vanwege het co-katalysatoreffect van de TiO2 en Fe2 O3 metaaloxiden, vertoonde de fotoanode lichtabsorptie over een breed bereik van 400-600 nm. Vergeleken met de elektrode vóór het patroonvormingsproces, vertoonde de fotoanode extra lichtabsorptie als gevolg van verbeterde lichtverstrooiing en absorptie van de periodieke patroonstructuur op het oppervlak. Deze verbetering wordt ook weerspiegeld in de lineaire scanning voltammetrie (LSV) getoond in Fig. 5b; de TiO2 /Fe2 O3 monster geproduceerd met behulp van het heetpersproces vertoonde de hoogste reactiestroom tijdens de LSV-scan. Verder zijn de EIS-meting en de Tafelhelling terug te vinden in het Aanvullend bestand 1:Fig. S3 en S5. Bovendien hebben we een fotoresponsonderzoek uitgevoerd onder nul bias en bestraling met wit licht, en dit monster vertoonde een tweevoudige verbetering vergeleken met de TiO2 /Fe2 O3 monster geproduceerd zonder gebruik van het heetpersproces en zevenvoudige stroomverbetering vergeleken met TiO2 alleen, zoals weergegeven in Fig. 5c. We hebben ook de groene laser met een golflengte van 532 nm en de rode laser met 633 nm geselecteerd voor de meting, en het resultaat is te vinden in Aanvullend bestand 1:Fig. S4.
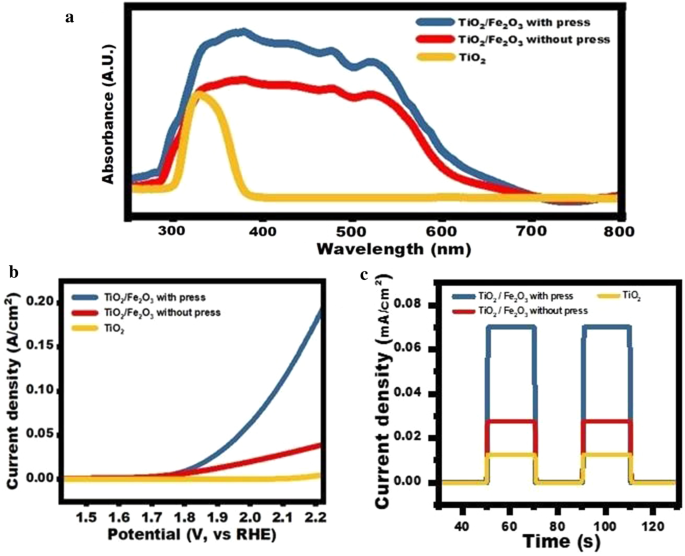
een UV-Vis absorptiespectra. b LSV-swipe-scan. c Fotoreacties van verschillende fotoanodes
Conclusie
In deze studie hebben we een eenvoudig heetpersproces gedemonstreerd om een periodiek patroon te fabriceren op een TiO2 /Fe2 O3 cokatalysator bimetaaloxide fotoanode. Een duidelijk periodiek patroon van gaten werd gereproduceerd op het oppervlak van de fotoanode. Een breedband UV–Vis-absorptiespectrum van de TiO2 /Fe2 O3 bimetaaloxide werd verkregen en vertoonde lichtabsorptie over een breed bereik van 400-600 nm. Eindelijk, de TiO2 /Fe2 O3 cokatalysator met een patroonoppervlak vertoonde een aanzienlijk verbeterde fotostroom dankzij de extra lichtabsorptie en verstrooiing van de oppervlaktestructuur.
Beschikbaarheid van gegevens en materialen
Alle gegevens die tijdens dit onderzoek zijn gegenereerd of geanalyseerd, zijn opgenomen in dit gepubliceerde artikel [en de ondersteunende informatiebestanden].
Afkortingen
- OER:
-
Zuurstofontwikkelingsreactie
- HAAR:
-
Reactie waterstofontwikkeling
- PVA:
-
Polyvinylalcohol
- NMP:
-
N-methyl-2-pyrrolidon
- SEM:
-
Scanning elektronenmicroscoop
- FIB:
-
Gefocuste ionenstraal
- TEM:
-
Transmissie elektronenmicroscoop
- EDS:
-
Energiedispersieve spectroscopie
- STEM:
-
Scanning transmissie-elektronenmicroscopie
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- UV–Vis:
-
Ultraviolet-zichtbare spectroscopie
- LSV:
-
Lineaire scanning voltammetrie
Nanomaterialen
- Bandtheorie van vaste stoffen
- Nanovezels en filamenten voor verbeterde medicijnafgifte
- Vooruitgang in op ijzeroxide gebaseerde nanostructuren voor toepassingen in energieopslag
- S, N co-gedoteerde grafeen Quantum Dot/TiO2-composieten voor efficiënte fotokatalytische waterstofgeneratie
- Een nieuwe methode zonder organisch oplosmiddel voor gerichte nanodrug voor verbeterde werkzaamheid tegen kanker
- Verbeterde prestaties van een nieuwe anodische PdAu/VGCNF-katalysator voor elektro-oxidatie in een glycerolbrandstofcel
- Een efficiënt en effectief ontwerp van InP-nanodraden voor maximale oogst van zonne-energie
- Een nanokristallijne Fe2O3-filmanode bereid door gepulseerde laserafzetting voor lithium-ionbatterijen
- Invloed van Mg-doping op ZnO-nanodeeltjes voor verbeterde fotokatalytische evaluatie en antibacteriële analyse
- Theoretisch systeem van contact-mode tribo-elektrische nanogeneratoren voor een hoge energieconversie-efficiëntie
- 5 tips voor energiezuinige perslucht



