Een ternair magnetisch recyclebaar ZnO/Fe3O4/g-C3N4 composiet fotokatalysator voor efficiënte fotodegradatie van monoazo kleurstof
Abstract
Om een zeer efficiënte door zichtbaar licht geïnduceerde en gemakkelijk recyclebare fotokatalysator te ontwikkelen, werd in deze studie een ternair magnetisch ZnO/Fe3 O4 /g-C3 N4 samengestelde fotokatalysator werd gesynthetiseerd voor de fotodegradatie van Monas-kleurstof. De structuur en optische prestaties van de samengestelde fotokatalysator werden gekarakteriseerd met behulp van röntgendiffractie (XRD), transmissie-elektronenmicroscopie (TEM), energiedispersieve spectroscopie (EDS), fotoluminescentie (PL) spectra, ultraviolet-zichtbare diffuse reflectie en foto-elektrochemie . De fotokatalytische activiteiten van het bereide ZnO/Fe3 O4 /g-C3 N4 nanocomposieten waren aanzienlijk verbeterd, en ze waren significant hoger dan die van pure g-C3 N4 en ZnO. Gezien de aanwezigheid van de heterojunctie tussen de interfaces van g-C3 N4 en ZnO, de hogere respons op zichtbaar licht en scheidingsefficiëntie van de foto-geïnduceerde elektronen en gaten verbeterde de fotokatalytische activiteiten van de ZnO/Fe3 O4 /g-C3 N4 nanocomposieten. Het stabiliteitsexperiment onthulde dat ZnO/Fe3 O4 /g-C3 N4 -50% vertoont een relatief hogere fotokatalytische activiteit na 5 recycles. De degradatie-efficiëntie van MO, AYR en OG over ZnO/Fe3 O4 /g-C3 N4 -50% was respectievelijk 97,87%, 98,05% en 83,35%, wat te wijten was aan het aantal kleurstofmoleculen dat op de fotokatalysator was geadsorbeerd en de structuur van het azokleurstofmolecuul. Azokleurstoffen zouden effectief en snel door de verkregen fotokatalysator kunnen worden afgebroken. Daarom zou de milieuvriendelijke fotokatalysator op grote schaal kunnen worden toegepast bij de behandeling van met kleurstof verontreinigd afvalwater.
Inleiding
Als een belangrijk mondiaal milieuprobleem wordt een aanzienlijke hoeveelheid verontreinigende stoffen geloosd in de meren, rivieren en grondwater als gevolg van snelle industrialisatie, wat leidt tot watervervuiling. Geschat wordt dat ongeveer 10-15% van de organische kleurstoffen vrijkomt, wat kankerverwekkende en mutagene effecten heeft op mensen [1]. Daarom worden momenteel methoden onderzocht die industrieel afvalwater afbreken, met name organische kleurstoffen. Van de verschillende methoden werd het gebruik van een fotokatalytische technologie met fotokatalysatoren om milieuverontreinigende stoffen af te breken als een mogelijke benadering beschouwd [2, 3].
Bovendien is ZnO een van de meest gebruikte fotokatalyse, gezien de hoge lichtgevoeligheid, de lage kosten en het milieuvriendelijke karakter ervan [4, 5]. Puur ZnO kent echter drie belangrijke nadelen. Ten eerste kan het alleen ultraviolet (UV) licht van zonne-energie absorberen met een golflengte van minder dan 368 nm vanwege de brede bandafstand (3,37 eV), wat de praktische toepassingen beperkt wanneer zonlicht de energiebron is [6]. Ten tweede leidt een snellere recombinatie van de fotogegenereerde elektron-gatparen tot een lagere fotokatalytische activiteit [7]. Ten derde is de herwinning van ultrafijne ZnO-nanodeeltjes uit het afvalwater met behulp van filtratie en centrifugatie moeilijk te bereiken, wat de grootschalige praktische toepassingen in de industrie beperkt. Daarom zijn er de afgelopen jaren verschillende pogingen ondernomen om multifunctionele fotokatalysatoren te ontwikkelen op basis van ZnO-nanomaterialen, met een hoge recycleerbaarheid en uitstekende fotokatalytische prestaties in het UV- en zichtbare stralingsbereik.
Daarom werden verschillende strategieën geïmplementeerd om de eerste en tweede nadelen van ZnO te overwinnen, zoals doping, oppervlaktemodificatie met metalen nanodeeltjes en de ontwikkeling van heterostructuur [8,9,10]. Hiervan kan het koppelen van ZnO met een halfgeleider met smalle bandafstand en een hoge geleidingsband (CB) het bereik van lichtabsorptie effectief vergroten en de scheidingssnelheid van de elektron-gatparen versnellen. Grafietachtig koolstofnitride (g-C3 N4 ), met een band gap van 2,70 eV, werd onderzocht als een veelbelovend metaalvrij materiaal voor de omzetting van zonne-energie in elektriciteit of chemische energie [11, 12]. Bovendien trok het veel aandacht vanwege zijn uitstekende fotokatalytische prestaties, chemische en thermische stabiliteit en gunstige elektronische structuur, gezien de sterke covalente bindingen tussen de koolstof- en stikstofatomen. Een hoge recombinatiesnelheid van foto-geïnduceerde elektron-gatparen beperkte echter de verbeterde fotokatalytische prestaties [13]. Halfgeleiders met brede bandgap kunnen worden gecombineerd met g-C3 N4 om een verbeterde ladingsscheiding te bereiken [7, 14, 15]. Gebaseerd op de bovengenoemde methoden, de combinatie van ZnO (wide-bandgap halfgeleider) en g-C3 N4 (smalle bandgap halfgeleider) als een samengestelde fotokatalysator voorkomt de recombinatie van fotogegenereerde elektron-gatparen en breidt het lichtabsorptiebereik van ZnO uit tot het zichtbare lichtspectrum. In de meeste van de gerapporteerde werken, ZnO/g-C3 N4 fotokatalysatoren hebben een lage katalytische prestatie en zijn moeilijk terug te winnen en opnieuw te gebruiken. Gelukkig, Fe3 O4 werd veel gebruikt bij de bereiding van magnetische fotokatalysatoren, vanwege de goede magnetische lage kosten, goede stabiliteit en milieuvriendelijke aard [16]. Vandaar de voorbereiding van nieuwe door zichtbaar licht aangedreven magnetische ZnO/Fe3 O4 /g-C3 N4 fotokatalysatoren is significant, en het is belangrijk om de fotokatalytische efficiëntie verder te verbeteren. Bovendien is nog niet gerapporteerd hoe de structuur van monoazokleurstoffen het fotodegradatieproces van de fotokatalysator beïnvloedt. Het is dus erg interessant om een betrouwbare theoretische basis te onderzoeken en te bieden voor de toepassing van fotokatalysatoren bij de efficiënte en snelle behandeling van kleurstofafvalwater.
In deze studie werd een nieuwe en efficiënte fotokatalysator van ZnO/Fe3 O4 /g-C3 N4 nanocomposieten werd met succes voorbereid. De kristalstructuur, chemische toestanden en optische eigenschappen van de fotokatalysator werden gekarakteriseerd met behulp van röntgendiffractie (XRD), transmissie-elektronenmicroscopie (TEM), energiedispersieve spectroscopie (EDS), röntgenfoto-elektronspectroscopie (XPS), fotoluminescentie (PL ), vibrerende monstermagnetometrie (VSM) en UV-vis diffuse reflectiespectroscopie (DRS). De fotokatalytische prestatie van de fotokatalysator werd onderzocht door de afbraak van methyloranje (MO) onder bestraling met zichtbaar licht. De afbraak van verschillende monoazokleurstoffen (MO, alizarine geel R (AYR) en oranje G (OG)) over ZnO/Fe3 O4 /g-C3 N4 werd ook onderzocht. Om het mogelijke mechanisme van de fotokatalytische afbraak van azokleurstoffen verder te evalueren, werden bovendien een experiment voor het vangen van vrije radicalen en een PL-techniek gebruikt.
Materialen en methoden
Materialen
Zinkacetaat werd geleverd door Tianjin Fuchen Chemical Reagent Co., Ltd. (Tianjin, China); ethanol (EtOH) (watervrije alcohol) werd gekocht bij Tianjin Fuyu Fine Chemical Co., Ltd. (Tianjin, China); ureum en oxaalzuur werden verkregen van de Tianjin Shengao Chemical Industry Co., Ltd. (Tianjin, China); en MO, AYR en OG werden geleverd door Tianjin Yongsheng Fine Chemical Co., Ltd. (Tianjin, China). De geselecteerde eigenschappen van MO, AYR en OG worden weergegeven in Tabel 1.
Voorbereiding van Fe3 O4
Voor de reparatie van Fe3 O4 , 0,540 g FeCl3 ∙6H2 O en 0,278 g FeSO4 ∙7H2 O (molverhouding 2:1) werden opgelost in 40 mL water. Na 30 min ultrasoonapparaat werd een bruingele oplossing verkregen en overgebracht naar een kolf van 100 ml. Daarna werd de oplossing 60 min bij 70°C in een stikstofatmosfeer geroerd, waarna onder roeren 5 mL waterige ammonia (25%) aan de oplossing werd toegevoegd. De verkregen donkerbruine suspensie werd nog eens 60 min geroerd en tweemaal gewassen met achtereenvolgens water en ethanol. De vaste stof werd vervolgens met een magnetisch veld gescheiden van de vloeibare fase. Het bereide donkerbruine monster werd 12 uur in een vacuümoven bij 40°C gedroogd.
Bereiding van ZnO/Fe3 O4
De fotokatalysator werd bereid op basis van eerdere studies [17]. In een representatieve synthese werd oplossing A bereid met behulp van de methode waarbij zinkacetaat (2,196 g) in ETOH (60 mL) wordt opgelost en 30 min bij 60 °C in een waterbad wordt geroerd. Bovendien werd oplossing B verkregen door 5,040 g oxaalzuuroplossing toe te voegen aan 80 mL ETOH onder roeren bij 50°C gedurende 30 min. Oplossing B werd vervolgens druppelsgewijs toegevoegd aan de warme oplossing A en gedurende 1 uur continu bij kamertemperatuur geroerd om de sol te verkrijgen. Daarna werd de sol, om een homogene gel te verkrijgen, gedurende een tijdsperiode verouderd in een afgesloten omgeving. Het product werd 24 uur gedroogd in een vacuümoven bij 80°C. Ten slotte werd ZnO verkregen door thermische behandeling gedurende 2 uur bij 400 ° C. Bereiden van ZnO/Fe3 O4 , 0,12 g Fe3 O4 werd gedispergeerd in oplossing A.
Bereiding van ZnO/Fe3 O4 /g-C3 N4
Voor de bereiding van ZnO/Fe3 O4 /g-C3 N4 , werd een homogeen mengsel verkregen door 1 g ZnO/Fe3 krachtig te malen O4 en melamine met een massaverhouding van 1:1 en vervolgens het mengsel dispergeren in 20 ml gedeïoniseerd water. De suspensie werd gedurende 1 uur ultrasoon behandeld. Daarna werden de voorlopers een nacht bij 70°C gedroogd om het oplosmiddel te verwijderen, en vervolgens werd de verkregen vaste stof gedurende 2 uur in lucht bij 550°C gegloeid. De magnetische ZnO/Fe3 O4 /g-C3 N4 -50% composiet werd vervolgens met succes verkregen. De hoeveelheid g-C3 N4 werd aangepast door de hoeveelheid melamine (0,25 g, 1 g en 2,3 g) te regelen tijdens de bereiding van de ZnO/Fe3 O4 /g-C3 N4 nanocomposieten, en de relevante producten werden aangeduid als ZnO/Fe3 O4 /g-C3 N4 -20%, ZnO/Fe3 O4 /g-C3 N4 -50% en ZnO/Fe3 O4 /g-C3 N4 -70%, respectievelijk.
Karakterisatiemethoden
De XRD-spectra van de monsters werden geanalyseerd met behulp van een Rigaku Giegerflex D/Max B-diffractometer met Cu-Ka-straling. De TEM werd samen uitgevoerd met behulp van een Tecnai G2F20 (VS) microscoop. EDS-spectra werden uitgevoerd met behulp van een energie-dispersieve röntgenspectrometer (EDS) die aan het TEM-instrument was bevestigd. Een oppervlakte-analysator (Micromeritics, ASAP-2020, VS) werd gebruikt om het porievolume, de poriegrootteverdeling en het specifieke oppervlak van de monsters onder N2 te karakteriseren adsorptie bij 77 K. Om de optische bandafstand van de fotokatalysatoren te bepalen, werd het UV-zichtbare absorptiespectrum verkregen met behulp van een UV-zichtbare spectrofotometer met een reflectiestandaard van BaSO4 (Hitachi UV-4100, Japan). De oppervlaktesamenstelling en chemische toestand van de monsters werden onderzocht met XPS (250XI ESCA) uitgerust met een Mg Kα-röntgenbron (1253,6 eV). De PL-spectra van de monsters werden bepaald met behulp van een fluorescentiespectrofotometer (FLsp920, Engeland) bij kamertemperatuur, met een Xe-lamp als excitatielichtbron. Foto-elektrochemische metingen werden uitgevoerd in kwartscellen met drie elektroden met een 0,1-M Na2 SO4 elektrolyt oplossing. Platinadraad werd gebruikt als de tegenelektrode en Ag/AgCl werden respectievelijk als referentie-elektroden gebruikt. De werkelektrode werd als volgt geprepareerd:10 mg van de voorbereide fotokatalysator werd gesuspendeerd in 1 mL gedeïoniseerd water, dat vervolgens werd gedompeld op een indium-tinoxide (ITO) glaselektrode met afmetingen van 10 mm × 20 mm en vervolgens gedroogd onder een infraroodlamp.
Fotokatalytische activiteit voor azokleurstof
Fotokatalytische experimenten werden uitgevoerd met een 500-W Xe-lamp met een 420-nm afsnijfilter bij 25°C, om de afbraak door zichtbaar licht van de MO-, AYR- en OG-oplossingen te bestuderen. In een traditionele test werd 10 mg katalysator toegevoegd aan 50 mL azokleurstofoplossing (30 mg/L). Het mengsel werd 30 min in het donker gehouden om de adsorptie van azokleurstof op het oppervlak van de fotokatalysator te bevorderen. Het mengsel werd vervolgens bestraald onder een Xe-lamp om de azokleurstof af te breken. Na het degradatie-experiment werd elk monster gefilterd met een 0,45 -μm filtermembraan om de fotokatalysatordeeltjes te verwijderen voor analyse, en de concentraties van MO, AYR en OG in de bovenstaande vloeistof werden gemeten met behulp van een UV-5100 N spectrofotometer bij λ max =respectievelijk 466 nm, 373 nm en 475 nm. De degradatie-efficiëntie (η ) van de azokleurstof werd als volgt berekend:
$$ \eta =\frac{C_0-{C}_{\mathrm{t}}}{C_0}\times 100\% $$waar C0 en Ct zijn de concentraties van de azokleurstof bij respectievelijk de initiële en gespecificeerde bestralingstijden.
Resultaten en discussie
XRD
Röntgendiffractie (XRD) analyse werd gebruikt om de fasestructuren van de ZnO, g-C3 N4 , en ZnO/Fe3 O4 /g-C3 N4 composieten met verschillende g-C3 N4 ladingen. De resultaten zijn weergegeven in Fig. 1. De pieken van de ZnO-monsters op 2θ =31,81°, 34,44°, 36,21°, 47,60°, 56,62°, 63,01° en 67,97° komen overeen met de (100), (002), (101), (102), (110), (103) en (112) kristalvlakken van de hexagonale wurtzietstructuur van ZnO. Alle relevante diffractiegegevens voor de ZnO kwamen goed overeen met de JCPDS 36-145 [17]. De sterkste piek van de g-C3 N4 monster komt overeen met het (002) vlak van zijn laagstructuur bij 2θ =27,3°. Zoals gemeld, de g-C3 N4 structuur heeft een zwakke diffractiepiek bij 2θ =13,2°, wat wordt toegeschreven aan het (100) kristalvlak van g-C3 N4 . De breedte van de diffractiepiek nam af, wat wijst op de invloed van geometrische beperkingen op de nanoporiënwand [7]. De XRD-patronen van de ZnO/Fe3 O4 /g-C3 N4 -x monsters bevatten alle typische pieken van g-C3 N4 , ZnO en Fe3 O4 . De diffractiepieken op 30,4°, 35,7° en 43,4° komen overeen met de (220), (311) en (400) vlakken van Fe3 O4 [18, 19]. Bovendien is de piekintensiteit van de karakteristieke piek van g-C3 N4 werd geleidelijk versterkt met een verhoging van de hoeveelheid g-C3 N4 , terwijl de piekintensiteit van ZnO en Fe3 O4 geleidelijk afgenomen. Geen g-C3 N4 karakteristieke piek werd waargenomen in de ZnO/Fe3 O4 /g-C3 N4 -20% monsters, wat kan worden toegeschreven aan het lage gehalte aan g-C3 N4 in de composiet. Uit de XRD-analyseresultaten werden geen andere pieken waargenomen in alle monsters, wat de hoge zuiverheid van de monsters bevestigt.
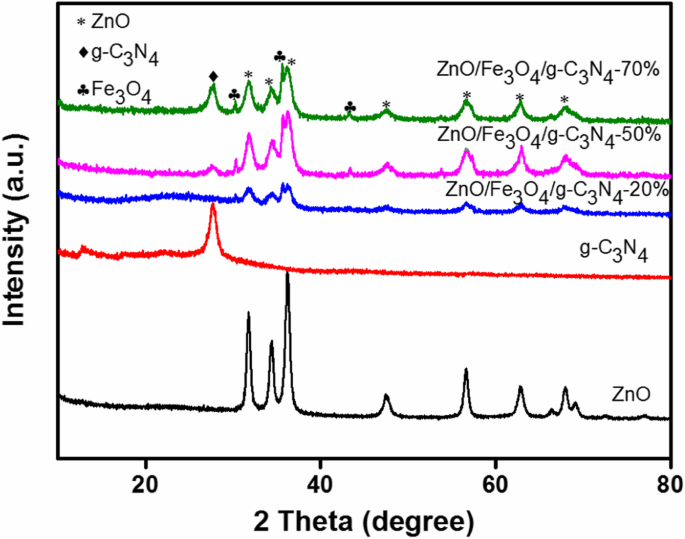
XRD-patronen van ZnO, g-C3 N4 , ZnO/Fe3 O4 /g-C3 N4 -20%, ZnO/Fe3 O4 /g-C3 N4 -50% en ZnO/Fe3 O4 /g-C3 N4 -70%
TEM en EDS
De structuur van het monster werd geëvalueerd met behulp van TEM, zoals weergegeven in Fig. 2. Het TEM-beeld van puur ZnO geeft de typische hexagonale wurtzietstructuur weer (Fig. 2a), wat consistent is met de XRD-resultaten. De TEM-afbeelding van g-C3 N4 (Fig. 2b) toont de gelaagde bloedplaatjesachtige morfologiestructuur en gladde, dunnere vellen met papiervouw, die vergelijkbaar is met de morfologie van grafeen-nanovellen. Zoals te zien is op de TEM-afbeelding van ZnO/Fe3 O4 /g-C3 N4 -50% (Fig. 2c), een grote hoeveelheid fotokatalysatoren geaccumuleerd op de gelaagde structuur van g-C3 N4 . De EDS-resultaten voor ZnO/Fe3 O4 /g-C3 N4 -50% wordt weergegeven in Fig. 3. Het is te zien dat het monster pieken van Zn-, C-, N-, Fe- en O-elementen bevatte, wat ook bewees dat de ZnO/Fe3 O4 /g-C3 N4 composiet werd met succes voorbereid. De piekwaarde van Fe is echter relatief laag, wat suggereert dat het gehalte aan Fe3 O4 is laag in ZnO/Fe3 O4 /g-C3 N4 composieten. Aangezien Cu als drager werd gebruikt in de TEM-analyse, werden karakteristieke pieken van Cu gedetecteerd in de EDS-analyse [20].
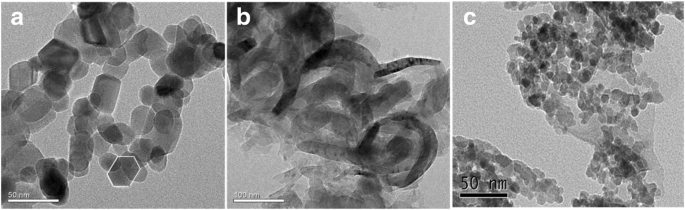
TEM-afbeeldingen van a ZnO, b g-C3 N4 , en c ZnO/Fe3 O4 /g-C3 N4 -50%
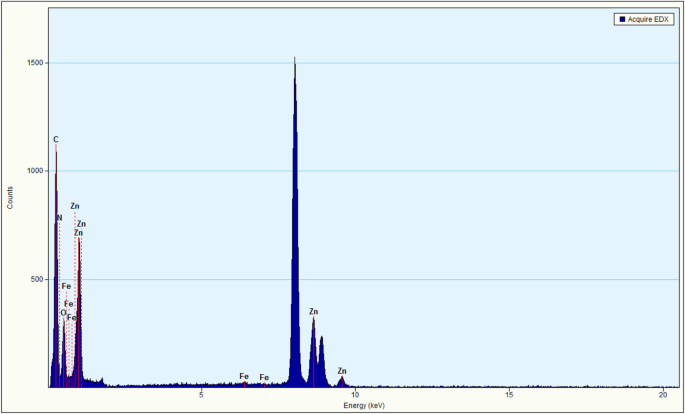
EDX van ZnO/Fe3 O4 /g-C3 N4 -50%
XPS
Om de oppervlaktesamenstelling en chemische toestanden van de bereide composietkatalysatoren te onderzoeken, werd XPS uitgevoerd op ZnO/Fe3 O4 /g-C3 N4 -50%. De spectrumscan van het onderzoek onthult de aanwezigheid van C, N, O, Zn en Fe (figuur 4a). Figuur 4b laat zien dat de C 1s drie karakteristieke pieken heeft. De piek bij 284,6 eV wordt toegeschreven aan de koolwaterstoffen in het XPS-instrument en de sp2-gehybridiseerde koolstofatomen in de aromatische ring, die waren gebonden aan N (N–C=N). De andere piek wordt toegeschreven aan de sp3-hybride koolstofbron (C–(N)3 ) met een bindingsenergie van 286.5 eV. De piek bij de bindingsenergie van 287,8 eV wordt toegeschreven aan de C–N–C in de grafietfase [21]. Het N 1s XPS-spectrum wordt weergegeven in figuur 4c. Een belangrijke piek was bij 397,9 eV, wat overeenkomt met de aromatische tussen N- en twee C-atomen (C =N-C). Een zwakkere karakteristieke piek bevindt zich bij 399,2 eV, wat voornamelijk wordt toegeschreven aan de tristikstof (N–(C)3 ) die de basisstructuur verbindt (C6 N7 ), of de aminogroepen die verband houden met de structurele defecten en onvolledige condensatie ( (C)2 –N–H) [22]. Het XPS-spectrum van O 1s wordt weergegeven in Fig. 4d, en de piek bij 530,1 eV komt overeen met de O2 − ion in de Zn-O binding van de ZnO hexagonale wurtzietstructuur [23]. De piek bij 531,8 eV komt overeen met het zuurstoftekort in ZnO. In het Zn 2p XPS-spectrum (Fig. 4e) zijn er twee karakteristieke pieken bij de bindingsenergieën van 1021,4 ev en 1044,3 eV, en de afstand tussen de twee pieken is 22,9 eV, wat is opgenomen in de standaardreferentiewaarde van zinkoxide . Het bindingsenergieverschil geeft aan dat het zinkion in de composiet zich in +2 toestanden bevond [23]. In het XPS-spectrum van de Fe 2p (Fig. 4f) bevinden de twee pieken zich op 710,6 ev en 724,4 eV, wat overeenkomt met respectievelijk de 2p1/2- en 2p3/2-orbitalen [24]. Deze resultaten laten zien dat g-C3 N4 zijn samengesteld op het ZnO, wat de absorptie van zichtbaar licht kan bevorderen en de overdracht en scheiding van ladingsdragers kan verbeteren; dus, het verbeteren van de fotokatalytische activiteit [25].
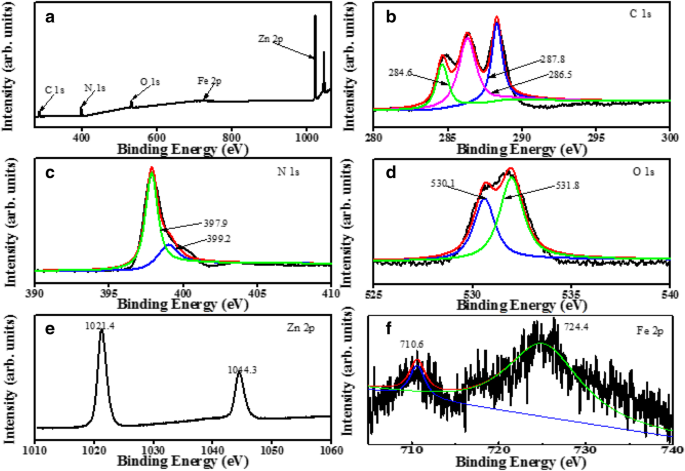
XPS-spectra van het gesynthetiseerde ZnO/Fe3 O4/ g-C3 N4 -50%:een onderzoek van de steekproef, b C 1s, c N 1s, d O1s, e Zn 2p en f Fe 2p
UV-vis DRS
Diffuse reflectiespectroscopie werd gebruikt om het lichtabsorptiegedrag van de fotokatalysatoren te onderzoeken. De resultaten zijn weergegeven in Fig. 5. De absorptie van licht met een significante roodverschuiving kan de fotokatalytische prestatie in het zichtbare gebied verbeteren. In het ultraviolette gebied vertoonde het zuivere ZnO een sterke absorptie bij de golflengte van 388 nm, wat overeenkomt met een bandafstand van 3,20 eV. Anders dan het ZnO-absorptiegedrag, g-C3 N4 levert een absorptieverschuiving op bij 460 nm, en de overeenkomstige bandgap-energie was 2,70 eV, wat wijst op een hogere respons voor fotokatalytische activiteit onder zichtbaar licht [26]. Vergeleken met puur ZnO of g-C3 N4 , de absorptierand van de ZnO/Fe3 O4 /g-C3 N4 composietmateriaal verschoof significant naar een langer golflengtegebied, wat suggereert dat de absorptierand van het composietmateriaal verschoof naar het lagere energiegebied. Deze resultaten kunnen te wijten zijn aan de synergetische relatie tussen g-C3 N4 en ZnO in de samengestelde monsters, wat consistent is met het rapport van Le et al. [7]. De roodverschuiving van de absorptierand van ZnO/Fe3 O4 /g-C3 N4 verhoogd met een toename van de g-C3 N4 laden tot 50%. De absorptierand nam echter af toen de g-C3 N4 belading was 70%. De afname van ZnO/Fe3 O4 /g-C3 N4 -70% kan zijn omdat g-C3 N4 belasting boven het optimale niveau kan de absorptie van de lichtintensiteit door ZnO afschermen. Daarom is van alle voorbereide monsters de ZnO/Fe3 O4 /g-C3 N4 -50% composiet vertoonde de meest uitgebreide en sterkste absorptie van zichtbaar licht. Dit is vergelijkbaar met de resultaten verkregen door Jo et al., die rapporteerden dat ZnO-50%/g-C3 N4 vertoonden de sterkste absorptie van zichtbaar licht [1]. Het composietmateriaal vertoonde de sterkste lichtabsorptie voor zichtbaar licht, wat de vorming van elektron-gatparen onder bestraling met zichtbaar licht verhoogde, wat resulteerde in een hogere fotokatalytische activiteit.
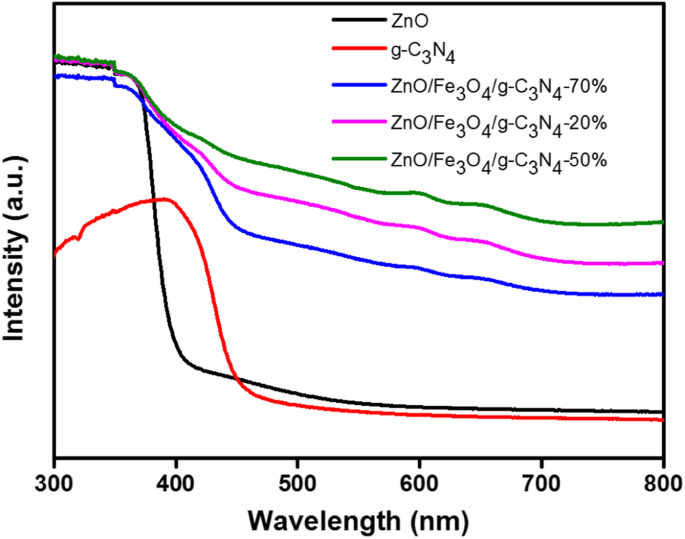
UV-vis diffuse reflectiespectra van ZnO, g-C3 N4 , ZnO/Fe3 O4 /g-C3 N4 -20%, ZnO/Fe3 O4 /g-C3 N4 -50% en ZnO/Fe3 O4 /g-C3 N4 -70%
PL
Het effect van de synergetische relatie tussen ZnO en g-C3 N4 op de fotokatalyse werd verder geëvalueerd met behulp van PL. De PL-spectra van ZnO, g-C3 N4, en ZnO/Fe3 O4 /g-C3 N4 -50% wordt weergegeven in Fig. 6. De excitatiegolflengte was 300 nm en de PL van de monsters werd getest bij kamertemperatuur. De emissiespectra in het bereik van 300-800 nm werden geregistreerd. Het is algemeen bekend dat bij de recombinatie van elektron-gatparen in halfgeleiders energie vrijkomt in de vorm van PL. In het algemeen duidt een lagere PL-intensiteit op een lagere recombinatiesnelheid van dragers, wat leidt tot efficiënte fotokatalytische activiteit. In het PL-spectrum, g-C3 N4 vertoonde een sterke emissiepiek bij ongeveer 460 nm, wat in overeenstemming is met de UV-vis-resultaten (Fig. 5) en literatuur [7]. De emissiepiek van zuiver ZnO was lager dan die van g-C3 N4 , bij ongeveer 410 nm [21]. Vergeleken met de PL-piek van puur ZnO, is de emissiepiek van de ZnO/Fe3 O4 /g-C3 N4 -50% samengestelde fotokatalysator was roodverschoven en de piekintensiteit was aanzienlijk verminderd. Bovendien, PL piekintensiteit van de ZnO/Fe3 O4 /g-C3 N4 -50% samengestelde fotokatalysator was het laagst. Op basis van deze resultaten werd geconcludeerd dat de elektron-gat-paren die door de ZnO/Fe3 O4 /g-C3 N4 -50% nanocomposieten onder bestraling met zichtbaar licht kunnen effectief worden overgedragen op het grensvlak van de heterostructuur. Zo nam de elektron-gat-recombinatiesnelheid af, wat resulteerde in de hoogste fotokatalytische activiteit onder bestraling met zichtbaar licht.
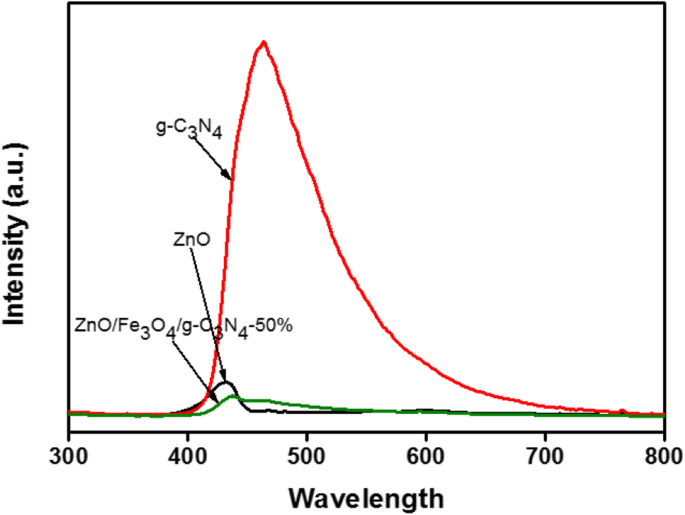
PL-spectra van ZnO, g-C3 N4 , en ZnO/Fe3 O4 /g-C3 N4 -50%
Elektrochemische analyse
De fotokatalytische redoxreacties tussen de scheiding, migratie en vangst van fotogegenereerde elektronen door halfgeleiderfotokatalysatoren zijn nauw verwant. Om de foto-geïnduceerde ladingsscheidingsefficiëntie tijdens de fotokatalytische reactie kwalitatief te evalueren, zijn de fotostroomreacties van de ZnO, g-C3 N4, en ZnO/Fe3 O4 /g-C3 N4 -50% nanocomposieten werden onderzocht onder bestraling met zichtbaar licht. Figuur 7a presenteert de fotostroom-tijd (I-t) curven van drie monsters onder intermitterende verlichting. Uit de figuur is te zien dat zodra de bestraling van licht was uitgeschakeld, de fotostroomwaarde abrupt afnam en de fotostroom een constante waarde behield toen het licht weer werd ingeschakeld. Bovendien is dit fenomeen reproduceerbaar, wat aangeeft dat de meeste door foto gegenereerde elektronen naar het oppervlak van het monster werden overgebracht en dat er een fotostroom werd gegenereerd onder bestraling met zichtbaar licht. Zuiver ZnO vertoont de zwakste fotostroomrespons onder bestraling met zichtbaar licht, vanwege de brede bandafstand. Bovendien is de ZnO/Fe3 O4 /g-C3 N4 -50% composietmonsters vertoonden de hoogste fotostroomintensiteiten. De resultaten suggereren dat de relatie tussen ZnO en g-C3 N4 is gunstig voor de verbetering van de scheidingsefficiëntie en overdracht van door foto gegenereerde elektronen en gaten [27]. Dit fenomeen komt overeen met de PL-resultaten.
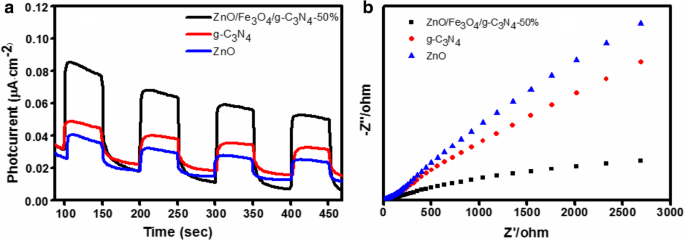
Tijdelijke fotostroomreactie (a ) en EIS-plots (b ) ZnO, g-C3 N4, en ZnO/Fe3 O4 /g-C3 N4 -50% bij bestraling met zichtbaar licht
De resultaten van de elektrochemische impedantiespectroscopie (EIS) van het monster worden weergegeven in Fig. 7b. De bogen op het EIS elektrochemische impedantiespectrogram weerspiegelen de weerstand van de ladingsoverdrachtslaag op de elektrode/elektrolyt-interface. Een kleinere boog vertegenwoordigt een lagere weerstand, wat wijst op een hogere efficiëntie van ladingsoverdracht [27]. De boogstraal van de ZnO/Fe3 O4 /g-C3 N4 -50% samengestelde fotokatalysator is kleiner dan die van ZnO en g-C3 N4 , wat aangeeft dat de weerstand van de ladingsoverdrachtslaag van de ZnO/Fe3 O4 /g-C3 N4 -50% interface was de kleinste. De foto-geïnduceerde elektron-gat-paren vertoonden dus de hoogste scheidings- en overdrachtsefficiëntie, wat de fotokatalytische activiteit verbeterde. Deze resultaten komen overeen met de resultaten van de fotostroom.
Magnetische eigenschappen
De hysteresislussen van ZnO, Fe3 O4 , en ZnO/Fe3 O4 /g-C3 N4 -50% wordt weergegeven in Fig. 8. De resultaten laten zien dat zuiver ZnO niet-magnetisch is, zuiver Fe3 O4 vertoonde de sterkste verzadigingsmagnetisatie en de verzadigingsmagnetisatie van ZnO/Fe3 O4 /g-C3 N4 -50% was lager dan die van het zuivere Fe3 O4 , die wordt toegeschreven aan de aanwezigheid van niet-magnetische stoffen, d.w.z. ZnO en g-C3 N4 . Er werden geen hysterese, remanentie en coërciviteit waargenomen in de hystereselus van ZnO/Fe3 O4 /g-C3 N4 -50%. Daarom was het monster superparamagnetisch. Bovendien was de verzadigingsmagnetisatie van de samengestelde fotokatalysator voldoende om van de oplossing te scheiden met behulp van een extern magnetisch veld, zoals weergegeven in Fig. 8 (inzet), wat het herstel van de fotokatalysator bevorderde en de recycleerbaarheid ervan verhoogde.
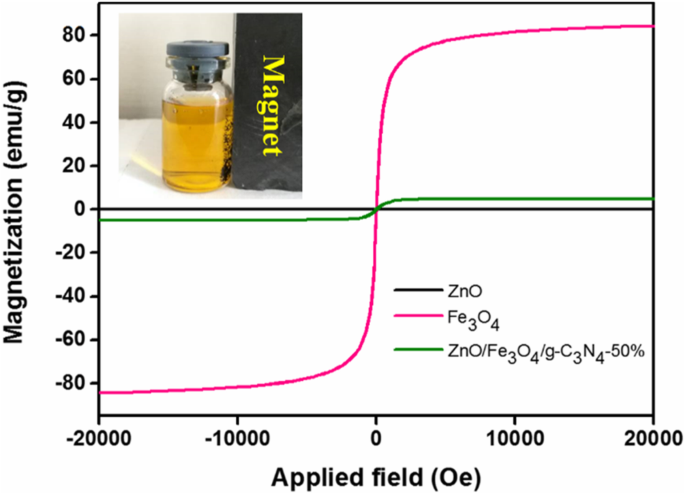
Magnetische hysteresiscurves van ZnO en ZnO/Fe3 O4 /g-C3 N4 -50% spectra bij kamertemperatuur
Fotokatalytische eigenschappen
De afbraak van MO over verschillende fotokatalysatoren wordt weergegeven in Fig. 9a. Het zuivere ZnO deed de methyloranje enigszins af onder bestraling met zichtbaar licht, aangezien de brede bandafstand van ZnO het mogelijk maakt om alleen op ultraviolet licht te reageren. De degradatie-efficiëntie van pure g-C3 N4 voor methyloranje was niet erg hoog, vanwege de hoge recombinatiesnelheid van het foto-elektron-gatpaar, ondanks de reactie op zichtbaar licht, wat resulteerde in de lage fotokatalytische activiteit van g-C3 N4 . De fotodegradatie-efficiëntie van MO op de ZnO/Fe3 O4 /g-C3 N4 -50% samengestelde fotokatalysator was hoger dan die van de andere katalysatoren, om de volgende drie redenen:Ten eerste gaven de UV-Vis-spectra aan dat de ZnO/Fe3 O4 /g-C3 N4 -50% composiet fotokatalysator vertoonde de sterkste respons-intensiteit van zichtbaar licht en een groot absorptiebereik voor zichtbaar licht. Ten tweede onthulden de PL- en elektrochemische resultaten dat de recombinatiesnelheid van het elektron-gatpaar van ZnO/Fe3 O4 /g-C3 N4 -50% was het laagst. Ten derde gaven de elektrochemische resultaten aan dat de foto-elektronenoverdrachtssnelheid van de ZnO/Fe3 O4 /g-C3 N4 -50% fotokatalysator was de snelste vergeleken met enkele fotokatalysator.
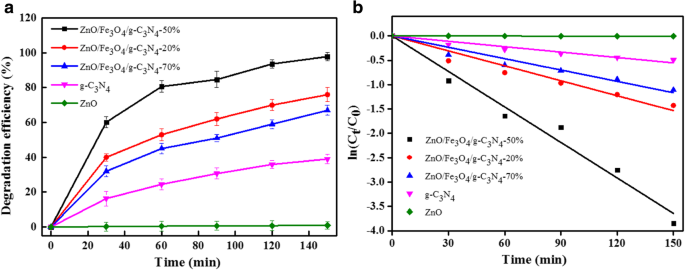
Fotokatalytische degradatie-efficiëntie (a ) en kinetische krommen (b ) van MO over verschillende fotokatalysatoren onder bestraling met zichtbaar licht (de relatieve fout van de gegevens was minder dan 5%)
Bovendien werd ook de kinetiek van de afbraak van MO op de fotokatalysatoren geëvalueerd (figuur 9b). De resultaten lieten zien dat de afbraakkinetiek van MO op verschillende fotokatalysatoren het eerste-orde kinetische model volgde, en alle afbraaksnelheidsconstanten zijn weergegeven in Tabel 2. De schijnbare snelheidsconstante van ZnO/Fe3 O4 /g-C3 N4 -50% was het hoogst (0,02430 min −1 ), en die hoger was dan de afbraaksnelheid van g-C3 N4 /Fe3 O4 /TiO2 en TiO2 /biochar composietkatalysatoren [28, 29]. Bovendien is de ZnO/Fe3 O4 /g-C3 N4 -50% vertoonde een hogere fotokatalytische snelheid ten opzichte van g-C3 N4 /Fe3 O4 /AgI over de afbraak van MO (0. 0016 min −1 ) [10].
Stability of ZnO/Fe3 O4 /g-C3 N4 -50% Composite Photocatalyst
In addition, the stability of photocatalysts is a critical factor in relation to large-scale technology application. To evaluate the stability of the ZnO/Fe3 O4 /g-C3 N4 -50% composite photocatalyst, recycling experiments were conducted on the photocatalyst for the degradation of MO under visible light irradiation. The photocatalyst was collected by magnetic decantation and then washed using distilled water and ethanol. Thereafter, it was dried in an oven at 80 °C. The sample was reused for subsequent degradation, and the results are presented in Fig. 10a. The composite photocatalyst maintained a very high photocatalytic activity, and the removal rate of MO on the ZnO/Fe3 O4 /g-C3 N4 -50% composite photocatalyst was 95.3% after 5 cycles. In addition, there was a slight decrease in the amount of photocatalysts during the cycle processes. Therefore, the ZnO/Fe3 O4 /g-C3 N4 -50% composite photocatalyst exhibited high stability under visible light irradiation. To further evaluate the stability of the ZnO/Fe3 O4 /g-C3 N4 -50%, samples were collected after 5 cycles for XRD testing and compared with the XRD pattern of the sample before cycling. The results are presented in Fig. 10b. No significant changes were observed in the structure of the photocatalyst before and after use, which indicates that the ZnO/Fe3 O4 /g-C3 N4 -50% photocatalyst was highly stable.
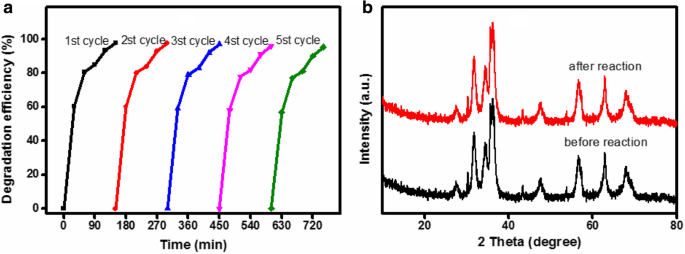
The recycling degradation efficiency (a ) and XRD patterns of before and after degradation (b ) of ZnO/Fe3 O4 /g-C3 N4 -50% for MO under visible light irradiation
Degradation of Monoazo Dyes on ZnO/Fe3 O4 /g-C3 N4 -50%
For the evaluation of the photocatalytic degradation behavior of different monoazo dyes, the degradation of MO, AYR, and OG over ZnO/Fe3 O4 /g-C3 N4 is presented in Fig. 11. The plots of the absorbance with respect to the wavelength for the MO, AYR, and OG degradations over ZnO/Fe3 O4 /g-C3 N4 -50% at various irradiation times are presented in Figs. 11a–c. The maximum absorption wavelength of MO, AYR, and OG before and after degradation were 466 nm, 372 nm, and 475 nm, respectively. With the gradual extension of the illumination time to 150 min, the intensity of the absorption peak gradually decreased, implying the gradual mineralization of MO, AYR, and OG. Furthermore, under visible-light irradiation for 150 min, the degradation efficiencies of MO, AYR, and OG were 97.87%, 98.05%, and 83.35%, respectively (Fig. 11d). There are two possible reasons for this phenomenon. First, as can be seen in Fig. 11d, the adsorption efficiency of OG on the photocatalyst was the lowest. The lower adsorption efficiency of OG can be explained by the steric limit of a large aromatic molecule, which reduced the number of OG molecules adsorbed on the photocatalyst. The lower adsorption efficiency of the azo dye therefore resulted in a small amount of molecules concentrated on the active site of the photocatalyst, which decreased the degradation efficiency of the azo dye [30]. Second, AYR has a high degradation efficiency, which is related to the presence of a carboxyl group that can react with H
+
in a light Kolbe reaction. However, the lower degradation efficiency of OG and MO could be due to the presence of a withdrawing SO3
−
group, and the increasing number of sulfonic acid groups could inhibit degradation of the dye [31]. The properties of the three dyes are listed in Table 1. The molecular weight and number of sulfonic acid was in the following order:AYR
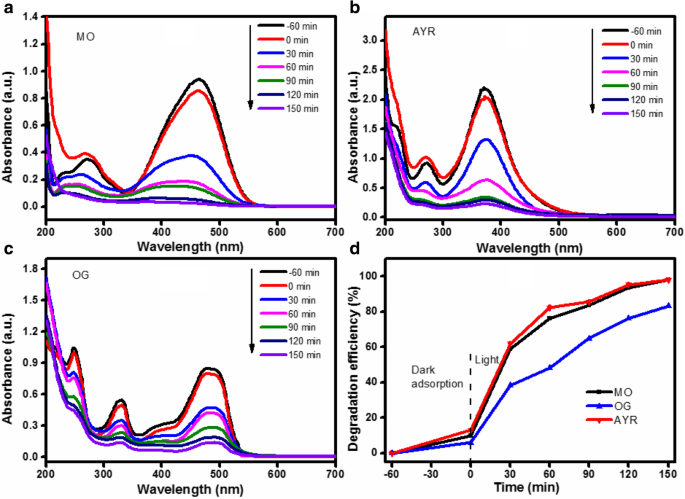
UV-vis spectra of a MO, b AYR, and c OG at different irradiation times, and d degradation efficiency curves of different dyes in the presence of ZnO/Fe3 O4 /g-C3 N4 -50%
It is necessary to investigate the relationship between the molecular weight of the azo dye and its degradation efficiency. Figure 12 reveals that the molecular weight of azo dye had a good negative correlation with the degradation efficiency (R 2 =0.9776). Moreover, a molecular weight of the azo dye would result in a low degradation efficiency. The results are consistent with those presented above.
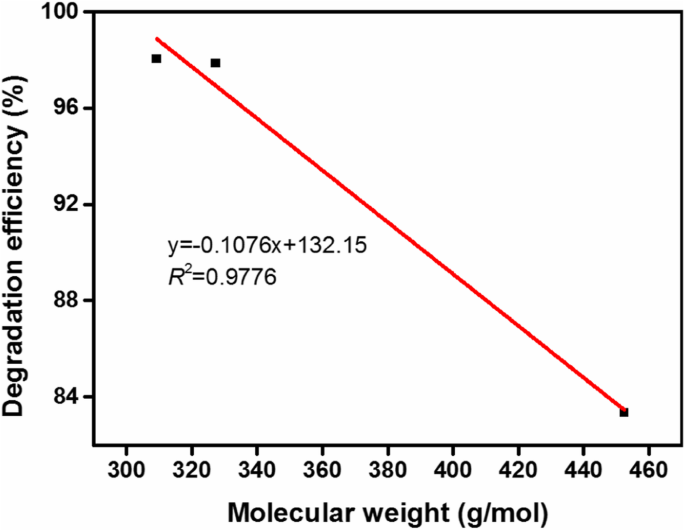
Correlation between molecular weight of azo dye and degradation efficiency
Mechanism for Photocatalytic Degradation
To further investigate the mechanism of the photocatalyst for the degradation of MO under visible light irradiation, radical, electron, and hole scavenging experiments were conducted to detect the main active species in the photocatalytic process. Moreover, ·OH, ·O2 − , h + , and e − were eliminated using tert-butanol (t -BuOH), p-benzoquinone (p -BQ), ammonium oxalate (AO), and K2 S2 O8 , respectievelijk. The degradation efficiencies of MO on the photocatalyst in the presence the scavengers are presented in Fig. 13. The removal rate of MO was significantly reduced after the addition of t -BuOH and p -BQ. Conversely, the removal efficiency of MO was not significantly reduced in the presence of AO and K2 S2 O8 . Therefore, the active species that play a critical roles during the photocatalytic degradation of MO over the ZnO/Fe3 O4 /g-C3 N4 -50% photocatalyst are ·OH and ·O2 −
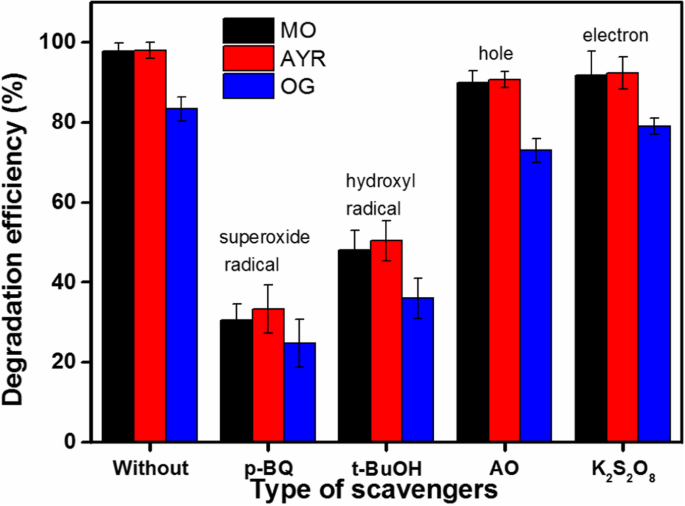
The degradation efficiencies of monazo dyes over ZnO/Fe3 O4 /g-C3 N4 -50% in the presence of various scavengers
Based on the relevant literature and experimental results (including the physicochemical properties, photocatalytic performance, and detected active components), a possible photocatalytic mechanism of the ZnO/Fe3 O4 /g-C3 N4 -50% nanocomposites prepared under visible light irradiation is proposed. It is common knowledge that ZnO and g-C3 N4 are typical n-type semiconductors. Therefore, an n–n heterojunction is formed at the interface between the g-C3 N4 and ZnO nanoparticles. The ZnO/Fe3 O4 /g-C3 N4 -50% can be excited to generate electrons and holes under visible light irradiation. The excited electrons are then transferred from the CB of the g-C3 N4 to the CB of the ZnO. The improvement of the photocatalytic performance of the composite photocatalyst is mainly due to the effective separation of photogenerated electrons and holes at the heterojunction interface [32]. Given that the CB edge potential of g-C3 N4 is more negative than that of ZnO, the excited electrons in g-C3 N4 are transferred to the CB of ZnO, and the holes are retained in the valence band (VB) of g-C3 N4 [33, 34]. In contrast, ZnO holes are injected into the holes of g-C3 N4 . Therefore, an internal electrostatic potential is formed in the space charge region, which promotes the separation of the photogenerated carriers. The charge transfer to the surface of the compound semiconductor reacts with water and dissolved oxygen to produce ·OH and ·O2 − , or it reacts directly with MO. From Fig. 13, it can be seen that ·OH and ·O2 − play a vital role in the degradation of MO on composite photocatalysts. Therefore, possible photocatalytic mechanisms are presented below:
$$ {\displaystyle \begin{array}{l}\mathrm{ZnO}/{\mathrm{Fe}}_3{\mathrm{O}}_4/\mathrm{g}\hbox{-} {\mathrm{C}}_3{\mathrm{N}}_4\hbox{-} 50\%+ h\nu \to {\mathrm{e}}_{\mathrm{C}\mathrm{B}}^{-}\left(\mathrm{ZnO}\right)+{\mathrm{h}}_{\mathrm{VB}}^{+}\left(\mathrm{g}\hbox{-} {\mathrm{C}}_3{\mathrm{N}}_4\right)\\ {}{\mathrm{e}}_{\mathrm{C}\mathrm{B}}^{-}+{\mathrm{O}}_2\to \cdot {\mathrm{O}}_2^{-}\\ {}{\mathrm{h}}_{\mathrm{VB}}^{+}+{\mathrm{H}}_2\mathrm{O}\to \cdot \mathrm{OH}+{\mathrm{H}}^{+}\\ {}\cdot \mathrm{OH}+\mathrm{MO}\to {\mathrm{H}}_2\mathrm{O}+{\mathrm{C}\mathrm{O}}_2\\ {}\cdot {\mathrm{O}}_2^{-}+\mathrm{MO}\to {\mathrm{H}}_2\mathrm{O}+{\mathrm{C}\mathrm{O}}_2\end{array}} $$Based on the above discussion, it was concluded that the photocatalytic activity of the ZnO/Fe3 O4 /g-C3 N4 -50% nanocomposite semiconductor was significantly improved. This was because of the following two reasons:(1) heterostructure between g-C3 N4 and ZnO improved the light absorption properties, and (2) the synergistic effect of the internal electric field and the matched band structure of g-C3 N4 and ZnO increased the separation rate of photogenerated carriers (Fig. 14).
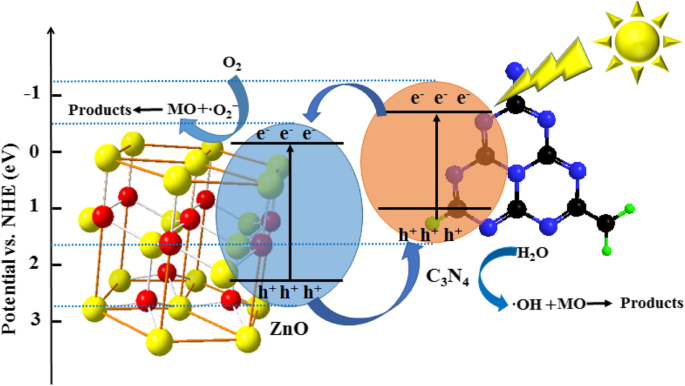
Mechanism for photocatalytic degradation of monazo dyes on the ZnO/Fe3 O4 /g-C3 N4 -50% photocatalyst
Conclusions
In this study, ternary magnetic ZnO/Fe3 O4 /g-C3 N4 nanocomposites were successfully fabricated, as novel recyclable visible-light-driven photocatalysts. Among all the prepared photocatalysts, the ZnO/Fe3 O4 /g-C3 N4 -50% composite photocatalyst exhibited the most efficient photocatalytic activity, due to the improved light absorption properties resulting from the heterojunction structure between g-C3 N4 and ZnO, in addition, to the synergistic effect of their internal electric field and matched energy band structure. Moreover, the separation rate of the photogenerated carriers was high. The degradation efficiencies of MO, AYR, and OG over ZnO/Fe3 O4 /g-C3 N4 -50% were 97.87%, 98.05%, and 83.35%. This was due to the number of dye molecule adsorbed on the photocatalyst, and the structure of the azo dye molecule had an influence on the degradation. The kinetics of the degradation of MO on the composite photocatalyst was in accordance with first-order kinetics. Furthermore, the addition of Fe3 O4 significantly improved the stability and recyclability of the photocatalyst. Superoxide ions are the main reactive species, which indicates that the azo dyes have the same degradation mechanism.
Afkortingen
- AO:
-
Ammonium oxalate
- AYR:
-
Alizarin yellow R
- CB:
-
Geleidingsband
- DRS:
-
Diffuse reflectance spectroscopy
- EDS:
-
Energy dispersive X-ray spectroscopy
- EIS:
-
Elektrochemische impedantiespectroscopie
- EtOH:
-
Ethanol
- Fe3 O4 :
-
Ferroferric oxide
- g-C3 N4 :
-
Graphite-like carbon nitride
- MO:
-
Methylsinaasappel
- OG:
-
Orange G
- p -BQ:
-
p-Benzoquinone
- PL:
-
Photoluminescence spectra
- t -BuOH:
-
Tert-butanol
- TEM:
-
Transmission electron microscopye
- UV:
-
Ultraviolet
- VB:
-
Valentieband
- VSM:
-
Vibrating sample magnetometry
- XRD:
-
Röntgendiffractie
- ZnO:
-
Zinkoxide
Nanomaterialen
- Nanodiamanten voor magnetische sensoren
- Effecten van co-adsorptie op grensvlakladingsoverdracht in een quantum dot@dye composiet
- S, N co-gedoteerde grafeen Quantum Dot/TiO2-composieten voor efficiënte fotokatalytische waterstofgeneratie
- Weinig gelaagde MoS2/acetyleenzwarte composiet als een efficiënt anodemateriaal voor lithium-ionbatterijen
- Verkenning van Zr–Metal–Organic Framework als efficiënte fotokatalysator voor waterstofproductie
- Zichtbare, door licht aangedreven fotokatalytische prestaties van N-gedoteerde ZnO/g-C3N4-nanocomposieten
- Polyaniline-gecoate actieve kool aerogel/zwavelcomposiet voor hoogwaardige lithium-zwavelbatterij
- Grote grensvlakeffecten in CoFe2O4/Fe3O4 en Fe3O4/CoFe2O4 Core/Shell Nanodeeltjes
- Vergelijking tussen foliumzuur en op gH625 peptide gebaseerde functionalisering van Fe3O4 magnetische nanodeeltjes voor verbeterde celinternalisatie
- PtNi-legering Cocatalyst-modificatie van eosine Y-gesensibiliseerde g-C3N4/GO-hybride voor efficiënte zichtbaar-licht fotokatalytische waterstofevolutie
- S-gedopeerd Sb2O3-nanokristal:een efficiënte zichtbaar-lichtkatalysator voor organische afbraak



