Zichtbare, door licht aangedreven fotokatalytische prestaties van N-gedoteerde ZnO/g-C3N4-nanocomposieten
Abstract
N-gedoteerde ZnO/g-C3 N4 composieten zijn met succes bereid via een gemakkelijke en kosteneffectieve sol-gel-methode. De nanocomposieten werden systematisch gekarakteriseerd door XRD, FE-SEM, HRTEM, FT-IR, XPS en UV-vis DRS. De resultaten gaven aan dat in vergelijking met het zuivere N-gedoteerde ZnO, de absorptierand van binair N-gedoteerd ZnO/g-C3 N4 verschoven naar een lagere energie met toenemende absorptie van zichtbaar licht en verbetering van de efficiëntie van de ladingsscheiding, wat de fotokatalytische activiteit ervan zou verbeteren. Vergeleken met de pure g-C3 N4 , ZnO, N-gedoteerde ZnO en het samengestelde ZnO/g-C3 N4 , de zoals geprepareerde N-gedoteerde ZnO/g-C3 N4 vertoont een sterk verbeterde fotokatalytische afbraak van methyleenblauw en fenol onder bestraling met zichtbaar licht. Ondertussen, N-gedoteerde ZnO/g-C3 N4 heeft een hoge stabiliteit. Ten slotte een voorgesteld mechanisme voor N-gedoteerde ZnO/g-C3 N4 wordt ook besproken. De verbeterde fotokatalyse kan worden toegeschreven aan het synergetische effect tussen N-gedoteerde ZnO en g-C3 N4 , inclusief de energiebandstructuur en verbeterde efficiëntie van de ladingsscheiding.
Achtergrond
Fotokatalytische afbraak van de organische verbindingen met behulp van zonne-energie als energiebron heeft veel belangstelling gewekt voor de bescherming van het milieu [1,2,3]. Zoals bekend is ZnO een van de belangrijkste halfgeleiderfotokatalysatoren vanwege zijn unieke voordelen, zoals de lage prijs, hoge fotokatalytische activiteit en niet-toxiciteit [4, 5]. De nadelen, zoals een lage efficiëntie van de ladingsscheiding, gevoeligheid voor fotocorrosie en een slechte absorptie van zichtbaar licht, beperkten echter de wijdverbreide commerciële toepassingen ervan [6, 7]. Doping met de metaal- en/of niet-metaalionen, koppeling met andere halfgeleiders en oppervlaktesensibilisatie met metaalcomplexen kunnen worden beschouwd als de haalbare benaderingen om het gebruik van zonne-energie en de efficiëntie van de ladingsscheiding te verbeteren [7, 8]. Er is gemeld dat de dotering van het niet-metalen element N de lichtabsorptie van ZnO in het zichtbare bereik effectief verbeterde [9]. Het stikstofatoom is qua atoomgrootte en elektronegativiteit het dichtst bij het zuurstofatoom [10], dus N-doping zou kunnen resulteren in de minimale spanning in ZnO. Helaas vertoont N-gedoteerde ZnO geen uitstekende fotokatalytische efficiëntie in tegenstelling tot N-gedoteerde TiO2 [11].
Grafitisch koolstofnitride (g-C3 N4 ) is een relatief nieuwe, veelzijdige en veelbelovende metaalvrije polymere halfgeleider fotokatalysator [12,13,14], vanwege zijn speciale halfgeleidende eigenschappen en lage kosten. Het is uitgebreid onderzocht vanwege zijn grote potentieel bij het afbreken van milieuverontreinigende stoffen [12], waardoor watersplitsing voor H2 wordt gekatalyseerd. evolutie [13], en vermindering van kooldioxide [14] onder bestraling. De gemakkelijke recombinatie van de fotogegenereerde ladingen beperkt echter de fotokatalytische prestaties en beperkt de brede praktische toepassing ervan aanzienlijk [15]. Het construeren van een geschikte heterojunctionele composiet is een van de meest algemene methoden om de fotogegenereerde ladingsscheiding te verbeteren [16,17,18]. Koppeling g-C3 N4 met ZnO zou een uitstekende heterostructuur kunnen opleveren, aangezien deze twee halfgeleiders goed op elkaar afgestemde, overlappende bandstructuren hebben [6]. Onder bestraling met zichtbaar licht kan het aanvankelijke elektron dat door de valentieband (VB) wordt geëxciteerd, overgaan naar de geleidingsband (CB) van de g-C3 N4 , dan verder overbrengen naar het CB van ZnO [6, 8, 19], wat resulteert in een verbeterde fotokatalytische activiteit van ZnO/g-C3 N4 . Onlangs hebben Shanker et al. [10] meldde dat N-gedoteerde ZnO/g-C3 N4 hybride kern-schil vertoont een sterk verbeterde fotokatalyse in zichtbaar licht voor de afbraak van rhodamine B. Voor zover ons bekend zijn er echter geen werken gerapporteerd over N-gedoteerde ZnO/g-C3 N4 voor de afbraak door zichtbaar licht van de vluchtige organische verontreinigende stoffen zoals fenol en methyleenblauw (MB) tot nu toe.
In dit werk, de N-gedoteerde ZnO/g-C3 N4 samengestelde fotokatalysatoren werden gesynthetiseerd via de sol-gel-methode. De samengestelde composiet vertoonde een significant verbeterde fotokatalytische afbraak van MB en fenol onder bestraling met zichtbaar licht. Ten slotte werd ook het mogelijke mechanisme rond de fotokatalytische afbraak van MB en fenol onderzocht.
Methoden
Voorbereiding van N-gedoteerd ZnO/g-C3 N4 Nanocomposieten
g-C3 N4 poeder werd bereid door melamine te verhitten [20]. In het kort werd 5 g melamine in een kroes van aluminiumoxide geplaatst met een deksel dat eerst werd verwarmd tot 80 ° C, gevolgd door 4 uur calcineren bij 550 ° C in een moffeloven. Na natuurlijke afkoeling tot kamertemperatuur werd het verkregen monster tot poeder gemalen. Dan, g-C3 N4 poeder werd ultrasoon behandeld in water en gecentrifugeerd om het niet-geëxfolieerde g-C3 te verwijderen N4 .
Om de sol van N-gedoteerd ZnO te bereiden, werden de gelijke mol zinkacetaat en ureum opgelost in ethanol [10, 21]. Een geschikte hoeveelheid g-C3 N4 werd onder continu roeren aan de bovenstaande oplossing toegevoegd. De oplossing werd vervolgens 5 uur op een waterbad van 80 ° C gehouden. Daarna werd het resulterende mengsel gedroogd en 1 uur verwarmd op 400 ° C om N-gedoteerde ZnO / g-C3 te verkrijgen N4 geladen met 50 mol% N-gedoteerde ZnO, gemarkeerd als N-ZnO/g-C3 N4 .
De sol voor het synthetiseren van ZnO werd bereid door gebruik te maken van de bovenstaande methode zonder toevoeging van ureum. Dan, de ZnO/g-C3 N4 nanocomposieten geladen met 50 mol% ZnO werden bereid onder dezelfde experimentele omstandigheden, behalve voor calcineren in lucht.
Karakterisering
Röntgendiffractie (XRD) patronen werden uitgevoerd op een Rigaku D/max 2000 diffractometer met Cu Kα straling. De morfologie en microstructuur van de monsters werden onderzocht met een veldemissie scanning elektronenmicroscopie (FE-SEM; Ultra 55, Zeiss) en hoge resolutie transmissie-elektronenmicroscopie (HRTEM; Tecnai G 2 F20 S-Twin, FEI). Fourier-transformatie-infraroodspectra (FT-IR) zijn opgenomen met een Nicolet Nexus-870 infraroodspectroscopie (Thermo Nicolet) in het bereik van 400–4000 cm −1 met behulp van KBr-pellets. Chemische samenstellingen van de deeltjesmonsters werden geanalyseerd door een röntgenfoto-elektronenspectroscopie (XPS; Thermo Fisher K-Alpha) met Al Kα straling, en alle spectra werden gekalibreerd door de piek toe te wijzen op 284,6 eV. Het Brunauer-Emmett-Teller (BET) oppervlak werd geschat door een oppervlakteapparaat (TriStar-3000, Micromeritics). UV-vis diffuse reflectiespectra (UV-vis DRS) werden geregistreerd door een UV-vis spectrofotometer (UV-3600, Shimadzu) uitgerust met een integrerende bol in het bereik van 200-800 nm, en BaSO4 werd gebruikt als referentie.
Fotokatalytische activiteit
De fotokatalytische activiteit van de voorbereide fotokatalysatoren werd geëvalueerd via de afbraak van MB en fenol in waterige oplossing. Een zonnesimulator (300 W Xe-lamp) met een 420 nm afsnijfilter zorgt voor de instraling van zichtbaar licht met een lichtintensiteit van 120 mW/cm 2 . De katalysator (0,5 g/L voor MB en 5 g/L voor fenol) en 100 ml waterige oplossing met 10 mg/L MB (of 5 mg/L fenol) werden in een glazen reactor geplaatst onder continu roeren bij 250 rpm. Voorafgaand aan de bestraling werden de verontreinigende oplossingen gesuspendeerd met fotokatalysatoren gedurende 30 minuten in afwezigheid van licht geroerd om het evenwicht tussen adsorptie/desorptie tussen fotokatalysatorpoeders en MB/fenol te bereiken. Tijdens de reactie werd de temperatuur op 25 ± 1 °C gehouden. Voor elke gegeven bestralingstijd werd ongeveer 3 ml van de gereageerde oplossing onttrokken en 30 minuten bij 12.000 tpm gecentrifugeerd om de fotokatalysator te verwijderen. Vervolgens werd de concentratie van de gecentrifugeerde oplossing bepaald met een UV-vis-NIR-spectrofotometer (UV-3600, Shimadzu) met de maximale absorptie van MB en fenol bij respectievelijk 664 m en 270 nm). Na bestraling met zichtbaar licht werden de fotokatalysatoren verzameld, gewassen en 12 uur bij 100 ° C gedroogd. De stabiliteit van de fotokatalysatoren werd gecontroleerd door vier afzonderlijke cycli uit te voeren. De totale organische koolstof (TOC) werd bepaald met behulp van een Shimadzu TOC-2000-analysator. Om de actieve soorten tijdens de fotokatalytische reactie te onderzoeken, werd het effect van verschillende scavengers op de afbraak van kleurstof onderzocht. De methode was vergelijkbaar met de eerdere fotokatalytische activiteitstest onder bestraling met zichtbaar licht.
Resultaten en discussie
Afbeelding 1 toont XRD-patronen van g-C3 N4 , ZnO, N-ZnO ZnO/g-C3 N4 , en N-ZnO/g-C3 N4 composieten. De belangrijkste karakteristieke pieken kunnen worden geïndexeerd als het hexagonale ZnO met wurtzietstructuur (JPCDS 36-1451). Een sterke piek bij 27,5 °, overeenkomend met de karakteristieke diffractiepiek (002) van g-C3 N4 [10, 22], kan ook worden waargenomen. Daarom kunnen we concluderen dat de introductie van stikstof de kristalstructuur van ZnO niet verandert. Bovendien, zoals weergegeven in Fig. 1b, pieken de diffractiepieken voor N-ZnO in N-ZnO/g-C3 N4 een lichte roodverschuiving hebben, vergeleken met die voor ZnO in ZnO/g-C3 N4 , wat wijst op een algehele samentrekking van de roosterparameters [10]. De kristallietgrootte van N-ZnO (38,6 nm) afgeleid van de Scherer-formule is kleiner dan die van ZnO (45,8 nm). Dit kan worden toegeschreven aan de N-doping die de groei van ZnO kan remmen [21]. Na dotering met N is de diffractiepiek duidelijk breder dan die van ZnO (figuur 1b), vanwege de lage kristalliniteit die het gevolg was van de introductie van N in het kristalrooster van ZnO. De waarden van een specifiek oppervlak zijn 15,3 en 18,5 m 2 /g voor ZnO/g-C3 N4 en N-ZnO/g-C3 N4 , respectievelijk. Door vergelijking van het zuivere ZnO en N-ZnO worden de BET-oppervlakken van de composieten sterk vergroot. De toename van het BET-oppervlak geeft aan dat de scheidings- en migratie-efficiëntie van de fotogegenereerde dragers zou worden verbeterd, wat gunstig zou kunnen zijn voor de fotokatalytische activiteit van composiet.
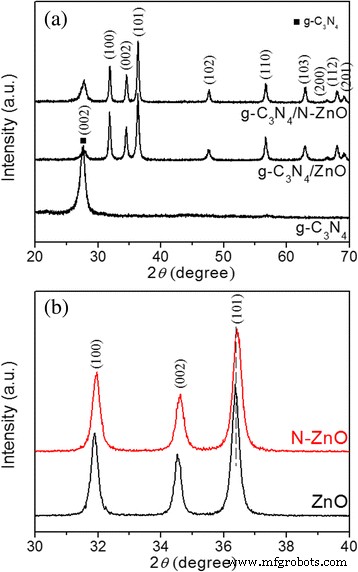
XRD-patronen (a ) van g-C3 N4 , ZnO/g-C3 N4 en N-ZnO/g-C3 N4 en de Bragg-hoekverschuiving (b ) van ZnO en N-ZnO in overeenkomstige composieten
De morfologie en microstructuur van de voorbereide fotokatalysatoren werden geanalyseerd met TEM en SEM. Zoals weergegeven in Fig. 2a, pure g-C3 N4 vertoont de bladachtige morfologie met de pluizige structuur. Figuur 2b, c toont de SEM-afbeeldingen van respectievelijk ZnO- en N-gedoteerde ZnO-monsters. In vergelijking met puur ZnO vertoont het met N-gedoteerde ZnO een kleinere kristallietgrootte met een relatief uniforme diameter, wat in overeenstemming is met de resultaten die zijn berekend met behulp van de Scherrer-formule op basis van de XRD-gegevens. Bovendien zijn de morfologieën van ZnO/g-C3 N4 en N-ZnO/g-C3 N4 samengestelde fotokatalysatoren verschillen duidelijk van die van g-C3 N4 . Het is duidelijk dat de ZnO- en N-ZnO-nanodeeltjes in ZnO/g-C3 N4 en N-ZnO/g-C3 N4 worden respectievelijk over het composietoppervlak verspreid (Fig. 2d, e). De uniforme verdeling van nanodeeltjes op g-C3 N4 zou de aggregatie van ZnO en N-ZnO kunnen minimaliseren en de reactieve plaatsen maximaliseren, wat gunstig zou kunnen zijn voor de fotokatalytische reacties [7]. In tegenstelling tot ZnO/g-C3 N4 , kan worden gevonden dat het oppervlak van N-ZnO/g-C3 N4 is duidelijk ruw en kan worden toegeschreven aan de N-ZnO-deeltjes die uniform zijn geassembleerd op het oppervlak van N-ZnO/g-C3 N4 tijdens de verwarmingsbehandeling.

SEM-afbeeldingen van a pure g-C3 N4 , b ZnO, c N-ZnO, d ZnO/g-C3 N4 , en e N-ZnO/g-C3 N4
De overeenkomstige TEM-afbeeldingen in Fig. 3 geven eveneens aan dat de juist heterogestructureerde composiet bestaat, waar N-ZnO-nanobolletjes op het oppervlak van N-ZnO/g-C3 N4 zijn goed gehecht aan de g-C3 N4 . Afbeelding 3b, c toont de HRTEM-beelden van N-ZnO/g-C3 N4 . De gemeten roosterrandafstanden van 3,25 en 2,43 Å komen goed overeen met de kristalvlakken (002) en (101) van g-C3 N4 en N-ZnO, respectievelijk.

TEM-beelden van N-ZnO/g-C3 N4
Fourier-transformatie infrarood (FT-IR) spectra van de g-C3 N4 , ZnO, N-ZnO en de composietmaterialen worden getoond in Fig. 4. Voor ZnO en N-gedoteerde ZnO, de pieken in het gebied van 400 tot 560 cm −1 komt overeen met de buigtrillingen van Zn-O-banden [6, 10], die werden waargenomen in alle monsters behalve g-C3 N4 . In het spectrum van g-C3 N4 , de pieken van 1243 en 1637 cm −1 corresponderen met de rektrillingen van respectievelijk C−N en C=N [10]. De pieken op 810 cm −1 afkomstig zijn van de ademhalingsmodus van de s-triazine-ringeenheden [23, 24]. De brede absorptieband bij een hoog golfgetal rond 3100-3400 cm −1 wordt toegeschreven aan de uitrekkende vibratie van N−H-bindingen in de −NH2 en/of =N−H-aminen, evenals de hydroxylgroepen van de chemisorbed en/of physisorbed H2 O-moleculen [10, 23]. Het is duidelijk te zien dat de belangrijkste karakteristieke IR-pieken van g-C3 N4 bestaan in de ZnO/g-C3 N4 en N-ZnO/g-C3 N4 composieten, wat suggereert dat de structurele kenmerken van g-C3 N4 worden behouden na het hybridisatieproces, in goede overeenstemming met de XRD-resultaten. Bovendien zijn de belangrijkste karakteristieke pieken van g-C3 N4 in de composieten verschuift enigszins naar een hoog golfgetal. Deze roodverschuiving kan worden toegeschreven aan het feit dat het uitgebreid geconjugeerde systeem voorkomt in de heterogestructureerde composieten [10, 25].
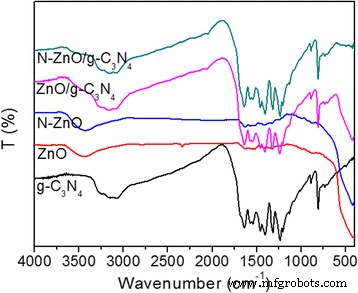
FT-IR-spectra van g-C3 N4 , ZnO, N-ZnO, ZnO/g-C3 N4 , en N-ZnO/g-C3 N4
Afbeelding 5 toont XPS-spectra van N-ZnO/g-C3 N4 . Twee pieken bij 1021,8 en 1044,9 eV in Fig. 5a worden toegeschreven aan Zn 2p3/2 en 2p1/2 , respectievelijk. De O 1s-piek is uitgerust met het niet-lineaire kleinste kwadraten-passingprogramma met behulp van Gauss-Lorentziaanse piekvormen. Na deconvolutie zijn er twee aangepaste pieken op 530,4 en 532,0 eV. De piek van 530,4 eV kan worden toegewezen aan de O 2− ionen in ZnO [26]. De andere piek van 532,0 eV kan worden toegeschreven aan de chemisch absorberende zuurstof- en/of hydroxylgroep [26] op het oppervlak van de samengestelde fotokatalysator. Het C1s-spectrum (Fig. 5c) van N-ZnO/g-C3 N4 kan ook in drie pieken worden gepast, overeenkomend met drie basissoorten C-toestanden. De bindingsenergie van 284,6 eV wordt toegeschreven aan de adventieve koolstof (C−C) op het oppervlak van N-gedoteerde ZnO/g-C3 N4 [3, 6]. De C1s-pieken bij 286,5 en 287,8 eV worden toegewezen aan de sp 3 - en sp 2 -gebonden koolstof in N−C=N van de composiet, respectievelijk. Met betrekking tot het N1s-spectrum van g-C3 N4 , zijn er drie pieken na deconvolutie, wat wijst op drie verschillende soorten N-toestanden [27, 28], de pyridine-N (C−N−C) bij 398,5 eV, pyrrolische N (N−[C]3 ) bij 399,8 eV en grafiet N (C−NH) bij 401,0 eV. Boven de drie soorten N-toestanden staan de basiseenheden van g-C3 N4 . In het N1s-spectrum (Fig. 5d) kunnen de pieken bij bindingsenergieën van 397,5 en 398,6 eV worden toegewezen aan de anionische N in O-Zn-N-koppeling [29] en sp 2 -gehybridiseerde N [28]. Hier kunnen we concluderen dat het raamwerk van g-C3 N4 wordt niet veranderd, zelfs niet als het is gecombineerd met N-ZnO-deeltjes. Bovendien bevestigen de resultaten van XRD, FT-IR en XPS dat er zowel N-gedoteerde ZnO als g-C3 zijn. N4 soorten in de heterojunctiestructuur.
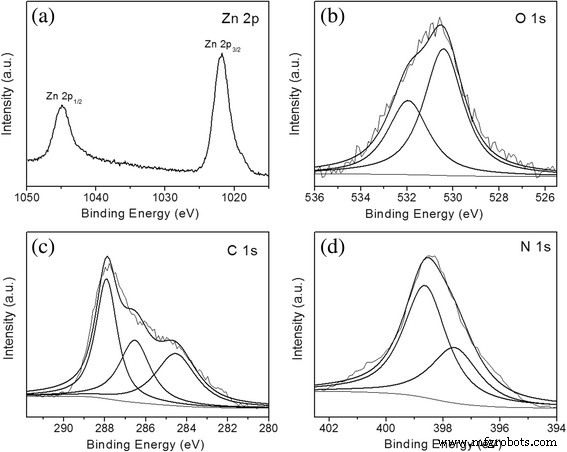
XPS-spectra van N 1s voor N-ZnO/g-C3 N4 :een Zn 2p, b O 1s, c C 1s en d N 1s
De UV-zichtbare diffuse reflectiespectra van de bereide poedermonsters werden ook gemeten met een geperste BaSO4 als een referentie. De resulterende gegevens worden uitgezet als de remissiefunctie die wordt weergegeven in Vgl. 1.
$$ F(R)=\raisebox{1ex}{${\left(1-R\right)}^2$}\!\left/ \!\raisebox{-1ex}{$2R$}\right. $$ (1)waar R is de diffuse reflectie op basis van de Kubelka-Monk-theorie. De band gap-energieën (E g ) van de directe bandgap-halfgeleider werden geschat op basis van de Vgl. 2 door het lineaire deel te extrapoleren.
$$ {\left(F(R)\cdot hv\right)}^2=A\left( hv-{E}_g\right) $$ (2)waar A is de absorptieconstanten bepaald door de directe bandgap halfgeleider van zuivere g-C3 N4 , ZnO, N-ZnO, het nanocomposiet ZnO/g-C3 N4 , en N-ZnO/g-C3 N4 . Afbeelding 6 toont de UV-vis-absorptiespectra van de voorbereide monsters. Het is duidelijk te zien dat de absorptierand van het zuivere g-C3 N4 is ongeveer 470 nm [6], wat overeenkomt met een band gap van 2,63 eV. Zoals weergegeven in Fig. 6, heeft ZnO een duidelijke absorptierand rond 390 nm in het UV-bereik. Vergeleken met het zuivere ZnO wordt een duidelijke rode verschuiving van de absorptierand naar een hogere golflengte gedetecteerd in het N-ZnO-monster, vanwege de bijdrage van stikstof aan de bovenkant van de valentieband (VB) van ZnO die de absorptie kan aansturen van N-gedoteerde ZnO dichtbij het zichtbare gebied [10]. Zo wordt de bandafstand van ZnO verminderd van 3,21 tot 3,10 eV na dotering met stikstof. Een andere belangrijke verandering is de verbeterde absorptie in het gebied van zichtbaar licht, variërend van 400 tot 600 nm voor de ZnO/g-C3 N4 en N-ZnO/g-C3 N4 , vergeleken met het zuivere ZnO en N-ZnO. Het kan worden toegeschreven aan de effectieve oppervlaktehybridisatie [6, 30] tussen g-C3 N4 en ZnO (N-gedoteerde ZnO) op het oppervlak. Verder N-ZnO/g-C3 N4 (2,73 eV) tonen de bredere absorptierand in het zichtbare gebied, vergeleken met ZnO/g-C3 N4 (2,85 eV), wat in het voordeel is van de fotodegradatie van kleurstoffen onder bestraling met zichtbaar licht.
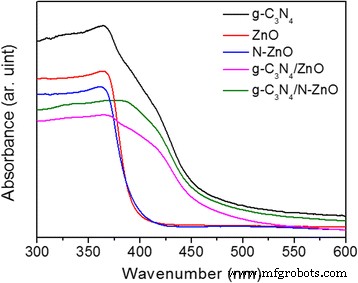
UV-zichtbare absorptiespectra van g-C3 N4 , ZnO, N-ZnO, ZnO/g-C3 N4 , en N-ZnO/g-C3 N4
De geleidingsband (CB) en valentieband (VB) randen van g-C3 N4 en ZnO lokaliseren ongeveer bij respectievelijk -1,3 eV/+-1,4 eV en − 0,5 eV/+-2,7 eV vs. NHE [6, 8, 31]. Voor N-ZnO kunnen de randpotentialen van VB en CB worden bepaald met behulp van de volgende vergelijking [32].
$$ {E}_{\mathrm{VB}}=X-{E}_{\mathrm{e}}+0,5{E}_{\mathrm{g}} $$ (3) $$ {E} _{\mathrm{CB}}={E}_{\mathrm{VB}}-{E}_{\mathrm{g}} $$ (4)waar E VB , X , en E e zijn de randpotentiaal van de valentieband, de absolute elektronegativiteit van de halfgeleider die wordt bepaald door het geometrische gemiddelde van de elektronegativiteit van de samenstellende atomen, en de energie van het vrije elektron op de waterstofschaal (~-4,5 eV), respectievelijk [10 , 24]. De E VB en E CB van N-gedoteerde ZnO worden berekend op respectievelijk 2,65 en − 0,45 eV.
Figuur 7 toont de fotokatalytische afbraak van MB met behulp van de voorbereide fotokatalysatoren onder de bestraling met zichtbaar licht. Elk monster heeft een lage adsorptiecapaciteit van MB. Er wordt bijna geen afbraak van MB waargenomen in afwezigheid van zichtbaar licht of katalysator, wat aantoont dat MB stabiel is onder de bovenstaande omstandigheden. Zoals getoond in Fig. 7a, is na N-doping de fotokatalytische stabiliteit van N-ZnO verbeterd, wat aangeeft dat de introductie van N-doping de recombinatie van fotogegenereerde ladingsdragers kan onderdrukken. Ondertussen zijn de fotokatalytische activiteiten van ZnO/g-C3 N4 en N-ZnO/g-C3 N4 samengestelde katalysatoren zijn duidelijk hoger dan die van de zuivere referentiemonsters. De verbeterde fotokatalytische activiteit wordt toegeschreven aan de heterostructuur van composieten, die de door foto gegenereerde elektronenoverdracht kan bevorderen en de recombinatie van de elektron-gatparen kan onderdrukken [7, 33]. Bovendien is de N-ZnO/g-C3 N4 katalysator vertoont een hogere fotokatalytische activiteit dan ZnO/g-C3 N4 , ondanks ZnO/g-C3 N4 heterostructuur. Het kan te danken zijn aan de verbeterde absorptie in het zichtbare gebied om de elektron-gatparen en smallere bandafstand-energie te produceren. De experimentele resultaten werden aangepast aan de pseudo-eerste-orde kinetiek. Bij een lage initiële concentratie verontreinigende stoffen, de constante snelheid k werd gegeven door vgl. 5.
$$ \ln \raisebox{1ex}{$C$}\!\left/ \!\raisebox{-1ex}{${C}_0$}\right.=- kt $$ (5)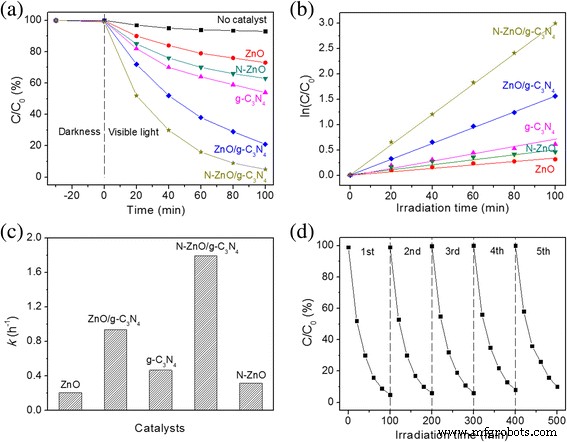
een Fotokatalytische afbraak van MB met behulp van ZnO, N-ZnO, g-C3 N4 , ZnO/g-C3 N4 , en N-ZnO/g-C3 N4 katalysatoren onder bestraling met zichtbaar licht, b de bijbehorende ln (C /C 0 ) vs. tijdcurven, c de snelheidsconstanten van MB-fotodegradatie, en d vijf cycli van MB-degradatie voor N-ZnO/g-C3 N4
Hier, k en t vertegenwoordigen de eerste-orde snelheidsconstante (h −1 ) en de bestralingstijd (h), respectievelijk. C 0 is de beginconcentratie van MB, en C is de concentratie bij een reactietijd van t . De corresponderende plots van ln (C 0 /C ) versus de bestralingstijd voor fotodegradatie van MB worden getoond in Fig. 7b. Een lineaire relatie tussen ln (C 0 /C ) en de bestralingstijd heeft geverifieerd dat de fotodegradatie van MB de eerste-ordekinetiek volgt. De berekende eerste-orde snelheidsconstanten (k ) worden weergegeven in Fig. 7c. De kinetische constante van N-ZnO/g-C3 N4 is 1,794 u −1 , wat 5,68, 3,85 en 1,91 keer hoger is dan die van N-ZnO (0,316 h −1 ), g-C3 N4 (0.466 u −1 ), en ZnO/g-C3 N4 (0.937 u −1 ). Blijkbaar is N-ZnO/g-C3 N4 vertoont de hoogste degradatie-efficiëntie van MB van alle katalysatoren. Om de stabiliteit van de fotokatalysator te evalueren, worden de recyclische experimenten over het door licht afgebroken MB uitgevoerd met de N-ZnO/g-C3 N4 katalysator. Zoals getoond in Fig. 7d, is de fotokatalytische activiteit van N-ZnO/g-C3 N4 vertoont een zeer beperkte daling. De degradatie-efficiëntie van de MB-oplossing is bijna 90% na 100 min, zelfs bij het vijfde recyclingexperiment.
Fenol werd ook gebruikt als een representatieve recalcitrante verontreinigende stof om de fotokatalytische prestaties van katalysatoren onder bestraling met zichtbaar licht te evalueren, en de resultaten worden getoond in Fig. 8. De fotokatalytische afbraaksnelheden worden uitgedrukt door Vgl. 5, waar C is de tijdelijke concentratie van fenol na bestraling, en C 0 is de concentratie na het adsorptieproces. Van alle katalysatoren is N-ZnO/g-C3 N4 presenteert de hoogste fotodegradatie-efficiëntie van fenol. Gebaseerd op de corresponderende plots (Fig. 8b) van ln (C 0 /C ) vs. de bestralingstijd, de kinetische constanten van g-C3 N4 , ZnO/g-C3 N4 , en N-ZnO/g-C3 N4 zijn 0,013, 0,026 en 0,034 h −1 , respectievelijk. Belangrijker is dat N-ZnO/g-C3 N4 vertoont uitstekende fietsstabiliteit (Fig. 8d) voor verwijdering van fenol. De bovenstaande resultaten bevestigen verder dat de N-ZnO/g-C3 N4 katalysator heeft een uitstekend fotodegradatievermogen van zowel MB als fenol, vanwege de kleinere bandafstand en bredere absorptierand in het zichtbare gebied vergeleken met die van ZnO/g-C3 N4 .
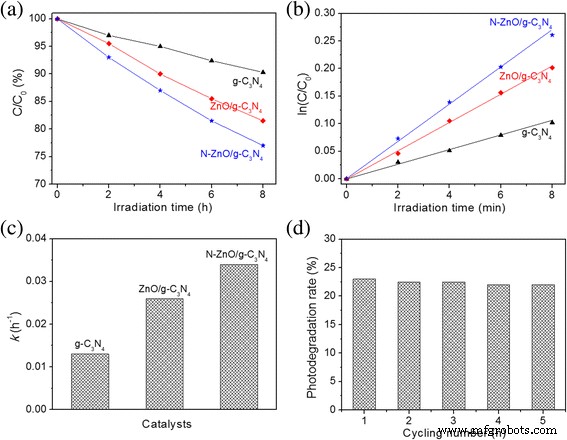
een Fotokatalytische afbraak van fenol met behulp van g-C3 N4 , ZnO/g-C3 N4 en N-ZnO/g-C3 N4 katalysatoren onder bestraling met zichtbaar licht, b de corresponderende eerste-orde kinetische plots en c de snelheidsconstanten van fenolafbraak, en d degradatie-efficiëntie na 8 uur gedurende vijf herhaalde processen door de N-ZnO/g-C3 N4 fotokatalysator
Door de totale organische koolstof (TOC) te meten, wordt de fotokatalytische mineralisatie van de N-ZnO/g-C3 N4 werd uitgevoerd door afbraak van MB en fenol in een waterige oplossing onder bestraling met zichtbaar licht. Afbeelding 9 toont de efficiëntie van de TOC-verwijdering van MB en fenol als functie van de reactietijd. Zoals te zien is in figuur 9a, was MB na 120 minuten volledig afgebroken en bereikt het TOC-verwijderingspercentage 93%. Tijdens het fotodegradatieproces werd MB afgebroken tot verschillende tussenproducten, wat de splitsing kan zijn van een of meer methylgroepensubstituent op de aminegroepen [34], en uiteindelijk volledig afgebroken tot CO2 en H2 O. Ter vergelijking:de mineralisatie van fenol bereikte slechts 18%. De belangrijkste tussenproducten zijn hydrochinon (HQ), p-benzochinon (p-BQ), 1,3-dihydroxybenzeen (DB), maleïnezuuranhydride (MA) en andere lage vetzuren (LFA's) [35, 36]. HQ en p-BQ kunnen gemakkelijk worden geoxideerd tot andere tussenproducten of anorganische koolstof. MA en LFA in het reactiesysteem zijn moeilijk verder te oxideren en te mineraliseren.
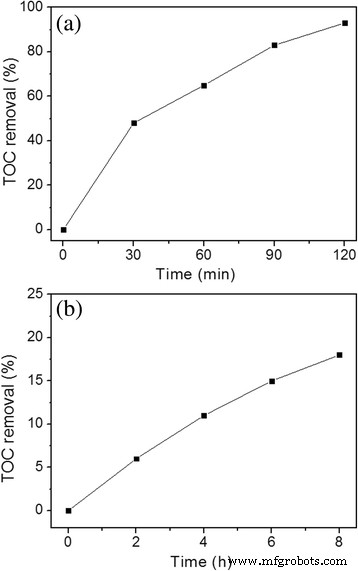
TOC verwijdering van a MB en b fenolafbraak door N-ZnO/g-C3 N4 fotokatalysator
Bij de fotokatalytische afbraak van organische verontreinigende stoffen zijn er reeksen fotogegenereerde reactieve soorten zoals gat (h + ), hydroxylradicalen (•OH) en superoxide-anionen (O2 •− ). Om te begrijpen hoe de verschillende reactieve soorten een rol spelen in het fotodegradatieproces, werden de verschillende scavengers gebruikt om de actieve soorten te detecteren tijdens het fotokatalytische afbraakproces. Hier werden EDTA, isopropylalcohol (IPA) en benzochinon (BQ) als gat aangenomen (h + ), hydroxylradicaal (•OH) en superoxide-anion (O2 •− ) aaseters in een concentratie van respectievelijk 1,0 mM. Door de fotokatalytische experimenten, de N-ZnO/g-C3 N4 composiet vertoonde de beste degradatie voor de MB-oplossing. Dus werd de MB-oplossing gekozen voor de opruimingsexperimenten. Zoals getoond in Fig. 10, werd ook een duidelijke afname van de fotokatalytische activiteit waargenomen door de toevoeging van respectievelijk EDTA en BQ, wat suggereert dat beide h + en O2 •− spelen een belangrijke rol bij de fotokatalytische reactie. Ondertussen werd de fotokatalytische afbraak van MB sterk onderdrukt door de toevoeging van IPA, wat aangeeft dat de hydroxylradicalen (•OH) de belangrijkste actieve soorten zijn en een dominante rol spelen in de fotokatalytische reactie.
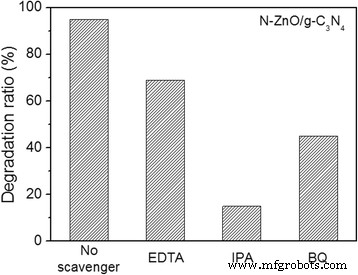
Effect van verschillende scavengers op de afbraak van MB over de N-ZnO/g-C3 N4 katalysator
De schematische illustratie van de ladingsoverdracht en het fotokatalytische mechanisme voor de N-ZnO/g-C3 N4 composiet fotokatalysator wordt getoond in Fig. 11. Onder de bestraling met zichtbaar licht, de elektron-gat-paren in de g-C3 N4 en N-ZnO-vormen. En dan transporteren de elektronen in aangeslagen toestand van het VB naar het CB. Het geleidingsbandelektron en het valentiebandgat scheiden zich dus op het oppervlak van de katalysator. De door foto gegenereerde elektronen worden overgedragen van het CB van g-C3 N4 aan de CB van N-ZnO vanwege het CB-potentieel van g-C3 N4 dat is negatiever dan de CB-rand van N-ZnO, dus de scheidingsefficiëntie van het elektron-gatpaar wordt verbeterd [10]. De CB-potentiaal van N-gedoteerde ZnO (−0,45 eV vs. NHE) ligt onder de standaard redoxpotentiaal E 0 (O2 /O2 − ) (−0,33 eV versus NHE). Dus de fotogegenereerde elektronen in het CB van N-gedoteerde ZnO zouden vervolgens reageren met de opgeloste O2 om de hoge oxidatieve hydroxylradicalen te vormen, die de verontreinigende stoffen zouden kunnen oxideren [5]. Bovendien hebben de foto-geïnduceerde elektronen een groter negatief potentieel om de moleculaire zuurstof te reduceren tot superoxide-anion (O2 •− ), die vervolgens de afbraak van organische verontreinigende stoffen induceert. Volgens de eerdere rapporten [6, 30] zouden de foto-geëxciteerde gaten op de VB van N-ZnO kunnen overgaan naar de VB van g-C3 N4 . De foto-geïnduceerde gaten van g-C3 N4 kan de geadsorbeerde H2 . niet oxideren O-moleculen om de hydroxylradicalen op te leveren omdat de VB-potentiaal van g-C3 N4 (+1,4 eV vs. NHE) is kleiner dan de standaard redoxpotentiaal E 0 (H2 O/OH·) (+2,4 eV vs. NHE) [7, 10]. Op basis van de bovenstaande discussie gaan de meerderheidsgaten bij de VB van N-ZnO niet over naar de VB van g-C3 N4 . Deze door licht opgewekte gaten kunnen de organische kleurstof direct oxideren om de reactieve tussenproducten [5] te verkrijgen en/of reageren met de H2 O om de hydroxylradicalen [2] te vormen, de belangrijkste reactieve soorten in de fotokatalytische reactie. Daarom stellen we voor dat de N-ZnO/g-C3 N4 heterojunctiestructuur kan de scheiding van elektron-gatparen verbeteren en de recombinatie van ladingsdragers verminderen, wat leidt tot een toename van het fotodegradatieproces.
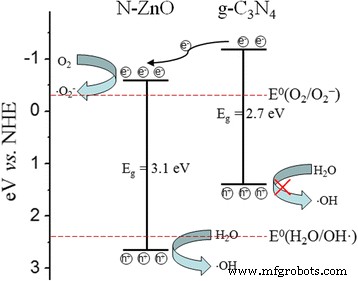
Schematic illustration of the band edge positions and proposed photocatalytic mechanism for the N-ZnO/g-C3 N4 composite catalyst
Conclusies
In summary, N-ZnO/g-C3 N4 composite photocatalyst was successfully prepared via a facile sol-gel method. The addition of g-C3 N4 enhances the light absorption in the visible region, generates more charge carriers, and simultaneously promotes the electron and hole segregation and migration. As compared with ZnO/g-C3 N4 , the N-ZnO/g-C3 N4 shows higher photocatalytic activity on the degradation of MB and phenol, due to its improved absorption in the visible region and narrower band gap energy. The mechanism of the photocatalysis is analyzed, and the stability is also evaluated by recycling photocatalytic ability.
Nanomaterialen
- Hoge fotokatalytische prestaties van twee soorten grafeen-gemodificeerde TiO2-composietfotokatalysatoren
- De effecten van Li/Nb-verhouding op de voorbereiding en fotokatalytische prestaties van Li-Nb-O-verbindingen
- Hydrothermische synthese van In2O3 nanodeeltjes hybride tweeling hexagonale schijf ZnO heterostructuren voor verbeterde fotokatalytische activiteiten en stabiliteit
- Voorbereiding en fotokatalytische prestaties van LiNb3O8-fotokatalysatoren met holle structuur
- Een nieuwe Bi4Ti3O12/Ag3PO4 heterojunctie-fotokatalysator met verbeterde fotokatalytische prestaties
- De fabricage en zeer efficiënte elektromagnetische golfabsorptieprestaties van CoFe/C Core-Shell gestructureerde nanocomposieten
- Zure peptiserende agent-effect op anatase-rutielverhouding en fotokatalytische prestaties van TiO2-nanodeeltjes
- PtNi-legering Cocatalyst-modificatie van eosine Y-gesensibiliseerde g-C3N4/GO-hybride voor efficiënte zichtbaar-licht fotokatalytische waterstofevolutie
- Fabrikatie en fotokatalytische eigenschap van nieuwe SrTiO3/Bi5O7I nanocomposieten
- Vervaardiging van hiërarchische ZnO@NiO Core-Shell heterostructuren voor verbeterde fotokatalytische prestaties
- Invloed van Mg-doping op ZnO-nanodeeltjes voor verbeterde fotokatalytische evaluatie en antibacteriële analyse



