Organische fosfor- en calciumbron induceren de synthese van in dooierschaal gestructureerde microsferen van calciumfosfaat met een hoog specifiek oppervlak:toepassing bij HEL-adsorptie
Abstract
Calciumfosfaatmicrosferen met een dooierschaalstructuur hebben een groot potentieel voor medische toepassingen vanwege hun uitstekende fysisch-chemische eigenschappen en biocompatibiliteit. Het ontwikkelen van calciumfosfaat met een dooierschaalstructuur en een hoog adsorptievermogen blijft echter een uitdaging. Hierin wordt een poreuze dooierschaal-gestructureerde microsfeer (ATP-CG) van calciumfosfaat met een hoog specifiek oppervlak [S BET =143 m 2 g −1 , die ongeveer drie keer zo hoog is als die van ATP-CL-microsferen die zijn gesynthetiseerd door calciumbron te vervangen door calcium-l-lactaatpentahydraat (CL)] werd met succes gesynthetiseerd door adenosine 5'-trifosfaatdinatriumzout (ATP) als fosforbron te gebruiken en calciumgluconaat-monohydraat (CG) als calciumbron via een zelftemplerende benadering. De invloeden van de molaire verhouding van Ca tot P (Ca/P), hydrothermische temperatuur en tijd op de morfologie van ATP-CG-microsferen werden ook onderzocht. Het is gebleken dat de organische calciumbron en de organische fosforbron een vitale rol spelen bij de vorming van de dooierschaalstructuur. Verder werd een reeks adsorptie-experimenten onderzocht om het adsorptiemechanisme te belichten van twee soorten microsferen met een dooierschaalstructuur, gesynthetiseerd met verschillende calciumbronnen. De resultaten laten zien dat de adsorptiecapaciteit van ATP-CG-microsferen (332 ± 36 mg/g) ongeveer twee keer hoger is dan die van ATP-CL-microsferen (176 ± 33 mg/g). Bovendien spelen het hogere specifieke oppervlak veroorzaakt door de calciumbron en de unieke chemische oppervlakte-eigenschappen voor ATP-CG-microsferen een belangrijke rol bij de verbetering van het HEL-adsorptievermogen. De studie geeft aan dat de in de vorm van een dooierschaal gestructureerde microsfeer veelbelovend is voor toepassing op het gebied van medicijnafgifte en een effectieve benadering biedt voor het verbeteren van het adsorptievermogen van geneesmiddelen.
Inleiding
Calciumfosfaat heeft de afgelopen jaren veel aandacht gekregen vanwege zijn uitstekende biocompatibiliteit [1], hoge laadcapaciteit en leveringsefficiëntie. Calciumfosfaat-gerelateerde biomaterialen zijn op grote schaal gebruikt in verschillende biomedische gebieden, zoals tissue engineering [2], botreparatie [3] en medicijnafgifte [4]. Om het toepassingsgebied uit te breiden en de prestaties van op calciumfosfaat gebaseerde materialen te verbeteren, verschillende calciumfosfaatmaterialen met verschillende morfologieën en microstructuren, waaronder koolzuurhoudende hydroxyapatiet (HAp) microsferen [5], HAp-microbuisjes [6], holle HAp-microsferen [7 ], mesoporeuze dooier@cage-shell nanosferen van amorf calciumfosfaat (ACP) [8] zijn gemeld.
Onder verschillende morfologieën hebben dooierschaal-gestructureerde microsferen steeds meer aandacht getrokken, omdat ze niet alleen grensverleggende materiaalwetenschap zijn, maar ook unieke morfologische kenmerken vertonen. In dooierschaal-gestructureerde microsferen kan de lege ruimte tussen dooierkern en schaal dienen als een opslagreservoir voor verschillende ladingen en de poreuze gestructureerde schaal kan een diffusieroute bieden voor gastmoleculen, waardoor ze een groot potentieel hebben voor diverse toepassingen, waaronder katalyse [9], lithium-ionbatterijen [10], fotokatalysator [11] en biogeneeskunde [12]. Traditioneel zijn het opofferen van sjabloonmethoden de primaire methoden om microsferen met een dooierschaal te bereiden [13, 14]. Deze sjabloonstrategieën hebben veel succes geboekt bij het aanpassen van de structuur en eigenschappen. Deze benaderingen hebben echter enkele nadelen. Bijvoorbeeld vervelende verwerkingsstappen en oppervlakteactieve of structuurbepalende reagentia, die gevaarlijk kunnen zijn voor de gezondheid van de mens. Momenteel zijn de zelf-template-methoden op grote schaal gebruikt bij het onderzoek naar met dooierschaal gestructureerde microsferen [15, 16]. In tegenstelling tot de traditionele sjabloonbenaderingen, zijn de sjablonen die worden gebruikt bij zelfsjabloonbenaderingen niet alleen de sjablonen voor het vormen van de holtes, maar ook de voorloper van met dooierschaal gestructureerde microsferen. Zelftemplerende methoden zijn dus handige benaderingen om met dooierschaal gestructureerde microsferen te bereiden. De introductie van zelftemplerende benaderingen voor de synthese van calciumfosfaatmicrosferen met een dooierschaalstructuur blijft echter een interessante uitdaging.
Verder zijn calciumfosfaatmaterialen gebruikt om verschillende soorten ladingen te vervoeren, zoals eiwitten [17], DNA [18] en siRNA [19]. Het slechte geneesmiddeladsorptievermogen van calciumfosfaat moet echter dringend worden opgelost. In het algemeen hangen de benaderingen van geneesmiddelmoleculen die immobiliseren over het oppervlak van de drager af van de oppervlakte-eigenschappen die oppervlaktepotentiaal [20], hydrofobiciteit/hydrofiliciteit [21], waterstofbinding [22] en specifiek oppervlak [23] bevatten. Het verbeteren van de oppervlakte-eigenschappen en het specifieke oppervlak is dus een geldige benadering om het adsorptievermogen van de drager voor geneesmiddelen te verbeteren.
Hierin hebben we een soort poreuze dooierschaal-gestructureerde microsferen van calciumfosfaat gemaakt door adenosine 5'-trifosfaat-dinatriumzout (ATP) als de fosforbron en calciumgluconaatmonohydraat (CG) als de calciumbron te gebruiken door middel van een zelftemplerende benadering. Zonder enige toevoeging van templaatmiddel vertonen de bereide calciumfosfaatmicrobolletjes met dooierschaalstructuur een bijzonder hoog specifiek oppervlak. Verder werd het adsorptiegedrag van kippenei-lysozym (HEL) van ATP-CG-microsferen onderzocht in vergelijking met de ATP-CL-microsferen bereid door de calciumbron te vervangen door calcium-l-lactaatpentahydraat (CL). De resultaten laten zien dat het verschil in specifiek oppervlak veroorzaakt door de calciumbron en chemische oppervlakte-eigenschappen een cruciale rol spelen bij de verbetering van het HEL-adsorptievermogen.
Methoden
Materialen
Adenosine-5'-trifosfaatdinatriumzout (ATP) werd verkregen van Macklin Biochemical Co., Ltd (Shanghai, China). Calciumgluconaatmonohydraat (CG) en calcium (l)-lactaatpentahydraat (CL) werden verkregen van Sangon Biotech Co., Ltd (Shanghai, China). Het kippenei-lysozym (HEL, ~ 70000 E/mg) werd gekocht bij Sigma-Aldrich (Taufkirchen, Duitsland).
Synthese en karakterisering van ATP-CG en ATP-CL Yolk-Shell-gestructureerde microsferen
De ATP-CG-dooierschaal-gestructureerde calciumfosfaatmicrosferen werden als volgt bereid:In het kort werd 0,9 g CG opgelost in 20 ml ultrazuiver water om oplossing C te vormen bij 60 °C en 0,11 g ATP werd opgelost in 5 ml van ultrapuur water om oplossing P te vormen. Vervolgens werd oplossing C afgekoeld tot kamertemperatuur en onder krachtig roeren gemengd met oplossing P en werd de pH van de oplossing met 2 M NaOH-oplossing op 5 ingesteld. Het uiteindelijke volume van de oplossing was 30 ml met de extra toevoeging van ultrapuur water en de molaire verhouding van Ca tot P (Ca/P) was 3,3. De uiteindelijke oplossing werd overgebracht naar een microgolfdigestiesysteem voor een hydrothermische microgolfreactie en gedurende 15 minuten bij 120 ° C behandeld. De resulterende precipitaten werden verzameld door centrifugeren (4500 rpm, 10 min), gespoeld met ultrapuur water en 48 uur gevriesdroogd. De ATP-CL-microsferen werden bereid volgens de literatuurprocedures [24].
De kristallijne fase van de microsferen werd gekenmerkt door röntgendiffractie (XRD, Cu Kα bron, λ =0,154). De morfologie van microsferen werd waargenomen door scanning-elektronenmicroscopie (SEM), transmissie-elektronenmicroscopie (TEM) en TEM met hoge resolutie (HRTEM). De samenstellingen van microsferen werden bestudeerd door Fourier-transformatie infrarood spectrofotometer (FTIR). Het specifieke oppervlak van microsferen werd bepaald door Brunauer-Emmett-Teller (BET). Thermogravimetrieanalyse (TGA) werd gebruikt om de thermische eigenschappen van monsters te bestuderen bij een verwarmingssnelheid van 10 °C/min in een stikstofatmosfeer.
HEL-adsorptie en karakterisering
De HEL-adsorptie-experimenten van twee soorten microsferen werden als volgt uitgevoerd:de bepaalde hoeveelheden dooierschaalmicrosferen (ATP-CG, Ca/P =3,3, 120 °C, 15 min, en ATP-CL, Ca/P =2,5, 120 ° C, 30 min) werden gedispergeerd in het water met constante ultrasone behandeling gedurende 10 min om 1,5 mg/ml microsferensuspensie te vormen. Vervolgens werd 0,5 ml waterige oplossingen die verschillende concentraties HEL bevatten onmiddellijk toegevoegd aan 1 ml bovenstaande suspensie en de uiteindelijke concentraties van het geneesmiddel waren 1-7,5 mg/ml. Elke oplossing werd 6 uur geschud (200 rpm) bij 37 ° C. Later werden de oplossingen gecentrifugeerd en werden de hoeveelheden HEL in de supernatanten gemeten met een UV-vis-spectrofotometer bij 280 nm. De zeta-potentialen en samenstellingen van microsferen voor en na het laden van geneesmiddelen werden gekarakteriseerd door zeta-potentiaalanalysator, FTIR-spectrometer en thermogravimetrische analysator (TGA, verwarmingssnelheid 10 °C min −1 , stikstofatmosfeer).
Adsorptie-isotherm
Om het adsorptiegedrag te onderzoeken, werd in ons onderzoek een Dubinin-Radushkevic isotherm (D-R) -model uitgevoerd. Het D-R-model is gebaseerd op de theorie van het vullen van microporiën, die wordt gebruikt om de niet-ideale sorptie op een heterogeen oppervlak te beschrijven en om het sorptiemechanisme (fysische sorptie of chemische sorptie) te onderscheiden. Het model wordt uitgedrukt door de volgende vergelijking:waarbij Q eq is de adsorptiecapaciteit van het adsorbens bij evenwicht (mg/g), C eq is de adsorbaatconcentratie in de waterige fase bij evenwicht (mL/L). V m is de maximale adsorptiecapaciteit. R is gasconstante, 8,314 J/(mol ∙ k). T absolute temperatuur is. E vertegenwoordigt de gemiddelde vrije energie voor het schatten van het type adsorptie. Als de E waarde lager is dan 8 kJ/mol, het adsorptietype kan worden verklaard door fysieke adsorptie, tussen 8 en 16 kJ/mol, het adsorptietype behoort tot ionenuitwisseling en groter is dan 16 kJ/mol, het adsorptietype kan worden beschreven door chemische adsorptie .
$$ {Q}_{\mathrm{eq}}={Q}_m\exp \left(-{K}_{\mathrm{DR}}\ {\varepsilon}^2\right) $$ (1) $$ \varepsilon =\text{RT1n}(1+\frac{1}{{C}_\text{eq}}) $$ (2) $$ \mathrm{E}=\frac{1}{\ sqrt{K_{\mathrm{DR}}}} $$ (3)Statistische analyse van geneesmiddeladsorptie
Gegevens werden gepresenteerd als gemiddelde ± standaarddeviatie (SD) waarde. Aanzienlijke verschillen (p <0,05) werden statistisch berekend tussen verschillende groepen met behulp van de one-way ANOVA. Alle experimenten werden in drievoud uitgevoerd en de gegevens werden geanalyseerd met behulp van de DPS-software.
Resultaten en discussie
Morfologie en chemische karakterisering van microsferen
ATP-CG Yolk-Shell-Structured Microspheres
SEM-afbeeldingen in Fig. 1 tonen de morfologieën van verschillende monsters die zijn verkregen onder verschillende reactieomstandigheden. Bij t =5 min of 15 min, alle producten zijn samengesteld uit uniforme microsferen. Toen de hydrothermische tijd echter verder werd verhoogd tot 30 minuten, werden zelf-geassembleerde microsferen van nanobladen gevormd (zoals weergegeven in Fig. 1 f, i, l). Ondertussen wordt het effect van Ca/P op de morfologie van producten ook waargenomen bij t =30 minuten. Naarmate de Ca / P toenam, werden de zelf-geassembleerde microsferen van nanobladen geleidelijk gevormd (zoals getoond in Fig. 1 f, i, l). De vorming van zelf-geassembleerde microsferen van nanosheets kan worden verklaard door de volgende redenen. Ten eerste kunnen ATP-moleculen onder het hydrothermische microgolfproces hydrolyseren om op adenosine gebaseerde moleculen te vormen, waaronder adenosinedifosfaat (ADP), adenosinemonofosfaat (AMP) en adenosine, en tegelijkertijd fosfaationen vrij te geven (PO4 3− ). Ondertussen kunnen CG-moleculen hydrolyseren om gluconaat- en calciumionen te vormen (Ca 2+ ). Vervolgens zouden fosfaationen reageren met calciumionen om primaire ACP-kernen te vormen [25]. Vervolgens groeien de initiële ACP-kernen en assembleren ze om ACP-microsferen te vormen. Daarom, wanneer de hydrothermische tijd verder wordt verlengd, worden de ATP- en CG-moleculen in oplossing verder gehydrolyseerd en geven ze meer PO4 af 3− en Ca 2+ ionen, die de vorming van zelf-geassembleerde microsferen van nanobladen veroorzaken door de oververzadiging van het systeem en de nucleatiesnelheid te verbeteren. Bovendien, door de Ca/P te verhogen, wordt de lokale hoge concentratie Ca 2+ versnelt ook de morfologische transformatie van producten op dezelfde manier als hierboven. Bovenstaande analyse geeft aan dat de hydrothermische tijd en Ca/P een belangrijke invloed hebben op de morfologie van producten.

SEM-beelden van ATP-CG-microsferen bereid met de hydrothermische microgolfmethode bij 120 °C
Vervolgens worden de FTIR-spectra van microsferen gesynthetiseerd met verschillende Ca / P bij 120 ° C gedurende 15 minuten onderzocht (Fig. 2). De pieken op 1620 cm −1 , 1383 cm −1 , en 912 cm −1 toegeschreven aan de karakteristieke pieken van respectievelijk de C=O, C–O van CG en P–O groepen van ATP [26], wat impliceert dat niet-gehydrolyseerde CG- en ATP-moleculen of hun derivaten worden geabsorbeerd op het oppervlak van de microsferen. De zwakke karakteristieke piek van de PO4 3− van HAp bevindt zich op 1035 cm −1 [27] en de absorptiepieken bij 1122 cm −1 en 567 cm −1 zijn toegewezen aan PO4 3− ionen van ACP [28], wat aangeeft dat de producten zijn samengesteld uit ACP en HAp. De FTIR-resultaten suggereren dat het calciumfosfaat met succes wordt bereid door ATP als fosforbron en CG als calciumbron te gebruiken.
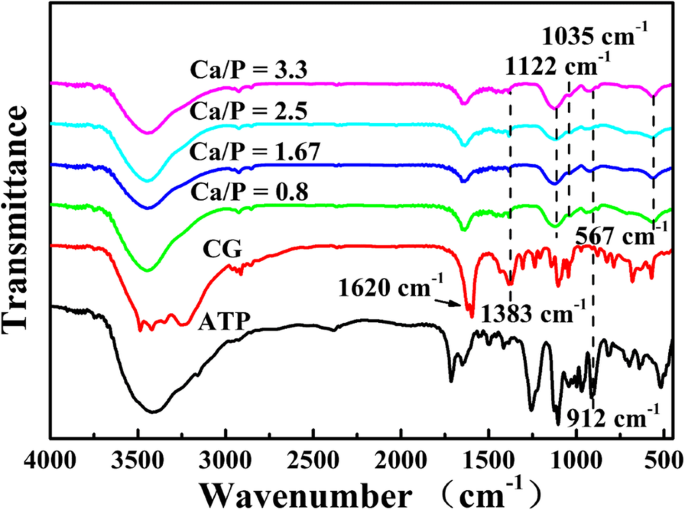
FTIR-spectra van ATP-CG-microsferen gesynthetiseerd met verschillende Ca/P bij 120 °C gedurende 15 minuten
Verder worden de SEM- en TEM-beelden van monsters die zijn gesynthetiseerd met verschillende Ca/P via microgolfhydrothermische methoden bij 120 °C gedurende 15 minuten weergegeven in Fig. 3. Wanneer de Ca/P 0,8 of 1,67 is, bestaan de monsters uit poreuze microsferen ( Afb. 3b, d). Wanneer de Ca / P 2, 5 is, begint de morfologie van producten te transformeren naar in dooierschaal gestructureerde microsferen (figuur 3f). Naarmate de Ca / P verder toeneemt tot 3,3, zijn de producten volledig samengesteld uit met dooierschaal gestructureerde microsferen (figuur 3h). Verder worden enkele gebroken bollen en de blootgestelde kernen van de dooierschaalmicrosferen (ingevoegd in Fig. 3g) waargenomen na mechanisch breken, wat het bewijs levert van een holle structuur tussen dooier en schaal. Op basis van de bovenstaande observatie stellen we voorlopig het vormingsmechanisme voor van met dooierschaal gestructureerde microsferen die zijn gesynthetiseerd met verschillende Ca / P. Wanneer de Ca/P lager is, worden eerst de poreuze ACP-microsferen gevormd, wat wordt toegeschreven aan het remmende effect van ATP- en CG-moleculen of hun derivaten die aan het oppervlak op de microsferen worden geadsorbeerd. Als de Ca/P verder wordt verhoogd, zal de metastabiele ACP verder groeien, wat wordt aangedreven door de hoge oververzadiging van het systeem. Ten slotte worden de kristallijne HAps gevormd op het buitenoppervlak, wat wordt bevestigd door het TEM (HRTEM) -beeld met hoge resolutie van microsferen in Fig. 3i (de interplanaire afstand van 0,308 nm kan worden geïndexeerd tot (210) van HAp). Als resultaat worden de holle structuren tussen dooier en schaal gegenereerd vanwege het verschil in volume of dichtheid tussen HAp en ACP [24]. De overeenkomstige EDS-toewijzing geeft aan dat de Ca-, P- en O-elementen gelijkmatig over de microsferen zijn verdeeld. De EDS-spectra in Fig. 3k en XPS-spectrum in Fig. 3l laten zien dat de chemische elementen van microsferen voornamelijk Ca, P en O omvatten, wat consistent is met het resultaat van FTIR (Fig. 2).

SEM- en TEM-beelden van ATP-CG-microsferen gesynthetiseerd met verschillende Ca/P. een , b Ca/P =0,8. c , d Ca/P =1,67. e , v Ca/P =2,5. g , u Ca/P =3,3. ik HRTEM, j EDS-mapping, k EDS-spectra, l XPS-spectra van ATP-CG-microsferen met Ca/P =3,3
De impact van microgolf-geassisteerde hydrothermische tijd en temperatuur op de morfologie van microsferen gesynthetiseerd met Ca/P =3.3 wordt verder onderzocht. Zoals getoond in Fig. 4a-b, wanneer de hydrothermische tijd 5 min is, zijn de monsters samengesteld uit poreuze microsferen. Zoals hierboven besproken, wanneer t =15 min, is het product ook samengesteld uit met dooierschaal gestructureerde microsferen (Fig. 4c-d). Wanneer de hydrothermische tijd wordt verlengd tot 60 min of de temperatuur wordt verhoogd tot 160 o C, vellen of staafgrenzen worden waargenomen (Fig. 4e-l). De morfologische transformatie van poreus naar dooierschaal naar vel of staaf wordt toegeschreven aan de verdere groei van ACP met de continue hydrolyse van ATP- en CG-moleculen in oplossing. Bovendien versnelt de hydrolyse van ATP- en CG-moleculen of hun derivaten geadsorbeerd aan het oppervlak op de ACP-microsferen ook de groei van ACP. Een interessant fenomeen deed zich voor op 60 min of 160 o C, deze vellen of staven zijn ook ontwikkeld op basis van ACP-nanodeeltjes (zoals weergegeven in rode vakken), wat wordt bevestigd door de DTA-analyse in Fig. S1. Een exotherme piek bij 650 °C wordt waargenomen in de DTA-curven [29, 30], die wordt toegeschreven aan de ACP-kristallisatie. De exotherme piek wordt geleidelijk zwak met de toename van de hydrothermische tijd of temperatuur, wat impliceert dat de transformatie van ACP in de producten naar crystillinecalciumfosfaat.

SEM- en TEM-beelden van ATP-CG-microsferen gesynthetiseerd met Ca/P =3,3 onder verschillende experimentele omstandigheden. een , b T =120 °C, t =5 minuten. c , d T =120 °C, t =15 minuten. e–h T =120 °C, t =60 minuten. i–l T =160 °C, t =15 minuten
De chemische samenstelling en structuur van monsters gesynthetiseerd met Ca/P =3.3 onder verschillende hydrothermische tijd of temperatuur worden onderzocht door de FTIR en XRD. Zoals getoond in Fig. 5a, zijn de karakteristieke pieken van PO4 3− ionen van HAp bevinden zich op 1037 cm −1 en 603 cm −1 [27]. De piek op 1122 cm −1 wordt toegewezen aan karakteristieke piek van PO4 3− ionen van ACP. De absorptie piekt bij 1620 cm −1 en 1383 cm −1 worden toegeschreven aan respectievelijk karakteristieke piek van C =O- en C-O-groepen van CG. De absorptiepiek bij 912 cm −1 verwijst naar de asymmetrische P-O-rektrilling van ATP. Door de hydrothermische tijd of temperatuur te verhogen, wordt de intensiteit van karakteristieke pieken van CG en ATP geleidelijk verlaagd, wat aangeeft dat de ATP- en CG-moleculen of hun derivaten die op het oppervlak van microsferen zijn geadsorbeerd, verder worden gehydrolyseerd. Ondertussen is de intensiteit van de karakteristieke piek van PO4 3− ionen in HAp vertonen een geleidelijk toenemende trend met de afname van de intensiteit van de ACP-karakteristieke piek, wat de transformatie van de kristallijne fase van producten naar de HAp-fase verlicht.
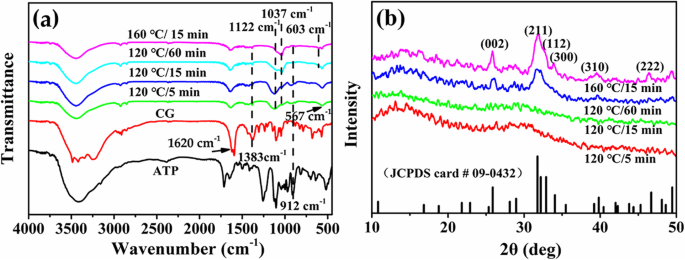
een FTIR-spectra en b XRD-patronen van ATP-CG-microsferen gesynthetiseerd met Ca/P =3,3 onder verschillende experimentele omstandigheden
Figuur 5b toont XRD-patronen van verschillende monsters. Een karakteristieke bult van amorfe fase rond 2θ =30° van microsferen gesynthetiseerd na 5 of 15 min wordt waargenomen. Wanneer de hydrothermische tijd echter wordt verlengd tot 60 minuten of de temperatuur wordt verhoogd tot 160 °C, transformeert de kristallijne fase van microsferen grondig naar HAp, wat kan worden geïndexeerd als de standaardgegevens (JDCPS nr. 09-0432). De verbetering in de relatieve intensiteit van (211), (300) en (002) roostervlakken zou de toename van de kristalliniteit van producten verder kunnen verklaren. De XRD- en FTIR-resultaten bevestigen dus verder de kristallijne fasetransformatie van producten met de toename van de hydrothermische temperatuur of tijd.
ATP-CL Yolk-Shell-Structured Microspheres
Om het adsorptiegedrag van geneesmiddelen te vergelijken, werden de andere met dooierschaal gestructureerde microsferen bereid door CL te gebruiken als organische calciumbron door middel van een hydrothermische microgolfmethode [24]. In termen van morfologie bestaan de monsters nog steeds uit dooierschaal-gestructureerde microsferen, wat wordt geverifieerd door de gebroken bollen (invoegen in Fig. 6a) en TEM-afbeeldingen (Fig. 6b, c). Het resultaat toont aan dat de verandering in calciumbron geen significant effect heeft op de morfologie van producten. Bovendien toont de elektronendiffractie van het geselecteerde gebied (SAED) de discrete SAED-spots (Fig. 6d), wat aantoont dat goed gekristalliseerde microsferen worden verkregen. Bovendien vertoont de EDS-mapping de gelijkmatige verdeling van Ca, P- en O-elementen in microsferen (figuur 6e). De overeenkomstige EDS-spectra bevestigen ook de aanwezigheid van Ca-, P- en O-elementen in microsferen (Fig. 6f), wat aangeeft dat de zoals bereide microsferen calciumfosfaat zijn.

een SEM. b , c TEM-afbeeldingen. d S elektronendiffractie met gekozen gebied (SAED). e EDS-mapping en f EDS-spectra van ATP-CL-microsferen
HEL-adsorptie- en adsorptiemechanisme van microsferen
Zoals getoond in Fig. 7, neemt de adsorptiecapaciteit van twee soorten microsferen toe met de toenemende initiële concentratie van HEL. Wanneer de initiële concentratie van HEL stijgt tot 6,5 mg/ml, bereikt de adsorptiecapaciteit van de ATP-CG-microsferen een plateau en is de maximale adsorptiecapaciteit van microsferen ongeveer 332 ± 36 mg/g (Fig. 7a), wat ongeveer tweemaal zo groot is. hoger dan die van ATP-CL-microsferen (176 ± 33 mg/g, 6 mg/ml, Fig. 7b).
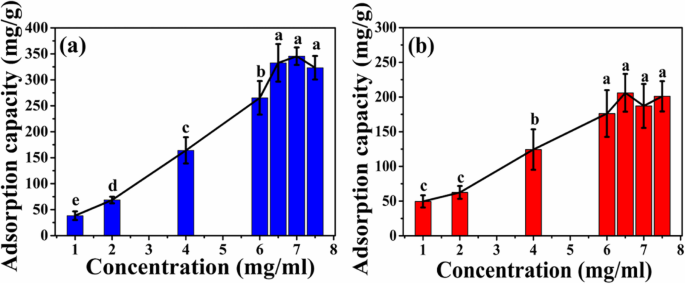
Adsorptiecurve van microsferen bij verschillende beginconcentraties van HEL. een ATP-CG-microsferen. b ATP-CL microsferen
Het HEL-adsorptieresultaat wordt verder ondersteund door de FTIR-spectra en TG-curven. Zoals getoond in Fig. 8a, b, pieken de absorptie bij 1134 cm −1 (1139 cm −1 ) en 563 cm −1 (568 cm −1 ) toegewezen aan de karakteristieke piek PO4 3− ionen van ACP en 1039 cm −1 (1040 cm −1 ) toegewezen aan karakteristieke piek van PO4 3− ionen van HAp worden waargenomen in de HEL-geadsorbeerde microsferen, wat aangeeft dat de introductie van HEL in microsferen geen significante verandering in de structuur van microsferen veroorzaakt. De adsorptie piekt bij 1542 cm −1 en 1545 cm −1 toegeschreven aan de amidegroep van HEL worden waargenomen in HEL-geadsorbeerde microsferen, wat bevestigt dat HEL met succes wordt geadsorbeerd op de microsferen. Ondertussen zijn de adsorptiebanden bij 2966, 2962, 2935 en 2927 cm −1 afkomstig uit –CH3 en –CH2 groepen HEL worden ook gedetecteerd in HEL-geadsorbeerde microsferen, wat de aanwezigheid van HEL op de microsferen verder verifieert. De TGA-curven laten zien dat het gewichtsverlies van ATP-CG-microsferen voor en na HEL-adsorptie respectievelijk 11,3% en 36,7% is (Fig. 8c). Daarom is de HEL-adsorptiecapaciteit van ATP-CG-microsferen ongeveer 340 mg/g. Er wordt echter een gewichtsverlies van 21,1% ATP-CL verkregen vóór HEL-adsorptie en 37% verschijnt op de HEL-geadsorbeerde microsferen (Fig. 8d). De HEL-adsorptiecapaciteit is dus 189 mg/g voor ATP-CL-microsferen. De TGA-resultaten zijn gesloten voor het resultaat uit Fig. 7.
FT-IR-spectra en TGA-curven van microsferen voor en na HEL-adsorptie. een FTIR-spectra en c TGA-curven van ATP-CG-microsferen, b FTIR-spectra en d TGA-curven van ATP-CL-microsferen
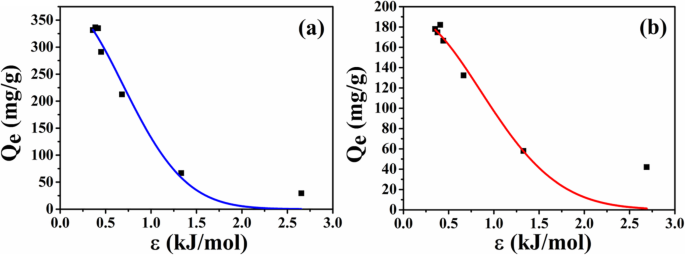
Om de oorzaak van het verschil in adsorptiecapaciteit tussen twee soorten microsferen te onderzoeken, worden de evenwichtsadsorptiegegevens van microsferen verder geanalyseerd volgens het D-R isothermmodel. De aanpascurves worden getoond in Fig. 9 en de aanpasparameters worden respectievelijk vermeld in Tabel 1. Uit de fittingresultaten blijkt dat de correlatiecoëfficiënt van ATP-CG hoger is dan die van ATP-CL, wat suggereert dat het D-R-model geschikt is voor het beschrijven van het geneesmiddeladsorptiegedrag van ATP-CG-microsferen. Sinds de E waarde lager is dan 8 kJ/mol, is de adsorptie van HEL op ATP-CG-microsferen fysieke sorptie. De maximale capaciteit (Q m ) van ATP-CG-microsferen voor HEL kan oplopen tot bijna 381 mg/g, wat dicht in de buurt komt van het resultaat van Fig. 7a.

een Adsorptie-isothermenmodel van HEL op ATP-CG-microsferen. b Adsorptie-isothermenmodel van HEL op ATP-CL-microsferen
Aangezien de adsorptie van HEL op de ATP-CG-microsferen fysieke sorptie is, wordt het oppervlaktepotentieel van microsferen onderzocht. Zoals getoond in Fig. 10a, is de zeta-potentiaalwaarde van ATP-CG, ATP-CL-microsferen en HEL in ultrapuur water respectievelijk - 17 mV, − 22 mV en 20 mV. Na HEL-adsorptie verandert de zeta-potentiaalwaarde van ATP-CG- en ATP-CL-microsferen in respectievelijk 2,7 mV en 1,5 mV, wat aangeeft dat de adsorptie van HEL-moleculen op het oppervlak van microsferen door de aantrekkende elektrostatische kracht. De aantrekkende elektrostatische kracht is echter niet de belangrijkste oorzaak van het verschil in adsorptiecapaciteit tussen twee soorten microsferen, omdat er geen significant verschil is in zeta-potentiaalwaarden (− 17 mV en – 22 mV) tussen microsferen.
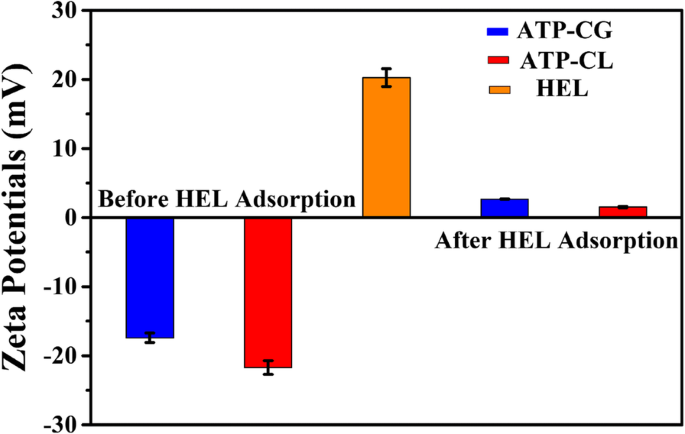
Zeta-potentialen van HEL en microsferen voor en na HEL-adsorptie
Om de reden die het verschil in absorptiecapaciteit tussen microsferen veroorzaakt verder te verhelderen, wordt daarom het specifieke oppervlak van microsferen onderzocht. Zoals getoond in Fig. 11a, is het BET-specifieke oppervlak (S BET ) van ATP-CG-microsferen is 143 m 2 g −1 , die ongeveer drie keer zo hoog is als de ATP-CL-microsferen (55 m 2 g −1 , Tafel 2). Het specifieke oppervlak kan dus bijdragen aan het verschil in absorptiecapaciteit tussen microsferen. Een dergelijk hoog specifiek oppervlak van ATP-CG-microsferen wordt voornamelijk toegeschreven aan de lage kristalliniteit [31]. Uit Fig. 11b vertonen ATP-CG-microsferen een lagere kristalliniteit dan die van ATP-CL-microsferen. Bovendien is het verschil in kristalliniteit tussen ATP-CG en ATP-CL voornamelijk te wijten aan de verschillende syntheseomstandigheden. In het algemeen neemt de kristalliniteit van het product toe met de mate van hydrolyse van reactanten onder bepaalde druk en temperatuur. Hierin is de zuurgraad van gluconzuur (pKa =3,39) hoger dan die van l-melkzuur (pKa =3,86), wat een langzamere hydrolysesnelheid zou veroorzaken en uiteindelijk een lagere kristalliniteit zou opleveren. Dientengevolge worden ATP-CG-microsferen met een hoger specifiek oppervlak verkregen door de calciumbron te veranderen.
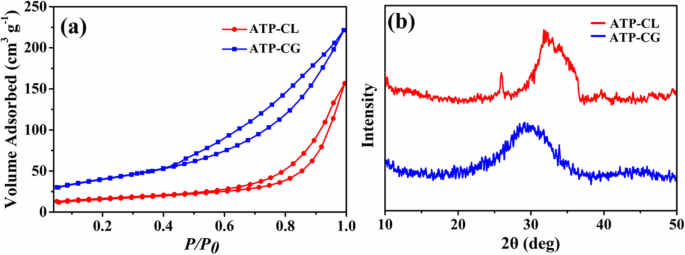
een Stikstofadsorptie-desorptie-isothermen. b XRD-patronen van microsferen
Conclusies
De ATP-CG dooierschaalmicrosferen zijn ontworpen door gebruik te maken van ATP als organische fosforbron en CG als organische calciumbron via een microgolfondersteunde hydrothermische methode. De microsferen vertonen een hoog specifiek oppervlak en een hoog adsorptievermogen. De invloeden van Ca/P, hydrothermische temperatuur en tijd op de morfologie en structuur van microsferen werden ook onderzocht. De studie geeft aan dat organische fosforbron en organische calciumbron een significant effect hebben op de vorming van dooierschaal-gestructureerde microsferen. Bovendien zijn de hydrothermische omstandigheden, waaronder Ca/P, hydrothermisch en temperatuur, verantwoordelijk voor de vorming van dooierschaalmicrosferen. Verder vinden we dat het specifieke oppervlak en chemische oppervlakte-eigenschappen zoals oppervlaktepotentiaal twee sleutelfactoren zijn die de adsorptiecapaciteit van microsferen beïnvloeden door het HEL-adsorptiegedrag van twee soorten microsferen te vergelijken die zijn gesynthetiseerd met verschillende calciumbronnen.
Beschikbaarheid van gegevens en materialen
Alle gegevens die de conclusies van dit artikel ondersteunen, zijn in het artikel opgenomen.
Afkortingen
- BET:
-
Brunauer-Emmet-Teller metingen
- FTIR:
-
Fourier-transformatie infraroodspectroscopie
- TEM:
-
Transmissie-elektronenmicroscopie
- XRD:
-
Röntgendiffractie
- TGA:
-
Thermogravimetrie analyse
- HRTEM:
-
TEM met hoge resolutie
- SAED:
-
Elektronendiffractie met geselecteerd gebied
Nanomaterialen
- Voorbereiding van met ICA geladen mPEG-ICA nanodeeltjes en hun toepassing bij de behandeling van door LPS geïnduceerde H9c2-celbeschadiging
- Ultra-smalle band Perfect Absorber en zijn toepassing als plasmonische sensor in het zichtbare gebied
- Eenvoudige synthese van gekleurd en geleidend CuSCN-composiet gecoat met CuS-nanodeeltjes
- Het effect van contactloos plasma op structurele en magnetische eigenschappen van Mn Х Fe3 − X О4 Spinels
- Effect van in situ gloeibehandeling op de mobiliteit en morfologie van op TIPS pentaceen gebaseerde organische veldeffecttransistoren
- De oppervlaktemorfologieën en eigenschappen van ZnO-films afstemmen door het ontwerp van grensvlakken
- Tribologische prestaties van gelaagde zirkoniumfosfaat-nanoplaatjes in olie afstemmen op oppervlakte- en tussenlaagmodificaties
- Synthese van ZnO-nanokristallen en toepassing in omgekeerde polymeerzonnecellen
- Lasing en transporteigenschappen van poly[(9,9-dioctyl-2,7-divinyleenfluorenyleen)-alt-co-(2-methoxy- 5-(2-ethylhexyloxy)-1,4-fenyleen)] (POFP) voor de toepassing van diode-gepompte organische vaste l…
- De koppelingseffecten van oppervlakteplasmonpolaritons en magnetische dipoolresonanties in metamaterialen
- Gecontroleerde synthese van BaYF5:Er3+, Yb3+ met verschillende morfologie voor de verbetering van upconversie-luminescentie



