Zeer efficiënte synthese van op koolstof gebaseerde molybdeenfosfide-nanodeeltjes voor elektrokatalytische waterstofevolutie
Abstract
Molybdeenfosfide in overgangsmetaalfosfidenleden worden beschouwd als een aantrekkelijke elektrokatalysator voor waterstofevolutiereactie (HER). De onbevredigende stabiliteit en geleidbaarheid in een alkalische omgeving heeft de ontwikkeling echter gehinderd. Hier hebben we met succes N, C co-gedoteerde MoP (MoP-NC) nanodeeltjes geïntroduceerd door een eenvoudige en efficiënte tweestapssynthesemethode met ureum als koolstofbron in het molybdeenfosfidesysteem. De lage prijs van ureum en de uitstekende koolstof-stikstofverhouding nemen de obstakels weg voor de ontwikkeling van MoP-NC-composieten. De verkregen composieten hebben uitstekende HER-elektrokatalytische activiteit en stabiliteit in 1-M kaliumhydroxide (KOH) -oplossing, waarvoor slechts een overpotentiaal van 131 mV nodig is om een stroomdichtheid van 10 mA cm −2 te bereiken en vertoont een verwaarloosbare prestatievermindering na 1000 CV-cycli.
Achtergrond
De snelle ontwikkeling van de mens heeft de afgelopen jaren geleid tot een geleidelijke uitputting van fossiele energie [1,2,3]. Daarom streven onderzoekers naar een milieuvriendelijke energiebron om deze vicieuze cirkel te beteugelen, zodat waterstof op de troon van energie kan worden gehouden. Traditionele fotolyse en elektrolyse van water om waterstof te produceren, vormen echter een moeilijk knelpunt in termen van efficiëntie. Terwijl mensen met de introductie van hoogrenderende geëlektrolyseerde watergekatalyseerde waterstofproductiekatalysatoren een kwalitatieve sprong hebben gemaakt in de massaproductie van waterstof. Dit katalysator-gemedieerde elektrokatalytische proces vereist dat de katalysator zelf een overpotentiaal heeft met een lage waterstofontwikkelingsreactie (HER). Hoewel de edele metalen zoals Pt in dit stadium een extreem lage overpotentiaal en uitstekende stabiliteit hebben, zijn ze duur [4,5,6]. De schaarste aan beschikbare grond beperkt de grootschalige toepassing van dergelijke katalysatoren [7,8,9]. Daarom is het vinden van een materiaal met lage kosten en relatief goede elektrokatalytische waterstofontwikkelingsprestaties de afgelopen jaren een hot spot geweest [10,11,12,13].
Het is vermeldenswaard dat recentelijk onderzoekers hebben ontdekt dat sommige niet-edelmetaalkatalysatoren een goede prijs/prestatieverhouding hebben in de richting van waterstofontwikkeling, waaronder het meest gebruikte Molybdeenfosfide (MoP) in overgangsmetaalfosfiden (TMP's) [14 ,15,16,17]. Zon et al. gemengd (NH4 )6 Ma7 O24 ·4H2 O, (NH4 )2 HPO4 en citroenzuur (CA) in verschillende molaire verhoudingen, wanneer Mo:P:CA =1:1:x en x =2, de vorming van verknoopte netwerkstructuur MoP-nanodeeltjes hebben de beste HER-prestaties [18]. Jozua et al. bereide amorfe MoP-nanodeeltjes met goede HER-eigenschappen door hexacarbonylmolybdeen en trioctylfosfine (TOP) [19] te verhitten. De geleidbaarheid van puur molybdeenfosfide is echter niet bevredigend, en de waterstofontwikkelingsprestaties en stabiliteit in een alkalische oplossing zijn niet zo goed als in een zure omgeving, zodat de geleidbaarheid en stabiliteit kunnen worden verbeterd door een op koolstof gebaseerd materiaal te introduceren [ 20,21,22].
We bereikten een zeer efficiënte tweestapssynthese door ureum als koolstofbron in het molybdeenfosfidesysteem te introduceren, en hebben met succes N,C co-gedoteerde MoP (MoP-NC) nanodeeltjes bereid, die een uitstekende katalytische activiteit en stabiliteit hebben, zelfs in alkalische elektrolyten . Daarnaast hebben we twee controlegroepen ontworpen die de werking van ureum onderzochten, inclusief geen koolstofbron en glucose in plaats van ureum als koolstofbron. Interessant is dat de eerste altijd zwakker is dan de laatste wanneer respectievelijk glucose en ureum als koolstofbronnen worden gebruikt. Dit kan worden toegeschreven aan de rol van ureum als zowel koolstofbron als stikstofbron voor de hulpsynthese van molybdeenfosfide [23].
Presentatie van de hypothese
Molybdeenfosfide wordt veel gebruikt als niet-edelmetaalkatalysator in de richting van waterstofontwikkeling. De introductie van een koolstofbron kan de geleidbaarheid en stabiliteit van de elektrokatalysator verbeteren. De introductie van een stikstofbron kan de waterstofontwikkelingsprestaties in een alkalische oplossing verbeteren.
De hypothese testen
Materialen
Ureum (CH4 N2 O), glucose (C6 H12 O6 ), ammoniumdiwaterstoffosfaat (NH4 H2 PO4 ), en ammoniumheptamolybdaat ((NH4 )6 Ma7 O24 ·4H2 O) werden gekocht bij Sinopharm Chemical Reagent Co., Ltd. KOH werd gekocht bij Aladdin Ltd. in Shanghai. Gedeïoniseerd water dat in het experiment werd gebruikt, was afkomstig van ultrapuur waterapparatuur.
Voorbereiding van monsters
In de typische synthese van MoP-NC, (NH4)6 Ma7 O24 ·4H2 O (0,240 g), NH4 H2 PO4 (0,167 g), en CO(NH2 )2 (2.000 g) werden opgelost in 50 m gedeïoniseerd water en onderworpen aan 15 min ultrasoonapparaat. Daarna werd de resulterende oplossing verwarmd tot 80°C en 90 min magnetisch geroerd, bleef gedurende de reactie relatief gesloten en werd vervolgens gedroogd in een vriesdroger. Het verkregen witte voorloperpoeder werd verwarmd van kamertemperatuur tot 900°C met een snelheid van 5°C/min onder een N2 atmosfeer gedurende 120 min. Om de invloed van koolstofbron op materiaalsynthese te onderzoeken, werd MoP-C bereid door glucose in plaats van ureum als koolstofbron te gebruiken. Wanneer er geen koolstofbron of fosforbron werd toegevoegd, werden respectievelijk Bulk-MoP en Mo-NC bereid.
Karakteriseringen
De informatie over röntgendiffractie (XRD) is verzameld op een röntgendiffractie (XRD, Bruker D8-Advance-diffractometer met Cu K-straling (λ =1,54056 Å)). De microstructuur van het monster werd verkregen door een veldemissie scanning elektronenmicroscopie (FE-SEM, S-4800, Hitachi, Japan). De TEM-afbeeldingen werden uitgevoerd op een transmissie-elektronenmicroscopie (TEM, JEM-2100, JEOL, Japan). De chemische componenten werden geanalyseerd met een röntgenfoto-elektronspectroscopie (XPS) met Mg Kα als monochromatische röntgenbron.
Elektrochemische test
Alle elektrochemische metingen werden uitgevoerd op een elektrochemisch werkstation (CHI 660E Chenhua, Shanghai) uitgerust met een conventioneel systeem met drie elektroden van Pine Modulated Speed Rotator (PINE, VS). De Pt-draad en de verzadigde calomelelektrode (SCE) kwamen overeen met respectievelijk de tegenelektrode en de referentie-elektrode, en de glasachtige koolstofelektrode en het roterende schijfapparaat waren verbonden als een werkelektrode. Bovendien werd 1 M KOH-elektrolyt verstrekt voor testen. De werkelektrode werd als volgt bereid:Eerst werd 5 mg van de katalysator opgelost in een oplossing gemengd met 350 L isopropanol, 650 μL gedeïoniseerd water en 50 L 5 wt% Nafion. Vervolgens werd, nadat de bovengenoemde gemengde oplossing gedurende 30 min met ultrasone trillingen was behandeld, een uniform gedispergeerde inkt verkregen. Ten slotte werd 10 L van de inkt op een glasachtige koolstofelektrode (diameter, 5 mm) gedruppeld voor natuurlijke luchtdroging, waarbij de katalysator een oppervlaktedichtheid had van 0,485 mg cm −2 . Om de prestatieparameters van het monster beter te beschrijven, gebruikten we ter vergelijking een Pt/C-katalysator (20 wt%) en het voorbereidingsproces was hetzelfde als dat van de bovenstaande werkelektrode. Een zwaaisnelheid van 10 mV s −1 werd gebruikt voor metingen van lineaire sweep-voltammetrie (LSV). Tafel werd verkregen door de juiste regiocurve aan te passen volgens de Tafel-vergelijking, en de elektrochemische stabiliteit werd verkregen door 1000 cycli uit te voeren met de zwaaisnelheid van 100 mV·S −1 . De dubbellaagse capaciteit (C dl ) gegevens zijn afgeleid van cyclische voltammetrie (CV), die wordt uitgevoerd bij hetzelfde spanningsbereik (0,847-0,947 V versus RHE) bij verschillende scansnelheidsbereiken (20-200 mV). Elektrochemische impedantiespectroscopie (EIS) metingen werden gedaan bij een constante potentiaalamplitude van 10 mV over het standaard frequentiebereik (1–10 5 Hz).
Implicaties van de hypothese
Figuur la liet zien dat het XRD-patroon van MoP-NC diffractiepieken vertoont op 27,95, 32,17, 43,15, 57,48, 57,95, 64,93, 67,03, 67,86 en 74,33, overeenkomend met de negen verschillende kristalvlakken van MoP. SEM-afbeeldingen van MoP-NC vertoonden amorfe microstructuren van kleine deeltjes (figuur 1b). De deeltjes verzamelden zich om kleine clusters te vormen, maar er was nog steeds een bepaalde opening tussen de clusters. Deze kleine en dichte structuur zorgde ervoor dat MoP-NC beide een aanzienlijke katalytische activiteit en een goede stabiliteit hebben (figuur 1c). Het is te zien aan TEM en TEM met hoge resolutie (HRTEM) (Fig. 1d, e) dat deze nanodeeltjes duidelijke roosterranden vertoonden, zoals roosterranden van het (100) vlak met een steek van 0, 28 nm. Bovendien waren buiten deze goed gedefinieerde roosterrandgebieden MoP-NC-nanodeeltjesranden, die de opname van MoP-NC-nanodeeltjes in de koolstofmatrix sterk ondersteunden. De overeenkomstige afbeelding van EDS-elementtoewijzing (Fig. 1f-i) verifieerde verder de uniforme verdeling van de vier elementen in het product MoP-NC.

een XRD-patronen voor MoP. b , c SEM-afbeeldingen van MoP-NC. d , e TEM- en HRTEM-beelden van MoP-NC. v –ik overeenkomstige EDS elementaire afbeeldingsafbeeldingen van Mo, P, C en N
Om de elementaire distributie van MoP-NC beter te begrijpen, werd XPS gekarakteriseerd. In het Mo 3d-spectrale gebied bevat Mo twee toestanden van Mo 3+ en Mo 6+ (Fig. 2a). De aanwezigheid van Mo 3d3/2 en Mo 3d5/2 in de Mo 3+ toestand leidde tot microvibratiepieken bij 231,5 en 228,2 ev, terwijl de pieken van 235,5 en 232,4 ev werden toegeschreven aan Mo 3d3/2 en Mo 3d5/2 in de Mo 6+ toestand, omdat het oppervlak van het MoP-NC-materiaal onvermijdelijk in de lucht werd geoxideerd [24, 25]. In het P 2p-gebied (Fig. 2b) werden microvibratiepieken van 130,7 en 129,4 eV toegewezen aan P 2p1/2 en P 2p3/2 , respectievelijk, onthullende de aanwezigheid van P 3− [26]. De piek bij 133,9 eV kan worden toegeschreven aan PO4 3− [27]. In het C 1s XPS-spectrum (Fig. 2c) waren de belangrijkste pieken die overeenkomen met de drie chemische bindingen respectievelijk 228,7 eV (OC=O), 284,8 eV (CN/C=C) en 286,3 eV (CC). ]. Het verschijnen van C-N/C=N suggereerde dat sommige koolstofatomen in MoP-NC werden vervangen door stikstofatomen om N-gedoteerde koolstof te vormen. In het spectrum van N1s (Fig. 2d), kunnen drie verschillende stikstofomgevingen worden opgelost vanuit dit gebied, waarbij de pieken van 398,4 en 402,1 eV met grotere bindingsenergieën overeenkwamen met de grote hoeveelheden pyridinium en de kleine hoeveelheid quaternaire stikstof, respectievelijk. Bovendien werd een piek bij 394,5 eV aangeduid als een combinatie van N en Mo 3p [29].
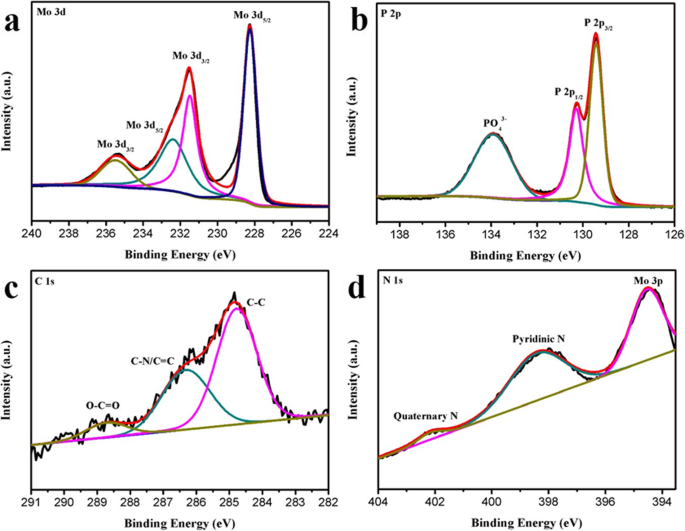
XPS-spectra van (a) Mo 3d, (b) P 2p, (c ) C 1s, en (d ) N 1s-regio's
De elektrokatalytische HER-activiteit van MoP-NC in 1 M KOH (pH =14) gebruikte een typisch systeem met drie elektroden met een zwaaisnelheid van 10 mV s −1 . Omdat de eigenschappen van de bereide materialen vergelijkende analyse vereisten, werden ook Mo-NC, Bulk-MoP en MoP-C bestudeerd. Figuur 3a toont LSV-curven. De toevoeging van Pt/C en een blanco glasachtige koolstofelektrode (Blank) zorgde ervoor dat de hele curven er meer hiërarchisch uitzagen. De overpotentiaal van MoP-NC bij een stroomdichtheid van 10 mA cm −2 vereist slechts 131 mV, wat aanzienlijk beter was dan die van Mo-NC en Bulk-MoP. Bovendien werden de LSV-prestaties van MoP-C bereid uit glucose in plaats van ureum als koolstofbron ook overschaduwd door MoP-NC. Het is vermeldenswaard dat in vergelijking met HER in een zure oplossing, de snelheid van H-ionenproductie tijdens de ontleding van HER-water in de alkalische laag langzamer was (ongeveer 2-3 ordes van grootte lager dan zure activiteit) en een grotere uitdaging had [30] ,31,32]. Figuur 3b toonde de aangepaste Tafel-grafiekvergelijking:η = een + b log j , waar b is de Tafelhelling en j is de stroomdichtheid [33]. De Tafelhelling van Pt/C is 58 mV dec −1 , vergeleken met Mo-NC (121 mV dec −1 ), Bulk-MoP (135 mV dec −1 ), en MoP-C (75 mV dec −1 ), had MoP-NC een lagere parameter van slechts 66 mV dec −1 , wat aangeeft dat de HER-katalytische kinetiek voor de MoP-NC-elektrode sneller was. Tegelijkertijd ontdekten we dat de MoP-NC in dit werk behoorlijk concurrerend was met de HER-prestaties van de eerder gerapporteerde op MoP gebaseerde composiet / koolstofelektrokatalysator (tabel 1). Zoals te zien is in tabel 1, waren de meeste op MoP gebaseerde materialen gebaseerd op zure omstandigheden en werden ze zelden getest onder alkalische omstandigheden [17,18,19, 22,23,24, 34,35,36,37]. Bovendien waren sommige ervan getest in zowel zure als alkalische omgevingen [38,39,40,41]. Alleen amorfe koolstof-gecoate MoP-materialen in deze materialen presteerden echter beter in alkalische omgevingen dan in zure omgevingen. De reden waarom MoP-NC in ons werk goede HER-prestaties kan bereiken in een alkalische omgeving, was omdat ureum werd gebruikt als zowel een koolstofbron als een stikstofbron in het syntheseproces, waarbij het ook wat gas ontleedde. Het vertraagde de polymerisatie van met N en C gedoteerd MoP, dat een uitstekende ondersteunende syntheserol speelde. De stabiliteit van de voorbereide materialen was continu CV met een scansnelheid van 100 mV s −1 . Na 1000 cycli had de LSV-curve een klein verlies aan stroomdichtheid in vergelijking met de initiële waarde (figuur 3c). Figuur 3d toonde de CV-plots van MoP-NC, die werd uitgevoerd bij hetzelfde spanningsbereik (0,847-0,947 V versus RHE) bij verschillende scansnelheidsbereiken (20-200 mV). Om de dubbellaagse capaciteit (C dl ) van het materiaal, de C dl van een reeks controlegroepen werd getoond in Fig. 3e. De C dl van Mo-NC, Bulk-MoP en MoP-C waren 0,8 mF cm −2 , 60 μF cm −2 en 1,6 mF cm −2 , respectievelijk, terwijl de C dl van MoP-NC was 10,9 mF cm −2 die veel groter was dan de bovengenoemde materialen. De suggestie gaf aan dat MoP-NC een hoger actief oppervlak had. Verder werd de geleidbaarheid van MoP-NC geëvalueerd door middel van elektrochemische impedantiespectroscopie (EIS). Figuur 3f toonde het Nyquist-diagram van de verschillende katalysatoren. De weerstand tegen ladingsoverdracht van de MoP-NC-katalysator was lager dan die van andere katalysatoren, wat betekende dat de snellere elektronenoverdrachtsverhouding van de MoP-NC-katalysator na N, C-co-doping de elektrokatalytische prestaties van HER verder verbeterde.
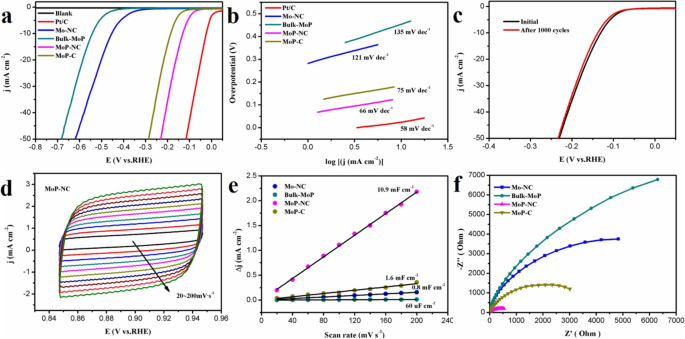
een LSV-curven met scansnelheid van 10 mV s −1 bij kamertemperatuur in 1 M KOH. b Tafelplots van de gesynthetiseerde monsters. c Stabiliteit van MoP-NC na 1000 cycli voltammetrie (CV) cyclus. d CV-plots van MoP-NC met een scansnelheid tussen 20 en 200 mV s −1 . e Dubbellaags condensator (C dl ) van Mo-NC, Bulk-MoP, MoP-NC en MoP-C met een condensatorstroom van 0,1 V. f De EIS-spectra van Mo-NC, Bulk-MoP, MoP-NC en MoP-C
Conclusies
Samenvattend hebben we de amorfe kleine deeltjes van MoP-NC gesynthetiseerd door een eenvoudige en efficiënte tweestapsmethode. Omdat de MoP-nanodeeltjes waren gecoat met koolstof, aggregeerden ze gedeeltelijk samen. Gelukkig verslechtert deze structuur de prestaties van het materiaal zelf niet, maar draagt ze ook bij aan de stabiliteit ervan. Deze algehele dispersie, lokaal geaggregeerd materiaal met kleine deeltjes bereikte een stroomdichtheid van 10 mA cm −2 in 1 M KOH die slechts een overpotentiaal van 131 mV vereist, wat superieur is aan de gerapporteerde HER-prestaties van een enkel molybdeenfosfidemateriaal in een alkalische omgeving. Bovendien vertoonde het materiaal een verwaarloosbare prestatievermindering, zelfs na het scannen van 1000 CV-cycli. Onze resultaten laten zien dat met koolstof gecoate MoP ook de alkalische omgeving kan overwinnen om uitstekende HER-elektrokatalytische activiteit en stabiliteit te bereiken.
Beschikbaarheid van gegevens en materialen
Alle gegevens zijn onbeperkt beschikbaar.
Afkortingen
- CA:
-
Citroenzuur
- C dl :
-
De dubbellaagse capaciteit
- CV:
-
Cyclische voltammetrie
- EIS:
-
Elektrochemische impedantiespectroscopie
- HAAR:
-
Reactie waterstofontwikkeling
- HRTEM:
-
Overgangselektronenmicroscopie met hoge resolutie
- KOH:
-
Kaliumhydroxide
- LSV:
-
Lineaire sweep-voltammetrie
- MoP:
-
Molybdeenfosfide
- MoP-NC:
-
N, C co-gedoteerde MoP
- SCE:
-
Verzadigde calomelelektrode
- SEM:
-
Scanning elektronenmicroscopie
- TEM:
-
Overgang elektronenmicroscopie
- TMP's:
-
Overgangsmetaalfosfiden
- TOP:
-
Trioctylfosfine
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- XRD:
-
Röntgenpoederdiffractie
Nanomaterialen
- Zeer efficiënt zuiveringsmiddel voor het blaasvormen van polyolefinen
- MoS2 met gecontroleerde dikte voor elektrokatalytische waterstofevolutie
- S, N co-gedoteerde grafeen Quantum Dot/TiO2-composieten voor efficiënte fotokatalytische waterstofgeneratie
- Eenvoudige synthese van SiO2@C-nanodeeltjes verankerd op MWNT als hoogwaardige anodematerialen voor Li-ionbatterijen
- One-Pot Green-synthese van met Ag versierde SnO2-microsfeer:een efficiënte en herbruikbare katalysator voor reductie van 4-nitrofenol
- Silica-nanodeeltjes voor intracellulaire eiwitafgifte:een nieuwe synthesebenadering met behulp van groene fluorescerende eiwitten
- Nabehandelingsmethode voor de synthese van monodisperse binaire FePt-Fe3O4-nanodeeltjes
- Verkenning van Zr–Metal–Organic Framework als efficiënte fotokatalysator voor waterstofproductie
- Hiërarchische heterostructuur van ZnO@TiO2 holle bollen voor zeer efficiënte fotokatalytische waterstofevolutie
- Op trifenylfosfine gebaseerd functioneel poreus polymeer als een efficiënte heterogene katalysator voor de synthese van cyclische carbonaten uit CO2
- Synthese en in vitro prestaties van met polypyrrool gecoate ijzer-platina nanodeeltjes voor fotothermische therapie en foto-akoestische beeldvorming



