Staaf-achtige nanoporeuze CeO2 gemodificeerd door PdO-nanodeeltjes voor CO-oxidatie en methaanverbranding met hoge katalytische activiteit en waterbestendigheid
Abstract
Een PdO/CeO2 composiet met een staafachtige nanoporeuze skeletstructuur werd bereid door de dealloying van Al-Ce-Pd-legeringslinten te combineren met calcineren. Voor CO-oxidatie en CH4 verbranding, de nanoporeuze PdO/CeO2 composiet vertoont uitstekende katalytische activiteit en de volledige reactietemperaturen van CO en CH4 zijn respectievelijk 80 °C en 380 °C. Bovendien bezit het composiet een uitstekende cyclusstabiliteit, CO2 toxiciteit en waterbestendigheid, en de katalytische activiteit neemt nauwelijks af na 100 h langdurige stabiliteitstests in de aanwezigheid van waterdamp (2 × 10 5 p.p.m.). De resultaten van een reeks karakteriseringen geven aan dat de verhoogde katalytische activiteit kan worden toegeschreven aan de goede dispersie van de PdO-nanodeeltjes, groot specifiek oppervlak, sterke redoxcapaciteit, interactie tussen PdO en CeO2 , en meer oppervlakte-actieve zuurstof op PdO. De resultaten van de karakterisering en experimenten geven ook aan dat de PdO-nanodeeltjes, bereid door dealloying en calcinering te combineren, een sterkere katalytische activiteit hebben dan Pd-nanodeeltjes. Ten slotte wordt een eenvoudig model gebruikt om het katalytische mechanisme van de PdO/CeO2 samen te vatten. composiet. Gehoopt wordt dat dit werk inzicht zal verschaffen in de ontwikkeling van hoogactieve katalysatoren.
Achtergrond
Op dit moment besteden steeds meer mensen aandacht aan milieukwesties en richten zij zich op het verminderen van verschillende belangrijke milieukwesties, zoals uitlaatemissies en het broeikaseffect [1, 2]. In het bijzonder de eliminatie van giftige CO en het broeikasgas CH4 is de focus van een overvloed aan onderzoek. Onder dergelijke onderzoeken is katalyse bij lage temperatuur een effectieve manier gebleken om deze vervuilende gassen te elimineren [3,4,5,6].
Hoewel veel onderzoeken hebben aangetoond dat goedkope metalen en hun metaaloxiden (bijv. overgangsmetalen en -oxiden, en zeldzame aardmetalen en -oxiden) kunnen worden gebruikt als katalysatoren voor CO-oxidatie en CH4 verbranding, valt niet te ontkennen dat het gebruik van edele metalen de katalytische prestatie doorgaans aanzienlijk verbetert [7, 8]. In de afgelopen jaren zijn Pd- en PdO-katalysatoren uitgebreid bestudeerd en worden ze beschouwd als enkele van de meest effectieve katalysatoren voor CO-oxidatie en CH4 verbranding. Ze vertonen niet alleen een lage vluchtigheid bij hoge temperaturen, maar ook een hoge katalytische activiteit bij lage temperaturen [9, 10].
Echter, vanuit een toepassingsoogpunt, aangezien de overvloed aan edele metalen in de aarde relatief laag is, worden de Pd- en PdO-katalysatoren die over het algemeen in praktische industriële toepassingen worden gebruikt, geladen op dragers zoals metaaloxiden, zeolieten, koolstofmaterialen en metaal-organische raamwerken. Deze configuratie is ook in lijn met de trend om duurzame katalyse te ontwikkelen door edele metalen te behouden en de interactie tussen drager en edelmetaal te gebruiken om de katalytische activiteit te verbeteren [11, 12]. Onder de soorten steunen, CeO2 wordt beschouwd als een veelbelovende ondersteuning vanwege zijn sterke zuurstofopslag/afgifte-eigenschappen en uitstekende thermische stabiliteit. MacLachlan et al. gebruikte een combinatie van impregnatie met beginnende vochtigheid en oppervlakteondersteunde reductie om een nanogestructureerde PdO/CeO2 te bereiden composiet, dat na calcinering een goede activiteit vertoonde als katalysator voor methaanverbranding [13]. Luo et al. meldde de voorbereiding van een PdO-CeO2 katalysator door een verbrandingsmethode in oplossing en bewezen dat de synergetische effecten van PdO en CeO2 zijn de reden voor de verhoogde katalytische activiteit [14].
Hoewel er veel goede resultaten zijn behaald, zijn er nog enkele uitdagingen. Veel organische chemicaliën of oppervlakteactieve stoffen kunnen bijvoorbeeld de nanomaterialen verontreinigen, wat resulteert in een onvoldoende katalytische activiteit, wat gebruikelijk is bij natte chemie [15]. Bovendien is het proces om een katalysator te bereiden op basis van de methode van veroudering van vloeibare precursoren gecompliceerd en is de opbrengst laag [16]. Daarom blijft de ontwikkeling van niet-vervuilende materialen met een hoog rendement en een hoge katalytische activiteit een uitdaging.
In dit werk hebben we een methode ontwikkeld voor de bereiding van PdO/CeO2 composieten door Al-Ce-Pd-legeringslinten te ontbinden en vervolgens te calcineren. De bereidingswijze is eenvoudig, de structuur van het materiaal is goed te controleren en er zijn geen organische reagentia nodig [17, 18], wat bijzonder geschikt is voor grootschalige industriële productie en een duurzame toekomst [19, 20]. Voor zover wij weten, zijn er echter geen literatuurrapporten over het gebruik van dealloying om de katalysatoren voor de verbranding van methaan te bereiden. Daarom is het te hopen dat dit werk inzicht kan geven in en kan helpen bij de synthese en bereiding van nanomaterialen.
Methoden
Materialen
Alle chemicaliën en metalen werden gebruikt zoals ontvangen van analytische kwaliteit zonder verdere zuivering. Zuiver Al (99,90 wt%), zuiver Ce (99,90 wt%) en zuiver Pd (99,90 wt%) waren van Sino-Platinum Metals Co., Ltd. Granulair NaOH (AR) was van Shanghai Aladdin Biochemical Technology Co., Ltd Argon van hoge zuiverheid was van Xi'an Jiahe Co., Ltd.
Synthese van PdO/CeO2 Composiet
Al92−X Ce8 PdX (X =0, 0,1, 0,3, 0,5, 0,7, 0,9 en 1,1) voorloperlegeringen werden bereid door het boogsmelten van zuiver Al, zuiver Ce en zuiver Pd onder een argonatmosfeer. Een verkregen Al-Ce-Pd-precursorlegering werd opnieuw gesmolten door middel van hoogfrequente inductieverhitting in een kwartsbuis onder argonbescherming. De gesmolten legering werd met argon op een met hoge snelheid roterende koperrol geblazen voor snelle stolling, en een Al-Ce-Pd-legeringslint met een breedte van ongeveer 3 tot 4 mm en een dikte van ongeveer 20 tot 30 m werd verkregen.
Het geprepareerde lint van Al-Ce-Pd-legering werd in een 20 gew.% natriumhydroxide-oplossing geplaatst en gedurende 2 uur bij omgevingstemperatuur gedeloyeerd en vervolgens tot 80 ° C verwarmd en gedurende 10 uur gedeloyeerd. Het gedeloyeerde monster werd herhaaldelijk gespoeld met gedeïoniseerd water en bij kamertemperatuur aan de lucht gedroogd. Het gedroogde monster werd gecalcineerd in O2 bij 200~600 °C gedurende 2 h, en de stroomsnelheid van O2 is 18 mL min −1 . De bereidingsmethode en structurele evolutie van de PdO/CeO2 composiet worden getoond in Fig. 1.
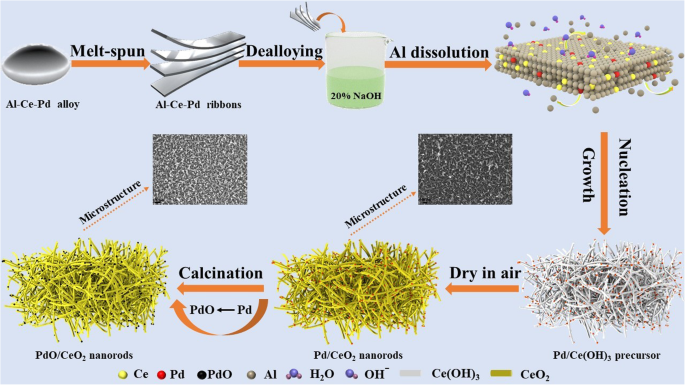
Schema voor de bereiding van de staafachtige nanoporeuze PdO/CeO2 composiet
Voorbeeldkarakterisering
Röntgendiffractie (XRD) patronen werden verkregen met behulp van een Shimadzu XRD-6100 diffractometer met Cu Ka-straling (20 kV en 40 mA). De morfologie en elementaire samenstelling van de monsters werden verkregen met een JSM-7000F scanning-elektronenmicroscoop (SEM) en een INCA X-Sight Oxford energiedispersieve spectrometer (EDS). Transmissie-elektronenmicroscoop (TEM) beelden, hoge resolutie transmissie-elektronenmicroscoop (HRTEM) beelden en scanning transmissie-elektronenmicroscopiebeelden gekoppeld aan energie-dispersieve röntgenspectra (STEM-EDX) werden opgenomen op een JEOL JEM-200 elektronenmicroscoop. Het specifieke oppervlak (S BET ), poriegrootte (D p ), en porievolume (V p ) van de monsters werden bepaald met een Micromeritics ASAP 2020-apparaat bij 77,4 K. De analyse met röntgenfoto-elektronspectroscopie (XPS) werd uitgevoerd met een multifunctionele spectrometermodel Axis Ultra Kratos. Waterstof temperatuurgeprogrammeerde verlaging (H2 -TPR) werd uitgevoerd op een Quantachrome Autosorb-iQC-TPX, waarin een monster van 50 mg werd verwarmd van 50 tot 800 °C met een hellingssnelheid van 10 °C/min in 10 vol% H2 /Ar menggas stroomt met een snelheid van 40 mL min −1 .
Katalysatortesten
De katalytische activiteit van de monsters werd geëvalueerd door CO-oxidatie en CH4 verbranding. De katalysator (100 mg) werd in een roestvrijstalen buisreactor geladen en de reactor werd in een buisoven geplaatst met nauwkeurige temperatuurregeling. Een voedingsgas bestaande uit ofwel 1 vol% CO, 10 vol% O2 , en 89 vol% N2 of 1 vol% CH4 , 10 vol% O2 , en 89 vol% N2 werd in de reactor gebracht met een totale stroomsnelheid van 50 mL min −1 (ruimtesnelheid =30000 h −1 ), en de stroomsnelheid van het reactiegas werd geregeld en aangepast door een massastroommeter (Brooks 5850E). Details over de bereiding van het voedingsgas met 20 vol% H2 O worden weergegeven in het aanvullende bestand 1:figuur S1. De CO en CH4 concentraties tijdens het verwarmingsproces werden in-line geanalyseerd door een Agilent GC-7890B gaschromatograaf uitgerust met een vlamionisatiedetector (FID). De conversie van CO en CH4 werd berekend volgens Vgl. (1):
$$ X=\frac{C_{\mathrm{in}}-{C}_{\mathrm{out}}}{C_{\mathrm{in}}}\times 100\% $$ (1)waar X staat voor de conversie van CO of CH4 , C in vertegenwoordigt de inlaatconcentratie van CO of CH4 , en C uit vertegenwoordigt de uitlaatconcentratie van CO of CH4 .
De reactiesnelheden van CO en CH4 werden berekend met behulp van Vgl. (2) [14, 21]:
$$ {r}_{\mathrm{CO}/{\mathrm{CH}}_4}=\frac{C_{\mathrm{CO}/{\mathrm{CH}}_4}\cdot {X}_{ \mathrm{CO}/{\mathrm{CH}}_4}\cdot P\cdot V}{m_{\mathrm{cat}}\cdot {W}_{\mathrm{Pd}}\cdot R\cdot T }\left(\mathrm{mol}\cdot {\mathrm{s}}^{-1}\cdot {\mathrm{g}}_{\mathrm{Pd}}^{-1}\right) $$ (2)waar r CO/CH4 staat voor de reactiesnelheid van CO of CH4; de concentratie van CO of CH4 wordt uitgedrukt als C CO/CH4 in het voedingsgas; de conversie van CO of CH4 wordt uitgedrukt als X CO/CH4; P is de atmosferische druk, die 101,3 KPa is; V is het totale debiet; m kat is de massa van de katalysator in de reactor; W Pd is het laden van Pd; R is de molaire gasconstante, die 8,314 Pa m 3 . is mol −1 K −1 ; en T is de omgevingstemperatuur (293 K).
Resultaten en discussie
Katalysatorkarakterisering
De XRD-spectra van de monsters worden getoond in Fig. 2. Een duidelijke reeks diffractiepieken voor CeO2 (JCPDS NO. 34-0394) werd gedetecteerd, zoals getoond in Fig. 2a, maar de diffractiepieken geassocieerd met Pd werden niet gedetecteerd in alle gedeloyeerde monsters die waren gecalcineerd bij 400 ° C. De dealloyed Al91,3 Ce8 Pd0.7 legering werd bij verschillende temperaturen gecalcineerd, zoals weergegeven in figuur 2b. Naarmate de temperatuur geleidelijk toenam, werden de diffractiepieken van CeO2 werd geleidelijk scherp en smal; zelfs na een calcinering van 800 ° C konden de diffractiepieken die verband houden met Pd echter niet worden gedetecteerd. Dit resultaat kan te wijten zijn aan de relatief lage concentratie van Pd in het monster, dat sterk gedispergeerd kan zijn in het monster in de vorm van ofwel een amorfe fase of kleine kristallijne korrels. Er werden geen diffractiepieken geassocieerd met Al waargenomen in de XRD-spectra voor geen van de monsters, wat aangeeft dat het resterende Al-gehalte in de monsters na deloying ofwel erg laag was of dat Al in een amorfe vorm in de monsters aanwezig was.
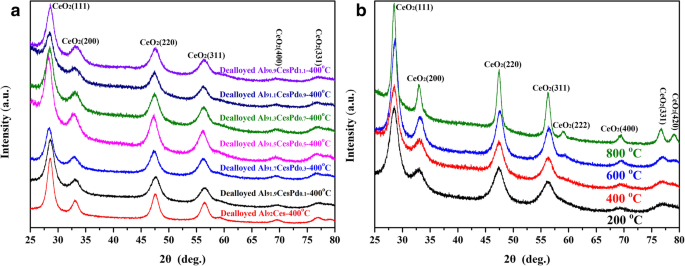
XRD-patronen van Al92−X Ce8 PdX (X =0,1, 0,3, 0,5, 0,7, 0,9 en 1,1) gedelegeerd bij 400 °C (a ) en de XRD-patronen van gedeloyeerd Al91,3 Ce8 Pd0.7 legeringen gecalcineerd bij verschillende temperaturen (b )
De EDS-resultaten en microstructuren van de gedeloyeerde Al91,3 Ce8 Pd0.7 gecalcineerd bij 400 °C worden getoond in Fig. 3. Na deloying was de inhoud van Ce en Pd in het monster zeer dicht bij die in de precursorlegering, zoals getoond in Fig. 3a, wat aangeeft dat het verlies van Ce en Pd was klein tijdens het dealloying-proces. Het resterende Al in het gedeloyeerde Al91,3 Ce8 Pd0.7 legering gecalcineerd bij 400 ° C was erg laag, slechts 2,73%, wat consistent is met de XRD-resultaten. Figuren 3b en c tonen de oppervlakte-SEM-afbeeldingen van het monster, en het monster vertoont een uniforme, ongeordende, geweven poreuze structuur die is samengesteld uit talrijke nanostaafjes met een diameter van ongeveer 10 nm; de nanostaafjes worden op elkaar gestapeld om verschillende microporiën en mesoporiën te vormen. Een dwarsdoorsnede-SEM-beeld van het monster wordt getoond in Fig. 3d, en de nanostaafjes zijn met elkaar verbonden om een driedimensionale skeletstructuur te vormen die de stabilisatie van de nanodeeltjes door een groot contactgebied vergemakkelijkt, wat resulteert in meer interactief op nanoschaal. interfaces.
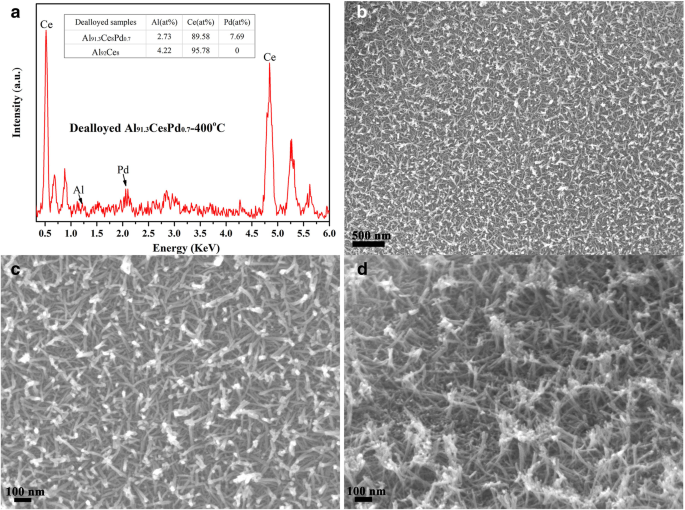
EDS-patroon (a ), oppervlakte-SEM-afbeeldingen (b , c ), en transversaal SEM-beeld (d ) van de toegewezen Al91,3 Ce8 Pd0.7 legering gecalcineerd bij 400 °C
TEM-afbeeldingen en TEM-EDX-mapping werden verder gebruikt om de structuren en deeltjesverdeling van het monster te karakteriseren, zoals weergegeven in Fig. 4. De gedeloyeerde Al91,3 Ce8 Pd0.7 gecalcineerd bij 400 ° C bestaat uit talrijke nanostaafjes, zoals weergegeven in Fig. 4a, en de nanostaafjes zijn op elkaar gestapeld om vele microporiën en mesoporiën te vormen, wat consistent is met de SEM-resultaten. Er zijn verschillende donkerdere deeltjes verdeeld over het oppervlak van de nanostaafjes, zoals weergegeven in de rode vakken in figuur 4a. Figuur 4b toont het HRTEM-beeld van het monster. De roosterafstandwaarden van de nanostaafjes zijn ongeveer 0,314 nm en 0,193 nm, wat overeenkomt met de (111) en (220) vlakken van CeO2 , respectievelijk. Het rode kader in Fig. 4b is het HRTEM-beeld van de donkere deeltjes die te zien zijn in Fig. 4a, die een diameter hebben van ongeveer 5 nm en zijn verdeeld over het oppervlak van de CeO2 nanostaafjes. De roosterafstand van de donkere deeltjes (0,201 nm) is echter vergelijkbaar met die van het (220) vlak van CeO2 (0,193 nm) en is moeilijk te onderscheiden. De karakterisering van de TEM-EDX-kartering werd uitgevoerd om deze deeltjes te identificeren. Zoals getoond in Fig. 4c en d, de deeltjes verdeeld over de CeO2 nanostaafjes zijn gerelateerd aan Pd, en rekening houdend met de roosterafstandwaarde van 0,201 nm, wordt vastgesteld dat de donkere deeltjes PdO-nanodeeltjes zijn die uniform zijn verspreid op het oppervlak van de CeO2 nanostaafjes (Fig. 4d), die een aantal ruwe interfaces vormen.
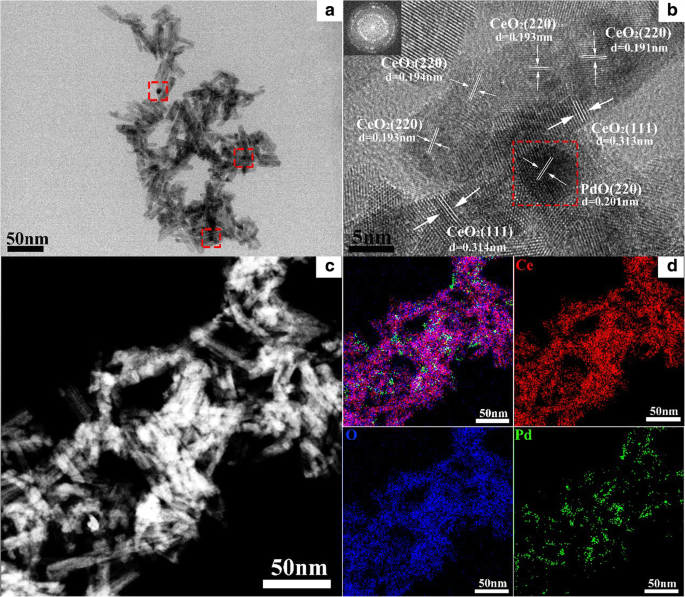
TEM (a ), HRTEM (b ), en TEM-EDS-toewijzing (c , d ) afbeeldingen van de gedelegeerde Al91,3 Ce8 Pd0.7 legering gecalcineerd bij 400 °C
De BET- en BJH-tests zijn uitgevoerd op de gedeloyeerde Al91,3 Ce8 Pd0.7 gecalcineerd bij verschillende temperaturen, en de overeenkomstige resultaten worden getoond in Fig. 5 en Tabel 1. Alle monsters vertoonden type IV isothermen met H2 en H3 hysteresislussen, zoals getoond in Fig. 5a. Dit resultaat geeft aan dat de monsters mesoporeuze structuren zijn, wat consistent is met de SEM- en TEM-resultaten. Bovendien bewijst de poriegrootteverdelingscurve getoond in Fig. 5b verder dat alle monsters een mesoporeuze structuur bezitten, en de gecalcineerde monsters vertoonden vergelijkbare smalle poriegrootteverdelingen met een gemiddelde poriediameter van ongeveer 12~14 nm. Het specifieke oppervlak (S BET ), poriegrootte (D p ), en porievolume (V p ) van de monsters bij de overeenkomstige calcineringstemperaturen zijn vermeld in Tabel 1. Het gecalcineerde monster van 400 ° C vertoont het grootste specifieke oppervlak en het grootste porievolume gelijk aan ongeveer 102 m 2 g −1 en 0,362 cm 3 g −1 , respectievelijk. Omdat de calcineringstemperatuur continu werd verhoogd, nam het specifieke oppervlak enigszins af; maar zelfs na de calcinering van 600 °C had het monster nog steeds een specifiek oppervlak van 84 m 2 g −1 . Deze resultaten geven aan dat de staafachtige nanoporeuze CeO2 skeletstructuur heeft een uitstekend anti-sintervermogen. Deze conclusie wordt ook bevestigd door de kristalgroottes in aanvullend bestand 1:tabel S1 en de SEM- en TEM-beelden in aanvullend bestand 1:figuur S2.
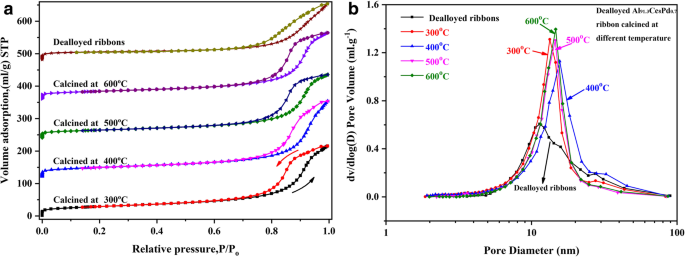
Stikstofadsorptie-desorptie isotherm curves (a ) en poriegrootteverdelingscurven (b ) van gedelegeerde Al91,3 Ce8 Pd0.7 linten gecalcineerd bij verschillende temperaturen
De XPS-spectra van de gedeloyeerde Al91,3 Ce8 Pd0.7 monster en het gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 monster worden getoond in Fig. 6 om de valentiesamenstelling van de oppervlakte-elementen van de monsters verder te karakteriseren. Het XPS-spectrum van Ce 3d wordt getoond in Fig. 6a, waarbij U Ce 4+ voorstelt en V staat voor Ce 3+ [22]. Over het algemeen is het bestaan van Ce 3+ hangt nauw samen met zuurstofvacatures. De berekende resultaten geven aan dat de concentraties van Ce 3+ in de gedelegeerde Al91,3 Ce8 Pd0.7 monster en het gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 monster waren respectievelijk 21,15% en 23,33%, met weinig verschil, zoals weergegeven in Tabel 2. Dit resultaat geeft aan dat de calcinering nauwelijks invloed heeft op de concentratie van de zuurstofvacatures aan het oppervlak. Om het effect van PdO-lading op de zuurstofvacatureconcentratie van het monster te begrijpen, is het XPS-spectrum van het gedeloyeerde Al92 Ce8 monster gecalcineerd bij 400 °C (zuiver CeO2 ) wordt weergegeven in Aanvullend bestand 1:Afbeelding S3. De Ce 3+ de concentratie werd berekend op ongeveer 14,27%, wat veel minder is dan die van het monster geladen met PdO. Dit fenomeen geeft aan dat er een interactie is tussen PdO en CeO2 en dat de aanwezigheid van PdO de valentietoestand van CeO2 . kan veranderen oppervlakte-elementen en verhoog de concentratie van zuurstoflekkage aan het oppervlak.
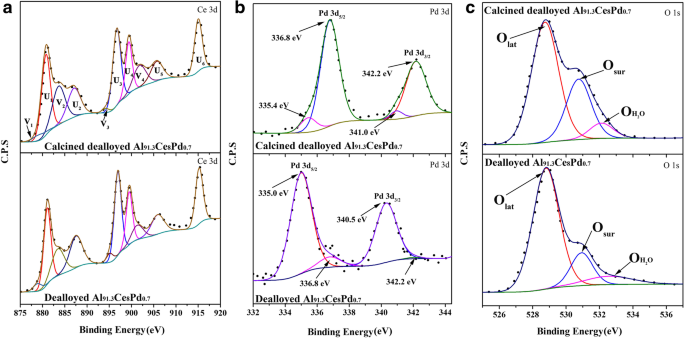
XPS-spectra van de Ce 3d (a ), Pd 3d (b ), en O 1s (c ) regio's van de gedelegeerde Al91,3 Ce8 Pd0.7 monster en de gedeloyeerde Al91,3 Ce8 Pd0.7 monster gecalcineerd bij 400 °C
Om de effecten van calcineren op het oppervlak van PdO-nanodeeltjes verder te onderzoeken, zijn de Pd 3d XPS-spectra van de gedeloyeerde Al91,3 Ce8 Pd0.7 monster en het gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 monster worden getoond in Fig. 6b. Er zijn twee vormen van Pd in het gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 lintje; de sterke pieken bij 336,8 eV en 342,2 eV kunnen worden toegeschreven aan PdO (Pd 2+ ) [23], en de zwakke pieken bij 335,4 eV en 341,0 eV kunnen worden toegeschreven aan metaal Pd (Pd 0 ) [24]. Tabel 2 laat zien dat de concentraties van Pd 2+ en Pd 0 waren respectievelijk ongeveer 91,25% en 8,75%. De analyseresultaten voor de gedeloyeerde Al91,3 Ce8 Pd0.7 monster zijn het tegenovergestelde, en de concentraties van Pd 2+ en Pd 0 waren respectievelijk ongeveer 6,45% en 93,55%. Deze bevinding geeft aan dat Pd aanwezig is in de vorm van metallisch Pd in het gedeloyeerde monster, terwijl na calcinering Pd werd geoxideerd tot PdO en uniform gedispergeerd op het oppervlak van CeO2 , wat consistent is met de resultaten van de HRTEM-beelden.
Het is algemeen bekend dat oppervlakte-actieve zuurstof (Osur ) is gewoonlijk een actieve zuurstofsoort voor katalytische reacties. Figuur 6c toont de O 1s XPS-spectra van de twee katalysatoren. Voor de gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 monster, komen de pieken bij 528,9 eV, 530.6 eV en 532.1 eV overeen met de roosterzuurstof (Olat ), oppervlakte-actieve zuurstof (Osur ), en zwak geadsorbeerd H2 O (OH2O ), respectievelijk [25, 26]. De verhouding van Osur (Oop /(Olat + Oop + OH2O )) werd berekend en staat vermeld in Tabel 2. De verhoudingen van Osur voor de gedelegeerde Al91,3 Ce8 Pd0.7 monster en het gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 monster waren respectievelijk ongeveer 16,2% en 29,3%, wat wijst op de aanwezigheid van meer oppervlakte-actieve zuurstofsoorten in het gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 steekproef. De concentraties van Ce 3+ in deze twee katalysatoren waren vergelijkbaar (Fig. 6a), wat suggereert dat PdO een sterker vermogen heeft om O2 te adsorberen en te activeren dan de metalen Pd-nanodeeltjes. Een afzonderlijk experiment (aanvullend bestand 1) is ontworpen om de interferentie van thermische activering op de experimentele resultaten te elimineren, zoals weergegeven in aanvullend bestand 1:figuur S4, en de verkregen resultaten ondersteunen ook de bovenstaande conclusie.
Om de verschillen in de reduceerbaarheid van de monsters voor en na het calcineren te vergelijken, H2 -TPR werd gebruikt om zowel de gecalcineerde gedeloyeerde Al91,3 Ce8 Pd0.7 monster en de gedeloyeerde Al91,3 Ce8 Pd0.7 monster, en de resultaten worden getoond in Fig. 7. Er zijn drie hoofdpieken in de twee TPR-curven, maar hun intensiteiten en posities zijn verschillend. De twee reeksen pieken, P2 , P2 ′ en P3 , P3 ′, in het hoge temperatuurbereik (> 300 °C) worden toegeschreven aan de vermindering van oppervlakte CeO2 en bulk CeO2 , respectievelijk [27], terwijl de P1 en P1 ′ pieken in het lage temperatuurbereik (< 300 °C) worden toegeschreven aan de vermindering van PdO-soorten en de Pd 2+ -O-Ce 4+ structuur [28]. Het gebied van de P1 piek is aanzienlijk groter dan die van de P1 ′-piek, wat aangeeft dat het gecalcineerde gedeloyeerde monster meer PdO-soorten bevatte, wat consistent is met de resultaten van XPS. Het feit dat de P1 piekoppervlak is groter dan dat van de P1 ′ piek geeft ook aan dat voor het gecalcineerde gedeloyeerde monster meer van de Ce 4+ ionen verbonden met PdO-soorten kunnen bij lage temperaturen worden gereduceerd, wat gunstig is voor de katalytische oxidatiereactie. De P2 en P2 ′ pieken in de buurt van 470 °C bewijzen dit vermoeden ook. Het gebied van de P2 ′ piek is aanzienlijk groter dan die van de P2 piek, wat aangeeft dat voor het gecalcineerde gedeloyeerde monster de concentratie van oppervlakte CeO2 soorten die alleen bij hoge temperaturen kunnen worden gereduceerd, was minder dan die van het gedeloyeerde monster; met andere woorden, een deel van de Ce 4+ ionen verbonden met PdO werd verminderd bij lage temperaturen. In combinatie met de XPS-analyse is het redoxvermogen van de PdO/CeO2 composieten is hoger dan die van de Pd/CeO2 , wat suggereert dat PdO/CeO2 composieten vertonen een hogere katalytische prestatie.
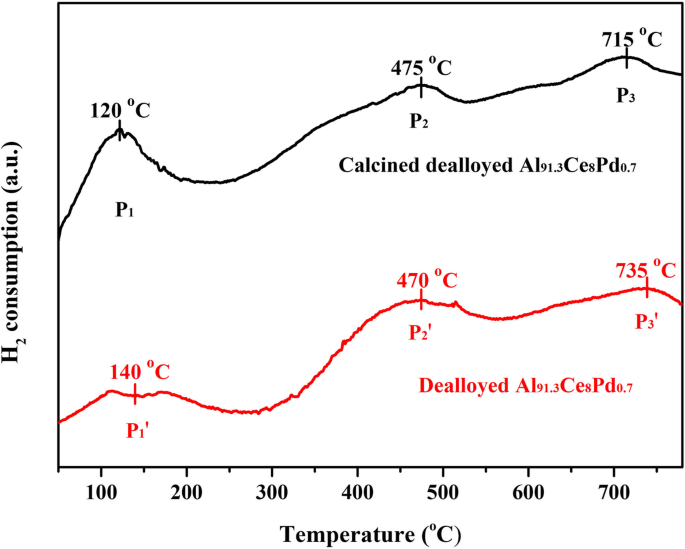
H2 -TPR-curven van de gedeloyeerde Al91,3 Ce8 Pd0.7 linten en de gedelegeerde Al91.3 Ce8 Pd0.7 linten gecalcineerd bij 400 °C
Op basis van de bovenstaande karakteriseringsresultaten, een mogelijk vormingsmechanisme voor de PdO/CeO2 composieten wordt voorgesteld (Fig. 1). Eerst wordt in de NaOH-oplossing Al opgelost en reageert Ce met OH − bij 80 °C om het staafachtige nanoporeuze Ce(OH)3 . te vormen skeletstructuur door de anisotropie van Ce(OH)3 groei. Tegelijkertijd diffunderen Pd-atomen naar het oppervlak van de Ce(OH)3 nanostaafjes. Omdat Ce(OH)3 is extreem onstabiel, het is gemakkelijk uitgedroogd en geoxideerd tot CeO2 tijdens het drogen aan de lucht. Na calcineren onder O2 , de meeste Pd-nanodeeltjes op het oppervlak van de CeO2 nanostaafjes werden geoxideerd om PdO te vormen (Fig. 6b) en werden gedeeltelijk ingebed in de CeO2 nanostaafjes (Fig. 4) bij de hoge temperatuur om een sterke metaal-oxide-drager interactie te produceren. Hierdoor is de PdO/CeO2 composieten werden gevormd.
Katalytische activiteitstest
De relatie tussen het gehalte aan Pd in de voorloper en de katalytische activiteit van de katalysatoren wordt getoond in Fig. 8a en b. Zoals getoond in Fig. 8a, CeO2 nanostaafjes vertonen een slechte katalytische activiteit tegen de oxidatie van CO (inzet), en de T 99 (corresponderende reactietemperatuur wanneer de conversie 99% is) is zo hoog als 280 °C. De katalytische activiteit was significant verhoogd voor CO-oxidatie door de belading van PdO. De steekproef van gedeloyeerde Al91,3 Ce8 Pd0.7 vertoonde de beste katalytische activiteit van CO, en de T 50 (overeenkomstige reactietemperatuur wanneer de conversie 50% is) en T 99 waren respectievelijk 15°C en 80°C. De licht-uit temperatuur was ook lager dan -20 °C. Wanneer het gehalte aan Pd in de voorloper echter verder werd verhoogd, werd de katalytische activiteit enigszins verlaagd. De katalytische activiteiten richting CH4 verbranding van de katalysatoren gegenereerd uit voorlopers met verschillende Pd-gehalten worden getoond in Fig. 8b. Vergelijkbaar met die gezien voor CO-oxidatie, de zuivere CeO2 nanostaafjes vertonen een slechte katalytische activiteit ten opzichte van CH4 verbranding, en de conversie bij 600 °C was slechts 65%. Na de toevoeging van PdO was de katalytische activiteit sterk verbeterd. Evenzo heeft de gedelegeerde Al91,3 Ce8 Pd0.7 monster vertoonde de beste katalytische activiteit tegen CH4 verbranding, met een uitschakeltemperatuur van ongeveer 250 °C, en de T 50 en T 99 waren respectievelijk 305 °C en 380 °C.
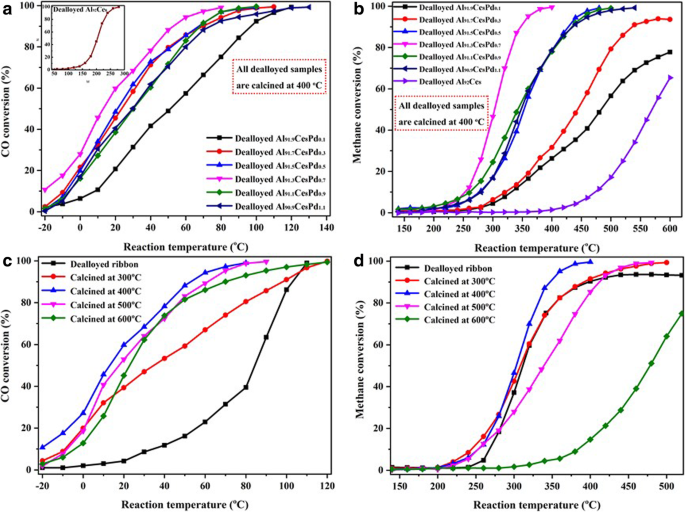
CO-conversie (a ) en CH4 conversie (b ) als functies van de reactietemperatuur op het gedeloyeerde Al90 Ce10 linten en de gedeloyeerde Al-Ce-Pd-linten met verschillende Pd-gehalten gecalcineerd bij 400 °C. De CO-conversie (c ) en CH4 conversie (d ) als functies van de reactietemperatuur op de gedeloyeerde Al91,3 Ce8 Pd0.7 gecalcineerd bij verschillende temperaturen
De CO en CH4 conversies als functies van de reactietemperatuur over gedeloyeerd Al91,3 Ce8 Pd0.7 linten gecalcineerd bij verschillende temperaturen worden getoond in Fig. 8c en d. Het gedeloyeerde lint (geen calcinering) vertoonde een slechte katalytische activiteit van CO in vergelijking met die van de gecalcineerde monsters, zoals getoond in Fig. 8c. In combinatie met de XPS-analyse geven deze resultaten aan dat PdO wordt ondersteund op CeO2 nanostaafjes vertonen een betere katalytische activiteit van CO dan die van Pd, wat consistent is met de H2 -TPR-analyse. Beneden 400 °C nam de katalytische activiteit ten opzichte van CO geleidelijk toe met de calcineringstemperatuur; wanneer echter gecalcineerd bij temperaturen hoger dan 400 ° C, nam de katalytische activiteit ten opzichte van CO af met toenemende calcineringstemperatuur. Voor de CH4 verbranding vertoonde op vergelijkbare wijze het monster dat bij 400 ° C was gecalcineerd de beste katalytische activiteit, zoals weergegeven in figuur 8d. Het gedeloyeerde lint vertoonde echter een licht-uit-temperatuur en T 50 vergelijkbaar met die van het gecalcineerde monster, en de omzetting van CH4 was altijd lager dan 93%. Volgens de experimentele resultaten en analyse van de katalytische activiteit van het gedeloyeerde lint en het gecalcineerde gedeloyeerde lint onder verschillende O2 atmosferen (Aanvullend bestand 1:Afbeelding S5), kunnen de redenen voor dit fenomeen zijn dat de licht-uit-temperatuur voor CH4 was hoog (>-240 °C) en een deel van het Pd was geoxideerd tot PdO; het monster vertoont dus een goede CH4 Katalytische activiteit. Omdat het composiet echter niet wordt gecalcineerd in een zuivere O2 atmosfeer, was de oxidatie onvoldoende in die mate dat het CH4 . niet volledig kan omzetten . Voor de gedelegeerde Al91,3 Ce8 Pd0.7 gecalcineerd bij verschillende temperaturen, de volgorde van katalytische activiteit richting CH4 is als volgt:gedeloyeerd monster (geen calcinering)
Cyclusstabiliteitstesten werden ook uitgevoerd op de gedeloyeerde Al91,3 Ce8 Pd0.7 linten gecalcineerd bij 400 ° C, zoals getoond in Fig. 9a en b. Of het nu gaat om de oxidatie van CO of voor de verbranding van CH4 laten de resultaten zien dat vergelijkbare curven kunnen worden verkregen voor deze drie opeenvolgende activiteitstesten en dat de katalysator stabiel is en niet gedeactiveerd. Dit resultaat geeft aan dat de katalysator verkregen door calcineren van gedeloyeerd Al91,3 Ce8 Pd0.7 linten bij 400 °C hebben praktische toepassingswaarde en kunnen meerdere keren worden gebruikt.
Cyclic stability tests (a , b ), resistance to CO2 toxicity tests (c , d ), and water resistance tests (e , v ) of the dealloyed Al91.3 Ce8 Pd0.7 ribbons calcined at 400 °C
Generally, for catalysts with practical application value, they must be stable in the presence of CO2 en H2 O. Reaction gases containing CO2 of H2 O were passed over the catalyst to examine the CO2 en H2 O tolerances of the dealloyed Al91.3 Ce8 Pd0.7 ribbons calcined at 400 °C, as shown in Figs. 9c–f. Compared with the response in the absence of CO2 in the reaction gas, the addition of 15 vol% CO2 reduced the activity of the catalyst towards CO oxidation, as shown in Fig. 9c, with a T 50 en T 99 of 80 °C and 130 °C, respectively. However, upon further increasing the CO2 to 30 vol%, the activity of the catalyst towards CO oxidation only slightly reduces, and the T 50 en T 99 are 88 °C and 140 °C, respectively. For methane combustion, the presence of 15 vol% CO2 in the reaction gas has little effect on the catalytic activity, and the T 50 en T 99 increased by only 5 °C and 30 °C, respectively, compared to those in the absence of CO2 , as shown in Fig. 9d. When the concentration of CO2 was doubled (30 vol% CO2 ), the catalytic activity continues to decrease, with a T 50 en T 99 of 350 °C and 460 °C, respectively. Thus, in cases where the reactant concentration is constant, increasing the concentration of the CO2 products will form a strong competitive relationship with CO and CH4 for adsorption on the PdO nanoparticles and at its interfaces, thereby reducing the amount of CO or CH4 adsorbed per unit time and, consequently, the conversion rate. However, due to the higher reaction temperature required for methane combustion, the desorption of CO2 is enhanced such that the CO2 effect on methane combustion seems to be weaker than the effect on CO oxidation.
The long-term stability and water resistance tests of the catalyst are shown in Figs. 9e and f. For CO oxidation, the catalytic activity hardly decreases after 100 h of testing, regardless of the presence or absence of a high concentration of water vapour (20 vol%), indicating that the catalyst has excellent long-term stability and water resistance for CO oxidation. For methane combustion at high conversion (99%), the catalyst possesses similar properties with respect to CO oxidation. At the same time, the effect of water vapour on methane combustion at low conversion (30%, 50%, and 85%) is also discussed in Additional file 1:Figure S6. The effect of water vapour on the catalytic activity at low conversion is greater than that at high conversion. Detailed descriptions and discussions are presented in Additional file 1:Figure S6. The conclusions obtained are similar to those reported by Burch et al. [29]. By comparison with the water resistance of some recently reported Pd-based catalysts for methane combustion (Additional file 1:Table S2), the PdO/CeO2 catalyst prepared in this study retains a relatively excellent catalytic activity after a higher water vapour concentration (20 vol%) and a longer reaction time (100 h), which is very helpful to further the practical application of methane combustion.
The flow rate of the reaction gas and the concentration of O2 are known to have an important influence on the catalytic activity of a catalyst. Here, the effect of the flow rate on the catalytic performance of the dealloyed Al91.3 Ce8 Pd0.7 ribbons calcined at 400 °C was first studied, as shown in Figs. 10a and b. As shown in Fig. 10a, for CO oxidation, when the total flow rate was increased from 20 mL min
−1
(space velocity 12,000 h
−1
) to 100 mL min
−1
(space velocity 60,000 h
−1
), the conversion of CO gradually decreased from the initial 78 to 31%. However, it is worth noting that although the conversion of CO decreased with increasing flow rate, the reaction rate (r CO ) gradually increased. This phenomenon was caused by a decrease in the contact time of the gases with the active sites when the gas flow rate was increased, causing a decrease in the conversion; however, the actual amount of the reactant flowing over the active sites per unit time was increased, thereby resulting in the increased reaction rate. A similar phenomenon was observed for methane combustion. However, it appears that the flow rate had a slightly smaller effect on the conversion of CH4 than on the conversion of CO. As the flow rate increased from 20 to 100 mL min
−1
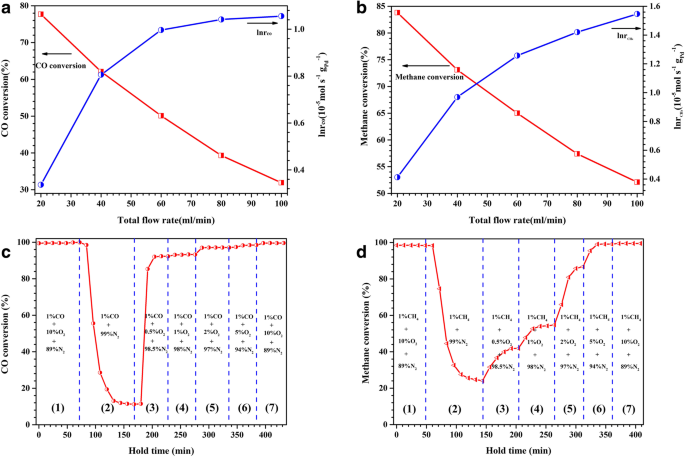
, the conversion of methane decreased from an initial value of 84 to 53%. Moreover, the reaction rate of methane combustion (r CH4 ) exhibited a linear increase with the flow rate, rather than tending to remain stable, similar to that seen for r CO . This indicates that the catalyst has a wider flow rate range for methane combustion than for CO oxidation. In this study, the calculated values of r CO en r CH4 under different test conditions were in the range of 1.40~2.87 \( \left(\times {10}^{-5}\mathrm{mol}\cdotp {\mathrm{g}}_{\mathrm{Pd}}^{-1}\cdotp {\mathrm{s}}^{-1}\right) \)and 1.51~4.70 \( \left(\times {10}^{-5}\mathrm{mol}\cdotp {\mathrm{g}}_{\mathrm{Pd}}^{-1}\cdotp {\mathrm{s}}^{-1}\right) \), respectively.
Catalytic activity and reaction rate of the dealloyed Al91.3 Ce8 Pd0.7 ribbons calcined at 400 °C for CO oxidation with different flow rates at 20 °C (a ) and for methane combustion with different flow rates at 320 °C (b ) (reaction gas 1 vol% CO/CH4 , 10 vol% O2 , and 89% vol% N2 .). The catalytic activity of the dealloyed Al91.3 Ce8 Pd0.7 ribbons calcined at 400 °C for CO oxidation in the presence of different O2 concentrations at 80 °C (c ) and for methane combustion in the presence of different O2 concentrations at 380 °C (d )
Next, the effect of the O2 concentration in the reaction gas on the catalytic activity of the catalyst was investigated. For CO oxidation, as shown in Fig. 10c, when under oxygen-rich conditions (10 vol% O2 ), the CO conversion was maintained at 99%, and as the O2 concentration suddenly decreased to 0 (anaerobic conditions), the CO conversion decreased rapidly before eventually stabilizing at approximately 12%. The reason for this phenomenon was that the surface lattice oxygen participated in the oxidation reaction of CO. Generally, the CO oxidation pathway involving lattice oxygen on the surface of the support is slow and inefficient compared to the direct adsorption activation of the O2 molecule [30]. Therefore, the CO conversion remained at a lower level under the anaerobic conditions in this study. This result also indicated that the CeO2 carrier has a strong ability to store/release oxygen. Subsequently, 0.5% O2 was introduced into the reaction gas, and the CO conversion rapidly recovered to 90%. As the O2 concentration continues to increase, the CO conversion eventually reached the initial 99%, and a new steady state was established. For methane combustion (Fig. 10d), a similar result to that of CO oxidation was observed but with two different points. The first point was that when in an anaerobic environment, the conversion of CH4 finally stabilized at 25%, higher than that of the anaerobic conversion of CO, which indicated that a high reaction temperature could accelerate the migration of surface lattice oxygen thereby improving the conversion efficiency. The second point was that as the O2 concentration increased, the increasing rate of CH4 conversion and the final establishment of a steady state were slower than those in the CO conversion, which may be due to the incomplete combustion of methane under oxygen-poor conditions (0.5~2 vol% O2 ). This result also shows that methane combustion is a more complicated and difficult reaction compared to CO oxidation.
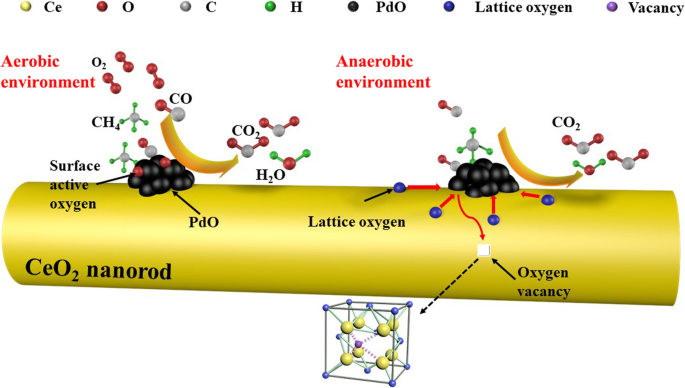
Based on the results of the characterization and experiments, a simple mechanism for CO oxidation and methane combustion is proposed, as shown in Fig. 11.
Schematic illustration of CO oxidation and methane combustion over the rod-like nanoporous PdO/CeO2 catalysts
First, the CO and CH4 molecules in the reaction gas are adsorbed onto the surface of PdO, reacting rapidly with the adsorbed and activated oxygen on the surface of PdO, and then CO2 en H2 O are produced and desorbed. The active sites become available again, and a high reaction rate for CO oxidation and CH4 combustion is maintained. It is worth noting that the catalytic oxidation reaction can still proceed slowly under anaerobic conditions, which is shown to be related to the participation of the surface lattice oxygen of the nanorods in the catalytic reaction (Figs. 10c, d), as shown in Fig. 11.
A large number of experimental results indicated that the PdO/CeO2 catalyst prepared by dealloying combined with calcination exhibited excellent catalytic activities towards CO oxidation and methane combustion and possesses outstanding cycle stability, resistance to CO2 toxicity, and water resistance. In addition to its inherent simplicity, the “green” preparation method of dealloying can effectively avoid the contamination of nanomaterials by organic chemicals and other surfactants, which are common to wet chemical synthesis methods. In addition, the PdO/CeO2 catalyst prepared by dealloying combined with calcination exhibits excellent reproducibility, and the repeated experiments detailed in Additional file 1:Figures S7–S10, Tables S3 and S4 proved this point very well. Therefore, this work can provide insight into the preparation of other new catalysts.
In summary, a simple method of dealloying an Al-Ce-Pd ribbon combined with calcination has been developed for the preparation of a PdO/CeO2 rod-like nanoporous composite. The experimental results indicate that the sample prepared by the dealloying of an Al91.3 Ce8 Pd0.7 ribbon in 20 wt% solution and then calcining at 400 °C showed the best catalytic activities towards CO oxidation and methane combustion, and the reaction temperatures for the complete conversions of CO and CH4 are 80 °C and 380 °C, respectively. The high catalytic activities could be attributed to the good dispersion of the PdO nanoparticles (having a large specific surface area of 102 m
2
g
−1
), a strong redox capacity, the interaction between PdO and CeO2 , and more surface active oxygen on PdO. In addition, the catalyst also exhibited excellent cycle stability, resistance to CO2 toxicity, and water resistance, where after 100 h of testing, the catalytic activity hardly decreased in the presence of H2 O. Furthermore, the catalytic reactions can occur even under anaerobic conditions. These results demonstrate the feasibility of the combined dealloying calcination method for the preparation of new catalysts. It is expected that the method can be applied to the preparation of similar composite materials.
The datasets supporting the conclusions of this article are included within the article.
Methane
Koolmonoxide
Pore size
Energiedispersieve spectrometer
Energy-dispersive X-ray spectra
Flame ionization detector
Hydrogen temperature-programmed reduction
Specific surface areas
Scanning elektronenmicroscoop
Transmissie elektronenmicroscoop
Pore volume
Röntgenfoto-elektronenspectroscopie
Röntgendiffractie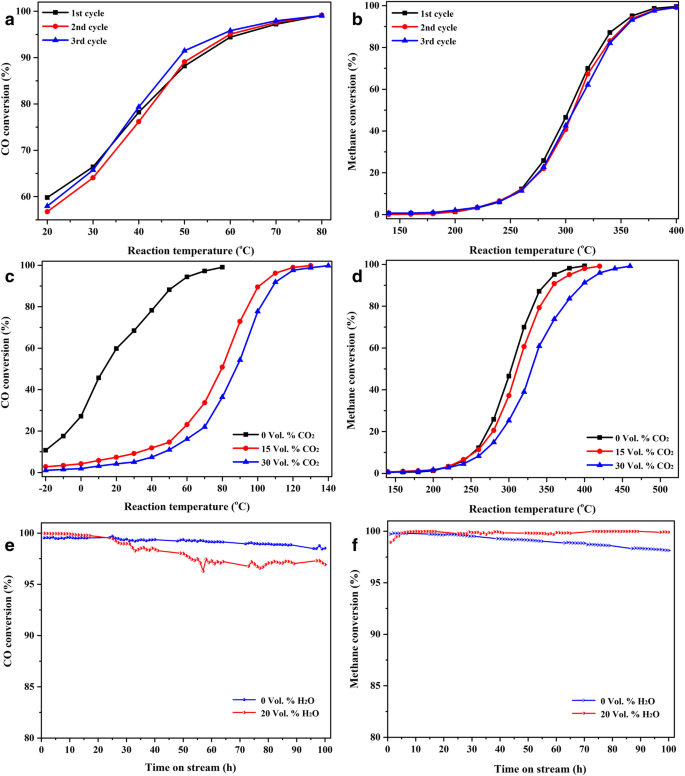
Conclusies
Beschikbaarheid van gegevens en materialen
Afkortingen
Nanomaterialen
- Nanodeeltjes voor kankertherapie:huidige vooruitgang en uitdagingen
- Voorbereiding en verbeterde katalytische hydrogeneringsactiviteit van Sb/Palygorskite (PAL) nanodeeltjes
- Met resveratrol geladen albumine-nanodeeltjes met verlengde bloedcirculatie en verbeterde biocompatibiliteit voor zeer effectieve gerichte pancreastumortherapie
- Gemodificeerd hypervertakte polyglycerol als dispergeermiddel voor groottecontrole en stabilisatie van gouden nanodeeltjes in koolwaterstoffen
- synergetische effecten van Ag-nanodeeltjes/BiV1-xMoxO4 met verbeterde fotokatalytische activiteit
- Bevordering van SH-SY5Y-celgroei door gouden nanodeeltjes gemodificeerd met 6-mercaptopurine en een neuron-penetrerend peptide
- Silica diatomeeënschalen op maat gemaakt met Au-nanodeeltjes maken gevoelige analyse van moleculen mogelijk voor biologische, veiligheids- en milieutoepassingen
- Onderkoeling van water gecontroleerd door nanodeeltjes en ultrageluid
- Eigenschappen van zinkoxide-nanodeeltjes en hun activiteit tegen microben
- Een gemakkelijke aanpak voor de bereiding van zinkoxide van nanoformaat in water/glycerol met extreem geconcentreerde zinkbronnen
- Nieuwe levering van mitoxantron met hydrofoob gemodificeerde pullulan-nanodeeltjes om blaaskankercellen te remmen en het effect van de grootte van nanomedicijnen op de remmingsefficiëntie



