PtNi-legering Cocatalyst-modificatie van eosine Y-gesensibiliseerde g-C3N4/GO-hybride voor efficiënte zichtbaar-licht fotokatalytische waterstofevolutie
Abstract
Een economische en effectieve cokatalysator van een op Pt gebaseerde legering heeft veel aandacht getrokken vanwege hun uitstekende katalytische activiteit en het verminderen van het Pt-gebruik. In deze studie werd de cokatalysator van een PtNi-legering met succes gedecoreerd op de g-C3 N4 /GO hybride fotokatalysator via een gemakkelijke chemische reductiemethode. De Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO-0,5% composiet fotokatalysator levert ongeveer 1,54 en 1178 keer hogere waterstofontwikkelingssnelheid dan de Eosine Y-gesensibiliseerde g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /Ni/GO-0,5% monsters, respectievelijk. Mechanisme voor verbeterde prestaties voor de g-C3 N4 /PtNi/GO-composiet werd ook onderzocht door verschillende karakteriseringen, zoals fotoluminescentie, tijdelijke fotostroomrespons en TEM. Deze resultaten gaven aan dat een verbeterde efficiëntie van de ladingsscheiding en meer reactieve plaatsen verantwoordelijk zijn voor de verbeterde prestaties van waterstofontwikkeling vanwege het positieve synergetische effect tussen Pt en Ni. Deze studie suggereert dat PtNi-legering kan worden gebruikt als een economische en effectieve cokatalysator voor waterstofontwikkelingsreacties.
Een significante verbetering van fotokatalytisch H2 evolutie wordt gerealiseerd via de Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO-composiet met PtNi-legering als efficiënte cokatalysator.
Achtergrond
Duurzame en grootschalige waterstofontwikkeling uit water met behulp van zonne-energie wordt beschouwd als een van de veelbelovende methoden om de energiecrisis en milieuvervuiling op te lossen [1, 2]. Om dit doel te bereiken, zijn een fotokatalysator met een zichtbaar lichtrespons en een efficiënte cokatalysator vereist [3,4,5]. Gewoonlijk is het laden van edelmetaal Pt als een efficiënte cokatalysator zeer noodzakelijk om een hoge waterstofontwikkelingssnelheid te bereiken [6,7,8]. Pt is echter zeldzaam en duur, wat de praktische toepassing ervan belemmert. Het is gewenst om de hoeveelheid Pt-gebruik te verminderen en tegelijkertijd de uitstekende katalytische activiteit ervan voor waterstofontwikkeling te behouden. Het vervangen van een deel van Pt door overgangsmetaal (Ni, Co, Cu, Fe, enz.) om een cokatalysator van een bimetaallegering te vormen, is een veelbelovende potentiële manier om uitstekende katalytische activiteit te bereiken en het gebruik van Pt te verminderen [9,10,11]. In sommige gevallen is de katalytische prestatie van een op Pt gebaseerde cokatalysator van een bimetaallegering vergelijkbaar met zuiver Pt vanwege het positieve synergetische effect tussen de twee metalen. Daarom is de laatste tijd meer aandacht besteed aan een fotokatalysator met een reactie op zichtbaar licht, geladen met een cokatalysator van een bimetaallegering.
Yu et al. meldde dat PtCo of PtNi-legering cokatalysator-gemodificeerd Cu2 ZnSnS4 toonde hogere H2 productie-efficiëntie dan de zuivere Pt-lading Cu2 ZnSnS4 [12]. Pt3 Co bimetaal cokatalysator versierde CdS werden bereid door Hu et al. en vertoonden verbeterde prestaties op het gebied van waterstofontwikkeling [13]. PtCo en/of PtFe laden Zn1 − x Cd x S werden ook geëvalueerd in eerdere onderzoeken [14, 15]. Fotokatalytische prestaties bij weinig zichtbaar licht van Cu2 ZnSnS4 of hoge toxiciteit van Cd belemmert hun praktische toepassing op grote schaal. Koolstofnitride (g-C3 N4 ) heeft de aandacht getrokken vanwege de lage kosten [16]. Han et al. meldde dat een H2 evolutiesnelheid van 960 μmol g −1 h −1 werd verkregen over de PtCo/g-C3 N4 fotokatalysator onder λ> 400 nm instraling [17]. PtNix /g-C3 N4 hybird fotokatalysator werd ook bestudeerd door Bi et al., en een H2 evolutiesnelheid van 8456 μmol g −1 h −1 werd bereikt onder volledige spectrale bestraling [18]. De fotokatalytische prestaties in zichtbaar licht voor de bimetaallegering, met cokatalysator gemodificeerde g-C3 N4 fotokatalysator is nog steeds een beetje laag vanwege de brede bandafstand van 2,7 eV en het slechte vermogen tot elektronenoverdracht. Eosine Y-gesensibiliseerde g-C3 N4 kan een breed scala aan zichtbaar licht oogsten [19, 20]. Grafeenoxide (GO) heeft een sterk elektronentransporterend vermogen en wordt veel gebruikt als elektronenacceptor [21,22,23,24,25]. G-C3 . combineren N4 en GO kan het vermogen tot elektronenoverdracht in g-C3 . bevorderen N4 en zo de scheiding van het elektron-gatpaar te verbeteren om de fotokatalytische prestatie voor waterstofontwikkeling te verbeteren [26,27,28,29,30,31]. De laatste tijd rapporteerden we een efficiënte Eosine Y-gesensibiliseerde g-C3 N4 /Pt/GO composiet fotokatalysator voor waterstofontwikkeling [23]. De dure Pt-cokatalysator speelt een belangrijke rol voor de relatief hoge waterstofproductieprestaties. Om het dure Pt-gebruik te verminderen en de zichtbare fotokatalytische prestaties verder te verbeteren, wordt gebruik gemaakt van goedkope Eosine Y-gesensibiliseerde g-C3 N4 /GO composiet fotokatalysator geladen met op Pt gebaseerde legering cokatalysator is nuttig.
Hier, de Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO composiet fotokatalysator werd bereid voor waterstofontwikkeling uit water. De hoogste waterstofontwikkelingssnelheid van 5,89 mmol g −1 h −1 wordt verkregen via de Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO-fotokatalysator, die veel hoger is dan de Eosine Y-gesensibiliseerde g-C3 N4 /Pt/GO en g-C3 N4 /Ni/GO samengestelde monsters. Voor zover ons bekend, is er geen eerdere melding dat de Eosin Y-gesensibiliseerde g-C3 N4 /PtNi/GO composiet wordt gebruikt voor de productie van waterstof uit water. De optimale molaire verhouding van Pt/Ni en hoeveelheid PtNi-cokatalysator werden in detail onderzocht. Bovendien, mechanisme van verbeterde fotokatalytische prestaties voor de g-C3 N4 /PtNi/GO-composiet werd ook onderzocht door middel van verschillende karakteriseringsmethoden.
Experimentele sectie
Synthese van de g-C3 N4
g-C3 N4 poeders werden gesynthetiseerd zoals beschreven in eerdere studie [32]. In een typische procedure werd ureum (8 g) in een aluminiumoxidekroes met een deksel geplaatst. De kroes werd verwarmd tot 600 ° C met een verwarmingssnelheid van 5 ° C / min en gedurende 2 uur in een buisoven gehouden. Na thermische behandeling wordt de lichtgele g-C3 N4 poeders werden verzameld voor verder gebruik.
Voorbereiding van GO
GO werd bereid met behulp van de gemodificeerde Hummers-methode [33]. Natuurgrafiet (10 g) en NaNO3 (5 g) werden in een beker gedaan. Vervolgens werd 230 ml geconcentreerd zwavelzuur toegevoegd en het proces moest zo langzaam mogelijk verlopen. De bovenstaande reactie werd onder roeren onder een ijswaterbad voortgezet. Vervolgens 10 g KMnO4 werd aan de mengseloplossing toegevoegd en gedurende 3 uur gereageerd. De temperatuur van de oplossing werd verhoogd tot 35°C en gedurende 4 uur gehandhaafd. Vervolgens werd 460 ml gedestilleerd water in de bovenstaande oplossing gegoten en gedurende 3 uur tot ongeveer 98°C verwarmd. Na reactie, een bepaalde hoeveelheid H2 O2 (30%) en geconcentreerd zoutzuur werden onder roeren toegevoegd om overtollig KMnO4 te verwijderen en SO4 2− . Ten slotte werd het GO-monster verkregen door 24 uur te vriesdrogen.
Synthese van g-C3 N4 /Ni/GO, g-C3 N4 /Pt/GO, en g-C3 N4 /Ptx Nij /GO Composite Photocatalysts
Synthese van g-C3 N4 /PtNi/GO-X (X vertegenwoordigt de gewichtsverhouding van PtNi-cokatalysator tot g-C3 N4 /GO-composiet en de molaire verhouding van Pt tot Ni is 1:1):in een typische, 133 mg g-C3 N4 werden gedispergeerd in 50 ml watervrije ethanol. Overtollig NaBH4 reductiemiddel werd onder roeren aan de mengseloplossing toegevoegd. Dan een bepaald volume NiCl2 ·6H2 O-oplossing (0,1 mol/L) en H2 PtCl6 oplossing (1,0 mmol/L) druppelsgewijs toegevoegd aan de bovenstaande oplossing. Om de toegevoegde procedure van NiCl2 . te onderzoeken ·6H2 O en H2 PtCl6 oplossingen werden drie methoden gekozen, waaronder gelijktijdig laden van Pt en Ni, laden van Pt en vervolgens Ni of omgekeerd. Vervolgens werd de suspensieoplossing 5 uur geroerd om een uniforme dispersie voor PtNi-cokatalysator in de g-C3 te verkrijgen. N4 . Daarna is de g-C3 N4 /PtNi-X-monsters werden verzameld door centrifugeren om overtollig NaBH4 weg te wassen voor meerdere keren. Daarna 67 mg GO en de g-C3 N4 /PtNi-X-monster werden gelijktijdig in 100 ml gedestilleerd water gedispergeerd. De suspensieoplossing werd gedurende 10 uur bij 500 W ultrasoon behandeld. Daarna een reeks van g-C3 N4 /PtNi/GO-X samengestelde fotokatalysatoren werden verkregen door gecentrifugeerd en vervolgens gedurende één nacht bij 60 ° C in een vacuümoven gedroogd. Andere co-katalysatoren van bimetalen PtNi-legeringen met verschillende Pt/Ni-molverhoudingen (9:1, 3:1, 1:3, 1:9) werden ook bereid op dezelfde manier als de bovengenoemde methode, die Pt9 Ni1 , Pt3 Ni1 , Pt1 Ni3 , en Pt1 Ni9 , respectievelijk, speciaal de 1:1 M-verhouding van Pt/Ni-naam als PtNi.
Synthese van g-C3 N4 /Ni/GO-0,5% en g-C3 N4 /Pt/GO-0,5% monsters (0,5% vertegenwoordigt de gewichtsverhouding van Ni of Pt tot de g-C3 N4 /GO composiet):De g-C3 N4 /Ni/GO-0,5% en g-C3 N4 /Pt/GO-0,5% monsters werden bereid met dezelfde voorbereidingsprocedure van g-C3 N4 /PtNi/GO-X-monsters behalve voor het toevoegen van een ander volume NiCl2 ·6H2 O oplossing of H2 PtCl6 oplossing. De 2:1 gewichtsverhouding van g-C3 N4 to GO is gekozen in alle g-C3 N4 /Ni/GO, g-C3 N4 /Pt/GO, en g-C3 N4 /Ptx Nij /GO samengestelde monsters volgens onze eerdere studie [32].
Karakterisatiemethoden
De XRD-patronen werden verkregen met behulp van een röntgendiffractiediffractometer (Bruker D8-Advance, Duitsland) met Cu-Ka-straling. TEM-beelden van de monsters werden opgenomen via de transmissie-elektronenmicroscopie (JEM-2100, Japan). Chemische oppervlaktetoestanden van de fotokatalysatoren werden gemeten met röntgenfoto-elektronenspectroscopie (XPS, AXISULTRA) met monochromatische Al Ka-röntgenstralen (1486,6 eV). De fotoluminescentie (PL) spectra werden gemeten op een JY HORIBA FluoroLog-3 spectrometer, en de geëxciteerde golflengte van 460 nm werd gekozen. De curven van de fotostroomrespons werden uitgevoerd in een elektrochemisch werkstation (CHI660E, Chenhua, China) met behulp van een conventionele standaard drie-elektrodecel onder bestraling met zichtbaar licht (λ > -420 nm). 0,1 mol/L Na2 SO4 oplossing werd gebruikt als elektrolyt.
Meting van fotokatalytische activiteit
Fotokatalytische experimenten werden uitgevoerd in een Pyrex-cel met een plat raam bovenaan bij 6 ° C. Gewoonlijk werden 50 mg fotokatalysatorpoeder en 50 mg Eosine Y-kleurstof toegevoegd aan 100 ml H2 O met 20 vol% (v /v) triëthanolamine (TEOA, pH = 7). Als lichtbron werd een 300 W xenonlamp (D59, Beijing China Education Au-light Co., Ltd) in combinatie met een UV-filter (> 420 nm) gebruikt. De hoeveelheden waterstof werden gemeten door middel van gaschromatografie (GC-7920, TCD, Ar-drager).
Resultaten en discussie
De XRD-patronen van g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5%-monsters worden getoond in Fig. 1. Er worden twee duidelijke diffractiepieken waargenomen voor de drie monsters. Een kleine piek gecentreerd op 2θ = 13,8° wordt toegewezen aan de (100) piek van g-C3 N4 , die voortkomt uit het structurele verpakkingsmotief in het vlak [34]. De sterke diffractiepiek bij 27,4° wordt geïndexeerd als de (002) piek van g-C3 N4 , wat overeenkomt met de tussenlaagstapeling van het geconjugeerde aromatische systeem [35]. Voor de drie geëvalueerde monsters werd geen GO-, Pt- en/of Ni-cokatalysatordiffractiesignaal gedetecteerd. Voldoende afschilfering van GO in de composiet kan resulteren in geen GO-informatie [28]. Terwijl de hoeveelheid Pt en/of Ni te klein is om te detecteren met de XRD-methode. Zoals getoond in Fig. 2 vertonen de drie verschillende monsters een vergelijkbare dunnere laminaire structuur na ultrasone behandeling. Een innig contact gevormd tussen 2D-gelaagde structuur van g-C3 N4 en de nanosheetstructuur van GO. In Fig. 2a, b zijn een beetje grotere Ni- of Pt-nanodeeltjes verspreid op de tussenlaag of het oppervlak van g-C3 N4 . Vergeleken met zuiver Ni en Pt, is de grootte van de cokatalysatordeeltjes van de PtNi-legering verminderd en is de dispersie van de cokatalysator van de PtNi-legering verbeterd (zie figuur 2c). De kleine omvang van de co-katalysator van een PtNi-legering zorgt voor meer reactieve plaatsen voor waterstofontwikkeling, en de hoge dispersie van de co-katalysator van een PtNi-legering is gunstig voor de elektronenoverdracht van g-C3 N4 en/of GA naar PtNi-cokatalysator. De verbeterde dispersie van de co-katalysator van een PtNi-legering werd ook waargenomen in eerdere studie [36]. De precieze reden moet verder worden onderzocht.
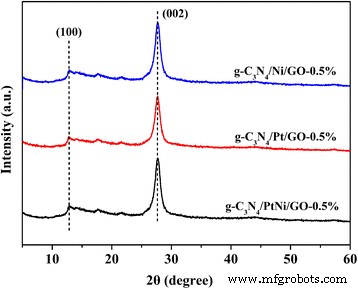
De XRD-patronen van g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters

TEM-afbeeldingen van g-C3 N4 /Ni/GO-0,5% (a ), g-C3 N4 /Pt/GO-0,5% (b ), en g-C3 N4 /PtNi/GO-0,5% (c )
Om het chemische oppervlakelement en de valentietoestanden van g-C3 . te onderzoeken N4 /Ni/GO, g-C3 N4 /Pt/GO, en g-C3 N4 /PtNi/GO-monsters, werden XPS-spectra met hoge resolutie van de drie verschillende monsters gemeten en de resultaten worden getoond in Fig. 3. In Fig. 3a kan het XPS-spectrum van C 1 s worden ingepast in twee sterke pieken met de binding energieën van ongeveer 284,8 eV en 288,2 eV, die respectievelijk worden toegewezen aan CC en N=CN [37]. De twee pieken zijn kenmerkend voor koolstofsoorten in g-C3 N4 . Twee kleine pieken bij 286,7 eV en 287,7 eV worden ook verkregen, die respectievelijk behoren tot de C-O en C=O functionele groepen op het oppervlak van GO [38]. In Fig. 3 (b), de karakteristieke pieken van C-N-C, N-(C)3 , en C-N-H-groepen in g-C3 N4 werden gedetecteerd, die zich bevinden bij de bindingsenergieën van respectievelijk 398,7, 400,3 en 401,4 eV [39]. In Fig. 3 (c) worden de banding-energieën van O 1 s gevonden bij 532,4 en 533,8 eV, die respectievelijk worden toegewezen aan zuurstofbevattende functionele groepen in het composietmonster en oppervlakte-adsorptie van zuurstofsoorten [40]. Figuur 3 (d) toont de XPS-spectra van het Pt 4f-doublet (4f7/2 en 4f5/2 ). De Pt 4f7/2 en 4f5/2 pieken bevinden zich op 70,97 en 74,28 eV voor de g-C3 N4 /Pt/GO-0,5% steekproef, die het signaal van Pt 0 vertegenwoordigen [41, 42]. Voor de g-C3 N4 /PtNi/GO-0,5% monster, de orbitale bindingsenergieën van Pt 4f verschuiven ongeveer 0,42 eV naar hoge bindingsenergie vergeleken met pure Pt. De duidelijke piekverschuiving suggereert dat Pt-elektron een klein verlies is, wat aangeeft dat de cokatalysator van de PtNi-legering wordt gevormd in de g-C3 N4 /PtNi/GO-0,5% monster. Zoals weergegeven in figuur 3e, kunnen de bindingsenergieën bij 852,54 en 870,18 eV worden toegewezen aan Ni 2p3/2 en Ni 2p1/2 voor de g-C3 N4 /Ni/GO-2% monster, respectievelijk, wat het karakteriseringssignaal is van Ni 0 [43]. Vergeleken met g-C3 N4 /Ni/GO-2%, de bindingsenergieën van Ni 2p verschoven naar lage bindingsenergie voor de g-C3 N4 /PtNi/GO-2% monster. Het resultaat suggereert dat er een verandering in de omgeving van Ni-atomen optreedt, wat verder bevestigt dat de cokatalysator van de PtNi-legering met succes wordt gesynthetiseerd [41]. De exacte molaire verhouding van Pt tot Ni in de g-C3 N4 /PtNi/GO-0,5% monster is 9:11 via XPS-meting. Op basis van bovenstaande analyse kan worden geconcludeerd dat de g-C3 N4 /PtNi/GO-composiet met PtNi-legering als cokatalysator werd verkregen door een gemakkelijke vloeistoffase sonochemische manier te combineren met een chemische reductiemethode.
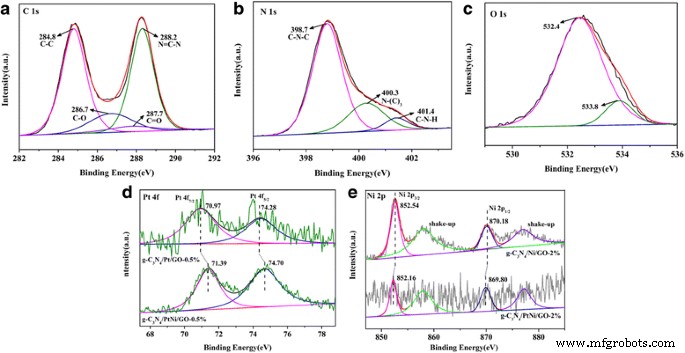
XPS-spectra van (a ) C 1 s, (b ) N 1 s en (c ) O 1 s voor de g-C3 N4 /PtNi/GO-0,5% monster. d XPS-spectra van Pt 4f voor de g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters. e XPS-spectra van Ni 2p voor de g-C3 N4 /Ni/GO-2% en g-C3 N4 /PtNi/GO-2% monsters
Afbeelding 4 toont de H2 evolutiesnelheid van reeksen van g-C3 N4 /PtNi/GO-0,5% monsters geladen met een ander type cokatalysator. Gelijktijdig laden van Pt- en Ni-namen als g-C3 N4 /PtNi/GO-0,5%; Laden van Pt- en vervolgens Ni-namen als g-C3 N4 /Pt-Ni/GO-0,5%; Laden van Ni en vervolgens Pt-namen als g-C3 N4 /Ni-Pt/GO-0,5%. Voor Eosine Y-gesensibiliseerde g-C3 N4 /Ni/GO-0,5% monster met zuiver Ni als cokatalysator, de H2 evolutiesnelheid is erg laag en bereikt slechts 0,005 mmol g −1 h −1 . Na vervanging van Ni door Pt als cokatalysator, een significante toename van H2 evolutiesnelheid wordt waargenomen, die sterk toeneemt tot 3,82 mmol g −1 h −1 voor de Eosine Y-gesensibiliseerde g-C3 N4 /Pt/GO-0,5% monster. Het resultaat suggereert dat het laden van een efficiënte Pt-cokatalysator nodig is om uitstekende prestaties voor H2 . te bereiken generatie. Bij gebruik van PtNi-legering als co-katalysator, de Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO-0.5% composiet toont de hoogste H2 evolutiesnelheid van 5,89 mmol g −1 h −1 , wat ongeveer 1,54 en 1178 keer hoger is dan de eosine Y-gesensibiliseerde g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /Ni/GO-0,5% monsters, respectievelijk. De verbeterde prestatie kan worden toegeschreven aan het positieve synergetische effect tussen Pt en Ni. Vergeleken met pure Pt-cokatalysator, versnelt de PtNi-legeringscokatalysator de accumulatie van fotogenereerde elektronen, wat meer elektronen zal opleveren voor waterstofontwikkeling [18]. Bovendien kan het kleine formaat en de hoge dispersie van de cokatalysator van een PtNi-legering meer H2 verschaffen evolutieplaatsen en verbeteren respectievelijk de elektronenoverdracht. Wanneer geladen Pt en dan Ni of omgekeerd, een duidelijke vermindering van H2 evolutieactiviteit wordt waargenomen. In feite vormt het laden van Pt en vervolgens Ni of omgekeerd geen cokatalysator van een PtNi-legering [44]. Het resultaat geeft aan dat het behalen van een hoge H2 generatiesnelheid is sterk afhankelijk van het gebruik van efficiënte PtNi-legering cokatalysator.
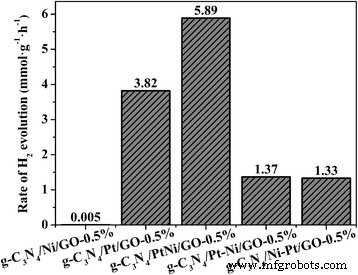
H2 evolutiesnelheid van reeksen van g-C3 N4 /PtNi/GO-0,5% monsters geladen met een ander type cokatalysator. Lichtbron:300 W Xenon-lamp (λ> 420 nm). Reactieoplossing:100 ml 20% (v /v) TEOA waterige oplossing (pH = 7)
De samenstelling van de cokatalysator van een PtNi-legering heeft een belangrijk effect op de katalytische activiteit voor H2 evolutie. Daarom is de H2 productiesnelheid van Eosine Y-gesensibiliseerde g-C3 N4 /Ptx Nij /GO-0,5% monsters geladen met verschillende Pt/Ni molaire verhoudingen werden onderzocht en de resultaten worden getoond in Fig. 5a. De H2 productiesnelheid wordt geleidelijk verhoogd met toenemende Ni/Pt molaire verhouding. Wanneer de molaire verhouding van Ni/Pt 1:1 is, is de hoogste waterstofproductiesnelheid van 5,89 mmol g −1 h −1 is verkregen. Verdere verhoging van de hoeveelheid Ni leidt tot een daling van de H2 evolutie activiteit. De degradatie van H2 generatieprestaties kunnen komen van het afnemende aantal Pt-actieve sites voor H2 evolutie. Pt-actieve plaatsen hebben een sterkere adsorptie van waterstofionen dan Ni [12]. Daarom, H2 evolutie vindt bij voorkeur plaats op Pt in plaats van Ni. Afbeelding 5b toont de H2 productiesnelheid van Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO-monsters geladen met verschillende hoeveelheden PtNi-legeringscokatalysator. Wanneer het gewichtsgehalte van de cokatalysator van een PtNi-legering 0,5% is, een waterstofontwikkelingssnelheid van 2,45 mmol g −1 h −1 wordt verkregen voor de g-C3 N4 /PtNi/GO-0,25% monster. De waterstofontwikkelingssnelheid neemt toe van 2,45 mmol g −1 h −1 tot de hoogste waarde van 5,89 mmol g −1 h −1 na de hoeveelheid PtNi-legering cokatalysator tot 0,5%. Bij het verder verhogen van de hoeveelheid co-katalysator van een PtNi-legering, vertoont de waterstofontwikkelingsprestatie een lichte afname. Overtollige cokatalysator van PtNi-legering kan de lichtabsorptie van eosine Y en g-C3 belemmeren N4 en verslechteren zo de fotokatalytische prestatie. De stabiliteit van waterstofgeneratie voor de g-C3 N4 /PtNi/GO-0,5% monster werd ook gemeten en het resultaat wordt getoond in Fig. 6. Na 4 cyclustest, de waterstofgeneratiesnelheid voor de g-C3 N4 /PtNi/GO-0,5% monster vertoont een lichte afname, wat aangeeft dat de g-C3 N4 /PtNi/GO-0,5% composietmonster heeft relatief stabiliteit voor waterstofontwikkeling. Een sterke covalente binding tussen koolstof en nitride in C3 N4 en de zwakke afbraak van Eosine Y zijn de twee belangrijkste redenen voor de stabiliteit van de waterstofontwikkeling van g-C3 N4 /PtNi/GO-0,5% steekproef [19, 45].
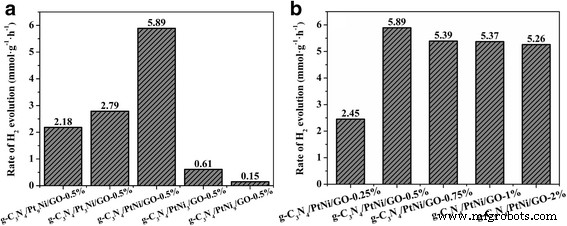
een H2 productiesnelheid van g-C3 N4 /Ptx Nij /GO-0,5% monsters geladen met verschillende Pt/Ni molaire verhoudingen. b H2 productiesnelheid van g-C3 N4 /PtNi/GO-monsters geladen met verschillende hoeveelheden PtNi-legeringscokatalysator. Lichtbron:300 W Xenon-lamp (λ> 420 nm). Reactieoplossing:100 ml 20% (v /v ) TEOA waterige oplossing (pH = 7)
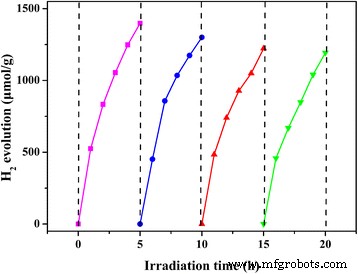
Cyclische H2 productie voor de g-C3 N4 /PtNi/GO-0,5% monster. Lichtbron:300 W Xenonlamp (λ > 420 nm), reactieoplossing:100 ml 20% (v/v) TEOA waterige oplossing (pH = 7), fotokatalysator, 50 mg, de gewichtsverhouding van eosine Y tot fotokatalysator is 1 :1
Om het mechanisme te onderzoeken voor de verbeterde fotokatalytische prestaties van g-C3 N4 /PtNi/GO-monster met PtNi-legering als cokatalysator, werden twee mogelijke redenen voor lichtabsorptie en efficiëntie van ladingsscheiding geëvalueerd. Afbeelding 7 toont de UV-Vis diffuse reflectiespectra van g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters. De drie verschillende monsters vertonen een duidelijke absorptie na ongeveer 450 nm, die afkomstig is van de metalen cokatalysator [18]. De g-C3 N4 /Ni/GO-0,5% monster met zuiver Ni als cokatalysator vertoont de sterkste absorptie na ongeveer 450 nm. Echter, de H2 evolutiesnelheid voor de g-C3 N4 /Ni/GO-0,5% monster is het laagst. Het resultaat suggereert dat de verbeterde H2 evolution-prestaties komen niet van de verbeterde lichtabsorptie.
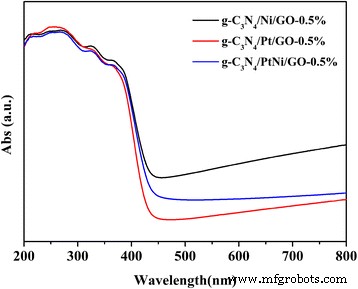
UV-Vis diffuse reflectiespectra van g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters
De efficiëntie van de ladingsscheiding kan worden gekarakteriseerd door de fotoluminescentie (PL) uitdovingsspectra [46, 47]. Over het algemeen duidt een sterke intensiteit van PL-spectra op ernstige recombinatie van ladingsdragers. Afbeelding 8a toont de fotoluminescentie (PL)-uitdovingsspectra van Eosine Y door de g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters. Alleen de Eosine Y-oplossing zonder fotokatalysator vertoont een uitgebreide emissiepiek bij ongeveer 540 nm vanwege de geconjugeerde xantheenstructuur van Eosine Y en de sterke recombinatiecapaciteit van fotogegenereerde elektron-gatparen in geëxciteerde Eosine Y. Duidelijke fluorescentie-uitdoving wordt waargenomen na toevoeging van verschillende soorten fotokatalysatoren aan de Eosine Y-oplossing. Het uitdoven van de fluorescentie suggereert dat de elektronen van geëxciteerd Eosine Y naar fotokatalysatoren worden overgebracht en vervolgens naar de cokatalysator migreren voor protonreductie. Bovendien is er een kleine blauwverschuiving (ca. 1,3 nm) van PL-quenching-spectra voor de drie verschillende geëvalueerde samengestelde fotokatalysatoren, die kan worden toegeschreven aan de niet-covalente π-π-stapelingsinteractie tussen Eosine Y, gC3 N4 en GA [48]. De PL-uitdovingsspectra van g-C3 N4 /Pt/GO-0,5% monster vertoont een gematigde intensiteit, die lager is dan de g-C3 N4 /Ni/GO-0,5% monster. Belangrijk is dat de g-C3 N4 /PtNi/GO-0,5%-monster vertoont de laagste fluorescentie-intensiteit, wat impliceert dat de cokatalysator van de PtNi-legering de meest efficiënte cokatalysator is voor het verbeteren van de efficiëntie van de ladingsscheiding dan zuiver Pt of Ni. Het resultaat is consistent met de H2-evolutieactiviteit (zie Fig. 4). Om het ladingsoverdrachtproces verder te verifiëren, zijn de tijdelijke fotostroomreacties van g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters werden gemeten en de resultaten worden getoond in Fig. 8b. De g-C3 N4 /PtNi/GO-0,5%-monster vertoont de hoogste fotostroomrespons onder bestraling met zichtbaar licht (λ > 420 nm), wat verder bevestigt dat het gebruik van een cokatalysator van een PtNi-legering essentieel is om de efficiëntie van de ladingsscheiding te verbeteren. Op basis van bovenstaande resultaten is de verbeterde H2-evolutieactiviteit voor de met eosine Y gesensibiliseerde g-C3 N4 /PtNi/GO-0,5% composiet wordt toegeschreven aan de verbeterde efficiëntie van de ladingsscheiding.
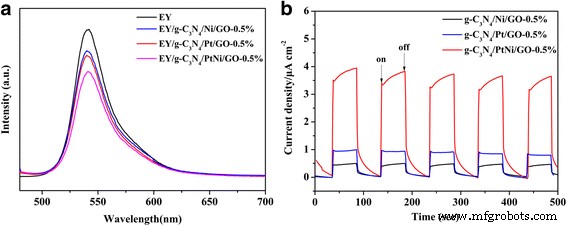
een De fotoluminescentie (PL) dovende spectra door g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters in 20% (v/v) TEOA waterige oplossing (pH = 7). Eosine Y-oplossing:0,01 mM (b ) Voorbijgaande fotostroomreacties van g-C3 N4 /Ni/GO-0,5%, g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /PtNi/GO-0,5% monsters
Volgens bovenstaande resultaten en mechanismeanalyse stellen we een schematisch diagram voor om de H2 . te begrijpen evolutieproces voor de Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO samengesteld monster (Fig. 9). Onder bestraling met zichtbaar licht worden de door foto gegenereerde elektronen in de LUMO van aangeslagen Eosine Y overgedragen naar g-C3 N4 en/of GO en vervolgens naar de cokatalysator van de PtNi-legering voor de reductie van protonen. Ondertussen zijn de foto-aangeslagen elektronen in het CB van g-C3 N4 stroom ook naar de cokatalysator van PtNi-legering voor H2 evolutie reactie. Tegelijkertijd oxideren de door foto gegenereerde gaten of geoxideerde Eosine Y-kleurstoffen het TEOA-opofferingsmiddel direct.
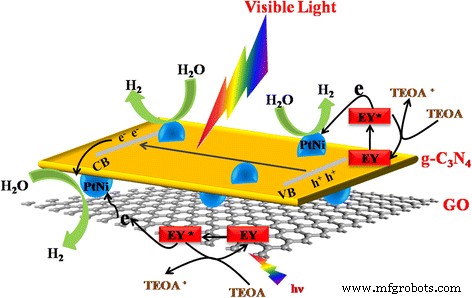
Een schematisch diagram van H2 evolutieproces voor de Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO-composietmonster onder bestraling met zichtbaar licht
Conclusie
Ternair g-C3 N4 /PtNi/GO-composiet werd gesynthetiseerd door een gemakkelijke vloeistoffase sonochemische manier te combineren met een chemische reductiemethode. De Eosine Y-gesensibiliseerde g-C3 N4 /PtNi/GO-0,5% composiet toont de hoogste waterstofontwikkelingssnelheid van 5,89 mmol g −1 h −1 , wat ongeveer 1,54 en 1178 keer hoger is dan de eosine Y-gesensibiliseerde g-C3 N4 /Pt/GO-0,5% en g-C3 N4 /Ni/GO-0,5% monsters, respectievelijk. De verbeterde fotokatalytische activiteit kan worden toegeschreven aan het positieve synergetische effect tussen Pt en Ni, evenals aan meer reactieve plaatsen, wat leidt tot een efficiënte scheiding van foto-geëxciteerde elektron-gatparen. Deze studie toont aan dat PtNi-legering kan worden gebruikt als een economische en efficiënte cokatalysator voor fotokatalytische waterstofontwikkeling.
Nanomaterialen
- MoS2 met gecontroleerde dikte voor elektrokatalytische waterstofevolutie
- S, N co-gedoteerde grafeen Quantum Dot/TiO2-composieten voor efficiënte fotokatalytische waterstofgeneratie
- Koolstofnanodots als dual-mode nanosensoren voor selectieve detectie van waterstofperoxide
- Waterstofperoxidedetectie op basis van binnenoppervlakken modificatie van vaste-stof nanoporiën
- Temperatuurafhankelijke kristallisatie van MoS2-nanovlokken op grafeen-nanobladen voor elektrokatalyse
- Hydrothermische synthese van In2O3 nanodeeltjes hybride tweeling hexagonale schijf ZnO heterostructuren voor verbeterde fotokatalytische activiteiten en stabiliteit
- Verkenning van Zr–Metal–Organic Framework als efficiënte fotokatalysator voor waterstofproductie
- Hiërarchische heterostructuur van ZnO@TiO2 holle bollen voor zeer efficiënte fotokatalytische waterstofevolutie
- Zichtbare, door licht aangedreven fotokatalytische prestaties van N-gedoteerde ZnO/g-C3N4-nanocomposieten
- Opeenvolgend door damp gegroeid hybride perovskiet voor vlakke heterojunctie zonnecellen
- Verbeterde fotokatalytische waterstofevolutie door Cd0.5Zn0.5S QD's op Ni2P poreuze nanosheets te laden



