Fotokatalytisch verbeterde kationische kleurstofverwijdering met Zn-Al gelaagde dubbele hydroxiden
Abstract
Gecalcineerde en organo-gemodificeerde Zn-Al gelaagde dubbele hydroxiden (LDH's) werden bestudeerd als adsorbentia en fotokatalysatoren voor het verwijderen van kationische kleurstoffen, namelijk methyleenblauw (MB). Zn-Al LDH's met een kationische verhouding van 2:4 werden verkregen door de coprecipitatiemethode. As-gesynthetiseerde monsters werden bij verschillende temperaturen gecalcineerd en de fasetransformaties werden onderzocht met XRD-, TG/DTG- en UV-vis-DR-methoden. De activiteit van gesynthetiseerde en gecalcineerde Zn-Al LDH's onder UV-licht werd toegeschreven aan de aanwezigheid van de ZnO-fase. De hoeveelheid ZnO in LDH's kan worden geregeld door de Zn/Al-verhouding en de verwarmingstemperatuur te variëren. De impact van de Zn/Al-verhouding op de fotokatalytische activiteit van LDH's werd overwegend waargenomen. De gecalcineerde Zn-Al LDH's vertoonden een lage adsorptie van MB. De modificatie van ZnAl LDH's door natriumdodecylsulfaat werd uitgevoerd met behulp van een reconstructiemethode. De organo/LDH-nanohybriden vertoonden een hoge adsorptiecapaciteit naar MB. De verwijdering van MB uit oplossingen met organo/Zn-Al LDH's werd verbeterd door UV-licht te gebruiken vanwege MB-fotodestructie.
Achtergrond
Het verwijderen van gevaarlijke organische kleurstoffen uit afvalwater en het saneren van verontreinigingen in oppervlaktewater, grondwater is een groot probleem in de wereld. Verschillende traditionele methoden, waaronder adsorptie, coagulatie, flocculatie, ozonisatie, membraanfiltratie, ionenuitwisseling, oxidatie en chemische precipitatie, zijn bekend voor de behandeling van kleurstofbevattende effluenten [1, 2]. Adsorptie is een goedkope techniek die geen speciale opstelling vereist. In de afgelopen jaren zijn er vele soorten adsorbentia met de katalytische functie ontwikkeld en gebruikt voor het verwijderen van nitraat, zware metalen en organische verontreinigende stoffen uit water [3,4,5].
Het gebruik van gelaagde dubbellaagse hydroxiden (LDH's) als alternatieve materialen voor het verwijderen van organische kleurstoffen uit waterige media is onderzocht [6,7,8]. LDH's staan bekend als anionogene kleien en hydrotalcietachtige materialen. Hun basisstructuur lijkt op die van bruciet, Mg(OH)2 , wanneer een breuk x van tweewaardige kationen isomorf vervangen door driewaardige kationen, waardoor positief geladen lagen ontstaan. De chemische samenstelling van LDH's wordt uitgedrukt door de algemene formule [M 2+ 1−x M 3+ x (OH)2 ][A n− ]x/n · zH2 O, waarbij M 2+ kan vaak voorkomen; Mg 2+ , Zn 2+ , of Ni 2+ , en M 3+ kan vaak voorkomen; Al 3+ , Ga 3+ , Fe 3+ , of Mn 3+ . Een niet-raamwerklading die een anorganisch of organisch anion compenseert (CO3 2− , Cl − , SO4 2− , KCO2 − ) is ondertekend als A n− ; x ligt normaal gesproken tussen 0,2−0,4. LDH-lagen krijgen een positieve lading door isomorfe substitutie van M 3+ voor M 2+ , die wordt gecompenseerd door anionen tussen de lagen en water [9].
De thermische behandeling van LDH's leidt tot het verlies van gefysisorbeerde en tussenlaagse watermoleculen, OH - groepen lagen en ladingsbalancerende anionen. De gelaagde structuur stort in en een gemengde metaaloxide vaste oplossing wordt gevormd. De gemengde oxiden bezaten typisch de grote specifieke oppervlakten, thermische stabiliteit en synergetische interacties tussen de verschillende metaalcomponenten. Daarom hebben de calcineringsproducten van LDH talloze toepassingen gevonden in verschillende katalytische processen [10,11,12].
Vanwege hun anionische uitwisselingscapaciteit zijn LDH's geschikt voor intercalatie en sorptie van anionische kleurstoffen, maar ze zijn niet van toepassing op kationische. De modificatie van het oppervlak van LDH met anionische oppervlakteactieve stoffen maakt het mogelijk om composieten te verkrijgen die verschillende soorten organische moleculen kunnen adsorberen [13, 14]. Met natriumdodecylsulfaat (DS) gemodificeerde LDH's vertoonden een extreem hoge sorptie van kationische kleurstoffen zoals safranine [15], methyleenblauw [16] en basisblauw [17].
Onlangs zijn LDH's intensief onderzocht als veelbelovende heterogene fotokatalysatoren vanwege hun intrinsieke fotoresponskenmerken, lage kosten en gemakkelijke voorbereiding en modificatie [18]. LDH's als fotokatalysatoren vertoonden een hoge energie-omzettingsefficiëntie als gevolg van de hoge dispersie van actieve soorten in een gelaagde matrix, wat de ladingsscheiding vergemakkelijkt. Gemengde oxiden met halfgeleidende eigenschappen worden verkregen door calcinering van geschikte overgangsmetaalbevattende LDH's. Een grote verscheidenheid aan metaalkationen, zoals Zn 2+ en Ti 4+ , kan in de lagen worden ingebracht [19, 20]. Hun relatieve verhoudingen kunnen binnen een groot bereik worden gevarieerd, wat de mogelijkheid biedt om halfgeleidende oxiden met instelbare eigenschappen te bereiden. Fotokatalytische toepassingen van LDH's zijn een interessant opkomend gebied. Verschillende halfgeleidende gemengde oxiden afgeleid van LDH, zoals Zn-Al [20], Zn-Ce, ZnFe, Zn-Cr [21], Mg-Zn-Al [22] en Zn-Ga [23], zijn onderzocht voor de fotokatalytische afbraak van verontreinigingen.
Naast de ongewenste kleur vertonen afbraakproducten van kleurstoffen ook een mutageen of kankerverwekkend effect op de mens en de inname ervan kan ernstige schade aan organismen veroorzaken. Chloor en hypochloorzuur, gegenereerd tijdens de afbraak, zijn sterk giftige oxidatiemiddelen. Ze kunnen organische stoffen oxideren en worden tegelijkertijd gereduceerd tot chloride [24]. Als een belangrijke basiskleurstof die wordt gebruikt voor het bedrukken van calico, het verven van katoen en leer, kan MB verschillende schadelijke effecten veroorzaken, zoals oogverbrandingen, irritatie van het maagdarmkanaal en de huid [25].
De hoge adsorptiecapaciteit van Zn-Al-tussenlagen gemodificeerd met DS voor methyleenblauw (MB) werd aangetoond [26]. De aanwezigheid van een fotoactieve component in het adsorbens kan de efficiëntie van op Zn-Al LDH gebaseerde materialen voor het verwijderen van kationische kleurstof verhogen door gebruik te maken van UV-straling. Zo werden de optimale omstandigheden voor de bereiding van Zn-Al LDH's voor de verwijdering van kationische kleurstof, zoals MB door adsorptie en fotodestructie, bepaald in het huidige werk.
Methoden
Synthese van Zn-Al LDH's
Alle chemicaliën waren van analytische kwaliteit en werden zonder verdere zuivering gebruikt. Zn-Al LDH's met carbonaat als tussenlaaganion, met [Zn]:[Al] = 1:2 werden gesynthetiseerd door middel van co-precipitatiemethode bij een constante pH vergelijkbaar met [9]. De eerste oplossing die Na2 . bevat CO3 (0,5 M) en NaOH (1,5 M) werden verkregen. De tweede oplossing met een mengsel van metaalnitraten van Zn(NO3 )2 ∙6H2 O en Al(NEE3 )3 ∙9H2 O (totale metaalconcentratie was 0,6 M, de molaire verhouding van Zn/Al 2:1, 3:1, 4:1) werd bereid en druppelsgewijs werd onder roeren verstandig aan de eerste oplossing toegevoegd. De pH werd door toevoeging van NaOH op 10 ingesteld. Nadat de toevoeging was voltooid, werd de temperatuur verhoogd tot 85 o C en de slurry werd gedurende 6 uur op deze temperatuur gehouden onder continu roeren. Daarna werd de slurry binnen enkele uren afgekoeld tot kamertemperatuur. Het product werd door filtratie geïsoleerd en verschillende keren met gedeïoniseerd water gewassen tot pH 7. Daarna werd de vaste stof gedroogd bij 100 °C. De monsters werden gelabeld als ZnAl21 LDH, ZnAl31 LDH en ZnAl41 LDH.
De hierboven gesynthetiseerde Zn-Al LDH's werden 2 uur gecalcineerd bij 450°C en 1, 2 en 5 uur bij 600°C in lucht. De monsters werden gelabeld als ZnAl21 -450, ZnAl31 -450, ZnAl41 -450, ZnAl 21 -600-1, ZnAl 31 -600-1, ZnAl 41 -600-1, ZnAl 21 -600-2, ZnAl 31 -600-2, ZnAl 41 -600-2, ZnAl 21 -600-5, ZnAl 31 -600-5, ZnAl 41 -600-5.
De Zn-Al LDH's werden gemodificeerd met natriumdodecylsulfaat CH3 (CH2 )11 SO4 Na door reconstructiemethode. De suspensies van 1 g gecalcineerde LDH's en 50 ml 0,05 M DS waterige oplossingen werden 24 uur bij kamertemperatuur geroerd. De verkregen composieten werden gelabeld als ZnAl 21 -450/DS, ZnAl 31 -450/DS, ZnAl 41 -450/DS, ZnAl 21 -600-1/DS ZnAl 31 -600-1/DS ZnAl 41 -600-1/DS.
Karakterisering
XRD-patronen van de monsters werden geregistreerd met een DRON-4-07-diffractometer (Burevestnik Inc., St. Petersburg, Rusland), (CuKα straling). De thermogravimetrische analyse (TGA) en differentiële thermische analyse (DTA) werden uitgevoerd met behulp van Derivatograph Q-1500 D-apparatuur (MOM, Hongarije) in stromende lucht met een verwarmingssnelheid van 10 ° min −1 . Diffuse reflectiespectra werden verkregen met een Lambda 35 UV-Vis (Perkin Elmer, Duitsland) spectrometer uitgerust met een integrerende Labsphere RSA-PR-20 in het bereik van golflengte 200-1000 nm. De UV-zichtbare spectra van de oplossingen werden geregistreerd met behulp van een Lambda 35 UV-Vis-spectrometer (Perkin Elmer, Duitsland).
Fotokatalytisch experiment
0,020 g Zn-Al LDH's werd gedispergeerd in 40 ml 9 × 10 -5 M (voor gecalcineerde LDH's) en 10 -4 M (voor DS-gemodificeerde LDH's) MB-waterige oplossing in de kwartsreactor. Vóór verlichting werden de suspensies 1 uur (gecalcineerde LDH's) en 24 uur (DS-gemodificeerde LDH's) in het donker geroerd om een adsorptie-desorptie-evenwicht tussen de fotokatalysator en MB-moleculen te bereiken. Vervolgens werd de oplossing 3 uur bestraald met een kwikdamplamp (λmax = 365 nm) onder magnetisch roeren. Op bepaalde tijdsintervallen werd de oplossing geanalyseerd door de absorptiespectra te meten met behulp van een UV-Vis-spectrometrie.
Resultaten en discussies
Karakterisering
Het XRD-patroon voor de gesynthetiseerde Zn-Al LDH's met de verschillende Zn 2+ /Al 3+ kationische verhouding worden weergegeven in Fig. 1a. De hydrotalciet-achtige structuur werd gevormd voor alle kationische verhoudingen. De XRD-patronen vertonen de karakteristieke reflecties die verband houden met de gelaagde dubbele hydroxiden. Een extra ZnO-fase was aanwezig in de ZnAl41 LDH zoals aangegeven door de XRD-patronen. De 2'-pieken bij 31,9 °, 34 ° en 36,2 ° behoren tot de ZnO-fase gevormd op het oppervlak van de brucietachtige platen. Alle reflecties zijn scherp en duiden op een zeer kristallijn materiaal.
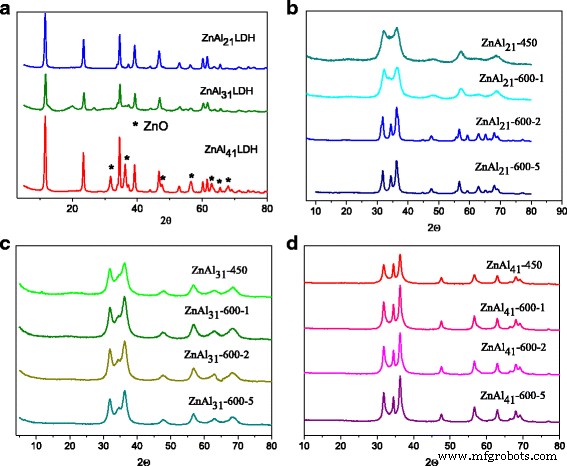
Röntgendiffractiepatronen van gesynthetiseerde Zn-Al LDH's (a ) en gecalcineerd:ZnAl21 LDH (b ), ZnAl31 LDH (c ), ZnAl41 LDH (d )
De analyse van XRD-patronen van de gecalcineerde derivaten toonde aan dat de gelaagde structuur van de oorspronkelijke LDH's volledig was vernietigd, wat suggereert dat de oorspronkelijke LDH's bijna volledig zijn afgebroken en dat de meeste tussenlaagse carbonaatanionen en water worden geëlimineerd (Fig. 1b-d). Alle reflecties konden perfect worden geïndexeerd als de hexagonale wurtzietstructuur ZnO. Geen karakteristieke reflecties die overeenkomen met Al2 O3 fasen werden waargenomen in de XRD-patronen. Opgemerkt moet worden dat de hogere kristalliniteit van ZnO werd verbeterd met een toename van Zn 2+ /Al 3+ kationische verhouding.
Het is bekend dat de hydratatie van gecalcineerde Zn-Al LDH's in waterige suspensie de reconstructie van de hydrotalcietfase veroorzaakte [9]. Het was te zien dat de gelaagde structuur werd hersteld onder hydratatie van gecalcineerde Zn-Al LDH's in waterige oplossingen van DS (Fig. 2). Het verschijnen van diffractiepatronen onder kleine hoeken bewees de aanwezigheid van DS-geïntercaleerde LDH's. Alle gereconstrueerde DS-gemodificeerde Zn-Al LDH's bevatten ook een met carbonaat geïntercaleerde fase. Het moet opmerkelijk zijn dat de volledige reconstructie van de gelaagde structuur alleen werd waargenomen voor ZnAl21 -450/DS LDH (afb. 2a). De XRD patronen van ZnAl 31 -450/DS en ZnAl 41 -450 / DS LDH's bevatten ZnO-reflecties (figuur 2a). Volgens [27] resulteerde de hydratatie van Zn-Al gemengde oxiden met Zn/Al-verhouding 1:5 in de vorming van hydrotalcietstructuur met Zn/Al = 2, ongeacht de initiële Zn/Al-verhouding. Dus, ZnAl 31 -450/DS, ZnAl 41 -450/DS LDH's bevatten een lagere hoeveelheid DS-geïntercaleerde fase. De XRD-patronen van alle DS-gemodificeerde LDH's verkregen uit Zn-Al gemengde oxiden gecalcineerd bij 600 ° C bevatten reflecties van de ZnO-fase (figuur 2b). Het is duidelijk dat de continue afgifte van Zn 2+ uit de amorfe oxidefase leidde tot vorming van meer ZnO-nanodeeltjes met toenemende calcineringstemperatuur.
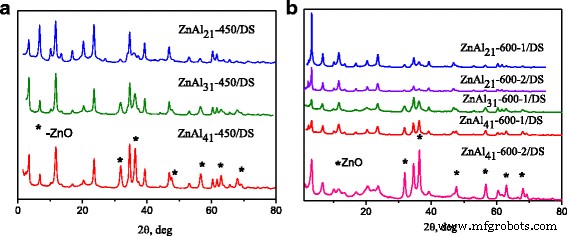
Röntgendiffractiepatronen van DS-gemodificeerde Zn-Al LDH's verkregen door reconstructie van LDH's gecalcineerd bij 450 °C (a ) en 600 °C (b )
De thermogravimetrische sporen geregistreerd voor Zn-Al LDH's waren zeer vergelijkbaar voor alle Zn/Al-verhoudingen. TG-, DTA- en DTG-curves voor de monsters met Zn/Al = 4:1 worden weergegeven in Fig. 3. De TGA-grafiek voor LDH-carbonaat (Fig. 3a) toonde het massaverlies in het temperatuurbereik van 60-190, 190-300 en 300-500 °C. Het massaverlies in de eerste stap is een algemeen kenmerk van hydrotalciet dat verband houdt met de afgifte van gefysisorbeerd en tussenlaagwater. Het tweede massaverlies werd toegeschreven aan de eerste stap van dehydroxylering en de verwijdering van carbonaationen uit de tussenlaag. Over dit temperatuurbereik onderging het hydrotalciet decarbonatatie- en dehydroxyleringsreacties, wat resulteerde in de vorming van metaaloxiden. In de derde stap van massaverlies dat optrad bij een temperatuur hoger dan 500 °C, werd het massaverlies herkend als de totale dehydroxylering en een ineenstorting van de structuur als gevolg van de verwijdering van de resterende anionen tussen de lagen [28]. Het onbeduidende massaverlies dat wordt waargenomen bij 500 - 1000 °C kan worden toegeschreven aan het verlies van sommige carbonaatanionen die sterk worden geadsorbeerd aan de kristallieten van gemengde oxiden [29].
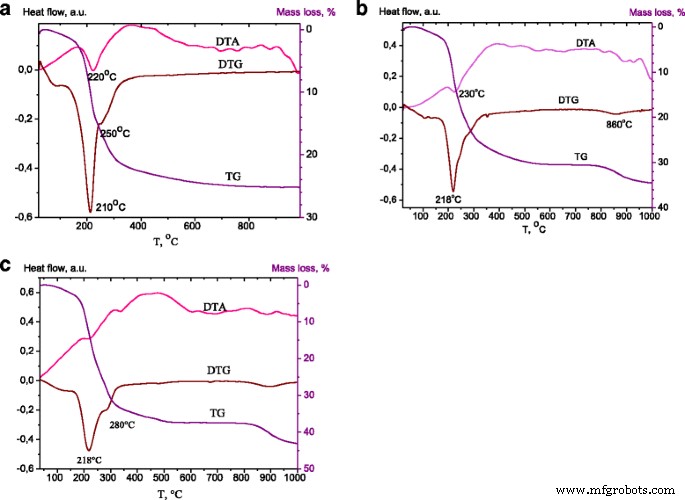
TG-, DTA- en DTG-curven van ZnAl41 LDH (een ), ZnAl41 -450/DS (b ), ZnAl41 -600-1/DS (c )
De thermische ontledingsstadia voor alle bestudeerde Zn-Al LDH's worden weergegeven in Tabel 1. Het totale massaverlies neemt af naarmate de Zn/Al-verhouding in ZnAl LDH's toeneemt, omdat de materialen met een lagere ladingsdichtheid minder carbonaatanionen bevatten. Bovendien, als ZnAl31 LDH en ZnAl41 LDH bevatte de fase van ZnO, hoe minder metaalhydroxiden en carbonaationen tussen de lagen in de monsters aanwezig waren. Dus de processen van dehydroxylering en decarboxylering voor ZnAl31 LDH en ZnAl41 LDH waren niet zo intensief als voor ZnAl21 LDH.
De thermogravimetrische sporen geregistreerd voor ZnAl41 -450/DS gepresenteerd in Fig. 3b. De eerste stap van de thermische ontleding werd toegeschreven aan het verlies van tussenlaagwater. De tweede ontledingsstap, de dehydroxylering van de brucietachtige platen, ging gepaard met DS-vernietiging. De ontleding van DS-ionen vond plaats in het bereik van 210-250 ° C [30, 31] en daarom werd een groter verlies waargenomen onder 200 ° C. Het massaverlies van DS-gemodificeerde LDH's bij 300-500 ° C werd toegeschreven aan de totale dehydroxylering en de ineenstorting van de gelaagde structuur. De toename van het massaverlies in deze fase was het gevolg van het laden van DS, waarvan de ontbinding werd weerspiegeld door het massaverlies in 400-900 ° C. Het massaverlies tussen 800-900 °C kan worden herkend als SO3 evolutie door de ontleding van (Zn, Al)sulfaat gevormd door ontleding van DS tijdens de tweede massaverliesfase [32].
De totale massaverliezen voor ZnAl31 -450/DS en ZnAl41 -450/DS waren minder in vergelijking met ZnAl21 -450/DS wees op het lagere gehalte aan DS-geïntercaleerde fasen in de monsters met een Zn/Al-verhouding van 3:1 en 4:1. De aanwezigheid van ZnO-reflecties in de patronen van deze LDH's duidde op de onvolledige reconstructie van LDH onder rehydratatie van gemengde dubbele oxiden in een waterige oplossing van DS (figuur 2a). Volgens [33] bestaan de extra fasen naast elkaar in de LDH's. De gesynthetiseerde en gerehydrateerde Zn-Al LDH's (Zn:Al = 2:1) bevatten ongeveer 25 en 23 gew.% van een amorfe fase [33]. De auteurs ontdekten dat de gerehydrateerde monsters nog ongeveer 3 gew.% bevatten. % ZnO-fase (zinkiet) was het gevolg van de segregatie van Zn uit de brucietachtige lagen. Waarschijnlijk de wijziging van ZnAl21 LDH's met DS veroorzaakten de extra vorming van de amorfe zinkhydroxidefase. Zoals gesuggereerd in [27], was er een voorlopige reactie van rehydratatie in een vroeg stadium van de reconstructie van de amorfe zinkhydroxidefase en vervolgens een rehydratatie van de Zn-Al-oxiden tijdens het reconstructieproces. Mogelijk resulteerde de rehydratatie van de amorfe fase in de vorming van een met carbonaat geïntercaleerde fase. De rehydratatie van Zn-Al-oxiden in DS-oplossingen veroorzaakte de vorming van DS-geïntercaleerde fase. De massaverliezen voor ZnAl21 -600-1/DS, ZnAl31 -600-1/DS, ZnAl41 -600-1/DS waren niet significant verschillend. Het is duidelijk dat Zn-Al LDH's gecalcineerd bij 600 °C minder amorfe fase bevatten.
De aanwezigheid van fotoactief ZnO breidt het toepassingsgebied voor LDH's en LDH-gebaseerde composieten uit, met name als fotokatalysatoren, UV-filters en kleurstofgevoelige zonnecellen. Het effect van fasetransformaties op het vermogen van Zn-Al LDH's om UV-licht te absorberen werd onderzocht. De optische absorptiespectra van gesynthetiseerde Zn-Al LDH's, gecalcineerde Zn-Al LDH's en DS gemodificeerde Zn-Al LDH's voor monsters met Zn:Al =2:1 worden getoond in Fig. 4a, b. De reconstructie van gemengde oxiden gecalcineerd bij 450 en bij 600 ° C gedurende 1 uur bevorderde de vorming van een extra hoeveelheid kristallijn ZnO resulterend in de rode verschuiving van de absorptieband van ZnAl21 -450/DS en ZnAl21 -600-1/DS (afb. 4a, b). De absorptieband van ZnAl21 -600-2 werd verschoven naar zichtbaar licht met ongeveer 35 nm. Er was geen verandering in de absorptie van gemengde oxiden met Zn:Al = 2:1 verkregen door 5 uur calcineren van LDH (Fig. 4b).
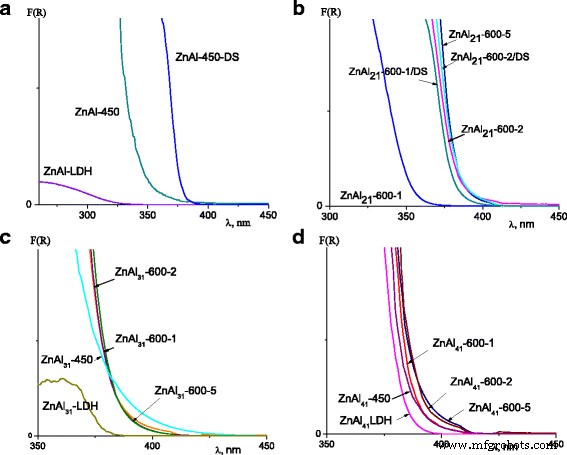
UV-Vis-spectra van Zn-Al LDH's met Zn/Al-verhouding:2:1 (a , b ), 3:1 (c ), 4:1 (d )
De positie van de absorptieband van gemengde oxiden met Zn:Al = 3:1 was bijna gelijk voor de bij 450 en 600 °C behandelde monsters en was onafhankelijk van de duur van de thermische behandeling (Fig. 4c). Voor Zn-Al LDH's en gemengde oxiden met Zn:Al = 4:1 waren de absorptiebanden gelegen op 382-390 nm (Fig. 4d).
Sinds Al2 O3 is een materiaal met een brede bandafstand (5,55 eV), de absorptie van licht in het UV-bereik veroorzaakt door ZnO dat in de monsters wordt gepresenteerd, waarvan de bandafstand 3,37 eV is [34]. De waarden van band gap-energie (Eg ) van de monsters werden berekend op basis van het snijpunt van UV–vis-spectra met behulp van de vergelijking:Eg = 1240/λ [35] (Tabel 3). Onder gecalcineerde Zn-Al LDH's werd de laagste waarde van bandafstand-energie waargenomen voor het monster met het hoogste Zn-gehalte (tabel 3).
Fotokatalytische studie
Om de fotokatalytische prestatie van Zn-Al LDH's te evalueren, is de afbraak van waterige 2*10 -5 M MB-oplossing onder UV-licht werd uitgevoerd. Het slechte lichtabsorptievermogen van LDH's met een Zn/Al-verhouding van 2:1 en 3:1 veroorzaakte een lage activiteit bij bestraling (tabel 2).
ZnO-bevat ZnAl41 LDH's onder de andere LDH's vertoonden de hogere fotokatalytische activiteit bij de vernietiging van MB. De fotokatalytische activiteit was sterk verbeterd wanneer monsters werden gecalcineerd bij 450 en 600 ° C vanwege de grotere hoeveelheden gevormde ZnO-fase. De MB-fotodegradatiecurves voor Zn-Al LDH's gecalcineerd bij 600 ° C worden weergegeven in Fig. 5a. Aangezien het verschil in fotokatalytische prestatie van gecalcineerde Zn-Al LDH's werd veroorzaakt door de ZnO-fase, vertoonden de LDH's met een Zn/Al-verhouding van 4:1 de beste resultaten bij MB-fotodestructie.
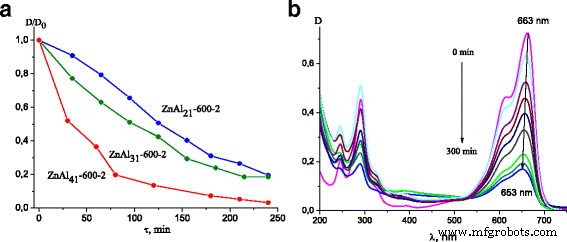
Afbraakcurven van MB over gecalcineerde Zn-Al LDH's onder bestraling met UV-licht (a ); Absorptieveranderingen van 2*10 -5 M MB-oplossing tijdens het fotodegradatieproces over ZnAl31 -600-1 (b )
De veranderingen in de absorptiespectra van MB-oplossing gedurende verschillende bestralingstijd in aanwezigheid van ZnAl31 -600-1 is te zien in figuur 5b. De pieken bij 610 en 663 nm werden toegeschreven aan de absorptie van het geconjugeerde π-systeem, terwijl de pieken dichtbij 300 nm werden toegewezen aan de absorptie van de aromatische ring [36]. Men kon zien dat de intensiteit van de oorspronkelijke pieken afnam met de toename van de bestralingstijd. Bovendien kon ook een parallelle afname van de intensiteit en een lichte blauwverschuiving van de banden op 663 nm worden waargenomen. Het werd veroorzaakt door de N-demethylering van het fenothiazine en de gelijktijdige afbraak ervan [37]. De vergelijkbare veranderingen in optische absorptiespectra van MB werden waargenomen voor fotokatalytische systemen met alle LDH's.
DS-modificatie van Zn-Al LDH's verhoogde de affiniteit voor MB vanwege hydrofobe interacties tussen de oppervlakteactieve stoffen en kleurstofmoleculen [26]. ZnAl41 -600-1/DS toonde het beste resultaat op MB-adsorptie (tabel 3). De fotokatalytische activiteit van organo / Zn-Al LDH's was vergelijkbaar met gecalcineerde Zn-Al LDH's (tabel 3). Het hogere niveau van MB-degradatie werd waargenomen voor de ZnAl41 -450/DS. De waarden van verwijdering van MB met DS-gemodificeerde Zn-Al LDH's door adsorptie waren hoger dan die van fotodestructie. De adsorptieverwijdering van MB met organo/Zn-Al LDH's zou dus kunnen worden verbeterd door lichtbestraling toe te passen.
Waarschijnlijk heeft de fotodestructie van kleurstof plaatsgevonden op het oppervlak van met DS gemodificeerde Zn-Al LDH's die niet onder de experimentele omstandigheden waren gefixeerd. Na het bereiken van het evenwicht hadden de DS-gemodificeerde Zn-Al LDH's met geadsorbeerd MB een intensieve blauwe kleur.
Conclusies
In dit werk werden de gesynthetiseerde en gecalcineerde Zn-Al LDH's met verschillende kationische verhoudingen bereid. De verkregen materialen werden gekarakteriseerd en gebruikt voor het verwijderen van kationische kleurstof MB uit waterige oplossingen. De onderzoeken naar MB-fotodestructie onder UV-licht over zowel LDH's als gecalcineerde LDH's geven aan dat:
De fotokatalytische activiteit van Zn-Al LDH's was afkomstig van de aanwezigheid van de ZnO-fase. De vorming van de ZnO-fase in LDH's zou kunnen worden gereguleerd door de toename van de Zn/Al-verhouding in LDH's en door de temperatuurbehandeling van LDH's.
De invloed van de Zn/Al-verhouding op de fotokatalytische activiteit van LDH's was overheersend. De fotodegradatie van MB in het heden van het gesynthetiseerde ZnAl41 LDH en ZnAl41 LDH bij 600 ° C was respectievelijk 72 en 95%. Voor gecalcineerd bij 600 °C ZnAl31 LDH en ZnAl21 LDH, de fotodegradatie van MB was respectievelijk 76 en 74%.
De organo/Zn-Al LDH's vertoonden een hoge adsorptiecapaciteit aan kationische kleurstof MB. Ze demonstreerden ook de fotokatalytische activiteiten bij de vernietiging van MB. Daarom zou de adsorptieverwijdering van MB uit oplossingen met DS-gemodificeerde Zn-Al LDH's kunnen worden verbeterd door gebruik te maken van UV-straling.
Nanomaterialen
- Fotokatalytische activiteiten verbeterd door Au-plasmonische nanodeeltjes op TiO2-nanobuisjesfoto-elektrode gecoat met MoO3
- Een nieuwe Bi4Ti3O12/Ag3PO4 heterojunctie-fotokatalysator met verbeterde fotokatalytische prestaties
- synergetische effecten van Ag-nanodeeltjes/BiV1-xMoxO4 met verbeterde fotokatalytische activiteit
- Nieuwe inzichten in CO2-adsorptie op op gelaagde dubbele hydroxide (LDH) gebaseerde nanomaterialen
- Verbeterde energieconversie-efficiëntie van perovskiet-zonnecellen met een up-conversiemateriaal van Er3+-Yb3+-Li+ tri-gedoteerde TiO2
- Verwijdering van antibiotica uit water met een koolstofvrij 3D-nanofiltratiemembraan
- Verbeterde energetische prestaties op basis van integratie met de Al/PTFE-nanolaminaten
- Verbeterde fotovoltaïsche eigenschappen in Sb2S3 vlakke heterojunctie zonnecel met een snelle selenyleringsbenadering
- Fotovoltaïsche prestaties van Pin Junction Nanocone Array-zonnecellen met verbeterde effectieve optische absorptie
- De extreem verbeterde fotostroomrespons in topologische isolator-nanoplaten met hoge geleiding
- Hiërarchische structuur kaoliniet nanosferen met opmerkelijk verbeterde adsorptie-eigenschappen voor methyleenblauw



