Veelkleurige emitterende N-gedoteerde koolstofstippen afgeleid van ascorbinezuur en fenyleendiamine-precursoren
Abstract
In dit onderzoek rapporteren we de groene, blauwe en oranje kleur emitterende N-gedoteerde koolstofstippen (CD's), die worden gesynthetiseerd uit ascorbinezuur en o -/m -/p -fenyleendiamine (o -PDA, m -PDA, en p -PDA, respectievelijk). De effecten van de polariteit van het oplosmiddel en de pH van de oplossing op de PL-emissie-eigenschappen van de gesynthetiseerde CD's zijn systematisch onderzocht. Er is waargenomen dat de PL-emissie van de gesynthetiseerde CD's afneemt met de toename van de oplosmiddelpolariteit als gevolg van de grotere agglomeratie. De oppervlaktelading van CD's vertoont ook prominente effecten op de pH-afhankelijke PL-emissie-eigenschappen.
Inleiding
Onlangs hebben fluorescerende koolstofpunten (CD's) veel aandacht getrokken vanwege hun hoge kwantumopbrengsten, lage toxiciteit, uitstekende biocompatibiliteit en gemakkelijke voorbereidingsprocedures [1,2,3,4]. Cd's kunnen op grote schaal worden gebruikt in detectie-, weergave- en bio-imaging-toepassingen. De meeste cd's zenden uit in een blauw of groen gebied dat hun toepassing in beeldvorming van levend weefsel beperkt, aangezien dit proces diepe penetratie van licht en verwijdering van autofluorescentie vereist, evenals beperkingen die verband houden met achtergrondlichtverstrooiing. Voortaan is de synthese van cd's die op grotere golflengten uitzenden belangrijk geworden. In dit opzicht is de groene chemische synthese van meerkleurige emitterende cd's belangrijk om de bijbehorende synthetische gevaren en kritische scheidingsstappen uit te sluiten [5].
Aanpassing van het oppervlak van cd's door het doteren van heteroatomen, zoals stikstof (N), boor (B) en zwavel (S) atomen, kan worden gebruikt om de fluorescentie-eigenschappen van cd's te wijzigen. Voor dit doel kunnen organische/anorganische moleculen met heteroatoomfunctionaliteiten worden gebruikt als co-precursor samen met de koolstofbron of als precursor [6,7,8]. Fenyleendiamine-isomeren [o -fenyleendiamine (o -PDA), m -fenyleendiamine (m -PDA), en p -fenyleendiamine (p -PDA)], met amine (–NH2 ) functionaliteiten, hebben bewezen een efficiënte heteroatoombron te zijn voor de synthese van N-gedoteerde CD's [3, 9, 10].
In dit werk werden de groene, blauwe en oranje kleur emitterende N-gedoteerde cd's met succes gesynthetiseerd uit hydrothermische behandeling van ascorbinezuur (AA) en individuele m -PDA, o -PDA, en p -PDA, respectievelijk (Am -, Ao -, en Ap -CD's, respectievelijk). De effecten van de reactieomstandigheden en oplosmiddelen en de pH van de oplossing op de fluorescentie-eigenschappen van elk type CD's werden systematisch onderzocht. In het bijzonder groene kleur emitterende cd's gesynthetiseerd uit ascorbinezuur en m -PDA vertoonde een zeer hoge kwantumopbrengst (QY) in het ethanoloplosmiddel.
Experimentele methoden
Gedetailleerde informatie over de materialen en instrumentele analyse wordt beschreven in Aanvullend bestand 1:sectie S1 en S2.
Synthese van Am -, Ao -, en Ap -CD's
Am . voorbereiden -CD's, ascorbinezuur (0,1 M, 0,8 mL) en m -fenyleendiamine (0,1 M, 0,8 ml) (verhouding van AA:m -PDA = 1:1) werden toegevoegd aan 10,4 ml gedeïoniseerd water en gedurende 5 minuten geroerd. Vervolgens werd het mengsel overgebracht in een met Teflon beklede autoclaaf van 50 ml en gedurende 6 uur in een oven verwarmd en op 160 °C gehouden voor verdere reactie. Na afkoeling tot kamertemperatuur (RT), zal de Am -CD's werden verzameld na verwijdering van de gesuspendeerde deeltjes via centrifugatie bij 10.000 tpm gedurende 20 minuten en verder gezuiverd door een dialysebuis gedurende 6 uur om de resterende chemicaliën te verwijderen. De zoals verkregen Am -CD's-oplossing is bewaard bij 4 °C voor verdere karakterisering.
Ao . voorbereiden -CD's en Ap -CD's, alle experimentele procedures waren hetzelfde als die van Am -CD's, behalve de voorloperverhouding. Voor Ao -CD's, ascorbinezuur (0,1 M, 1,2 mL) en o -fenyleendiamine (0,1 M, 0,8 ml) (verhouding van AA:o -PDA = 3:2) werden gebruikt; en voor Ap -CD's, ascorbinezuur (0,1 M, 0,8 mL) en p -fenyleendiamine (0,1 M, 0,4 ml) (verhouding van AA:p -PDA = 2:1) werden respectievelijk gebruikt.
Aanvullend bestand 1:Fig. S1 laat zien dat de reactietemperatuur en de voorloperverhouding werden geoptimaliseerd om de hoogste fluorescentie voor elke cd te verkrijgen.
Figuur 1 laat zien dat de emissie-intensiteit en golflengte van de gesynthetiseerde cd's totaal verschillen van die van de voorlopermaterialen. De algemene vergelijking is samengevat in Aanvullend bestand 1:Tabel S1. Het is interessant op te merken dat groen uitstralende Am -CD's kunnen worden verkregen van cyaan en blauw emitterende AA en m -PDA, terwijl blauwe kleur Ao . uitstraalt -CD's kunnen worden verkregen van cyaan en geel emitterende AA en o -PDA, die de nieuwe geconjugeerde structuur aangeeft die is gevormd door de reactie tussen AA en PDA's.
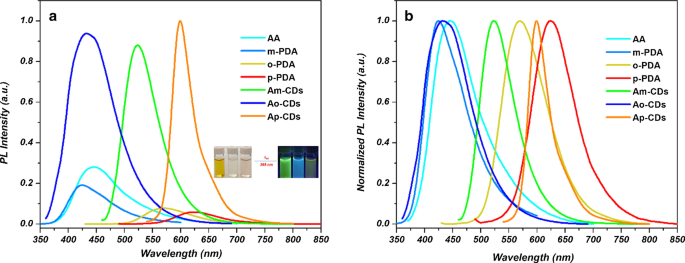
een Fluorescentiespectra, en b genormaliseerde fluorescentiespectra van Ax -CD's en diverse voorlopermaterialen. Inzet:foto's van Am -CD's, Ao -CD's en Ap -CD's verspreid in water onder natuurlijk licht (links) en onder UV-straling (λ ex = 365 nm) (rechts)
Kwantumopbrengstmeting
De kwantumopbrengsten (QY's) van de Am -, Ao -, en Ap -CD's werden verkregen door een bekende relatieve hellingsmethode bij kamertemperatuur met behulp van verschillende kleurstoffen die overeenkomen met hun emissies met die van elke CD [9]. Voor Am -CD's (excitatiegolflengte van 450 nm), Rhodamine 101 in ethanol (QY = 100%) werd als referentie gekozen; voor Ao -CD's (excitatiegolflengte van 360 nm), kininesulfaat (QS) in 0,1 M zwavelzuuroplossing (QY = 54%); en voor Ap -CD's (excitatiegolflengte van 514 nm), rhodamine B in water (QY = 31%).
Om de QY's te berekenen, werden de geïntegreerde PL-intensiteiten van het monster en de referentie uitgezet tegen de absorptie bij verschillende concentraties, en de gradiënten werden verkregen en vergeleken.
De QY's van de drie cd's werden verkregen met de volgende vergelijking:
$$\Phi_{{\text{s}}} =\Phi_{{\text{r}}} *\frac{{K_{{\text{s}}} }}{{K_{{\text{ r}}} }}*\frac{{\eta_{{\text{s}}} }}{{\eta_{{\text{r}}} }}$$ (1)waarbij Φ de relatieve kwantumopbrengst is, K is de helling van de gepaste lijn, en η is de brekingsindex van het oplosmiddel. Het subscript "r" verwijst naar de verwijzing en "s" naar het voorbeeld. De waarden van de brekingsindex voor water en ethanol zijn respectievelijk 1,33 en 1,36.
Resultaten en discussie
Karakterisering van de As-Synthesized CD's
De morfologie en grootte van de Ax -CD's (x = m , o , en p ) werden geanalyseerd op basis van TEM-afbeeldingen. Figuren 2, 3 en 4 laten zien dat de gemiddelde diameters van Am -CD's, Ao -CD's en Ap -CD's waren respectievelijk 3,39 nm, 3,65 nm en 4,45 nm. De interplanaire afstanden van Ax -CD's waren respectievelijk 0,23 nm, 0,21 nm en 0,35 nm geanalyseerd op basis van HR-TEM-beelden, die overeenkomen met de (100) en (002) vlakken van grafietkoolstof [11].
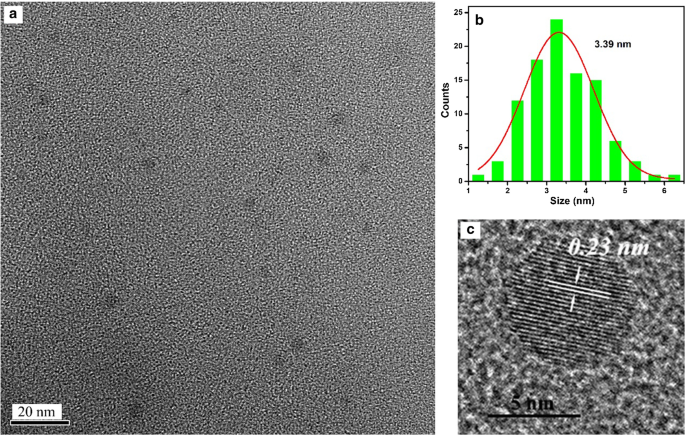
een TEM-afbeeldingen van Am -CD's, b de histogrammen van de deeltjesgrootteverdeling, en c HR-TEM-beelden
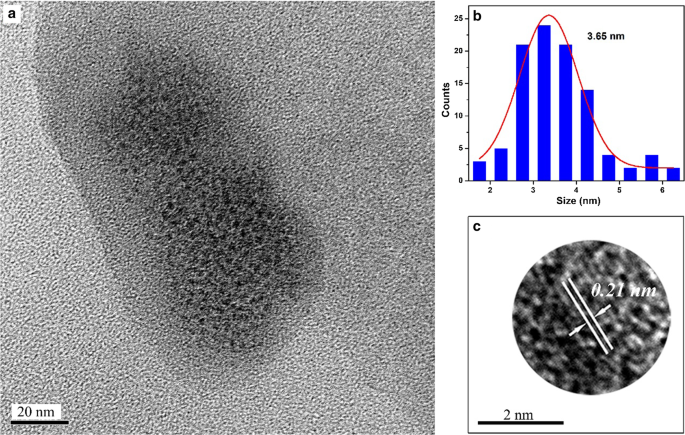
een TEM-afbeeldingen van Ao -CD's, b de histogrammen van de deeltjesgrootteverdeling, en c HR-TEM-beelden
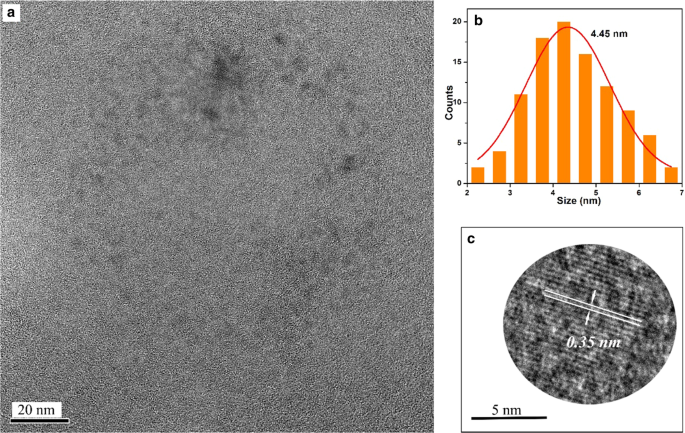
een TEM-afbeeldingen van Ap -CD's, b de histogrammen van de deeltjesgrootteverdeling, en c HR-TEM-beelden
De kristalstructuren van de Ax -CD's werden onderzocht door XRD. Afbeelding 5a laat zien dat de drie cd's een brede enkele diffractiepiek hebben rond de 2θ = 21°–23°, die afkomstig is van de grafiet-koolstofstructuur [3, 12].
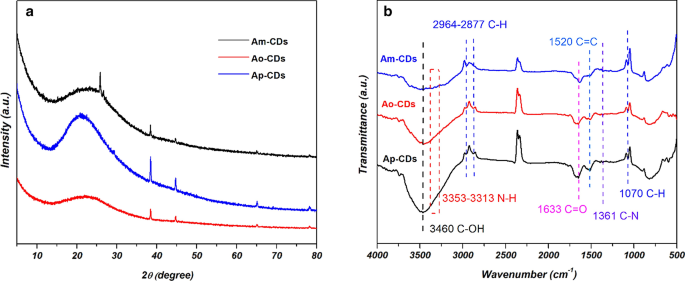
een XRD-patronen, en b FTIR-spectra van Ax -CD's
De chemische bindingen en functionele oppervlaktegroepen van Ax -CD's werden geanalyseerd met FT-IR-spectra. Afbeelding 5b toont de pieken bij ~ 3460 en ~ 3313–3353 cm −1 dat kan worden toegeschreven aan de strekkende trillingen van respectievelijk O-H en N-H. De aanwezigheid van hydrofiele groepen kan de oplosbaarheid van CD's in polair oplosmiddel verbeteren door de vorming van waterstofbindingen [13, 14]. De pieken bij ~ 1070, ~ 2877 en ~ 2964 cm −1 kunnen worden toegeschreven aan de strektrillingen van C–H [8]. De sterke piek waargenomen bij ~ 1633 cm −1 kan worden toegeschreven aan de rektrilling van de C=O-binding in de amidegroep, wat de amideringsreactie tussen de carbonzuren van AA en aminen van PDA's bevestigt [15]. De pieken die verschijnen op ~ 1520 cm −1 kan ontstaan door de buigtrilling van C=C [16]. Bovendien zijn de pieken waargenomen bij ~ 1361 cm −1 kan worden toegeschreven aan de rektrilling van C-N, wat de aanwezigheid van een stikstofatoom in de gesynthetiseerde cd's bevestigt [10]. De bijna identiteit van de FT-IR-spectra van alle drie de cd's duidt op de aanwezigheid van vergelijkbare chemische bindingen en functionele groepen op de cd's, ongeacht de positie van de aminegroep in PDA-isomerensoorten.
XPS werd gebruikt om de elementaire samenstelling en functionele groepen van de Ax . te analyseren -CD's. Afbeelding 6a toont het XPS-onderzoeksspectrum van Am -CD's, die het bestaan van C-, O- en N-atomen in het gesynthetiseerde Am aangeven -CD's. Aanvullend bestand 1:Afb. S2 en S3 laten zien dat de drie cd's vergelijkbare elementaire samenstellingen hebben, zoals samengevat in tabel 1. De XPS-analyses geven ook vergelijkbare oxidatietoestand en functionaliteiten in de drie cd's aan. Afbeelding 6 en aanvullend bestand 1:Afb. S2 en S3 tonen de hoge resolutie C1s XPS-spectra voor Ax -CD's, die laten zien dat koolstof kan worden gedeconvolueerd in verschillende pieken gecentreerd op ~ 284.0, ~ 285.2, ~ 286.9 en ~ 290.1 eV, die overeenkomen met C=C, C–C, C–O en N–C=O groepen resp. De O1s-spectra met hoge resolutie kunnen worden gedeconvolueerd in pieken die worden weergegeven bij ~ 531.8 en ~ 532.8 eV die kunnen worden toegeschreven aan respectievelijk C=O- en C-O-groepen [17]. De N1s spectra onthullen de aanwezigheid van N–H, C–N–C en grafitische N-groepen weergegeven bij respectievelijk ~ 399.0, ~ 400,0 en ~ 401.4 eV [18].
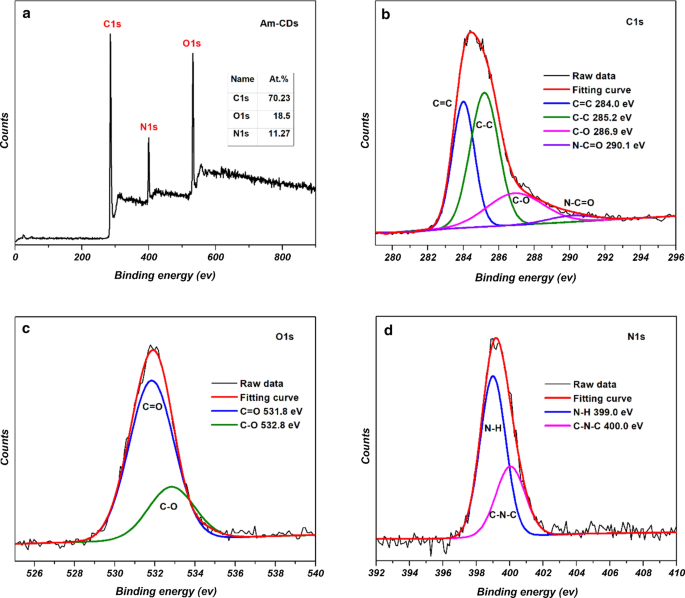
een XPS-onderzoeksspectrum van Am -CD's. De hoge resolutie b C1s , c O1s , en d N1s XPS-spectra van Am -CD's
Optische eigenschappen van de Ax -CD's
De optische eigenschappen van de Ax -CD's werden onderzocht door de UV-Vis-absorptie en PL-spectra. Afbeelding 7 toont de UV–Vis-absorptie, fotoluminescentie-excitatie (PLE) en PL-spectra van de Ax -CD's. Twee absorptiepieken gecentreerd op 289 en 400 nm worden waargenomen in de UV–Vis-absorptie van Am -CD's (Fig. 7a), die overeenkomen met de π –π * overgangen van de C=C structuur, en de n –π * overgangen van C=O groepen [15]. Ao -CD's en Ap -CD's vertoonden twee pieken in de UV-Vis-spectra, maar de piekposities en intensiteiten waren verschillend (Fig. 7c, e). Dit verschil kan worden toegeschreven aan de verschillende mate van elektronische overgangen. Bovendien kan de extra brede absorptiepiek bij ~ 510 nm worden toegeschreven aan de oppervlakteabsorptie van de Ap -CD's en successieve excitatie van de PL-emissie [19]. Dienovereenkomstig zijn de PLE- en PL-spectra verschillend voor alle drie de Ax -CD's. De Am -CD's vertonen emissie in het groene gebied bij 521 nm wanneer ze worden geëxciteerd bij 450 nm. De Ao -CD's en Ap -CD's vertonen excitatiepieken bij 360 en 580 nm en zenden uit in respectievelijk het blauwe gebied bij 432 nm en het oranje gebied bij 596 nm.
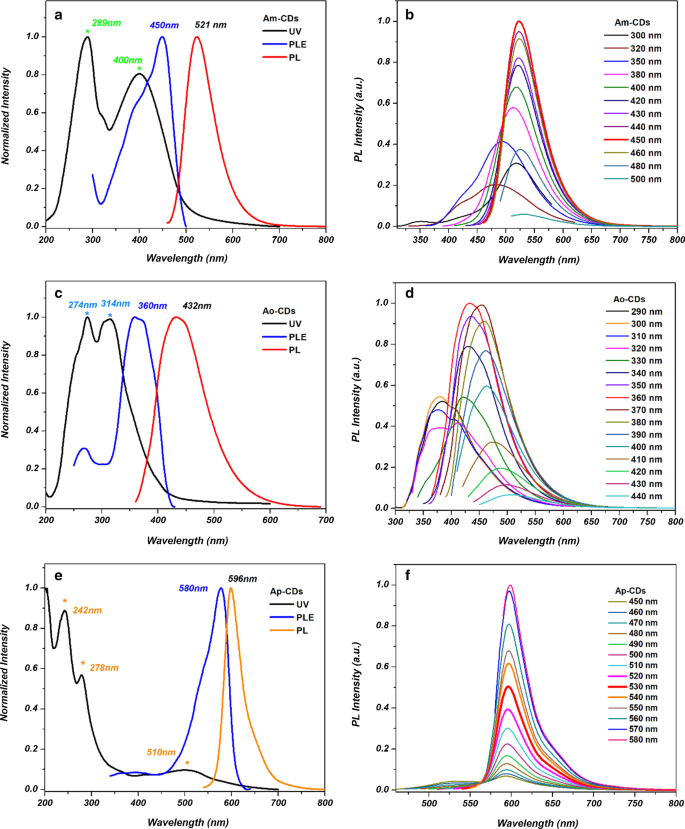
De genormaliseerde UV–Vis-absorptiespectra, PL-excitatie- en PL-emissiespectra van de a Am -CD's, c Ao -CD's en e Ap -CD's. De genormaliseerde PL-emissiespectra van de b Am -CD's, d Ao -CD's en f Ap -CD's bij verschillende excitatiegolflengten
Figuren 7b, d, f laten zien dat Am - en Ao -CD's vertonen excitatie-afhankelijke emissie terwijl Ap -CD's vertonen excitatie-onafhankelijke emissie. Het excitatiegolflengteafhankelijke PL-emissiegedrag kan afkomstig zijn van de niet-uniforme CD's-grootte en de aanwezigheid van verschillende oppervlaktedefecten en verschillende functionele oppervlaktegroepen in de CD's [20, 21]. Het excitatiegolflengte-onafhankelijke PL-emissiegedrag van Ap -CD's geven uniforme emissietoestanden aan, die ook resulteren in een smalle emissiebreedte. De verschillende excitatiegolflengte-gerelateerde PL-eigenschappen onder de Ax -CD's impliceren de verschillende energietoestanden en hun morfologie [22, 23].
Oplosmiddeleffecten en QY op de PL-emissie-eigenschappen
De effecten van oplosmiddel, inclusief gedeïoniseerd water (H2 O), Methanol (MeOH), Ethanol (EtOH), Isopropylalcohol (IPA), Aceton (ACE), Acetonitril (ACN), N ,N -Dimethylformamide (DMF) en dimethylsulfoxide (DMSO) op de PL-emissie-eigenschappen van de Ax -CD's werden onderzocht. Aanvullend bestand 1:Fig. S4 laat zien dat de PL-emissiegolflengte verandert bij verschillende oplosmiddelen. Dit toont de typische solvatochrome eigenschappen van cd's die worden veroorzaakt door de interactie tussen functionele oppervlaktegroepen van cd's en oplosmiddelen [21, 24].
Aanvullend bestand 1:Afb. S5 laat zien dat de Am -CD's bezaten de hoogste QY van de drie CD's. Bovendien is de Ax -CD's in ethanoloplosmiddel vertonen een hogere QY dan die in water, wat kan worden verklaard door (1) hogere mate van agglomeratie van CD's in hoog polair oplosmiddel, (2) verhoogde snelheid van niet-stralingsverval tijdens de interactie tussen zeer polair oplosmiddel en CD's, en (3) door water geïnduceerde morfologische verandering [25].
pH-effecten op de fluorescentie-emissie van Ax -CD's
De PL-emissie-intensiteiten van de voorbereide Am -, Ao -, en Ap -CD's werden gecontroleerd bij verschillende pH-omstandigheden. Afbeelding 8 laat zien dat Am - en Ao -CD's vertonen een vergelijkbaar PL-emissiegedrag als de pH van de oplossing verandert. De afname van de PL-emissie naarmate de pH toeneemt, kan worden toegeschreven aan de deprotonering van de functionele oppervlaktegroepen van de Am - en Ao -CD's, resulterend in de agglomeratie van CD's [26,27,28,29].
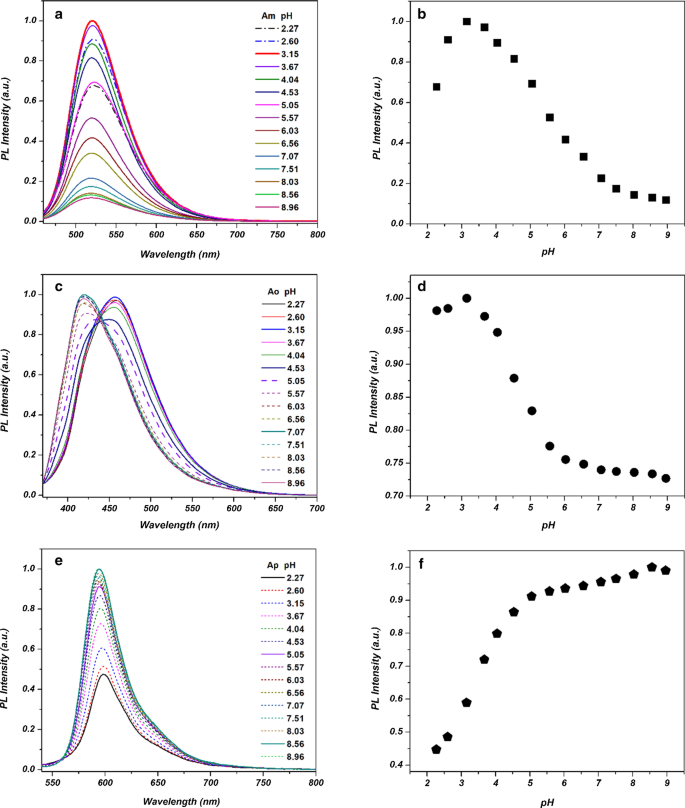
PL-emissie en intensiteitsverandering van a , b Am -CD's, c , d Ao -CD's en e , v Ap -CD's onder verschillende pH-omstandigheden
Aan de andere kant, voor Ap -CD's, de PL-intensiteit neemt toe naarmate de pH van de oplossing toeneemt. Dit fenomeen kan worden toegeschreven aan de verschillende oppervlaktelading van Ap -CD's van de andere CD's.
Om de verschillende pH-afhankelijke gedragingen tussen Ax . te onderzoeken -CD's, de zeta-potentiaal werd gevolgd bij verschillende pH-waarden. Zoals weergegeven in Fig. 9 zijn de zeta-potentialen van de Am - en Ao -CD's namen geleidelijk af met toenemende pH, terwijl de zeta-potentiaal van Ap -CD's namen toe met toenemende pH. Dit kan resulteren in minder agglomeratie en een verhoogde PL-intensiteit van Ap -CD's [30, 31].
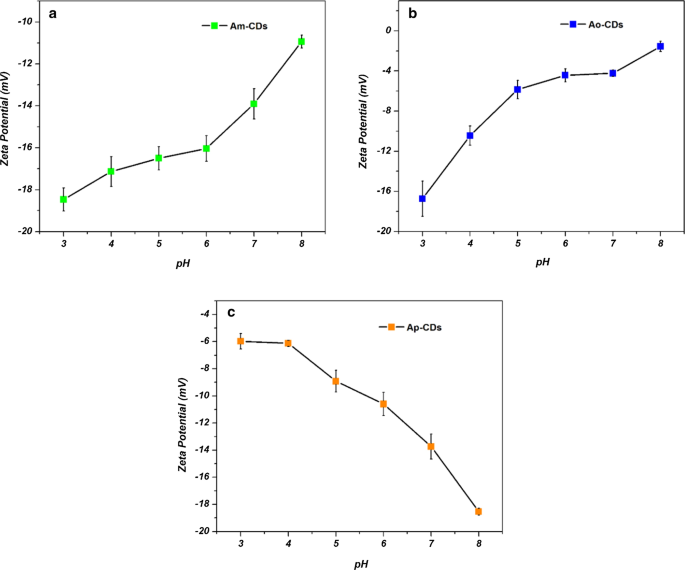
Zeta-potentieel van a Am -CD's, b Ao -CD's en c Ap -CD's onder verschillende pH-waarden, respectievelijk
Conclusie
In dit werk zijn de groene, blauwe en oranje kleur emitterende N-gedoteerde cd's met succes gesynthetiseerd uit de reactie tussen ascorbinezuur (AA) en m -PDA, o -PDA, en p -PDA, respectievelijk. Voor dit doel is een eenvoudige hydrothermische synthesemethode bij lage temperatuur gebruikt. De fotofysische en optische eigenschappen van de drie CD's zijn grondig onderzocht bij verschillende oplosmiddelen en pH. De as-synthesized Ax -CD's vertoonden hogere QY's in ethanol dan die in water. De kleinere agglomeratie, de verminderde snelheid van niet-stralingsverval en de kleinere morfologische verandering van CD's kunnen de reden zijn achter dergelijk gedrag. Bovendien is de oppervlaktelading van gesynthetiseerde Ax -CD's resulteerden in verschillende pH-afhankelijke PL-emissie-eigenschappen. Deze unieke eigenschappen van de gesynthetiseerde cd's maken hun toepassingen op verschillende gebieden van beeldvorming en detectie mogelijk.
Beschikbaarheid van gegevens en materialen
Alle gegevens die tijdens dit onderzoek zijn gegenereerd of geanalyseerd, zijn opgenomen in dit artikel en de aanvullende informatiebestanden.
Afkortingen
- CD's:
-
Koolstofstippen
- AA:
-
Ascorbinezuur
- m -PDA:
-
m -Fenyleendiamine
- o -PDA:
-
o -Fenyleendiamine
- p -PDA:
-
p -Fenyleendiamine
- Ax -CD's:
-
x = m , o , En p
- QY:
-
Kwantumopbrengst
- SI:
-
Aanvullende informatie
- RT:
-
Kamertemperatuur
- QS:
-
Kininesulfaat
- PLE:
-
Fotoluminescentie-excitatie
- H2 O:
-
Gedeïoniseerd water
- MeOH:
-
Methanol
- EtOH:
-
Ethanol
- IPA:
-
Isopropylalcohol
- ACE:
-
Aceton
- ACN:
-
Acetonitril
- DMF:
-
N ,N -Dimethylformamide
- DMSO:
-
Dimethylsulfoxide
- HR-TEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- FT-IR:
-
Fourier-transformatie infraroodspectroscopie
- XRD:
-
Röntgendiffractie
- XPS:
-
Röntgenfoto-elektronenspectroscopie
Nanomaterialen
- Cyclocarbon maken en in beeld brengen
- Koolstof nanobuisgaren, spierweefsel en transparante vellen
- Onthulling van de atomaire en elektronische structuur van gestapelde koolstof nanovezels
- Hoog-efficiënte excitatie-onafhankelijke blauwe lichtgevende koolstofstippen
- Grafeen- en polymeercomposieten voor toepassingen met supercondensatoren:een recensie
- Synthese van door reabsorptie onderdrukte Type-II/Type-I ZnSe/CdS/ZnS Core/Shell Quantum Dots en hun toepassing voor immunosorbentassay
- Geactiveerde koolstofvezels met hiërarchische nanostructuur afgeleid van afval katoenen handschoenen als hoogwaardige elektroden voor supercondensatoren
- Een eenvoudige aanpak voor het synthetiseren van fluorescerende koolstofkwantumstippen uit tofu-afvalwater
- Materiële en optische eigenschappen van fluorescerende koolstof Quantum Dots vervaardigd uit citroensap via hydrothermische reactie
- Zeer actieve en stabiele Fe-N-C-zuurstofreductie-elektrokatalysatoren afgeleid van elektrospinning en in-situ pyrolyse
- Eenvoudige synthese van polydopamine-koolstofstippen voor fotothermische therapie



