Verbetering van de elektrochemische eigenschappen van LaCoO3 door Sr-Doping, rGO-compounding met rationeel ontwerp voor energieopslagapparaat
Abstract
Perovskietoxiden, als een soort functionele materialen, zijn de afgelopen jaren uitgebreid bestudeerd vanwege de unieke fysische, chemische en elektrische eigenschappen. Hier hebben we met succes perovskiet-type LaCoO3 . geprepareerd (LCO's) nanomaterialen via een verbeterde sol-gel-methode gevolgd door calcineren, en onderzochten de invloed van calcineringstemperatuur en -tijd op de morfologie, structuur en elektrochemische eigenschappen van LaCoO3 nanomaterialen. Vervolgens vertoonden de nieuw gesynthetiseerde nanocomposieten van Sr-doping (LSCO-0.2) en rGO-compounding (rGO@LCO) door rationeel ontwerp een 1,45-voudige en 2,03- vouwverbetering in zijn specifieke capaciteit (specifieke capaciteit). De rGO@LCO-elektrode met betere elektrochemische prestaties werd verder onderzocht door rGO@LCO//rGO asymmetrisch supercondensatorsysteem (ASS) te assembleren met waterige elektrolyt. Het resultaat toonde aan dat de ASS een hoge energiedichtheid levert van 17,62 W h kg −1 en een uitstekende cyclische stabiliteit met 94,48% van de initiële capaciteit na 10.000 cycli, wat goede elektrochemische prestaties zijn onder waterige elektrolyten voor groene en nieuwe efficiënte energieopslagapparaten.
Inleiding
Met de uitputting van de fossiele brandstofreserves, de stijging van de energiekosten en de verergering van de milieuvervuiling, staan het onderzoek naar en de ontwikkeling van efficiënte en betrouwbare energieopslag- en conversieapparatuur die volledig hernieuwbare energiebronnen kan verkrijgen en gebruiken voor grote uitdagingen en hebben ze aangetrokken uitgebreide aandacht [1,2,3]. Supercapacitors (SC's), ook bekend als ultracapacitors (UC's), als een brug die het enorme verschil tussen conventionele condensatoren en batterijen verbindt, hebben de afgelopen decennia uitgebreid onderzoek gedaan vanwege hun unieke voordelen, zoals een hogere energiedichtheid dan conventionele condensatoren, een hogere vermogensdichtheid , ultralange levensduur en milieuvriendelijk in vergelijking met batterijen, evenals hoge veiligheid en snel laad-ontlaadvermogen [4,5,6]. SC's kunnen worden onderverdeeld in elektrische dubbellaagse condensatoren (EDLC's) en faraday-condensatoren volgens het verschillende reactieproces en het ladingsopslagmechanisme. De ionenaccumulatie vond plaats op het grensvlak tussen de elektrode en de elektrolyt om lading op te slaan is EDLC's, wat een fysiek proces is en voornamelijk verschillende koolstofelektrodematerialen gebruikt [7,8,9,10,11]. Terwijl de lading die aan het oppervlak of de ondergrond van de elektrodematerialen wordt opgeslagen door een snelle omkeerbare Faraday-reactie of ion-intercalatie/de-intercalatie, Faraday-condensatoren zijn, wat een chemisch reactieproces is en de elektrodematerialen ervan voornamelijk overgangsmetaaloxiden (hydroxiden), nitriden omvatten , geleidende polymeren, enzovoort [12,13,14,15,16,17]. Omdat elektrodemateriaal een cruciale rol speelt in de elektrochemische eigenschappen van SC's, terwijl pure koolstofmaterialen meestal een lage energiedichtheid hebben, zijn veel onderzoeken en inspanningen gericht op de elektrodematerialen voor faraday-condensatoren met een hoge specifieke capaciteit en hoge energiedichtheid [12, 18, 19,20].
Onlangs heeft ABO3 -type perovskietoxiden, waarbij A lanthanide of aardalkali-element is en B een overgangsmetaal is, zijn op grote schaal bestudeerd en toegepast op het gebied van energieopslag als een soort elektrodemateriaal met een uitzonderlijke elektronische structuur, uitstekende ionische geleidbaarheid en thermische stabiliteit [ 21,22,23,24]. Che et al. [25] meldt een nieuwe anion-geïntercaleerde pseudocapacitieve elektrode van perovskietoxide LaNiO3 gesynthetiseerd met behulp van de sol-gel-methode, en het vertoont uitstekende elektrochemische prestaties met een hoge specifieke capaciteit van 478,7 F g −1 bij 0,1 mV s −1 en een goede cyclusstabiliteit van het verminderen van 5,5% laad-ontlaadefficiëntie na 15.000 cycli. Shafi et al. [26] synthetiseert 3D veelvlak gestructureerde LaMnO3 nanodeeltjes die natuurlijk citroensap (LJ) gebruiken als een groene oppervlakteactieve stof, en het gedefinieerde LMO-nanodeeltje vertoont een drievoudige verbetering in zijn specifieke capaciteit. Bovendien levert de symmetrische cel met twee elektroden geassembleerd met LMO/3.0 een hoge energiedichtheid van 52,5 Wh kg −1 bij een vermogensdichtheid van 1000 W kg −1 en een uitstekende cyclische stabiliteit met 97% behoud van zijn maximale capaciteit en 117% van zijn initiële capaciteit gedurende 10.000 cycli. Als het overgangsmetaal op de B-positie in ABO3 -type perovskieten, Mn, Ni en Fe zijn veel bestudeerd voor materialen voor energieopslag [22, 27,28,29]. Daarom is het Co-element met vergelijkbare eigenschappen ook verder onderzoek waard, vooral vanwege het gemodificeerde nanocomposiet [30,31,32,33,34]. De gerapporteerde elektrochemische eigenschappen van LaCoO3 en de gemodificeerde composieten zijn minder dan die van LaNiO3 , LaMnO3 , en andere soortgelijke materialen, die nader onderzoek waard zijn.
Met het oog hierop hebben we in dit artikel het syntheseproces rationeel ontworpen en geoptimaliseerd en met succes het perovskiet-type LaCoO3 gesynthetiseerd. nanocomposiet door sol-gel-methode gevolgd door calcinering, en onderzocht de invloed van calcineringstemperatuur en -tijd op de morfologie, structuur en elektrochemische eigenschappen van LaCoO3 nanomaterialen. Bovendien zijn het veranderen van de roosterstructuur en het zuurstoftekort van het materiaal door dotering en het vormen van het composietmateriaal door te combineren met het materiaal met een hoog specifiek oppervlak de twee meest gebruikte technieken om de elektrochemische prestatie van een enkelvoudig zuiver fase-elektrodemateriaal te verbeteren. Daarom kiezen we, gebaseerd op het optimale LCO-700-4 elektrodemateriaal, twee strategieën van A-site element substitutie (Sr) en composiet met gereduceerd grafeenoxide (rGO) materiaal met een hoog specifiek oppervlak om de invloed van Sr- verder te onderzoeken. doping en rGO-compounding op zijn elektrochemische prestaties van de nieuw gesynthetiseerde LSCO-0.2 en rGO-compounding LaCoO3 (rGO@LCO) nanocomposieten door rationeel ontwerp. Vergeleken met pure LaCoO3 (LCO) elektrodematerialen, zijn de elektrochemische eigenschappen van LSCO-0.2 en rGO@LCO nanocomposietelektroden aanzienlijk verbeterd, vooral voor rGO@LCO-elektrode. De betere elektrochemische prestatie van de rGO@LCO-elektrode vertoont een hoge specifieke capaciteit van 416 F g −1 (specifieke capaciteit:63,56 mAh g −1 ) bij een stroomdichtheid van 0,5 A g −1 , en een goed tarief vermogen. Wanneer een asymmetrisch supercondensatorsysteem (ASS) wordt geassembleerd met een rGO@LCO-elektrode als positieve elektrode en rGO-elektrode als negatieve elektrode, vertoont de rGO@LCO//rGO ASS een hoge energiedichtheid van 17,62 W h kg −1 bij een vermogensdichtheid van 170 W kg −1 , en een uitstekende cyclische stabiliteit met 94,48% van de initiële capaciteit na 10.000 cycli bij een hoge scansnelheid van 100 mV s −1 . Dit resultaat toont aan dat LaCoO3 en LaCoO3 -gebaseerde nanocomposieten als elektrodematerialen hebben een groot potentieel in groene en efficiënte nieuwe energieopslagapparaten.
Experimentele methoden
Synthese van poreuze LaCoO3 en Sr-Doped LaCoO3 Nanomaterialen
Alle chemische reagentia waren van analytische kwaliteit en werden niet verder gezuiverd voordat ze in dit experiment werden gebruikt. In een typisch syntheseproces werden 1 mM lanthaannitraathexahydraat en 1 mM kobaltnitraathexahydraat opgelost in 40 ml N ,N -dimethylformamide (DMF) en gedurende 2 uur magnetisch geroerd. Later werd 0,45 g polyvinylpyrrolidon (PVP-K30) langzaam toegevoegd aan het bovenstaande mengsel om een homogene oplossing te verkrijgen door continu magnetisch roeren gedurende 3 uur. En vervolgens werd het homogene mengsel verwarmd en geroerd totdat de gel zich vormde. Vervolgens werd de verkregen gel overgebracht naar de smeltkroes en in een moffeloven geplaatst voor een gloeibehandeling bij 600 °C gedurende 4 uur met een verwarmingssnelheid van 5 °C min −1 . Het verkregen monster dat op natuurlijke wijze tot kamertemperatuur was gekoeld, was LaCoO3 -600 °C-4 uur (geregistreerd als LCO-600-4) nanomaterialen. Onder hetzelfde synthetische proces, een reeks LCOS nanomaterialen werden verkregen door de reactietemperatuur en -tijd te regelen en geregistreerd als LCO-700-4, LCO-800-4, LCO-700-2 en LCO-700-3.
Het syntheseproces van Sr-gedoteerde LaCoO3 nanocomposieten was vergelijkbaar met de bovengenoemde LCO's-materialen, behalve dat in de eerste stap:1 mM lanthaannitraathexahydraat werd veranderd in 0,8 mM lanthaannitraathexahydraat en 0,2 mM strontiumnitraat, en het daaropvolgende proces was precies hetzelfde. De gesynthetiseerde Sr-gedoteerde LCO-700-4 nanocomposiet was La0,8 Sr0,2 CoO3-δ en geregistreerd als LSCO-0.2.
Synthese van poreuze rGO@LaCoO3-δ Nanomaterialen
Grafeenoxide (GO) werd bereid uit natuurlijk vlokgrafietpoeder met een gemodificeerde Hummer-methode [15]. In een eenvoudige vaste-stofmethode gevolgd door een syntheseproces met hoge temperatuur warmtebehandeling, werd 10 mg bereid GO in een vijzel tot poeder vermalen. Vervolgens werd er 90 mg gesynthetiseerd LCO-700-4-monster aan toegevoegd en bleef het malen. Nadat twee materialen volledig waren gemalen en gelijkmatig gemengd, werd het mengsel overgebracht naar een kroes en in de kwartsbuis van de buisoven geplaatst. De warmtebehandelingsconditie was 700 ° C gedurende 1 uur onder Ar-atmosfeer. Na natuurlijke afkoeling tot kamertemperatuur en het verzamelen van de materialen, wordt de rGO@LaCoO3-δ -700-4 nanocomposiet werd verkregen en geregistreerd als rGO@LCO.
Kenmerken van materialen
De fase-identificatie van de voorbereide monsters werd uitgevoerd op het poederröntgendiffractiepatroon (Bruker D8 Advance) met Cu Kα-bestraling (λ =0,154056 nm) bij een scansnelheid van 0,2°s −1 . De microstructuur en morfologie van de monsters werden onderzocht met een scanning elektronenmicroscoop (SEM; Quanta 250 FEG, VS) en transmissie-elektronenmicroscoop (TEM, JEOL JEM-2100). Het specifieke oppervlak verkregen uit de resultaten van stikstofadsorptie-desorptie-isothermen bij 77 K gebruikte de meerpunts Brunauer-Emmett-Teller (BET) -methode (ASAP 2020-analysator, Micromeritics, VS). Voorafgaand aan de metingen werden de monsters gedurende 6 uur in vacuüm bij 150 ° C ontgast. De poriegrootteverdelingen en porievolumegegevens van monsters werden berekend uit de desorptietak op basis van de Barrett-Joyner-Halenda (BJH) -vergelijking. Röntgenfoto-elektronspectroscopie (XPS) uitgevoerd met een Thermo Scientific ESCALAB 250 Xi met behulp van Al Ka-straling (VS) was om de oppervlaktetoestanden van monsters te onderzoeken. Het Raman-spectrum wordt verkregen met een Renishaw inVia Raman-microscoop die gebruik maakt van een laserexcitatie van 532 nm (25% laservermogen).
Elektrochemische metingen
De elektrochemische prestaties van deze elektroden werden getest met behulp van een conventioneel systeem met drie elektroden en een systeem met twee elektroden in 6 M KOH-elektrolyt, dat presteerde op een CHI660E elektrochemisch werkstation (Shanghai Chenhua, China) bij kamertemperatuur. In dit systeem met drie elektroden dienden de geprepareerde elektrode, een platinaplaatelektrode en de verzadigde calomelelektrode (SCE) respectievelijk als werkelektrode, tegenelektrode en referentie-elektrode. Het fabricageproces van de werkelektrode als volgt:het bereide monster (80 gew.%), geleidend roet (10 gew.%) en polytetrafluorethyleen (PTFE, 10 gew.%) bindmiddel werden grondig gemengd door isopropylalcohol toe te voegen. Na mengen om een homogene fase te vormen, werden de slurries op het nikkelschuim aangebracht en samengeperst met een walspers. Daarna werd de gefabriceerde elektrode zorgvuldig bijgesneden en een nacht gedroogd in een vacuümoven bij 75°C. De belasting van elke elektrode was ongeveer 1,8 mg.
De elektrochemische prestatiemetingen omvatten cyclische voltammetrie (CV), galvanostatische lading/ontlading (GCD) en elektrochemische impedantiespectroscopie (EIS). De werkelektrode werd voor de test een nacht in de elektrolyt ondergedompeld om het volledige contact tussen de elektrolyt en het actieve materiaal van de werkelektrode te bevorderen. De gravimetrische specifieke capaciteiten van de elektrode werden berekend op basis van de Eq. (1):
$$ Sc=\frac{I\times \Delta t}{m\times \Delta V} $$ (1)waar Sc (F g −1 ) is de specifieke capaciteiten, Δt (s) is de ontlaadtijd, m (g) is de massa van actief materiaal, en ΔV is het bereik van het potentiële venster.
Wat betreft het systeem met twee elektroden, een asymmetrisch supercondensatorsysteem (ASS) op basis van de rGO@LCO-elektrode als de positieve elektrode en de rGO-elektrode als de negatieve elektrode. En de massa van beide elektroden werd berekend volgens de Vgl. (2). Verder is de specifieke capaciteit (C , F g −1 ), energiedichtheid (E , W h kg −1 ) en vermogensdichtheid (P , kW kg −1 ) van de ASS werden berekend op basis van de vergelijkingen. (3), (4) en (5) respectievelijk:
$$ \frac{m_{+}}{m_{-}}=\frac{Sc_{-}\times {\Delta V}_{-}}{Sc_{+}\times {\Delta V}_{ +}} $$ (2) $$ C=\frac{I\Delta t}{M\Delta V}\kern0.5em $$ (3) $$ E=\frac{1}{2\times 3.6} C{\left(\Delta V\right)}^2\kern0.5em $$ (4) $$ P=\frac{3600E}{\Delta t} $$ (5)waar m + (g) en m − (g) zijn respectievelijk de massa van de positieve elektrode en de negatieve elektrode. Sc + (F g −1 ) en Sc − (F g −1 ) is de specifieke capaciteit van de positieve elektrode en de negatieve elektrode, respectievelijk berekend volgens het drie-elektrodensysteem. M (g) is de totale massa van beide elektroden.
Resultaten en discussie
Effecten van de calcineringstemperatuur en -tijd op de morfologie, structuur en elektrochemische eigenschappen van LCO's-materialen
De scanning-elektronenmicroscopie (SEM) -beelden van LCO's-nanomaterialen bereid bij verschillende calcineringstemperaturen en -tijden worden weergegeven in Fig. 1a-e. Het kan worden gezien dat de morfologieën van alle monsters die onder verschillende calcineringscondities zijn bereid, over het algemeen vergelijkbaar zijn, en de subtiele verschillen worden voornamelijk weerspiegeld in de deeltjesgrootte en porositeit. Met de toename van de calcineringstemperatuur hebben de verkregen LCO-materialen een meer losse en overvloedige poriestructuur, maar door een te hoge temperatuur (figuur 1c) zullen de kleine deeltjes een compacte en grote blokstructuur vormen, wat de porositeit van het LCO-materiaal vermindert. En met dezelfde calcineringstemperatuur en verschillende calcineringstijden vertoont het LCO-materiaal een zeer vergelijkbare morfologie. Figuur 1f toont de X-ray power diffraction (XRD) patronen van alle geprepareerde LCOs-materialen. De sterke diffractie piekt bij 2θ =23,3°, 32,9°, 33,3°, 40,7°, 47,5° en 59,0° zijn met succes geïndexeerd op de kristalvlakken (012), (110), (104), (202), (024) en (214) , respectievelijk, die wordt toegeschreven aan de facetten van zeshoekige LaCoO3 volgens JCPDS nr:48-0123. Het is te zien dat alle LCO's-monsters dezelfde diffractiepieken en geen onzuiverheidspiek hebben, wat een hoge zuiverheid van de monsters bevestigt. Bovendien kan door zorgvuldige vergelijking worden gezien dat in vergelijking met de calcineringstijd, het verschil in calcineringstemperatuur een grotere invloed heeft op de kristalliniteit van materialen. En hoe hoger de temperatuur, hoe hoger de kristalliniteit voor de bereide LCO's-monsters. Volgens verschillende hoofddiffractiepieken van LCO-monsters en berekend volgens de formule van Scherer, is de gemiddelde kristallijne grootte van het LCO-700-4-monster ongeveer 44,87 nm, wat enigszins verschilt van andere monsters bij verschillende calcineringscondities (LCO-600-4 (43,65 nm), LCO-800-4 (47,15 nm), LCO-700-2 (44,53 nm), LCO-700-3 (44,15 nm)). Een typische type IV isotherm in de N2 adsorptie-desorptie-isothermen geven het bestaan van de mesoporeuze structuur in alle LCO's-monsters aan (figuur 1g). Bovendien kan aan de inzet (Tabel 1) in Fig. 1g worden gezien dat een te hoge calcineringstemperatuur het specifieke oppervlak en de porositeit van het materiaal ernstig zal aantasten.
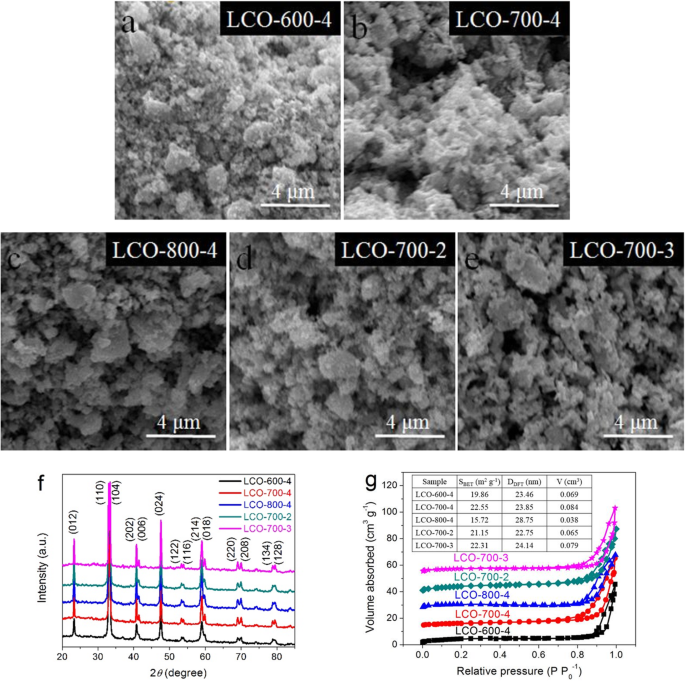
een –e SEM-afbeeldingen, f XRD-patronen en g N2 adsorptie-desorptie-isothermen van de bereide LCO's-monsters bij verschillende calcineringstemperaturen en -tijden
Figuur 2a toont de CV-curven van alle elektroden met een scansnelheid van 50 mV s −1 . Het is duidelijk te zien dat het reactieproces de kenmerken omvat van het dubbele elektrische laagproces (quasi rechthoek in laag potentiaalgebied) en Faraday-reactie (duidelijke oxidatie-reductiepieken), wat aangeeft dat de gegenereerde capaciteit dubbele elektrische laagcapaciteit en Faraday-capaciteit omvat. Bovendien kan ter vergelijking worden geconcludeerd dat het gebied dat wordt ingesloten door de CV-curve van de LCO-700-4-elektrode groter is, wat betekent dat deze een grotere capaciteit heeft. De corresponderende GCD-curven van deze elektroden bij 0,5 A g −1 worden weergegeven in Fig. 2b. De GCD-curven met de niet-lineaire driehoeken laten verder zien dat de capaciteit die wordt gegenereerd in het laad-ontlaadproces de dubbellaags capaciteit en de faraday-capaciteit omvat. En berekend op basis van GCD-curven, is de specifieke capaciteit van de LCO-700-4-elektrode 205,04 F g −1 (specifieke capaciteit:31,33 mAh g −1 ), die iets hoger is dan die van de LCO-600-4-elektrode (140.03 F g −1 , 21,39 mAh g −1 ), LCO-800-4 elektrode (166,23 F g −1 , 25,40 mAh g −1 ), LCO-700-2 elektrode (174.37 F g −1 , 26,64 mAh g −1 ), en LCO-700-3 elektrode (185,22 F g −1 , 28,30 mAh g −1 ), respectievelijk.
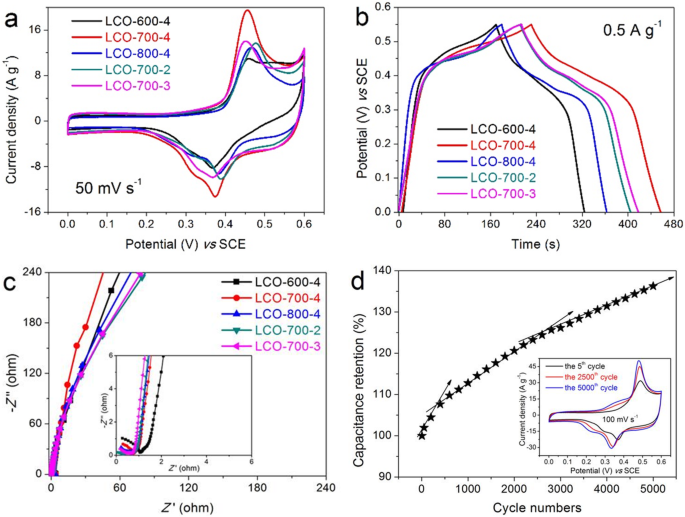
een CV-curven bij 50 mV s −1 , b GCD-curven bij 0,5 A g −1 , en c Nyquist-plots in het frequentiebereik van 100 kHz tot 0,01 Hz voor alle voorbereide LCO's-elektroden bij verschillende calcineringstemperaturen en -tijden. d Cyclusstabiliteit van LCO-700-4 elektrode bij 100 mV s −1 voor 5000 cycli (invoegen toont de vergelijking van CV-curven bij 5e cyclus, 2500e cyclus en 5000e cyclus)
Het impedantiegedrag van deze LCO's-elektroden wordt gemeten in het frequentiebereik van 100 kHz tot 0,01 Hz met een amplitude van 5 mV om het ladingsoverdrachtproces te begrijpen. Zoals getoond in figuur 2c, bevatten alle Nyquist-grafieken een boog in de hoge frequentie en een benaderende rechte lijn met een hoge helling in de lage frequentie. De diameter van de vervormde boog in het hoogfrequente gebied vertegenwoordigt de ladingsoverdrachtsweerstand (R ct). Uit het inzetstuk in Fig. 2c is te zien dat alle LCO's-elektroden een zeer kleine R hebben ct behalve voor LCO-600-4 elektrode met een iets grotere R ct, wat aangeeft dat de perovskiet LaCoO3 materiaal is zeer gunstig voor de snelle overdracht van lading [35, 36]. De helling van de rechte lijn in het laagfrequente gebied vertegenwoordigt Warburg-impedantie (W o), wat voornamelijk de diffusieweerstand van elektrolyt en proton in het actieve materiaal weerspiegelt [24, 37]. Een grotere helling betekent een lager W O. Daarom kan worden gezien dat het LCO-700-4-elektrodemateriaal betere diffusie-dynamische eigenschappen van elektrolyt en proton heeft.
De cyclusstabiliteit van de LCO-700-4-elektrode met de optimale elektrochemische prestatie voor 5000 cycli bij een grote scansnelheid van 100 mV s −1 wordt weergegeven in Fig. 2d. Er kan worden waargenomen dat de capaciteit toeneemt met het aantal cycli. En met verdere zorgvuldige observatie neemt de capaciteit sneller toe naarmate het aantal cycli toeneemt, vooral in de eerste 800 cycli. Na ongeveer 3000 cycli neemt de toename van de capaciteit geleidelijk af naarmate het aantal cycli toeneemt, wat te zien is aan de afname van de geschatte helling van de capaciteitsretentiecurve in figuur 2d. Daarom leiden we af dat de LaCoO3 nanomateriaal heeft een stabiele structuur en kan de volumeverandering bufferen onder een grote scansnelheid, zodat de LaCoO3 nanomateriaal wordt continu geactiveerd in het vroege stadium van de redoxreactie totdat het volledig is geactiveerd. In het latere stadium, met de continue voldoende infiltratie van elektrolyt en actieve stof, wordt de activering van interne actieve plaatsen verder bevorderd, waardoor de specifieke capaciteit verder wordt verbeterd [24, 38]. De toename van de capaciteit wordt volledig geïllustreerd door de CV-curven bij de 5e, 2500e en 5000e cycli, zoals weergegeven in het bijvoegsel in figuur 2d, waaruit blijkt dat het gebied dat wordt ingesloten door de CV-curve toeneemt met de toename van het aantal cyclussen. /P>
Effecten van Sr-Doping en rGO-compounding op de morfologie, structuur en elektrochemische eigenschappen van de nieuw gesynthetiseerde nanocomposieten
Door een redelijke aanpassing en controle van de hoeveelheid Sr-doping en het gehalte aan rGO-compounding, onderzoeken we de invloed van Sr-doping en rGO-compounding op de nieuw gesynthetiseerde op LCO-700-4 gebaseerde nanocomposieten, om betere prestaties van de Op LCO gebaseerde composietelektrode. De specifieke capaciteit van elektroden uit de Sr-doping LCO-serie worden getoond in figuur 3a. Met de toename van het Sr-dopinggehalte, de specifieke capaciteit van Sr-doping LaCoO3 (LSCO's) composietelektrode neemt eerst toe en vervolgens af, en de LSCO-0.2-elektrode (La1-x Srx CoO3 , x =0.2) toont de beste capaciteitsprestaties. Tegelijkertijd wordt de specifieke capaciteit van rGO-compounderende elektroden uit de LCO-serie weergegeven in figuur 3b. Het is te zien dat de rGO@LCO-10 (LCO:90 mg, rGO:5 mg, 10 mg, 20 mg, 30 mg) elektrode de beste capaciteitseigenschap heeft. Door de overmaat aan rGO in composieten neemt de specifieke capaciteit echter sterk af. We speculeren dat de agglomeratie veroorzaakt door overmatige rGO niet alleen de capaciteit niet effectief vergroot, maar ook de poriestructuur van de composiet beïnvloedt, wat niet bevorderlijk is voor het ion / elektronentransport, waardoor de elektrochemische prestatie van de rGO@LCO-composieten wordt verminderd . Om de invloed van Sr-doping en rGO-compounding op de elektrochemische prestaties van de nieuw gesynthetiseerde LCO-700-4-gebaseerde nanocomposieten verder te onderzoeken, en een vergelijkende analyse te maken met LCO-700-4 elektrodemateriaal. Daarom concentreren we ons in het volgende onderzoek van dit artikel op het verkennen van de elektrodematerialen met de optimale capaciteitseigenschap in hun respectievelijke series om te vergelijken met LCO-materialen.
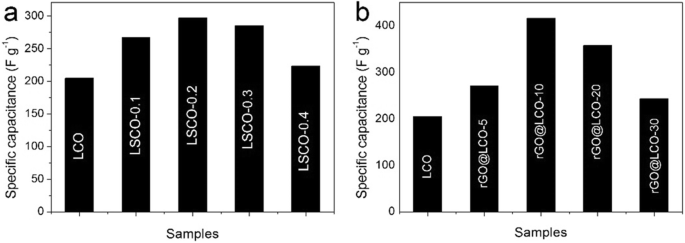
De specifieke capaciteit van a LSCO's en b rGO@LCOs-elektroden bij 0,5 A g −1
De morfologie en microstructuur van LCO-700-4, LSCO-0.2 en rGO@LCO-monsters worden weergegeven in Fig. 4a-c. Het kan worden waargenomen dat de LSCO-0.2 en rGO@LCO nanocomposieten een meer poreuze structuur en kleinere deeltjesmorfologie hebben met meer gelijkmatige verspreiding. Verder kan ook worden waargenomen dat het LCO-materiaal goed kan worden gedispergeerd in en tussen de rGO-platen, waardoor het optreden van geagglomereerd grafeen effectief wordt verminderd met de eigenschap van gemakkelijke agglomeratie. De gedetailleerde structuur van rGO@LCO-composiet wordt verder gekenmerkt door HRTEM-afbeelding, zoals weergegeven in figuur 4d. De poreuze structuur van LCO-materialen kan goed worden verspreid in rGO-materialen. Bovendien kan door de invloed van GO-reactanten worden gezien dat de roosterranden van de LCO-materialen niet duidelijk zijn, wat erop wijst dat de kristalliniteit van de LCO-materialen in rGO@LCO-composieten wordt verminderd door de invloed van GO-materialen. De kristalstructuur en fasesamenstelling van de gesynthetiseerde LSCO-0.2 en rGO@LCO worden gekenmerkt door XRD, en de vergelijking van het XRD-patroon voor hun en LCO-700-4-monster wordt weergegeven in figuur 4e. Het is te zien dat de positie van de hoofddiffractiepiek van het LSCO-0.2-monster in principe hetzelfde is als dat van het LCO-700-4-monster. Maar door de invloed van Sr-doping neemt de intensiteit van de diffractiepiek af en verschijnen er een klein aantal kleine pieken. Evenzo worden de belangrijkste diffractiepieken van LCO-700-4-monsters ook weerspiegeld in rGO@LCO-nanocomposieten. Echter, vanwege de hoge temperatuurreactie tussen LaCoO3 en rGO-materialen, een kleine hoeveelheid bijproduct van LaCO3 OH-materialen (JCPDS-nr:26-0815) verschijnen in de rGO@LCO-nanocomposieten, wat overeenkomt met de diffractiepiek van de positie op ongeveer 2θ =29,8°. Bovendien ligt de zwakke piek rond 2θ =26,2 ° moet worden beschouwd als de diffractiepiek van rGO-materialen. Figuur 4f toont de Raman-spectra van rGO- en rGO@LCO-monsters. De karakteristieke piek op ongeveer 1331,17 cm −1 komt overeen met de D-band, die voornamelijk het defect en de ongeordende structuren van grafeen vertegenwoordigt. En de karakteristieke piek op ongeveer 1594,53 cm −1 komt overeen met de G-band, die voornamelijk wordt geproduceerd door de rektrilling in het vlak van sp 2 koolstof atoom. Daarnaast een lichte daling van de I D /Ik G waarde van rGO naar rGO@LCO duidde op minder defecten in de invloed van het LCO-monster dat deelnam aan de reactie.
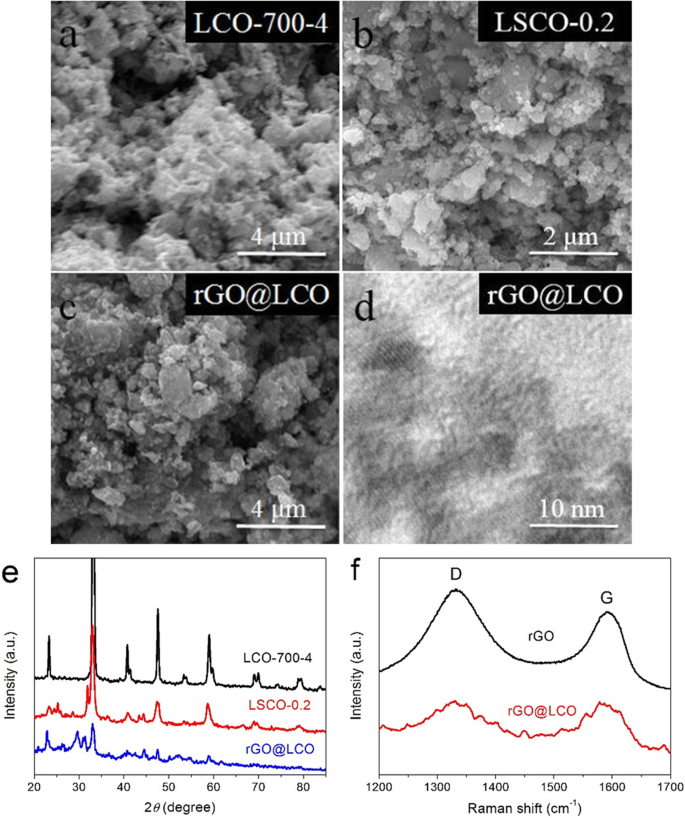
een –c SEM-afbeeldingen van de LCO-700-4, LSCO-0.2 en rGO@LCO-monsters. d HRTEM-beeld van rGO@LCO-composiet. e XRD-patronen van de LCO-700-4, LSCO-0.2 en rGO@LCO-samples. v Raman-spectra van rGO- en rGO@LCO-monsters
De stikstofadsorptie-desorptie-isothermen van LCO-700-4, LSCO-0.2 en rGO@LCO-monsters geïllustreerd in Fig. 5a vertonen een typische type IV isotherm met een hysteresislus bij P P 0 −1 van ongeveer 0,75, wat wijst op het bestaan van een groot aantal mesoporische nanostructuren. Tegelijkertijd treedt capillaire condensatie op bij hogere druk, wat betekent dat deze monsters zowel mesoporiën als macroporiën hebben [39]. De overeenkomstige poriegrootteverdelingscurves worden weergegeven in Fig. 5b. Opgemerkt kan worden dat de poriegrootte van deze materialen voornamelijk geconcentreerd is in 10-50 nm. Vanwege het bestaan van rGO-materialen zijn er echter meer poriën met een diameter van minder dan 5 nm in rGO@LCO-composiet. De specifieke oppervlakten (S BET ) van LCO-700-4, LSCO-0.2 en rGO@LCO zijn berekend op 22,55, 29,74 en 59,89 m 2 g −1 , respectievelijk (Tabel 1). De rGO@LCO met de grootste S BET wordt voornamelijk toegeschreven aan de hoge specifieke oppervlaktekenmerken van rGO-nanobladen. Door de invloed van S-doping en rGO-compounding wordt de S BET en het porievolume van het gesynthetiseerde LSCO-0.2 en rGO@LCO zijn tot op zekere hoogte verhoogd in vergelijking met het pure LCO-700-4-materiaal, wat de reactieplaatsen en ladingsopslagplaatsen zal vergroten, waardoor de capaciteit van de composieten wordt verbeterd.
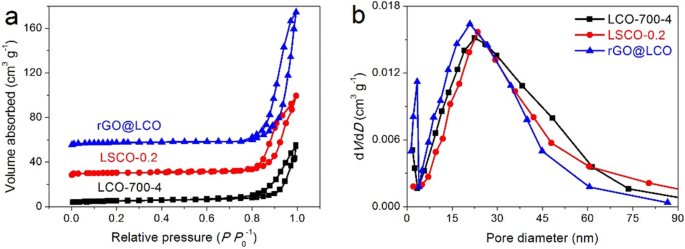
een Stikstofadsorptie-desorptie-isothermen en b de overeenkomstige poriegrootteverdelingscurves van LCO-700-4, LSCO-0.2 en rGO@LCO-monsters
De oppervlakte-eigenschappen van het gesynthetiseerde rGO@LCO nanocomposiet worden bevestigd door XRS. Zoals weergegeven in Fig. 6a, toont het volledige XPS-spectrum van de onderzoeksscan de aanwezigheid van La-, Co-, O- en C-elementalen aan. Het gedeconvolueerde spectrum van Co 2p gepresenteerd in Fig. 6b geeft het bestaan van Co elementair aan in twee oxidaties van Co 2+ en Co 3+ . En de bindingsenergieën bij 779,7 en 794,8 eV worden toegeschreven aan Co 3+ , terwijl de bindingsenergieën bij 780,8 en 796,2 eV worden toegeschreven aan Co 2+ [40, 41]. Het spectrum met hoge resolutie van O 1s dat wordt getoond in Fig. 6c vertoont vier pieken bij 532,4, 531,8, 529,8 en 529,5 eV na deconvolutie van O 1s, wat overeenkomt met aan het oppervlak geadsorbeerd H2 O, respectievelijk oppervlakte-geadsorbeerde zuurstof of hydroxylgroepen, sterk oxidatieve zuurstofsoorten en oppervlakteroosterzuurstof [24, 41, 42]. Er wordt aangenomen dat de hogere zuurstofvacatures in perovskietoxiden gunstig zijn voor de adsorptiecapaciteit van OH - , waardoor de kinetiek van de oxidatie-reductiereactie aan het oppervlak wordt versneld en de geleidbaarheid en elektrochemische prestaties worden verbeterd [24, 43]. Het spectrum met hoge resolutie van Cl's geïllustreerd in Fig. 6d bestaat voornamelijk uit vier pieken en de bindingsenergieën bij 289,4, 288,7, 286,0 en 284,8 eV komen overeen met de groepen OC=O, CO, CC en CH, en C=C, respectievelijk [15]. Deze resultaten komen overeen met de eerdere SEM- en XRD-resultaten, die het bestaan van rGO en LaCoO3 sterk bewijzen. materialen.
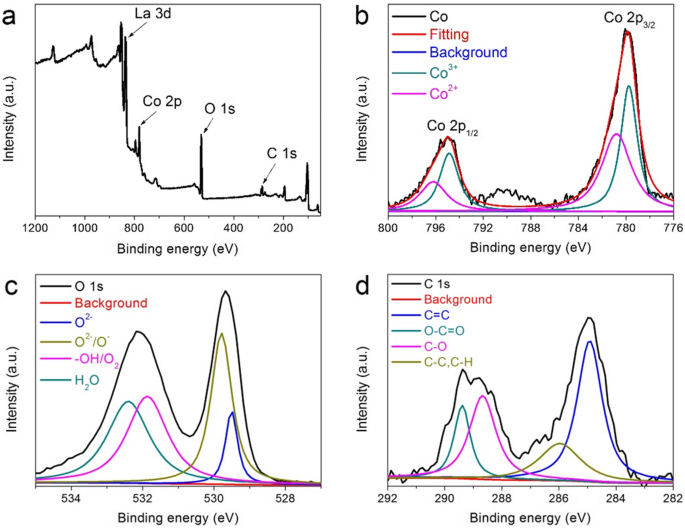
een XPS-enquêtescan van rGO@LCO-oppervlak en spectrum met hoge resolutie van b Co 2p, c O 1s en d C 1s
De effecten van Sr-doping en rGO-compounding op de elektrochemische eigenschappen van de nieuw gesynthetiseerde nanocomposieten worden geïllustreerd in Fig. 7. De CV-curven van LCO-700-4, LSCO-0.2 en rGO@LCO-elektroden met een scansnelheid van 50 mV s −1 zijn geïllustreerd in Fig. 7a. Het is te zien dat de vormen van de CV-curve niet veel zijn veranderd, en de gebieden die worden ingesloten door de CV-curve van de LSCO-0.2-elektrode en rGO@LCO zijn aanzienlijk groter dan die van de LCO-700-4-elektrode, wat betekent dat de capaciteit is verbeterd met Sr-doping of rGO-compounding. Na berekening op basis van de GCD-curven (Fig. 7b), is de capaciteit van de LSCO-0.2-elektrode en de rGO@LCO-elektrode 297,09 F g −1 (specifieke capaciteit:45,39 mAh g −1 ) en 416 F g −1 (63,56 mAh g −1 ) bij een stroomdichtheid van 0,5 A g −1 , which are 1.45 times and 2.03 times of that of LCO-700-4 electrode, respectively. The equation of specific capacitance changing with current density of LCO-700-4, LSCO-0.2, and rGO@LCO electrodes are illustrated in Fig. 7c. When the current increased by 10 times (from 0.5 to 5 A g −1 ), the capacitance of LSCO-0.2 electrode and rGO@LCO electrode remained 47.01% and 58.40%, which is higher than that of LCO-700-4 electrode (39.71%), indicating that the rate capability of LSCO-0.2 electrode and rGO@LCO electrode is significantly improved. The comparison of Nyquist plots for LCO-700-4, LSCO-0.2, and rGO@LCO electrode is displayed in Fig. 7d. After careful observation and comparison, it can be seen that the values of R ct and W o for three electrodes are as follows:R ct (LSCO-0.2) <R ct (rGO@LCO) <R ct (LCO-700-4), W o (rGO@LCO) <W o (LSCO-0.2) <W o (LCO-700-4), which shows that the nanocomposites have better conductivity and ion diffusion dynamics than the pure LCO-700-4 material. These results show that the new nanocomposites obtained by Sr-doping or rGO-compounding can greatly enhance the electrochemical performance, especially for the rGO@LCO nanocomposites. Therefore, based on rGO@LCO nanocomposites as positive material, we will then assemble it into an asymmetric two-electrode system for further research.
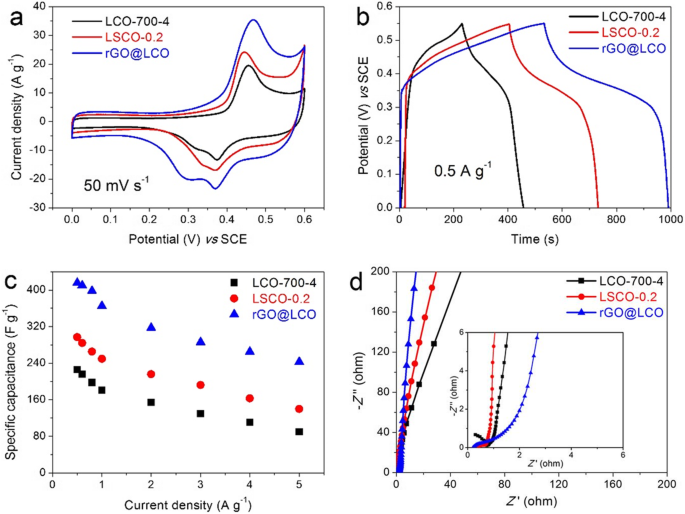
een CV curves at 50 mV s −1 , b GCD curves at 0.5 A g −1 , c rate capability, and d Nyquist plots in the frequency range of 100 kHz to 0.01 Hz for LCO-700-4, LSCO-0.2, and rGO@LCO electrodes
An assembled asymmetric supercapacitor system (ASS) using the rGO@LCO as positive electrode and the rGO as negative electrode to explore the rGO@LCO nanocomposite as an efficient energy storage electrode material in the practical application. A comparative CV curves of different potential window ranges from 0–1 to 0–1.8 V at 50 mV s −1 are presented in Fig. 8a. It can be clearly observed that 0–1.7 V is the optimal voltage window selection, which is judged from the fact that 0–1.7 V is a stable voltage window and can avoid polarization phenomenon. Therefore, the CV curves and GCD curves based on the optimal voltage window are displayed in Fig. 8b, c, respectively. The oxidation-reduction peaks of CV curves and the asymmetric triangles of GCD curves confirm the formation of fine EDLC and faraday capacitance in rGO@LCO//rGO ASS. In addition, even if the scanning rate increases from 10 to 500 mV s −1 , the CV curves still maintain a similar shape, showing excellent characteristics of large current charging and discharging. Moreover, the less obvious IR drop on the GCD curves indicates that the electrode material has a very small resistance [44]. The energy and power densities of the rGO@LCO//rGO ASS derived from the GCD curves are also estimated and the results in the form of Ragone plot is displayed in Fig. 8d. Calculated by Eqs. (4) and (5), the rGO@LCO//rGO ASS delivers a high energy density of 17.62 W h kg −1 at a power density of 170 W kg −1 , which is mainly due to the improvement of specific capacitance and the extended voltage window. And even at power density as high as 4250 W kg −1 , the ASS still delivers a high energy density of 8.73 W h kg −1 , which is an attractive result and competitive compared to previous reports [45,46,47,48].
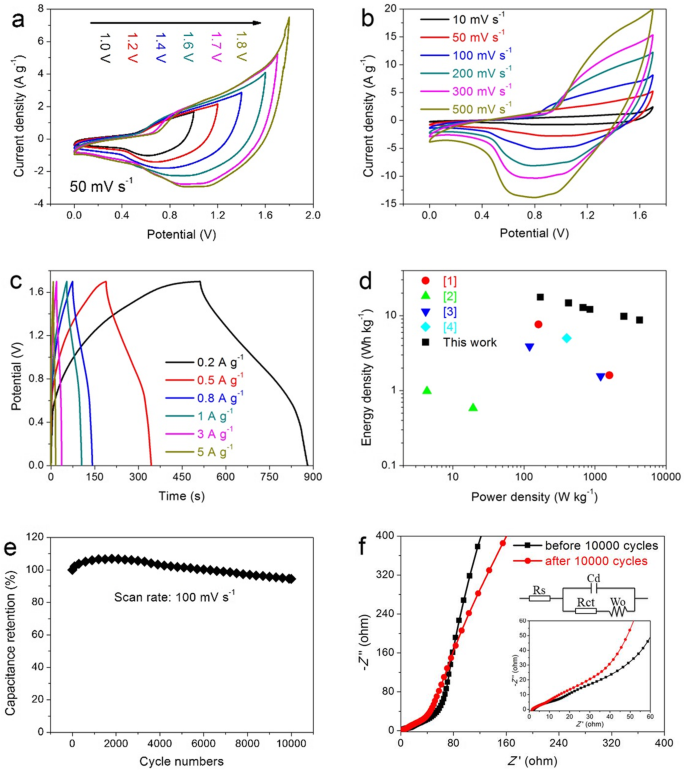
Electrochemical performances of rGO@LCO//rGO asymmetric supercapacitor system (ASS) in 6 M KOH electrolyte:a CV curves at various potential windows from 0–1.0 to 0–1.8 V with a scan rate of 50 mV s −1 . b CV curves. c GCD curves. d Ragone plot. e Cycle stability at 100 mV s −1 for 10,000 cycles. v Nyquist plots of rGO@LCO//rGO ASS before and after 10000 cycles
The ultra-long cycle stability is another important performance index of new energy storage devices. Therefore, we have conducted 10,000 cycle tests on rGO@LCO//rGO ASS at a large scanning rate of 100 mV s −1 , and the analysis result is presented in Fig. 8e. It can be seen that the specific capacitance of the first 2000 cycles increases gradually with the increase of the cycle numbers, up to 106.82% of the initial capacitance. This is mainly attributed to the continuous full penetration of the electrolyte, which promotes the activation of the internal reaction site more fully, thus resulting in the improvement of the capacitance. And with the number of cycles further increased to 10,000, the rGO@LCO//rGO ASS still retains 94.48% of the initial capacitance, showing excellent ultra-long cycle stability, which also means that the electrode material still has a stable nanostructure and is favorable for ion/electron transport under the condition of large current charge-discharge. Figure 8f shows the Nyquist plots of rGO@LCO//rGO ASS before and after 10,000 cycles. In contrast, the rGO@LCO//rGO ASS shows a smaller R ct and a slightly increased W o after 10,000 cycles, which further demonstrates the stable nanostructure of the electrode material. The above results show that the synthesized rGO@LCO nanomaterial electrode exhibits attractive electrochemical performance, which is comparable and superior to those previously reported literature in many cases (Table 2).
Conclusies
In summary, we successfully synthesized the perovskite LaCoO3 nanomaterials by a simple and usual sol-gel method followed by calcination, which is applied to electrode materials for supercapacitors and explored the influence of calcination temperature and time on their electrochemical properties. The results showed that the calcination temperature has a greater influence on the electrochemical properties than calcination time. Based on the optimal electrochemical properties of the LCO-700-4 electrode materials, the LSCO-0.2 and rGO@LCO nanocomposites were successfully synthesized by rational design. The results of the investigation of the electrochemical performance for these newly synthesized nanocomposites showed that the specific capacitance, rate capability, and conductivity of LSCO-0.2 and rGO@LCO are significantly enhanced, with the specific capacitance being 1.45 and 2.03 times of that of LCO-700-4 electrode, respectively. The practical performance of rGO@LCO composite electrode was further studied by assembling an asymmetric supercapacitor system (ASS) of aqueous electrolyte using rGO@LCO as the positive electrode and rGO as the negative electrode. The test results showed that the rGO@LCO//rGO ASS exhibits excellent energy and power density, as well as an outstanding cyclic stability with 94.48% of initial capacitance after 10,000 cycles. As a potential energy storage electrode material, LaCoO3 and LaCoO3 -based nanocomposites electrode with excellent electrochemical properties was worthy of further exploration, so as to make more breakthroughs and move toward practical application in green and efficient new energy storage devices.
Beschikbaarheid van gegevens en materialen
Alle gegevens zijn onbeperkt beschikbaar.
Afkortingen
- GO:
-
Grafeenoxide
- rGO:
-
Reduced graphene oxide
- LCO:
-
LaCoO3
- LSCO:
-
Sr-doping LaCoO3
- rGO@LCO:
-
rGO-compounding LaCoO3
- ASS:
-
Asymmetric supercapacitor system
- SCs:
-
Supercapacitors
- UCs:
-
Ultracapacitors
- EDLCs:
-
Electrical double layer capacitors
- DMF:
-
N ,N -Dimethylformamide
- PVP-K30:
-
Polyvinylpyrrolidon
- XRD:
-
X-ray power diffraction
- SEM:
-
Scanning elektronenmicroscoop
- TEM:
-
Transmissie-elektronenmicroscopie
- BET:
-
Brunauer-Emmett-Teller
- BJH:
-
Barrett-Joyner-Halenda
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- SCE:
-
Verzadigde calomelelektrode
- PTFE:
-
Polytetrafluorethyleen
- CV:
-
Cyclische voltammetrie
- GCD:
-
Galvanostatic charge/discharge
- EIS:
-
Elektrochemische impedantiespectroscopie
- R ct:
-
Charge transfer resistance
- W o:
-
Warburg impedance
- HRTEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- S BET :
-
Specific surface areas
- D DFT :
-
DFT desorption average pore diameter
Nanomaterialen
- Ontwerpen voor duurzaamheid:begin met het einde voor ogen
- Het belang van ontwerp voor productie
- Drie grote vragen voor iedereen die de arena voor energieopslag betreedt
- Het ontwerp van de emissielaag voor elektronenvermenigvuldigers
- Vooruitgang in op ijzeroxide gebaseerde nanostructuren voor toepassingen in energieopslag
- Synthese en elektrochemische eigenschappen van LiNi0.5Mn1.5O4-kathodematerialen met Cr3+ en F− composietdoping voor lithium-ionbatterijen
- De oppervlaktemorfologieën en eigenschappen van ZnO-films afstemmen door het ontwerp van grensvlakken
- Monodispergerende koolstofnanosferen met hiërarchische poreuze structuur als elektrodemateriaal voor supercondensator
- Een efficiënt en effectief ontwerp van InP-nanodraden voor maximale oogst van zonne-energie
- Gereduceerde grafeenoxide/koolstof nanobuiscomposieten als elektrochemische energieopslagelektrodetoepassingen
- Hydrothermische synthese en opconversie-eigenschappen van ongeveer 19 nm Sc2O3:Er3+, Yb3+ nanodeeltjes met gedetailleerd onderzoek van het energieoverdrachtsmechanisme



