Rationeel ontwerp van 3D-honingraatachtige SnS2 Quantum Dots/rGO-composieten als hoogwaardige anodematerialen voor lithium-/natrium-ionbatterijen
Abstract
Structuurverpulvering en slechte elektrische geleidbaarheid van metaaldichalcogeniden leiden tot ernstig capaciteitsverlies, zowel in lithium-ionbatterijen (LIB's) als in natriumionbatterijen (SIB's). Om de bovenstaande problemen op te lossen, heeft een combinatie van metalen dichalcogeniden met geleidende steigers als hoogwaardige elektrodematerialen de laatste tijd enorme belangstelling gewekt. Hierin synthetiseren we een 3D honingraatachtige rGO verankerd met SnS2 kwantumstippen (3D SnS2 QDs/rGO) composiet via sproeidrogen en sulfidatie. De unieke 3D-geordende honingraatachtige structuur kan de volumeverandering van SnS2 beperken QD's in de processen van lithiëring/delithiëring en sodiatie/desodiatie, bieden voldoende ruimte voor elektrolytreservoirs, bevorderen de geleidbaarheid van de SnS2 QD's, en het verbeteren van de elektronenoverdracht. Het resultaat is dat de 3D SnS2 QDs/rGO-composietelektrode levert een hoge capaciteit en lange cyclusstabiliteit (862 mAh/g voor LIB bij 0,1 A/g na 200 cycli, 233 mAh/g voor SIB bij 0,5 A/g na 200 cycli). Deze studie biedt een haalbare syntheseroute voor het voorbereiden van 3D-geordende poreuze netwerken in gevarieerde materialen voor de ontwikkeling van hoogwaardige LIB's en SIB's in de toekomst.
Achtergrond
Energieopslag speelt een opmerkelijke rol in het moderne leven. Li-ionbatterijen (LIB's) worden op grote schaal toegepast als stroombron voor draagbare elektronische apparaten en elektrische voertuigen vanwege hun lange levensduur en hoge energiedichtheid. Ondertussen hebben Na-ion-batterijen (SIB's) enorme aandacht getrokken in de opslag van hernieuwbare energie vanwege hun lage kosten en milieuvriendelijkheid. Hoewel de commerciële grafietanodes van LIB's een lage theoretische capaciteit (372 mAh/g) vertonen en last hebben van structurele instabiliteit en veiligheidsproblemen tijdens een snel laad-ontlaadproces, kunnen ze ook niet worden gebruikt in SIB's vanwege hun kleine ruimte tussen de lagen [ 1,2,3,4]. Daarom moeten er nieuwe anodematerialen met een hoge capaciteit worden ontwikkeld voor de volgende generatie LIB's en SIB's.
Metaaldichalcogeniden, die een hoge theoretische capaciteit hebben, zijn veelbelovende kandidaten voor het vervangen van het commerciële grafiet in LIB- en SIB-toepassingen. Onder de metalen dichalcogeniden, gelaagde SnS2 vertoont een hogere theoretische capaciteit dan grafiet en wordt beschouwd als een aantrekkelijk anodemateriaal. SnS2 is een typische CdI2 -type, waarbij elke laag voornamelijk door een zwakke Van der Waals-kracht met elkaar verbonden is. Een dergelijke functie maakt het een gewenste kandidaat voor intercalatie/de-intercalatie voor Li + en Na + in de eerste stap van de omzettingsreactie. Echter, SnS2 lijdt aan grote volumeverandering en slechte elektrische geleidbaarheid in het laad-ontlaadproces, wat resulteert in ernstig capaciteitsverlies.
SnS2 integreren met andere geleidende steigers om een rationele structuur te ontwerpen, werd met name een driedimensionaal (3D)-geordend poreus netwerk beschouwd als haalbare strategieën om de elektrische geleidbaarheid en fietsstabiliteit van LIB's en SIB's te verbeteren [5, 6]. Grafeen wordt beschouwd als een veelbelovende kandidaat voor steigers vanwege zijn uitstekende mechanische eigenschappen en elektronische geleidbaarheid. Ten eerste is een 3D-geordend poreus netwerk, vergeleken met 1D- en 2D-structuren, meer bevorderlijk voor het volledige contact tussen de elektrode en het elektrolyt. Het kan dus fungeren als een kanaal voor snel elektronentransport langs de 3D-richting en de aggregatie effectief beperken [7]. Ten tweede kunnen de rijke poriën in een 3D-geordend poreus netwerk de volume-uitbreiding in de driedimensionale ruimte verlichten, waardoor het een lange levensduurstabiliteit vertoont [8,9,10,11,12,13,14]. Zhu et al. ontworpen Co3 O4 met een 3D mesoporeus netwerk en vertoonde uitstekende prestaties in LIB's [15]. Deng et al. demonstreerde een nieuwe 3D-geordende macroporeuze MoS2 /carbon nanostructuur is gunstig voor het verkrijgen van hoge prestaties van LIB's [16]. Choi et al. gesynthetiseerde gelaagde WS2 met nanosheets versierde 3D-RGO-microsferen als anodemateriaal voor SIB's [17]. Op basis van de bovenstaande discussie hebben we een unieke 3D-honingraatachtige structuur ontworpen om de grote volumeverandering te bufferen en de elektrische geleidbaarheid van SnS2 te verbeteren. door sproeidrogen en sulfidering. Het composiet bereikt uitstekende elektrochemische prestaties in zowel LIB's als SIB's (862 mAh/g voor LIB bij 0,1 A/g na 200 cycli, 233 mAh/g voor SIB bij 0,5 A/g na 200 cycli).
De 3D-gestructureerde honingraatachtige rGO verankerd met SnS2 quantum dots composiet (3D SnS2 QDs/rGO) via een tweestapsmethode. Ten eerste, de 3D honingraatachtige rGO verankerd met SnO2 composiet (3D SnO2 /rGO) wordt gesynthetiseerd door sproeidrogen en nacalcineren. Vervolgens wordt het uitgegloeid met thioureum om de 3D SnS2 te verkrijgen QDs/rGO-composiet onder de argonatmosfeer. De 3D-honingraatachtige structuur kan de contactweerstand tussen de platen effectief verminderen, een groot toegankelijk actief oppervlak bieden voor de adsorptie/desorptie van ionen, de aggregatie van SnS2 beperken QD's en buffer de volume-uitbreiding van SnS2 QD's [18,19,20]. Het resultaat is dat de SnS2 QD's met een diameter van ~ 6 nm zijn gelijkmatig verdeeld in de rGO-laag na 200 laad-/ontlaadcycli in de LIB-test. Bovendien is de 3D SnS2 QDs/rGO-composietelektrode heeft een hoge capaciteit en een lange cyclusstabiliteit (862 mAh/g voor LIB bij 0,1 A/g na 200 cycli, 233 mAh/g voor SIB bij 0,5 A/g na 200 cycli). De unieke op metaalsulfide gebaseerde 3D-poreuze grafeenmaterialen die in deze studie worden gepresenteerd, bieden een manier voor de ontwikkeling van hoogwaardige LIB's en SIB's.
Methoden
Synthese van polystyreen nanosferen
Alle gebruikte reagentia waren van analytische kwaliteit en werden direct zonder enige zuivering gebruikt. Styreen werd alternatief gewassen met DI-water en 1 M NaOH om de polymeerremmers te verwijderen. Daarna 8 ml styreen, 92 ml DI-water en 0,2 g K2 S2 O8 werden gemengd en vervolgens 10 uur bij 80 ° C in argonatmosfeer geroerd. Tenslotte werd door centrifugeren een wit product verkregen. Na ten minste vijf keer wassen met gedemineraliseerd water en ethanol, werd het product 24 uur gevriesdroogd bij -50 °C [16].
Vervaardiging van 3D SnS2 QD's/rGO-composiet
In een typische synthese werd 24 g grafeenoxide (GO) colloïdaal (2,5 wt%) dat werd verkregen door de gemodificeerde Hummer-benadering toegevoegd aan 500 ml DI-water. Vervolgens werden 3 g polystyreen (PS) nanosferen gedispergeerd in de eerdere oplossing [21, 22]. Verder 1,5 g tin (IV) chloride-pentahydraat (SnCl4 . 5H2 O) werd in het mengsel geplaatst en gedurende 1 uur met ultrasoonapparaat behandeld. De mengseloplossing werd gesproeidroogd met een uitgangstemperatuur van 140 °C en een stroomsnelheid van 800 ml/u. Vervolgens werd het verzamelde product gedurende 2 uur bij 450 °C gegloeid met een oplopende snelheid van 3 °C min −1 in Ar-atmosfeer om PS-nanosferen te verwijderen, en vervolgens de 3D SnO2 /rGO is verkregen. Ten slotte werd thioureum, dat dienst doet als zwavelbron, gemengd met de SnO2 /rGO. En daarna werd het 12 uur gegloeid bij 350 °C met een verwarmingssnelheid van 2 °C min −1 in Ar-atmosfeer om de 3D SnO2 . te garanderen /rGO composiet volledig getransformeerd in 3D SnS2 QDs/rGO-composiet [23]. De pure SnS2 composiet werd gesynthetiseerd in afwezigheid van GO- en PS-nanobolletjes.
Karakterisering
De kristallijne structuur en fase van de composieten werden getest met röntgendiffractie (XRD, D8-Advance Bruker) met Cu-Kα-straling (λ =-1,5418 Å) bij 40 kV en 40 mA, variërend van 10 tot 80 ° C bij kamertemperatuur temperatuur. De chemische samenstelling van het oppervlak van de composieten werd geanalyseerd met een gemodificeerde röntgenfoto-elektronenspectroscopie (XPS, PHI 5600). De morfologieën en structuren werden onderzocht door veldemissie scanning elektronenmicroscoop (FESEM, JEOL S-4800) en transmissie-elektronenmicroscoop (TEM, JEOL JEM-2010). Het Brunauer-Emmett-Teller (BET) oppervlak en de poriegrootte werden geïdentificeerd met behulp van de stikstofadsorptie/desorptie-isothermen verkregen bij 77 K op een oppervlakte- en porositeitsanalysator (Quadrasorb SI-MP, Quantachrome). Het Raman-spectrum werd verkregen door een INVIA Raman-microsonde (Renishaw Instruments) met een laserbron van 532 nm en een objectieflens van × 50. De curve van de thermogravimetrische analysator (TGA) is uitgevoerd met een STD Q600 TA met 100 ml min −1 luchtstroom van 30 tot 800 °C bij een verwarmingssnelheid van 10 °C min −1 .
Elektrochemische test
Voor geprepareerde werkelektroden, 70 gew.% 3D SnS2 QD's/rGO-composiet, 20 gew.% acetyleenzwart en 10 gew.% polyvinylideenfluoride werden gemengd en opgelost in N -methyl-2-pyrrolidinon. Na 5 uur roeren werd de verkregen slurry gecoat op de koperfolie (fungeerde als een stroomcollector) en een nacht onder vacuüm bij 80 °C gedroogd. De elektrochemische tests werden uitgevoerd met behulp van twee-elektrodecellen die in een met argon gevulde handschoenenkast waren gemonteerd. Li- en Na-metalen fungeerden als de tegenelektrode. De organische elektrolyt in LIB's bestond uit 1,0 M LiPF6 in ethyleencarbonaat (EC) en diethylcarbonaat (DEC) (1:1, v /v ). Voor SIB's was de elektrolyt 1 M NaClO4 in een mengsel van EC/DEC (1:1, v /v ). Galvanostatische ladings- / ontladingsmetingen werden uitgevoerd door een batterijtestsysteem (NEWARE, Shenzhen Xinwei Electronics, Ltd) bij verschillende stroomdichtheden met een spanningsbereik van 0,01-3,00 V. Cyclische voltammetrie (CV) en de cyclische voltammogrammen werden geregistreerd over het potentiaalbereik van 0,01–3,00 V met een scansnelheid van 0,1 mV/s.
Resultaten en discussie
Schema 1 illustreert het syntheseproces van de 3D SnS2 QDs/rGO-composiet. Een colloïdale oplossing, bestaande uit uniform gedispergeerde GO-nanobladen, PS-nanosferen en tin (IV) chloride-pentahydraat wordt 6 uur bij kamertemperatuur geroerd. Om ervoor te zorgen dat er geen neerslag wordt gevormd, laat men de colloïdale oplossing enkele uren staan voordat deze wordt verneveld. Vervolgens wordt het Sn-zout-GO-PS-composiet in 10 s in de reactor gevormd (figuur 1a). Ten tweede, de 3D SnO2 /rGO-composiet wordt gesynthetiseerd door middel van calcinering in Ar-atmosfeer, zoals weergegeven in aanvullend bestand 1:Figuren S1a en S1b. Tijdens de vorming van de 3D SnO2 /rGO-composiet, de PS-nanosferen met een gemiddelde grootte van 200-300 nm fungeren als een opgeofferde sjabloon die uniform is verankerd op de rGO-lagen. Na calcinering resulteert de ontleding van de PS-nanosferen in holtes van 200-300 nm, wat leidt tot de vorming van een 3D-honingraatachtige structuur, zoals weergegeven in aanvullend bestand 1:figuur S1c. Ten slotte wordt thioureum gebruikt als zwavelbron en reductiemiddel om te reageren met de voorloper 3D SnO2 /rGO om honingraatachtige 3D SnS2 . te verkrijgen QDs / rGO-composiet (Fig. 1b, c). Het TEM-beeld in Fig. 1d demonstreert verder de 3D-honingraatachtige structuur, die consistent is met de morfologie die wordt gepresenteerd in de SEM-afbeeldingen. Bovendien zijn de verdunde lagen van rGO-nanobladen van de 3D SnS2 QDs/rGO-composiet kan duidelijk worden waargenomen in de TEM-afbeelding die wordt weergegeven in aanvullend bestand 1:figuur S1d. De ultrafijne SnS2 QD's met een grootte van enkele nanometers worden verdeeld binnen de 3D rGO-lagen, terwijl vergeleken Fig. 1e, f met aanvullend bestand 1:figuur S1d. Het vergrote TEM-beeld van de SnS2 QD's getoond in Fig. 1f geven duidelijke roosterranden aan, gescheiden door 0,32 nm, wat overeenkomt met het (100) vlak van SnS2 . De verdeling van Sn, S en C in de composiet was uniform, zoals weergegeven in Fig. 1g–j.
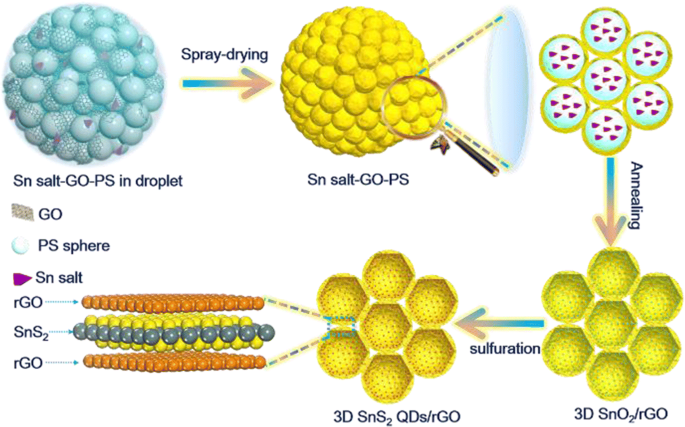
Schema van de fabricage van de 3D SnS2 QDs/rGO-composiet door sproeidrogen en zwaveling en het interface-microstructuurmodel van de SnS2 /rGO composiet

een SEM-afbeelding van de Sn salt-GO-PS-composiet. b SEM-afbeelding van de 3D SnS2 QDs/rGO-composiet. c Foto van een honingraatachtige structuur. d , e TEM-afbeeldingen van de 3D SnS2 QDs/rGO-composiet. v HRTEM-beeld van de 3D SnS2 QDs/rGO-composiet. g–j Elementaire afbeeldingsafbeeldingen van Sn-, S- en C-elementen
De XRD-patronen van rGO en de 3D SnS2 QD's / rGO-composiet worden getoond in Fig. 2a. De rGO presenteert drie diffractiepieken bij 2θ =-15,04 °, 26,14 ° en 44,52 °. De eerste piek behoort tot de karakteristieke piek van GO, die verder wordt geverifieerd door het volgende Raman-spectrum. De volgende twee pieken worden toegeschreven aan de (002) en (100) roostervlakken van het hexagonale grafeen (JCPDS No. 03-065-2023). De diffractiepieken van 3D SnS2 QDs/rGO kan worden waargenomen bij 15,0°, 28,2°, 30,26°, 41,9°, 49,96°, 58,35° en 70,33°, wat overeenkomt met de kristalvlakken (001), (100), (002), (102) , (110), (200) en (113) (JCPDS nr. 23-0677) van SnS2 , respectievelijk [24]. Vergeleken met de pure SnS2 getoond in Aanvullend bestand 1:Figuur S2a, de relatief brede diffractiepieken van de 3D SnS2 QD's/rGO-composiet duiden op kleinere deeltjesgroottes, die in overeenstemming zijn met de TEM-resultaten. Om de structuur van de 3D SnS2 . verder te onderzoeken QDs / rGO-composiet, de Raman-spectra van de composiet en rGO worden verkregen in Fig. 2b. De Raman-pieken van rGO die verschenen op 1596 en 1348 cm −1 worden respectievelijk toegeschreven aan de G- en D-banden van de koolstofstructuur. Over het algemeen is de D-band relevant voor de defecten van koolstofatomen in grafietlagen, terwijl de G-band behoort tot de rektrilling van -C=C- in een 2D hexagonaal rooster. Er verscheen een veel zwakkere piek op ongeveer 309 cm −1 in de 3D SnS2 QDs/rGO-composiet, wat overeenkomt met de karakteristieke piek van de A1g modus van de SnS2 fase [25]. Bovendien werd de D-band waargenomen op 1349 cm −1 en de G-band waargenomen op 1587 cm −1 behoorde tot 3D SnS2 QD's/rGO [26]. Terwijl de SnS2 de vermindering van GO kan beïnvloeden en de vermindering ervan kan belemmeren, vertoont de composiet een iets hogere intensiteit in D-piek dan rGO [27]. Een dergelijk resultaat kan ook de piek verklaren die verschijnt bij 2θ = 15,04° in XRD-patronen. Om het BET-oppervlak en de poriegrootte te onderzoeken, de interne porositeit en microstructuur van de als voorbereide 3D SnS2 QD's/rGO-composiet worden gemeten door stikstofadsorptie-desorptiemetingen. De opmerkelijke hysteresislussen van N2 adsorptie-desorptie-isothermen getoond in figuur 2c kunnen worden toegewezen aan de type IV-lus, die de standaard nanoporeuze structuur van de composiet aantoont. Het specifieke oppervlak van het composiet wordt berekend op 21,99 m 2 g −1 door een multi-point BET-methode te gebruiken volgens de adsorptietak van de isotherm. Als gevolg hiervan is de 3D SnS2 QD's/rGO-composiet met een dergelijke poriestructuur kan voor meer actieve plaatsen zorgen en is bevorderlijk voor de iondiffusie in het laad-/ontlaadproces [28, 29].
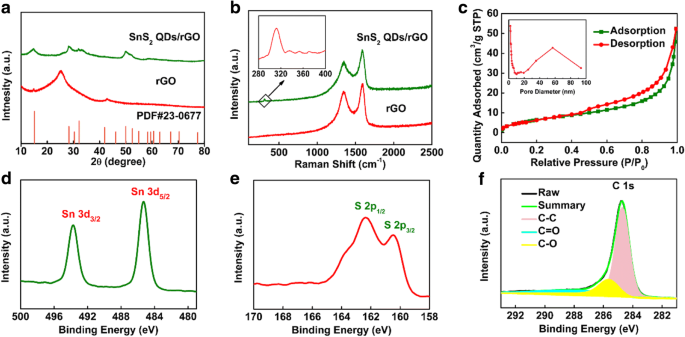
een XRD-patroon en b Raman-spectra van de rGO en 3D SnS2 QDs/rGO-composiet. c N2 adsorptie-desorptie-isothermen en de bijbehorende poriegrootteverdelingen van de 3D SnS2 QDs/rGO-composiet. XPS-spectra met hoge resolutie van d Sn 3d, e S 2p en f C 1 s van de 3D SnS2 QDs/rGO-composiet
De chemische samenstelling van het oppervlak en de oxidatietoestand van het composiet worden geanalyseerd door het XPS-systeem. In Fig. 2d worden de twee prominente pieken bij 487,3 en 495,7 eV toegeschreven aan Sn 3d3/2 en Sn 3d5/2 , respectievelijk. Het energieverschil tussen Sn 3d5/2 en Sn 3d3/2 is 8,4 eV, wat de Sn 4+ . aangeeft oxidatietoestand [30]. Het survey XPS S 2p-spectrum wordt weergegeven in Fig. 2e. De karakteristieke pieken die verschijnen bij 161.3 en 163.4 eV worden toegeschreven aan S 2p3/2 en S 2p1/2 voor S 2− in SnS2 [27, 31]. Het XPS-spectrum van C 1s getoond in figuur 2f kan worden aangepast en opgesplitst in drie verschillende pieken van respectievelijk 284,7, 285,7 en 288,1 eV. De drie pieken behoorden respectievelijk tot de C-C-, C-O- en C=O-bindingen [25, 32].
Het massapercentage van SnS2 in 3D SnS2 QDs / rGO-composiet werd uitgevoerd door TGA van 30 tot 800 ° C bij een verwarmingssnelheid van 10 ° C / min in lucht. In Aanvullend bestand 1:Afbeelding S4a, de 3D SnS2 QDs/rGO-composiet was volledig geoxideerd tot SnO2 boven 800 °C, wat een totaal gewichtsverlies van ongeveer 29,5% oplevert. Het proces van gewichtsverlies omvatte drie processen, namelijk de desorptie van watermoleculen (1,4%) geadsorbeerd op de 3D SnS2 QDs/rGO-composiet, oxidatie van SnS2 , en het achtereenvolgens verbranden van rGO. De gewichtspercentages van SnS2 in de 3D SnS2 QDs/rGO-composiet kan worden berekend op 83,7%, gebaseerd op het volledige gewichtsverlies van rGO-verbranding en het gedeeltelijke gewichtsverlies door de transformatie van SnS2 in SnO2 [28].
Onderzoek naar de lithiumopslagprocessen van de 3D SnS2 QDs/rGO en de pure SnS2 als anodematerialen voor LIB's worden hun CV-curven getest met een scansnelheid van 0,1 mV/s, zoals weergegeven in Fig. 3a, b. In figuur 3a worden de reductiepieken bij 1,0-1,5 V toegeschreven aan fase-ontleding, instorting van de structuur en vorming van een vaste elektrolytinterface (SEI) -laag. In Fig. 3b wordt de eerste reductiepiek bij 1,7 V toegewezen aan de intercalatie van Li + in de SnS2 nanostructuur tijdens de eerste cyclus [33]. De tweede reductiepiek bij 1,1 V wordt toegeschreven aan de ontbinding van SnS2 QD naar metallic Sn en Li2 S (zoals getoond in reactie (1)) [34]. De derde reductiepiek onder 0,5 V geeft het uiterlijk van Lix . aan Sn legeringen volgens reactie (2) en de Li + ingevoegd in de rGO gelaagde nanostructuur [35, 36]. Tijdens omgekeerd scannen geeft de eerste oxidatiepiek bij 0,52 V de ontlegering van Lix aan Sn volgens reactie (2). De tweede oxidatiepiek bij 1,8 V kan worden toegeschreven aan het feit dat de Li2 S kan gedeeltelijk ontleden en het Sn kan worden geoxideerd tot Sn 4+ (zie de omgekeerde reactie (1)) [34, 37, 38]. De reacties van de bovengenoemde zijn als volgt:
$$ \mathrm{Sn}{\mathrm{S}}_2+4{\mathrm{Li}}^{+}+4\ {\mathrm{e}}^{-}\to 2{\mathrm{Li }}_2\mathrm{S}+\mathrm{Sn} $$ (1) $$ \mathrm{Sn}+\mathrm{x}\ {\mathrm{Li}}^{+}+\mathrm{x} {\mathrm{e}}^{-}\leftrightharpoons {\mathrm{Li}}_x\mathrm{Sn}\ \left(0\le \mathrm{x}<4.4\right) $$ (2)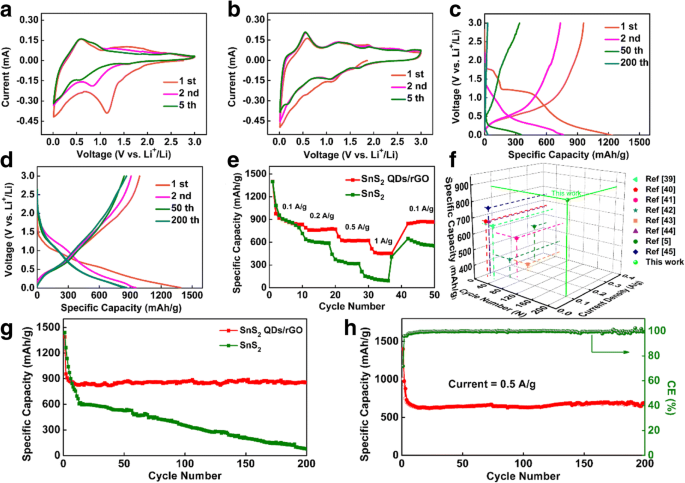
Elektrochemische prestaties van de pure SnS2 en 3D SnS2 QD's/rGO composietelektroden voor LIB's:a , b CV-curven van de pure SnS2 en 3D SnS2 QDs/rGO-composietelektroden met een scansnelheid van 0,1 mV/s gedurende de eerste vijf cycli. c Laad-/ontlaadcurven van de pure SnS2 composietelektrode en d de 3D SnS2 QDs/rGO-composietelektrode met een stroomdichtheid van 0,1 A/g in het spanningsbereik van 0,01–3,0 V vs. Li + /Li. e Beoordeel de prestaties van de 3D SnS2 QDs/rGO en pure SnS2 composietelektroden met snelheden van 0,1 tot 1 A/g. v Vergelijking van elektrochemische prestaties tussen de 3D SnS2 QDs/rGO-composiet (de huidige studie) en eerder gerapporteerde SnS2 -gebaseerd materiaalcomposiet. g Fietsprestaties van 3D SnS2 QDs/rGO en pure SnS2 composietelektroden met een stroomdichtheid van 0,1 A/g. u Fietsprestaties en Coulomb-efficiëntie van 3D SnS2 QDs/rGO-composietelektrode met een stroomdichtheid van 0,5 A/g
Merk op dat de intensiteiten van de reductiepieken van SnS2 drastisch afnemen in de tweede en vijfde scan. Daarentegen zijn de reductiepieken van de 3D SnS2 De QD's/rGO-elektrode overlappen elkaar perfect in de tweede en vijfde scan, wat de uitstekende elektrochemische omkeerbaarheid en stabiliteit suggereert.
Galvanostatische ladings-/ontladingsmetingen van de zuivere SnS2 en 3D SnS2 QDs/rGO-elektroden worden ook uitgevoerd bij een stroomdichtheid van 0,1 A/g tussen 0,01 en 3,00 V vs Li + /Li. De laad- / ontlaadcurven (1e, 2e, 50e en 200e cycli) worden respectievelijk getoond in Fig. 3c, d. In Fig. 3c, de laad-/ontlaadcurve van de zuivere SnS2 elektrode vertoont een drastische afname tot 16 mAh/g na de 200e cyclus. In Fig. 3d, de initiële ontladingscapaciteit voor de 3D SnS2 QDs/rGO-elektrode is 1400 mAh/g. Het is hoger dan de theoretische opslagcapaciteit van Li + (1231 mAh/g) van SnS2 berekend uit beide reacties (1) en (2) volgens de vergelijking van Faraday. Dit wordt toegeschreven aan de vorming van een SEI-laag op het oppervlak van de 3D SnS2 QDs/rGO-elektrode veroorzaakt door de onomkeerbare insertie van Li + en de ontleding van de elektrolyt [3]. Bij het verhogen van de cycli naar 2, 50 en 200, worden de capaciteiten van de 3D SnS2 QDs/rGO-elektrode wordt op respectievelijk 975, 867 en 870 mAh/g gehouden. Het is duidelijk dat de 3D SnS2 QDs/rGO-elektrode heeft een uitstekende laad-/ontlaadstabiliteit en een lange levensduur dan de pure SnS2 elektrode.
De snelheidsprestaties van de elektroden worden weergegeven in Fig. 3e. Het is te zien dat de ontlaadcapaciteit met een snelheid van 0,1, 0,2, 0,5 en 1 A/g respectievelijk 870, 770, 622 en 452 mAh/g is. Daarna keert het gemakkelijk terug naar 867 mAh/g bij 0,1 A/g, wat aangeeft dat de 3D SnS2 QD's/rGO-composiet is bestand tegen geleidelijke snelheidsvariaties en bezit een opmerkelijke elektrochemische stabiliteit en omkeerbaarheid. Terwijl de pure SnS2 De capaciteit van de elektrode neemt af tot 792, 587, 319 en 106 mAh/g, waarbij de ontladings-/oplaadsnelheden worden verhoogd tot respectievelijk 0,1, 0,2, 0,5 en 1 A/g. En het herstelt alleen naar 662 mAh/g wanneer de ontlaad-/oplaadsnelheid is hersteld tot 0,1 A/g. De uitstekende elektrochemische prestaties van 3D SnS2 QDs/rGO-composietelektroden worden verder weergegeven in Fig. 3g. De capaciteit van de pure SnS2 elektrode neemt drastisch af tot bijna 16 mA/g na 200 cycli, terwijl de 3D SnS2 QDs/rGO-elektrode kan na 200 cycli nog steeds een waarde van 870 mAh/g behouden bij een stroomdichtheid van 0,1 A/g. Bovendien wordt in Fig. 3h de test uitgevoerd om de betere fietsprestaties van de composiet aan te tonen bij een scansnelheid van 0,5 A/g. Na 200 laad-/ontlaadcycli bleef een hoge omkeerbare capaciteit van 622 mAh/g over en de gemiddelde Coulomb-efficiëntie is maar liefst 99,44%.
Om de langere levensduur van de 3D SnS2 . beter te begrijpen QDs/rGO-elektrode, wordt een TEM-beeld verkregen om de verdeling van de SnS2 te bewijzen QD's (in aanvullend bestand 1:figuur S3, door 100 representatieve deeltjes te meten met behulp van de Nano-Measure-software). De SnS2 QD's met ~ 6 nm zijn bijna gelijkmatig verankerd en beperkt binnen de rGO-lagen, wat wijst op een sterke adsorptie tussen SnS2 QD's en de rGO-lagen. Over het algemeen tonen de resultaten van zowel de elektrochemische test als de deeltjesverdeling aan dat de introductie van rGO en het 3D-honingraatachtige netwerk overvloedige lege ruimtes biedt voor volume-expansie van SnS2 QD's. Deze structuren fungeren als kanalen voor snel transport van elektronen langs alle drie de richtingen en beperken effectief de aggregatie. Zo worden de snelheidsprestaties en fietsstabiliteit van de composiet verbeterd. Afbeelding 3f toont een vergelijking van de elektrochemische prestaties tussen de 3D SnS2 QDs/rGO-composiet (de huidige studie) en de eerder gerapporteerde SnS2 -gebaseerde materialen composiet. Opgemerkt kan worden dat de capaciteit van 3D SnS2 QDs/rGO in ons onderzoek blijft 862 mAh/g LIB bij 0,1 A/g na 200 cycli, wat hoger is dan de andere rGO en SnS2 -gebaseerd materiaal, zoals grafeen-SnS2 hybriden [39], acetyleen zwart-SnS2 [40], SnS2 @gereduceerd grafeenoxide [41], mesoporeuze koolstof verankerd met SnS2 nanosheets [42], grafeen-SnS2 [43], SnS2 met nanodeeltjes geladen grafeem [44], SnS2 @graphene [5] en Ultrathin SnS2 nanodeeltjes op grafeen nanosheets [45].
Onderzoek naar de natriumopslagprocessen van 3D SnS2 QDs/rGO en pure SnS2 als anodemateriaal voor SIB's wordt cyclische voltammetrie uitgevoerd met een scansnelheid van 0,1 mV/s tussen 0,01 en 3,00 V vs Na + /Na, zoals weergegeven in Fig. 4a, b. In figuur 4a komt de reductiepiek bij 0,3-1,0 V overeen met de conversie, legeringsreacties (Vgl. (4) en (5)) en de vorming van de SEI-laag in de eerste cyclus. In figuur 4b komt de vrij brede piek bij ~-1,0 V in het eerste reductieproces overeen met de insertie van Na + in de SnS2 lagen (analoog aan die van Li-intercalatie) volgens Vgl. (3) [46, 47]:
$$ \mathrm{Sn}{\mathrm{S}}_2+\mathrm{x}\ {\mathrm{Na}}^{+}+{\mathrm{x}\mathrm{e}}^{-}\ naar {\mathrm{Na}}_{\mathrm{x}}\mathrm{Sn}{\mathrm{S}}_2 $$ (3) $$ {\mathrm{Na}}_{\mathrm{x} }\mathrm{Sn}{\mathrm{S}}_2+\left(4-\mathrm{x}\right){\mathrm{Na}}^{+}+\left(4-\mathrm{x}\ rechts){\mathrm{e}}^{-}\to \mathrm{Sn}+2{\mathrm{Na}}_2\mathrm{S} $$ (4) $$ \mathrm{Sn}+\mathrm {x}{\mathrm{Na}}^{+}+\mathrm{x}{\mathrm{e}}^{-}\to {\mathrm{Na}}_{\mathrm{x}}\mathrm {Sn} $$ (5)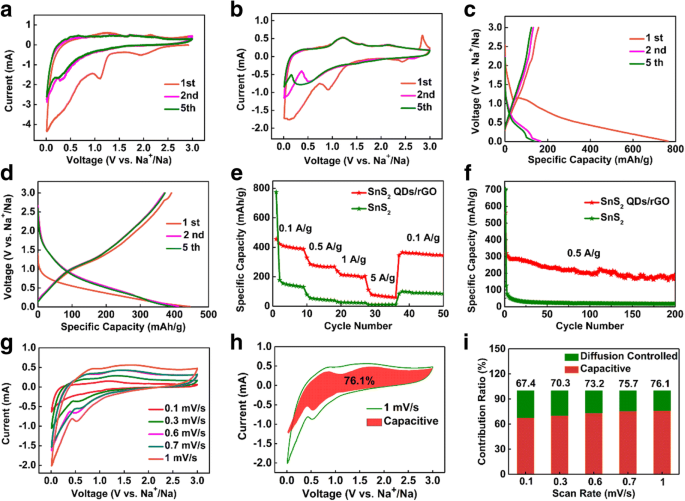
Elektrochemische prestaties van de pure SnS2 en 3D SnS2 QDs/rGO composiet elektroden voor SIBs. een , b CV-curven van de pure SnS2 elektrode en 3D SnS2 QDs/rGO-composietelektrode met een scansnelheid van 0,1 mV/s gedurende de eerste vijf cycli. c Laad-/ontlaadcurven van de pure SnS2 composietelektrode en d de 3D SnS2 QDs/rGO-composietelektrode met een stroomdichtheid van 0,1 A/g in het spanningsbereik van 0,01–3,0 V vs. Na + /Na. e Beoordeel de prestaties van 3D SnS2 QDs/rGO en de pure SnS2 composietelektrode met snelheden van 0,1 tot 5 A/g. v Fietsprestaties van 3D SnS2 QDs/rGO-composietelektrode en de pure SnS2 elektrode met een stroomdichtheid van 0,5 A/g. g CV-curven van 3D SnS2 QDs/rGO composietelektrode bij verschillende scansnelheden. u Capacitieve bijdrage bij de scansnelheid van 1 mV/s. ik Bijdrageverhouding van de capacitieve en diffusiegestuurde lading versus verschillende scansnelheden
Bij reverse scanning worden de onopvallende oxidatiepieken bij 0,35, 1,2 en 2,25 V toegeschreven aan de desodiatie van Nax sn. De voor de hand liggende oxidatiepiek bij 1,2 V behoort tot de veerkracht van de initiële 3D SnS2 QDs/rGO-elektrode [25]. Merk op dat de daaropvolgende CV-scans van 3D SnS2 QD's/rGO overlappen elkaar ruim na de eerste cyclus, wat wijst op een goede omkeerbaarheid ervan voor de sodiatie- en desodiatiereacties.
De ontlaad-laadspanningsprofielen van de pure SnS2 en 3D SnS2 QDs/rGO-elektroden worden uitgevoerd tussen 0,01 en 3 V bij een stroomdichtheid van 0,1 A/g. De corresponderende laad-/ontlaadprofielen (1e, 2e en 5e cyclus) worden respectievelijk getoond in Fig. 4c, d, die in overeenstemming zijn met de CV-resultaten. In figuur 4c verschijnt een opmerkelijk plateau bij ~-1,0 V in het ontladingsproces, behorend bij de vorming van Nax SnS2 . Het plateau bij 0,5-1,0 V wordt toegeschreven aan de omzetting, terwijl dat onder 0,5 V wordt toegeschreven aan de legeringsreacties tussen Na + en Sn. Vervolgens de CV-curve van de 3D SnS2 QDs/rGO-elektrode (Fig. 4d) geeft aan dat de onopvallende plateauspanning bij ~-1,0 V is toegewezen aan de intercalatie van Na + in SnS2 lagen tijdens het eerste ontladingsproces en deze reactie wordt uitgedrukt als Vgl. (3). Het hellingsplateau bij 0,3–1,0 V komt overeen met de conversiereactie (Vgl. (4)), de vorming van de SEI-laag door de onomkeerbare insertie van Na + en de ontleding van het elektrolyt. Het plateau onder 0,3 V komt overeen met de legeringsreactie (Vgl. (5)) [48,49,50]. De elektrode toont een plateau bij ~-1,0 V en een hellingsplateau bij ~-1,6 V in het laadproces, die ook in overeenstemming zijn met de CV-resultaten.
De snelheidscapaciteit van de pure SnS2 en 3D SnS2 QDs/rGO-elektroden van 0,1 tot 5 A/g in de SIB-test worden gegeven in Fig. 4e. De 3D SnS2 QDs/rGO-elektrode is in vergelijking opmerkelijk superieur. Het is te zien dat de ontladingscapaciteiten met een snelheid van 0,1, 0,5, 1 en 5 A/g respectievelijk 397, 286, 213 en 95 mAh/g zijn, en dan gemakkelijk terugkeren naar 393 mAh/g bij 0,1 A /G. Maar voor de pure SnS2 elektrode, neemt de ontladingscapaciteit af tot 180, 59, 25 en 11 mAh/g, terwijl de ontladingssnelheid wordt verhoogd tot respectievelijk 0,1, 0,5, 1 en 5 A/g. Dan komt de ontlaadcapaciteit pas weer op 102 mAh/g als de ontlaadsnelheid weer op 0,1 A/g komt. De 3D SnS2 QDs/rGO-elektrode vertoont kleine veranderingen in ontladingscapaciteit na ontlading bij verschillende stroomdichtheden, wat wijst op een betere veerkracht van de nanostructuur. Het is duidelijk dat de unieke 3D-honingraatachtige structuur Na + . mogelijk maakt transport met hoge stroomdichtheid zonder veel onomkeerbare veranderingen van de nanostructuur van de elektrode te veroorzaken, wat resulteert in uitstekende prestaties in SIB's. De ontlaadcapaciteit van de pure SnS2 electrode retains only 6 mAh/g after 200 cycles at a scan rate of 0.5 A/g, which is significantly lower than that 233 mAh/g in the 3D SnS2 QDs/rGO electrode, as presented in Fig. 4f. A serious capacity decay of the pure SnS2 electrode can result from the low electronic conductivity of the unsupported SnS2 and the uncontrollable aggregations of Sn (or its discharge products) during the cycling. Thus, the outstanding electrochemical performance of the electrode corresponds to the 3D honeycomb-like structure. The existing porous in the structure can efficiently adjust the volume change in the process of alloying and de-alloying.
To better understand the charge storage process, the CV curves at various scan rates (0.1–1 mV/s) are performed to understand the electrochemical process (Fig. 4g). A peak shift appears with the scanning rate rising from 0.1 to 1 mV/s, indicating the polarization of the electrode. The capacity contribution from capacitive and diffusion-controlled charge can be quantified according to the relation [51] i (V) = k1 v + k2 v 1/2 , where k1 v and k2 v 1/2 are the contributions from the capacitive and diffusion-controlled processes, respectively. From Fig. 4h, it can be observed that the capacitance-controlled capacity accounts for 76.1% of the total charge storage at a scan rate of 1 mV/s. With the scan rate increases in the order of 0.1, 0.3, 0.6, 0.7, and 1 mV/s, the proportion of the capacitance-controlled process increases from 67.4, 70.3, 73.2, 75.7, to 76.1%, respectively (Fig. 4i). The result indicates that the capacitive charge storage plays an important role in the total capacity of the electrode [52]. However, the relative rapid capacity decreases at higher scan rate is attributed to the diffusion-limited electrochemical energy conversion process [53].
The structural advantages of the 3D SnS2 QDs/rGO composite in LIBs and SIBs can be summarized as follows (Fig. 5):(i) the 3D structure can buffer the volume expansion and inhibit the agglomeration of SnS2 QDs during the charge/discharge process. (ii) The 3D honeycomb-like porous structure can provide sufficient space for electrolyte storage. (iii) The 3D interconnected network is beneficial for enhancing electron conductivity and allowing the electron to transfer quickly in the continuous paths. (iv) The SnS2 QDs with a particle size about ~ 6 nm can shorten the diffusion distance of Li + /Na + , resulting in good electrochemical performance.
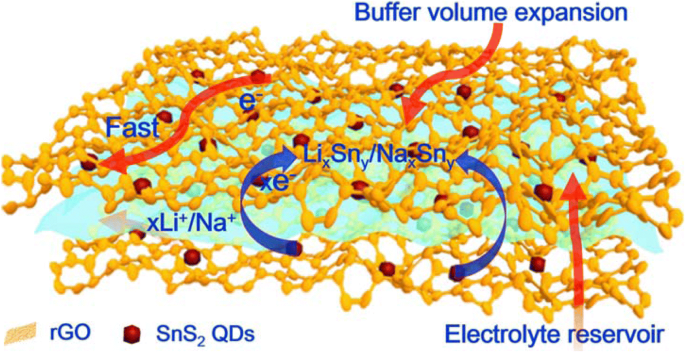
Schematic illustration highlights the structural benefits of the 3D SnS2 QDs/rGO composite during the charge/discharge process
Conclusies
A novel 3D honeycomb-like SnS2 QDs/rGO composite was synthesized by one-pot spray drying and sulfidation. The SnS2 QDs (~ 6 nm) was uniformly distributed in the rGO layers. The thicknesses of the rGO sheets could be regulated by changing the concentration of GO in the spray solution. What is more, the size of the rGO nanovoids could be easily adjusted by using different size of the PS nanospheres. The 3D honeycomb-like rGO could not only buffer the volume expansion of the SnS2 QDs but also enhance their poor electrical conductivity. In addition, it can provide enough space for electrolyte reservoirs. As a result, the retention of the reversible capacity of the 3D SnS2 QDs/rGO electrode for LIB at 0.1 A/g was nearly 862 mAh/g and the capacity was as high as 622 mAh/g after 200 cycles at 0.5 A/g. Moreover, a capacity of 233 mAh/g could be delivered after 200 cycles at 0.5 A/g in the SIB test. The novel 3D honeycomb-like SnS2 QDs/rGO composite suggested a new strategy for preparing anode material in LIBs and SIBs. This advanced anode materials is predicable to have a significant influence on the energy storage field, and thus, provide fresh opportunities to enhance the electrochemical performance of Li + and Na + storage devices.
Afkortingen
- 3D SnS2 QDs/rGO:
-
3D Honeycomb-like SnS2 Quantum Dots/rGO
- 3D:
-
Driedimensionaal
- BET:
-
The Brunauer–Emmett–Teller
- CV:
-
Cyclische voltammetrie
- DEC:
-
Diethyl carbonate
- EC:
-
Ethylene carbonate
- GO:
-
Grafeenoxide
- LIB's:
-
Lithium-ionbatterijen
- PS:
-
Polystyreen
- SEI:
-
Solid electrolyte interface
- SEM:
-
Veldemissie scanning elektronenmicroscoop
- SIB's:
-
Sodium-ion batteries
- TEM:
-
Transmissie elektronenmicroscoop
- TGA:
-
Thermogravimetrische analysator
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Tinnen nanokristallen voor toekomstige batterij
- S, N co-gedoteerde grafeen Quantum Dot/TiO2-composieten voor efficiënte fotokatalytische waterstofgeneratie
- Eenvoudige synthese van SiO2@C-nanodeeltjes verankerd op MWNT als hoogwaardige anodematerialen voor Li-ionbatterijen
- Een eenvoudige aanpak voor het synthetiseren van fluorescerende koolstofkwantumstippen uit tofu-afvalwater
- Een nanokristallijne Fe2O3-filmanode bereid door gepulseerde laserafzetting voor lithium-ionbatterijen
- Transformatie van slib Si naar nano-Si/SiOx-structuur door diffusie van zuurstof naar binnen als voorloper voor hoogwaardige anoden in lithium-ionbatterijen
- Humaat-geassisteerde synthese van MoS2/C-nanocomposieten via co-precipitatie/calcineringsroute voor hoogwaardige lithium-ionbatterijen
- Synthese en onderzoek van CuGeO3-nanodraden als anodematerialen voor geavanceerde natrium-ionbatterijen
- Ontwerp van door spanning ontworpen GeSn/GeSiSn Quantum Dots voor Mid-IR Direct Bandgap Emission op Si-substraat
- Mesoporeuze siliciummicrosferen geproduceerd uit in situ magnesiothermische reductie van siliciumoxide voor hoogwaardig anodemateriaal in natrium-ionbatterijen
- Rationeel ontwerp van Ni(OH)2 holle poreuze architectuur voor hooggevoelige enzymvrije glucosesensor



