Humaat-geassisteerde synthese van MoS2/C-nanocomposieten via co-precipitatie/calcineringsroute voor hoogwaardige lithium-ionbatterijen
Abstract
Er is een gemakkelijke, kosteneffectieve, niet-toxische en oppervlakteactieve stofvrije route ontwikkeld om MoS2 te synthetiseren /koolstof (MoS2 /C) nanocomposieten. Kaliumhumaat bestaat uit een grote verscheidenheid aan zuurstofbevattende functionele groepen, die worden beschouwd als veelbelovende kandidaten voor functionalisering van grafeen. Kaliumhumaat gebruiken als koolstofbron, tweedimensionale MoS2 /C-nanobladen met een onregelmatige vorm werden gesynthetiseerd via een gestabiliseerd co-precipitatie / calcinatieproces. De elektrochemische prestatie van de monsters als anode van een lithium-ionbatterij werd gemeten, wat aantoont dat de MoS2 /C nanocomposiet gecalcineerd bij 700 °C (MoS2 /C-700) elektrode vertoonde uitstekende prestaties met een hoge ontladingscapaciteit van 554,9 mAh g − 1 bij een stroomdichtheid van 100 mA g − 1 en de Coulomb-efficiëntie van het monster handhaafde een hoog niveau van ongeveer 100% na de eerste 3 cycli. Tegelijkertijd moet de MoS2 De /C-700-elektrode vertoonde goede fietsstabiliteit en snelheidsprestaties. Het succes bij het synthetiseren van MoS2 /C-nanocomposieten via co-precipitatie/calcinatieroute kunnen een nieuwe manier zijn om veelbelovende anodematerialen voor hoogwaardige lithium-ionbatterijen te realiseren.
Achtergrond
Vanwege hun hoge energiedichtheid, lange levensduur en milieuvriendelijkheid worden lithium-ionbatterijen (LIB's) veel gebruikt in draagbare elektronische apparaten [1] (bijv. mobiele telefoons en horloges), elektrische voertuigen [2, 3] en hernieuwbare energieopslag [4,5,6,7,8]. Grafiet is het meest gebruikte anodemateriaal in commerciële LIB's en profiteert van zijn lage werkspanning, goede geleidbaarheid en lage kosten [9,10,11]. De karakteristieke structuur van grafiet leidt echter tot een haalbare generatie van LiC6 , waardoor slechts één lithiumion-intercalatie per zes koolstofatomen mogelijk is, wat resulteert in een lage theoretische specifieke capaciteit van 372 mAh g − 1 , wat ver verwijderd is van de huidige zakelijke vereisten [12].
Momenteel verdient het de voorkeur om geschikte elektrodematerialen in LIB's te verkrijgen voor een hogere batterijcapaciteit, een langere levensduur en een beter snelheidsvermogen. Dientengevolge worden anodematerialen op basis van Li-legeringen [13], overgangsmetaaloxiden [14], oxyzouten en overgangsmetaalsulfiden [15] vaak gediend als anodematerialen in LIB's, aangezien deze materialen alle noodzakelijke eigenschappen vertonen voor een geschikte elektrode materialen. Onder deze materialen zijn overgangsmetaalsulfiden (bijv. CuS2 [16], WS2 [17], en MoS2 [18,19,20] waren een opwindend onderwerp in onderzoek omdat ze overvloedig aanwezig zijn op aarde en een hoge specifieke capaciteit vertonen wanneer ze worden gebruikt als anodematerialen in LIB's [21]. Als een typische vertegenwoordiger, MoS2 heeft veel aandacht gekregen vanwege zijn specifieke S-Mo-S gelaagde structuur [22], hoge theoretische specifieke capaciteit in vergelijking met traditionele grafietanode, en er is een overdrachtsreactie van vier elektronen wanneer gebruikt als anodematerialen in LIB's [23, 24]. Bovendien hebben de van der Waals-krachten tussen de MoS2 lagen zijn erg zwak, waardoor diffusie van lithium-ionen mogelijk is zonder een significante volumeverandering te veroorzaken [25, 26]. Echter, MoS2 is nog steeds een onbevredigend anodemateriaal vanwege de lage elektrische geleidbaarheid, wat leidt tot slechte cyclische en snelheidsprestaties [27]. Om dit probleem op te lossen, zijn een aantal strategieën ontwikkeld om de elektrische geleidbaarheid te verbeteren, zoals de opname van MoS2 met koolstofmaterialen [28,29,30].
Tot op heden een verscheidenheid aan MoS2 /koolstofcomposieten zijn gesynthetiseerd als anodematerialen in LIB's, namelijk gelaagde MoS2 /grafeencomposieten [31], MoS2 /C meerlagige nanobolletjes [32], MoS2 -CNT composiet [33], meerlagig grafeen/MoS2 heterostructuren [34], of bloembladachtige MoS2 nanosheets in de ruimte beperkt in holle mesoporeuze koolstofbollen [35]. Ondanks bevredigende vooruitgang in elektrische geleidbaarheid, cyclische en snelheidsprestaties van de elektrode, zijn enkele andere conflicten in de synthesemethode blijven bestaan. Op dit moment is de meest gebruikte synthetische methode de hydrothermische benadering gevolgd door een gloeiproces, dat een koolstofmatrix kan introduceren met sommige oppervlakteactieve stoffen zoals natriumoleaat of oleyamine en zwavelelement met wat L-cysteïne in de eerste procedure. Bovendien waren dure en giftige organische reagentia altijd onmisbaar en onvermijdelijk tijdens het syntheseproces in vergelijking met de co-precipitatiemethode. Momenteel begint de co-precipitatiemethode net aan populariteit te winnen bij de synthese van anorganische nanogestructureerde materialen vanwege zijn kosteneffectieve, niet-toxische, betrouwbare en stabiele [36, 37]. Voor zover ons bekend, is er weinig gerapporteerd over de synthese van MoS2 /C nanocomposiet door co-precipitatie/calcinatieproces, vooral met kaliumhumaat.
Kaliumhumaat, een soort aromatisch hydroxycarboxylaat, dat bestond uit een grote verscheidenheid aan zuurstofbevattende functionele groepen, kan worden beschouwd als gefunctionaliseerde grafeenkandidaat [38]. Over het algemeen is er veel onderzoek gedaan naar het gebruik van kaliumhumaat als koolstofbron om koolstofmaterialen te synthetiseren onder extreem zware omstandigheden [38, 39]. Huang [38] rapporteerde dat kaliumhumaat ongecompliceerde carbonisatie kan zijn om gereduceerde grafietoxidematerialen te bereiden. In dit artikel, MoS2 /C-nanocomposieten werden gesynthetiseerd via een co-precipitatie/calcineringsroute, door gebruik te maken van een organische stof (kaliumhumaat) en een anorganische stof ((NH4 )6 Ma7 O24 ) als reagentia. De elektrochemische prestatie van de monsters als LIBs-anode werd gemeten en de resultaten toonden aan dat het monster calcineerde bij 700 °C (MoS2 /C-700) vertoonden beter fietsvermogen en snelheidsgedrag. De ontlaadcapaciteit van het monster bleef op 554,9 mAh g − 1 na 50 cycli bij de stroomdichtheid van 100 mA g − 1 , wat veel beter is dan de andere twee monsters die zijn gecalcineerd bij respectievelijk 600 ° C en 800 ° C. Ondertussen, de zoals voorbereide MoS2 /C-700 vertoont vergelijkbare elektrochemische prestaties [40, 24].
Methoden/experimenteel
Kaliumhumaat werd verkregen van Double Dragons Humic Acid Co., Ltd. Xinjiang (China), en de samenstellingsanalyse van kaliumhumaat werd getoond in Aanvullend bestand 1:Tabel S1. Alle chemische reagentia (behalve kaliumhumaat) waren van zuiver analytische kwaliteit en werden zonder verdere zuivering gebruikt.
Synthese van MoS2 /C
De voorloper werd bereid door co-precipitatie van (NH4 )6 Ma7 O24 en kaliumhumaat in aanwezigheid van HNO3 gevolgd door een gevriesdroogd proces gedurende 2 dagen. In een typische procedure werd 4 g kaliumhumaat opgelost in 40 ml 0,25 M (NH4 )6 Ma7 O24 oplossing. Vervolgens werd de bovengenoemde oplossing druppelsgewijs toegevoegd aan 100 ml 0,5 M HNO3 oplossing onder krachtig magnetisch roeren. De duur van het magnetisch roeren was enkele uren. De lagere precipitatie werd vervolgens gescheiden van de mengseloplossing, gevriesdroogd en gelabeld als Mo-HA-voorloper. De voorloper werd gemengd met watervrij Na2 SO4 (met een verhouding van 1:10) en vermalen in een vijzel tot een homogeen mengsel. Het mengsel werd vervolgens 3 uur bij 700 °C gecalcineerd (met een verwarmingssnelheid van 10 °C min − 1 ) en vervolgens natuurlijk afgekoeld tot kamertemperatuur. Ten slotte werden de producten drie keer gewassen met gedeïoniseerd water en ethanol, gevolgd door een gevriesdroogde procedure om de MoS2 te verkrijgen. /C poeder. Tegelijkertijd werden ook de bij 600 en 800 °C gecalcineerde monsters gesynthetiseerd.
Karakterisering
De oppervlakte-organische functionele groepen van kaliumhumaat werden gemeten met een Fourier-transformatie-spectrofotometer (FT-IR, VERTEX 70, Bruker) met KBr als referentiemonster. De structuur en morfologie van verschillende monsters werden gekarakteriseerd door röntgendiffractie (XRD, BRUKER D8 Advance) met Cu Kα-straling (λ = 1.54178 Å), transmissie-elektronenmicroscopie (TEM, Hitachi H-600), transmissie-elektronenmicroscopie met hoge resolutie (HRTEM, JEM-2100F), LEO 1450VP scanning-elektronenmicroscoop (SEM), energiedispersieve röntgenspectrometer (EDX) en röntgenfoto-elektronspectroscopie (XPS, ESCALAB 250Xi-spectrometer). Thermogravimetrische analyses (TGA) werden uitgevoerd op een thermogravimetrische analysator (Netzsch TGA 409). Raman-spectrum werd uitgevoerd op Bruker Senterra met een golflengte van 532 nm.
Elektrochemische metingen
Elektrochemische metingen werden uitgevoerd op muntcellen. De werkelektroden werden vervaardigd door 80 gew.% van het bereide MoS2 te mengen /C actieve materialen, 10 gew.% acetyleenzwart en 10 gew.% polyvinylideenfluoride (PVDF) in N-methyl-2-pyrrolidinon (NMP) oplosmiddel om een homogene slurry te vormen. De slurry werd gecoat op de koperfolie en 12 uur onder vacuüm bij 110°C gedroogd. De muntcellen werden geassembleerd in een met argon gevulde handschoenenkast. Bij de meting werd lithiumfolie gebruikt als tegenelektrode en referentie-elektrode, en een polypropyleenfilm (Celgard-2400) als separator. De elektrolytoplossing was 1 mol L − 1 LiPF6 in ethyleencarbonaat (EC), dimethylcarbonaat (DMC) en diethylcarbonaat (DEC) (EC/DMC/DEC, 1:1:1, volumeverhouding). De galvanostatische lading-ontladingsmetingen werden uitgevoerd in een potentieel bereik van 0,01-3,0 V met behulp van een LAND CT2001A-batterijtestinstrument (Wuhan) bij kamertemperatuur. Cyclische voltammetrie (CV) metingen werden uitgevoerd op een elektrochemisch werkstation (CHI 660D) met een scansnelheid van 0,1 mV s − 1 tussen 0,01 en 3,0 V.
Resultaten en discussie
De oppervlaktechemie van kaliumhumaat werd bestudeerd met behulp van het FTIR-spectrum. In Fig. 1a zijn de brede pieken gecentreerd op 3400 cm − 1 werden toegeschreven aan de rektrillingen van −OH, −COOH en H2 O-obligaties, de pieken bij 1627, 1413 en 1050 cm − 1 werden toegeschreven aan de rektrillingen van respectievelijk de −COO-groepen en −CH, −OH enzovoort [41], wat wijst op de rijke zuurstofbevattende functionele groepen op het oppervlak van zuiver kaliumhumaat, wat gunstig is voor de complexeringsreactie of adsorptie . TGA-curve van het homogene mengsel van Mo-HA-precursor en watervrij Na2 SO4 (met een verhouding van 1:10) in een argonatmosfeer met een verwarmingssnelheid van 10 °C min − 1 wordt getoond in Fig. 1b. Het is te zien dat er drie stappen van gewichtsverlies zijn in de TGA-curve. Het eerste gewichtsverlies is 1,59% van kamertemperatuur tot 250 °C, wat te wijten kan zijn aan ontleding van het water in het oppervlak van de Mo-HA-precursoren. Er zijn nog twee opeenvolgende stappen van gewichtsverlies, met een gewichtsverlies van 1,35% van 250 tot 500 °C en een gewichtsverlies van 3,17% van 500 tot 800 °C, en dan blijft de massa constant, wat aangeeft dat de voorloper volledig ontleed bij 800 ° C. Voor een dergelijk systeem kiezen we die drie temperaturen voor calcineren als 600, 700 en 800 °C, aangeduid als MoS2 /C-600, MoS2 /C-700 en MoS2 /C-800, respectievelijk.
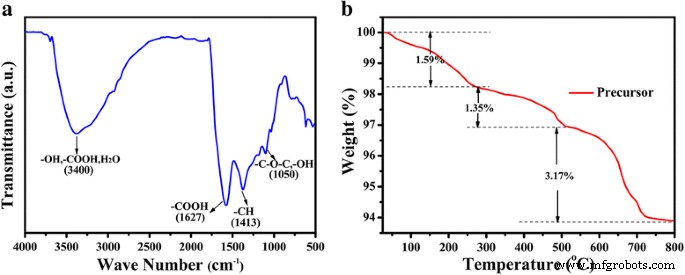
een FT-IR-spectra van zuiver kaliumhumaat. b TGA-curve van het homogene mengsel van Mo-HA-precursor en watervrij Na2 SO4 (met een verhouding van 1:10)
Volgens de literatuur [34] is een mogelijk mechanisme van het reactieproces voorgesteld en schematisch weergegeven in Schema 1. Bovendien staan de corresponderende formules vermeld in Aanvullend bestand 1:Vergelijkingen 1-5. In deze vergelijkingen werd kaliumhumaat afgekort als K-HA. Er kan een complexering zijn wanneer kaliumhumaat wordt opgelost in (NH4 )6 Ma7 O24 oplossing, met medewerking van HNO3 oplossing, die leidt tot de vorming van Mo-HA. Na verwarming van het mengsel van de Mo-HA-precursor en watervrij Na2 SO4 in een argonatmosfeer bij een relatief hoge temperatuur zou de Mo-HA-precursor worden verkoold om het tussenproduct van amorfe koolstof te vormen, en dan zou het tussenproduct watervrij Na2 reduceren SO4 om Na2 . te genereren S, verder gehydrolyseerd tot zwavelwaterstof. Ten slotte kan zwavelwaterstof reageren met MoOx , wat leidde tot de vorming van MoS2 /C nanocomposieten.
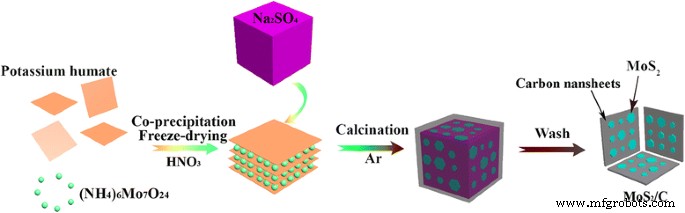
Schema's die de fabricageprocedure van MoS2 . weergeven /C nanocomposiet
Afbeelding 2a–b toont de XRD-patronen en Raman-spectra van de MoS2 /C nanocomposieten gecalcineerd bij verschillende temperaturen. Figuur 2a laat zien dat bijna alle diffractiepieken van MoS2 /C-600 en MoS2 /C-700 kan goed worden geïndexeerd met de hexagonale MoS2 fase (JCPDS-kaart nr. 86-2308), wat consistent is met die van het vorige rapport [42]. Er zijn nog enkele andere pieken die niet overeenkomen met de standaardkaart in de MoS2 /C-800 monster. We speculeren dat het kristallijne van MoS2 /C is vernietigd bij hoge temperatuur. Uit de Raman-spectra (Fig. 2b) is te zien dat de pieken tussen 379 en 400 cm − 1 behoorde tot E 1 2g (de verplaatsing in het vlak van Mo- en S-atomen) en A 1g (Out-of-plane symmetrische verplaatsing van Mo- en S-atomen) Raman-modi, respectievelijk [24, 43]. De banden verschenen op 1347 en 1589 cm − 1 waren de karakteristieke D- en G-band, en de waarde van I D /Ik G waren 0,96, 0,91 en 0,94 naarmate de temperatuur van 600 tot 800 °C gaat. De eerste komt overeen met de amorfe koolstof of sp 3 -gehybridiseerde koolstof (D-band), en de laatste toegewezen aan de sp 2 -gehybridiseerde koolstof (G-band) [44]. Hoewel er geen groot onderscheid is tussen de mate van grafitisering, is de MoS2 /C-700-monster is tot op zekere hoogte nog steeds iets hoger dan de andere twee monsters, wat aangeeft dat de koolstof in dit monster niet alleen in de vorm van amorfe koolstof is, maar ook enige grafietkoolstof. Daarom hebben we ons gericht op de MoS2 /C-700 monster in de volgende onderzoeken.
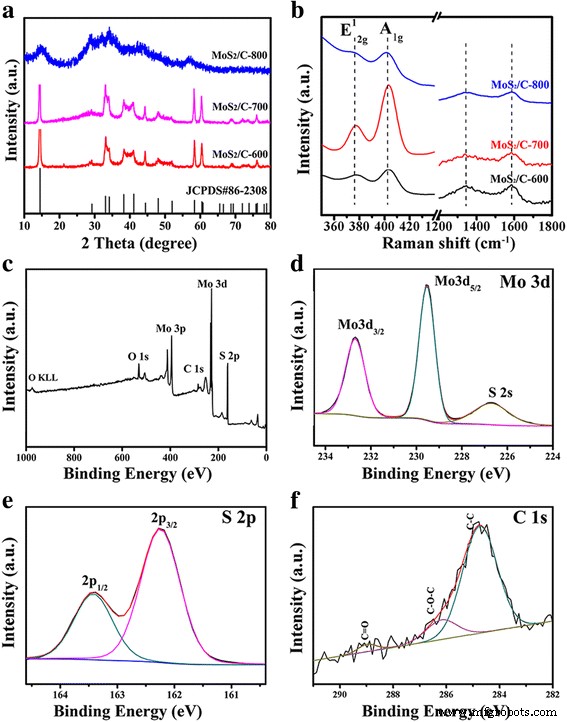
een XRD-patronen. b Raman-spectra van MoS2 /C nanocomposieten gecalcineerd bij verschillende temperaturen. c Onderzoek XPS-spectra van MoS2 /C-700. d XPS-spectra met hoge resolutie van Mo 3d. e S 2p. v C 1 s
Om de chemische samenstelling en chemische bindingen van MoS2 . verder te bestuderen /C-700, Röntgenfoto-elektronspectroscopie (XPS)-analyse werd uitgevoerd. Het XPS-spectrum van het onderzoek (Fig. 2c-f) onthult de aanwezigheid van Mo-, S-, C- en O-elementen in de MoS2 /C-700 nanocomposiet. De XPS-spectra met hoge resolutie van Mo 3d en S 2p worden respectievelijk getoond in Fig. 2d, e. De pieken bij 229,4 en 232,6 eV worden toegewezen aan de Mo 3d5/2 en Mo 3d3/2 , wat het bestaan van Mo in MoS2 . bevestigt /C-700 [45, 46]. De aanwezigheid van een andere XPS-piek bij 226,5 eV is geïndexeerd op S 2 s, die het gevolg is van het oppervlak van de MoS2 /C-700 [47]. Bovendien zijn de XPS-pieken bij 162,3 en 163,4 eV in S 2p-spectra karakteristieke pieken van de S 2p3/2 en S 2p1/2 van MoS2 , respectievelijk. Figuur 2f laat zien dat het spectrum van C1 kan worden verdeeld in drie pieken, respectievelijk aangeduid als C–C, C–O en C=O-groepen.
Het EDX-spectrum geeft aan dat het bij 700 °C gecalcineerde monster Mo-, S- en C-elementen bevat, zoals weergegeven in figuur 3a. Afbeelding 3b, c toont de SEM-afbeeldingen van het monster van MoS2 /C-700. Ter vergelijking:de SEM-afbeeldingen van MoS2 /C-600 nanocomposiet en MoS2 /C-800 nanocomposiet werden ook getoond in Aanvullend bestand 1:Afbeelding S1. Om de corresponderende elementverdeling in de steekproef van MoS2 . te onderzoeken /C-700, werden de overeenkomstige elementaire mapping-analyses uitgevoerd. Zoals getoond in Fig. 4a–d, zijn de elementaire afbeeldingsafbeeldingen van MoS2 /C-700 demonstreerde de uniforme verdeling van Mo, S en C over de hele MoS2 /C-700 nanocomposiet, wat consistent is met de EDX- en XPS-resultaten.

een EDX-spectrum van MoS2 /C-700. b , c SEM-afbeeldingen van MoS2 /C-700 nanocomposiet

een -d Elementaire afbeeldingsafbeeldingen van MoS2 /C-700; (e ) TEM-afbeelding, (f ) de SAED en (g ) TEM-beeld met hoge resolutie van MoS2 /C-700 nanocomposiet, (h ) Vergrote HR-TEM-afbeelding van het gemarkeerde gebied in afbeelding (g )
Zoals weergegeven in Fig. 4e-h, de morfologie en structuur van de gesynthetiseerde MoS2 /C-nanocomposieten werden onderzocht met transmissie-elektronenmicroscopie (TEM), geselecteerde gebiedselektronendiffractie (SAED) en transmissie-elektronenmicroscopie met hoge resolutie (HRTEM). De TEM-afbeelding (Fig. 4e) en de SEM-afbeeldingen (Fig. 3b, c) laten duidelijk zien dat de structuur van MoS2 /C-700 nanocomposiet is gerimpelde tweedimensionale nanosheets met een breedte van ~ 800 nm en een dikte van ~ 20 nm. SAED-patroon in Fig. 4f laat zien dat de hexagonale roosterstructuur van MoS2 is goed gekristalliseerd. Verder werden de kristalroosters van het monster getoond op HRTEM-profielen ((afb. 4g, h) en aanvullend bestand 1:figuur S2). De profielen vertoonden zeer kristallijne MoS2 nanosheets met een tussenlaagafstand van 0,27 nm overeenkomend met (100) vlak van hexagonaal MoS2 [24, 34]. Bovendien laat aanvullend bestand 1:figuur S2 duidelijk zien dat de koolstofnanobladen waren versierd met MoS2 nanobladen.
Afbeelding 5a toont de CV-curven van de eerste 3 cycli van MoS2 /C-700 elektrode met een scansnelheid van 0,1 mV s − 1 in het potentiaalvenster van 0,01–3,00 V vs. Li + /Li. Tijdens de eerste cyclus geeft de reductiepiek bij 1,0 V het lithium-insertiemechanisme aan, dat te wijten is aan de insertie van lithiumionen in de MoS2 lagen om Lix . te vormen MoS2 . Tegelijkertijd heeft er een faseovergang plaatsgevonden van 2H (trigonaal prismatisch) naar 1T (octaëdrisch) [48]. Een andere reductiepiek bij 0,4 V wordt toegeschreven aan de omzetting van Lix MoS2 in metallic Mo en Li2 S. De brede oxidatiepiek bij 2,35 V vertegenwoordigt de de-intercalatie van Li2 S tot S. Tijdens de daaropvolgende cycli verdwijnen de twee kathodische pieken bij 1,0 en 0,4 V en verschijnen er drie nieuwe pieken bij 2,0, 1,2 en 0,3 V, wat wijst op de reductie van MoS2 en de conversie van S8 naar polysulfiden en vervolgens naar Li2 S [24].
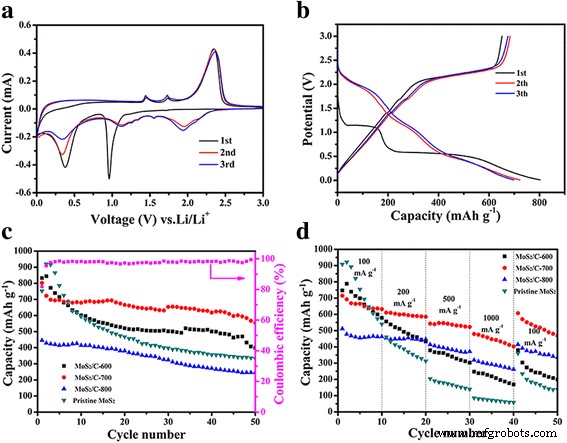
een CV-curven van de eerste drie cycli van MoS2 /C-700 elektrode met een scansnelheid van 0,1 mV s − 1 . b Ontlaad- en laadcurves van de eerste 3 cycli van MoS2 /C-700 elektrode met een stroomdichtheid van 100 mA g − 1 . c Fietsprestaties MoS2 /C-elektrode en de ongerepte MoS2 elektrode met een stroomdichtheid van 100 mA g − 1 , en Coulomb-efficiëntie van MoS2 /C-700 elektrode. d Prestaties beoordelen van MoS2 /C en de ongerepte MoS2 elektrode met stroomdichtheden variërend van 100 tot 1000 mA g − 1
De ontlaad- en laadcurves van de eerste 3 cycli van MoS2 /C-700-elektrode werden opgenomen en de overeenkomstige resultaten werden getoond in Fig. 5b. In de eerste cyclus zijn de ontlaad- en laadcapaciteiten van MoS2 /C-700-elektroden zijn 802.8 en 651.4 mAh g − 1 , respectievelijk, met een Coulomb-efficiëntie van 81,14%. Het onomkeerbare capaciteitsverlies kan te wijten zijn aan een onomkeerbare reactie zoals de ontleding van elektrolyt en de vorming van een vaste elektrolytinterface (SEI) film [49, 50].
De cyclusstabiliteit van hele MoS2 /C-elektrode en de ongerepte MoS2 elektrode met een stroomdichtheid van 100 mA g − 1 worden weergegeven in Fig. 5c. Tegelijkertijd is de Coulomb-efficiëntie van MoS2 /C-700 is ook opgenomen. Na 50 cycli is de ontlaadcapaciteit van MoS2 /C-600, MoS2 /C-700, MoS2 /C-800, en ongerepte MoS2 elektrode met een stroomdichtheid van 100 mA g − 1 blijven op 399,7, 554,9, 245,7 en 332,9 mAh g − 1 , respectievelijk. Zoals weergegeven in Aanvullend bestand 1:Tabel S1 heeft het de ontlaadcapaciteiten samengevat na 50 cycli van MoS2 -gebaseerde elektrode gepresenteerd in andere literatuur, de als voorbereide MoS2 /C-700 vertonen vergelijkbare elektrochemische prestaties in vergelijking met het vorige werk. Er wordt geconcludeerd dat de MoS2 De /C-700-elektrode vertoont de meest uitstekende cyclusprestaties en de Coulomb-efficiëntie van het monster handhaafde een hoog niveau van ongeveer 100% na de eerste 3 cycli. Het kan profiteren van de kleine hoeveelheid grafietkoolstof in dit monster, wat leidt tot een verbeterde elektrische geleidbaarheid van het nanocomposiet.
Naast de fietsstabiliteit zijn de high-rate prestaties ook een belangrijke factor voor high-power toepassingen. Afbeelding 5d toont de snelheidsprestaties van MoS2 /C en de ongerepte MoS2 elektrode met stroomdichtheden variërend van 100 tot 1000 mA g − 1 . Bij 1000 mA g − 1 , de ontlaadcapaciteit van MoS2 /C-700 kan nog steeds een relatief hoge waarde behouden van ~ 450 mAh g − 1 , wat hoger is dan de andere MoS2 /C-elektroden en ongerepte MoS2 elektrode die we hebben geprepareerd met dezelfde stroomdichtheid. Wanneer de stroomdichtheid weer wordt gewijzigd in 100 mA g − 1 , de capaciteit van MoS2 /C-700-monster kan tot ~ 500 mAh g − 1 . herstellen na 50 cycli bij verschillende stroomdichtheden, wat de goede snelheid van het monster onthult.
De elektrochemische impedantiespectra (EIS) metingen op de MoS2 /C en de ongerepte MoS2 elektrode werden uitgevoerd om meer inzicht te krijgen in de uitstekende elektrochemische prestaties van de MoS2 /C-700 monster (Fig. 6). Er is een halve cirkel in het hoge frequentiegebied gevolgd door een hellingslijn in het lage frequentiegebied op deze Nyquist-plots. Het is te zien dat de halve cirkel in het hoge frequentiegebied van de MoS2 /C-700 monster is duidelijk kleiner dan dat van de andere drie monsters, wat verband houdt met de ladingsoverdrachtsweerstand (R ct ) trad op bij de elektrolyt- en elektrodeninterfaces. Daarom impliceert dit resultaat verder dat de opname van kaliumhumaat de geleidbaarheid van MoS2 aanzienlijk verbetert. , wat leidt tot een verdere verbetering van de elektrochemische prestaties.
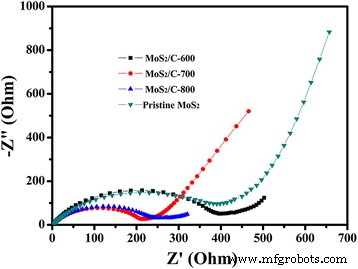
Nyquist-plots van de MoS2 /C-elektrode en de ongerepte MoS2 elektrode getest in een frequentiebereik van 0,01 Hz tot 100 kHz
Conclusies
In dit werk, tweedimensionale MoS2 /C-nanobladen werden met succes gesynthetiseerd via een co-precipitatie/calcineringsroute door gebruik te maken van een organische stof (kaliumhumaat) en een anorganische stof ((NH4 )6 Ma7 O24 ) als reagentia. Structurele karakteriseringen tonen aan dat zoals voorbereide MoS2 /C-700 nanocomposiet is tweedimensionaal (2D) MoS2 /C nanosheets met een onregelmatige vorm. De 2D MoS2 /C nanosheets vertoonden verbeterde elektrochemische prestaties wanneer ze werden vervaardigd als anodemateriaal voor LIB's. Verder werd een mogelijk reactieproces voorgesteld. De huidige synthesestrategie kan worden uitgebreid naar de synthese van ander nanocomposiet dat kan dienen als anodemateriaal voor hoogwaardige lithium-ionbatterijen.
Afkortingen
- 2D:
-
Tweedimensionaal
- CV:
-
Cyclische voltammetrie
- DEC:
-
Diethylcarbonaat (DEC)
- DMC:
-
Dimethylcarbonaat
- EG:
-
Ethyleencarbonaat
- EDX:
-
Energie-dispersieve röntgenspectrometer
- EIS:
-
Elektrochemische impedantiespectroscopie
- FT-IR:
-
Fourier-transformatie spectrofotometer
- HRTEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- Ik D :
-
De intensiteit van de D-band
- Ik G :
-
De intensiteit van de G-band
- LIB's:
-
Lithium-ionbatterijen
- Ma-HA:
-
De voorlopers
- MoS2 /C:
-
MoS2 /koolstof
- MoS2 /C-600:
-
MoS2 /C nanocomposiet gecalcineerd bij 600 °C
- MoS2 /C-700:
-
MoS2 /C nanocomposiet gecalcineerd bij 700 °C
- MoS2 /C-800:
-
MoS2 /C nanocomposiet gecalcineerd bij 800 °C
- NMP:
-
N-methyl-2-pyrrolidinon
- PVDF:
-
Polyvinylideenfluoride
- R ct :
-
Weerstand ladingsoverdracht
- SEM:
-
Scanning elektronenmicroscoop
- TEM:
-
Transmissie-elektronenmicroscopie
- TGA:
-
Thermogravimetrische analyses
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Tinnen nanokristallen voor toekomstige batterij
- MoS2 met gecontroleerde dikte voor elektrokatalytische waterstofevolutie
- Eenvoudige synthese van SiO2@C-nanodeeltjes verankerd op MWNT als hoogwaardige anodematerialen voor Li-ionbatterijen
- Synthese en elektrochemische eigenschappen van LiNi0.5Mn1.5O4-kathodematerialen met Cr3+ en F− composietdoping voor lithium-ionbatterijen
- Temperatuurafhankelijke kristallisatie van MoS2-nanovlokken op grafeen-nanobladen voor elektrokatalyse
- Weinig gelaagde MoS2/acetyleenzwarte composiet als een efficiënt anodemateriaal voor lithium-ionbatterijen
- Na4Mn9O18/Carbon Nanotube-composiet als materiaal met hoge elektrochemische prestaties voor waterige natrium-ionbatterijen
- Eenvoudige synthese van oppervlaktegefunctionaliseerde magnetische nanocomposieten voor effectieve selectieve adsorptie van kationische kleurstoffen
- Transformatie van slib Si naar nano-Si/SiOx-structuur door diffusie van zuurstof naar binnen als voorloper voor hoogwaardige anoden in lithium-ionbatterijen
- Synthese en onderzoek van CuGeO3-nanodraden als anodematerialen voor geavanceerde natrium-ionbatterijen
- Eenvoudige synthese van met stikstof gedoteerde microporeuze koolstofbollen voor hoogwaardige symmetrische supercondensatoren



