Eenvoudige synthese van ligandvrije iridium-nanodeeltjes en hun in vitro biocompatibiliteit
Abstract
Anorganische nanodeeltjes met hoge dichtheid zijn veelbelovend gebleken in medische toepassingen die gebruikmaken van straling, waaronder röntgenbeeldvorming en als versterkers van de stralingsdosis voor radiotherapie. We hebben een waterige synthetische methode ontwikkeld om kleine (~ 2 nm) iridium-nanodeeltjes (IrNP's) te produceren door iridium (III) chloride te reduceren met behulp van een boorhydride-reductiemiddel. In tegenstelling tot andere op oplossing gebaseerde synthesemethoden, worden uniforme en monodisperse IrNP's geproduceerd zonder het gebruik van oppervlakteactieve stoffen of andere solubiliserende liganden. Deze nanodeeltjes zijn zeer kristallijn, zoals waargenomen door röntgendiffractie en transmissie-elektronenmicroscopie met hoge resolutie (TEM). In vitro metabole toxiciteitstesten met behulp van hepatocyt- en macrofaagcellen tonen aan dat zowel IrNP's als iridium(III)chloride goed worden verdragen bij concentraties tot 10 μM iridium. Bovendien werden de IrNP's beoordeeld in een hemolytische test en bleken ze geen significante invloed te hebben op rode bloedcellen bij blootstelling aan concentraties tot 100 μM. Over het algemeen ondersteunen deze resultaten het potentieel voor de in vivo toepassing van dit nanomateriaal.
Achtergrond
Edele metalen nanodeeltjes zijn een steunpilaar van opkomende nanotechnologieën vanwege hun interessante optische, elektronische en oppervlaktekatalytische eigenschappen. In de nanogeneeskunde hebben deze unieke biomaterialen veel aandacht getrokken vanwege het vermogen om hun biologische interacties aan te passen door middel van oppervlaktemodificaties voor een breed scala aan toepassingen [1]. Gouden nanodeeltjes (AuNP's) zijn uitgebreid onderzocht voor detectie en therapeutische toepassingen [2, 3], terwijl andere edele metalen, waaronder zilver, nichetoepassingen hebben gevonden zoals antimicrobiële middelen [4]. Nanodeeltjes die zijn samengesteld uit platinoïde elementen, die vaak worden gebruikt vanwege hun katalytische eigenschappen aan het oppervlak [5], moeten echter nog grondig worden onderzocht voor biomedische toepassingen. De uitzonderlijke oppervlaktestabiliteit en bekende biologische compatibiliteit van deze elementen, evenals hun potentiële nieuwe fysische eigenschappen op nanoschaal, maken ze tot unieke alternatieven voor AuNP's.
Hoogenergetische straling wordt op grote schaal gebruikt in de geneeskunde, inclusief bij diagnostische beeldvorming en bestralingstherapie. Daarom kunnen functionele materialen die interageren met straling, zoals een hoog atoomnummer en nanodeeltjes met een hoge dichtheid, de prestaties van deze modaliteiten verbeteren. De meeste chemische en technische onderzoeken tot nu toe waren gericht op AuNP's om de stralingsinteracties te verbeteren, hoewel bismut en hafnium zijn onderzocht voor respectievelijk diagnostische en therapeutische toepassingen [6, 7].
Hier presenteren we een synthetische methode om iridium-nanodeeltjes (IrNP's) te produceren, waarvan wordt voorspeld dat ze een sterke stralingsverzwakking hebben vanwege de hoge dichtheid. Iridium is een van de minst reactieve metalen, die in het algemeen biologisch compatibel wordt geacht, en heeft een elementaire dichtheid van 22,56 g/cm 3 (de tweede alleen voor osmium, waarvan bekend is dat het zeer giftig is). Een isotoop van iridium, 192 Ir is een veelgebruikte brachytherapie-gamma-straler en een deel van het succes van dit materiaal is te danken aan de hoge dichtheid, d.w.z. het grote aantal atomen in een klein volume van het materiaal. In de huidige studie presenteren we de synthese van IrNP's en hun in vitro biocompatibiliteit, evenals die van iridium-ionen, die niet eerder is geëvalueerd in de geselecteerde cellijnen. Deze nieuwe IrNP's zijn niet gemakkelijk onderzocht voor medische doeleinden, ondanks de chemische inertie en superieure dichtheid van het materiaal. Hoewel iridium een relatief duur materiaal is, net als andere edele metalen, is de huidige waarde ervan als grondstof ongeveer driekwart van de prijs van goud en de helft van die van rhodium, waardoor het een interessant economisch alternatief is.
Methoden
Synthese van IrNP's
Alle synthesereacties werden uitgevoerd bij kamertemperatuur onder aerobe omstandigheden in gezuiverd 18 MΩ water. Een 20 mM iridium (III) chloride (Acros Organics) voorraad werd bereid door badsonicatie en gedurende ten minste 20 min geroerd om een optisch heldere oplossing te genereren. Een oplossing van 1,0 M boraanmorfoline (Alfa Aesar) werd ook bereid door badsonicatie. Voor syntheses op grotere schaal van 500 ml totaal volume werd 25 ml iridium (III) chloride-oplossing gebruikt (verdund tot 1,0 mM) en 5,0 ml boraanmorfoline werd toegevoegd (eindconcentratie 10 mM) onder snel roeren. De oplossing veranderde in 30 minuten geleidelijk van donkerbruin in zwart. Men liet de nanodeeltjes ten minste 60 minuten stabiliseren. Deze colloïdale oplossing werd direct toegevoegd aan centrifugale spinfilters (Amicon Ultra-4, 10k MWCO geregenereerde cellulose), en de nanodeeltjes werden verzameld bij 4000×g en gewassen in gezuiverd water. De nanodeeltjes werden vervolgens gesuspendeerd in water, door een spuitfilter (Millex-MP 0,22 μm EO) geleid en opgeslagen voor kwantificering.
Nanodeeltjeskarakterisering
Voor analyse met röntgenfoto-elektronspectroscopie (XPS) werden nanodeeltjes gesuspendeerd in een gelijk volume salpeterzuur, verzameld door centrifugatie in een microcentrifugebuis (5 min, 17 rcf) en voorafgaand aan analyse in water gesuspendeerd. Transmissie-elektronenmicroscopie (TEM) werd uitgevoerd op een FEI Tecnai F-20 TEM die werkte bij 200 kV. Gezuiverde IrNP's werden druppelgegoten op door koolstof Cu ondersteunde TEM-roosters (Ted Pella) en een nacht bij kamertemperatuur gedroogd. Lijndiffractieanalyse werd uitgevoerd met behulp van ImageJ-softwareanalyse. Voor röntgendiffractie (XRD) -analyse werden geconcentreerde IrNP's op een glasplaatje gegoten en bij kamertemperatuur gedroogd. XRD-gegevens werden verzameld in een gefocusseerde bundel (Bragg-Brentano) geometrie op een Rigaku Ultima IV röntgendiffractiesysteem met behulp van grafiet-monochromatische Cu Ka-straling. Scans werden uitgevoerd over het hoekbereik van 20-80 ° 2θ met een scansnelheid van 0, 1 ° / min bij kamertemperatuur. Dynamische lichtverstrooiing (DLS) werd uitgevoerd op een Malvern Nano ZSP in wegwerpbare polystyreencuvetten. Nanodeeltjes werden in water gesuspendeerd en de gegevens worden gerapporteerd als gedistribueerd op nummer. UV-Vis-absorptiespectra werden verzameld op een Tecan M200 Pro in een zwarte plaat met 96 putjes en een totaal oplossingsvolume van 100 L. Concentraties van iridium werden aangepast om relatieve absorptiepieken te illustreren. XPS-analyse werd uitgevoerd op een PHI Versaprobe II uitgerust met een halfbolvormige elektronenanalysator en aluminium Kɑ (1486,7 eV) röntgenbron. Spectrumanalyse werd uitgevoerd met behulp van de Multipak-softwaresuite. De kalibratie van de bindingsenergie werd uitgevoerd met behulp van de C1s-piek bij 284,6 eV, en de piekaanpassing was gebaseerd op asymmetrische pieken en een herhaalde Shirley-achtergrond, wat resulteerde in een chi-kwadraatwaarde van 1,13. Inductief gekoppelde plasma-massaspectrometrie (ICP-MS) van IrNP's en iridium (III) chloride-oplossing werden beoordeeld voorafgaand aan biologische toxiciteitstests. Vijftig microliter van elke IrNP-oplossing werd een nacht bij 70 ° C in een digestiebuis verteerd in 50 μL koningswater (3:1 M geconcentreerd salpeterzuur tot zoutzuur). Monsters werden vervolgens voor analyse verdund in 5,0 ml 1% salpeterzuur. ICP-MS werd uitgevoerd op een Agilent 7900 met helium als botsingsgas. Kalibratiecurven werden opgesteld met 100-0,1 μg/ml iridium-voorraadoplossingen (in 1% HCl) en alle monsters werden zodanig verdund dat concentraties werden gemeten in het bereik van tientallen ppb.
Cytotoxiciteitsanalyse
HepG2- en J774A.1-cellijnen werden gezaaid bij 2 × 10 5 cellen per putje (100 μL) in een plaat met 96 putjes (DMEM met 10% FBS) en 24 uur laten bezinken. Iridium-nanodeeltjes, iridiumzout, water of DMSO werden toegevoegd in een volume van 10% (10 μL extra volume). Cellen werden vervolgens 24 of 48 uur geïncubeerd. Voor levensvatbaarheidsanalyse werden media verwijderd en werden cellen eenmaal gewassen in PBS. Honderd microliter kweekmedia met 10% Alamar Blue (Thermo Scientific) werd gedurende 2 uur met cellen geïncubeerd. Het medium werd vervolgens opnieuw uitgeplaat in een zwarte plaat met 96 putjes en de fluorescentie werd afgelezen (ex530/em590) op een Tecan M200 Pro. Alle gegevens werden in viervoud uitgevoerd en experimenten werden op onafhankelijke dagen herhaald om algemene trends te bevestigen. Er werd een hemolytische test uitgevoerd zoals eerder gemeld [8].
Resultaten
Synthese en karakterisering van iridium nanodeeltjes
In deze synthese vormen we elementaire IrNP's uit iridium (III) chloridezout door reductie met een 10-voudige molaire overmaat boraanmorfoline in water. De reactie is gemakkelijk schaalbaar tot meerdere liters, en deeltjes worden gevormd bij kamertemperatuur onder aerobe omstandigheden. Deze synthetische methode produceert kleine (2-3 nm) uniforme IrNP's (figuur 1a) met een hoge mate van kristalliniteit zoals waargenomen door TEM-beeldvorming met hoge resolutie. Diffractiepatronen verkregen van TEM bevestigen verder de identiteit van de nanokristallen, met een lijnafstand van 0, 22 nm die indicatief is voor het diffractierooster van iridium (figuur 1b). Het röntgendiffractiepatroon komt nauw overeen met dat van elementair iridium (PDF Card No.:9008470, Fig. 1c). Zoals gesynthetiseerd, zijn IrNP's colloïdaal stabiel in water en blijven ze enkele maanden in oplossing gesuspendeerd bij kamertemperatuur (figuur 1d).
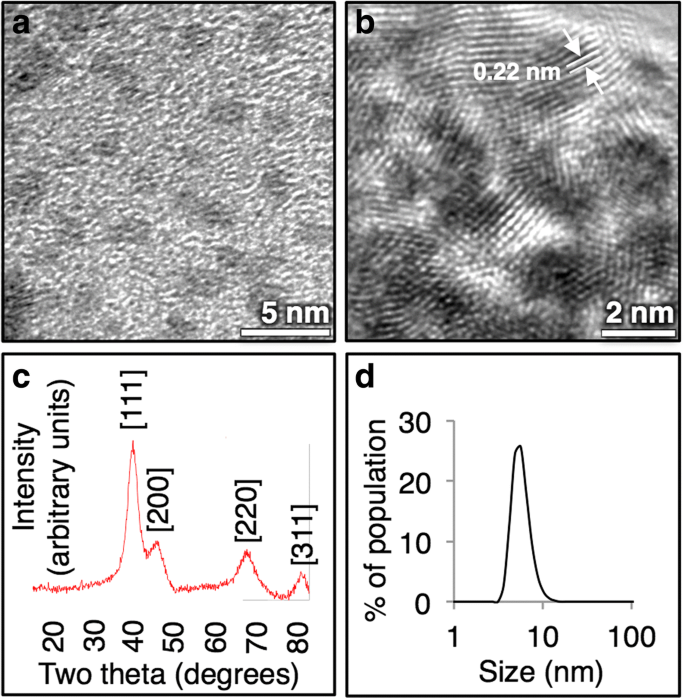
een Iridium nanodeeltjes zijn 2-3 nm door TEM-beeldvorming, met b met een sterk kristallijne roosterparameter. c XRD-spectrum komt overeen met elementair iridium en d deeltjes hebben een hydrodynamische grootte van 5 nm in water door DLS
Nanokristallen vormen zich in de loop van 30 minuten, zoals waargenomen door een kleurverandering van de lichtgele iridium(III)-voorloper naar een donkerzwarte nanodeeltjesoplossing (Fig. 2). Bij blootstelling aan een basische omgeving vormen deze IrNP's een voorspeld iridiumoxide, dat blauw lijkt. Zure omstandigheden, zoals incubatie in puur salpeterzuur, lijken de kristalliniteit van de deeltjes of de integriteit van het materiaal niet te beïnvloeden; het veroorzaakt echter wel uitvlokking en neerslag. Bovendien werd in de loop van uren ook aggregatie waargenomen in biologisch relevante oplossingen (fosfaatgebufferde zoutoplossing en weefselkweekmedia), wat suggereert dat verdere oppervlaktemodificatie nodig zal zijn voor toekomstige biomedische toepassingen. Röntgenfoto-elektronspectroscopie-analyse van de IrNP's gespoeld in salpeterzuur en gesuspendeerd in water onthult een overheersend iridium (0) -oppervlak, hoewel piekpassende analyse van gegevens 20% oppervlakte-oxidatie aangeeft (Fig. 3). Geen voorkeurskristallietoriëntatie van deeltjes wordt waargenomen, noch door XRD noch door XPS. Als alternatief resulteerde de introductie van een oppervlakteactieve thiol in de reactieoplossing tijdens het syntheseproces (vóór nucleatie) in remming van de deeltjesvorming.
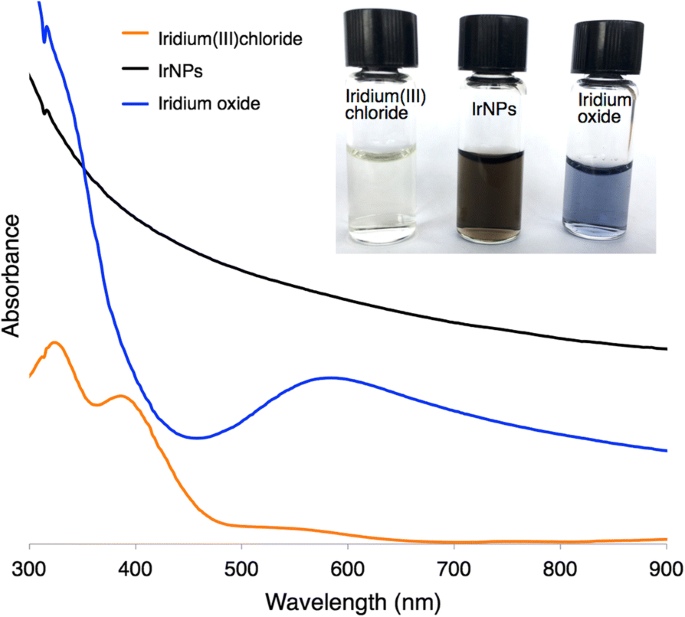
Iridium(III)chloride lijkt bleekgeel met absorptiepieken bij 324 en 386 nm. IrNP's zijn breedspectrumabsorbeerders en zien er zwart uit. Iridiumoxide (voorspeld), geproduceerd uit geoxideerde IrNP's behandeld in een basische oplossing, lijkt blauwpaars paars met een absorptiepiek bij 584 nm
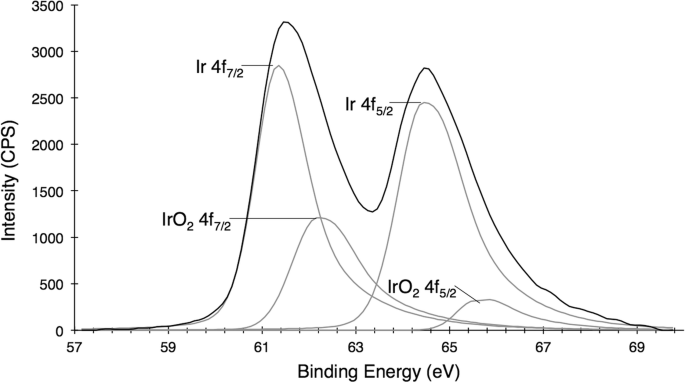
Röntgenfoto-elektronspectroscopie (XPS) van IrNP's, een overwegend elementaire iridium-oppervlaktetoestand, met ongeveer 20% oxide-oppervlakteverontreiniging
Iridiumcytotoxiciteit
We evalueerden de in vitro biologische compatibiliteit van de niet-afgetopte IrNP's en vergeleken dit met iridium (III) chloridezout in twee soorten zoogdiercellen. HepG2, een hepatocytcarcinoomcellijn, werd gebruikt om mogelijke toxiciteit voor de lever te evalueren. J774A.1-macrofaagcellen werden gebruikt om de toxiciteit voor het mononucleaire fagocytische systeem te evalueren. Cellen werden gedurende 24 of 48 uur geïncubeerd met IrNP's of iridium (III) chloride (genormaliseerd voor totale concentratie van iridium) en gewassen om extracellulair iridium te verwijderen, en metabole activiteit werd geëvalueerd met behulp van de Alamar Blue-assay (Fig. 4). HepG2-cellen vertonen verhoogde metabolische activiteit in de aanwezigheid van iridium (III) na 24 uur (tot 115% levensvatbaarheid), maar de respons wordt verminderd na 48 uur, waarbij 500 μM iridium (III) de levensvatbaarheid vermindert tot 90%. De HepG2-cellen hadden een verminderde cellulaire levensvatbaarheid, van 94 tot 78% in aanwezigheid van 50 μM IrNP's na 24 en 48 uur. Interessant is dat J774A.1-cellen een toename in metabole activiteit vertonen als reactie op IrNP's bij een concentratie van 50 μM met een levensvatbaarheid van 122% na 24 uur; na 48 uur werd de normale cellulaire functie echter hervat (98% levensvatbaarheid), wat wijst op een voorbijgaande metabole stimulatie als reactie op de nanomaterialen. J774A.1-cellen die gedurende 24 uur zijn geïncubeerd met 500 μM IrNP's vertonen een schijnbaar neutrale metabole respons, maar de afname van de levensvatbaarheid bij deze concentratie na 48 uur suggereert dat dit een gevolg is van toxiciteit en metabolische stimulatie die verschijnt als een neutrale levensvatbaarheidsreactie. Daarnaast evalueerden we de in vitro biocompatibiliteit van IrNP's met bloed door middel van een hemolytische test en ontdekten dat IrNP's geen significante hemolyse induceerden wanneer ze gedurende 1 uur bij 37 ° C met erytrocyten in PBS werden geïncubeerd (aanvullend bestand 1:Afbeelding S1).
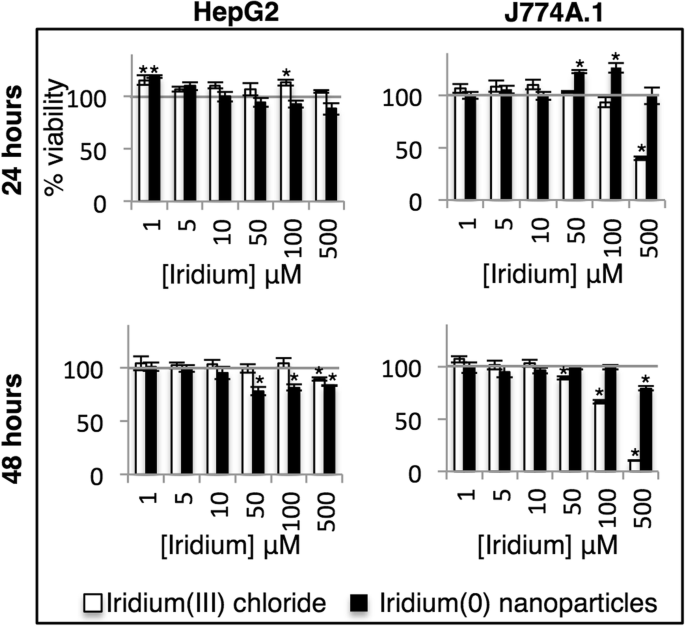
Cellulaire levensvatbaarheid van HepG2- en J774A.1-cellen die 24 of 48 uur zijn geïncubeerd met Ir(0)-nanodeeltjes of Ir(III)-zout. *Statistisch significante waarden (p < 0.05) ten opzichte van onbehandelde cellen
Discussie
Er zijn verschillende synthetische processen onderzocht om iridium op nanoschaal te produceren voor katalytische toepassingen, waaronder reductie van iridiumzouten door hydriden en waterstofgas [9,10,11,12,13], UV- en gammastraling [14,15,16,17], en polyol- of alcoholreductie [18,19,20]. Veel van deze synthetische methoden zijn echter ontworpen voor integratie van iridium op een substraat of drager voor chemische reacties en zijn niet compatibel met biologische toepassingen [21]. Onlangs verstoven 192 Ir werd gebruikt als modelmateriaal op nanoschaal voor longtoxiciteit en werd gekozen vanwege zijn uitzonderlijke inertie [22, 23]. Het primaire doel van deze onderzoeken was om de klaring en translocatie van ingeademde fijne deeltjes uit de longen te onderzoeken; het benadrukt echter ook de biocompatibiliteit van dit element.
We evalueerden de in vitro biologische compatibiliteit van de niet-afgetopte IrNP's en vergeleken dit met iridium (III) chloridezout in twee soorten zoogdiercellen waarvan wordt verwacht dat ze de hoogste concentraties geïnjecteerde nanodeeltjes accumuleren. Iridium(III)-toxiciteit in J774A.1-cellen volgt een dosis-responscurve van normale toxiciteit; 100 μM iridium (III) vermindert de cellulaire levensvatbaarheid tot 93 en 66%, en 500 μM resulteert in een cellulaire levensvatbaarheid van 40 en 10% na respectievelijk 24 en 48 uur. Deze gegevens weerspiegelen een interessante celspecifieke respons op iridium(0) en iridium(III), en we verwachten deze effecten in vivo verder te onderzoeken. Kleinere IrNP's en andere slecht oplosbare anorganische nanomaterialen zullen naar verwachting worden getransloceerd naar de nier en de lever, met een korte tijdelijke verblijfplaats in de nieren en een langere verblijfplaats in de lever, wat de celspecifieke toxiciteitsprofielen verder kan beïnvloeden. Uitscheiding wordt verwacht via de feces voor grotere iridiumdeeltjes, hoewel we verwachten dat de extreem kleine omvang van deze IrNP's gemakkelijk door het niersysteem kan worden gefilterd als de colloïdale stabiliteit in vivo kan worden gehandhaafd [23].
Ter voorbereiding op in vivo toepassingen werd de bloedcompatibiliteit van de IrNP's geëvalueerd met een hemolytische test. Gebruikmakend van volbloed muizen, evalueerden we het effect van deze IrNP's op de ruptuur van erytrocyten en mogelijke afgifte van hemoglobine. Hoewel diepgaande studies van het uiteindelijke, aan het oppervlak gemodificeerde IrNP moeten worden geëvalueerd, wekken de huidige IrNP-bouwstenen geen detecteerbare hemolytische respons op tot extreem hoge concentraties (500 μM).
Conclusies
We concluderen uit deze onderzoeken dat iridium(0)-nanokristallen gemakkelijk kunnen worden gesynthetiseerd door een eenvoudige waterige boorhydridereductie van iridium(III)chloride, wat resulteert in zeer kristallijne nanodeeltjes van 2-3 nm die colloïdaal stabiel zijn in water met een hydrodynamische capaciteit van ongeveer 5 nm. maat. Tijdens acute blootstelling zijn deze deeltjes niet-toxisch bij concentraties tot 50 M iridium (vergeleken met 10 μM voor iridiumchloride) in hepatocyten, stimuleren ze de metabole activiteit in macrofaagcellen en wekken ze geen hemolytische respons op bij praktische concentraties. Deze ligandvrije nanodeeltjes kunnen dienen als bouwstenen of kernen voor daaropvolgende oppervlakte-gemodificeerde IrNP's voor gebruik in biologische en medische toepassingen. Verder onderzoek naar de functionele eigenschappen van deze nanomaterialen met hoge dichtheid in aanwezigheid van röntgenstralen of andere straling biedt de mogelijkheid voor nieuwe therapeutische en diagnostische middelen.
Afkortingen
- AuNP:
-
Gouden nanodeeltje
- DLS:
-
Dynamische lichtverstrooiing
- ICP-MS:
-
Inductief gekoppelde plasma massaspectrometrie
- IrNP:
-
Iridium nanodeeltje
- PDF:
-
Poederdiffractiebestand
- UV:
-
Ultraviolet
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Multifunctionele gouden nanodeeltjes voor verbeterde diagnostische en therapeutische toepassingen:een overzicht
- Eenvoudige synthese en optische eigenschappen van kleine selenium nanokristallen en nanostaafjes
- Eenvoudige synthese van gekleurd en geleidend CuSCN-composiet gecoat met CuS-nanodeeltjes
- In vitro onderzoek naar de invloed van Au-nanodeeltjes op HT29- en SPEV-cellijnen
- Synthese en luminescentie-eigenschappen van in water oplosbare α-NaGdF4/β-NaYF4:Yb,Er Core–Shell-nanodeeltjes
- Synthese en in vitro prestaties van met polypyrrool gecoate ijzer-platina nanodeeltjes voor fotothermische therapie en foto-akoestische beeldvorming
- Synthese van in water oplosbare antimoonsulfide Quantum Dots en hun foto-elektrische eigenschappen
- Effect van de synthesemethode van La1 − xSr x MnO3 manganite nanodeeltjes op hun eigenschappen
- One-Pot-synthese van Cu2ZnSnSe4-nanoplaten en hun door zichtbaar licht aangedreven fotokatalytische activiteit
- Milieuvriendelijke en gemakkelijke synthese van Co3O4-nanodraden en hun veelbelovende toepassing met grafeen in lithium-ionbatterijen
- Eenstaps sonochemische synthese en fotokatalytische eigenschappen van grafeen/Ag3PO4 Quantum Dots Composites in één stap



