Groene en kosteneffectieve synthese van tinoxide-nanodeeltjes:een overzicht van de synthesemethodologieën, het vormingsmechanisme en hun potentiële toepassingen
Abstract
Nanotechnologie is het meest veelbelovende onderzoeksgebied geworden met zijn gedenkwaardige toepassing op alle wetenschapsgebieden. In de afgelopen jaren heeft tinoxide enorme aandacht gekregen vanwege zijn fascinerende eigenschappen, die zijn verbeterd met de synthese van dit materiaal in het nanometerbereik. Er worden tegenwoordig tal van fysische en chemische methoden gebruikt om nanodeeltjes van tinoxide te produceren. Deze methoden zijn echter duur, vereisen veel energie en maken ook gebruik van verschillende giftige chemicaliën tijdens de synthese. De toegenomen bezorgdheid met betrekking tot de menselijke gezondheid en de gevolgen voor het milieu hebben geleid tot de ontwikkeling van een kosteneffectief en milieuvriendelijk proces voor de productie ervan. Onlangs zijn tinoxide-nanodeeltjes met succes gesynthetiseerd door groene methoden met behulp van verschillende biologische entiteiten zoals plantenextract, bacteriën en natuurlijke biomoleculen. Productie op industriële schaal met behulp van groene synthesebenaderingen blijft echter een uitdaging vanwege de complexiteit van de biologische substraten die een probleem vormen voor de opheldering van de reacties en het mechanisme van formaties die optreden tijdens de synthese. Daarom vat de huidige review de verschillende bronnen van biologische entiteiten en methodologieën samen die worden gebruikt voor de groene synthese van tinoxide-nanodeeltjes en de impact op hun eigenschappen. Dit werk beschrijft ook de vorderingen in het begrip van het vormingsmechanisme dat in de literatuur wordt gerapporteerd en de verschillende analytische technieken die worden gebruikt voor het karakteriseren van deze nanodeeltjes.
Inleiding
In de afgelopen decennia is nanotechnologie naar voren gekomen als een nieuw onderzoeksgebied dat zich bezighoudt met de synthese, karakterisering, modificatie en het gebruik van nanomaterialen voor hun enorme toepassing in gebieden zoals de farmacie, de voedingsindustrie, cosmetica, textielindustrie, geneeskunde, optica, elektronica, energiewetenschap en elektrochemische toepassingen [1,2,3,4]. Nanomaterialen zijn materialen met één dimensie in een groottebereik van 1-100 nm. De zeer grote oppervlakte-tot-volumeverhouding en het extreem kleine formaat van deze materialen kunnen resulteren in een volledig nieuwe of verbeterde elektrische, optische, magnetische, katalytische en antimicrobiële activiteit in vergelijking met hun bulkmaterialen [5,6,7]. Vanwege deze unieke eigenschappen vinden nanodeeltjes toepassing in verschillende gebieden van moderne wetenschap en techniek, zoals nanogeneeskunde, fotokatalyse, biosensoren, reinigingsmiddelen en de textielindustrie [1, 8]. Onder de nanodeeltjes bevindt zich tin(IV)oxide (SnO2 ) in het bijzonder heeft enorme aandacht gekregen vanwege hun veelzijdige toepassingen zoals opto-elektronische apparaten [9], solid-state gassensoren [10], elektroden voor lithium-ionbatterijen [11], veldemissiedisplays [12], lichtgevende diodes [13], katalyse [14], op kleurstof gebaseerde zonnecellen [15], medicijnen [16], fotosensoren en antistatische coatings [17].
In materiaalkunde, SnO2 wordt beschouwd als een zuurstofarme n-type halfgeleider, die kristalliseert als de tetragonale rutielstructuur met roosterconstanten a = b = 4.7374 Å en c = 3.1864 . De eenheidscel bestaat uit twee zesvoudig gecoördineerde tin- en vier drievoudig gecoördineerde zuurstofatomen [18, 19]. Een brede energiekloof (3,6 tot 3,8 eV), sterke thermische stabiliteit (tot 500 °C), een hoge mate van transparantie in het zichtbare spectrum, sterke chemische en fysische interacties met de geadsorbeerde soorten maken SnO2 een veelbelovende kandidaat voor een mogelijke toepassing in de lithium-ionbatterijen, sensoren, katalyse, energieopslag, glascoatings, medicijnen en milieusanering [20,21,22,23]. SnO2 wordt gebruikt als een sensor om de responstijd en gevoeligheid te verbeteren vanwege het hoge specifieke oppervlak, de hoge chemische stabiliteit, de lage elektrische weerstand en de lage dichtheid [24]. Van de afgelopen jaren, SnO2 werd grondig onderzocht voor zijn toepassingen in de zonnecellen [25] en gassensoren om de brandbare gassen zoals CO, NO, NO2 te detecteren , H2 S en C2 H5 OH [26,27,28,29]. Vanwege de unieke fysisch-chemische eigenschappen en mogelijke toepassingen van nanodeeltjes (NP's), heeft de wetenschappelijke gemeenschap verschillende methoden ontwikkeld om nanodeeltjes te produceren. De chemische en fysische methoden die worden gebruikt voor de synthese van metaal- en metaaloxidenanodeeltjes zijn echter vrij duur en maken gebruik van giftige stoffen die schadelijk zijn voor het milieu en de menselijke gezondheid [30]. In de afgelopen jaren hebben de meeste onderzoekers hun onderzoeksinteresse veranderd in de richting van de groene synthese van NP's omdat het veel voordelen heeft, zoals een kosteneffectieve, eenvoudige fabricageprocedure, reproduceerbaarheid bij de productie en vaak resulteert in stabielere nanodeeltjes [31]. In de afgelopen tien jaar zijn er verschillende onderzoeken uitgevoerd naar de groene synthese van SnO2 NP's werden gemeld. Er is echter geen enkel overzichtsartikel beschikbaar in de literatuur dat de methodologie van de synthese en het vormingsmechanisme aantoont. Daarom beschrijft dit artikel de groene synthese, het vormingsmechanisme, karakteriseringstechnieken en mogelijke toepassingen van SnO2 NP's.
Groene synthese van tinoxide-nanodeeltjes
SnO2 NP's worden gesynthetiseerd door verschillende fysische, chemische en groene methoden. De chemische methoden omvatten sol-gel, hydrothermisch, precipitatie, mechanochemische methode, micro-emulsie, enzovoort [31,32,33,34,35,36,37]. Van de chemische methoden is de meest gebruikte techniek de sol-gel-synthese, waarbij gebruik wordt gemaakt van tinprecursorzout en chemische reagentia die de vorming van de tinbevattende gel reguleren. Daarna wordt de gel blootgesteld aan een warmtebehandeling bij temperaturen tot 800 °C om SnO2 te verkrijgen NP's [32, 38]. Chemische stabilisatoren en afdekmiddelen, zoals oxaalzuur of ethyleenglycolen, kunnen worden toegevoegd tijdens de synthese van SnO2 NP's om de grootte te regelen en agglomeratie van de nanodeeltjes te verbieden [32, 39]. Een oplossing-pH, de concentratie van chemicaliën, reactietijd en calcineringstemperatuur kunnen ook de grootte en morfologie van nanodeeltjes beïnvloeden [31, 34,35,36,37]. De bovengenoemde methoden voor het synthetiseren van SnO2 NP's gebruiken verschillende gevaarlijke chemische reagentia, oplosmiddelen en oppervlakteactieve stoffen, die een ernstige bedreiging vormen voor het milieu en de menselijke gezondheid [4, 30].
SnO2 NP's kunnen ook worden gesynthetiseerd door fysieke technieken zoals spraypyrolyse, thermische oxidatie, chemische dampafzetting, laserablatie en ultrasone trillingen [40,41,42,43,44]. Van deze methoden wordt laserablatie beschouwd als een kosteneffectieve en eenvoudige methode voor het synthetiseren van metaal- en metaaloxidenanodeeltjes in vloeistof [44, 45]. In tegenstelling tot de andere conventionele methoden, vereist deze methode geen capping / reductiemiddelen, hoge temperatuur of hoge druk, en kunnen we nanodeeltjes van hoge zuiverheid produceren [44, 45]. De variatie in de parameters van de pulsen die door de laserstraal worden toegepast en de ablatietijd zijn belangrijke parameters die de deeltjesgrootte, morfologie en oppervlaktechemie van de nanodeeltjes bepalen [44]. De meeste fysieke methoden vereisen echter complexe apparatuur, veel energie en geschoolde mankracht [46]. Daarom is het van groot belang om synthesemethoden te ontwikkelen die milieuvriendelijk, goedkoop en efficiënt zijn en die werken bij omgevingscondities. Een dergelijke oplossing is een groene synthese, en veel onderzoekers hebben een groene-chemische benadering ontwikkeld voor het synthetiseren van tinoxide-nanodeeltjes. In de groene synthesestrategie zouden biologische entiteiten zoals plantenextract, micro-organismen of andere groene bronnen kunnen worden gebruikt als alternatief voor de conventionele fysische en chemische methoden [47]. Tegenwoordig worden de biologisch geïnspireerde synthesemethoden ook wel groene synthese genoemd omdat ze in overeenstemming zijn met de twaalf principes van groene chemie [48]. Enkele van de duidelijke voordelen die biologische synthese heeft ten opzichte van fysische en chemische methoden zijn (a) schone en milieuvriendelijke methode, aangezien niet-toxische chemicaliën worden gebruikt, (b) het gebruik van hernieuwbare bronnen, (c) de actieve biologische componenten zoals enzym zelf als evenals fytochemicaliën werken als reductie- en afdekmiddel, waardoor de totale kosten van het syntheseproces worden geminimaliseerd, (d) externe experimentele omstandigheden zoals hoge druk en temperatuur zijn niet vereist, wat aanzienlijke energiebesparingen oplevert [49, 50].
In het laatste decennium is de interesse in het synthetiseren van SnO2 NP's via de biologische methode zijn aanzienlijk toegenomen, omdat het proces betrouwbaarder, milieuvriendelijker, kosteneffectiever, lage input-hoge opbrengst en eenvoudige procedures is zonder nadelige gevolgen voor het milieu. Een verscheidenheid aan biologische substraten zoals plantenextracten, bacteriën en natuurlijke biomoleculen zijn met succes gebruikt voor de groene synthese van SnO2 NP's. De fytochemicaliën van verschillende planten en enzymen van bacteriën zijn primair verantwoordelijk voor de groensynthese. De actieve verbindingen die in de groene bronnen aanwezig zijn, spelen ook als reductie-, capping- en stabilisator tijdens de synthese. De gewenste NP's worden vaak verkregen na calcineren of gloeien bij gespecificeerde temperaturen [51,52,53,54].
Plant-gemedieerde synthese van tinoxide-nanodeeltjes
Plant-gemedieerde synthese is het beste platform voor synthese geworden ten opzichte van conventionele fysisch-chemische methoden, omdat het vrij is van giftige chemicaliën en natuurlijke afdekkingen en reductiemiddelen biedt. Bovendien is het gemakkelijk en milieuvriendelijk en geeft het een kwantitatief verrijkt product vrij van onzuiverheden. Bij deze methode is het niet nodig om hoge temperatuur, hoge druk en dure apparatuur te gebruiken. Bovendien leidt plant-gemedieerde synthese tot grootschalige productie van stabielere nanodeeltjes met verschillende vormen en maten [55, 56]. Voor de groene synthese van SnO2 zijn extracten van een groot aantal delen van verschillende plantensoorten gebruikt NP's. In het algemeen is de plant-gemedieerde synthese van SnO2 NP's is een heel eenvoudig proces waarbij een dun zout wordt toegevoegd aan het eerder bereide extract. Na de reactie wordt de oplossing gecentrifugeerd. Ten slotte worden de pellets onderworpen aan een thermische behandeling gevolgd door karakterisering met behulp van verschillende analytische technieken zoals Fourier-transformatie-infraroodspectroscopie (FTIR), röntgendiffractometer (XRD), energiedispersieve röntgenanalyse (EDS), scanning-elektronenmicroscopie ( SEM), transmissie-elektronenmicroscopie (TEM), deeltjesgrootte-analysator (PSA) en dynamische lichtverstrooiing (DLS). UV-zichtbare spectroscopie (UV-Vis) wordt gebruikt om de vorming van nanodeeltjes te volgen. Het gedetailleerde protocol voor de plant-gemedieerde synthese van SnO2 NP's worden schematisch geïllustreerd in Fig. 1. Diallo et al. rapporteerde de groene synthese van SnO2 NP's met behulp van Aspalathus linearis en tinchloridepentahydraat (SnCl4 ·5H2 O) als voorloper [51]. Het zout werd opgelost in het plantenextract en na 10 minuten werd de vorming van een witte afzetting waargenomen. De witte afzetting werd na het centrifugatieproces verzameld en bij ongeveer 80 °C gedroogd. Het poeder werd ongeveer 4 uur bij verschillende temperaturen gegloeid en onderworpen aan verschillende analytische technieken zoals transmissie-elektronenmicroscopie met hoge resolutie (HR-TEM), EDS, XRD en röntgenfoto-emissiespectroscopie (XPS). De NP's waren quasi-bolvormig met een gemiddelde grootte in het bereik van 2,5-11,40 nm. Er werd waargenomen dat de deeltjesgrootte en kristallijne aard van de NP's toenemen met het verhogen van de uitgloeitemperatuur. Bovendien werken de bioactieve componenten zoals aspalathine, nothofagine en aspalalinine die aanwezig zijn in het plantenextract als zowel chelerende als reductiemiddelen. Camellia sinensis bladextract werd ook gebruikt om SnO2 . te synthetiseren NP's [53]. De polyfenolen die in het bladextract aanwezig zijn, werken zowel stabiliserend als afdekkend. Scanning-elektronenmicroscopie met hoge resolutie (HR-SEM) en XRD-analyse onthulden bolvorm SnO2 NP's met een grootte in het bereik van 5-30 nm. Verder bleek de bandgap van de NP's af te nemen met toenemende annealingtemperatuur. De Catunaregam spinosa -gemedieerde groene gesynthetiseerde SnO2 NP's vertoonden uitstekende fotokatalytische activiteit tegen Congo-rode kleurstof [57]. De gebiosynthetiseerde NP's zijn bolvormig en hebben een gemiddelde grootte van 47 nm.
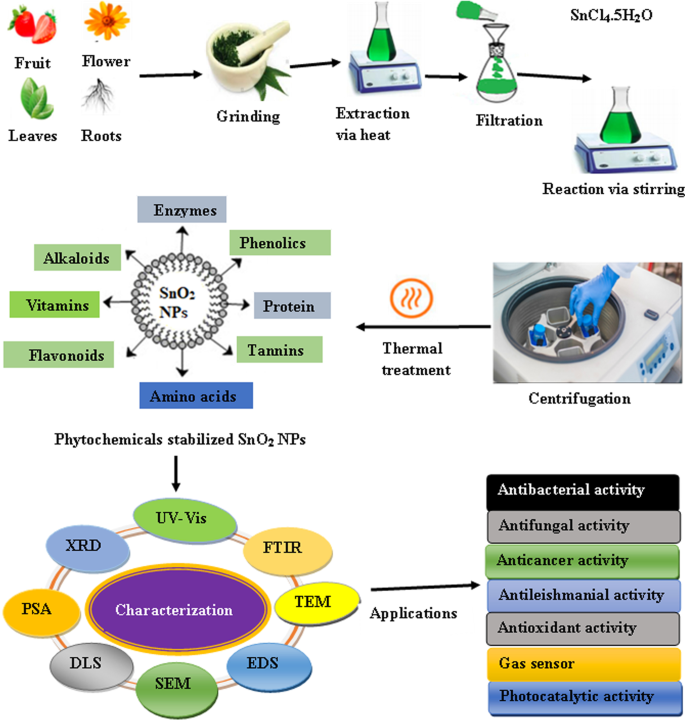
Een schematisch diagram van door plantenextract gemedieerde synthese van SnO2 NP's
Het bladextract van Aloe barbadensis miller is gebruikt om SnO2 . te synthetiseren NP's van SnCl2 ·2H2 O als voorloper [58]. De resulterende NP's bleken bolvormig te zijn met een gemiddelde grootte variërend van 50 tot 100 nm. Bovendien vertoonden de gesynthetiseerde nanodeeltjes een uitstekende antibacteriële activiteit tegen S. aureus en E. coli.
In een andere studie, de groene synthese van SnO2 NPs werd gedaan door een efficiënte en goedkope methode met behulp van Plectranthus amboinicus bladextract en SnCl2 ·2H2 O als uitgangsmateriaal [59]. Het plantenextract werkt als een reductie- en stabilisator. De resulterende NP's werden gekenmerkt door SEM, EDX, XRD en PSA. De NP's waren tetragonaal van vorm met een gemiddelde deeltjesgrootte van 63 nm. Verder onthulden de auteurs dat de gebiosynthetiseerde NP's een grotere fotokatalytische activiteit vertoonden tegen Rhodamine B in vergelijking met de commerciële SnO2 . Groene synthese van SnO2 NP's werden gerapporteerd met behulp van Nyctanthes arbor-tristis (Parijataka) bloemenextract [60]. Zoals blijkt uit SEM- en PSA-analyse, vertoonden de gesynthetiseerde nanodeeltjes de morfologie van fijne korrels met een klein agglomeratiestadium en een gemiddelde korrelgrootte van 2-8 nm. De studie onderzocht ook het hydrolyse- en capping-potentieel van het plantenextract.
De groene synthese van SnO2 NP's werden uitgevoerd door een goedkoop en milieuvriendelijk proces met behulp van Psidium guajava bladextract [61]. Het UV–Vis-resultaat onthulde een oppervlakteplasmonresonantiepiek bij 314 nm, wat de vorming van SnO2 bevestigt NP's. Bovendien waren de NP's bolvormig met een grootte variërend van 8 tot 10 nm. De studie toonde ook aan dat de NP's 90% afbraak van reactief geel 186 vertonen binnen 180 minuten onder bestraling met zonlicht. Bhosale et al. [62] identificeerde het bladextract van Calotropis gigantea als natuurlijke bron voor de synthese van SnO2 NP's. De secundaire metabolieten van het extract werken zowel als stabilisator als cappingsmiddel bij de omzetting van tinchloride in SnO2 NP's. De auteurs suggereerden dat de NP's bolvormig waren en een gemiddelde grootte tussen 30 en 40 nm hadden. De gesynthetiseerde NP's breken de methyloranjekleurstof binnen 120 minuten tot 80% af. Singh et al. [63] rapporteerde de biosynthese van SnO2 NP's die Piper betle gebruiken blad extract. SEM- en TEM-analyse onthulde de vorming van bolvormige NP's met een gemiddelde grootte van 8,4 nm. De NP's degraderen het reactieve gele 186 in een pseudo-eerste orde met een efficiëntie van 92,17%. Bovendien vertoonden de NP's een uitstekende selectiviteit voor de verwijdering van reactief geel 186 in vergelijking met reactief rood 120 en reactief groen 119. In de literatuur zijn verschillende planten en plantenextracten gebruikt voor de bereiding van SnO2 (Tafel 1). Uit de tabel blijkt dat de aard van plantensoorten en de reactieomstandigheden de grootte en vorm van SnO2 beïnvloeden. NP's.
Bacteriën-gemedieerde synthese van tinoxide-nanodeeltjes
Microben zijn belangrijke nanofabrieken die een enorm potentieel hebben als milieuvriendelijke en kosteneffectieve hulpmiddelen, waarbij giftige chemicaliën en de hoge energie die nodig is voor fysisch-chemische synthese worden vermeden. Verschillende microben zoals bacteriën, schimmels en gisten zijn gebruikt voor de synthese van metaal- en metaaloxide-nanodeeltjes, zowel intracellulair als extracellulair. Intracellulaire synthese omvat het transporteren van de metaalionen naar de microbiële cel en de vorming van de NP's in aanwezigheid van het enzym, co-enzymen en andere biomoleculen in de cel. Bij extracellulaire synthese worden de metaalionen gevangen op het oppervlak van de microbiële cel. De enzymen en eiwitten die aan het oppervlak beschikbaar zijn, verminderen de metaalionen en zijn verantwoordelijk voor het stabiliseren van de NP's [73]. De extracellulaire synthese is echter voordeliger in vergelijking met de intracellulaire route omdat deze kan worden gebruikt om grote hoeveelheden NP's te fabriceren en verschillende synthesestappen elimineert die nodig zijn voor het herstel van NP's [74].
Biologische synthese met behulp van bacteriën is een groene en kosteneffectieve benadering in vergelijking met chemische synthese. Deze methode heeft echter verschillende nadelen:(a) het screenen van de microben is een tijdrovend proces, (b) vereist zorgvuldige monitoring van de kweekbouillon en het hele proces, en (c) is moeilijk om de grootte en morfologie van de NP's. Niet alle bacteriën kunnen NP's synthetiseren vanwege hun intrinsieke metabolische proces en enzymactiviteiten. Daarom is een zorgvuldige selectie van een geschikte bacterie nodig om NP's te produceren met een goed gedefinieerde grootte en morfologie [74]. Een studie uitgevoerd door Srivastava en Mukhopadhyay [54] rapporteerde bijvoorbeeld een goedkope, groene en eenvoudigste procedure voor de synthese van SnO2 NP's met verse en schone Erwinia herbicola bacteriële cellen en een waterige tin(II)chloride-oplossing. De gesynthetiseerde SnO2 NP's waren meestal bolvormig met een grootte van 10 tot 42 nm. Er werd gemeld dat het bacteriële eiwit en andere biomoleculen dienen als een reducerend en stabiliserend middel tijdens de synthese van SnO2 NP's. Deze biomoleculen hielpen ook bij het beheersen van de grootte en aggregatie van SnO2 NP's.
Biomoleculen en andere door groene bronnen gemedieerde syntheses van tinoxide-nanodeeltjes
Afgezien van de door planten en bacteriën gemedieerde synthese van SnO2 NP's hebben onderzoekers een niet-toxische, milieuvriendelijke en groene chemische benadering ontwikkeld door andere biomoleculen te gebruiken, zoals aminozuren, vitamines, enzymen en suikers (tabel 2). Yang et al. [75] gesynthetiseerde SnO2 NP's met behulp van een goedkope en milieuvriendelijke methode met vitamine C (ascorbinezuur), een natuurlijk beschikbaar biomolecuul. TEM-analyse toonde de vorming van bolvormige NP's met een gemiddelde grootte van ongeveer 30 nm. Vitamine C werkt tijdens de synthese zowel als een afdekking als een reductiemiddel. De studie suggereerde de vitamine C op het oppervlak van SnO2 NP's verminderden de oxidatieve stress veroorzaakt door SnO2 NP's op de cellen, wat leidt tot een verminderd gewichtsverlies bij neonatale muizen. Sferische SnO2 NP's met een gemiddelde deeltjesgrootte van 13 nm werden bereid met koolhydraat (zetmeel) [76]. Er werd gesuggereerd dat het koolhydraat fungeert als een sjabloon, dat verschillende metaalkationen zou kunnen binden via hun functionele groepen, en daarom werd een uniforme dispersie van de kationen waargenomen. In een ander onderzoek werd resterend water verzameld uit geweekte Bengaalse grambonen (Cicer arietnum L.) werd gebruikt voor het synthetiseren van niet-gedoteerde SnO2 , en Ni, Fe en Au-gedoteerde SnO2 NP's [77,78,79]. De auteurs suggereerden dat de pectine in het extract verantwoordelijk was voor de synthese van de SnO2 NP's. De gemiddelde kristallietgrootte van de bolvormige niet-gedoteerde SnO2 , Ni-gedoteerde SnO2 , en Au-gedoteerde SnO2 NP's bleken respectievelijk 11 nm, 6 nm en 25 nm te zijn.
Een andere studie heeft een groene benadering aangetoond om SnO2 . te synthetiseren NP's met behulp van een eierschaalmembraan (ESM) [80], een natuurlijk bio-afval van de kippeneierschaal. Er werd gesuggereerd dat de ESM-bestanddelen biomoleculen vormen zoals uronzuur en sacchariden die de aldehydegroepen bevatten, die tijdens de synthese als een reductiemiddel werken. Morfologische analyse toonde de vorming van staaf, hexagonale en bolvorm van SnO2 NP's met een deeltjesgrootte tussen 13 en 40 nm.
Verschillende aminozuren zoals glycine, arginine, asparaginezuur, lysine en tyrosine [81,82,83,84,85] zijn gebruikt voor de groene synthese van SnO2 NP's vanwege hun goede capping- of complexvormers. Aminozuur-gemedieerde synthese elimineert het gebruik van giftige chemicaliën tijdens de synthese. Sferische SnO2 NP's werden gesynthetiseerd met behulp van arginine [81]. De morfologische studies suggereren dat de gesynthetiseerde SnO2 NP's waren bolvormig met een gemiddelde grootte in het bereik van 4-5 nm. Bhattacharjee et al. [83] gebruikte glycine om SnO2 . te produceren NP's uit tin(II)chloride. Er werd gesuggereerd dat de NP's gevormd bij 200 ° C, 400 ° C en 600 ° C bolvormig, polykristallijn en monodispers van aard zijn met een gemiddelde grootte van respectievelijk 6, 16 en 33 nm. Verder was het bij 400 °C verkregen nanodeeltje luminescerend. Evenzo Begum et al. [84] demonstreerde de synthese van tetragonale rutielstructuur SnO2 NP's die L-lysine gebruiken met een grootte in het bereik van 4–17 nm.
Mechanisme van vorming van tinoxide-nanodeeltjes door groene synthese
In de afgelopen jaren zijn verschillende plantenextracten, micro-organismen en andere biologische derivaten gebruikt bij de groene synthese van metaal en metaaloxide NP's. Studies suggereerden dat de secundaire metabolieten zoals fenolen, flavonoïden, tannines, saponinen, terpenoïden en koolhydraten die aanwezig zijn in het plantenextract een belangrijke rol spelen door zowel als reductie- als stabiliserende middelen te werken bij de synthese van metaal- of metaaloxide-NP's [87]. Bovendien kan door microben gemedieerde synthese zowel intracellulair als extracellulair worden bereikt, afhankelijk van de locatie waar de NP's worden gevormd. Bij extracellulaire synthese vindt bioreductie plaats op het oppervlak van de microbiële cellen in aanwezigheid van de enzymen die aan het oppervlak beschikbaar zijn. Bovendien worden bij intracellulaire biosynthese metaalionen getransporteerd naar de microbiële cel, en de NP's vormen daar gemakkelijk in aanwezigheid van enzymen in de cel [73]. Selvakumari et al. [53] gebruikte Camellia sinensis extract voor de biosynthese van SnO2 NP's. Ze toonden uit hun studies aan dat de polyfenolische verbindingen (epicatechine, epigallocatechine, epicatechinegallaat en epigallocatechinegallaat) die in het extract aanwezig zijn, zowel als afdekkende als stabiliserende middelen werken. De SnO2 NP's die door deze methode worden gevormd, bestaan uit enkele belangrijke stappen, waaronder (i) reductie van Sn 2+ tot Sn 0 , (ii) het reducerende effect van fenolische verbindingen (-OH) van extract om Sn-soorten te vormen, en (iii) thermische transformatie van de Sn-soort in de SnO2 NP's. In de SnO2 NP's gesynthetiseerd met behulp van Calotropis gigantean bladerenextract, zijn polyfenolische verbindingen verantwoordelijk voor de biochemische transformaties van tinionen [62]. Sferische SnO2 NP's met een grootte in het bereik van 3,62-6,34 nm werden gesynthetiseerd met behulp van bloemkoolextract [52]. Er werd gesuggereerd dat de polyfenolen en de flavonoïden van het extract coördineren met de metaalionen, wat resulteert in de vorming van Sn(OH)2 tussenproducten, die bij calcinering leiden tot de vorming van SnO2 NP's. In een andere studie rapporteerden Srivastava en Mukhopadhyay [54] zowel intracellulaire als extracellulaire synthese van sferische SnO2 NP's door de enzymen die worden uitgescheiden door de bacterie E. herbicola . Bij deze methode wordt de Sn 2+ ionen worden gevangen door de extracellulaire enzymen die worden uitgescheiden door de bacteriële cel of door membraan-geassocieerde eiwitten op het celoppervlak, en de reductie werd geïnitieerd door dehydrogenase-enzymen. De Sn 2+ ionen worden gereduceerd door het verkrijgen van twee elektronen en een molecuul NAD + wordt geoxideerd om NADH te vormen, wat uiteindelijk resulteert in de productie van extracellulaire Sn NP's. De gebiosynthetiseerde Sn-nanodeeltjes worden vervolgens geoxideerd door de zuurstof die in de oplossing aanwezig is, wat leidt tot de vorming van SnO2 NP's. FTIR-analyse onthulde de aanwezigheid van eiwitachtige moleculen op het oppervlak, die zorgen voor natuurlijke ondersteuning en stabiliteit van de SnO2 NP's. Bovendien spelen aminozuren als capping- of complexvormers, waardoor het gebruik van giftige chemicaliën tijdens de synthese wordt geminimaliseerd. Het mogelijke mechanisme voor de groene synthese van SnO2 NP's worden weergegeven in Afb. 2:
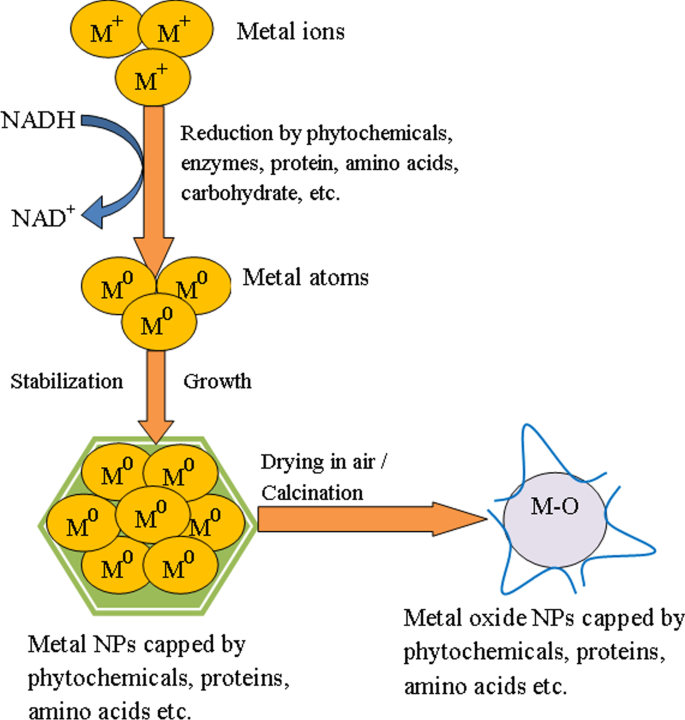
Diagram met het mogelijke mechanisme voor de biologisch gemedieerde synthese van metaaloxide (SnO2 ) NP's
Karakterisatie van tinoxide-nanodeeltjes
Karakterisering van NP's is zeer cruciaal om de syntheseprocedure en -toepassing te kennen en te beheersen. De oppervlaktemorfologie en conformationele details over grootte, vorm, kristalliniteit en oppervlakte van de gesynthetiseerde NP's worden bestudeerd met behulp van verschillende technieken. Enkele van de technieken die worden gebruikt voor het karakteriseren van groen gesynthetiseerde SnO2 NP's zijn UV-Vis, FTIR, XRD, EDS, SEM en TEM. UV-Vis-spectroscopie wordt gebruikt om de vorming van nanodeeltjes te volgen door hun optische eigenschappen te bestuderen. UV–Vis-spectra van de SnO2 NP's gesynthetiseerd met behulp van Catunaregam spinosa extract vertoonde de hoogste absorptiepiek van 223 nm vanwege de oppervlakte-plasmonresonantie [57]. XRD is een krachtige techniek die wordt gebruikt voor het bestuderen van de kristalstructuur van materialen. Bhattacharjee et al. [81] gekenmerkt SnO2 NP's met XRD-pieken bij diffractiehoeken (2θ ) van 26,7, 34,2, 38,07, 51,9, 54,9, 58,1, 62,1, 64,9, 66,08, 71,6 en 79,07 overeenkomend met (110), (101), (200), (211), (220), (002), (310), (112), (301), (202) en (321) vlakken, respectievelijk (Fig. 3). De standaard diffractiepieken tonen de tetragonale rutielstructuur van SnO2 NP's met een gemiddelde kristallietgrootte van 4,6 nm berekend met behulp van de Debye-Scherer-vergelijking [81].
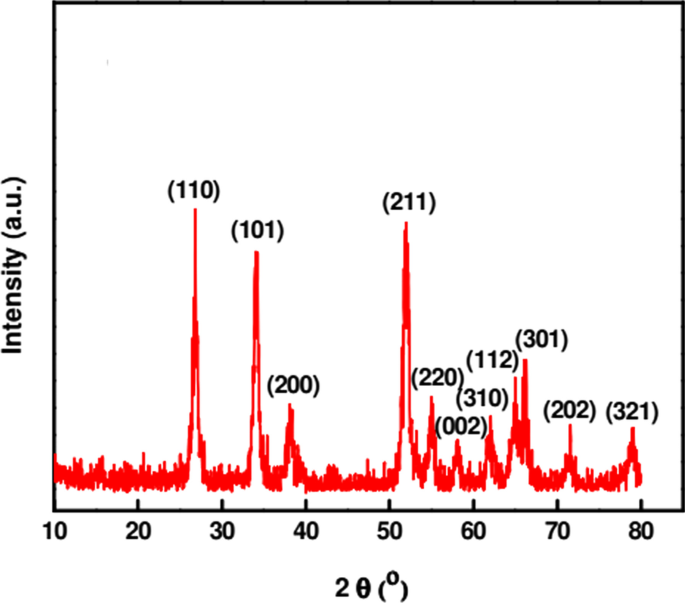
XRD-patronen van SnO2 NP's gesynthetiseerd met arginine onder microgolfstraling [81]
FTIR-spectroscopie wordt gebruikt om de oppervlaktechemie te onderzoeken en de functionele groepen te identificeren die aanwezig zijn op het oppervlak van de NP's, die verantwoordelijk kunnen zijn voor reductie, capping en stabilisatie van NP's [88]. FTIR-analyse van SnO2 NP's gesynthetiseerd met behulp van Pruni flos extract vertoonde grote absorptiebanden bij 3308, 2153, 1634, 423, 403 en 383 cm −1 . De sterke banden waargenomen bij 3308, 2153 en 1634 cm −1 zijn toegewezen aan uitrekkende trillingen van Sn-OH-groepen als gevolg van watermoleculen geadsorbeerd op de SnO2 oppervlak, respectievelijk C-H-uitrekking van alkynen en C =O-trillingen van flavonoïden. De banden tussen 423 en 383 cm −1 worden toegeschreven aan anti-symmetrische Sn-O-Sn-uitrekking [70]. Op microscopie gebaseerde technieken zoals SEM en TEM zijn op grote schaal gebruikt om de morfologische eigenschappen van de nanodeeltjes te bepalen. TEM geeft echter een betere resolutie en informatie over de interne structuur, zoals kristalstructuur en morfologie, in vergelijking met SEM. De meer nauwkeurige resultaten van de oppervlakte-eigenschappen kunnen worden verkregen met behulp van de FE-SEM. Deze technieken zijn ook nuttig bij het schatten van de gemiddelde grootte van de gesynthetiseerde nanodeeltjes [89]. FE-SEM- en TEM-analyse onthulde de vorming van licht geagglomereerd bolvormig SnO2 NP's met een gemiddelde grootte van 30–40 nm (Fig. 4) [62].

een TEM-afbeeldingen van gebiosynthetiseerde SnO2 NP's; b HR-TEM-beelden van SnO2 NP's; c FE-SEM-afbeeldingen van SnO2 NP's en d SAED-patronen van SnO2 NP's
Verder toonde selectieve gebiedselektronendiffractie (SAED) analyse aan dat de deeltjes nanokristallijn van aard zijn (Fig. 4) [62]. De vorming van bolvorm SnO2 NP's gesynthetiseerd met behulp van Piper betle waterig extract werd bepaald met FE-SEM [63]. Uit TEM- en XRD-analyse bleek de gemiddelde grootte van de NP's 8,4 nm te zijn.
EDS is een analytische techniek die wordt gebruikt om de elementaire samenstelling van een monster te analyseren. De EDS-spectra van SnO2 NP's gesynthetiseerd met behulp van Psidium Guajava bladextract onthulde de aanwezigheid van Sn- en O-pieken, wat de vorming van zuiver SnO2 bevestigt NP's [61].
Biologische toepassing van groene gesynthetiseerde tinoxide-nanodeeltjes
Groene gesynthetiseerde SnO2 NP's vertoonden verbeterde fotokatalytische, antimicrobiële, antioxiderende en antikankeractiviteit in vergelijking met hun bulkvorm. In deze sectie hebben we de toepassingen besproken van groen gesynthetiseerd SnO2 NP's op verschillende gebieden als leidraad voor nieuwe onderzoekers voor toekomstperspectief.
Antimicrobiële activiteit
Veel onderzoekers hebben antimicrobiële activiteit SnO2 . waargenomen NP's. Bijvoorbeeld de antibacteriële activiteit van SnO2 NP's gesynthetiseerd met behulp van aloë vera plantenextract werd bestudeerd met behulp van E. coli en S. aureus . Er werd gesuggereerd dat de NP's actiever waren tegen S. aureus dan E. coli [58]. Dit kan zijn omdat de celwand van E. coli is complexer dan S. aureus . S. aureus heeft een membraan dat bestaat uit dik peptidoglycaan. Echter, de celwand van E. coli heeft een peptidoglycaanlaag plus een buitenmembraan bestaande uit lipopolysaccharide. Het buitenmembraan van E. coli acts as a barrier that lowers the penetration level of ROS into the cell [90,91,92]. Another reason could be the difference in the polarity of their cell membrane. The membrane of S aureus has a more positive charge than E. coli , which result in greater penetration level of negatively charged free radicals causing more cell damage and death in S. aureus than in E. coli [93, 94]. The antibacterial activity of SnO2 NPs synthesized using Punica granatum seed extract has been tested against E. coli. The bactericidal effect increased with increasing the concentration of the nanoparticles [95]. SnO2 NPs synthesized using Trigonella foenum-graecum seed extract also showed similar antibacterial activity against E. coli [72]. In a recent study, Clerodendrum inerme leave extract was used for the synthesis of un-doped and Co-doped SnO2 NPs [96]. The green synthesized un-doped and Co-doped SnO2 NPs were subjected toward antimicrobial activity against five disease-causing pathogens such as E. coli , B. subtillis , A. niger , A. flavus , and C. Albicans, , and their zone of inhibition diameters (ZOIs), minimum inhibitory concentration (MIC), and minimum bactericidal concentration (MBC) were calculated. The Co-doped SnO2 NPs showed substantial antibacterial activity against E. coli and B. subtillis in a concentration-dependent manner compared to the un-doped SnO2 NPs, plant extract, and standard drugs in terms of their MIC (22 ± 0.7, 18 ± 0.8 mg/mL) and MBC (31 ± 0.9, 21 ± 0.6 mg/mL) as well as ZOIs (30 ± 0.08, 26 ± 0.06 nm), respectively. The authors suggested that the broad-spectrum antibacterial activity of Co-doped SnO2 NPs is due to cobalt doping, which leads to increased grain size and surface area of the NPs as compared to un-doped SnO2 NP's. As more is the surface area with smaller particle sizes, the greater will be the antimicrobial activity. The associations of biomolecules like flavonoids and phenolic compounds with Co-doped SnO2 NPs are also responsible for the enhancement of their antimicrobial activity. Furthermore, the green synthesized Co-doped SnO2 NPs showed extraordinary antifungal activity with maximum ZOIs of 17 ± 0.04, 23 ± 0.08, and 26 ± 0.06 nm against A. niger , A. flavus, and C. Albicans, respectively, in comparison with plant extract, un-doped SnO2 NPs, and standard drugs [96].
The actual mechanism of action of SnO2 NPs against microbial strains is still unknown. However, several mechanisms of action against bacteria have been suggested for metal oxide nanoparticles, such as the decomposition of nanoparticles, electrostatic interaction of nanoparticles with the cell wall of microorganisms, and formation of reactive oxygen species (ROS) by the effect of light radiation [97,98,99]. One possible cause for the antibacterial effect of SnO2 NPs may be the accumulation of the NPs on the surface of the bacterial cell membrane. The ROS generated due to the presence of SnO2 NPs interacts with the cell membrane and disturbs the membrane permeability and respiration system of the bacteria, which leads to cell death [72, 95, 100]. For instance, Khan et al. suggested that the release of Sn 4+ en Co 2+ is responsible for the damage of bacterial DNA and mitochondria, which inactivates the bacterial enzyme and finally leads to cell death [96].
Antioxidant Activity
Many researchers examined the antioxidant activity of NPs by monitoring the ability in quenching of stable DPPH (2,2-diphenyl-1-picrylhydrazyl) radical into non-radical form (DPPH-H). Kamaraj et al. [101] reported the antioxidant activity of SnO2 NPs biosynthesized using Cleistanthus Collinus leaves extract. The antioxidant activity of SnO2 NPs increased with increasing concentration of SnO2 NPs and reaction time. In another study [95], the free radical scavenging activity of green synthesized SnO2 NPs increased in a dose-dependent manner. However, the annealed sample exhibited a lower scavenging activity as compared to the as-prepared sample. The decrease in scavenging activity with increasing annealing temperature may be due to a decrease in surface area-to-volume ratio of the NPs. Moreover, the antioxidant efficacy of SnO2 NPs against DPPH is due to the transfer of electron density between the NPs and the free radical located at nitrogen in DPPH. A similar result was found for SnO2 NPs synthesized using Trigonelle foenum-graecum aqueous extract [72]. Hong et al. [67] reported significant antioxidant properties of biosynthesized SnO2 NP's. The antioxidant activity of the biosynthesized SnO2 increased with increasing concentration of the NPs, with IC50 (half-maximal inhibitory concentration) value of 2257.4 µg/ml. Recently, Khan et al. reported significant antioxidant activity of Co-doped SnO2 NPs, as compared to un-doped SnO2 NPs and plant extract [96].
Cytotoxic Activity
SnO2 NPs synthesized using an aqueous extract of agricultural waste of dried peel of Annona squamosa were evaluated for cytotoxicity test against the hepatocellular carcinoma cell line (HepG2) [64]. TEM results revealed the loss of cell volume, considerable swelling of the cells, and nuclear condensation. The nuclear condensation seen in SnO2 NP-treated HepG2 cells might be due to the breakdown of chromatin in the nucleus. SnO2 NPs inhibited cell proliferation in a dose- and time-dependent manner with an IC50 value of 148 µg/mL. SnO2 NPs synthesized using piper nigrum seed extract exhibited higher cytotoxic activity against colorectal (HCT116) and lung (A549) cancer cell lines [69]. The proliferation of both cancer cell lines increased with increasing NPs size. Besides, a gradual decline in cell viability was observed with increasing dosage of SnO2 NP's. The authors concluded that the cytotoxic effect was associated with the generation of oxidative stress from reactive oxygen species (ROS). SnO2 NPs fabricated by using Pruni spinosae flos aqueous extract revealed an excellent cytotoxic effect against non-small cell lung cancer cell A549 and lung fibroblast CCD-39Lu cells, in concentration- and time-dependent manner [70]. Recently, Khan et al. [96] investigated the in vitro cytotoxic effect of green synthesized un-doped SnO2 NPs and Co-doped SnO2 NPs against mammary gland breast cancer (MCF-7), human amnion (WISH), and human lung fibroblast (WI38) cell lines by a colourimetric technique 3-(4,5-dimethylthiazol-2yl)-2,5-diphenyl tetrazdium bromide (MTT) assay. The green synthesized Co-doped SnO2 NPs showed significant and substantial mortality rate compared to un-doped SnO2 NPs, plant extract, and standard drug 5-FU (5-5-5-fluorouracil), while un-doped SnO2 NPs exhibited a similar mortality rate to that of the standard drug, but the lowest cytotoxicity against breast cancer cell line was observed with the plant extract. The cytotoxic effect of the plant extract, green synthesized un-doped SnO2 , and Co-doped SnO2 NPs was performed with IC50 values of 31.56 ± 1.4, 26.99 ± 1.9, and 18.15 ± 1.0 µg/mL for MCF-7, and 40.69 ± 0.9, 38.97 ± 0.8, and 36.80 ± 0.6 µg/mL for WI38, and 38.56 ± 0.8, 35.56 ± 0.9, and 31.10 ± 0.7 µg/mL, respectively, and depicted that the cytotoxicity of Co-doped SnO2 NPs was more proficient as compared to plant extract and un-doped SnO2 NPs alone. Additionally, the authors reported excellent observational results showing greater in vitro inhibition of breast cancer MCF-7 cell lines in a concentration- and dose-dependent manner. The green synthesized NPs also showed robust cytotoxicity against MCF-7 as compared to WI38 and WISH normal cell lines with Co-doped SnO2 NPs unveiling higher ROS generation than the un-doped SnO2 NP's. Figure 5 shows the probable cytotoxicity mechanism of green synthesized SnO2 NP's.
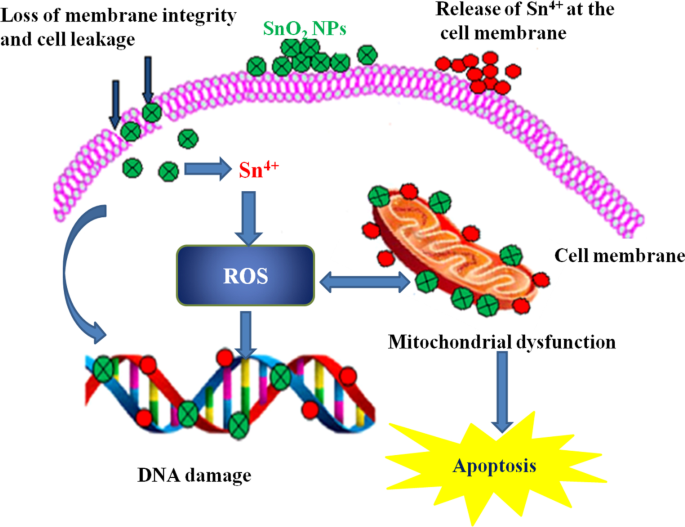
Mechanism during cytotoxicity of green synthesized SnO2 NP's
Photocatalytic Activity
The uncontrolled release of toxic chemicals, hazardous textile dyes, and pesticides from various industries into the running water has led to severe environmental problems. These superfluous water contaminants cause long-term adverse effects and pose a real threat to aquatic and human life. Besides, some organic dyes are carcinogenic and toxic. Hence, treating water that contains poisonous chemicals before disposal to the environment is very crucial to reduce environmental pollution. Recent studies have shown that nanostructured semiconductor metal oxides act as an excellent photocatalyst for the removal of various water pollutants [102,103,104,105]. Among the semiconductor metal oxides, SnO2 is extensively used in the removal of common textile dyes and organic compounds owing to its beneficial characteristics, which include physical and chemical stability, high surface reactivity, high photocatalytic efficiency, low cost, and low toxicity [68, 106]. Manjula et al. [107] synthesized SnO2 nanoparticles using glucose. The NPs were effectively used as a catalyst in degrading methyl orange (MO) dye. The effect of calcination temperature (150–500 °C) on the photocatalytic activity of the NPs was investigated, and the results revealed that the as-synthesized SnO2 NPs calcinated at 150 °C is the best photocatalyst for the reaction under study among the studied materials. Moreover, the as-prepared SnO2 nanoparticles degraded methyl orange completely in 30 min, and also, the nanomaterials may be recycled with enhanced efficiency a minimum of five times. In another study [108], the photocatalytic activity of the SnO2 QDs (quantum dots) synthesized by using serine was evaluated by monitoring the optical absorption spectra of eosin Y solution under direct sunlight. It was observed that the rate of degradation of eosin Y using SnO2 QDs (98%) is higher than that using commercial SnO2 (96%) and P25 (88%). Begum et al. [84] reported the synthesis of SnO2 NPs using an amino acid, L-lysine monohydrate. The synthesized nanoparticles were evaluated for their photocatalytic behavior toward toxic organic dyes, namely malachite green oxalate (MGO) and Victoria blue B (VBB) under direct sunlight. The absorption peak of these dyes has begun to reduce, which shows that the chromophore structure has been demolished (Fig. 6). Furthermore, the as-prepared SnO2 NPs exhibited an outstanding photocatalytic degradation of MGO (97.3%) and VBB (98%) dye within 120 min. Literature reports on the photocatalytic activity of green synthesized SnO2 NPs are summarized in Table 3.
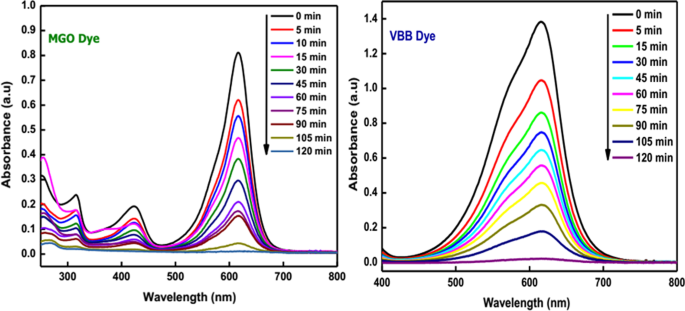
Photocatalytic degradation of malachite green oxalate dye under solar irradiation using SnO2 NP's
Gas-Sensing Property
Many metal oxide-based gas sensors are widely used for gas-sensing applications. However, SnO2 NPs has gained tremendous attention in gas sensing under atmospheric conditions because of its beneficial properties, which include high sensitivity, high selectivity, easy reversibility, and cheap manufacturing costs. Green synthesized porous SnO2 nanospheres demonstrated excellent gas sensing capabilities [107]. It was observed that the assimilation of 0.5 wt% Pd into the SnO2 matrix improved the sensitivity and made it highly selective for low-temperature hydrogen detection. Moreover, the fabric was able to respond to even 50 ppm H2 in N2 at room temperature with an interval of 10 s. These sensing properties are due to the synergetic effect of both the porous structure of SnO2 nanospheres and also the catalytic property of Pd nanoparticles. Gattu et al. [77] reported the gas-sensing behavior of biosynthesized and chemically synthesized Ni-doped SnO2 NPs thin films. The biosynthesized Ni-doped SnO2 NPs thin film showed higher NO2 gas-sensing response as compared to the chemically synthesized ones. The sensor response was found to be increased with Ni doping for both biosynthesized and chemically synthesized Ni-doped SnO2 NP's. This may be due to the reduction of particle size with Ni-doping, which results in increased surface area for adsorption of NO2 gas. Furthermore, the Ni-doped SnO2 thin film exhibited excellent selectivity toward NO2 gas when put next to other gases like NH3 , LPG and H2 S. In another study [78], the gas-sensing properties of un-doped and Fe-doped SnO2 NPs synthesized using Cicer arietnum L. extract were reported. The gas response within the presence of 100 ppm NH3 gas at 200 °C operating temperature was found to be 28% for un-doped SnO2 and 46% for Fe-doped SnO2 dunne films. Moreover, the Fe-doped SnO2 -based sensor was found to be more selective for NH3 gas as compared to the un-doped SnO2 sensor. The biosynthesized Au-doped SnO2 NPs were found to be highly sensitive to NO2 gas at 200 °C operating temperature [79]. Gas sensor supported Au-doped SnO2 NPs showed the gas response of ~ 30% for 100 ppm of NO2 gas. Additionally, the gas sensor of Au-doped SnO2 NPs showed excellent selectivity toward NO2 gas when put next to other gases like H2 S, LPG, and NH3 . The improved gas response and selectivity toward NO2 gas are because of the lattice distortion induced by Au-doping and also the oxygen vacancies generation within the SnO2 lattice.
Conclusies
The use of green methods for the production of NPs has been the area of focused research because it is an eco-friendly, inexpensive, nontoxic, and sustainable method. Numerous studies report the possibility of producing SnO2 NPs via a green protocol using a range of plant materials, bacteria, and natural biomolecules. The literature survey shows that the green substrates act as reducing and stabilizing agents or capping agents regardless of their source. Among the various green methods of SnO2 synthesis, plant-mediated synthesis is cost-effective, easy to process, and less hazardous than microorganisms. However, the plant extracts consist of a large number of active compounds in a different composition, which makes it difficult to know the exact amount of the molecules responsible for the reduction of metal ions. Due to this complexity, it is difficult to evaluate the synthesis of nanoparticles. Therefore, further study on the mechanism of formation of SnO2 NPs is required to understand the chemical reactions that occur during the synthesis. With the knowledge of the actual reaction mechanism, it will be possible to monitor and optimize the biosynthesis process, which is essential for the large-scale production of SnO2 NP's. Hence, understanding of the rapidly growing method of synthesis discussed herein will help facilitate future research progress on SnO2 NPs and their enormous potential for industrial-scale production in the near future.
Beschikbaarheid van gegevens en materialen
Not available.
Afkortingen
- NPs:
-
Nanodeeltjes
- SnO2 NP's:
-
Tin oxide nanoparticles
- UV-Vis:
-
Ultraviolet-zichtbare spectroscopie
- SEM:
-
Scanning elektronenmicroscopie
- FE-SEM:
-
Veldemissie scanning elektronenmicroscopie
- TEM:
-
Transmissie-elektronenmicroscopie
- HR-TEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- FTIR:
-
Fourier-transformatie infraroodspectroscopie
- EDS:
-
Energy dispersive X-ray analysis
- PSA:
-
Particle size analyzer
- XPS:
-
Röntgenfoto-emissiespectroscopie
- SAED:
-
Selective area electron diffraction
Nanomaterialen
- Speciale oxidevuurvaste materialen en hun toepassingen
- Multifunctionele gouden nanodeeltjes voor verbeterde diagnostische en therapeutische toepassingen:een overzicht
- Voorbereiding van met ICA geladen mPEG-ICA nanodeeltjes en hun toepassing bij de behandeling van door LPS geïnduceerde H9c2-celbeschadiging
- Biogene synthese, karakterisering en antibacteriële potentiële evaluatie van koperoxide-nanodeeltjes tegen Escherichia coli
- De potentiële lever-, hersen- en embryotoxiciteit van titaniumdioxide-nanodeeltjes op muizen
- Vorming en lichtgevende eigenschappen van Al2O3:SiOC-nanocomposieten op basis van aluminiumoxide-nanodeeltjes gemodificeerd door fenyltrimethoxysilaan
- De voorbereiding van Au@TiO2 Yolk–Shell Nanostructure en zijn toepassingen voor afbraak en detectie van methyleenblauw
- Gemakkelijke synthese van wormgatachtig mesoporeus tinoxide via verdamping-geïnduceerde zelfassemblage en de verbeterde gasdetectie-eigenschappen
- Groene bekwaamheid in de synthese en stabilisatie van kopernanodeeltjes:katalytische, antibacteriële, cytotoxiciteits- en antioxidantactiviteiten
- Platycodon-saponinen van Platycodi Radix (Platycodon grandiflorum) voor de groene synthese van gouden en zilveren nanodeeltjes
- Groene synthese van metaal- en metaaloxidenanodeeltjes en hun effect op de eencellige alg Chlamydomonas reinhardtii



