Gerestaureerd microRNA-133a-3p of uitgeput PSAT1 beperkt endotheelcelschade-geïnduceerd intracraniaal aneurysma via onderdrukking van de GSK3β/β-Catenin-route
Abstract
Het is onduidelijk over de functionele rol van microRNA-133a-3p (miR-133a-3p) in intracraniaal aneurysma (IA). Daarom was het doel van de huidige studie om de regulerende rol van miR-133a-3p op de regulatie van vasculaire endotheliale schade-geïnduceerde IA te onderzoeken via fosfoserine-aminotransferase 1 (PSAT1) / glycogeensynthasekinase 3β (GSK3β) / β-catenine-signalering pad. Normale intracraniële arteriole weefsels en IA-weefsels werden verzameld van patiënten met hersentrauma en IA. De expressie van miR-133a-3p, PSAT1, GSK3β en β-catenine in weefsels werd bepaald door RT-qPCR en western blot-analyse. De endotheelcellen (EC's) van de menselijke IA werden gekweekt en behandeld met miR-133a-3p-nabootsing en si-PSAT1 om hun functies bij endotheelcelmigratie, apoptose en proliferatie te bepalen. De expressie van miR-133a-3p, PSAT1, GSK3β, β-catenine, Ki-67, CyclinD1, Bax en Bcl-2 in EC's werd getest met RT-qPCR of western blot-analyse. Bovendien werd een IA-rattenmodel opgezet om de pathologische veranderingen en de expressie van miR-133a-3p, PSAT1, GSK3β, β-catenine, VEGF en MMP-9 in IA-weefsels in vivo te detecteren. Expressie van miR-133a-3p was gerelateerd aan het aantal en de grootte van IA. MiR-133a-3p-expressie was overleden en de PSAT1-, GSK3β- en β-catenine-expressie was verhoogd in IA. Hersteld miR-133a-3p en verarmd PSAT1 verlichtten de pathologische verandering; verminderde PSAT1-, GSK3β- en β-catenine-expressie in IA; onderdrukte apoptose en geavanceerde proliferatie en migratie van IA EC's, evenals verminderde VEGF- en MMP-9-expressie in IA-weefsels in vivo. Onze studie suggereert dat overexpressie van miR-133a-3p of downregulatie van PSAT1 endotheelcelbeschadiging beperkt en endotheelcelproliferatie bevordert via remming van de GSK3β/β-catenine-route in IA. MiR-133a-3p is mogelijk een potentiële kandidaat-marker en therapeutisch doelwit voor IA.
Presentatie van de hypothese
In deze huidige studie zouden we kunnen speculeren dat miR-133a-3p/PSAT1-as de door endotheelcelschade geïnduceerde IA zou kunnen beïnvloeden door modulatie van de GSK3β/β-catenine-route.
De hypothese testen
Om deze hypothese te verifiëren, hebben we klinische monsters, endotheelcellen (EC's) van de menselijke IA verzameld en IA-rattenmodellen opgesteld om de functies van miR-133a-3p en PSAT1 in het IA-proces op te helderen.
Implicaties van de hypothese
Onze studie bevestigt onze hypothese dat overexpressie van miR-133a-3p of downregulatie van PSAT1 endotheelcelbeschadiging beperkt en endotheelcelproliferatie bevordert via remming van de GSK3β/β-catenine-route in IA. Deze bevindingen bieden een nieuw inzicht in een nieuwe doeltherapie voor IA.
Inleiding
Intracraniaal aneurysma (IA) is een soort cerebrovasculaire aandoening, die wordt gekenmerkt door onconventioneel opgezwollen slagader in de hersenen, evenals subarachnoïdale bloeding (SAH) veroorzaakt door IA-ruptuur, gepaard gaand met een hoge sterfte en morbiditeit [1]. Net als een destructieve ziekte is de pathogenese van IA niet opgehelderd [2]. IA is een zeldzame familiale vorm, maar algemeen wordt aangenomen dat het het gevolg is van verworven vaatletsel veroorzaakt door hypertensie, roken en andere traditionele risicofactoren [3]. Endovasculaire coiling of microchirurgische clipping zijn gebruikt om toekomstige ruptuur van ongescheurd aneurysma te voorkomen bij patiënten met een hoog risico op ruptuur [4]. Hoewel er aanzienlijke vooruitgang is geboekt in IA-chirurgische operaties, is er nog steeds een slecht postoperatief herstel bij IA-patiënten [5]. De moeilijke situatie van IA-behandeling maakt het noodzakelijk om het mechanisme verder te onderzoeken en een nieuwe therapeutische strategie te vinden.
MicroRNA's (MiRNA's) zijn een klasse van niet-coderende RNA's die de expressie van doelgenen moduleren door translatie op post-transcriptioneel niveau te remmen of mRNA-afbraak te bemiddelen [6]. Er is onthuld dat miR-133a-3p als tumorremmer in verschillende kwaadaardige neoplasieën en overexpressie van miR-133a-3p de groei van colorectale kankercellen (CRC) kan remmen [7]. Een eerdere studie heeft betoogd dat miR-133a-3p, in het licht van het blokkeren van autofagie-gemedieerde glutaminolyse, de metastase en groei van maagkanker verder onderdrukt [8]. Ook heeft een onderzoek aangetoond dat miR-133a-3p betrokken is bij het reguleren van de hartontwikkeling en cardiale hypertrofie [9]. Een studie heeft aangetoond dat opregulatie van miR-195-5p de angiogenese en cisplatineresistentie bij eierstokkanker vermindert door de fosfoserine-aminotransferase 1 (PSAT1)-afhankelijke GSK3β/β-catenine-signaleringsroute [10] te onderdrukken. Een andere studie heeft gemeld dat miR-365 celinvasie en groei in slokdarm-plaveiselcelcarcinoom (ESCC) onderdrukt door PSAT1 te moduleren [11]. PSAT1 is een enzym dat betrokken is bij de biosynthese van serine; het wordt oorspronkelijk gezuiverd uit de schapenhersenen en heeft een hoog gehalte in veel weefsels [12]. Er is gedocumenteerd dat PSAT1 de voortgang van de celcyclus bij borstkanker medieert door modulatie van de GSK3β/β-catenine-signaleringsroute [13]. Liu et al. wijst er ook op dat PSAT1 een functie uitoefent op de ontwikkeling van ESCC en een slechte overleving voorspelt; daarom kan het een veelbelovend doelwit zijn voor geneesmiddelen tegen kanker [14]. Gezien de bovengenoemde analyses werd verwacht dat deze studie bijdragen zou leveren aan een nieuwe benadering voor de functionele rol van de miR-133a-3p/PSAT1/GSK3β/β-catenine-as in IA.
Materialen en methoden
Ethische verklaring
De studie werd goedgekeurd door de Institutional Review Board van het First Teaching Hospital van de Tianjin University of Traditional Chinese Medicine. Alle deelnemers ondertekenden een document van geïnformeerde toestemming. Alle dierproeven zijn door internationale comités geteld met de Gids voor de verzorging en het gebruik van proefdieren.
Studieonderwerpen
Van januari 2016 tot maart 2018 werden de gevallen van SAH, veroorzaakt door IA, die werden behandeld in de neurochirurgie van het eerste academisch ziekenhuis van de Tianjin University of Traditional Chinese Medicine, geselecteerd. De pathologische monsters van 75 gevallen van IA verkregen door microchirurgie werden verzameld en geclassificeerd als IA-groep, waaronder 29 mannen en 46 vrouwen in de leeftijd van 31-55 jaar, met een gemiddelde leeftijd van 44,98 ± 6,79 jaar. Patiënten met hersentrauma die tegelijkertijd in de neurochirurgie werden behandeld in het First Teaching Hospital van de Tianjin University of Traditional Chinese Medicine, werden geselecteerd als de controlegroep. Ook werden 75 gevallen van normale intracraniële arteriole weefsels vergaard door traumatische operatie of interne decompressie, waaronder 43 mannen en 32 vrouwen in de leeftijd van 34-56 jaar, met een gemiddelde leeftijd van 48,14 ± 8,68 jaar. Patiënten werden uitgesloten als ze een voorgeschiedenis hadden van hypertensie, diabetes of tumoren. Er was geen duidelijk verschil in geslacht en leeftijd tussen de IA-groep en de controlegroep (beide P> 0,05).
Voorbeeldbehandeling en conservering
Na chirurgische resectie werden enkele van de monsters in twee groepen gefixeerd met formaldehyde, gedehydrateerd met gradiëntalcohol van lage naar hoge concentratie en ingebed met paraffine. Vervolgens werden de monsters gesneden voor hematoxyline-eosine (HE) kleuring en immunohistochemische kleuring. Sommige monsters werden snel in tanks met vloeibare stikstof geplaatst en vervolgens overgebracht naar een cryogene koelkast van -80 ° C voor de detectie van western-blot-analyse en kwantitatieve polymerasekettingreactie van omgekeerde transcriptie (RT-qPCR). Sommige monsters werden gefixeerd met glutaaraldehyde voor observatie met een elektronenmicroscoop en sommige monsters werden gebruikt voor isolatie van EC's.
Elektronenmicroscoopobservatie
Monsters werden gefixeerd met 3% glutaaraldehyde en vervolgens opnieuw gefixeerd met 1% osmiumtetroxide. Monsters werden gedehydrateerd met aceton, ingebed met Epon812 en in halfdunne secties met een dikte van 3 m gesneden. Ten slotte werden de monsters dubbel geverfd met uranylacetaat en loodcitraat en waargenomen door een H-600IV transmissie-elektronenmicroscoop (Hitachi, Tokyo, Japan).
HE-kleuring
De bereide paraffinecoupes werden gedurende 30 minuten bij 60°C gebakken. Nadat de bovenstaande stappen waren voltooid, werden de weefselplakken gefixeerd in xyleen, gedehydrateerd met gradiënt absolute alcohol en gereinigd met fosfaatgebufferde zoutoplossing (PBS). De weefselplakjes werden gekleurd met hematoxyline, enkele seconden in ammonia behandeld, 2 minuten gekleurd met eosine, gedehydrateerd en geklaard. Vervolgens werden de weefselplakken gedruppeld met neutrale gom en afgesloten met dekglas. Ten slotte werd een microscoop (Nikon, Tokyo, Japan) gebruikt voor observatie en opname.
Immunohistochemische kleuring
Immunohistochemiekit werd geproduceerd door Zymed Laboratories (San Francisco, CA, VS). De paraffineschijfjes werden van was ontdaan en gehydrateerd en de paraffineschijfjes werden 5 min x 3 keer ondergedompeld in xyleenoplossing. De plakjes werden 3 minuten x 2 keer in 100% absolute alcohol geplaatst en vervolgens 3 minuten achter elkaar in 95-75% alcohol gedrenkt. Na het ontparaffineren werden de schijfjes 15 minuten geïncubeerd met 3% waterstofperoxide om de activiteit van endogeen peroxidase te elimineren. De plakjes werden gedruppeld met een blokkerende oplossing en gedurende 15 minuten geïncubeerd met normale geitenserum-werkoplossing, vervolgens onderzocht met primair antilichaam tegen matrix metalloprotease (MMP)-9 (5 g / ml) en vasculaire endotheliale groeifactor (VEGF) (1:250 , Abcam, Cambridge, MA, VS) (PBS voor negatieve controle (NC)) en gedurende 1-2 uur geïncubeerd. De plakjes werden gedurende 30-60 minuten opnieuw onderzocht met een secundaire antilichaam-werkoplossing van biotinylering. De plakjes werden toegevoegd met streptavidine/peroxidase-werkvloeistof gelabeld met mierikswortelperoxidase, gedruppeld met nieuw bereide diaminobenzidine (DAB)-oplossing, tegengekleurd en geblokkeerd. Het beeld was bekend met het Nikon SPOT FlexTM-beeldvormingssysteem. Het gebied van MMP-9- en VEGF-eiwitexpressie werd gemeten met immunohistochemische kwantitatieve analysesoftware. Vijf krachtige visuele velden werden willekeurig gedetecteerd in het accumulatiegebied van positieve cellen in elk monster, en de gemiddelde absorptie van elk scherm werd gebruikt als de gemiddelde waarde voor statistische analyse.
Isolatie en cultuur van EC's
De EC's werden geïsoleerd uit normale intracraniële arteriole weefsels en IA-weefsels en gekweekt. Het weefsel werd gesneden in 3 mm 2 fragmenten en gedurende 25 min geïncubeerd in 0,1% collagenase B/0,1% dispase (Roche, Basel, Zwitserland). Het weefsel werd losgemaakt, 2 minuten getritureerd met een pipet van 2 ml en gefilterd DOOR een zeef van 100 m (BD Biosciences, NJ, VS) om EC's te isoleren. Celsuspensie werd gecentrifugeerd en vervolgens opnieuw gesuspendeerd in een kweekmedium MV2 dat groeifactoren en 20% foetaal runderserum bevat (PromoCell, Heidelberg, Duitsland). Vervolgens werden de cellen gezaaid op met fibronectine (Sigma Aldrich Inc., St. Louis, MO, VS) gecoate schaaltjes met een dichtheid van 10 4 cellen/cm 2 (1 μg/cm 2 ) en gedurende 1 dag gekweekt met 5% CO2 . De dag na het zaaien werden de cellen gespoeld met PBS om losse cellen te verwijderen en in een vers medium geplaatst. Bij het bereiken van ongeveer 80-100% samenvloeiing werden de culturen blootgesteld aan immunoscheiding door Ulex europaeus Agglutinine I (UEA)-gecoate (Vector Laboratories, Ltd., Peterborough, VK) kralen (Dynabeads M-450 Tosylactivated, Oxoid, Hampshire, VK) om zuivere EC's verkrijgen. EC's gebonden aan de met lectine beklede kralen werden verzameld met een magnetische deeltjesconcentrator terwijl ongebonden cellen werden verwijderd door tweemaal te wassen met basaal medium. UEA-positieve cellen werden opnieuw gesuspendeerd in kweekmedium en uitgezaaid op met fibronectine beklede schalen om hun hechting en groei te verbeteren. Culturen werden binnen 4-6 dagen confluent.
Identificatie van EC's
De EC's werden geïdentificeerd door middel van immunocytochemische kleuring met een celoppervlak CD31 antilichaam en een FVII-factor-gerelateerd antigeen. De cellen werden tweemaal schoongemaakt met PBS, gefixeerd met 4% paraformaldehyde, geïncubeerd met 3% H2 O2 gedurende 10-15 minuten om endogene peroxidase-activiteit te elimineren en vervolgens gedurende 10 minuten geïncubeerd met 0, 1% Triton X-100 tot geperforeerde cellen. De cellen werden gedruppeld met specifiek primair antilichaam:Factor VII (1:200), CD31 (1:400, Roche, Basel, Zwitserland) en een nacht bij 4 ° C geïncubeerd. Vervolgens werden de cellen gedruppeld met immunoglobuline G (1:50) gelabeld met mierikswortelperoxidase secundair antilichaam. De cellen werden gedurende 45 minuten bij 37 ° C geïncubeerd en ontwikkeld door DAB gedurende 4 minuten waarbij licht werd vermeden. Daarna werd de kleurontwikkeling met het gedestilleerde water beëindigd en werd de foto onder de microscoop bekeken. De cellen werden waargenomen onder de fluorescentie-inverted phase-difference-microscoop, en de positieve cellen en het totale aantal cellen werden willekeurig geteld uit 10 gezichtsvelden. De positieve kleuring celsnelheid =(het aantal positieve cellen/het totale aantal cellen) × 100%. De overeenkomstige NC-groep werd vastgesteld en het primaire antilichaam werd vervangen door PBS en de andere stappen werden uitgevoerd zoals hierboven.
Groepering en transfectie van cellen
Om de effecten tussen miR-133a-3p en PSAT1 op EC's van IA te bestuderen, werden EC's gegroepeerd in controlegroep (normale vasculaire EC's zonder enige transfectie), IA-groep (IA vasculaire EC's zonder enige transfectie), nabootsende NC-groep (getransfecteerd met miR -133a-3p mimic NC), miR-133a-3p mimic groep (getransfecteerd met miR-133a-3p mimic), kleine interfererende RNA (si)-NC groep (getransfecteerd met si-PSAT1 NC), si-PSAT1 groep (getransfecteerd met si-PSAT1) en miR-133a-3p mimic + overexpression (oe)-PSAT1 groep (getransfecteerd met miR-133a-3p mimic en oe-PSAT1). Onder hen werden mimic NC, miR-133a-3p mimic, si-PSAT1, si-NC en oe-PSAT1 bedacht en samengesteld door GenePharma Co., Ltd. (Shanghai, China). Transfectie werd uitgevoerd in strikte overeenstemming met de instructies van Lipofectamine TM 2000 transfectiereagens (Thermo Fisher Scientific, MA, VS).
Flowcytometrie
Het medium in de kweekschaal werd weggegooid en de cellen werden tweemaal gespoeld met PBS. Cellen werden losgemaakt met 0,25% trypsine, 5 minuten gecentrifugeerd bij 800 rpm en gesuspendeerd met 1 × bindingsbuffer, en de celdichtheid werd aangepast tot 1 × 10 7 cellen/ml. De celsuspensie (100 L) werd gedurende 20 minuten geïncubeerd met 5 μL propidiumjodide (PI, 20 g/mL) en annexine V-FITC, vervolgens gemengd met 400 μL 1 × bindingsbuffer. Flowcytometer (BD FACSArial I-celsorteerder) werd gebruikt om celapoptose binnen 1 uur te detecteren. De resultaten waren dat het linker onderste kwadrant (Q4) op de spreidingskaart gezonde levende cellen liet zien (FITC − /PI − ), het kwadrant rechtsonder (Q3) als de vroege apoptotische cellen (FITC + /PI − ), en het rechter bovenste kwadrant (Q2) waren de late apoptotische en apoptotische cellen (FITC + /PI + ); apoptosepercentage =percentage vroege apoptose (Q3) + percentage late apoptose (Q2).
3-(4,5-dimethylthiazol-2-Yl)-2, 5-difenyltetrazoliumbromide (MTT)-assay
De cellen werden losgemaakt met trypsine om celsuspensie te bereiden. Cellen werden geteld onder een omgekeerde microscoop. De celconcentratie werd aangepast tot 5 × 10 4 cellen/ml. Cellen werden gezaaid in een kweekplaat met 96 putjes. Na 48 uur werden de cellen gedurende 4 uur geïncubeerd met 20 L MTT-oplossing. MTT in elk putje werd opgelost met 150 L dimethylsulfoxide. De waarde van de optische dichtheid (OD) van EC's werd gemeten bij de golflengte van 570 nm. De proliferatiesnelheid van EC's werd gerekend in het licht van de OD-waarde.
Krastest
De cellen in elke groep werden gezaaid in een plaat met 24 putjes met 2 x 10 5 cellen/put. In elke groep werden drie parallelle putjes geplaatst. Toen ongeveer 90% samenvloeiing werd bereikt, werd het celgroeivlak bekrast met een gesteriliseerde wegwerpbare micropipetpunt van 1 ml; elk putje werd eenmaal bekrast en de kraslengte en diepte van elk putje waren consistent. Na het krabben werden de drijvende cellen verwijderd, het kweekmedium werd vervangen door vers en de krasafstand werd na 24 uur kweken onder de microscoop waargenomen. Het genezingsgebied van de kraswond werd geteld door de National Instrument Vision Assistant 8.6-software. De celmigratie =wondgenezingsgebied/eerste kraswondgebied × 100%.
Experimenteer dieren en vestiging van IA-ratmodellen
Vierentachtig Sprague-Dawley (SD) ratten van 7 weken oud en met een gewicht van 180 tot 200 g (Laboratory Animals Center, de Academie voor Militaire Medische Wetenschappen, Peking, China) werden geselecteerd. De ratten werden gehuisvest in het proefcentrum voor dieren. De voedingscondities werden gecontroleerd bij 22-25 ° C en 50-60% vochtigheid met natuurlijk licht. Alle ratten werden gevoerd in standaard rattenkooien met 4 ratten per kooi. De ratten werden gevoed met stedelijk sanitair drinkwater en gewoon rattenvoer. De kussens werden om de 3 dagen vervangen en de kooi werd gewassen en gesteriliseerd. De IA-ratten werden gemodelleerd in overeenstemming met de referentie [15]. Gescheurd aneurysma werd vastgesteld wanneer de volgende symptomen optraden bij ratten [16]:1, verminderde eet- of drinkactiviteit door gewichtsverlies (ongeveer 10% gewichtsverlies) gedurende 24 uur; 2, flexie van de romp en voorpoten bij het optillen; 3, aan één kant lopen in een normale houding; 4, leunend naar één kant in rust, geen spontane activiteit. De ratten met deze symptomen werden 3 maanden na de operatie geëuthanaseerd. IA-weefsels werden tijdens de operatie verkregen en geperfuseerd met PBS, en de blauwe kleurstof die glutaminezuur bevatte werd in de hersenslagader geperfuseerd.
Behandeling en interventie van IA-ratten
De bovenstaande 84 ratten werden willekeurig verdeeld in 7 groepen met 12 ratten in elke groep. De behandelmethoden waren als volgt:normale groep (er werd geen modellering uitgevoerd); IA-groep (stereotactisch geïnjecteerd met 100 L mengsel van PBS en Lipofectamine 2000); nabootsen van NC-groep (stereotactische injectie met 100 L mengsel van miR-133a-3p nabootsen van NC en Lipofectamine 2000); miR-133a-3p-nabootsingsgroep (stereotactische injectie met 100 L mengsel van miR-133a-3p-nabootsing en Lipofectamine 2000); si-NC-groep (stereotactische injectie met 100 L mengsel van si-PSAT1 NC en Lipofectamine 2000); si-PSAT1-groep (stereotactische injectie met 100 L mengsel van si-PSAT1 en Lipofectamine 2000); en miR-133a-3p mimic + oe-PSAT1-groep (stereotactische injectie met 100 L mengsel van miR-133a-3p mimic en oe-PSAT1 en Lipofectamine 2000). Alle bovenstaande injecties werden eenmaal per dag uitgevoerd en deze ratten werden gedurende 12 weken grootgebracht in een specifiek pathogeenvrij (SPF) dierlaboratorium. Na 12 weken werden de ratten in elke groep verdoofd en werd de borstholte geopend zoals hierboven beschreven. Vanuit het linkerventrikel dat intubeerde in de aorta, kwam bloed vrij door de cava door te snijden. Tegelijkertijd werd 30 ml zoutoplossing die heparine-natrium (37 °C) bevatte door het kanaal geperfuseerd en vervolgens werd 10% polyformaldehyde/0,1 M fosfaatbuffer (pH 7,4) langzaam via het kanaal in de hersenen geïnjecteerd. Nadat de perfusie was gefixeerd, werden de hersenen geopend. De arteriële ring aan de basis van de schedel werd gescheiden en verwijderd onder de chirurgische microscoop, de veranderingen van aneurysma's werden waargenomen onder de microscoop en de pathologische kenmerken werden onderzocht. De mimic NC, miR-133a-3p mimic, si-NC, si-PSAT1 en oe-PSAT1 werden samengesteld door Shanghai Sangon Biotechnology Co., Ltd. (Shanghai, China).
Detectie van hemodynamica
De stroomsnelheid van bloed aan het einde van de linker gemeenschappelijke halsslagader van ratten werd getest vóór 3 dagen operatie en 12 weken na de interventiebehandeling. De methode was als volgt:de ratten werden in het dierenframe van de anesthesiemachine geplaatst voor inhalatie en de stroomparameters werden aangepast. Nadat de ratten stabiel ademden en er geen duidelijke reactie was wanneer de staart van de ratten werd aangeraakt, werden de ratten met een rubberen band op de experimentele operatietafel gefixeerd. Het haar van de nek van de rat werd geschoren met een elektrisch scheerapparaat. De kleuren Doppler-ultrageluiddetector werd aangezet en de bloedstroomsnelheid aan het einde van de linker gemeenschappelijke halsslagader werd gemeten en de gegevens werden geregistreerd nadat de sonde was ingesmeerd met geschikt koppelingsmiddel. Na de meting werden de ratten voorzichtig terug in de kooi gezet om de luchtwegen vrij te houden totdat de ratten wakker werden na anesthesie.
RT-qPCR
Het totale RNA werd geabstraheerd op basis van een eenvoudige RNA-extractiekit voor totaal RNA (TIANGEN Biotechnology Co., Ltd., Beijing, China). Het hoogwaardige RNA werd bevestigd door ultravioletanalyse en formaldehyde-denaturatie-elektroforese, en RNA werd omgekeerd getranscribeerd in complementair DNA door PrimeScript RT-reagenskit. PCR-reactie werd uitgevoerd door SYBR Permix Ex Taq II (Takara, Dalian, Liaoning, China). PCR-primers werden bedacht en samengesteld door Beijing ComWin Biotech Co., Ltd. (Beijing, China) (Tabel 1). U6 werd geselecteerd als een interne parameter voor miR-133a-3p, PSAT1, GSK3β, β-catenine, Bax, Bcl-2, Ki-67 en CyclinD1 met glyceraldehydefosfaatdehydrogenase (GAPDH) als interne parameter. De gegevens zijn gemeten met 2 −ΔΔCt .
Western Blot-analyse
De totale eiwitten werden geëxtraheerd uit cellen en weefsels en de eiwitmonsters werden gekwantificeerd door Bicinchoninic Acid Protein Assay Kit (Beyotime Institute of Biotechnology, Shanghai, China). De monsters werden gemengd met 1/4 volume 5 x monsterbuffer en 5 minuten gekookt. De 10% scheidingsgel en 5% geconcentreerde gel werden geselecteerd voor elektroforese. Het membraan werd gedurende 60 minuten uitgebroed in 5% magere melkpoeder. Het membraan werd bevestigd met primair antilichaam PSAT1 (1:500), GSK3β (1:500), β-catenine (1:5000), Bax (1:1000), Bcl-2 (1:1000), CyclinD1 (1:):200), Ki-67 (1:5000), MMP-9 (1 μg/mL), VEGF (1:1000) (allemaal van Abcam, Cambridge, MA, VS). Vervolgens werd het membraan 60 minuten met secundair antilichaam (1:2000) uitgebroed. Het membraan werd gedurende 1 minuut ondergedompeld in de elektrochemiluminescentiereactie-oplossing (Beyotime Institute of Biotechnology, Shanghai, China) en vervolgens bedekt met voedselverpakking na het verwijderen van de vloeistof. Het membraan werd belicht met röntgenstraling en het resultaat werd waargenomen na ontwikkeling en fixatie. GAPDH (1:10000, Abcam) werd gebruikt als laadcontrole en het eiwitbeeld werd geanalyseerd door de ImageJ2x-software.
Dual Luciferase Reporter Gene Assay
De doelrelatie tussen miR-133a-3p en PSAT1 en de bindingsplaats tussen miR-133a-3p en PSAT1 3 'niet-vertaalde regio (3'UTR) werden voorspeld door een bio-informatica-website (//cm.jefferson.edu/rna22 /Voorberekend/). De sequentie van het PSAT1 3'UTR-promotergebied dat de miR-133a-3p-bindingsplaats bevat, werd geamplificeerd en gekloneerd in pGL3-basic luciferaseplasmide (Takara Bio Inc., Otsu, Shiga, Japan) om het wildtype (WT) plasmide te construeren ( PSAT1-WT) van PSAT1 3'UTR, terwijl het mutante (MUT) PSAT1-MUT-recombinante plasmide werd geformuleerd door de miR-133a-3p-bindingsplaats op PSAT1-WT te muteren met een puntmutatiekit (Takara Bio Inc., Otsu, Shiga , Japan). De vasculaire EC's in de logaritmische groeifase werden uitgezaaid in een plaat met 96 putjes. Wanneer de samenvloeiing ongeveer 70% bereikt, werden de PSAT1-WT- en PSAT1-MUT-plasmiden gemengd met nabootsende NC- en miR-133a-3p-nabootsende plasmiden door Lipofectamine 2000 en gecotransfecteerd in vasculaire EC's. De cellen werden verzameld en 48 uur na transfectie gelyseerd en luciferase-activiteit werd geverifieerd door een luciferase-detectiekit (Promega Corporation, Madison, WI, VS).
Statistische analyse
Alle gegevens werden verklaard door SPSS 21.0-software (IBM Corp., Armonk, NY, VS). De opsommingsgegevens werden aangegeven door snelheid of percentage, en de analyse werd bepaald door chi-kwadraattest of Fisher's test. De meetgegevens onderworpen aan normale verdeling werden overgebracht door gemiddelde ± standaarddeviatie. Vergelijking tussen twee groepen werd uitgevoerd door t test, terwijl vergelijking tussen meerdere groepen werd geanalyseerd door eenrichtingsanalyse van variantie (ANOVA) gevolgd door Tukey's post hoc-test. EEN P waarde <0,05 werd als significant beschouwd.
Resultaten
Algemene gegevens van patiënten met IA
Zoals weergegeven in Tabel 2, werden de algemene gegevens van de IA-groep en de controlegroep vergeleken. De specifieke informatie staat vermeld in Tabel 2.
Uitdrukking van miR-133a-3p is gerelateerd aan het aantal en de grootte van IA
Door de relatie tussen miR-133a-3p-expressie en de klinisch-pathologische kenmerken van IA te analyseren, werd in Tabel 3 gedetailleerd dat in het licht van de gemiddelde relatieve expressie van miR-133a-3p in IA 75 gevallen van IA werden verdeeld in twee groepen:miR-133a-3p hoge expressiegroep (n =47) en miR-133a-3p lage expressiegroep (n =28). De relatie tussen miR-133a-3p en verschillende klinisch-pathologische parameters werd statistisch geanalyseerd met een chi-kwadraattest of Fisher's test. De resultaten toonden aan dat miR-133a-3p-expressie niet gerelateerd was aan leeftijd, geslacht, vorm en positie van het aneurysma (alle P> 0,05), maar geassocieerd met het aantal en de grootte van het aneurysma (beide P <0,05).
MiR-133a-3p-expressie wordt afgewezen en de PSAT1-, GSK3β- en β-Catenine-expressie wordt verhoogd in IA-weefsels
De expressie van miR-133a-3p in IA werd bepaald met RT-qPCR en de resultaten onthulden dat in relatie tot de normale intracraniële arteriolenweefsels (de controlegroep), miR-133a-3p-expressie was verminderd in de IA-weefsels (de IA-groep) (P <0,05) (Fig. 1a). RT-qPCR en western blot-analyse toonden aan dat PSAT1-, GSK3β- en β-catenine-expressie verhoogd was in de IA-weefsels in vergelijking met die in de normale intracraniële arteriolenweefsels (alle P <0,05) (Fig. 1a–c).
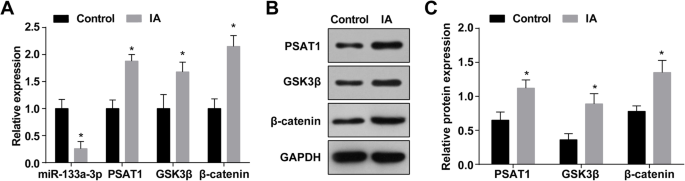
MiR-133a-3p-expressie is verlaagd en de PSAT1-, GSK3β- en β-catenine-expressie is verhoogd in IA-weefsels. een Expressie van miR-133a-3p, PSAT1, GSK3β en β-catenine in de IA-groep en de normale groep. b Eiwitband van PSAT1-, GSK3β- en β-catenine-expressie. c Eiwitexpressie van PSAT1, GSK3β en β-catenine in de IA-groep en de normale groep door western blot-assay. n =75, *P <0,05 vs. de controlegroep. Meetgegevens werden weergegeven als gemiddelde ± standaarddeviatie en vergelijkingen tussen twee groepen werden uitgevoerd door een onafhankelijke steekproef t testen
Pathologische veranderingen van aneurysma en MMP-9 en VEGF-expressie in IA-weefsels
Door direct het normale intracraniale arteriolenweefsel en de IA-weefsels te observeren, werd gepresenteerd dat in de controlegroep de bloedvaten in de arteriële weefsels helderrood waren en dat er geen duidelijke atherosclerotische plaques en laterale trombus werden gevonden in het lumen. De tumor van de aneurysmaweefsels van de IA-groep was meestal bruin of donkerrood, en het uiterlijk was scrotiform of fusiformis, en de textuur was meestal taai. Toen de tumor werd opengesneden, verschenen er witte of donkerrode atherosclerotische plaques op de tumorwand van sommige tumormonsters, die plat, rond of ovaal van vorm waren. In sommige tumormonsters was er een murale trombus in de tumorholte en de textuur van de trombus was zacht. De dikte van de tumorwand werd geleidelijk dunner vanaf de hals van de tumor, waarvan sommige slechts een dun vezelmembraan aan de bovenkant van de tumor hadden, en sommige waren zelfs gescheurd. De spleet van het gescheurde aneurysma bevond zich op of nabij de bovenkant van de tumor.
HE-kleuring toonde aan dat onder de lichtmicroscoop de dikte van de wand van de normale intracraniale arteriolenweefsels uniform was; de anatomische structuur van de binnenste, middelste en buitenste lagen was duidelijk en intact; de morfologie van de cellen in elke laag was normaal; het sarcolemma van de aangrenzende cellen vaak dicht gevormd; en de ontstekingscellen van de wand waren zeldzaam. In de IA-groep werden de lokale uitsteeksels gevormd in de distale laterale vasculaire holte aan de bovenkant van de bifurcatie van de intracraniale slagader in de aneurysmawand stomp en kleiner, en de lokale EC's gingen verloren. Een klein aantal monsters vertoonde een migratie van de gladde spiercellaag naar de intimalaag en myogene proliferatie van intimacellen. EC's daalden of verdwenen zelfs. De endotheelcellaag bestond uit hyperplastische myo-intimale cellen en lineair gerangschikte EC's, of door apoptotische EC's en bloedcellen die aan het lumen waren bevestigd. De vacuole degenereerde en vertoonde een continuïteitsonderbreking. Sommige werden samen met het basaalmembraan afgepeld en de intima-collageenvezels werden vergroot. De atherosclerose was veranderd en de arteriolenwand was duidelijk dunner en gevuld met een groot aantal bindweefsels. Infiltratie van ontstekingscellen en gedeeltelijke diffusie werden waargenomen in alle lagen, voornamelijk in de middelste en buitenste membranen. In sommige cellen werden afzettingen van lipiden en cholesterolkristallen waargenomen. Sommige tumorwanden waren volledig of lokaal uitgedund en naar buiten toe uitgezet (Fig. 2a, b).
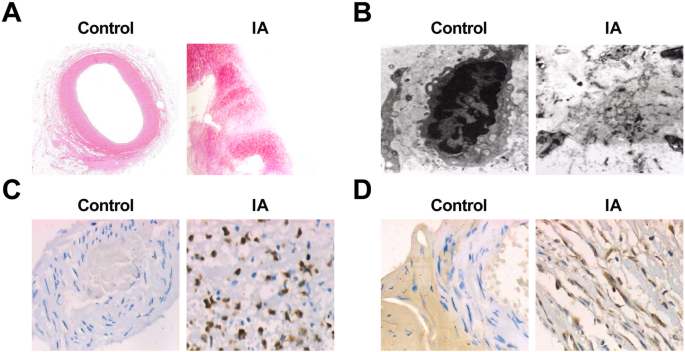
Pathologische veranderingen van aneurysma en de expressie van MMP-9 en VEGF in IA. een Normale intracraniële arteriolen weefselcoupes in de controlegroep onder HE-kleuring (× -10). b IA weefselcoupes geverfd met HE (× -10). c Ultrastructure of normal intracranial arterioles tissues in the control group under an electron microscope (× 10,000). d Ultrastructure of IA tissues under an electron microscope (× 10,000). e Expression of MMP-9 in the control group and the IA group by immunohistochemical staining (× 200). v Expression of VEGF in the control group and the IA group by immunohistochemical staining (× 200)
The sections of the normal intracranial arterioles tissues and IA tissues were observed by an electron microscope, and it performed that in normal intracranial arterioles tissues, the matrix fibers of the cerebral vascular wall could be seen clearly, and there was no endothelial injury, cell pyknosis, or degeneration. In the IA tissues, obvious endothelial cell injury, cell pyknosis, or vacuole degeneration were observed, the number of middle smooth muscle cells was declined, most of the nucleus pyknosis was appeared, and chromatin aggregation and apoptotic bodies could be seen. Some cells showed swelling of the mitochondria and disappearance of normal internal structure. The extracellular matrix that formed the cytoskeleton was blurred and showed amorphous floc. There were many fragments in the missing parts of the cells (Fig. 2c, d).
Immunohistochemical staining was utilized to test MMP-9 and VEGF expression, and the results revealed that there was no expression of MMP-9 and VEGF in 75 cases of the control group. It existed 60 cases of positive expression of MMP-9 in the 75 cases of IA samples. MMP-9 positive expression appeared in the inner and the outer membranes of IA wall, but the expression was not uniform. The positive expression was mainly characterized by a brownish yellow cytoplasm. The positive expression of VEGF was 66 cases in 75 cases of IA samples. In the wall of IA, there was a high positive expression in the middle and the outer membranes and a low positive expression in the intima. The positive expression was also mainly characterized by a brownish yellow cytoplasm (Fig. 2e, f). The expression of MMP-9 and VEGF in the two groups is shown in Table 4.
Identification of Vascular ECs
The expression of factor VIII and CD31 in ECs were analyzed by immunohistochemical staining. The results reported that vascular ECs reacted positively to factor VIII and CD31-related antigen antibodies, and the positive rate was 95%. In addition, there were a large number of brown particles in the cytoplasm, and the fifth passage of cells of brown staining was dramatically higher than the primary passage of cells (Fig. 3a, b).
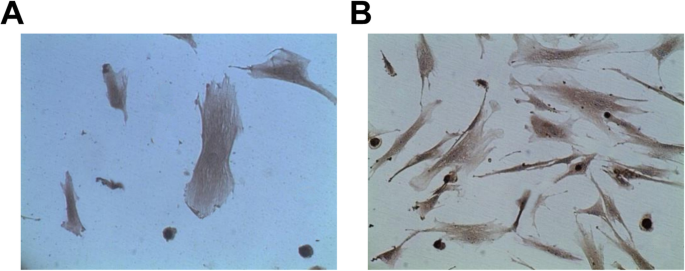
Vascular ECs react positively to FVIII and CD31 related antigen antibodies. een Identification of ECs by CD31. b Identification of ECs by FVII
Upregulation of miR-133a-3p and Downregulation of PSAT1 Suppress Apoptosis and Advance Proliferation and Migration of ECs in IA
Flow cytometry, RT-qPCR, and western blot analysis were adopted for observing the apoptosis and Bax and Bcl-2 expression in ECs of IA after treated with miR-133a-3p mimic or si-PSAT1. It was indicated that compared to the control group, the apoptosis rate of cells and Bax expression was elevated in the IA group and the Bcl-2 expression was decreased (all P <0,05). The cell apoptosis and Bax and Bcl-2 expression in the IA group, mimic NC group, and si-NC group had no significant change (all P> 0.05). By comparison with the si-NC group and mimic NC group, the apoptosis rate of cells in the si-PSAT1 group and miR-133a-3p mimic group was suppressed, the Bax expression was declined, and the Bcl-2 expression was raised (all P <0,05). Versus the miR-133a-3p mimic group, the apoptosis rate and Bax expression were enhanced, and the Bcl-2 expression was reduced in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 4a–e).
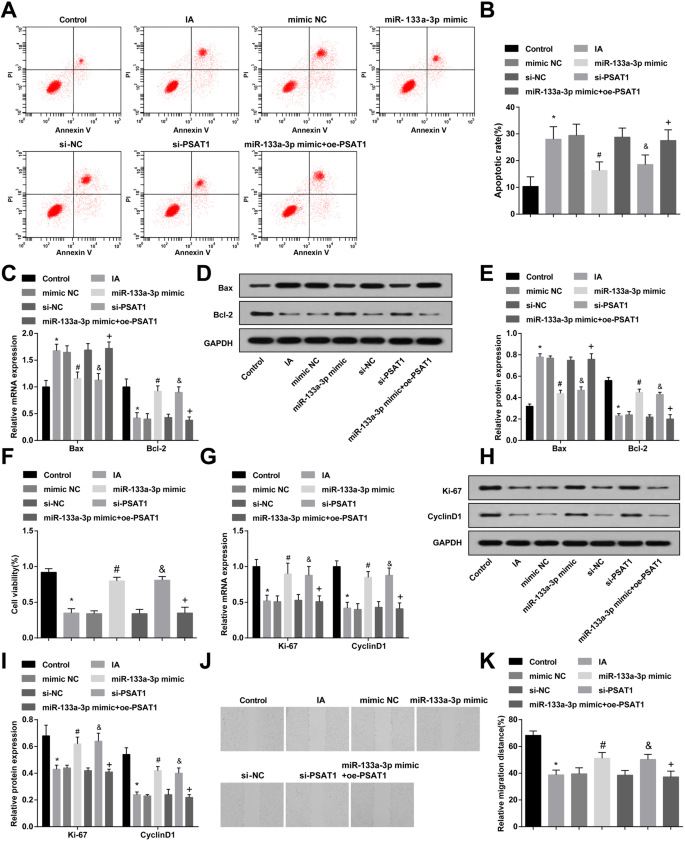
Highly expressed miR-133a-3p and lowly expressed PSAT1 inhibit apoptosis and promote proliferation and migration of IA ECs. een Detection of apoptosis of ECs by flow cytometry. b Detection of apoptosis rate of ECs in each group. c Bax and Bcl-2 expression in ECs detected by RT-qPCR. d Protein band of Bax and Bcl-2 expression. e Bax and Bcl-2 protein expression in ECs detected by western blot analysis. v MTT assay was used to detect proliferation activity of ECs in each group. g RT-qPCR was used to detect the expression of Ki-67 and CyclinD1 in each group of ECs. u Protein band of Ki-67 and CyclinD1 expression. ik Ki-67 and CyclinD1 protein expression in ECs detected by western blot analysis. j Detection of the migration of ECs in each group by scratch test. k Statistical results of endothelial cell migration in each group. N =3, *P <0.05 vs. the control group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation; data were assessed by one-way analysis of variance followed by Tukey’s post hoc test
MTT assay, RT-qPCR, and western blot analysis were utilized to observe the proliferation and the expression of Ki-67 and CyclinD1 in ECs of IA after treated with miR-133a-3p mimic or si-PSAT1. It was displayed that in contrast to the control group, the proliferation activity and Ki-67 and CyclinD1 expression were reduced in the IA group (all P <0,05). There was no significant difference in the proliferation activity and Ki-67 and CyclinD1 expression of the IA group, mimic NC group, and si-NC group (all P> 0.05). In relation to the si-NC group and the mimic NC group, the proliferation activity and Ki-67 and CyclinD1 expression were heightened in the si-PSAT1 group and the miR-133a-3p mimic group (all P <0,05). In comparison to the miR-133a-3p mimic group, the proliferation activity and Ki-67 and CyclinD1 expression were reduced in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 4f, i).
The migration of ECs in each group after treatment with miR-133a-3p mimic or si-PSAT1 for 24 h was observed by scratch test. It was revealed that the migration of cells in the IA group was inhibited relative to that in the control group (P <0,05). There was no markedly change in cell migration of the IA group, the si-NC group, and the mimic NC group (all P> 0.05). Compared to the si-NC group and the mimic NC group, the cell migration in the si-PSAT1 group and the miR-133a-3p mimic group was elevated (both P <0,05). Versus the miR-133a-3p mimic group, the cell migration was declined in the miR-133a-3p mimic + oe-PSAT1 group (P <0.05) (Fig. 4j, k).
Restored miR-133a-3p and Depleted PSAT1 Reduce PSAT1, GSK3β, and β-Catenin Expression in ECs of IA
RT-qPCR was used to detect miR-133a-3p expression in ECs of IA; it was yielded that compared to the control group, miR-133a-3p expression in the IA group was reduced (P <0,05). miR-133a-3p expression in the IA group, mimic NC group, and si-NC group did not change markedly (P> 0.05). MiR-133a-3p expression in the miR-133a-3p mimic group was enhanced relative to that in the mimic NC group (P <0,05). In contrast with the si-NC group, there was no distinct change in miR-133a-3p expression in the si-PSAT1 group (P> 0.05). Versus the miR-133a-3p mimic group, miR-133a-3p expression was showed no significant difference in the miR-133a-3p mimic + oe-PSAT1 group (P> 0.05) (Fig. 5a).
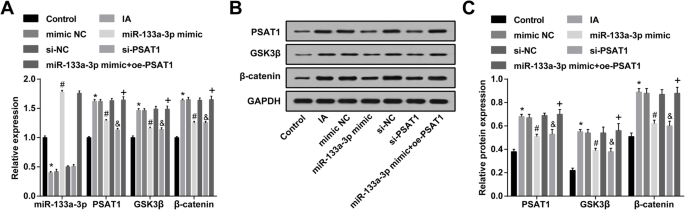
Upregulation of miR-133a-3p and downregulation of PSAT1 decrease PSAT1, GSK3β, and β-catenin expression in ECs of IA. een miR-133a-3p, PSAT1, GSK3β, and β-catenin expression in ECs detected by RT-qPCR. b Protein bands of PSAT1, GSK3β, and β-catenin. c PSAT1, GSK3β, and β-catenin protein expression in ECs in each group detected by western blot analysis. N =3, *P <0.05 vs. the control group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation, and data were assessed by one-way analysis of variance followed by Tukey’s post hoc test
The expression of PSAT1, GSK3β, and β-catenin in ECs of IA was tested by western blot analysis and RT-qPCR. It was indicated that in relation to the control group, PSAT1, GSK3β, and β-catenin expression in the IA group was raised (all P <0,05). PSAT1, GSK3β, and β-catenin expression in the IA group, mimic NC group, and si-NC group did not change dramatically (all P> 0.05). PSAT1, GSK3β, and β-catenin expression in the miR-133a-3p mimic group and si-PSAT1 group was degraded relative to that in the mimic NC group and si-NC group (all P <0,05). In relation to the miR-133a-3p mimics group, PSAT1, GSK3β, and β-catenin expression was elevated in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 5a–c).
Upregulating miR-133a-3p and Downregulating PSAT1 Alleviate the Pathological Changes of IA Tissues
By testing the hemodynamic changes of rats after modeling, we monitored the blood flow velocity of rats in each group 3 days before operation and 12 weeks after intervention treatment. It was performed that there was no obvious difference in blood flow velocity in each group 3 days before operation (P> 0.05). After 12 weeks of intervention, the blood flow velocity of rats in the IA group depressed relative to that in the normal group (P <0,05). There was no distinct difference in the degree of decrease of blood flow velocity in the IA group, mimic NC group, si-NC group, and miR-133a-3p mimic + oe-PSAT1 group (all P> 0.05). By comparison with the si-NC group and the mimic NC group, the blood flow velocity was heightened in the miR-133a-3p mimic group and the si-PSAT1 group (both P <0,05). In contrast to the miR-133a-3p mimic group, the blood flow velocity was declined in the miR-133a-3p mimic + oe-PSAT1 group (P <0.05) (Fig. 6a).
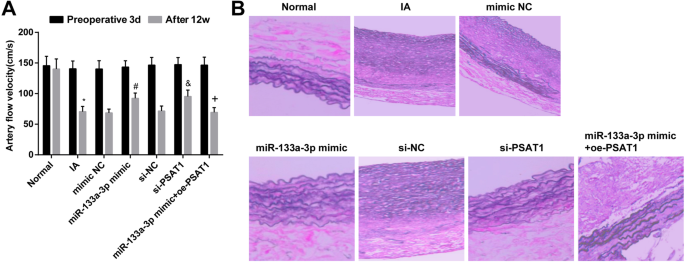
Upregulated miR-133a-3p and downregulated PSAT1 alleviate the pathological changes of IA tissues. een Hemodynamic changes at each time point after successful modeling in rats. b Changes of IA tissue after transfection. n =12, *P <0.05 vs. the normal group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation, and data were assessed by one-way analysis of variance followed by Tukey’s post hoc test.
The changes of IA tissues were verified by HE staining. The results displayed that in the normal group, the elastic fibers in the middle layer of intracranial vascular tissue were neat, the normal elastic protein wave-like structure was appeared, and there was no broken and degradation. In relation to the normal group, the lumen of intracranial vascular tissue was enlarged, the normal elastic protein wave-like structure was disappeared, the elastic fiber in the middle layer of local elastic protein vessel was broken, and some of the elastic fibers were completely degraded in the IA group. There was no distinct change in the morphology of IA tissues in the si-NC group, mimic NC group, IA group, and miR-133a-3p mimic + oe-PSAT1 group. In contrast with the si-NC group and the mimic NC group, the wave structure of elastic protein in intracranial vascular tissue of rats in the miR-133a-3p mimic group and the si-PSAT1 group was existed, and the local elastic protein vascular structure was slightly disordered, but there was no fracture and dissolution (Fig. 6b).
Highly Expressed miR-133a-3p and Lowly Expressed PSAT1 Reduce PSAT1, GSK3β, β-Catenin, VEGF, and MMP-9 Expression in IA Tissues in Vivo
The expression of miR-133a-3p in IA tissues in vivo was tested by RT-qPCR, it was suggested that in relation to the normal group, miR-133a-3p expression was declined in the IA group (P <0,05). miR-133a-3p expression in the IA group, mimic NC group, and si-NC group did not change obviously (all P> 0.05). MiR-133a-3p expression in the miR-133a-3p mimic group was elevated relative to that in the mimic NC group (P <0,05). By comparison with the si-NC group, there was no marked change in miR-133a-3p expression in the si-PSAT1 group (P> 0.05). Versus the miR-133a-3p mimic group, miR-133a-3p expression showed no significant difference in the miR-133a-3p mimic + oe-PSAT1 group (P> 0.05) (Fig. 7a).
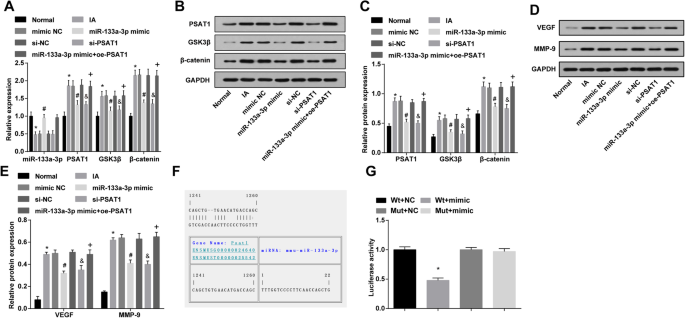
Overexpression of miR-133a-3p and low expression of PSAT1 decrease PSAT1, GSK3β, and β-catenin, VEGF and MMP-9 expression in IA tissues in vivo and PSAT1 is a target gene of miR-133a-3p. een Detection of miR-133a-3p, PSAT1, GSK3β, and β-catenin expression in IA tissues of rats in each group by RT-qPCR. b Protein bands of PSAT1, GSK3β, and β-catenin. c Detection of PSAT1, GSK3β, and β-catenin protein expression in IA tissues of rats in each group by western blot analysis. d Protein bands of VEGF and MMP-9. e Detection of VEGF and MMP-9 protein expression in IA tissues of rats in each group by western blot analysis. v Prediction of the target site of PSAT1 binding to the corresponding miR-133a-3p by Target Scan. g Result of dual luciferase reporter gene assay. een –e , n =12; v –g , N =3, *P <0.05 vs. the normal group/the Wt + NC group. #P <0.05 vs. the mimic NC group. &P <0.05 vs. the si-NC group. +P <0.05 vs. the miR-133a-3p mimic group. Measurement data were depicted as mean ± standard deviation, and data were assessed by one-way analysis of variance followed by Tukey’s post hoc test
The expression of PSAT1, GSK3β, and β-catenin in IA tissues in vivo was tested by western blot analysis and RT-qPCR. It was appeared that in contrast with the normal group, PSAT1, GSK3β, and β-catenin expression in the IA group was increased (all P <0,05). PSAT1, GSK3β, and β-catenin expression in the IA group, mimic NC group, and si-NC group did not change markedly (all P> 0.05). PSAT1, GSK3β, and β-catenin expression in the miR-133a-3p mimic group and si-PSAT1 group was decreased compared with that in the mimic NC group and si-NC group (all P <0,05). Versus the miR-133a-3p mimic group, PSAT1, GSK3β, and β-catenin expression was enhanced in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 7a–c).
Western blot analysis was used to verify the VEGF and MMP-9 expression in IA tissues in vivo; the results perceived that by comparison with the normal group, VEGF and MMP-9 expression in the IA group were enhanced (both P <0,05). VEGF and MMP-9 expression in the IA group, mimic NC group, and si-NC group did not change obviously (all P> 0.05). In relation to the mimic NC group and si-NC group, VEGF and MMP-9 expression in the miR-133a-3p mimic group and si-PSAT1 group were declined (all P <0,05). Versus the miR-133a-3p mimic group, VEGF and MMP-9 expression were elevated in the miR-133a-3p mimic + oe-PSAT1 group (all P <0.05) (Fig. 7d, e).
PSAT1 Is a Target Gene of miR-133a-3p
The online prediction software (https://cm.jefferson.edu/rna22/Precomputed/) was utilized to forecast and analyze the target site of PSAT1 binding to the miR-133a-3p, and the sequence of 3′UTR region combined by PSAT1 and miR-133a-3p. In order to prove that the predicted binding site of miR-133a-3p resulted in a change in the luciferase activity, the mutation sequence and the wild sequence of PSAT1 3′UTR deleting miR-133a-3p binding site were devised. Luciferase activity was verified by co-transfection of miR-133a-3p mimic and WT (Wt-miR-133a-3p/PSAT1) or MUT (Mut-miR-133a-3p/PSAT1) recombinant plasmids in vascular ECs. The results revealed that miR-133a-3p mimic had no distinct effect on luciferase activity in the Mut-miR-133a-3p/PSAT1 group (P> 0.05), while the luciferase activity in the Wt-miR-133a-3p/PSAT1 group was markedly declined (P <0.05) (Fig. 7f, g).
Discussion
IA is an abnormal dilatation of the intracranial artery, which weakens the arterial wall through continuously pushing outwards the vascular wall, which results in a higher risk of aneurysm rupture [17]. In a study conducted by Liu et al., it has shown that some miRNAs are involved in modulating the cell proliferation of vascular smooth muscle cells, which is closely associated with IA [18]. Also, a recent study has provided a proof that circulating miRNAs can be used as a new biomarker to assess the possibility of IA occurred in high-risk individuals [19]. It is customarily considered that PSAT1 may be involved in schizophrenia spectrum conditions and alters serine metabolism [20]. The current study was designed to explore the regulatory role of miR-133a-3p modulated vascular endothelial injury and triggered IA through modulating the PSAT1/GSK3β/β-catenin signaling pathway.
In this present study, the relationship among miR-133a-3p expression and clinicopathological features of IA was analyzed, and the results demonstrated that the expression of miR-133a-3p was not related to age, gender, shape, and position of aneurysm but associated with the number and size of aneurysm. Some scholars considered that the shear stress of regional blood flow in the arterial wall induced the induction of monocyte chemoattractant protein-1 (MCP-1) and macrophage inflammatory protein 1α (MIP-1α) expression by fibroblasts and vascular ECs within the vascular wall. The highly reactive chemotactic factors MCP-1 and MIP-1α made an aggregation of macrophagocyte in the vascular wall and mediated inflammatory response, then, induced the excitation of nuclear transcription factor c-Jun and then regulated the activation of activated protein 1 (AP-1), then activated MMP-9 promoter in its structural domain to raise MMP-9 mRNA expression, and finally induced the dissolution of extracellular matrix of vascular wall, causing the formation of intracranial aneurysm [21,22,23]. Saito et al. [24] found that MMP-9 positive cells were mainly from the middle and the outer membranes of the artery macrophages, which certified that MMP-9 expressed by macrophages mediated the degeneration of the arterial wall, leading to the formation of arterial aneurysm. The above studies have indicated that MMP-9 was linked to the formation of IA. The results of our study revealed that MMP-9 was upregulated in IA; thus, we speculated that mR-133a-3p might be involved in the occurrence and development of IA by regulating the PSAT1/GSK3β/β-catenin pathway and further regulating MMP-9. In our study, we found that restoring miR-133a-3p reduced the expression of PSAT1, GSK3β, β-catenin, and MMP-9 in intracranial aneurysm tissues. We will carry out relevant research in the future study to verify our findings.
Our study has provided substantial evidence in relation to the notion that miR-133a-3p expression was decreased and the PSAT1, GSK3β, and β-catenin was elevated in IA. Emerging evidence has suggested that miR-133a-3p plays a suppressive role in different kinds of tumors. Recent study has presented that miR-133a-3p expression was dramatically degraded in breast cancer tissues in contrast with that in non-cancer tissues [25]. Another study has purported that miR-133a-3p expression is declined in advanced prostate cancer (PCa) tissues relative to that in the adjacent normal tissues or benign prostate lesion tissues, especially in bone metastatic PCa tissues [26]. The promoting effect of PSAT1 in other types of diseases are found in some literatures. It is reported that PSAT1 expression was remarkably heightened in non-small cell lung cancer (NSCLC) and forecasted poor clinical outcome of NSCLC patients [27]. Furthermore, PSAT1 is considered as the highest upregulated gene in CRC tumors as well as highly expressed in chemoresistant disease patients [28]. It has been manifested that GSK3β activity was elevated in cancerous tissues [29]. Moreover, the phosphorylation level of GSK3β as well as the expression of nuclear β-catenin are also enhanced, suggesting that GSK3β/β-catenin pathway may be participated in osteopontin regulation [30].
Other results emerged from our data suggested that upregulation of miR-133a-3p and downregulation of PSAT1 suppressed apoptosis and advanced proliferation and migration of IA ECs, reduced VEGF, and MMP-9 expression in IA tissues. It has been suggested previously that the over-expression of miR-133a-3p retrains the invasion, growth, and mitosis of oral squamous cell carcinoma cells by targeting collagen type I alpha 1 (COL1A1) [31]. It is reported that highly expressed miR-133a-3p can repress the propagation of ESCC cells, advance cell apoptosis, and decline the migration and invasion of ESCC cells by targeting COL1A1 [32]. Another study has verified that transient upregulation of miR-133a-3p suppresses the migration, invasion, and growth abilities of gallbladder carcinoma cells through directly targeting recombination signal-binding protein Jκ [33]. In like manner, this study suggests that miR-133a-3p exerts its role in IA through targeting PSAT1. It is displayed that PSAT1 overexpression boosts ESCC cell growth and matrigel invasion in vitro, and injection of mice with ESCC cells with high expression of PSAT1 induces tumor formation in vivo [14]. Other study also has reported that PSAT1 is highly expressed and forecasts a poor clinical outcome of patients, as well as enhances cell tumorigenesis and proliferation in vivo and in vitro [13]. Prior research generally confirms that PSAT1 advances cell cycle progression, proliferation, and tumorigenesis through loss- and gain-of-function experiments [27]. It has been indicated that MMPs are composed of a series of enzymes which cleaves protein substrates on the basis of a conserved mechanism referring activation of an active site-bound water molecule through a Zn 2+ ion [34]. MMP-9 is a distinct protease which push forward an immense influence on many biological processes [35]. A study has contended that MMP-9 is elevated in the aneurysm groups compared to the control group [36]. Vascular endothelial growth factor-A (VEGF-A) is recognized as the key modulator of endovascular differentiation of trophoblast [37]. A study has revealed that silenced PSAT1 expression suppresses VEGF, β-catenin, and GSK3β phosphorylation expression [10].
Conclusion
To briefly conclude, our study confirms our hypothesis that overexpression of miR-133a-3p or downregulation of PSAT1 restrain endothelial cell damage and advance endothelial cell proliferation via inhibiting the GSK3β/β-catenin pathway in IA. These findings provide a new insight in a novel target therapy for IA. These findings underscore the role of miR-133a-3p in IA in relation the PSAT1/GSK3β/β-catenin pathway. However, a conclusion about the effects of miR-133a-3p and PSAT1 cannot be made clearly due to limited known researches on this. It needs to be monitored rigorously and reported appropriately in the future clinical trials.
Beschikbaarheid van gegevens en materialen
Not applicable
Afkortingen
- miR-133a-3p:
-
MicroRNA-133a-3p
- IA:
-
Intracranial aneurysm
- PSAT1:
-
Phosphoserine aminotransferase 1
- GSK3:
-
β-glycogen synthase kinase 3β
- SAH:
-
Subarachnoid hemorrhage
- MiRNAs:
-
MicroRNAs
- CRC:
-
Colorectal cancer
- ESCC:
-
Esophageal squamous cell carcinoma
- HE:
-
Hematoxylin-eosin
- PBS:
-
Fosfaatbuffer zoutoplossing
- MMP:
-
Matrix metalloprotease
- VEGF:
-
Vascular endothelial growth factor
- NC:
-
Negative control
- DAB:
-
Diaminobenzidine
- FBS:
-
Foetaal runderserum
- UEAI:
-
Ulex europaeus agglutinins I
- PI:
-
Propidium iodide
- FITC:
-
V-fluorescein isothiocyanate
- DMSO:
-
Dimethylsulfoxide
- OD:
-
Optische dichtheid
- SD:
-
Sprague-Dawley
- SPF:
-
Specific pathogen-free
- GAPDH:
-
Glyceraldehyde phosphate dehydrogenase
- BCA:
-
Bicinchoninic acid
- 3′UTR:
-
3′ Untranslated region
- WT:
-
Wild type
- MUT:
-
Mutant
- ANOVA:
-
Analysis of variance
- NSCLC:
-
Non-small cell lung cancer
- VEGF-A:
-
Vascular endothelial growth factor-A
Nanomaterialen
- De Common-emitter versterker
- Voorbereiding van met ICA geladen mPEG-ICA nanodeeltjes en hun toepassing bij de behandeling van door LPS geïnduceerde H9c2-celbeschadiging
- Nanodeeltjesafgifte van artesunaat verbetert de antitumorefficiëntie door mitochondria-gemedieerde celapoptose te activeren
- Groei beheersen Hoge uniformiteit Indiumselenide (In2Se3) nanodraden via het snelle thermische gloeiproces bij lage temperatuur
- Gemakkelijke synthese van wormgatachtig mesoporeus tinoxide via verdamping-geïnduceerde zelfassemblage en de verbeterde gasdetectie-eigenschappen
- Ontwerp en aanpassing van de grafeen-werkfunctie via grootte, modificatie, defecten en doping:een eerste-principe theorie-onderzoek
- Een onderzoek naar een kristallijn-silicium zonnecel met zwarte siliciumlaag aan de achterkant
- De Slide-Roll Motion-modus van koolstofnanobuisjes afstemmen via hydroxylgroepen
- Effectieve lichtabsorptie met behulp van de dubbelzijdige piramideroosters voor dunne-film silicium zonnecel
- Het apoptose-effect op leverkankercellen van gouden nanodeeltjes gemodificeerd met lithocholzuur
- Kleine zeldzame-aarde-fluoride-nanodeeltjes activeren tumorcelgroei via elektrische polaire interacties



