Een eenvoudige aanpak voor het synthetiseren van fluorescerende koolstofkwantumstippen uit tofu-afvalwater
Abstract
We presenteren een onderzoek naar koolstofkwantumdots (CQD's) die zijn gesynthetiseerd uit afvalwater dat wordt geïnduceerd tijdens de productie van tofu. We vinden dat afvalwater van tofu een goede grondstof is voor het maken van fluorescerende CQD's. De overeenkomstige CQD's kunnen eenvoudig worden vervaardigd via een hydrothermische reactie om de organische stof in de gele serofluide van tofu-afvalwater te carboniseren. Er kunnen twee soorten CQD's worden verkregen in respectievelijk gedeïoniseerd water en NaOH-oplossing, waarbij de CQD's in water (NaOH-oplossing) blauw (groen) licht kunnen uitstralen onder de UV-straling. Uit röntgenfoto-elektronspectroscopie (XPS) blijkt dat het fundamentele verschil tussen deze twee soorten CQD's de inhoud van C–O- en C=O-bindingen op het oppervlak van de CQD's is. Dit verschil kan verschillende kenmerken van de fotoluminescentie (PL) spectra van de CQD's veroorzaken. Op basis van de verkregen resultaten van de XPS- en PL-metingen stellen we een mechanisme voor om de door fotonen geïnduceerde lichtemissie van CQD's te begrijpen en te verklaren. Deze studie is relevant voor de fabricage en toepassing van fluorescerende CQD's als bijvoorbeeld lichtweergavematerialen.
Achtergrond
Tofu, gemaakt van sojabonen, is het dagelijkse voedsel in China en in de Aziatische gemeenschap. Vroeger werden tofu en aanverwante producten vooral in relatief kleine hoeveelheden gemaakt door families en kleine fabriekjes. Nu de vegetariër wereldwijd steeds populairder wordt, is de vraag naar tofu-producten de afgelopen twee decennia snel toegenomen sinds de grote internationale supermarkten zoals WalMart en Carrefour deze als gezondheidsvoedsel verkochten. Tofu en aanverwante producten worden tegenwoordig vooral in massa geproduceerd door grote fabrieken op het industrieterrein in China. Een van de milieuproblemen van de massaproductie van tofu in het industriepark is echter het afvalwater. De productie van sojaproducten zou resulteren in afvalwater vermengd met sojagele serofluid. Dit afvalwater kan milieuvervuiling veroorzaken. Aan de andere kant is tofu gele serofluid sterk geconcentreerd met organische stoffen en bevat koolhydraten, eiwitten, organische zuren, functionele oligosachariden, in water oplosbare niet-eiwit stikstof en vitamines, lipiden en andere pigmentstoffen. Daarom is het een goede bron van grondstoffen voor het vervaardigen van koolstofkwantumdots (CQD's) voor optica, biogeneeskunde en andere toepassingen. Door tofu-afvalwater toe te passen om CQD's te maken, kan het afval van de massaproductie van tofu dus worden hergebruikt en de milieuvervuiling grotendeels worden verminderd. Deze worden de belangrijkste motivatie van onze huidige studie.
Koolstofkwantumdots is een nieuwe klasse van op koolstof gebaseerd nanomateriaal dat normaal gesproken een ruimtelijke grootte heeft van 20 nm of minder [1, 2]. Er is gevonden dat de CQD's goed oplosbaar zijn in water, hoge chemische inertie, lage toxiciteit en uitstekende biocompatibiliteit [3, 4]. Vanuit een natuurkundig oogpunt is het elektronische energiespectrum voor een CQD verwant aan een halfgeleider met directe bandgap. Zo zijn de CQD's voorgesteld als fluorescerende materialen voor geavanceerde optische en opto-elektronische apparaten [5, 6]. In de afgelopen jaren zijn de CQD's vrij intensief onderzocht. Een verscheidenheid aan fabricagemethoden en verschillende bronnen van grondstoffen zijn toegepast om de CQD's voor optische toepassingen te realiseren [5,6,7]. Over het algemeen kan de synthese van CQD's worden bereikt door top-down en bottom-up benaderingen [8]. De top-down-methode is voornamelijk een fysieke benadering bij het vormen van koolstofstippen door grotere koolstofmateriaalstructuren te breken of af te pellen, waaronder boogontlading [9], elektrochemische oxidatie [10], chemische oxidatie [11], laserablatie [12], enz. De bottom-up methode is om de kleine moleculen te gebruiken als voorlopers om CQD's te verkrijgen door middel van chemische reacties, waaronder verbranding [13], microgolf [14] en ultrasone [15] benaderingen samen met chemische oplossingssynthese [16], hydrothermische reactie [17] ], enz.
In de afgelopen jaren is biomassa zoals tarwestro [18] en plantenbladeren [19] op grote schaal gebruikt als koolstofbronnen voor de synthese van de CQD's. Bovendien zijn in water oplosbare fluorescerende CQD's bereid door hydrothermische behandelingen van sinaasappelsap [20] en Jinhua bergamot [21] die als koolstofbronnen worden gebruikt. Een dergelijke eenvoudige benadering is toegepast voor de grootschalige synthese van in water oplosbare CQD's uit vele soorten van voedselafval afgeleide bronnen [22].
In deze studie nemen we tofu gele serofluid als koolstofbron om de CQD's te synthetiseren via de hydrothermale methode om de organische stoffen in de gele serofluide te carboniseren. Er is op gewezen [17] dat de hydrothermische methode een gemakkelijke en goedkope benadering is die kan worden toegepast op grootschalige en eenstapssynthese van in water oplosbare fluorescerende CQD's. Voor optische toepassing van de CQD's, in het bijzonder als lichtweergavematerialen, is het wenselijk om de fluorescerende CQD's te kunnen produceren die blauwe, groene en rode straling kunnen uitzenden. Ons huidige onderzoekswerk wordt in deze richting uitgevoerd. In de huidige studie bereiden we een reeks fluorescerende CQD's voor op onderzoek. De transmissie-elektronenmicroscopie en de röntgenfoto-elektronenspectroscopie worden toegepast voor de karakterisering van de gefabriceerde CQD's. Het fotoluminescentie-experiment wordt gebruikt om de optische eigenschappen van de CQD's te meten.
Methoden
In deze studie wordt het afvalwater van de tofu-productie gehaald uit het Tofu Industrial Park in Shi Ping County, Yunnan, China. De algemene processen om de CQD's uit gele serofluïde in tofu-afvalwater te synthetiseren, kunnen als volgt worden beschreven:(i) We bereiden de koolstofprecursoren voor via pyrolyse van de tofu-gele pulp in afvalwater. Hier wordt 300 ml tofu-gele siroop in de beker van 500 ml gedaan en op het verwarmingsplatform geplaatst voor constante verwarming. We vinden dat wanneer de verwarmingstemperatuur ongeveer 93 ° C is en de verwarmingstijd 3 tot 5 uur is, de tofu-gele serovloeistof in het bekerglas droog kan worden. (ii) We laten het spul in de beker op natuurlijke wijze afkoelen tot kamertemperatuur en voegen 50-200 ml gedeïoniseerd water toe aan de beker. (iii) Het mengsel wordt gedurende 4 minuten magnetisch geroerd om de uniforme en volledige mix van de stoffen en het water te verkrijgen. (iv) Het mengsel wordt gedurende 5 minuten ultrasone schok genomen om de verliezende clusters te breken. We kunnen dus het supernatant verkrijgen dat koolstofstippen bevat. (v) Het supernatant wordt verder gecentrifugeerd met een snelheid van 12.000 omw/min gedurende 20 min, en het verdere supernatant kan worden verkregen. Als gevolg hiervan kunnen de CQD's uiteindelijk worden verkregen in gedeïoniseerd water. Het is gebleken dat de verwarmingstemperatuur, de verwarmingstijd en de pH-waarde van het gele pulpwater in het syntheseproces de groei van de CQD's vrij sterk kunnen beïnvloeden. Daarom kunnen de CQD's worden vervaardigd met bepaalde fluorescerende kenmerken door de bovenstaande syntheseomstandigheden te variëren. We merken op basis van observatie met het blote oog bij daglicht dat het supernatant met CQD's bereid onder bovengenoemde experimentele omstandigheden er geel uitziet. Het kan er echter blauw uitzien onder de UV-straling. We noemen dit soort fluorescerende CQD's in dit artikel als CQD's-1.
Door de vergelijkbare synthesebenadering te volgen, kunnen we de CQD's produceren door NaOH te gebruiken als oplossing voor het verbranden van droge tofu-gele serofluid na pyrolyse, in plaats van het gebruik van gedeïoniseerd water dat hierboven is besproken. We voegen 100 ml NaOH-oplossing toe met een pH-waarde van ongeveer 12,4. Door dezelfde processen van magnetisch roeren, ultrasoon schokken en centrifugeren te volgen zoals hierboven vermeld, kunnen we ook de CQD's in de NaOH-oplossing verkrijgen. Deze CQD's zien er ook geel uit bij observatie met het blote oog bij daglicht. Ze kunnen er echter groen uitzien onder de UV-straling. We noemen dit soort fluorescerende CQD's in dit artikel als CQD's-2.
In dit werk hebben we twee soorten CQD's gemaakt die groen en blauw licht kunnen uitzenden onder de UV-straling. Het verdere onderzoek van het huidige werk wordt voornamelijk uitgevoerd voor deze twee soorten CQD's die zijn gerealiseerd uit tofu-afvalwater.
Resultaten en discussies
Voor karakterisering van de CQD's die zijn gesynthetiseerd uit tofu-afvalwater, voeren we eerst de morfologische analyse voor deze CQD's uit. In Fig. 1 tonen we het typische beeld van de CQD's in gedeïoniseerd water en NaOH-oplossing (CQDs-1 en CQDs-2), verkregen met transmissie-elektronenmicroscopie met hoge resolutie (TEM). Zoals we kunnen zien, zijn de bereide CQD's bolvormig en mono-dispersief in het gedeïoniseerd water (voor CQD's-1) of NaOH-oplossing (voor CQD's-2). Door een statistisch gemiddelde van het TEM-beeld ligt de deeltjesgrootte van deze CQD's in het bereik van 2 tot 10 nm. We vinden dat deze CQD's sterk gekristalliseerd zijn met een typische roosterstructuur van koolstof. De roosterranden zijn helder en de corresponderende roosterafstand is respectievelijk ongeveer 0,22 en 0,21 nm. We willen opmerken dat de resultaten die worden getoond in Fig. 1 erg lijken op de resultaten die eerder zijn gerapporteerd voor het N- en S-dopinggehalte in N- en S-CQD's met hoge opbrengst [23, 24]. Bovendien vinden we dat de grootteverdeling van de CQD's in gedeïoniseerd water (CQDs-1) of in NaOH-oplossing (CQDs-2) voornamelijk rond 3,5-5,5 nm ligt en dat de dikte van deze CQD's ongeveer 3,5 nm is.

een TEM-afbeeldingen voor CQD's in gedeïoniseerd water (CQDs-1) en b TEM-afbeeldingen voor CQD's in NaOH-oplossing (CQD's-2). c , d Ingezoomde afbeelding van een enkele CQD van a en b , respectievelijk
Zoals we weten, is de röntgenfoto-elektronenspectroscopie (XPS) een krachtig hulpmiddel voor het meten en begrijpen van de elementaire samenstellingen en de inhoud van de CQD's, met name voor het onderzoek van oppervlakte-gemodificeerde kenmerken van de CQD's zoals de functionele groepen op het oppervlak van de CQD's [25]. In Fig. 2 worden de volledige XPS-spectra voor CQD's-1 en CQD's-2 weergegeven en worden de bijbehorende bevindingen aangegeven. We merken op dat de hier gemeten CQD's voornamelijk C (met een typische bindingsenergie C ls = 284.8 eV), N (met een typische bindingsenergie N ls = 400 eV) en O (met een typische bindingsenergie O ls = 532 eV) bevatten ). De andere elementen zoals S en P (Na en Cl) zijn ook te vinden in CQDs-1 (CQDs-2). Als resultaat zien we dat CQDs-1 voornamelijk is samengesteld uit C-, N-, O-, S- en P-elementen, waarbij de atomaire verhouding van deze elementen C1s:O1s:N1s:S2p:P2p = 61.0:29.6:8.5 is. :0.5:0.4. We zien ook dat CQDs-2 voornamelijk bestaat uit C-, O-, N-, Na- en Cl-elementen. De atomaire verhouding van deze elementen is C1s:O1s:N1s:Na1s:Cl2p = 66,7:26,2:6,8:0,1:0,1. Omdat het tofu-afvalwater zelf chloride en sulfaat bevat, geïnduceerd door het proces bij het maken van tofu, zijn er vrij brede spectra van S- en Cl-signalen in Fig. 2. Bovendien, omdat CQDs-2 voor CQD's in NaOH-oplossing is waarin NaOH een rol kan spelen rol als passivering van de CQD's, is er een Na-signaal in het onderste paneel van Fig. 2.
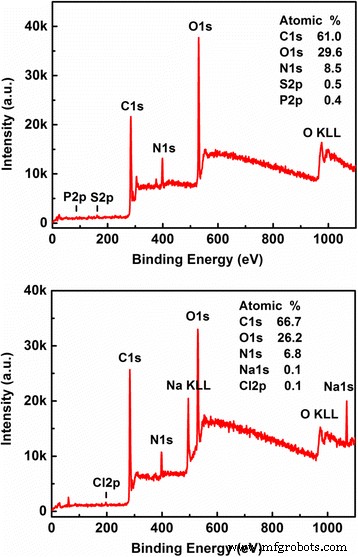
Het volledige XPS-spectrum voor respectievelijk CQDs-1 (bovenste paneel) en CQDs-2 (onderste paneel), waarbij de verkregen inhoud van elementen wordt aangegeven
In Fig. 3 tonen we de C1s-spectra met hoge resolutie voor respectievelijk CQDs-1 en CQDs-2, uitgerust met een bindingsenergie Cls. Uit het C1s-spectrum in het bovenste paneel van figuur 3 is te zien dat drie chemische bindingen C-C/C=C bij 284,7 eV, C-O bij 286,08 eV en C=O bij 287,86 eV aanwezig in CQDs-1 . Er zijn vier chemische bindingen C-C bij 284,8 eV, C-O bij 286,16 eV, C=O bij 288 eV en COOH bij 289,14 eV aanwezig in CQDs-2, zoals weergegeven in het onderste paneel van Fig. 3. Van de XPS-resultaten getoond in Fig. 3, leren we dat het fundamentele verschil tussen CQD's-1 en CQD's-2 de inhoud is van C–O- en C=O-bindingen op het oppervlak van de CQD's in respectievelijk water en NaOH-oplossing. Het is bekend dat de OH − in NaOH-oplossing kan koppelen met C–O- en C=O-bindingen op het oppervlak van de CQD's om COOH en de carboxylgroep te vormen en zo de inhoud van de C–O- en C=O-groepen in CQDs-2 te verminderen. Dit is de belangrijkste reden waarom het gehalte aan C–O- en C=O-bindingen in CQD's-1 aanzienlijk hoger is dan die in CQD's-2.
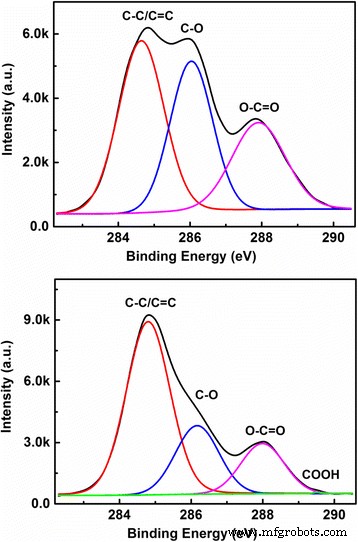
Het hoge resolutie C1s-spectrum voor respectievelijk CQDs-1 (bovenste paneel) en CQDs-2 (onderste paneel), voorzien van een bindende energie C1s
In deze studie nemen we een standaard experimentele opstelling om de fotoluminescentie (PL) -emissie van CQD's te meten die worden gerealiseerd uit tofu-afvalwater in zichtbare bandbreedte. Voor de meting wordt het HORIBA-fluorescentiesysteem (VS) toegepast, waarbij een xenonlamp wordt genomen als breedbandbekrachtigingslichtbron, de GEMIMI 180 monochromator wordt gebruikt voor het kiezen van de optische pompgolflengte en de iHR320-roosterspectrometer samen met een foto-elektrische vermenigvuldiger buis (PMT) detector wordt gebruikt voor het opnemen van het spectrum van de lichtemissie van monsters. De metingen worden uitgevoerd bij kamertemperatuur. In Fig. 4 tonen we de PL-emissiespectra voor CQD's-1 in het bovenste paneel en CQD's-2 in het onderste paneel bij verschillende excitatiegolflengten λ ex . Voor de PL-meting begint de registratie van de intensiteit van het emissielicht vaak na de excitatiegolflengte om de schade aan de PMT-detector teniet te doen. Er zijn dus afsnijdingen geweest in de curven van de PL-spectra in Fig. 4. We merken de volgende kenmerken op:(i) De intensiteit van de PL-emissie neemt eerst toe en neemt vervolgens af met toenemende excitatiegolflengte. De sterkste PL-emissie kan worden waargenomen bij ongeveer λ ex ~ 410 nm voor respectievelijk CQDs-1 en 480 nm voor CQDs-2. (ii) De piekgolflengtepositie λ em in het PL-spectrum varieert met het veranderen van de excitatiegolflengte voor zowel CQDs-1 als CQDs-2. In de inzetstukken van Afb. 4 laten we λ . zien em als een functie van λ ex zodat we duidelijker kunnen zien hoe de PL-pieken verschuiven met de excitatiegolflengte. Zoals weergegeven in Afb. 4, λ em neemt monotoon toe met λ ex voor zowel CQDs-1 als CQDs-2. (iii) In een relatief korter excitatiegolflengteregime kunnen twee PL-pieken worden waargenomen voor CQD's-1, terwijl slechts één PL-piek kan worden gezien voor CQD's-2 over het golflengteregime van 420-510 nm. (iv) CQDs-1 kan resulteren in een breder PL-spectrum dan CQDs-2. (v) De PL-piekgolflengte geïnduceerd door CQDs-1 is korter dan die geïnduceerd door CQDs-2. Bij 410 nm excitatiegolflengte kan de blauwe fluorescentie worden bereikt door CQDs-1, terwijl bij 480 nm excitatiegolflengte de groene fluorescentie kan worden gezien voor CQDs-2. (vi) De fluorescentie van de CQDs-1 met 8,5% N-dopinggehalte is hoger dan die van de CQDs-2 met 6,8% N-dopinggehalte. De reden waarom de PL-emissie toeneemt met het N-dopinggehalte van CQD's, is dat N-doping een nieuw soort oppervlaktetoestand kan introduceren. Elektronen die worden ingevangen door de nieuw gevormde oppervlaktetoestanden, kunnen een hoge opbrengst aan stralingsrecombinatie mogelijk maken [24]. De PL-resultaten die uit dit onderzoek zijn verkregen, geven aan dat de emissie van blauw en groen licht kan worden bereikt door respectievelijk CQDs-1 en CQDs-2 onder optisch pompen.
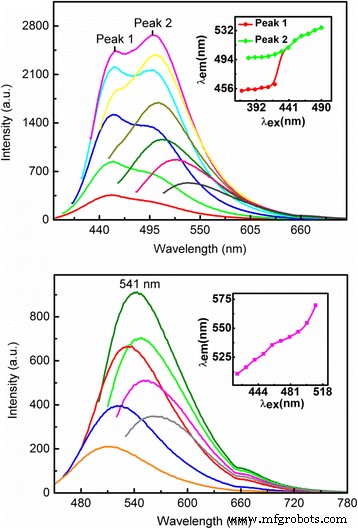
Het PL-spectrum voor CQDs-1 in het bovenste paneel en CQDs-2 in het onderste paneel bij verschillende excitatiegolflengten λ ex . In het bovenste paneel, λ ex zijn 370 nm (rood), 380 nm (groen), 390 nm (blauw), 400 nm (lichtblauw), 410 nm (donkerroze), 420 nm (geel), 430 nm (lichtgroen), 440 nm (donker groen), 450 nm (lichtrood) en 490 nm (donker olijfgroen). In het onderste paneel, λ ex zijn 420 nm (oranje), 440 nm (blauw), 460 nm (geel), 480 nm (rood), 490 nm (groen), 500 nm (roze) en 510 nm (donker olijfgroen). De inzetstukken tonen de piekgolflengte in het PL-spectrum, λ em, als functie van de excitatiegolflengte
Op dit moment is het fysieke mechanisme voor door fotonen geïnduceerde lichtemissie van CQD's nog steeds onduidelijk. De resultaten verkregen uit verwante onderzoeken [12, 26, 27] hebben echter aangetoond dat de oppervlaktemodificatie van de CQD's door amino- en carboxyl-functionele groepen een belangrijke rol kan spelen voor de PL-emissie van CQD's. De kenmerken van het PL-spectrum van CQD's worden niet alleen bepaald door de deeltjesgrootte van de CQD's [1] maar ook door de oppervlakte-eigenschappen van CQD's [26, 27]. Op basis van onze XPS- en PL-resultaten die zijn verkregen uit de huidige studie, bespreken we nu het fysieke mechanisme achter de experimentele bevindingen getoond in Fig. 4 voor CQD's die zijn gerealiseerd uit tofu-afvalwater. We weten dat de elektronische bandstructuur van CQD's erg lijkt op die van een halfgeleider met directe bandgap. Voor CQD's die zijn gesynthetiseerd uit tofu-afvalwater in verschillende oplossingen zoals water en NaOH, zijn er echter op CO, C =O en COOH-binding gebaseerde functionele groepen op het oppervlak van de CQD's, zoals getoond door de XPS-resultaten in Fig. 3. De energietoestanden van deze functionele groepen zijn oppervlaktetoestanden die zich tussen de geleidings- en valentiebanden van de CQD's bevinden. Ze spelen een rol als tussenliggende toestanden, die sterk lijken op onzuiverheidstoestanden in een halfgeleider met directe bandgap. In aanwezigheid van een excitatielichtveld worden de elektronen in de valentieband van de CQD's via een optisch absorptiemechanisme in de geleidingsband gepompt. Omdat de positie van de PL-piek in het spectrum afhangt van de excitatiegolflengte, is de PL-emissie via het excitonisch mechanisme [28] niet het geval voor deze CQD's. De door fotonen geïnduceerde lichtemissie van CQD's is daarom een gevolg van de directe foto-emissie die wordt veroorzaakt door elektronische overgangen van hogere energieniveaus naar lagere energietoestanden. Zoals we weten, hebben de elektronen normaal gesproken een snellere of kleinere relaxatietijd in de hogere energietoestanden dan die in de lagere energietoestanden. De resultaten van onze XPS- en PL-metingen suggereren dat de stralingselektronische overgang in CQD's voornamelijk wordt bereikt via relaxatie van elektronen van de oppervlaktetoestanden naar de valentieband van de CQD's. De verkregen experimentele resultaten laten zien dat de intensiteit van de PL-emissie van CQD's bereid door KOH veel sterker is dan die bereid door NaOH. Met dezelfde excitatiegolflengte vinden we dat het alkali-ion in alkalische oplossingen de positie van de PL-emissiegolflengte niet significant beïnvloedt.
Voor het geval dat de CQD's zich in water bevinden (CDQ's-1), zijn er twee tussentoestanden die worden geïnduceerd door oppervlaktetoestanden van de C–O- en C =O-bindingen en gerelateerde functionele groepen. Deze twee oppervlaktetoestanden hebben verschillende energieniveaus en overeenkomstige selectieregels voor stralingselektronische overgangen, die verantwoordelijk zijn voor de emissie van PL met twee emissiegolflengten onder lichtexcitatie met een relatief korte golflengte. De foto-geëxciteerde elektronen in de hogere energietoestanden in de geleidingsband van CQD's ontspannen eerst snel in de oppervlaktetoestanden via niet-stralingsontspanningsmechanisme zoals elektron-fononverstrooiing en elektron-elektron-interactie. Wanneer de niet-stralingselektronische relaxatietijd voor elektronen in de oppervlaktetoestanden langer of groter is dan de stralingselektronische relaxatietijd, kunnen deze elektronen teruggaan naar de valentieband en fotonen uitzenden. Met afnemende pompgolflengte kunnen meer toestanden in de valentieband en vooral in de geleidingsband deelnemen aan dit pomp-, relaxatie- en lichtemissieproces en dus neemt de piekgolflengte in het lichtemissiespectrum af met de excitatiegolflengte. Daarom hangt de golflengte van de lichtemissie af van de golflengte van het excitatielicht. De toename van de piekgolflengte van lichtemissie met excitatiegolflengte impliceert dat de niet-stralingselektronische relaxatietijd toeneemt met het verlagen van de energieniveaus in de oppervlaktetoestanden. Voor lichtexcitatie met een relatief lange golflengte worden de foto-geëxciteerde elektronen in CQD's snel ontspannen van de geleidingsband naar de lagere energieniveaus van de oppervlaktetoestanden en zenden ze fotonen uit. De mogelijkheid voor de emissie van fotonen van hogere energieniveaus van de oppervlaktetoestanden wordt laag genoeg zodat het effect niet duidelijk kan worden gemeten.
Voor het geval waarin de CQD's zich in NaOH-oplossing (CDQ's-2) bevinden, is er slechts één tussentoestand voor de stralingselektronische overgangen. Omdat de inhoud van de C–O- en C=O-bindingen en de gerelateerde functionele groep in dit geval relatief laag is, zijn de stralingsoppervlaktetoestanden voornamelijk geïnduceerde COOH-gebaseerde groepen voor CQD's-2. Als resultaat kan slechts één piek van de PL-emissie worden waargenomen. Aangezien de energieniveaus van de oppervlaktetoestanden die worden geïnduceerd door C–O- en C =O-bindingen en gerelateerde functionele groepen normaal gesproken hoger zijn dan die welke worden geïnduceerd door COOH-groepen, kan de PL-emissie met kortere golflengte worden waargenomen voor CQD's-1. Dit is de belangrijkste reden waarom CQDs-1 blauw licht kan uitstralen, terwijl CQDs-2 groen licht kan uitstralen onder optische excitatie.
De kwantumefficiëntie Q van de fluorescentie voor CQDs-1 kan worden geëvalueerd uit de experimentele gegevens via [29, 30]
$$ Q={Q}_{\mathrm{s}}\times \frac{I_{\mathrm{s}}}{I}\times \frac{A}{A_{\mathrm{s}}}\ tijden \frac{\eta^2}{{\eta_{\mathrm{s}}}^2} $$ (1)Hier Q s is de kwantumefficiëntie van de fluorescentie voor een standaardmonster ter referentie. Onder een vaste excitatiegolflengte bij bijvoorbeeld 364 nm, I en ik s zijn de geïntegreerde emissie-intensiteiten van respectievelijk het CQDs-1-monster en het standaardmonster. A en A s zijn respectievelijk de absorptie van het voorbereide monster en het standaardmonster bij dezelfde excitatiegolflengte. η en η s zijn respectievelijk de refractiviteit van het voorbereide monster en het standaardmonster. Het is gevonden dat de fluorescente kwantumefficiëntie van CQDs-1 ongeveer 54,49% is. Omdat we het referentiemonster voor CQDs-2 niet kunnen vinden, wordt de fluorescerende kwantumefficiëntie van CQDs-2 niet geëvalueerd in de huidige studie.
Conclusies
In deze studie hebben we de koolstofkwantumdots (CQD's) gefabriceerd uit afvalwater dat wordt geïnduceerd tijdens de productie van tofu. We hebben aangetoond dat het tofu-afvalwater een goede grondstof is voor het maken van CQD's. De fluorescerende CQD's kunnen eenvoudig worden vervaardigd via een hydrothermische reactie om de organische stoffen in de gele serofluide van tofu-afvalwater te carboniseren. De gemiddelde grootte van de CQD's die worden gesynthetiseerd uit tofu-afvalwater kan oplopen tot 3,5 nm. We hebben twee soorten CQD's verkregen in respectievelijk de gedeïoniseerde water- en NaOH-oplossing. Ze kunnen respectievelijk blauw en groen licht uitstralen onder de UV-straling. Uit de röntgenfoto-elektronenspectroscopie (XPS) blijkt dat het fundamentele verschil tussen deze twee soorten CQD's de inhoud van C–O- en C=O-bindingen op het oppervlak van de CQD's is. Dit verschil kan verschillende kenmerken van het fotoluminescentie (PL) -spectrum van de CQD's veroorzaken. Op basis van de verkregen resultaten van de XPS- en PL-metingen hebben we een mechanisme voorgesteld om de door fotonen geïnduceerde lichtemissie van CQD's te begrijpen en te verklaren. Een van de belangrijkste conclusies uit dit onderzoek is dat het gebruik van tofu-afvalwater om de CQD's te synthetiseren niet alleen nuttig kan zijn om een oplossing te bieden voor het milieuprobleem dat door het afvalwater wordt veroorzaakt, maar ook veelbelovend kan zijn voor een eenvoudige en goedkope massaproductie van CQD's voor bio- en optische toepassingen. We hebben tot nu toe met succes de blauw en groen fluorescerende CQD's verkregen uit tofu-afvalwater. De uitdaging van ons huidige werk is om de CQD's te verkrijgen die rood licht kunnen uitzenden onder optisch pompen.
Nanomaterialen
- N,N-dimethylformamide die de fluorescentie van MXene Quantum Dots reguleert voor de gevoelige bepaling van Fe3+
- Geactiveerde koolstofvezels met hiërarchische nanostructuur afgeleid van afval katoenen handschoenen als hoogwaardige elektroden voor supercondensatoren
- Synthese van pyridinic-rijke N, S Co-gedoteerde Carbon Quantum Dots als effectieve enzymnabootsers
- Silica-nanodeeltjes voor intracellulaire eiwitafgifte:een nieuwe synthesebenadering met behulp van groene fluorescerende eiwitten
- Groene synthese van InP/ZnS Core/Shell Quantum Dots voor toepassing in licht-emitterende diodes zonder zware metalen
- Magnetische koolstofmicrosferen als herbruikbaar adsorbens voor het verwijderen van sulfonamide uit water
- Eliminatie van bimodale grootte in InAs/GaAs Quantum Dots voor de voorbereiding van 1,3-μm Quantum Dot Lasers
- Materiële en optische eigenschappen van fluorescerende koolstof Quantum Dots vervaardigd uit citroensap via hydrothermische reactie
- Ontwerp van door spanning ontworpen GeSn/GeSiSn Quantum Dots voor Mid-IR Direct Bandgap Emission op Si-substraat
- Eenvoudige synthese van polydopamine-koolstofstippen voor fotothermische therapie
- Carbon Dots @ Platinum Porphyrin Composite als theranostic nanoagent voor efficiënte fotodynamische kankertherapie



