One-Pot Green-synthese van met Ag versierde SnO2-microsfeer:een efficiënte en herbruikbare katalysator voor reductie van 4-nitrofenol
Abstract
In dit artikel, hiërarchische Ag-versierde SnO2 microsferen werden gesynthetiseerd door een gemakkelijke hydrothermische methode in één pot. De resulterende composieten werden gekarakteriseerd door XRD-, SEM-, TEM-, XPS-, BET- en FTIR-analyse. De katalytische prestaties van de monsters werden geëvalueerd met de reductie van 4-nitrofenol tot 4-aminofenol door kaliumboorhydride (KBH4 ) als een modelreactie. Tijdafhankelijke experimenten gaven aan dat de hiërarchische microsferen samengesteld uit SnO2 en Ag-nanodeeltjes kunnen worden gevormd wanneer de reactietijd minder dan 10 uur is. Met de toename van de hydrothermische tijd, SnO2 nanodeeltjes zullen zichzelf assembleren tot SnO2 nanosheets en Ag nanodeeltjes versierd SnO2 nanosheets werden verkregen. Wanneer geëvalueerd als katalysator, de verkregen Ag-versierde SnO2 microbolletjes bereid voor 36 uur vertoonden uitstekende katalytische prestaties met genormaliseerde snelheidsconstante (κ noch ) van 6,20 min −1 g −1 L, wat veel beter is dan die van sommige eerder gerapporteerde katalysatoren. Bovendien is deze met Ag versierde SnO2 microsfeer vertoont een goede herbruikbaarheid na de eerste vijf cycli. Daarnaast speculeren we over het vormingsmechanisme van de hiërarchische Ag-versierde SnO2 microsfeer en bespraken de mogelijke oorsprong van de uitstekende katalytische activiteit.
Achtergrond
SnO2 is een belangrijke n-type halfgeleider met een grote bandgap (bijv. = 3.6 eV, bij 300 K), hoge elektronenmobiliteit en lage kosten, waardoor het uitstekende eigenschappen heeft in gasdetectie [1], lithium-ionbatterijen [2], opto-elektronische apparaten en met kleurstof gesensibiliseerde zonnecellen [3,4,5,6,7,8]. In de afgelopen twee decennia heeft de robuuste SnO2 materiaal heeft veel aandacht gekregen en er zijn verschillende nanostructuren gerapporteerd [9, 10]. Waarvan driedimensionale (3D) hiërarchische structuren die zelf samengesteld zijn door nanosheets-bouwstenen, veel interessanter zijn vanwege hun speciale structuur en fascinerende eigenschappen [11, 12]. Desalniettemin zijn er slechts enkele rapporten over de katalytische prestaties van SnO2 en de katalytische efficiëntie is relatief laag [13,14,15]. Het is dus belangrijk om hiërarchische SnO2 . te synthetiseren structuren en bestudeer de katalytische prestaties. Vooral, zoals we weten, zullen edelmetaalnanodeeltjes (NP's) zoals Au-, Ag-, Pt- en Pd-gemodificeerde 3D-hiërarchische structuren veel verbeterde katalytische prestaties vertonen [16]. De meeste processen van de synthese van de bovengenoemde edelmetaal-gemodificeerde oxiden zijn echter meer gecompliceerde meerstapsprocessen en zijn gewoonlijk giftig en schadelijk voor het milieu [17]. Dus het ontwikkelen van gemakkelijke en efficiënte methoden om edelmetaal NP-gemodificeerde hiërarchische SnO2 te fabriceren en het bestuderen van de katalytische prestaties zijn zeer wenselijk.
Toenemende vervuiling van onze beperkte watervoorraden als gevolg van de wijdverbreide verspreiding van verschillende industriële kleurstoffen, zware metaalionen en andere aromatische verontreinigende stoffen brengen onze planeet in gevaar [18]. Het 4-nitrofenol (4-NP), een bekende giftige verontreinigende stof, is wijdverbreid aanwezig in industrieel afvalwater en landbouwafvalwater [19]. Onder verschillende behandelingstechnieken, zoals membraanfiltratie [20], fotodegradatie [21], adsorptie [22] en chemische reductie [23,24,25,26,27,28,29,30], de chemische reductie van 4 -NP tot 4-aminofenol (4-AP) is een gunstige route, dankzij het product (4-AP) dat een belangrijk tussenproduct is voor de vervaardiging van pijnstillende en koortswerende geneesmiddelen, fotografische ontwikkelaar, corrosieremmer, anticorrosief smeermiddel en haar -kleurstof [31, 32]. Daarom is de reductie van 4-NP tot 4-AP van groot belang voor de vermindering van de vervuiling en de regeneratie van hulpbronnen [33].
In dit artikel hebben we een groene synthese gerapporteerd van edelmetaal Ag-nanodeeltjes (NP)-gemodificeerd SnO2 hiërarchische architecturen door een eenvoudige hydrothermische route met één pot zonder de assistent van sjablonen en oppervlakteactieve stoffen bij milde temperatuur. De effecten van reactietijd op morfologieën van met Ag versierde SnO2 microbolletjes werden onderzocht en een mogelijk groeimechanisme van met Ag versierde SnO2 hiërarchische structuren werd voorgesteld. De katalytische resultaten geven aan dat de gesynthetiseerde producten uitstekende katalytische prestaties vertonen voor de reductie van 4-NP tot 4-AP, met een genormaliseerde snelheidsconstante (κ noch ) van 6,20 min −1 g −1 L. Bovendien is de met Ag versierde SnO2 hiërarchische structuren behouden een hoge katalytische efficiëntie in tien cycli en vertonen stabiliteit na de eerste vijf cycli. Dit leverde Ag-versierde SnO2 . op hiërarchische structuren kunnen potentiële toepassingen hebben voor de behandeling van waterverontreinigingen, en deze eenvoudige hydrothermische route in één stap kan worden uitgebreid om andere edelmetalen NP-gemodificeerde composieten te ontwerpen met een breed scala aan praktische toepassingen voor de toekomst.
Methoden
Materialen
Zilvernitraat (AgNO3 , 99,8%), ureum (CO(NH2 )2 , 99%), ammoniakoplossing (NH3 ·H2 O, 25~28% en kaliumboorhydride (KBH4 , 97%) werden gekocht bij Sinopharm Chemical Reagent Co. Ltd. Natriumstannaatrehydraat (Na2 SnO3 ·3H2 O, 98%) en 4-nitrofenol (C6 H5 NEE3 , 98%) werden geleverd door Aladdin Reagent Co. Ltd. Alle materialen werden zonder verdere zuivering gebruikt.
Synthese van met Ag versierde SnO2 Microsfeer
Met Ag versierde SnO2 poeder (molverhouding van Ag:SnO2 =-1:1) werd gesynthetiseerd met een hydrothermische methode in één pot. In een typische procedure werden 2,67 g natriumstannaat gerehydrateerd en 0,2 g ureum opgelost in 25 ml ultrazuiver water en 30 min krachtig geroerd om een mengsel te vormen. Vervolgens werd 1,69 g zilvernitraat gedispergeerd in 25 ml ultrazuiver water en vervolgens werd 2,4 ml ammoniumhydroxide toegevoegd aan de zilvernitraatoplossing om een zilver-ammoniakoplossing te vormen. Na 5 minuten roeren werd de vers bereide zilver-ammoniakoplossing gedurende 1 uur onder magnetisch roeren aan het mengsel toegevoegd. Vervolgens werd het resulterende mengsel gemigreerd naar een met Teflon beklede autoclaaf van 50 ml en gedurende 5, 10, 24 en 36 uur op 150°C verwarmd. Na de hydrothermische procedure werd de autoclaaf op natuurlijke wijze afgekoeld tot kamertemperatuur en de SnO2 /Ag-product werd verzameld door centrifugeren, gevolgd door spoelen met gedeïoniseerd water en ethanol en drogen in een vacuümoven bij 60°C. SnO2 /Ag-microbolletjes met verschillende molverhoudingen (1,5:1, 1:1, 0,5:1, 0,01:1) van Ag tot SnO2 worden op een vergelijkbare manier gesynthetiseerd, behalve de hoeveelheden AgNO3 en NH3 ·H2 O. Ter vergelijking, pure SnO2 en Ag werden ook gesynthetiseerd door de vergelijkbare procedure zonder de toevoeging van AgNO3 en Na2 SnO3 .
Voorbeeldkarakteriseringen
De kristallijne fase van de voorbereide monsters werd onderzocht met röntgenpoederdiffractie (XRD, Cu Kα-straling (λ = 1,5418 )). De scanning elektronenmicroscopie (SEM) metingen werden uitgevoerd op een SU-70 veldemissie SEM-microscoop met een versnellingsspanning van 20 kV. Transmissie-elektronenmicroscoop (TEM) en transmissie-elektronenmicroscopie met hoge resolutie (HRTEM) werden genomen op een Tecnai G2 F20 S-TWIN transmissie-elektronenmicroscoop met een versnellingsspanning van 200 kV. Röntgenfoto-elektronenspectroscopie (XPS) werd uitgevoerd om de chemische samenstelling van het oppervlak en de chemische toestanden van de katalysatoren te identificeren op een MARK II röntgenfoto-elektronspectrometer met behulp van Mg Kα-straling. Het specifieke oppervlak van het monster werd geëvalueerd door het Langmuir-model en het Brunauer-Emmett-Teller (BET) -model op basis van de stikstofadsorptie-isotherm verkregen met een V-sorb X2008-serie, terwijl de poriegrootteverdeling werd geschat door Barrett-Joyner- Halenda (BJH) theorie.
Katalytische activiteit van met Ag versierde SnO2 Microsfeer
De reductie van 4-NP met KBH4 oplossing werd gebruikt als een modelreactie om de katalytische activiteit van Ag-versierde SnO2 composieten. Het katalytische reductieproces werd uitgevoerd in een standaard kwartscel met een padlengte van 1 cm en een volume van ongeveer 4 ml met 0,3 ml vers bereide waterige oplossingen van 4-NP (20 mg/L) en KBH4 (1,5 mg). De hoge molverhouding van KBH4 tot 4-NP zorgde voor een overmaat van de eerste, en daarom bleef de concentratie ervan in wezen constant tijdens de reductiereactie. Na toevoeging van KBH4 in de 4-NP-oplossing, veranderde de kleur onmiddellijk van lichtgeel in donkergeel door de vorming van 4-nitrofenolaat-ion (gevormd door de hoge alkaliteit van KBH4 ). Later vervaagde de donkergele kleur met de tijd (vanwege de omzetting van 4-NP naar 4-AP) na de toevoeging van 1,5 mg met Ag versierde SnO2 hybriden. De UV-Vis-absorptiespectra werden geregistreerd door een UV-Vis-spectrometer in een scanbereik van 250-500 nm bij kamertemperatuur met een tijdsinterval van 1 minuut. Verschillende opeenvolgende reactierondes werden gemeten om de stabiliteit van de katalysator te bepalen.
Resultaten en discussie
Karakterisering van met Ag versierde SnO2 Microsfeer
De samenstelling en fasestructuur van de gesynthetiseerde Ag-versierde SnO2 poeders voor verschillende tijden werden onderzocht met XRD, en de overeenkomstige patronen worden getoond in Fig. 1. Het is te zien dat de karakteristieke diffractiepieken goed overeenkomen met de tetragonale rutielfase SnO2 (JCPDS-bestand nr. 41-1445, a = 4.738Å en c = 3.187 Å) en face-centered cubic (fcc) phase Ag (JCPDS file no. 04-0783). Er werden geen diffractiepieken van andere onzuiverheden gedetecteerd, wat aangeeft dat de poeders het mengsel zijn van puur SnO2 en Ag. Voor het monster dat 5 uur heeft gereageerd, zijn de karakteristieke diffractiepieken bij 38,12 ° en 44,2 °, overeenkomend met de (111) en (200) vlakken van Ag, relatief zwak. Met toenemende hydrothermische tijd nemen de piekintensiteiten van Ag toe en nemen ook de volledige breedtes van de diffractiepiek af, wat wijst op de verbeterde kristalliniteit van Ag-nanodeeltjes of het verhoogde gewicht van Ag. Dit kan verder worden geverifieerd door de XRD-patronen van de monsters die zijn verkregen bij verschillende temperaturen en verschillende molverhoudingen van Ag en SnO2 (Extra bestand 1:Afbeelding S1).
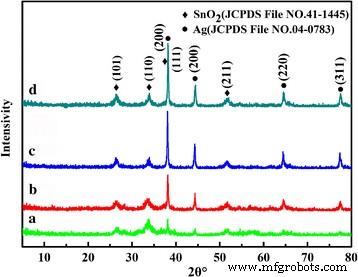
XRD-patronen van de met Ag versierde SnO2 microsferen bereid bij 150°C voor verschillende tijden (a ) 5 u, (b ) 10 u, (c ) 24 uur, en (d ) 36 u
De SEM-afbeeldingen in Fig. 2 tonen de interessante morfologische evolutie van monsters die zijn bereid op verschillende hydrothermische tijden van 5 tot 36 uur. Monster bereid gedurende 5 uur was een onregelmatige microsfeer en het vergrote beeld van het oppervlak van microsferen in de inzet die de microsfeer illustreert, wordt geassembleerd door nanodeeltjes (figuur 2a). Met toenemende hydrothermische tijd werd de microsfeer regelmatiger. Toen de hydrothermische tijd toenam tot 24 uur (figuur 2c), werd de microsfeer groter ten koste van de kleinere nanodeeltjes en de oppervlakte-nanodeeltjes zelf-geassembleerd tot nanosheets. Deze nanosheets verzamelden zich om een hiërarchische microsfeerstructuur te vormen. Bij het verder verhogen van de hydrothermische tijd tot 36 uur, werden de grove nanosheets gladder en zijn de microsferen met diameters van 2 tot 4 μm uniformer. Verdere toename van de hydrothermische tijd leidde niet tot een duidelijke verandering van de morfologie en kristallijn (niet getoond in dit artikel). De morfologie van het gedurende 36 uur bereide monster werd verder waargenomen via TEM en HRTEM. Zoals getoond in Fig. 2e, de verkregen SnO2 /Ag is van microsfeermorfologie met een diameter van ~ 5 μm en de microsfeer is samengesteld uit nanosheets. In het typische HRTEM-beeld (Fig. 2f) werden Ag NP's met een gemiddelde grootte van ongeveer 5 nm gevormd en homogeen verdeeld over SnO2 . De roosterranden van d = 0.26 nm-afstand kan worden toegewezen aan de Ag (111)-vlakken terwijl de roosterranden van d = 0.33 nm kan worden toegewezen aan het (110) vlak van SnO2 , respectievelijk. Om de uniforme verdelingen van Ag-nanodeeltjes in de microsfeer verder te illustreren, analyse van elementmapping van de SnO2 /Ag-microsfeer werd uitgevoerd (Fig. 3). Zoals weergegeven in figuur 3, past de kaart van Ag-, Sn- en O-elementen in de monstermorfologie, wat aangeeft dat Ag-nanodeeltjes uniform in de microsferen zijn verspreid.
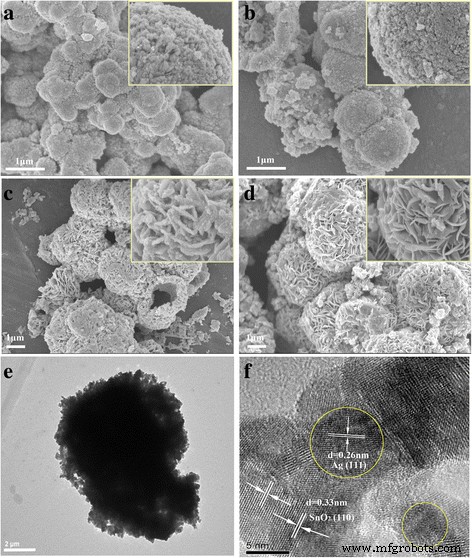
Representatieve FESEM-afbeeldingen en TEM-afbeeldingen van de met Ag versierde SnO2 microsferen bereid bij 150°C voor verschillende hydrothermische tijden a 5u, b 10u, c 24 uur, en d 36 uur en e , v TEM-beeld met lage vergroting en TEM (HRTEM) met hoge resolutie van het monster, voorbereid voor 36 h
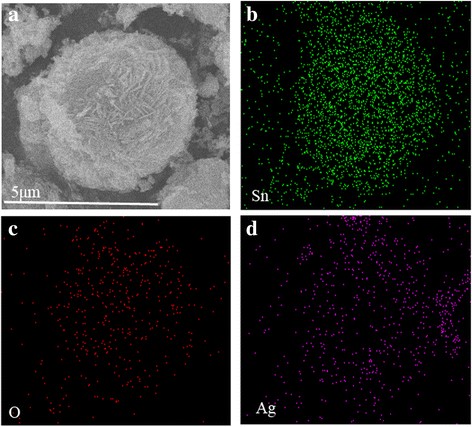
EDS-elementtoewijzing van SnO2 /Ag-microsferen. een SEM-afbeeldingen en elementenkaarten van b Sn, c O, en d Ag
De N2 adsorptie-desorptie-isothermen van monsters en hun corresponderende poriegrootteverdeling worden geïllustreerd in figuur 4. Alle monsters vertoonden type IV isothermen met H3 hysteresislus, wat staat voor typische mesoporeuze structuren met uniforme poriegrootte [34]. De BET-specifieke oppervlakten werden bepaald op 21,8, 22,4, 24,6. en 25,7 m 2 g −1 , respectievelijk. Inzet geeft de poriegrootteverdelingen van monsters weer. De poriegrootteverdeling is monomodaal voor alle monsters. De gemiddelde poriediameter is ~2 nm voor de as-hiërarchische Ag-versierde SnO2 poeders. Opgemerkt wordt dat het berekende BET-oppervlak en de gemiddelde poriediameter geen duidelijke verandering hebben met toenemende hydrothermische tijd.
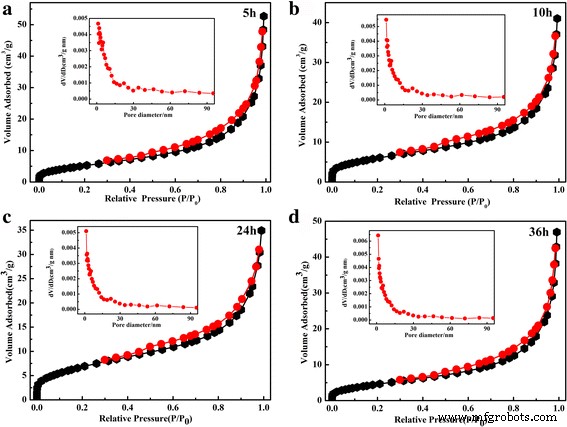
Typische stikstofadsorptie-desorptie-isotherm van de bereide SnO2 /Ag-microsferen bereid bij 150°C voor verschillende hydrothermische tijden a 5 u, b 10 u, c 24 u, en d 36 u
XPS werd gebruikt om de chemische toestanden en oppervlaktesamenstelling van met Ag versierde SnO2 te onderzoeken. microsferen. Brede onderzoeksscans werden eerst opgenomen, gevolgd door een gedetailleerde scan van de randen van elk element, zoals Sn 3d, Ag 3d en O 1s (Fig. 5). Er kan worden vermeld dat het oplaadeffect op het monster werd gecorrigeerd door de bindingsenergie van de koolstof (C 1s) in te stellen op 284,6 eV en deze koolstofpiek werd gebruikt als referentiepositie voor het schalen van alle andere pieken. Zoals weergegeven in Fig. 5b, verschijnt de piek als een spin-orbit doublet bij 369,1 eV (Ag 3d5/2 ) en 375,2 eV (Ag 3d3/2 ) voor Ag 0 [35, 36] in het product. De twee satellietpieken van 366,5 en 372,3 eV kunnen verantwoordelijk zijn voor Ag 3d in met Ag versierde SnO2 nanocomposieten [37]. Bovendien zijn twee XPS-pieken op 488 en 496,7 eV relevant voor Sn 3d5/2 en Sn 3d3/2 , wat de aanwezigheid van Sn 4+ . aangeeft in SnO2 . En de pieken rond 485,7 en 494,7 eV kunnen worden veroorzaakt door de binding tussen Sn en Ag [38, 39]. De licht bindende energieverschuiving van deze elementen in Ag-versierde SnO2 microsfeer betekent dat elektronen kunnen worden overgedragen tussen Ag en SnO2 , wat een sterke interactie aantoont tussen Ag-nanodeeltjes en SnO2 nanosheets in plaats van alleen fysiek contact. De sterke interactie is gunstig voor de elektronenoverdracht tussen de aangrenzende deeltjes, wat de katalytische activiteiten kan verbeteren en gunstig is voor een soortgelijk fenomeen, dat werd waargenomen in andere literatuur [38,39,40]. In figuur 5d kwamen O 1s-spectra bij 530,5 eV overeen met de roosterzuurstof, terwijl de piek bij 532,6 eV overeenkomt met chemisch gesorbeerde zuurstof of hydroxylionen zoals O − , O2 − , of OH − aan het oppervlak van SnO2 [41,42,43,44].
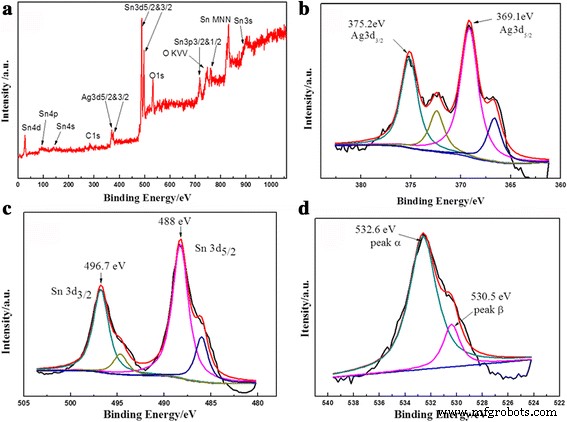
Representatieve XPS-spectra van SnO2 /Ag-microsferen bereid bij 150 °C gedurende 36 uur. een XPS volledige spectra. Hoge-resolutiespectra van de elementen b Ag, c Sn en d O
Katalytische reductie van 4-NP
De reductie van 4-NP door KBH4 in aanwezigheid van katalysator is een goed bestudeerde groene chemische reactie en werd gekozen als de modelreactie om de katalytische activiteit van de zoals bereid met Ag versierde SnO2 te bestuderen composieten. Het UV-Vis-absorptiespectrum met een maximale absorptie bij 400 nm wordt gevormd door de nitroverbinding. Met de met Ag versierde SnO2 katalysator toegevoegd, de absorptiepiek bij 400 nm, toegeschreven aan nitroverbindingen, nam sterk af in 1 minuut en een nieuwe piek bij 300 nm die overeenkomt met 4-AP verscheen, wat aangeeft dat de katalytische reductie van 4-NP succesvol was verlopen (Fig. 6a) . Rekening houdend met het eigen risico KBH4 , kan worden aangenomen dat de concentratie ervan constant is tijdens de reactie. Daarom kan een pseudo-kinetische vergelijking van de eerste orde worden toegepast om de katalytische snelheid te evalueren. De kinetische vergelijking van de reductie kan als volgt worden geschreven:
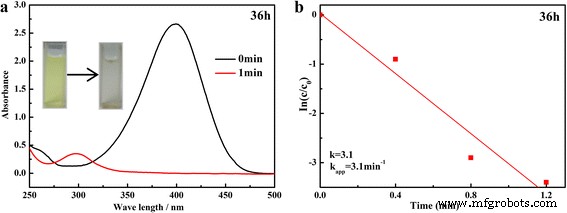
een , b Tijdsafhankelijke UV–Vis-absorptiespectra en de plot van ln(C .) t /C 0 ) versus reactietijd voor de reductie van 4-NP van het monster bereid bij 150 °C gedurende 36 uur
waarbij de verhoudingen van 4-NP-concentraties C t (op het moment t ) naar de beginwaarde C 0 (t = 0) werden direct gegeven door de relatieve intensiteit van de respectieve absorptie At /A0 , κ app komt overeen met de schijnbare snelheidsconstante. De schijnbare snelheidsconstante, κ app , werd berekend als 3,10 min −1 voor de reductie van 4-NP van de bereide Ag-versierde SnO2 microbolletje bij 150 ° C gedurende 36 uur (Fig. 6b). Om de katalytische prestaties van de met Ag versierde SnO2 . verder te beoordelen , werden alle monsters bereid voor verschillende hydrothermische tijden uitgevoerd voor katalytische reductie van de 4-NP. De UV–Vis absorptiespectra van de reductie worden getoond in Aanvullend bestand 1:Figuur S2–S5, en de bijbehorende grafieken van ln(C) t /C 0 ) versus tijd worden getoond in Fig. 7. Het is duidelijk dat bijna 100% van 4-NP binnen 1 minuut na de eerste cyclus kan worden verminderd. Met de toename van de cyclustijden wordt de tijd langer. Toch kan meer dan 80% van 4-NP binnen 8 minuten worden hergebruikt. Het kan worden opgemerkt dat ln(C t /C 0 ) waarden tonen een goede lineaire correlatie met de reactietijd voor alle katalysatoren, wat aangeeft dat de reductie een eerste-orde reactiewet volgt. De berekende schijnbare snelheidsconstanten κ app verschillende cycli voor alle monsters worden weergegeven in tabel 1.
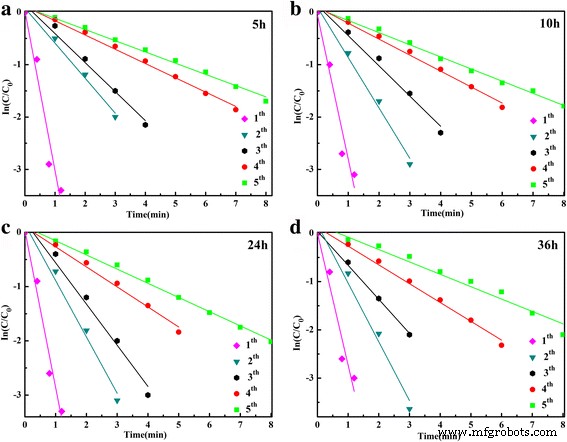
Plot van ln(C t /C 0 ) versus reactietijd in aanwezigheid van Ag-versierde SnO2 microsferen voorbereid voor verschillende hydrothermische tijden a 5 u, b 10 u, c 24 u, en d 36 u
Zoals weergegeven in Afb. 7 en Tabel 1, zijn de schijnbare snelheidsconstanten (κ app ) toenemen met de verlenging van de hydrothermische tijd en afnemen met de cyclustijden, vooral voor de eerste en tweede cyclus. De verlagingen van de snelheidsconstante kunnen het gevolg zijn van het afpellen en coaguleren van Ag NP's uit de microsfeer tijdens het centrifugeren. Om de stabiliteit van het in het werk bereide monster te bewijzen, werd de afgescheiden katalysator (bereid voor 36 uur) hergebruikt voor katalytische reductie van 4-NP gedurende meer dan vijf cycli. De tijdsafhankelijke UV-Vis-absorptiespectra van de zesde cyclus tot de tiende cyclus worden weergegeven in aanvullend bestand 1:figuur S6. De bijbehorende schijnbare snelheidsconstanten (κ app ) getoond in Fig. 8 laat zien dat er slechts een lichte afname is in de κ app waarde met het toenemen van opeenvolgende cycli, wat aangeeft dat na de eerste vijf cycli de katalysatoren veel stabieler zijn dan de vers bereide monsters. Dit bewijst dat de as-bereide Ag-versierde SnO2 monsters bezit een goede stabiliteit voor de katalytische reductie van 4-NP tot p-AP door KBH4 en kan worden gebruikt als een alternatieve actieve en stabiele katalysator voor de katalytische reductie van 4-NP.
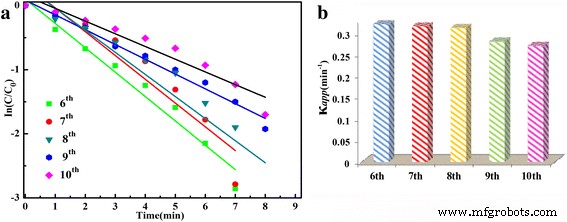
een , b Plot van ln(C t /C 0 ) versus reactietijd van de zesde tot tiende cycli voor het monster van 36 uur
Ook werden de FTIR-spectra van de katalysator voor en na vijf cycli en tien cycli van katalytische reductie getoond in ESI. Zoals te zien is in Aanvullend bestand 1:Afbeelding S7, waren de belangrijkste pieken van de monsters na vijf en tien cycli van katalytische reductie bijna hetzelfde als in het voorbereide monster en dit illustreert dat de katalysatoren zeer stabiel zijn.
Om onze resultaten te vergelijken met andere katalysatoren in de literatuur, evalueerden we het katalytische vermogen van Ag-versierde SnO2 door de κ . te normaliseren app waarden naar κ noch [45, 46]. De genormaliseerde snelheidsconstante κ noch (κ noch = κ app /c kat , waar c kat is de concentratie van de katalysator) is een belangrijke indicator voor het schatten van de katalytische activiteit. De genormaliseerde snelheidsconstanten κ noch werden berekend op 6,20, 0,64 en 0,54 min −1 g −1 L van de eerste cyclus, vijfde cyclus en tiende cyclus voor de SnO2 /Ag-microbolletjes reageerden respectievelijk 36 uur. De vergelijking van κ noch van de SnO2 /Ag (36 h) en andere katalysatoren in de literatuur worden getoond in Tabel 2. Uit Tabel 2 is het duidelijk dat de genormaliseerde schijnbare snelheidsconstante κ noch van het monster in dit werk is veel hoger dan dat van sommige gerapporteerde katalysatoren in de literatuur [47,48,49,50,51,52,53,54,55,56,57,58], zoals core-shell Ag@ Punt (0,92 min −1 g −1 L), AgNP's/GR-G3.0PAMAM (0,78 min −1 g −1 L), rGO/Fe3 O4 /Au (0.52 min −1 g −1 L). Bovendien geldt voor de vijfde en tiende cyclus de berekende κ noch (0,64 en 0,54 min −1 g −1 L) zijn zelfs hoger dan deze katalysatoren [51.52.53.54.55.56.57.58]. Al deze resultaten illustreren dat de voorbereide SnO2 /Ag-microbolletjes kunnen worden beschouwd als een potentieel efficiënte katalysator voor de reductie van 4-NP.
Gebaseerd op de eerdere resultaten en de traditionele theorie over de katalytische reductie van p-NP door edele metalen, het vormingsmechanisme en de oorsprong van de uitstekende katalytische efficiëntie van hiërarchische Ag-versierde SnO2 microbolletjes werden gespeculeerd en het schema wordt getoond in Fig. 9 en 10. In de gemakkelijke eenpots hydrothermische methode, de Ag en SnO2 NP's werden gelijktijdig in de oplossing gevormd en de pas geboren oppervlakken hebben de neiging om met elkaar te hechten. Met de toename van de hydrothermische tijd, wordt de SnO2 nanodeeltjes geassembleerd tot nanosheets [59] en Ag-nanodeeltjes verspreid in de microsfeer. Tijdens de katalytische reductie starten de Ag-nanodeeltjes de katalytische reductie door elektronen van de donor BH4 door te sturen. − aan de acceptor 4-NP op de adsorptieplaatsen van de monsters, die werd versneld door de innige binding tussen SnO2 en Ag NP. Bovendien kunnen de gedispergeerde Ag NP's in de microsfeer agglomeratie tijdens de katalytische reactie vermijden vanwege het sterische hinderingseffect. Bovendien is het synergetische effect van Ag NP's en SnO2 nanosheets dragen bij aan de uitstekende katalytische activiteit van met Ag versierde SnO2 composieten. Om de aanname te verifiëren, pure SnO2 en Ag NP's werden gesynthetiseerd door de vergelijkbare procedures zonder de toevoeging van AgNO3 en Na2 SnO3 , respectievelijk, en diende vervolgens voor de katalytische reductie van 4-NP. De tijdsafhankelijke UV–Vis-spectra en bijbehorende grafieken van ln(C .) t /C 0 ) versus tijd voor SnO2 en Ag NP's worden weergegeven in aanvullend bestand 1:figuur S8 en figuur S9. Er kan worden waargenomen dat de reductie ook een reactiewet van de eerste orde volgt. De snelheidsconstante (κ app ) waarden berekend op basis van de helling van het lineaire gebied bleken 1,24 min −1 te zijn , en 1,16 min −1 voor SnO2 en Ag, wat lager is dan die van SnO2 /Ag. Dus de uitstekende katalytische activiteit van SnO2 /Ag kan voortkomen uit het synergetische effect tussen Ag-nanodeeltjes en SnO2 nanobladen. Het nauwkeurige mechanisme moet echter verder worden onderzocht.
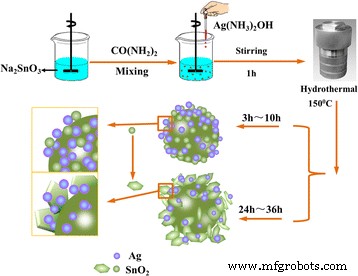
Schematische illustraties van de synthese van met Ag versierde SnO2 microbol
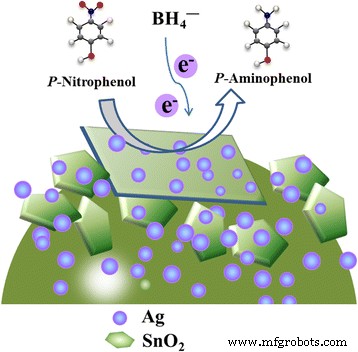
Schematische illustraties van de katalytische reductie van 4-NP tot 4-AP via Ag-versierde SnO2 microbol
Conclusies
Samenvattend, hiërarchische Ag-versierde SnO2 microbolletje met uniforme Ag-nanodeeltjes en SnO2 nanosheets is met succes bereid door een gemakkelijke eenpotsmethode. De katalysatoren die met deze eenvoudige maar effectieve methode zijn bereid, vertonen uitstekende katalytische prestaties voor de reductie van 4-NP tot 4-AP met κ noch van 6,20 min −1 g −1 L. Bovendien kan de katalysator na de eerste vijf cycli een hoge katalytische prestatie behouden en kan worden verwacht dat hij werkt als zeer efficiënte katalysatoren voor de reductie van 4-NP. Bovendien geloven we dat deze methode kan worden gebruikt als een nieuwe strategie om andere met metaaldeeltjes gemodificeerde halfgeleidercomposieten te maken.
Nanomaterialen
- Vooruitgang en uitdagingen van fluorescerende nanomaterialen voor synthese en biomedische toepassingen
- Silica-nanodeeltjes voor intracellulaire eiwitafgifte:een nieuwe synthesebenadering met behulp van groene fluorescerende eiwitten
- Op trifenylfosfine gebaseerd functioneel poreus polymeer als een efficiënte heterogene katalysator voor de synthese van cyclische carbonaten uit CO2
- Een efficiënt en effectief ontwerp van InP-nanodraden voor maximale oogst van zonne-energie
- Synthese en in vitro prestaties van met polypyrrool gecoate ijzer-platina nanodeeltjes voor fotothermische therapie en foto-akoestische beeldvorming
- One-Pot-synthese van Cu2ZnSnSe4-nanoplaten en hun door zichtbaar licht aangedreven fotokatalytische activiteit
- Groene bekwaamheid in de synthese en stabilisatie van kopernanodeeltjes:katalytische, antibacteriële, cytotoxiciteits- en antioxidantactiviteiten
- Platycodon-saponinen van Platycodi Radix (Platycodon grandiflorum) voor de groene synthese van gouden en zilveren nanodeeltjes
- S-gedopeerd Sb2O3-nanokristal:een efficiënte zichtbaar-lichtkatalysator voor organische afbraak
- Nieuwe Anodic Catalyst Support voor Direct Methanol Fuel Cell:Karakteriseringen en Single-Cell Performances
- Voorbereiding van hiërarchische poreuze Silicalite-1 ingekapselde Ag NP's en zijn katalytische prestaties voor 4-nitrofenolreductie



