Voorbereiding en evaluatie van nieuwe, met emodine geladen stearinezuur-g-chitosan-oligosaccharide-nanomicelles
Abstract
Het doel van deze studie was om met emodine beladen stearinezuur-g-chitosan-oligosaccharide (CSO-SA/EMO) te bereiden en te karakteriseren en om de antitumoractiviteit in vitro te evalueren. In deze studie werd stearinezuur-g-chitosan-oligosaccharide gebruikt als drager en werden de fysisch-chemische eigenschappen ervan bepaald met verschillende methoden. Het celopnamegedrag werd onderzocht met behulp van FITC-gelabeld stearinezuur-g-chitosan-oligosaccharide. CSO-SA/EMO werd bereid met behulp van ultrasone trillingen en dialyse. Deeltjesgrootte, oppervlaktepotentieel, invangefficiëntie en afgiftegedrag van geneesmiddelen werden in vitro bestudeerd. De effecten van CSO-SA/EMO op maagkankercellen werden onderzocht met behulp van MTT-assay en flowcytometrie. De resultaten toonden aan dat de deeltjesgrootte van CSO-SA/EMO groter was en dat het potentieel kleiner was dan dat van stearinezuur-g-chitosan-oligosaccharide. De micellaire opname van 12 h door MGC803- en BGC823-cellen was voldoende en de micellen konden zich overvloedig ophopen op laesieplaatsen bij muizen, waardoor een goede passieve EPR-targeting werd bereikt. MTT- en celcyclusstop-assays toonden CSO-SA / EMO-versterkte antitumoractiviteit significant tegen MGC803- en BGC823-cellen in vergelijking met die van vrij emodine. Tumorvolume, hematoxyline- en eosinekleuring en terminaal deoxynucleotidetransferase dUTP nick-end labeling-assay bewezen dat CSO-SA/EMO een significant antitumoreffect had op tumorweefsels in vivo. Concluderend, de methode met ultrasone trillingen en dialyse bood een eenvoudige en effectieve methode voor het voorbereiden van CSO-SA/EMO. De afgifte van emodine met behulp van een micelsysteem verbeterde de antitumoreffecten effectief.
Inleiding
Emodine (EMO) is een natuurlijk antrachinonderivaat dat voornamelijk wordt gewonnen uit traditionele Chinese kruiden zoals rabarber, cuspidatum en multiflorum. Traditionele Chinese geneeskunde (TCM) wordt veel gebruikt in klinisch onderzoek vanwege de lage toxiciteit, weinig bijwerkingen en lage kosten [1].
Studies hebben aangetoond dat EMO een brede farmacologische activiteit heeft, waaronder immuunsuppressie, anti-pertussis, antihypertensieve, ontstekingsremmende, antibacteriële en antikankeractiviteiten. Van EMO is gevonden dat het de groei van kankercellen remt [2,3,4] en verwante genen reguleert om tumorcelapoptose, tumorigenese, celproliferatie, invasie en metastase te beheersen [5,6,7,8,9]. Studies hebben aangetoond dat EMO verschillende kankercellen kan remmen, zoals menselijke colorectale adenocarcinoomcellen, hepatocarcinoomcellen, lymfoïde leukemiecellen [10] en menselijke tongkanker SCC-4 [11]. EMO kan de proliferatie van tumorcellen in maag-, borst- en prostaatkanker remmen [7, 12]. EMO vertoont echter geen cytotoxische effecten op normale cellen zoals normale menselijke gingivale fibroblasten [13], menselijke bronchiale epitheelcellen [14] en menselijke borstcellen [15]. Deze tonen aan dat EMO selectieve cytotoxiciteit vertoont ten opzichte van tumorcellen in vergelijking met normale cellen.
Chitosan, een natuurlijk polysacharide, is de gedeacetyleerde vorm van chitine. Dit natuurlijke polymeer heeft een uitstekende oplosbaarheid in water, biofunctionaliteit, bloedcompatibiliteit en microbiële afbreekbaarheid en staat bekend om zijn verschillende biomedische toepassingen. We hebben chitosan met hoog molecuulgewicht (450 kDa) afgebroken met chitosanase onder zure omstandigheden om chitosan-oligosaccharide met laag molecuulgewicht (CSO, 18 kDa) te verkrijgen. CSO kan celmembranen [16] sterk binnendringen en stearinezuur (SA) kan de kern binnendringen via de glycoproteïneroute. CSO werd hydrofoob gemodificeerd met SA met behulp van carbodiimide (EDC) als koppelingsreagens om amfipathisch stearinezuur-g-chitosan-oligosaccharide (CSO-SA) te synthetiseren.
Hoewel EMO een uitgebreide biologische activiteit heeft, is de antrachinonstructuur ervan slecht oplosbaar in water. Omdat therapeutische geneesmiddelen door de bloedbaan worden getransporteerd, heeft hun oplosbaarheid direct invloed op hun absorptie en distributie. CSO-SA-transplantaten kunnen zichzelf assembleren in een waterige oplossing om nanocellen te vormen die van binnen hydrofoob en van buiten hydrofiel zijn. We hebben de nanocellen uit de verzamelde staat verspreid met behulp van een ultrasone sonde. Omdat zowel EMO als CSO hydrofoob waren, werd EMO ingekapseld in het midden van de micellen.
Verschillende modelgeneesmiddelen worden toegepast op CSO-SA, waarvoor molecuulgewicht, structuur en hydrofobiciteit van modelgeneesmiddelen vereist zijn. Bestaande onderzoeken omvatten curcumine [17], doxorubicine [18], lamivudinestearaat [19] en oxaliplatine [20] die de antitumoreffecten aanzienlijk kunnen verbeteren. We onderzochten optimale beladingstoestanden van CSO-SA/EMO. CSO-SA/EMO creëert nieuwe doseringsvormen met een hogere oplosbaarheid en efficiënter gebruik. CSO-SA/EMO kan ideeën aandragen voor het selecteren van modelgeneesmiddelen of dragers en klinische toepassing van micellen.
Experimentele materialen en methoden
Experimentele materialen
BALB/C+/nu mannelijke naakte muizen werden verkregen van het Zhejiang University Experimental Animal Center. Maagkankercellijnen met lage differentiatie MGC803 en BGC823 werden gekocht bij de ATCC-celbank. RPMI-1640 kweekmedium en FBS werden verkregen van Hangzhou Holly Leaf Biotechnology Company. EMO, MTT, FITC, Hoechst 33342, DiR, trinitrobenzeensulfonzuur en pyreen werden geleverd door Sigma Aldrich. Zhejiang University heeft CSO-SA ingericht. Andere gekochte reagentia waren van AR-kwaliteit.
Bepaling van de CMC en 1 H NMR-spectra van CSO-SA
In dit rapport werd kritische micelconcentratie (CMC) van CSO-SA bepaald door fluorescentiespectrofotometrie met behulp van pyreen als een fluorescerende sonde. Verschillende concentraties CSO-SA-oplossing werden toegevoegd aan een pyreenacetonoplossing, waarna de aceton overnacht werd verdampt. De emissiespectra en piekwaarden van pyreen in CSO-SA-oplossingen van verschillende concentraties werden geanalyseerd met fluorescentiespectrofotometrie. De eerste piek (I 1 =374 nm) en de derde piek (I 3 =385 nm) van het spectrum werden geregistreerd. We hebben de logaritmische concentratie (Log C) uitgezet als de abscis en I 1 /Ik 3 als ordinaat en berekende de CMC voor de polymeermicellen.
CSO en CSO-SA werden opgelost in D2 O bij een concentratie van 10 mg/ml. 1 H NMR-spectra werden opgenomen, vergeleken en geanalyseerd op karakteristieke CSO- en CSO-SA-pieken.
Gedetecteerde aminesubstitutiegraad
De aminesubstitutiegraad (SD%) werd gedetecteerd met behulp van de trinitrobenzeenzwavelzuur (TNBS)-methode.
Er werden verschillende concentraties CSO- en CSO-SA-oplossingen bereid waarna 4% NaHCO3 en 0,1% TNBS werden achtereenvolgens toegevoegd. Na 2 uur incubatie bij 37°C in een waterbad, werd 2 mol/L zoutzuur toegevoegd. Absorptie werd gemeten bij 344 nm door ultraviolet-zichtbare spectrofotometrie na 30 min ultrasone trillingen. Er werd een standaardcurve getekend en het SD% van het CSO-SA-monster werd berekend.
CSO-SA-deeltjesgrootte en potentieel
Er werd een CSO-SA-oplossing van 1,0 mg/ml bereid en micellen werden volledig gedispergeerd met een ultrasone celverstorende sonde. De deeltjesgrootte en het potentieel van CSO-SA werden bepaald met een deeltjesgrootte- en oppervlaktepotentiaalanalysator.
Celopname van CSO-SA
FITC- en CSO-SA-oplossingen werden gemengd, overnacht geroerd en overgebracht naar een dialysezak. Niet-gereageerde FITC en absolute ethanol werden verwijderd door dialyse met gedeïoniseerd water gedurende 24 u. Ten slotte werd een FITC-gelabelde CSO-SA (FITC-CSO-SA) -oplossing met een concentratie van 1,0 mg / ml verkregen.
MGC803- en BGC823-cellen werden gebruikt als doelcellen om celopname van CSO-SA te onderzoeken. Op basis van de celproliferatiesnelheid werden cellen gezaaid in platen met 24 putjes en een nacht gekweekt totdat ze volledig hechtend werden. Tachtig μL FITC-CSO-SA-oplossing werd vervolgens op een bepaald tijdstip toegevoegd. Cellen werden gedurende 15 min geïncubeerd met 10 L Hoechst 33342 (1 mg / ml) om de celkern te kleuren. Opname van CSO-SA door FITC-CSO-SA werd gedetecteerd door confocale laser scanning microscopie.
In vivo distributie van CSO-SA
De verdeling van CSO-SA in vivo werd bepaald door DiR-fluorescerende kleurstofkleuring. CSO-SA/DiR-oplossing werd bereid door dialyse.
Als experimenteel model werden zes weken oude mannelijke naakte muizen gebruikt. Naakte muizen werden subcutaan ingeënt met 1 × 10 8 /mL MGC803-cellen. CSO-SA/DiR werd via de staartader toegediend met een tumorcelvolume van ongeveer 200 mm 3 . De muizen werden vervolgens op vaste tijdstippen verdoofd. Getimede distributie van CSO-SA/DiR in vivo werd opgenomen met behulp van een live body imager van kleine dieren (golflengtebereik, 580-700 nm, belichtingstijd 1000 ms).
Detectie van EMO-concentratie door HPLC
EMO-concentratie werd bepaald met HPLC. EMO werd aangebracht op een Eclipse XDB-C18 gepakte kolom (4,6 × 250 mm, 5 μm) met een beschermingskolom (4,6 × 10 mm, 5 μm). De kolomtemperatuur was ingesteld op 30 °C, de stroomsnelheid was 1,0 mL/min, de detectiegolflengte was 254 nm en het injectievolume was 20 μL. De mobiele fase was methanol/0,1% fosforzuur (85:15, v/v). De EMO-concentratie werd uitgezet als de abscis en het piekgebied als de ordinaat. Standaardkrommen van EMO werden getekend om het optimale lineaire bereik te bepalen. Alle HPLC-geïnjecteerde monsters werden gefilterd door een organisch filter van 0,45 m om de kolom te beschermen.
Voorbereiding van CSO-SA/EMO
In deze studie werd EMO ingekapseld met een ultrasone sonde. Een initiële formuleringsverhouding van 10% (EMO:CSO-SA, w/w) werd als uitgangspunt gebruikt. De EMO-oplossing werd langzaam druppelsgewijs toegevoegd aan de micellaire oplossing in een ijsbad. De ultrasone sonde werd vervolgens gedurende 20 cycli aangebracht (400 W, werk 2 s, stop 3 s).
De met geneesmiddel beladen micellen werden overgebracht naar een dialysezak (MWCO, 3,5 kDa) en 24 uur gedialyseerd tegen gedeïoniseerd water om ethanol uit het oplosmiddel te verwijderen. Pure CSO-SA/EMO werd verkregen door het dialysaat te centrifugeren om vrij EMO te verwijderen.
Eigenschappen van CSO-SA/EMO (Particle Diameter Potential, TEM, EE%)
De deeltjesgrootte en oppervlaktepotentiaal van CSO-SA/EMO werden gemeten met een deeltjesgrootte- en oppervlaktepotentiaalanalysator.
Een 0,1 mg/ml CSO-SA/EMO-oplossing werd druppelsgewijs toegevoegd aan een met koolstoffilm bedekte koperdraad, gekleurd met 2% fosfowolfraamzuur en gedroogd. De morfologie en deeltjesgrootte van CSO-SA/EMO werden waargenomen met transmissie-elektronenmicroscopie.
Beknellingsefficiëntie (EE%) en geneesmiddelbelading (DL%) van CSO-SA/EMO werden gedetecteerd door extractie met organisch oplosmiddel en HPLC. Aan een monster van 200 L van CSO-SA/EMO micellaire oplossing werd 1,8 l methanol toegevoegd om de micellen te dispergeren en het medicijn te extraheren. De EMO-concentratie werd gemeten als CEMO . Een andere 400 L CSO-SA/EMO micellaire oplossing werd in een ultrafiltratie centrifugebuis geplaatst en gecentrifugeerd (12.000 pm, 5 min) om het supernatant te verkrijgen. De EE% en DL% werden berekend volgens de volgende formules:
$$ \mathrm{EE}\%=\left(10\times {C}_{\mathrm{EMO}}-C\right)\times V/{M}_{\mathrm{EMO}}\times 100 \% $$$$ \mathrm{DL}\%=\left(10\times {C}_{\mathrm{EMO}}-C\right)\times \mathrm{V}/\left[\left( 10\times {C}_{\mathrm{EMO}}-C\right)\times V+{M}_{\mathrm{CSO}-\mathrm{SA}}\right]\times 100\% $$waar C EMO is de concentratie van EMO in micellen, C is de EMO-concentratie van de met geneesmiddel beladen micellen na ultrafiltratiecentrifugatie, V is het volume van met geneesmiddel beladen micel dat wordt gedialyseerd, M EMO is de hoeveelheid EMO die wordt toegediend tijdens het laden van medicijnen, M CSO-SA is de massa van CSO-SA.
Evaluatie van geneesmiddelafgifte in vitro
Geneesmiddelafgifte van CSO-SA/EMO werd onderzocht met behulp van PBS (pH 7,2) als afgiftemedium. Eén milliliter met geneesmiddel beladen miceloplossing werd in een dialysezak van 3,5 kDa geplaatst die aan beide uiteinden was afgesloten en vervolgens in een geschikt buisje met afgiftemedium geplaatst. De dialysezak werd in een horizontale thermostaatschudder van 37°C geplaatst. Monsters werden op vaste tijdstippen genomen en vervangen door hetzelfde volume vers afgiftemedium. Het gehalte aan EMO in de monsters werd bepaald door HPLC en de cumulatieve hoeveelheid vrijgekomen EMO werd berekend.
Cytotoxiciteit van CSO-SA/EMO
De overlevingspercentages van maagkankercellen die werden behandeld met CSO-SA/EMO, CSO-SA en EMO werden gedetecteerd met MTT-assay. Cellen werden gezaaid in platen met 96 putjes in een concentratie van ongeveer 10 5 /ml. CSO-SA/EMO, CSO-SA en EMO werden in verschillende concentraties toegevoegd. Na incubatie gedurende verschillende tijdsperioden werd 20 L MTT-werkoplossing toegevoegd. Na 4 uur incubatie werd 200 μL DMSO toegevoegd en werd de optische dichtheid (OD) van de oplossing bij 570 nm gemeten met een microplaatlezer.
Effect van CSO-SA/EMO op de celcyclus
Cellen van de twee cellijnen werden uitgezaaid in een plaat met 6 putjes met een dichtheid van 10 5 /ml. Na 12 uur kweken werden CSO-SA, CSO-SA/EMO en EMO toegevoegd en 24 uur geïncubeerd. De cellen werden vervolgens verteerd, verzameld en gewassen. Een 500 μL PI-kleuringsoplossing werd vervolgens aan elk celmonster toegevoegd, de celpellet werd langzaam opnieuw gesuspendeerd en de cellen werden gedurende 30 min in het donker bij 37 ° C geïncubeerd. Rode fluorescentie werd gedetecteerd door een flowcytometer bij een excitatiegolflengte van 488 nm. DNA-inhoud werd geanalyseerd door de FlowJo-software.
Antitumoreffecten van CSO-SA/EMO geëvalueerd door in vivo en histologische analyses
Dierproeven werden uitgevoerd volgens de Guidelines for Animal Care and Use Committee, Zhejiang University. MGC803-cellen (1 × 10 6 ) werden subcutaan geïnjecteerd in de rechter voorflank van mannelijke naakte muizen op een leeftijd van 5 tot 6 weken. Men liet tumoren groeien tot een diameter van ongeveer 5 mm. Op dat moment werden de muizen willekeurig verdeeld in een controlegroep, een EMO-injectiegroep en een CSO-SA/EMO-injectiegroep, met 3 dieren in elke groep. Alle muizen werden gedurende 2 weken eenmaal per dag intraveneus met de relevante reagentia via de staartader geïnjecteerd. Een elektronische schuifmaat werd gebruikt om de lange (a) en korte (b) diameters van de tumor (b) te meten. Het tumorvolume werd berekend volgens de formule V =a × b 2 /2. Het lichaamsgewicht van elke muis werd geregistreerd waarna de tumoren werden verzameld voor histologische analyse. De tumorremmingssnelheid werd bepaald in de tumorweefsels na kleuring met hematoxyline en eosine (HE). Terminale deoxynucleotide transferase dUTP nick-end labeling (TUNEL) werd uitgevoerd om cellulaire apoptose in terminaal ileumweefsel te detecteren met behulp van een in situ celdooddetectiekit volgens de instructies van de fabrikant.
Resultaten en discussie
CMC en 1 H NMR-spectra van CSO-SA
De amfifiele polymeren assembleerden zichzelf tot micellen in hydrofiel medium. Lagere CMC resulteerde in grotere micelvorming. Dit was gunstig voor het behoud van de micellenstructuur na intraveneuze toediening. Toen CSO-SA micellen vormde, kon de pyreen-fluorescerende sonde gemakkelijk de hydrofobe kern van de micellen binnendringen, waardoor de fluorescentie-intensiteit van het geladen pyreen toenam, wat de intensiteit van het emissiespectrum verhoogde. Op dit moment ik 3 aanzienlijk sneller gestegen dan I 1 , dus de ik 1 /Ik 3 fluorescentie-intensiteitsverhouding nam abrupt af. Een significant breekpunt kon worden waargenomen in de I 1 /Ik 3 plot en Log C-waarden (Fig. 1). Uit buigpuntberekeningen bleek dat de CMC 179,02 g/ml was. Hoe kleiner de CMC, hoe sterker het vermogen om micellen te vormen en hoe sterker de weerstand tegen verdunning, wat de bescherming van de micelstructuur na intraveneuze toediening verbeterde.
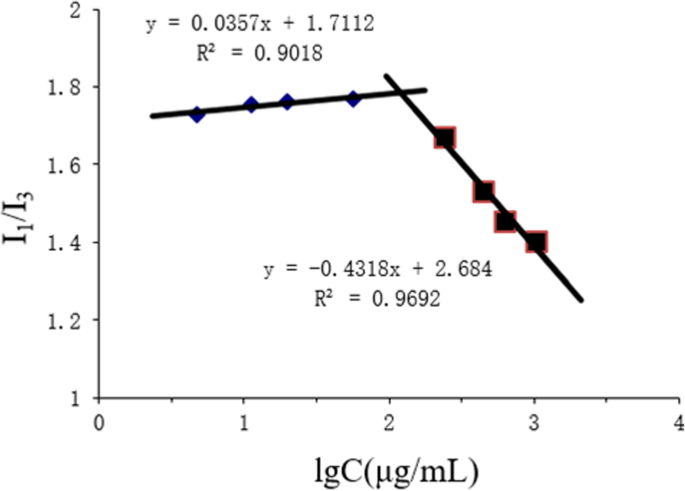
Variatie van fluorescentie-intensiteitsverhouding (I 1 /Ik 3 ) versus logaritmeconcentratie van CSO-SA
EDC werd gebruikt als een verknopingskoppelingsmiddel om te reageren met de carboxylgroep van SA en het actieve tussenproduct -OO-acylisoureumderivaat te vormen. Dit kan reageren met de primaire aminegroep van CSO om een amidebinding te vormen. De structuur van CSO-SA werd bepaald en bevestigd op basis van het kernspinresonantie-protonenspectrum. 1 H NMR (400 MHz, D2 O) δ 1,06 (m, CH2), 1,02 (m, CH3) komen respectievelijk overeen met het methyleenproton en methylproton van SA.
Vervangende graden van aminogroep
Het SD% van CSO-SA is het percentage stearinezuur-gesubstitueerde aminogroepen op chitosan. TNBS reageerde met vrije aminogroepen op chitosan en vormde trinitrobenzeenderivaten met een UV-absorptie bij 344 nm. De standaardcurve van het trinitrobenzeenderivaat van chitosan werd bepaald door UV-absorptie bij 344 nm. Het SD% van CSO-SA werd berekend op 9,3 ± 8%. Dit bevestigde dat CSO en SA met succes waren gekoppeld op basis van hun graft-ratio.
CSO-SA, CSO-SA/EMO deeltjesgrootte en potentieel
Tabel 1 laat zien dat het Z-gemiddelde van CSO-SA 139,3 ± 2,2 nm was. PDI was 0,179 ± 0,03, wat wijst op een relatief uniforme dispersie. Vergeleken met CSO-SA zijn het Z-gemiddelde en de PDI van CSO-SA/EMO gestegen. Na het laden van EMO was de positieve oppervlaktelading van CSO-SA/EMO hoger dan die van CSO-SA.
Celopname
FITC had geen invloed op de fysisch-chemische eigenschappen van CSO-SA. We hebben FITC-CSO-SA verkregen door fluoresceïne FITC te enten in CSO-SA. Nadat cellen waren gekleurd met Hoechst 33342, werd de opname van FITC-CSO-SA-cellen waargenomen met behulp van confocale laserscanmicroscopie. We ontdekten dat de opname van MGC803 geleidelijk toenam met toenemende tijd en dat de FITC-fluorescentie geleidelijk toenam. De micellaire opname van BGC823 was vergelijkbaar met MGC803 op een tijdsafhankelijke manier. FITC-CSO-SA had een goed celpenetrerend vermogen en was gelijkmatig verdeeld in het cytoplasma van maagkankercellen (Fig. 2).
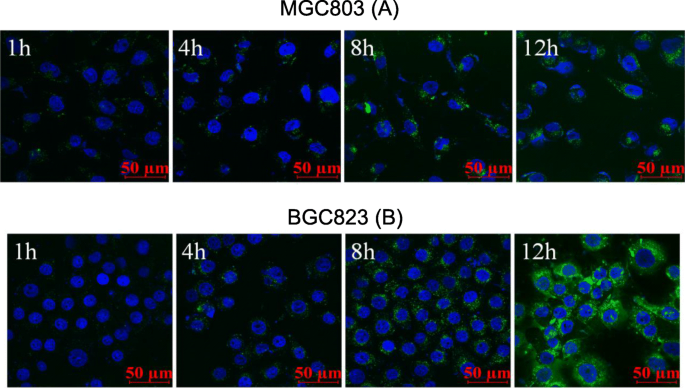
In vitro cellulaire tijdsafhankelijke opname van CSO-SA-micellen in MGC803 (a ) en BGC823 (b ) cellen voor respectievelijk 1, 4, 8, 12 h (blauw, Hoechst 33342; groen, FITC; schaalbalk =50 μm)
Distributie van CSO-SA in vivo
Nabij-infrarood (NIR) beeldvormingstechnologie is voordelig voor het doordringen van biomaterialen en weefsels. Nadat CSO-SA/DiR in de staartader van naakte muizen was geïnjecteerd, werd de verdeling van CSO-SA/DiR op verschillende tijdstippen waargenomen en vastgelegd met behulp van een beeldvormer van het levende lichaam van kleine dieren. Zoals getoond in Fig. 3, was de verdeling van CSO-SA / DiR vergelijkbaar met andere micellen op 4 uur na injectie in de staartader en werd voornamelijk verdeeld in de lever, milt en tumorweefsels. De verdeling van nanocellen in de tumor nam geleidelijk in intensiteit toe met toenemende tijd. Dit gaf aan dat CSO-SA-transplantaat een goed passief richtvermogen had, voornamelijk vanwege het EPR-effect van nanocellen (Fig. 3).
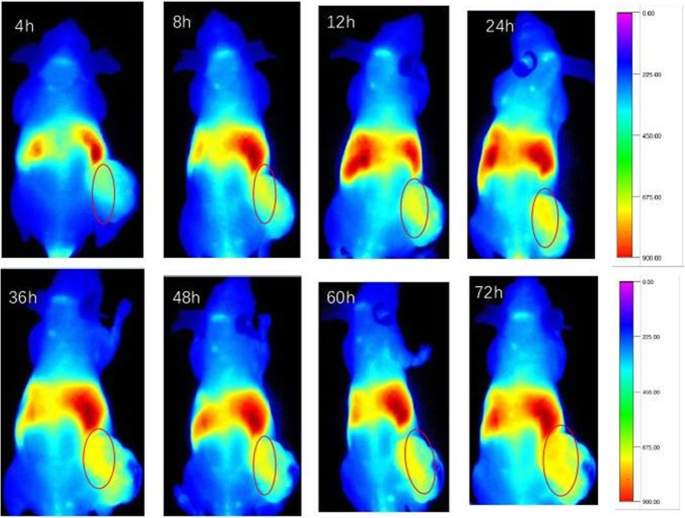
Hele lichaamsbeeld van CSO-SA/DiR op verschillende tijdstippen na i.v. injectie
Voorbereiding van CSO-SA/EMO
De invloed van verschillende pH-omgevingen op het laden van medicijnen
We hebben een CSO-SA-oplossing gemaakt en de pH van de CSO-SA aangepast om het effect van pH op het laden van geneesmiddelen te onderzoeken. Zoals getoond in Fig. 4, had CSO-SA een goede capaciteit voor het laden van medicijnen en vertoonde het een parabolische trend in het pH-bereik van -6,4-6,8. Het hoogste niveau van medicijnbelading werd gezien bij pH 6,6, waardoor deze waarde de optimale pH is voor medicijnbelading (Fig. 4).
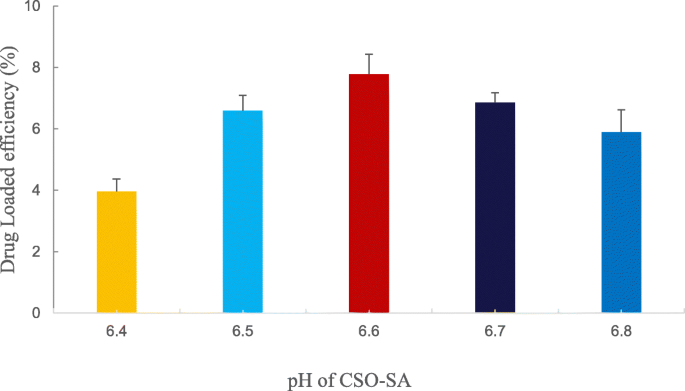
Effecten van verschillende pH-waarden van CSO-SA-transplantaten op het laden van geneesmiddelen. Gegevens worden weergegeven als gemiddelden ± SD (n =3)
Inkapselingsefficiëntie, TEM en laden van medicijnen
CSO-SA assembleert zichzelf tot shell-core nanocomposietmicellen. De hydrofobe delen vormen spontaan hydrofobe kernstructuren om de hydrofiele media af te weren. Deze structuur vormt een belangrijk vehikel voor het laden van geneesmiddelen, omdat EMO vanwege zijn hydrofobe structuur gemakkelijk kan worden ingekapseld in de hydrofobe kern. We onderzochten het effect van CSO-SA op de laadcapaciteit van EMO door de dosering van EMO te variëren. Zoals getoond in Fig. 5, neemt met toenemende EMO-dosering de hoeveelheid geneesmiddelbelading toe. De laadsnelheid van CSO-SA bereikte een hoogte van 21,16% wanneer de verhouding 30% was (Fig. 5).
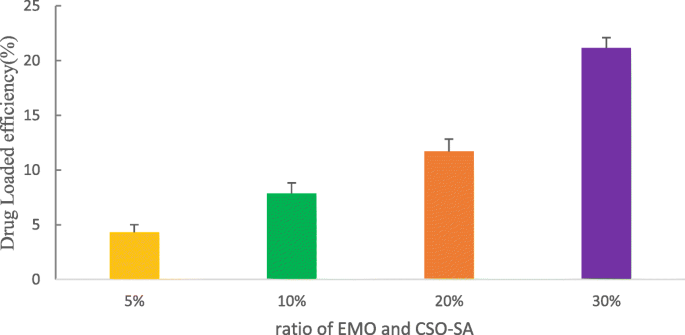
De invloed van verschillende verhoudingen van EMO en CSO-SA (5-30%) op medicijnbeladingen. Gegevens worden weergegeven als de gemiddelden ± SD (n =3)
CSO-SA/EMO werd 30.000 keer vergroot met een transmissie-elektronenmicroscoop. De vorm en grootte van de nanocellen werden waargenomen en vastgelegd.
EMO-release van CSO-SA/EMO
De met geneesmiddel beladen miceloplossing werd toegevoegd aan een dialysezak van 3,5 kDa waarbij PBS (pH> 7,2) werd gebruikt als afgiftemedium. Elke keer dat een monster werd verwijderd, werd het vervangen door hetzelfde volume vers afgiftemedium.
De concentratie EMO op verschillende tijdstippen werd bepaald met HPLC, waarna het cumulatieve afgiftepercentage werd berekend. Zoals getoond in Fig. 6, vertoonde CSO-SA/EMO een significant aanhoudende afgifte-effect vergeleken met vrij EMO. Deze resultaten laten zien dat het afgiftepercentage van vrije EMO 38,4% was bij 0,5 h, terwijl het afgiftepercentage van EMO van CSO-SA/EMO ongeveer 6,6% was. Na 4 h was het afgiftepercentage van vrije EMO 83,7% en het afgiftepercentage van CSO-SA/EMO ongeveer 32,5%. Binnen 72 h bereikte de afgifte van gratis EMO 97,2%, terwijl de afgifte van EMO door CSO-SA/EMO 78,4% was. EMO werd op twee manieren vrijgemaakt uit CSO-SA/EMO-medicijnbeladen micellen:door EMO-dissociatie van de micellaire kern en door penetratie van de micelkern in het afgiftemedium.
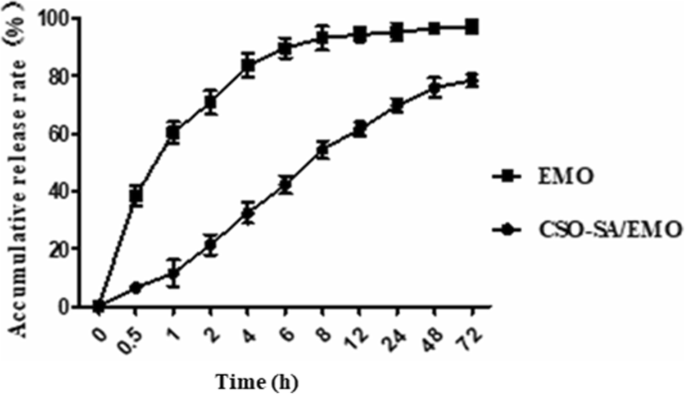
EMO-vrijgaveprofiel van CSO-SA/EMO over 72 h. Foutbalken in de grafiek vertegenwoordigen de standaarddeviaties (n =3)
Toxiciteit van CSO-SA/EMO voor maagkankercellen
De MTT-assay is een standaardmethode voor het detecteren van de levensvatbaarheid van cellen. De cytotoxiciteit van vrije EMO, CSO-SA en CSO-SA/EMO voor MGC803 en BGC823 maagkankercellen werd gemeten met behulp van de MTT-assay. Het toonde aan dat EMO en CSO-SA/EMO MGC803- en BGC823-cellen op een dosis- en tijdsafhankelijke manier konden remmen. Bij dezelfde concentratie had CSO-SA/EMO echter een sterker remmend effect op MGC803- en BGC823-cellen in vergelijking met de vrije EMO-oplossing. De IC50 waarden (Tabel 2) van EMO en CSO-SA/EMO voor maagkankercellen werden berekend. De IC50 van CSO-SA/EMO was significant lager dan die van EMO op elk tijdstip (24 h, 48 h, 72 h). De IC50 waarden van CSO-SA toonden aan dat CSO-SA een veilige biologische drager was met weinig biologische toxiciteit, wat bevestigde dat de cytotoxiciteit van CSO-SA/EMO werd veroorzaakt door EMO (Fig. 7).
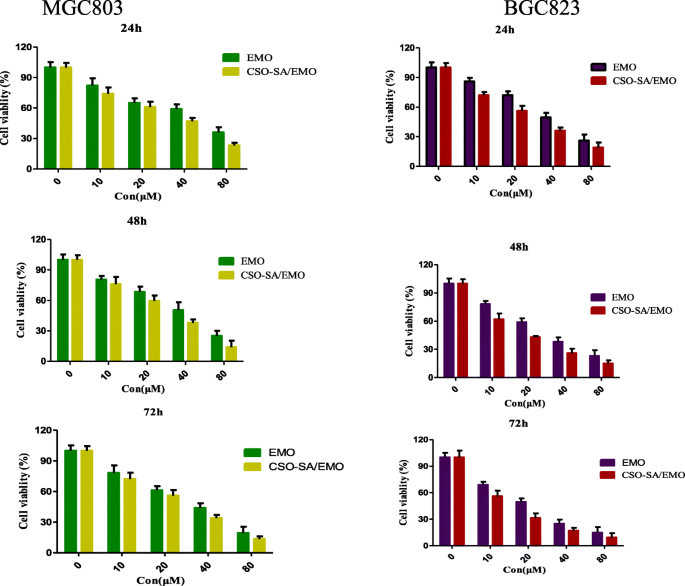
Levensvatbaarheid van de cellen van MGC803 en BGC823 maagkankercellen behandeld met CSO-SA, EMO en CSO-SA/EMO gedurende 24 h, 48 h en 72 h. Gegevens worden weergegeven als de gemiddelden ± SD (n =3)
Tabel 2 en Fig. 7 toonden aan dat de cytotoxiciteit van het CSO-SA/EMO geneesmiddelafgiftesysteem significant hoger was dan die van vrij EMO. Toen echter de afgifte van CSO-SA/EMO en vrije EMO in een in vivo omgeving werd gesimuleerd, bereikte de afgifte van vrije EMO 38,4% bij 0,5 h, terwijl de afgifte van CSO-SA/EMO slechts 6,6% was. Over het algemeen was de concentratie van vrije EMO op elk tijdstip hoger dan die van CSO-SA/EMO.
Dit fenomeen is gemakkelijk te verklaren. Hoewel CSO-SA/EMO EMO relatief langzaam afgeeft, vertraagt of neemt het antitumoreffect van CSO-SA/EMO niet af. Veel onderzoeken hebben aangetoond dat nanodrug-afgiftesystemen de antitumoractiviteit van chemotherapiemedicijnen kunnen verbeteren [21].
Ten eerste, hoewel vrij EMO een aanvankelijke uitbarsting van activiteit vertoont, kan EMO niet efficiënt door de cellen worden opgenomen, terwijl CSO-SA de celopname aanzienlijk versnelde via endocytose of fagocytose.
Ten tweede, wanneer CSO-SA/EMO de celmembranen nadert, kan de interactie tussen nanodeeltjes en celmembranen de structuur en eigenschappen van nanocellen beïnvloeden, evenals de functie van biologische macromoleculen zoals ionenkanalen. Daarom resulteert de hechting van CSO-SA/EMO aan de celmembranen niet in een eenvoudige fysieke adsorptie, maar kan het de dynamische balans van de cel veranderen en daardoor de cytotoxiciteit van CSO-SA/EMO verder bevorderen.
Ten slotte heeft vrij EMO een hydrofobe antrachinonstructuur, wat resulteert in een slechte verdeling in het bloed. Het CSO-SA/EMO-medicijnafgiftesysteem verhoogt de oplosbaarheid van EMO en verbetert de oplossing, wat leidt tot een hogere moleculaire concentratie in de omringende cellen.
Detectie van celcyclusstop door FCM
Celcyclusanalyse is een belangrijk aspect van de klinische behandeling van kwaadaardige tumoren. Het is aangetoond dat toepassing van cyclusspecifieke geneesmiddelen op tumorcellen tijdens geneesmiddelgevoelige perioden een grote werkzaamheid heeft. Hoewel ethidiumbromide-analogen niet in normale cellen kunnen doordringen, kunnen ze celkernen kleuren door beschadigde celmembranen binnen te dringen. In PI ingebed dubbelstrengs DNA produceert rode fluorescentie en de fluorescentie-intensiteit is evenredig met het niveau van dubbelstrengs DNA. Het DNA-gehalte werd bepaald met flowcytometrie (FCM) na DNA-kleuring met PI. Celcyclusdistributie en apoptose werden geanalyseerd op basis van DNA-inhoudsdistributie.
Studies hebben aangetoond dat EMO de verdeling van de celcyclus beïnvloedt [11, 22]. FCM-analyse toonde aan dat CSO-SA/EMO en EMO MGC803- en BGC823-cellen in de G2/M-fase van de celcyclus konden blokkeren.
MGC803-cellen werden 24 uur lang blootgesteld aan dezelfde concentratie (20 M) CSO-SA, vrije EMO en CSO-SA/EMO-oplossing. Het percentage MGC803-cellen in de G2/M-fase bleek respectievelijk 8,95%, 15,29% en 23,12% te zijn. Het percentage controlegroep was 6,47%. De percentages BGC823-cellen in G2/M behandeld met 20 μM CSO-SA, vrije EMO of CSO-SA/EMO onder dezelfde omstandigheden waren respectievelijk 14,25%, 16,79% en 35,71%, wat hogere waarden waren dan in de controlegroep (13,66%). Deze gegevens toonden aan dat CSO-SA/EMO de G2/M-fase van MGC803- en BGC823-cellen efficiënter en significanter blokkeerde dan vrij EMO bij dezelfde concentratie. De CSO-SA toonde geen verschil met de controles (Fig. 8).
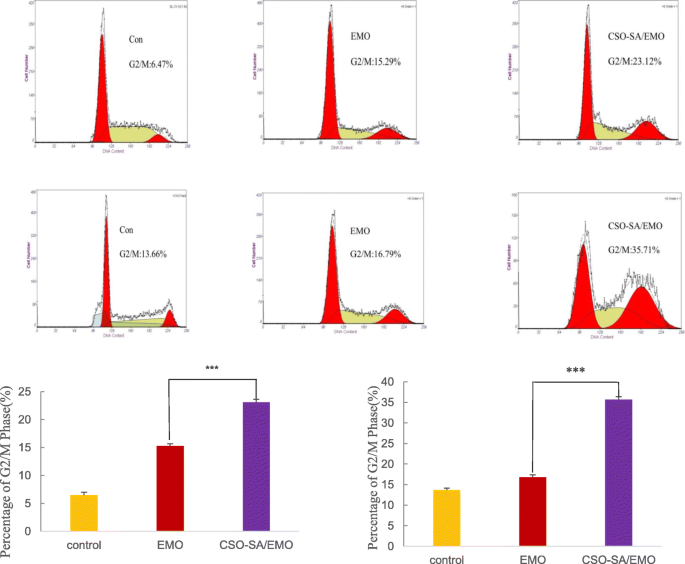
Celcyclusverdelingen van MGC803- en BGC823-cellen behandeld met EMO en CSO-SA / EMO gedurende 24 h. Studenten t test is berekend en de gegevens worden weergegeven als de gemiddelden ± SD (n =3), (*p <0,05, ** p <0,005, *** p <0,001)
Antitumoreffect van CSO-SA/EMO in vivo
Om het antitumoreffect van CSO-SA/EMO verder te bestuderen, werden de tumorremmingssnelheid en cellulaire apoptoseniveaus in vivo geëvalueerd. De resultaten toonden aan dat zowel CSO-SA / EMO als EMO een opmerkelijk remmend effect hadden op de tumorgroei (figuur 9a). De tumorremmingssnelheid van de CSO-SA / EMO-groep was driemaal die van de EMO-groep (figuur 9d). Het gewicht van muizen in elke groep veranderde niet significant (Fig. 9b). Hieruit bleek dat zowel CSO-SA/EMO als EMO relatief veilig waren. Morfologische veranderingen en apoptose in tumorweefsels van elke groep toonden aan dat CSO-SA/EMO significante antitumoreffecten had (Fig. 9e, f).
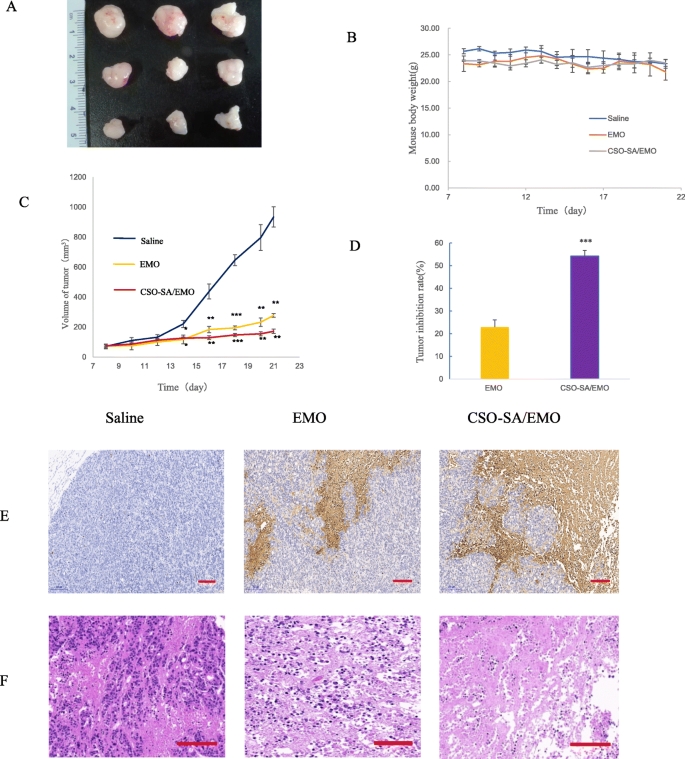
Antitumoreffect van CSO-SA/EMO in vivo. een Tumorvorm in elke groep. b Muis lichaamsgewicht in elke groep. c Tumorvolume in elke groep. d Tumorremmingspercentage. e Representatieve afbeeldingen van TUNEL-gekleurd tumorweefsel van elke groep (schaalbalk =200 m). v Representatieve afbeeldingen van HE-gekleurd tumorweefsel van elke groep (schaalbalk =200 m)
Conclusies
In deze studie hebben we structuur, CMC, SD%, deeltjesgrootte en potentieel van CSO-SA gedetecteerd met verschillende methoden. Resultaten bewijzen dat amfifiele CSO-SA goed presteerde als drager. Fluorescentie-intensiteit van maagkankercellen toonde aan dat CSO-SA binnen 12 uur snel was opgenomen. Nude mice were used as a model to study the distribution of CSO-SA within 72 h. Over time, CSO-SA distribution in lesion became more concentrated exhibiting a good passive targeting effect.
CSO-SA/EMO was prepared with ultrasound-dialysis method. CSO-SA had strong drug-loading capacity. When environment pH was set at 6.6, the level of drug loading reached 21.6% at a 30% formulation ratio. Compared with CSO-SA, CSO-SA/EMO had bigger particle size and zeta potential. The shape of CSO-SA/EMO could be recorded directly using TEM. The release of EMO from CSO-SA/EMO was 78.4% within 72 h, it indicated a smooth and continuous process in body. Considering the antitumor effect of CSO-SA/EMO compared with free EMO, we confirmed it with various experiments.
CSO-SA toxicity to gastric cancer cells was detected by MTT assay. The results showed that CSO-SA was a safe biological carrier. Compared with that of free EMO, CSO-SA/EMO significantly enhanced the antitumor activity against gastric cancer cells. MGC803 and BGC823 cell cycle could be arrested in the G2/M phase more effectively by CSO-SA/EMO. Tumor volume, HE staining, and TUNEL assay proved more significant antitumor effect of CSO-SA/EMO than free EMO.
Based on above results, CSO-SA is both biocompatible and safe carrier. CSO-SA/EMO in this study utilizes a new and effective dosage formulation for the treatment of cancer and exhibits good passive targeting effect in vivo.
Beschikbaarheid van gegevens en materialen
Alle gegevens die tijdens dit onderzoek zijn gegenereerd of geanalyseerd, zijn opgenomen in dit gepubliceerde artikel.
Afkortingen
- CSO-SA:
-
Chitosan oligosaccharide-stearic acid
- EMO:
-
Emodin
- FITC:
-
Fluoresceïne isothiocyanaat
- MTT:
-
Thiazolylblauwtetrazoliumbromide
- TEM:
-
Transmissie-elektronenmicroscoop
- 1 H NMR:
-
Proton nuclear magnetic resonance
- EPR:
-
Enhanced permeability and retention
- TCM:
-
Traditional Chinese medicine
- CMC:
-
Critical micelle concentration
- Log C:
-
Logarithm of concentration
Nanomaterialen
- Preparatie en magnetische eigenschappen van kobalt-gedoteerde FeMn2O4-spinel-nanodeeltjes
- Analyse van actine en focale adhesieorganisatie in U2OS-cellen op polymeernanostructuren
- Op weg naar TiO2-nanovloeistoffen:deel 1:voorbereiding en eigenschappen
- Voorbereiding en verbeterde katalytische hydrogeneringsactiviteit van Sb/Palygorskite (PAL) nanodeeltjes
- Nieuwe biocompatibele Au Nanostars@PEG-nanodeeltjes voor in vivo CT-beeldvorming en eigenschappen voor nierklaring
- Synthese van ZnO-nanokristallen en toepassing in omgekeerde polymeerzonnecellen
- Voorbereiding en fotokatalytische prestaties van LiNb3O8-fotokatalysatoren met holle structuur
- Bereiding van palladium(II)-ion-imprinted polymere nanosferen en de verwijdering van palladium(II) uit waterige oplossing
- Voorbereiding en thermo-elektrische kenmerken van ITO/PtRh:PtRh Thin Film Thermokoppel
- Frequentie-gemoduleerde golfdiëlektroforese van blaasjes en cellen:periodieke U-bochten bij de crossover-frequentie
- Fabrikatie en fotokatalytische eigenschap van nieuwe SrTiO3/Bi5O7I nanocomposieten



