Orale toediening van met resveratrol geladen vast lipide nanodeeltje verbetert de insulineresistentie door gerichte expressie van SNARE-eiwitten in vet- en spierweefsel bij ratten met diabetes type 2
Abstract
In de huidige studie hebben we resveratrol (RES)-geladen vaste lipide nanodeeltjes (SLN-RES) ontwikkeld om de insulineresistentie te verbeteren door de opregulatie van het SNARE-eiwitcomplex bij ratten met type 2-diabetes. De SLN-RES-kenmerken omvatten het volgende:de gemiddelde grootte van 248 nm, de zeta-potentiaal van − 16,5 mV en 79,9% RES-insluitingsefficiëntie. Het afgifteprofiel van SLN-RES toonde een aanvankelijke uitbarsting gevolgd door een aanhoudende afgifte in natuurlijke toestand. Resultaten van infraroodspectroscopie lieten een goede opname van RES in kern SLN zien. Sferische nanodeeltjes met minder aggregatie werden waargenomen onder elektronisch microscopisch onderzoek. Orale toediening van SLN-RES verhinderde gewichtsverlies en vertoonde een beter hypoglycemisch effect dan RES. Serum oxidatieve stress status werd hersteld naar het normale niveau door SLN-RES. Bovendien werd de expressie van synaptosomaal-geassocieerd eiwit 23 (Snap23), syntaxine-4 (Stx4) en vesikel-geassocieerd membraaneiwit 2 (Vamp2) als de belangrijkste elementen van het SNARE-eiwitcomplex significant verminderd door SLN-RES dan behandeling met RES in spierweefsel. SLN-RES heeft echter een vergelijkbaar effect als RES-behandeling in vetweefsel. Al met al onthulden onze resultaten dat SLN-RES een moderne en interessante therapeutische benadering zou kunnen zijn voor de verbetering van insulineresistentie door zich te richten op de expressie van Snap23, Stx4 en Vamp2 in vet- en spierweefsel.
Presentatie van de hypothese
De inkapseling van resveratrol (RES) in lipide-kern-nanodeeltjes versterkte de voordelen ervan door de stabiliteit en orale intestinale absorptie te verbeteren wanneer oraal geconsumeerd. SLN-RES verbetert de insulineresistentie meer dan RES. Het antioxiderende effect van RES neemt toe wanneer het wordt opgenomen in SLN's.
De hypothese testen
Spectroscopische analyse van SLN-RES werd uitgevoerd om de werkzaamheid van inkapseling te bepalen. De tweede hypothese was om het effect van SLN-RES-behandeling op de oxidatieve stressparameters en het hypoglycemische effect ervan tegen diabetes type 2 in diermodellen te evalueren.
Implicaties van de hypothese
Verhoogde stabiliteit en intestinale absorptie leiden tot de biologische beschikbaarheid van RES bij orale toediening. Verhoogde biologische beschikbaarheid van RES bij opname in SLN's leidt tot een verhoogde concentratie van RES in beoogde weefsels. Verhoogde concentratie van RES in beoogde weefsels leidt tot meer hypoglycemisch effect van RES wanneer opgenomen in SLN's dan RES.
Achtergrond
Diabetes mellitus type 2 is een stofwisselingsziekte die wordt gekenmerkt door insulineresistentie. Insulineresistentie wordt voornamelijk ontwikkeld door de verstoring van het glucosetransportsysteem (GLUT 2 en 4) in spier- en vetweefsel [1]. De SNARE-eiwitten immobiliseerden het GLUT 4-systeem aan het celmembraan en spelen een belangrijke rol bij de membraantransport, koppeling en vesikelfusie. Het synaptosomaal-geassocieerde eiwit 23 (SNAP-23), syntaxine-4 (STX4) en vesikel-geassocieerd membraaneiwit 2 (VAMP-2) staan bekend als de belangrijkste component van het SNARE-eiwitcomplex [2]. Eerdere rapporten identificeerden dat de neerwaartse regulatie van SNARE-eiwitten de insulineresistentie versnelt [3]. In de afgelopen jaren heeft een groot aantal gegevens aangetoond dat kruidencomponenten veel gunstige effecten hebben die veel stofwisselingsstoornissen kunnen verbeteren [4,5,6]. Onderzoekspoging van Côté et al. toonde aan dat de acute intraduodenale infusie van RES-gecompenseerde insulineresistentie via afnemend duodenaal SIRT1-eiwit en verminderde leverglucoseproductie in het rattenmodel [4]. Het is ook, Gencoglu et al. rapporteerde dat de intraperitoneale toediening van RES de insulineresistentie bij diabetische ratten verlichtte door de expressie van visfatine te normaliseren en de SIRT1-expressie in skeletspieren te verhogen. RES-voeding leidt tot verhoogde GLUT4- en GLUT2-expressie bij streptozotocine-geïnduceerde diabetes bij ratten. Over het algemeen gaven deze bevindingen nieuwe inzichten in de gunstige effecten van RES-suppletie tegen insulineresistentie. Ondanks de veelbelovende therapeutische toepassing leiden lage intestinale absorptie en gastro-intestinale afbraak voornamelijk tot een lage biologische beschikbaarheid van RES bij orale toediening [7].
In de afgelopen jaren biedt nanogeneeskunde een intelligente benadering voor de toediening van medicijnen van veel medicijnen om de lage biologische beschikbaarheid, slechte stabiliteit en verbetering van targetingstrategieën te overwinnen [8]. Als zodanig zijn micellen, liposomen, polymere nanodeeltjes en vaste lipide-nanodeeltjes (SLN's) de meest bekende medicijnafgiftesystemen [9, 10]. Recente onderzoeken hebben aangetoond dat het opnemen van RES in toedieningssystemen op nanoschaal een handige methode is om de beperking ervan te omzeilen en bij klinische pogingen effectiever zou kunnen zijn dan de pure suspensie van geneesmiddelen [11]. Recent bewijs toonde aan dat de opname van geneesmiddelen in vaste lipide-nanodeeltjes (SLN's) de biologische beschikbaarheid van RES zou kunnen verhogen bij orale toediening [11, 12]. Frozza et al. toonde aan dat nano-inkapseling van RES het neuroprotectieve effect tegen de ziekte van Alzheimer verbeterde door de concentratie van geneesmiddelen in het hersenweefsel te verhogen [13]. Volgens de eerdere rapporten die hierboven werden genoemd, is voorgesteld dat de inkapseling van RES in lipide core nanodeeltjes de insulineresistentie beter kan verbeteren dan RES door de verhoging van de orale biologische beschikbaarheid.
Het huidige werk was gericht op de ontwikkeling, optimalisatie en karakterisering van met RES geladen SLN (SLN-RES) met het oog op het verbeteren van de orale biologische beschikbaarheid ervan. Daarom hebben we in de huidige studie SLN-RES voorbereid en geprobeerd de eigenschappen ervan te bepalen. Vervolgens werd het effect van orale behandeling van SLN-RES op de nuchtere bloedsuikerspiegel (FBS), insuline en oxidatieve stressparameters geëvalueerd bij ratten met type 2-diabetes. Verder onderzochten we het effect van orale toediening van SLN-RES op de genexpressie van Snap23, Stx4 en Vamp2 in vet- en spierweefsel.
Materialen en methoden
Materialen
Trans-resveratrol (> 99%) werd geleverd door Mega Resveratrol (VS), streptozotocine (STZ) en nicotinamide (NA) werden gekocht bij Sigma-Aldrich (Duitsland) en de gehydrogeneerde sojalecithine (S100) werd cadeau gegeven door Lipoid KG (Ludwigshafen, Duitsland). Gehydrogeneerde palmolie (S154) werd cadeau gedaan door Condea (Witten, Duitsland), en TRIzol-reagens en cDNA-synthesekit werden geleverd door Invitrogen (VS). Insuline Rat ELISA Kit werd gekocht bij Bio-Equip (China). Andere producten en oplosmiddelen werden gebruikt in analytische kwaliteit.
Voorbereiding van SLN-RES
SLN-RES werd geproduceerd volgens de vorige studie met kleine aanpassingen [14]. In het kort werden 40 mg S100 en 1 g sorbitol toegevoegd aan een 15 ml gedestilleerd water en werden verwarmd tot 70 °C als de waterige fase. De organische fase met 100 mg S154, 70 mg S100 en RES werd gesmolten bij 70 °C en vervolgens werd 5 ml chloroform toegevoegd als een organisch oplosmiddel. Vervolgens werd de organische fase snel gemengd met de voorverwarmde waterige fase onder roeren bij 1000 rpm/min totdat het organische oplosmiddel was verwijderd. De resulterende suspensie werd gesoniceerd gedurende 2 min en vervolgens geïnjecteerd in koud water (2 °C) onder continu roeren bij 1000 tpm/min gedurende 2 u om de lipidematrix snel te laten stollen. Vervolgens werd het monster in donkere toestand gehouden totdat het was gedroogd. Het resulterende monster werd tweemaal gewassen met gedestilleerd water door centrifugeren om het supernatant dat het vrije geneesmiddel bevatte te verwijderen. De supernatanten werden onderworpen aan meting van de invangefficiëntie ( EE). Een reeks SLN werd bereid door een andere hoeveelheid pure RES (30, 50 en 70 mg) toe te voegen aan de gesmolten lipidefase om een hoge EE te bereiken. Het effect van RES-lading op de gemiddelde deeltjesgrootte, polydispersiteitsindex (PDI), oppervlaktelading (zeta-potentiaal) en EE van SLN's werd geëvalueerd (tabel 1).
Karakterisering van SLN-RES
De nanodeeltjes met gemiddelde diameter, zeta-potentiaal en PDI van SLN-RES werden gemeten door laserdiffractie (Zetasizer Nano-ZS; Malvern Instrument, VK). Karakterisering werd uitgevoerd na SLN-RES-verdunning in gedestilleerd water (1/30).
Entrapment-efficiëntie
EE-waarde wordt gedefinieerd als het percentage gevangen RES in SLN ten opzichte van de totale RES met behulp van de volgende vergelijking. De hoeveelheid ingevangen RES werd bepaald door vrij RES te scheiden van ingekapseld RES. Vrije RES werd gekwantificeerd met behulp van een UV-spectrofotometer bij 310 nm.
$$ \mathrm{EE}\%\kern0.5em =\kern0.5em \left[\left(\mathrm{weight}\kern0.5em \mathrm{of}\kern0.5em \mathrm{total}\kern0. 5em \mathrm{drug}-\mathrm{weight}\kern0.5em \mathrm{of}\kern0.5em \mathrm{untrapped}\kern0.5em \mathrm{drug}\right)/\left(\mathrm{weight }\kern0.5em \mathrm{of}\kern0.5em \mathrm{total}\kern0.5em \mathrm{drug}\right)\right]\times 100 $$In vitro onderzoek naar geneesmiddelafgifte
Het in vitro geneesmiddelafgiftepatroon van RES werd als volgt geanalyseerd. Het bereide SLN-RES werd onder roeren opgelost in plasmamedium bij pH -7,4 en 1,2. Op de gedefinieerde tijdstippen (0,5, 1, 2, 4, 6 en 8 h) werd de gedefinieerde hoeveelheid medium onttrokken en vervolgens gefilterd door een 0,24-μm spuitfilter voor de kwantificering van de vrije vorm van RES. De gefilterde RES vertegenwoordigde de hoeveelheid RES die vrijkwam in het medium.
Transmissie-elektronenmicroscopie
Morfologische karakterisering werd geëvalueerd door transmissie-elektronenmicroscopie (TEM). In het kort, SLN-RES werd uitgespreid op een met koolstof gecoat koperen rooster en bekeken onder TEM ZEISS. Oppervlaktemorfologie, aggregatie en onregelmatigheid van SLN-RES werden gekarakteriseerd.
Fourier Transform Infraroodspectroscopie
Het S100-, RES- en gedroogde monster van SLN en SLN-RES werden geanalyseerd om hun intermoleculaire interacties en oppervlaktechemiekarakterisering van nanodeeltjes te bevestigen door Fourier-transformatie-infraroodspectroscopie (FTIR), met behulp van een infraroodspectrometer (FTIR PerkinElmer, VS). De spectra werden verkregen in het bereik van 400 en 4000 cm −1 . De gedroogde monsters werden bereid met KBr om pellets te vormen.
Ontwerp dierenonderzoek
Twintig mannelijke Wistar-ratten (200-250 g) werden geleverd door het Animal House of Razi Institute (Iran). De dieren werden behandeld volgens de protocollen die zijn goedgekeurd door de ethische commissie van de Hamadan University of Medical Sciences. Ratten werden gevoed met vers water en een standaard voer en onder gecontroleerde omstandigheden gehouden (25 ± 2 °C en 12 uur licht/donker cycli aansteken). Type 2-diabetes werd geïnduceerd door intraperitoneale injectie van STZ 65 mg / kg (0,1 M in natriumcitraat; pH, 4,5) en nicotinamide 110 mg / kg in een enkele dosis [15]. Het FBS-niveau werd na 3 dagen gemeten. Ratten met glucosespiegels boven 150 werden beschouwd als diabetische modellen. Na een week werden RES en SLN-RES in poedervorm opgelost in gedestilleerd water en dagelijks oraal toegediend via een sonde gedurende 1 maand. De dieren werden willekeurig verdeeld in vier groepen van 5 ratten in elke groep:HC, gezonde controle; DC, diabetescontrole; RES, diabetische rat behandeld met 10 mg/kg resveratrol oraal; en SLN-RES, diabetische rat die oraal werd behandeld met met resveratrol beladen vaste lipidenanodeeltjes (gepoederd SLN-RES-monster met 10 mg / kg RES). Aan het einde van het onderzoek werden de dieren gewogen en vervolgens intraperitoneaal verdoofd met ketamine en xylazine (respectievelijk 100 mg/kg en 10 mg/kg). Daarna werd bloed verzameld uit een hartpunctie en serum gescheiden en bewaard bij -20 ° C. Vervolgens werden skeletspieren en visceraal vetweefsel geoogst en onmiddellijk ingevroren en bewaard bij -80 °C voor verdere analyse.
Meting van nuchtere bloedsuiker
De FBS werd gemeten met een colorimetrische testkit (Pars Azmun, Iran).
De meting van seruminsuline
Het insulineniveau in het serum werd gemeten met een commerciële ELISA-kit (Bio-Equip, China) volgens de instructies van de fabrikant. Insulineresistentie werd berekend met behulp van de homeostase model assessment (HOMA) formule.
Totale antioxidantcapaciteit
Het vermogen van het monster om ijzer (Fe +3 ) naar ferro (Fe +2 ) werd bepaald als de totale antioxidantcapaciteit (TAC). De reactie tussen Fe 2+ en 2,4,6-Tri(2-pyridyl)-s-triazine (TPTZ) leidt tot een blauw gekleurd complex [16].
Totaal Thiol-groep
Totale thiolgroepen (-SH) werden gemeten met behulp van 5,5'-dithiobis(2-nitrobenzoëzuur) (DTNB) reagens. Dit reagens reageert met thiolgroepen om een geelgekleurd complex te produceren [17].
Lipideperoxidatietest
Malondialdehyde (MDA) als eindproduct van het lipideperoxidatieproces werd gemeten met behulp van de colorimetrische methode. De geperoxideerde lipiden reageren met thiobarbituurzuur (TBA) en produceren een roze gekleurd complex. 1,1,3,3-Tetraethoxypropaan werd als standaard gebruikt [18].
Totale oxidatieve status
Het oxidatiepotentieel van het monster werd gemeten met de totale oxidantstatus (TOS)-methode. In het kort, Fe +3 en xylenol oranje produceren een gekleurd complex, in een zure toestand. De test is gekalibreerd met H2 O2 , en de resultaten werden uitgedrukt in μM H2 O2 equivalent/L [19].
Kwantitatieve omgekeerde transcriptie polymerase kettingreactie
Kwantitatieve reverse transcriptie polymerase kettingreactie (qRT-PCR) werd uitgevoerd om de genexpressie van Snap23, Stx4 en Vamp2 te bepalen. Totaal mRNA werd geëxtraheerd uit snel ingevroren vet- en spierweefsel met behulp van TRIzol-reagens. De kwantiteit en kwaliteit van het mRNA werden bepaald met behulp van een NanoDrop UV-spectrofotometer (BioTek Laboratories, Inc., VS). Het mRNA werd omgekeerd getranscribeerd naar cDNA met behulp van de RevertAid First Strand cDNA Synthesis Kit. Kwantitatieve amplificatie werd uitgevoerd met specifieke primersequenties met behulp van het CFX96 real-time PCR-detectiesysteem. De voorwaartse en achterwaartse primers werden respectievelijk gebruikt voor genamplificatie:5'-dTTCCGTTTCTGTGTCCAATAG en 5'-dTTGTGCTTTCCAGAGACTCAT voor Snap23, 5'-dTCAGCAGACTATGTGGAAC en 5'-dCCAAGATGAGAACAGTGACAGA voor Stx4 en 5'-dCTAGAGAATCCAGGTCCAT2. Relatieve verandering van genexpressie werd berekend volgens 2 -ΔΔCt formule. 18s rRNA als huishoudgen werd gebruikt. Alle experimenten werden in drievoud uitgevoerd.
Statistische analyse
Statistische analyse werd uitgevoerd met behulp van SPSS 16 en GraphPad Prism 6.00-software, LaJolla, CA (VS). Gegevens werden uitgedrukt als gemiddelde ± standaarddeviatie (SD). Eenrichtingsanalyse van variantie (ANOVA) werd gebruikt om verschillen tussen groepen te vergelijken. p < 0,05 werd als significant niveau beschouwd.
Resultaten en discussie
Fysisch-chemische karakterisering van SLN-RES
Zoals te zien is in tabel 1, waren de deeltjesgrootte en PDI-waarde bijna constant toen de verhouding tussen geneesmiddel en lipide toenam, wat te wijten kan zijn aan de vorming van meerdere fosfolipidelagen in SLN [11]. Het groottebereik van het huidige nanodeeltje was ongeveer 250 nm, wat geschikt zou kunnen zijn voor intestinale absorptie en bypass-lever- en miltfiltratiesysteem [20]. Dit groottebereik kan ook leiden tot een verhoogde biologische beschikbaarheid van RES door een langere circulatietijd van SLN-RES en een verlengde afgifte van geneesmiddelen. De ontwikkeling van nanodeeltjes met kleinere afmetingen en PDI-waarde kan hun intestinale absorptie vergemakkelijken. Als suggestie zou de modificatie van SLN met polyethyleenglycol (PEG) onze formulering kunnen verbeteren om hun permeabiliteit en systemische circulatietijd te verbeteren [21].
Zoals weergegeven in tabel 1 wordt aangenomen dat de PDI-waarde van 0,4 heterogeen is verdeeld, wat de aanwezigheid van agglomeraten uitdrukt. In SLN-RES-30 helpt de verhoging van het RES-gehalte om de kans te vergroten om in de SLN te worden ondergebracht, hoewel het EE-percentage duidelijk was afgenomen, gevolgd door een toename van het geneesmiddelgehalte in de SLN-RES-70-formulering. Er werd geconcludeerd dat een verhoogd lipidengehalte in SLN-RES-70 niet voldoende is om alle hoeveelheden RES in de SLN-matrix op te nemen [22]. Dus werd SLN-50 geselecteerd als de geoptimaliseerde formulering voor verder onderzoek.
Zeta-potentiële resultaten toonden een negatieve oppervlaktelading (− 16.5 ± 17.7 mV) voor de huidige formuleringen. Met betrekking tot morfologische observatie werd de oppervlaktelading van SLN-RES voldoende geacht om deeltjesaggregatieverschijnselen en fijne SLN-stabiliteit te voorkomen [21]. Het zeta-potentieel van alle formuleringen met of zonder medicijn was bijna gelijk aan elkaar, wat betekent dat de inkapseling van het medicijn in SLN geen significante invloed had op de oppervlaktelading van de drager. Als gevolg hiervan werd het medicijn aan de binnenkant van de SLN geplaatst vanwege het lipofiele karakter van RES [23].
De in vitro afgifte-assay
Zoals de resultaten worden weergegeven in Fig. 1 werden verschillende afgiftegedragingen gedetecteerd bij pH = 7.4 en pH = 1.2. Na 6 uur en 1 uur kwam ongeveer 70% van de RES vrij uit nanodeeltjes bij respectievelijk neutrale en zure pH-omstandigheden. De initiële burst-afgifte was te wijten aan de afgifte van geneesmiddelen die in de beginfase op het oppervlak van nanodeeltjes waren geadsorbeerd [24]. Daarna kon een manier van aanhoudende afgifte worden toegeschreven aan geneesmiddel-lipide-interactie, concentratiegradiënt en opname van geneesmiddel in de olieachtige dragerkern. Het profiel van aanhoudende afgifte leidt tot een verhoogde geneesmiddelserumconcentratie en helpt bijgevolg de biologische beschikbaarheid en gerichte afgifte van RES te verhogen. Als suggestie kan de intraveneuze toediening van RES de zure toestand van de maag omzeilen [22].
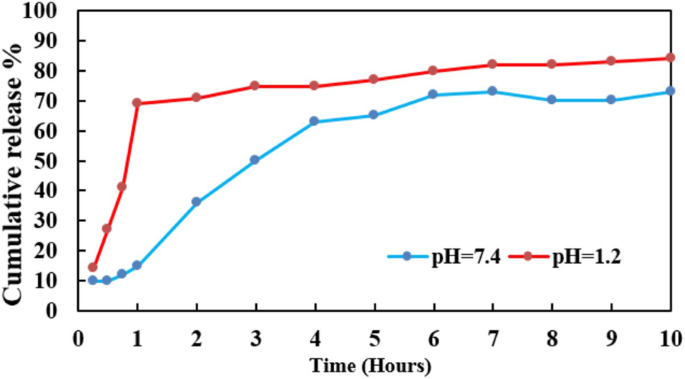
In vitro afgifteprofielen van RES van SLN-RES in zure en natuurlijke omstandigheden
Morfologie-evaluatie
Zoals te zien is in Fig. 2 gaf de TEM-analyse aanleiding tot goede resultaten waarbij de meeste deeltjes een regelmatige bolvorm en grootte bereikten in het bereik van 20-30 nm. Ook werden de staafvormige en amorfe nanodeeltjes waargenomen met minder aggregatie. De deeltjesgrootte van SLN werd geschat tussen 20 en 30 nm, wat niet overeenkomt met de DLS-bevindingen (tabel 1). Deze discrepantie kan het gevolg zijn van de hydratatie van nanodeeltjes door monsterverdunning in DLS-analyse. Er was ook een staafvormig nanodeeltje dat mogelijk te wijten is aan de constante injectie van een emulsie in het koude water door een injectienaald. We hebben geen SLN-aggregaties waargenomen in TEM-observatie, die voldoende oppervlaktelading en stabiliteit vertegenwoordigt voor onze formulering [23].

Transmissie-elektronenmicroscoop van SLN-RES. Bar=100 nm
De laadefficiëntie van RES valideren door middel van infraroodspectroscopie
Zoals weergegeven in Fig. 3, lieten de FTIR-resultaten van het lecithinespectrum een brede piek zien bij 3370-3390 cm −1 dat verwijst naar NH symmetrische rek van choline functionele groep. Een piek van 1735 cm −1 vertegenwoordigde C=O dat zich uitstrekt van de esterverbinding in lecithine. Ook de karakteristieke pieken bij 2922, 2853 en 3010 cm −1 zijn te wijten aan het uitrekken van C-H-groepen. Het SLN-spectrum vertoonde verschillende karakteristieke pieken die vergelijkbaar waren met het lecithinespectrum zonder verschuiving, maar de intensiteit van de pieken die tot lecithine behoorden, was sterk verminderd wanneer ze in SLN werden geplaatst. Dit kan te wijten zijn aan de hydrofiele omgeving en het afschermende effect van de oppervlakteactieve stof. In de huidige studie vertoonde het RES-spectrum een functionele groep inclusief absorptiebanden bij 3290 cm −1 vanwege O-H stretching behorend tot de alcoholische groep, 965 cm −1 voor trans C=C binding, 1154 cm −1 voor C-O stretching, 1445 cm −1 en 1587 cm −1 voor C=C rekken in aromatische (AR) ring, en 1606 cm −1 voor C-C rekken van alkeengroep. Ook vertoonde de RES karakteristieke pieken met een sterke intensiteit van monogesubstitueerde C-H-bocht bij 770 cm −1 en Ar-C-H strekken zich uit op 3020 cm −1 . Er waren pieken met intensiteit bij 1175-1263 die de ArO-H-groep van RES vertegenwoordigden. Onze resultaten valideerden de opname van RES in SLN, terwijl de RES-vingerafdruk werd herhaald in SLN-RES, maar het SLN-spectrum was niet geassocieerd met deze vingerafdruk. Ook een piek rond 1735–1740 cm −1 werd toegeschreven aan C=O stretching (R-C(O)-O-R) dat verwijst naar ester in lecithine fosfolipide in alle spectrum verwacht RES.
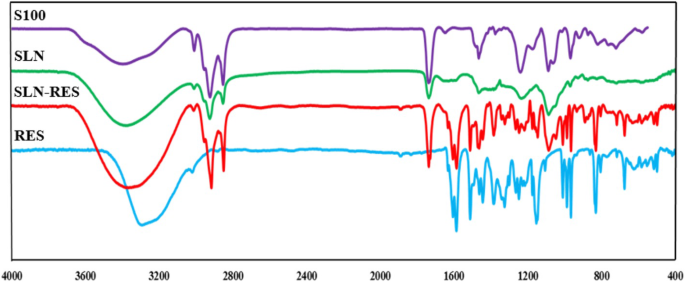
FTIR-spectrum van SLN (vast lipide-nanodeeltje), SLN-RES (met resveratrol geladen vast lipide-nanodeeltje), S100 (lecithine) en RES (puur resveratrolpoeder)
FTIR-gegevens valideerden de aanwezigheid van het medicijn in de drager. Er was een brede piek bij 3040–3670 cm −1 in lecithine, SLN en SLN-RES die het gevolg was van O-H-uitrekking, wat bijdraagt aan de sterke hydrofobe aard van monsters. De brede piekverschuiving tussen SLN en SLN-RES kan worden verwezen naar de vorming van waterstofbruggen wanneer RES in SLN wordt geplaatst. We concludeerden dat het deeltjesoppervlak bedekt was met lecithine vanwege de verbetering van C-H-uitrekking in SLN-RES. Aan de andere kant verwijst de verminderde intensiteit van de RES-vingerafdruk in het SLN-RES-spectrum naar de lipidebedekking van RES in de SLN-structuur. Het verschil tussen karakteristieke pieken van RES en SLN-RES bevestigde dat er een potentiële chemische interactie is tussen RES en andere formuleringscomponenten. Een nieuwe piek die zichtbaar werd op 1000 cm −1 in SLN-RES werd toegeschreven aan Ar-O-R dat verwees naar de interactie tussen RES en lecithine. Aan de andere kant, in het RES-spectrum, is de absorptieband bij 1106 cm −1 was gerelateerd aan de Ar-O-H-groep die verdween in SLN-RES. Deze verandering levert een ander bewijs voor interactie tussen RES en SLN. Bovendien werd een verhoogde intensiteit zichtbaar bij 2850-2900 cm −1 in SLN-RES dan in SLN, wat wijst op de verbetering van CH-uitrekking die mogelijk te wijten is aan toenemende oppervlaktelokalisatie van oppervlakteactieve stof en het plaatsen van RES in het kernnanodeeltje. Over het algemeen valideerden onze resultaten de opname van RES in lipidekern SLN dat wordt gesneden door lecithine [11, 22].
Het effect van RES- en SLN-RES-behandeling op de lichaamsgewichtstoename, nuchtere bloedsuikerspiegel, insuline en HOMA-index
De resultaten in tabel 2 toonden aan dat in de DC-groep de STZ-injectie het lichaamsgewicht aanzienlijk verminderde dan in de HC-groep. RES-toediening voorkwam gewichtsverlies in vergelijking met de DC-groep. SLN-RES dient significanter voor het normale lichaamsgewicht dan RES-behandeling, terwijl het zijn toevlucht nam tot de HC-groep. Op basis van eerdere rapporten had de orale toediening van SLN-RES een vergelijkbaar effect als vrij RES bij intraperitoneale toediening. Gencoglu et al. rapporteerde dat de intraperitoneale behandeling van RES het lichaamsgewicht diende na diabetes-inductie, terwijl het uiteindelijke lichaamsgewicht van diabetische modellen die RES kregen 10% lager was dan dat van de gezonde ratten [25].
Zoals weergegeven in Tabel 2, was FBS significant verhoogd in de DC-groep in vergelijking met de HC-groep. Aan het einde van het onderzoek was de serum-FBS verlaagd door zowel RES- als RES-SLN-behandeling in vergelijking met de DC-groep. Diabetes-inductie verlaagde de serumspiegel van insuline in vergelijking met de HC-groep. Interessant is dat de serumspiegel van insuline bij diabetische ratten werd gecompenseerd door RES-SLN-behandeling. De toediening van RES en SLN-RES verbeterde HOMA opmerkelijk dan de DC-groep. In de SLN-RES-groep was HOMA beter dan RES-behandeling die in de buurt komt van de HC-groep.
Het hypoglycemische effect verkregen met de SLN-RES was significant beter dan RES, wat mogelijk te wijten is aan de verbeterde intestinale absorptie en verhoogde circulatietijd van nano-ingekapselde RES in het bloed. In overeenstemming met ons voorstel, Sadi et al. toonde aan dat de intraperitoneale behandeling van RES samenviel met een diepgaand hypoglycemisch effect en een verbeterde insulineresistentie bij STZ-geïnduceerde diabetes [26].
Het effect van RES- en SLN-RES-behandeling op het serumniveau van oxidatieve stressparameters
Zoals vermeld in tabel 3, leidt diabetes-inductie in de huidige studie tot verminderde antioxidantindicatoren en verhoogde oxidatiemiddelindicatoren in vergelijking met de HC-groep. RES-behandeling verhinderde de uitputting van de serum-TAC-spiegel en remde de verhoging van MDA. Verrassend genoeg kon de SLN-RES-behandeling het serum-TAC- en MDA-niveau volledig herstellen. Waarschijnlijk heeft de verhoogde circulatietijd van RES geleid tot een beter modulerend effect van RES-SLN [27]. In overeenstemming met het huidige resultaat hebben Gokce et al. rapporteerde dat SLN en nanogestructureerde lipidedragers (NLC) die RES bevatten, intracellulaire ROS in celkweekfibroblasten verminderden [28]. Coradini en co-auteurs rapporteerden ook dat de co-inkapseling van RES en curcumine in een lipidedrager de hydroxylradicaal in vitro opmerkelijk verminderde [29]. Bovendien leidde de toediening van RES-SLN tot een significant verlaagde TOS-waarde en een verhoogd -SH-niveau in vergelijking met de DC-groep. RES-behandeling verbeterde echter het TOS- en -SH-niveau niet, wat het zwakke antioxiderende effect van RES aantoonde, wat zou kunnen worden toegeschreven aan de lage biologische beschikbaarheid van RES bij orale toediening.
Het effect van RES- en SLN-RES-behandeling op de genexpressie van Snap23, Stx4 en Vamp2 in vetweefsel
Eerdere pogingen toonden aan dat de verhoging van de genexpressie van Snap23, Stx4 en Vamp2 leidde tot een verbetering van de insulineresistentie. O et al. rapporteerde dat de overexpressie van Stx4 in de pancreascellen van het transgene model de insulineresistentie verbeterde [30]. Hier induceerde de RES-behandeling duidelijk de genexpressie van Snap23, Stx4 en Vamp2 in vet (Fig. 4a-c). Farmani et al. toonde aan dat de RES-behandeling de genexpressie van Stx4 en Vamp2 significant verlaagde in het vetweefsel van het diabetische rattenmodel [31]. Er werden geen significante veranderingen waargenomen tussen RES- en SLN-RES-behandeling in vetweefsel, waarbij waarschijnlijk de halfwaardetijd van serumeliminatie van RES niet voldoende is voor blootstelling aan vetweefselgeneesmiddelen. De genexpressie van Snap23 had geen invloed op RES en SLN-RES, wat mogelijk het gevolg is van de overproductie van SNAP23-eiwit in de adipocyten die kan leiden tot transcriptionele repressie via een feedbackmechanisme. Om deze vraag te beantwoorden, zou de meting van het eiwitniveau van SNAP23 de huidige gegevens in meer detail kunnen verklaren. Ook zou de meting van de hepatische Snap23-expressie met behulp van de tijdsverloopmethode onze waarneming duidelijk verklaren.
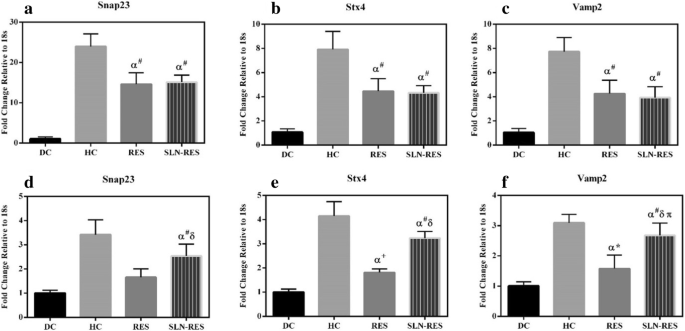
Het effect van RES- en SLN-RES-behandeling op het mRNA-niveau van Snap23, Stx4 en Vamp2 in vet (a –c ) en spierweefsel (d –f ). α , vergeleken met de DC-groep; δ , was er een significant verschil tussen de RES- en de SLN-RES-groep (p < 0,05); π , hersteld in de HC-groep (er was geen significant verschil met de HC-groep (p> 0.05)). Gegevens werden uitgedrukt als gemiddelde ± SD.*p < 0.05, + p < 0.01, # p < 0,001
Het effect van RES- en SLN-RES-behandeling op de genexpressie van Snap23, Stx4 en Vamp2 in spierweefsel
Zoals geïllustreerd in Fig. 4d-f, was STZ-injectie in de DC-groep geassocieerd met downregulatie van Snap23, Stx4 en Vamp2 in spierweefsel in vergelijking met de HC-groep. SLN-RES induceerde de expressie van Snap23 en Stx4 in spierweefsel beter dan de vrije vorm van RES. We hebben het beste resultaat waargenomen over de genexpressie van Vamp2. De orale toediening van SLN-RES compenseerde de neerwaartse regulatie van Vamp2 tot bijna het normale niveau. Vergelijkbaar met onze resultaten, Mullainadhan et al. toonde aan dat de toediening van bisfenol-A aan volwassen mannelijke albinoratten de eiwitexpressie van Snap23, Stx4 en Vamp2 in de gastrocnemius-spier verhoogde [32]. Waarschijnlijk verhoogde absorptie van RES door toediening van RES-SLN kan de kans vergroten dat RES-SLN het spierweefsel bereikt, wat leidde tot een beter regulerend effect op de genexpressie van Snap23, Stx4 en Vamp2. Op basis van het eerdere bewijs, beïnvloeden het potentiële penetratievermogen en de celopnamecapaciteit van SLN-RES de weefselaccumulatie van RES die verantwoordelijk kan zijn voor de verschillende effecten van SLN-RES op de genexpressie van SNARE-eiwitten in vet- en spierweefsel. Met andere woorden, onze resultaten ondersteunden een verschillend in vivo biodistributiepatroon van RES in intacte vorm binnen de SLN.
Conclusie
We hebben een geschikte nanodrager gemaakt in termen van fysisch-chemische en morfologische eigenschappen voor orale afgifte van RES. In het licht van ons resultaat hebben we geconcludeerd dat SLN's kunnen dienen als een veelbelovend toedieningssysteem om het therapeutische effect van orale behandeling van RES tegen insulineresistentie te versterken door het hypoglycemische effect te verbeteren en de expressie van Snap23, Stx4 en Vamp2 in vet- en spierweefsel te verhogen. zakdoek. Er zullen echter vervolgonderzoeken nodig zijn om de in vivo biodistributie en farmacokinetische eigenschappen van SLN-RES te identificeren.
Beschikbaarheid van gegevens en materialen
Alle gegevens die tijdens dit onderzoek zijn gegenereerd of geanalyseerd, zijn opgenomen in dit gepubliceerde artikel.
Afkortingen
- RES:
-
Resveratrol
- SLN:
-
Vast lipide nanodeeltje
- SLN-RES:
-
Met resveratrol geladen vast lipide nanodeeltje
- SNAP-23:
-
Synaptosomaal-geassocieerd eiwit 23
- STX4:
-
Syntaxin-4
- VAMP-2:
-
Vesikel-geassocieerd membraaneiwit 2
- TEM:
-
Transmissie-elektronenmicroscopie
- FTIR:
-
Fourier-transformatie infrarood spectroscopie
- -SH:
-
Totale thiolgroep
- TAC:
-
Totale antioxidantcapaciteit
- MDA:
-
Malondialdehyde
- TOS:
-
Totale oxidantstatus
Nanomaterialen
- C#-expressies, statements en blokken (met voorbeelden)
- Koolstof nanobuisgaren, spierweefsel en transparante vellen
- type() en isinstance() in Python met voorbeelden
- Slim nanomateriaal en nanocomposiet met geavanceerde agrochemische activiteiten
- Met resveratrol geladen albumine-nanodeeltjes met verlengde bloedcirculatie en verbeterde biocompatibiliteit voor zeer effectieve gerichte pancreastumortherapie
- Endotheelcellen targeten met multifunctionele GaN/Fe-nanodeeltjes
- Afhankelijkheid van de toxiciteit van nanodeeltjes van hun fysische en chemische eigenschappen
- Een vergelijkend in vivo onderzoek van gebiosynthetiseerde koper- en zinkoxide-nanodeeltjes via intraperitoneale en intraveneuze toedieningsroutes bij ratten
- Verminderde contactweerstand tussen metaal en n-Ge door invoeging van ZnO met argonplasmabehandeling
- Grafeenfamiliemateriaal bij botweefselregeneratie:perspectieven en uitdagingen
- meo klasse 4 elektrische mondelinge vragen en antwoorden



