Ontwerpen van met aptameer gouden nanodeeltjes geladen pH-gevoelige liposomen kapselen morine in voor de behandeling van kanker
Abstract
Deze studie stelt de synthese voor van een type antikanker nanodeeltje, aptameren en Au nanodeeltje (Apt-Au)-gemodificeerd Morin pH-gevoelig liposoom (MSL), dat targeting-eigenschappen vertoont. Tumoren zijn moeilijk te genezen omdat hun micro-omgeving verschilt van die van normaal weefsel; de pH is lager dan die van normaal weefsel, wat over het algemeen de effectiviteit van medicijnen belemmert. Zo hebben pH-responsieve geneesmiddelen uitgebreide aandacht getrokken. Gouden nanodeeltjes (AuNP's) vertonen potentieel als medicijndragers vanwege hun kleine formaat, goede biocompatibiliteit, gemakkelijke oppervlaktemodificatie en sterke celpenetratie. Apt-Au@MSL vertoont uitstekende monodispersiteit en tumortargeting-eigenschappen en kan via dialyse worden afgegeven in een gedeeltelijk zure omgeving. We hebben onze modelkankercel gescreend met MTT-assay en ontdekten dat SGC-7901-cellen proliferatie effectief kunnen onderdrukken. In vivo resultaten tonen aan dat de toediening van Apt-Au@MSL tumorgroei in xenograft muismodellen zou kunnen remmen. H&E-kleuring en TUNEL-assay bevestigden verder dat Apt-Au@MSL tumorapoptose kan bevorderen. Apt-Au@MSL kan apoptose induceren door overproductie van reactieve zuurstofspecies (ROS) teweeg te brengen en meervoudige signaaloverspraak te reguleren. Zowel bloedbiochemische tests als H&E-kleuring suggereerden dat deze materialen verwaarloosbare acute toxiciteit en goede biocompatibiliteit in vivo vertonen. Met zijn krachtige functie kan Apt-Au@MSL worden gebruikt als een target-based antikankermateriaal voor toekomstige klinische kankerbehandeling.
Inleiding
Een van de meest voorkomende doodsoorzaken [1], kanker, kan leiden tot aanzienlijk economisch verlies en schade voor de mens. Aanzienlijke inspanningen zijn gericht op de ontwikkeling van slimme medicijnen voor de behandeling van kanker [2]. Vanwege hun vermogen om medicijnen te beschermen totdat ze de doellocatie bereiken, kunnen polymere nanodeeltjes de afgifte van therapeutische medicijnen mogelijk verbeteren [3]. Om ervoor te zorgen dat het therapeutische middel op de actieve plaats wordt afgeleverd, worden zeer reactieve nanodeeltjes gebruikt. Dergelijke nanodeeltjes kunnen worden ontworpen om te variëren in materiaaleigenschappen onder verschillende biologische stimuli. Reactieve nanodeeltjes zijn ontworpen met behulp van verschillende stimuli, waaronder externe stimuli (bijvoorbeeld temperatuur en licht) en biologische stimuli (bijvoorbeeld pH- of redox-omstandigheden). NP's die reageren op pH hebben onderzoeksinteresse gewekt vanwege veranderingen in pH na endocytose van nanodeeltjes. Materialen die reageren op pH trekken ook de aandacht omdat de pH-responsieve functie gemakkelijk kan worden geïntegreerd in een reeks polymeerstructuren om een set nanodeeltjes te ontwerpen die reageren op pH. Nanodeeltjes kunnen reageren op pH door verandering van oppervlaktechemie, verandering in deeltjesgrootte of vorm, en afbraak of afgifte van stoffen. Deze verandering in eigenschappen van nanodeeltjes kan worden gebruikt om cellulaire opname en gecontroleerde afgifte te reguleren. Daarom bieden pH-responsieve nanodeeltjes een krachtige strategie voor het ontwerpen van therapeutische toedieningssystemen.
Morinehydraat (3,5,7,2′,4′-pentahydroxyflavon) (Fig. 1) is een natuurlijke werkzame stof die wordt geïsoleerd uit Chinese kruidengeneesmiddelen of planten [4]. Het is een progesteronverbinding en een secundaire metaboliet van fenol in planten. Morin is wijdverbreid in de natuur en oefent goede antioxiderende, kankerbestrijdende [5] en significante ontstekingsremmende effecten uit. Het potentieel van Morin voor verschillende toepassingen heeft veel belangstelling gewekt [6], maar dit potentieel wordt aanzienlijk beperkt door de lage oplosbaarheid in water en de biologische beschikbaarheid van de stof [7].
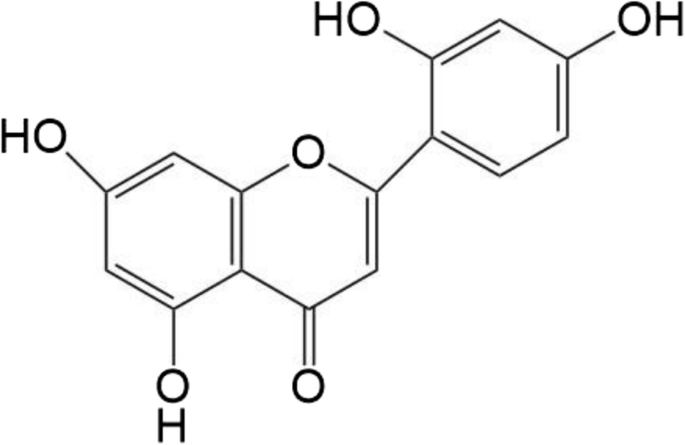
Chemische structuur van Morin-hydraat
Liposomen (hol) bestaande uit onder andere lecithine en ceramide hebben een dubbellaagse structuur bestaande uit amfifiele lipidemoleculen [8]. Liposomen bieden gewenste eigenschappen, zoals biocompatibiliteit, functionaliteit, verminderde bijwerkingen en het vermogen om grote hoeveelheden medicijnen in te kapselen [9, 10]. Ze kunnen efficiënt hydrofiele en hydrofobe middelen vervoeren en ze beschermen tegen externe omstandigheden, en ze met succes naar gerichte weefselgebieden transporteren [11]. Verbeterde werkzaamheid is opgenomen in het ontwerp om de pH-getriggerde afgifte van het antikankermateriaal in het tumorinterstitium te vergemakkelijken via pH-gevoelige liposomen [12,13,14,15]. Deze pH-gevoelige liposomen zijn speciale liposomen die medicijnen afgeven in weefselomgevingen en snel destabiliseren in zure omgevingen, zoals endosomen van kankerweefsel [16,17,18].
Voor verbeterde selectiviteit en werkzaamheid van tumorbehandeling, moeten pH-gevoelige liposomen worden gemodificeerd om op tumor gerichte nanodeeltjes te vormen [19]. DNA-aptameren zijn recentelijk ontwikkeld als zeer selectieve en gevoelige biosensing- en beeldsensoren, evenals potentiële middelen voor op kanker gerichte therapieën [20]. Het is aangetoond dat het enkelstrengs DNA-aptameer AS1411 functioneert als een chemotherapeutisch middel vanwege zijn hoge bindingsaffiniteit voor kankercelkernen [21]. Deze aptamer (Apt) werd gecombineerd met Au NP's om een tweecomponenten nanoconstruct te fabriceren van met Apt geladen Au NP's die kunnen interageren met kankercelkernen. Sommige studies hebben ook aangetoond dat het ontwerp van liposoom-nanodeeltjeshybriden een rijke toolbox kan bieden voor de fabricage van dergelijke multifunctionele modaliteiten [22]. Een hybride liposoom-Au NP vesiculair systeem bestaande uit kationische liposomen en Au NP's is ontworpen om de penetratie van geneesmiddelen in het interstitium van de tumor te verbeteren en de activiteit tegen kanker te verbeteren [23, 24].
Gouden nanodeeltjes (Au NP's) worden beschouwd als goede medicijndragers en kunnen worden gemodificeerd met biogerelateerde moleculen om de op kanker gerichte specificiteit te verbeteren [25]. Met de oppervlaktemodificatie van Au NP's, kan het aptameer van de sulfhydrylgroep worden gebruikt om het oppervlak van Au NP's te modificeren, die het doelwit kunnen zijn van de Au-S covalente binding, en de juiste sulfhydrylgroep op het nanogold-oppervlak kan worden bevestigd aan het nanogold-oppervlak [26]. Vanuit een technisch en toepassingsperspectief bieden ligandgebonden gouden nanomaterialen een krachtig platform om gerichte identificatie, detectie en behandeling te vergemakkelijken.
In de huidige studie hebben we pH-gevoelige liposomen gebruikt die Morin inkapselen en Au-Apt geassembleerd dat was gemodificeerd op het oppervlak van de liposomen (Apt-Au@MSL, Fig. 3a). Morin, dat wordt gekenmerkt door een lage oplosbaarheid in water en biologische beschikbaarheid, werd getransformeerd. De morfologie, grootte en andere eigenschappen van het bereide Apt-Au@MSL werden gekarakteriseerd. Het nieuwe nanodeeltje vertoonde tumorgerichte eigenschappen en een hoge antikankeractiviteit. De antikankeractiviteit van Apt-Au@MSL werd in vitro en in vivo onderzocht (Fig. 2).
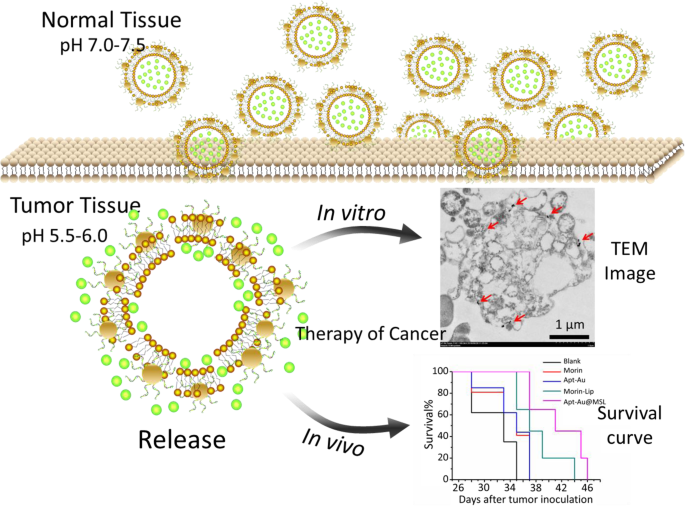
Voorgesteld schematisch diagram van onze ontworpen Apt-Au@MSL die Morin bevat voor medicijnafgifte aan kankercellen met tumorgerichte eigenschappen.
Materialen en methoden
Materialen
L-α-fosfatidylcholine (PC), cholesterol (Chol), cholesterylhemisuccinaat (CHEMS), Morin (≥ 99,99%), natriumcitraat (99,9%), HAuCl4 ·3H2 O (-99,9%), polyvinylpyrrolidon (PVP, gew. 40.000), NaOH (-98,0%) en HCl (37%) werden gekocht bij Sigma-Aldrich Chemical Co. (VS). Het AS1411-aptameer met een disulfidemodificatie werd gesynthetiseerd door TaKaRa (Dalian, China) met de volgende sequentie:5'-HS-T-(C6-S-S-C6)-TTG GTG GTG GTG GTT GTG GTG GTG GTG G-3'. Thiazolylblauwtetrazoliumbromide (MTT), propidiumjodide (PI), calceïne en Alexa Fluor 488 Annexine V werden gekocht bij Sigma-Aldrich Chemical. Alle waterige oplossingen werden bereid in dubbel gedestilleerd water. Alle andere reagentia waren de beste die in de handel verkrijgbaar waren.
Synthese van Au NP's
Tot 1 mL HAuCl4 ·4H2 O (1%) werd opgelost in 25 mL Milli-Q-water (pH =-5,5) en 50 mg PVP werd aan de oplossing toegevoegd. De verkregen oplossing werd in een driehalskolf (150 mL) gegoten en werd gedurende 5 min onder mechanisch roeren behandeld met microgolf (MW) bestraling. Vervolgens werd 1,5 mL natriumcitraatoplossing (1%) snel aan de oplossing toegevoegd en werd gedurende 3 min met MW bestraald. De oplossing werd verzameld door centrifugeren bij 10000 tpm gedurende 5 min.
Synthese van Apt-Au NP's
De disulfidebinding van de aptameren werd gesplitst met behulp van tris(2-carboxyethyl)fosfine. Na 30 min werd de aptamer (100 L, 100 μM) oplossing toegevoegd aan 10 mL 5 nM oplossing van Au NP's en vervolgens gedurende 24 h geïncubeerd om Au-Apt NP's te vormen. Na 1 dag hebben we de mengseloplossing tweemaal gezouten met 2,5 mL van een 500 M-oplossing van NaCl, gescheiden door 4 h [27].
Voorbereiding van pH-gevoelige liposomen
Liposomen samengesteld uit ei-PC tot CHEMS tot Chol in de molaire verhouding van 33:13:5 en 5% Morin werden bereid door filmhydratatie. Egg PC, CHEMS, Chol en 2 mg Morin werden opgelost in 8 mL CHCl3 en de organische oplosmiddelen werden verwijderd bij 40°C met een roterende verdamper. Voor Morin-liposomen werd de resulterende dunne lipidefilm gehydrateerd met behulp van 2% (w / v) PBS en vervolgens gesoniceerd met behulp van een ijsbadsonde gedurende 15 min. Het uiteindelijke liposoom werd gesynthetiseerd en gestabiliseerd in het colloïdale systeem. Voor Apt-Au@Morin pH-gevoelige liposomen (Apt-Au@MSL) werd de lipidefilm gehydrateerd met 475 μg/ml Au-Apt NP's in 5% dextrose gevolgd door sonicatie [23].
Karakterisering
Ultraviolet-zichtbare spectroscopie (UV-Vis, S-3100 Photodiode Array, Scinco Co., Ltd., Korea) en Fourier-transform infraroodspectroscopie (FT-IR) werden uitgevoerd (Nicolet iS50, VS, Thermo Fisher Scientific). De morfologie van de Apt-Au@MSL werd onderzocht met transmissie-elektronenmicroscopie (TEM, HT7700, Tokyo Japan, Hitachi). Het afgiftepercentage van Morin werd gedetecteerd met UV-vis-spectroscopie. De morfologie van de Morin-liposomen en Apt-Au@MSL werden ook waargenomen door scanning-elektronenmicroscopie (SEM, S-4800, Hitachi, Japan). Dynamische lichtverstrooiing (DLS) en zeta-potentiaalmetingen werden gebruikt om de optische eigenschappen en afmetingen van Morin-liposomen en Apt-Au@MSL op een Brookhaven ZetaPALS-potentiaalanalysator te karakteriseren.
Celcultuur
De menselijke kankercellijnen, SGC-7901, BGC-823, A549, HeLa, MCF-7 en Hs68, werden gekocht bij American Type Culture Collection (ATCC) en in RPMI gehouden met 10% foetaal runderserum bij 37°C en 5% CO2 .
In vitro onderzoek naar antikankeractiviteit
SGC-7901, BGC-823, A549, HeLa, MCF-7 en Hs68 werden gezaaid op platen met 96 putjes (2.0 × 10 3 cellen/putje) en vervolgens gekweekt met Apt-Au@MSL in verschillende concentraties (0, 5, 10, 15, 20 en 30 g/ml). Au NP's en Morin werden toegewezen als de controlegroepen. De blanco groep bestond uit onbehandelde cellen. De platen met 96 putjes werden geïncubeerd in een bevochtigde incubator. Na incubatie werd 9,6 mL MTT-oplossing (5 mg / ml) aan elk putje toegevoegd en gedurende 2 uur verder geïncubeerd. Elke groep werd in drievoud getest en IC50 waarden werden afgeleid van de gemiddelde OD-waarden van de drievoudige tests versus de geneesmiddelconcentratiecurven. De helderheid van elke groep werd verkregen door confocale fluorescentiemicroscopie [28].
Celadhesie werd gevolgd met behulp van een real-time elektronisch celdetectiesysteem (RT-CES; ACEA Biosciences, Inc.) elke 10 min gedurende 75 h. Om celadhesie te bepalen, werd elk putje in de plaat bezaaid met cellen (1.0 × 10 4 cellen / putje) met een vers medium tot een eindvolume van 200 L en vervolgens geïncubeerd in een Apt-Au@MSL-oplossing in verschillende concentraties (10, 20 en 30 g/mL) bij 10 h geïncubeerd gedurende 12 h [29] . De blanco groep bestond uit onbehandelde cellen en de controlegroepen bestonden uit de Morin- en Morin-liposoomgroepen.
Fluorescentiemicroscopie
SGC-7901-cellen werden 's nachts gekweekt in de platen met 48 putjes bij 37 ° C, 5% CO2 . De cellen werden vervolgens gedurende 12 uur in verschillende concentraties behandeld met Apt-Au@MSL-oplossingen (10 en 30 g/ml). De controlegroepen bestonden uit de Morin- en Morin-liposoomgroepen. Vervolgens werd het medium verwijderd. De blanco groep bestond uit onbehandelde cellen. De cellen werden driemaal gewassen met PBS. De cellen werden gekleurd en vervolgens gemeten door co-kleuring van levende en dode cellen (de LIVE/DEAD-assay). Na co-kleuring met Calcein-AM/PI gedurende 30 min, werden de cellen tweemaal gewassen met PBS om de overtollige kleurstof te verwijderen, en fluorescentiebeelden werden verkregen door confocale laser scanning microscopie (CLSM) (voor calcein-AM, Ex = 488 nm en Em = 515 nm; PI Ex = 535 nm en Em = 615 nm [30]).
Apoptotische celdoodanalyse
Om de antikankereffecten van Apt-Au@MSL te meten, werd elk putje in een plaat met zes putjes bezaaid met SGC-7901-cellen (1,0 × 10 5 cellen/putje) en vervolgens geïncubeerd in Apt-Au@MSL-oplossingen in verschillende concentraties (5, 10, 20 en 30 g/ml) gedurende 12 u. De blanco groep bestond uit onbehandelde cellen en de controlegroepen bestonden uit de Morin- en Morin-liposomen-groepen. Na behandeling werden de cellen verzameld en tweemaal gewassen met PBS. De cellen werden gekleurd met PI en annexine V-FITC en vervolgens geanalyseerd met behulp van een CytoFLEX-analysator (Beckman Coulter) (voor PI, Ex = 535 nm en Em = 615 nm; Annexin V-FITC, Ex = 488 nm en Em = 525 nm ) [31].
Studies over muurvernietiging
Om celwandvernietiging te bestuderen in een antikankertest, werden de SGC-7901-cellen gekweekt in platen met zes putjes bij 37 ° C en 5% CO2 . De cellen gekweekt zonder het materiaal werden gebruikt als de blanco groep. Nadat de cellen gedurende 12 h waren gekweekt met Apt-Au@MSL in verschillende concentraties (5, 10, 20 en 30 g / ml), werden ze behandeld met Trypsine-EDTA-oplossing 0, 25%. Alle cellen (inclusief de drijvende cellen in het medium) werden verzameld met 2000 r/min gedurende 5 min. De verzamelde cellen werden vervolgens gedurende 4 uur gefixeerd in 2,5% glutaardialdehyde-oplossing [32]. De gefixeerde cellen werden gedurende 20 min in een acetongradiëntreeks gedehydrateerd. De cellen werden uiteindelijk onderworpen aan een reeks procedures, gemonteerd op koperen roosters en geobserveerd door TEM (HT-7700, Hitachi, Japan).
Western Blot-assay
De eiwitexpressie van SGC-7901-cellen werd gedetecteerd met Western-blot-analyse. SGC-7901-cellen (4,0 x 105 cellen / putje) werden gedurende 1, 6, 12 en 24 uur op een kweekplaat van 9 cm en 20 μg / ml Apt-Au@MSL geënt. Cellen werden na behandeling geoogst en gedurende 1 uur in een cellysisbuffer op ijs gesuspendeerd. Het mengsel werd in een centrifuge geplaatst bij 11.000g bij 4°C gedurende 10 min, en het supernatant dat totaal cellulair eiwit bevatte, werd verzameld. De totale eiwitconcentratie in het supernatant werd bepaald met behulp van de BCA-methode. Het eiwit werd vervolgens opnieuw gesuspendeerd in de laadbuffer en gedurende 10 minuten bij 100°C gekookt. Monsters die gelijke hoeveelheden eiwit bevatten (40 g/laan) werden onderworpen aan SDS-PAGE (10% tricinegels). Ze werden vervolgens gedurende 1, 5 uur bij 100 V bij 100 V overgebracht en geblokkeerd met 5% magere melk in Tris-gebufferde zoutoplossing met 0, 1% Tween-20 (TBST) gedurende 1 uur. Vervolgens werd het NC-membraan geïncubeerd met respectievelijk de primaire antilichamen en het tweede antilichaam. Doeleiwitbanden werden zichtbaar gemaakt op het membraan met behulp van de ECL western blotting-detectiereagentia. β-actine werd gebruikt als een interne controle van het laden en overbrengen van gelijke eiwitten. De eiwitexpressie werd gekwantificeerd door Hoeveelheid-One Software, en de expressiesnelheid werd gelabeld onder de band [33].
Dierenmodel
BALB / c mannelijke naakte muizen (~ 17 g) werden gekocht bij het Model Animal Research Center van Nanjing University en gefokt in een axenische omgeving (specifieke pathogeenvrije dieren). Tumormodellen werden vastgesteld door subcutane injectie van celsuspensie (SGC-7901 cellen, 100 μL, 1 × 10 6 /mL) in de schouder van de naakte muizen. Heldere beelden van de tumor werden 15 dagen na de subcutane injectie van tumorcellen gegenereerd. Alle dierproeven werden uitgevoerd in overeenstemming met de protocollen die zijn goedgekeurd door het Anhui Agricultural University Laboratory Animal Center (vergunningsnummer:SYXK 2016-007). Een schuifmaat werd gebruikt om de maximale longitudinale diameter (lengte) en maximale transversale diameter (breedte) van elke tumor te bepalen. Het tumorvolume werd vervolgens berekend met behulp van de formule lengte × breedte 2 × 0.5 [34].
In vivo antikankeronderzoek
Vervolgtests werden uitgevoerd toen het tumorvolume 50 mm bereikte 3 . Muizen die willekeurig in vijf groepen waren verdeeld, werden onderworpen aan de volgende intraveneuze behandelingen:PBS (100 L), Morin, Morin-liposomen, Au-Apt en Apt-Au@MSL. De muizen werden intraveneus in de staart geïnjecteerd met een dosis van 2 mg/kg van het te behandelen materiaal. De tumorgroottes van de muizen werden na 24 dagen gemeten. Het lichaamsgewicht en de overleving van de muizen werden ook bepaald. De muizen werden geëuthanaseerd en tumor- en orgaanweefsels van de muizen werden verzameld voor H &E-kleuring [35, 36].
Na blokkering en permeabilisatie werden de tumorglaasjes gewassen met PBS, gekleurd met TUNEL-assay en onderworpen aan DAPI-tegenkleuring. Fluorescentiebeelden werden verkregen door CLSM. Voor DAPI-beeldvorming Ex = 358 nm en Em = 461 nm, en voor TUNEL-assay Ex = 450–500 nm en Em = 515-565 nm [37].
Toxiciteitsevaluatie-assay
Om de toxiciteit van Apt-Au@MSL-behandeling op vitale organen te evalueren, werden de muizen in de vier behandelingsgroepen na 30 dagen opgeofferd. De belangrijke organen (lever, milt, nieren, hart, longen en tumor) van de muizen uit alle groepen werden verzameld en gekleurd met H&E. Ook werden bloedmonsters verzameld en werd de bloedglucose gemeten. Daarnaast werden de gewichten van de muizen bepaald [38].
Resultaten en discussie
Karakterisering
De huidige studie had tot doel een nieuw liposoom te ontwikkelen dat de voordelen van nanodeeltjes (Apt-geladen Au NP's) bezit en effectief kan worden gebruikt als een middel tegen kanker. De basiseigenschappen van de nieuwe liposomen zijn belangrijk voor verder onderzoek. Apt-Au@MSL werd gesynthetiseerd zoals beschreven in een eerdere studie [23], met kleine aanpassingen, en vervolgens gekarakteriseerd met behulp van verschillende methoden (Fig. 3). Figuur 3b presenteert de resultaten van UV-vis-spectroscopie, die de karakteristieke piek laat zien en de vorming van Au NP's kan volgen. Karakteristieke pieken werden waargenomen in het UV-vis spectrum van Au NP's bij ongeveer 530 nm. In het bijzonder vertoonde UV-vis-spectra-analyse een sterke UV-absorptie, die werd beïnvloed door Apt-modificatie van het oppervlak. Dezelfde resultaten werden waargenomen. Karakteristieke pieken werden verplaatst nadat pH-gevoelige liposomen waren gecoat met Morin. De karakteristieke piek van de gefabriceerde Apt-Au@MSL bevond zich op 362 en 550 nm. Deze resultaten gaven aan dat de synthese met succes was voltooid. Voor verdere karakterisering werd FT-IR-spectroscopie uitgevoerd om de resultaten van de synthese te verifiëren. De karakteristieke rode verschuiving van pieken van Morin-liposomen en Apt-Au@MSL duidden verder op de succesvolle modificatie van Morin (figuur 3c). We hebben Morin-afgiftetest uitgevoerd in PBS op verschillende pH-niveaus om de pH-gevoeligheid van Apt-Au@MSL te bepalen. Deze drie pH-waarden simuleren de neutrale omgeving van de bloedcirculatie, de licht zure omgeving van de tumor en de zure omgeving van het intracellulaire lichaam. Het afgiftepercentage van Morin werd gedetecteerd met UV-vis-spectroscopie. Bij pH 5,0 kwam ongeveer 54% Morin vrij binnen 24 h, en continue afgifte werd waargenomen in de volgende 96 h; ondertussen werd bij pH 7,4 slechts ongeveer 10% Morin binnen 24 uur vrijgegeven. Deze resultaten laten zien dat Apt-Au@MSL een goede stabiliteit vertoont onder normale fysiologische omstandigheden, waardoor medicijnlekkage wordt voorkomen; het medicijn komt echter snel vrij in het kernlichaam. Dit gedrag van medicijnafgifte kan het effect van de behandeling effectief verbeteren (figuur 3d). TEM en SEM werden uitgevoerd om de structuren van het liposoom en Apt-Au@MSL op te helderen (figuur 3f). TEM werd uitgevoerd om de structuren van de AuNP's op te helderen. Zoals weergegeven in figuur 3g, hebben de AuNP's een deeltjesgrootte van ongeveer 10 nm, wat consistent is met de grootte van de modificatie op de liposomen (figuur 3g). De SEM-resultaten in Fig. 3e geven aan dat onbewerkte liposomen uitsluitend unilamellaire blaasjes vormen met een niet-uniforme diameter van ongeveer 120 nm, wat consistent is met de grootte bepaald door DLS. Daarentegen laat Apt-Au@MSL zien dat de morfologie van hybride blaasjes wordt toegeschreven aan Au-Apt-modificatie. De diameter van 150 nm was ook consistent met de grootte bepaald door DLS (Fig. 3i). Met name TEM-onderzoek van de interacties tussen de pH-gevoelige liposomen en Au-Apt onthulde dat de Au NP's bijna uitsluitend geassocieerd waren met de vesiculaire lipidedubbellaag en gelokaliseerd waren aan de periferie van de blaasjes (figuur 3h). De ζ-potentiaalmetingen worden weergegeven in Fig. 3j en de zeta-potentialen van Au NP's en Au-Apt zijn negatief. Het resultaat laat zien dat zowel Au NP's (− 57.1 ± 0.3 mV) als Au-Apt negatief geladen zijn (− 31,7 ± 0.2 mV). Apt-Au@MSL werd gemodificeerd met positief geladen Morin-liposomen en de potentiaal veranderde in 36,4 ± 0,3 mV. Positieve en negatieve ladingsadsorptie is het mechanisme waarmee Au-Apt en Morin-liposomen binden. Bovendien geeft figuur 3k de verandering in de inkapselingssnelheid van het deeltje in de loop van de tijd weer, wat de stabiliteit van het deeltje in de loop van de tijd aangeeft. Zoals te zien is in figuur 3k, verandert de inkapselingssnelheid van het deeltje nauwelijks binnen 24 h, wat aangeeft dat het deeltje een goede stabiliteit vertoont over een bepaalde periode. De standaardcurve van Morin-concentratie versus de UV-Vis-absorptie van Morin werd opgesteld om de inkapselingssnelheid van Morin-liposoom en Apt-Au@MSL te bestuderen. De resultaten lieten zien dat de invangefficiëntie van Morin-liposoom en Apt-Au@MSL 90,2% en 89,6% kan bereiken, zoals weergegeven in Tabel S1 en Fig. S1
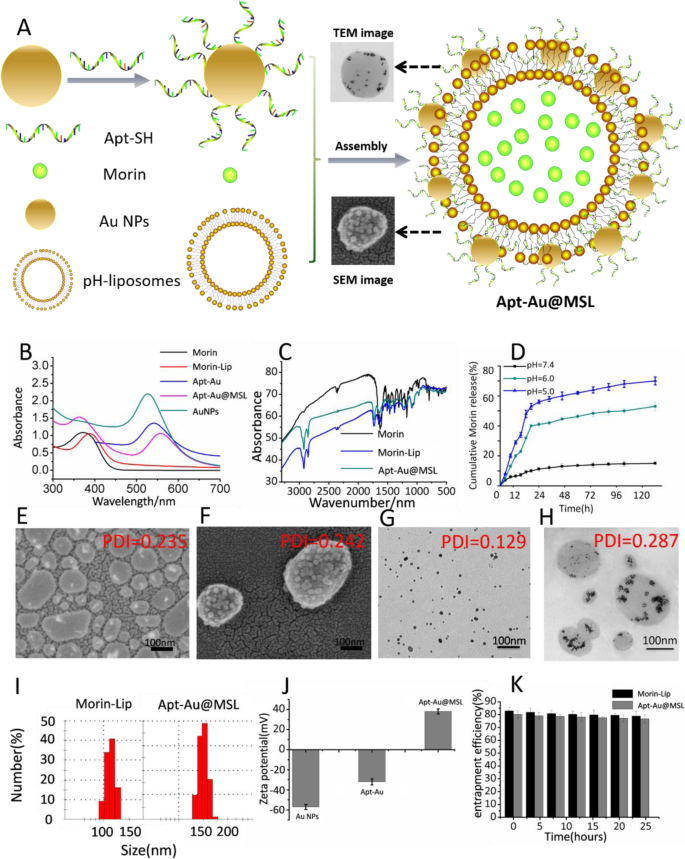
Karakterisering afbeeldingen. een Schematische weergave van de synthese van Apt-Au@MSL. b Ultraviolette absorptiespectra van Morin, Au NP's, Au-Apt, Morin-liposoom en Apt-Au@MSL. c FT-IR-spectrometers van Morin, Morin-liposoom en Apt-Au@MSL. d Het afgiftegedrag van Morin van Apt-Au@MSL bij verschillende pH-omstandigheden. e SEM-beeld van het Morin-liposoom. v SEM-afbeelding van de Apt-Au@MSL. g TEM-afbeelding van de Au NP's. u TEM-afbeelding van de Apt-Au@MSL. ik Diameters van Morin-liposoom en Apt-Au@MSL zijn ten minste driemaal bepaald via DLS. j ζ-Potentieel van Au NP's, Apt-Au en Apt-Au@MSL. k Beknellingsefficiëntie (EE%) van Morin-liposoom en Apt-Au@MSL
Antikankeractiviteitstest van Apt-Au@MSL
In vitro
Morin vertoont superieure antitumoractiviteit maar heeft een lage biologische beschikbaarheid vanwege de lage oplosbaarheid in water. Nadat Morin was ingekapseld door pH-gevoelige liposomen en getransformeerd in een in water oplosbaar materiaal, werd het oppervlak van het liposoom gemodificeerd met Au-Apt om het beoogde antitumoreffect te verkrijgen. Figuur 4a toont de antikankeractiviteit van Apt-Au@MSL door MTT-assay in vitro. De geneesmiddelconcentratie wordt bepaald door de Morin-concentratie. De met Morin behandelde groep vertoonde geen duidelijke antikankeractiviteit, vergeleken met de blanco groep. De groep die werd behandeld met Morin ingekapseld door pH-gevoelige liposomen vertoonde echter verhoogde antikankeractiviteit. Het resultaat suggereert dat de antitumoractiviteit van Morin-liposomen superieur was aan die van onbewerkte Morin. Tegelijkertijd vonden we dat de antitumoractiviteit van het liposoom gemodificeerd door Apt (Apt-Au@MSL) was verbeterd. Tabel 1 geeft een overzicht van de IC50 waarden van Morin, Morin-liposomen, Apt-Au@MSL en cisplatine. Morin, Morin-liposomen en Apt-Au@MSL vertoonden een breed scala aan antikankeractiviteit op tumorcellen. Ze vertoonden een duidelijke voorkeur voor SGC-7901-cellen met een hoge potentie en lage toxiciteit voor normale menselijke cellen. De IC50 waarde van Apt-Au@MSL was 15,6 ± 1,5 μg/ml voor de SGC-7901-cellen. Deze resultaten werden verder bevestigd door RTCA-testen. De SGC-7901-cellen werden in verschillende concentraties gekweekt met Apt-Au@MSL; de blanco groep werd behandeld met PBS en de controlegroep bestond uit Morin en Morin-liposomen. Adhesie en verspreiding werden gevolgd met behulp van iCELLigence (Fig. 4b). De resultaten waren grotendeels vergelijkbaar met die verkregen door MTT-testen. De antitumoractiviteit van Apt-Au@MSL was significant hoger dan die van Morin en Morin-liposomen. Apt-Au@MSL zou de proliferatie van SGC-7901-cellen kunnen remmen met een verhoging van de concentratie. Veranderingen in celmorfologie na behandeling met Apt-Au@MSL werden ook waargenomen met fluorescentiemicroscopie. Zoals weergegeven in figuur 4c, behouden de SGC-7901-cellen zonder Apt-Au@MSL de structurele integriteit van de cel. Daarentegen wordt de celintegriteit aangetast nadat cellen zijn behandeld met Apt-Au@MSL in verschillende concentraties.
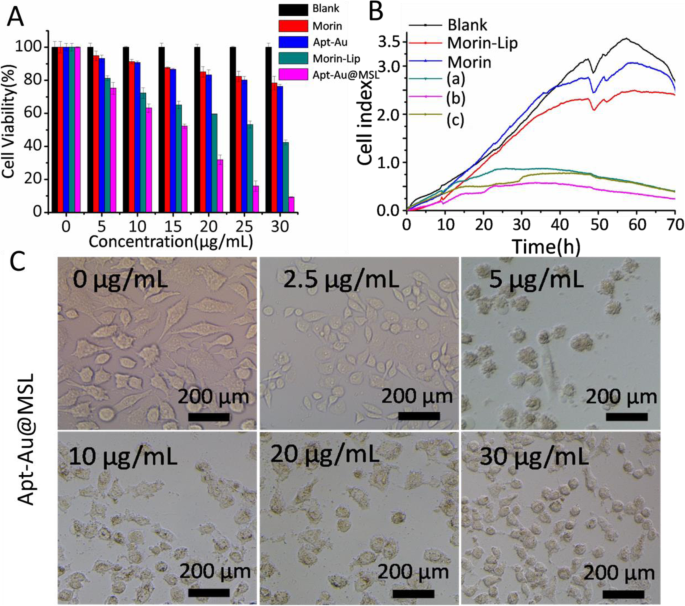
een Levensvatbaarheid van de cellen van SGC-7901-cellen geïncubeerd met ander materiaal (Morin, Au-Apt, Morin-liposoom en Apt-Au@MSL) in verschillende concentraties (0, 5, 10, 15, 20 en 30 g/ml). De door PBS behandelde cel werd als blanco groep ingesteld. b De celproliferatiecurve van SGC-7901-cellen werd gedetecteerd door het RT-CES-systeem. De verschillende verbindingen werden toegevoegd bij 10 h. De concentraties van a , b , en c zijn verschillende Apt-Au@MSL (10, 20 en 30 μg/mL), respectievelijk. c De heldere celbeelden bij de verschillende concentraties (0, 2,5, 5, 10, 20 en 30 μg/mL)
Apoptotische celdoodanalyse
Kwantitatieve analyse van apoptose werd uitgevoerd door flowcytometrie met behulp van Annexin-FITC-kleuring. De cellen werden gekleurd met PI en Annexine V-FITC en vervolgens geanalyseerd met behulp van een CytoFLEX-flowcytometer (Beckman Coulter). Annexine V werd gebruikt om vroege apoptotische cellen gebonden aan de blootgestelde fosfatidylserine te detecteren, en PI-labeling werd gebruikt om de late apoptotische cellen te kleuren. De apoptose-ratio was 1,57% voor de blanco groepen. De met Morin behandelde cellen vertoonden een apoptoseverhouding van 3,51%. Apt-Au@MSL vertoonde bij verschillende concentraties een hoger inducerend vermogen met apoptoseverhoudingen van 7,44%, 10,75%, 15,53% en 40,77% (Fig. 5). De versterkte apoptose bevestigde ook de uitstekende antikankeractiviteit die wordt veroorzaakt door Apt-Au@MSL. De apoptoseverhouding van de SGC-7901-cellen nam toe met een verhoogde Apt-Au@MSL-concentratie.
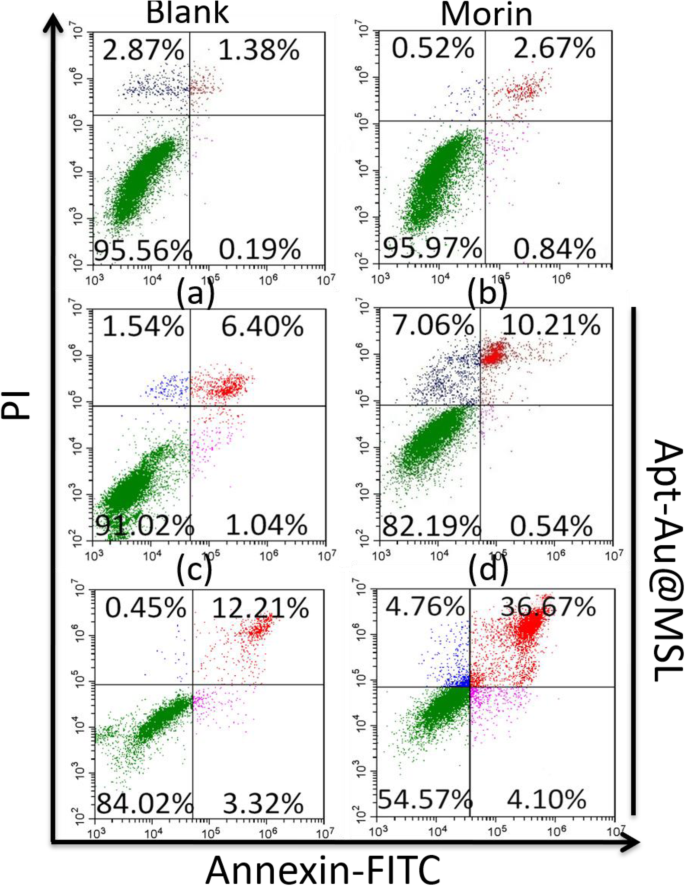
Op annexine V-FITC/PI-kleuring gebaseerde flowcytometrie-analyse van SGC-7901-apoptose na behandeling met verschillende methoden. De concentratie van a , b , c , en d is respectievelijk 5, 10, 20 en 30 g/ml
Antikankeractiviteitsonderzoek door fluorescentieassay
Het antitumoreffect op SGC-7901-cellen, geïnduceerd door Apt-Au@MSL, werd intuïtief geëvalueerd met LIVE/DEAD-fluorescentie-assays. Nadat cellen waren geïncubeerd met Morin, Morin-liposomen en Apt-Au@MSL in verschillende concentraties, werden ze gedurende 30 min onder donkere omstandigheden samen met de LIVE/DEAD-kit gekleurd. In Fig. 6 laten de cellen in de blanco groep zien dat alle groene fluorescentiecellen levende cellen vertegenwoordigen. De controlegroepen, waaronder Morin en Morin-liposomen, tonen het aantal rode fluorescerende cellen. De cellen die werden behandeld met Apt-Au@MSL in verschillende concentraties vertoonden echter duidelijk een groot aantal apoptotische cellen. Met een toename van de concentratie namen levende cellen geleidelijk af. Het percentage dode cellen nam voornamelijk toe en de celdichtheid nam af. Het resultaat bevestigde dat Apt-Au@MSL tumorapoptose effectief kan bevorderen.
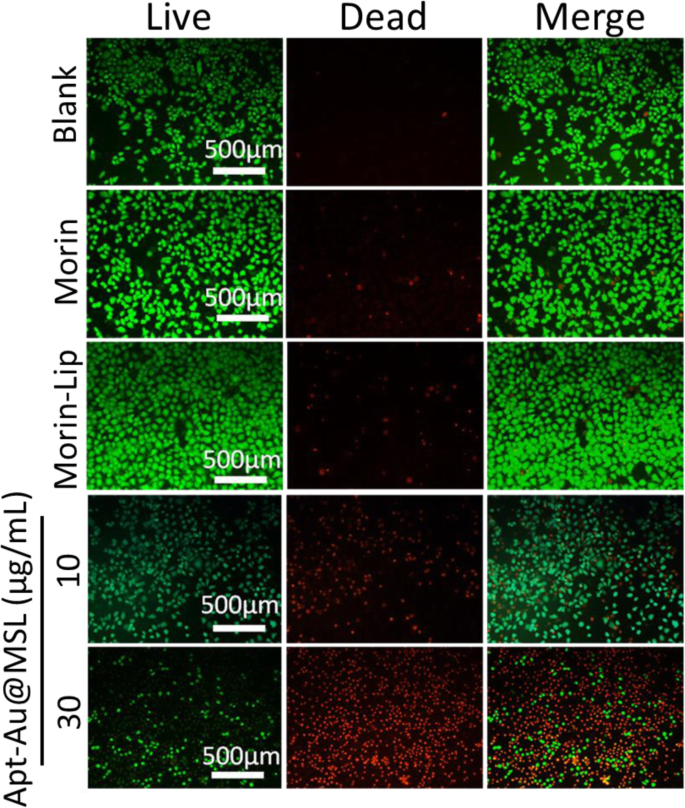
Fluorescentiemicroscopische beelden van SGC-7901 geïncubeerd met verschillende concentraties Apt-Au@MSL en daaropvolgende korte kleuring. De blanco groep was PBS. De Morin en Morin-liposoom werden ingesteld als controlegroep
Onderzoek naar celintegriteit
Om de invloed van opname en transport van de Apt-Au@MSL naar de SGC-7901-cel te bevestigen, hebben we een TEM-assay uitgevoerd. De verandering in celmorfologie werd waargenomen door TEM. TEM-beelden werden uitgevoerd om de interne structuur van de cellen te observeren en een referentie te bieden voor antikankermechanismen. Zoals weergegeven in figuur 7, vertoonden de blanco afbeeldingen van de SGC-7901-cellen zonder behandeling significante veranderingen in de morfologie en het uiterlijk van heldere celwanden. In de controlegroep (Morin en Morin-liposomen) vertoonde de celmorfologie gedeeltelijke schade en trok het nucleaire gebied samen. Er werden echter ook significante veranderingen in de celwand en interne structuur waargenomen na blootstelling aan Apt-Au@MSL. Het cytoplasma lekte en de nucleaire structuur werd onduidelijk. Rond holle cellen werden veel celfragmenten gevormd. Bovendien vielen de celwanden uiteen of werden vernietigd. Hele profielen werden onduidelijk, cellen werden beschadigd en het cytoplasma lekte. De rode pijlen vertegenwoordigden het Au NP-gebied. As the concentration of the Apt-Au@MSL increased, more Au NP regions appeared in the nucleus. This occurrence suggested the release of Morin after Apt-Au@MSL entered the cell interior, hence the appearance of a large amount of Au NPs. These aforementioned results suggest that antitumor activity was associated with compromised cell integrity and nuclear structure.
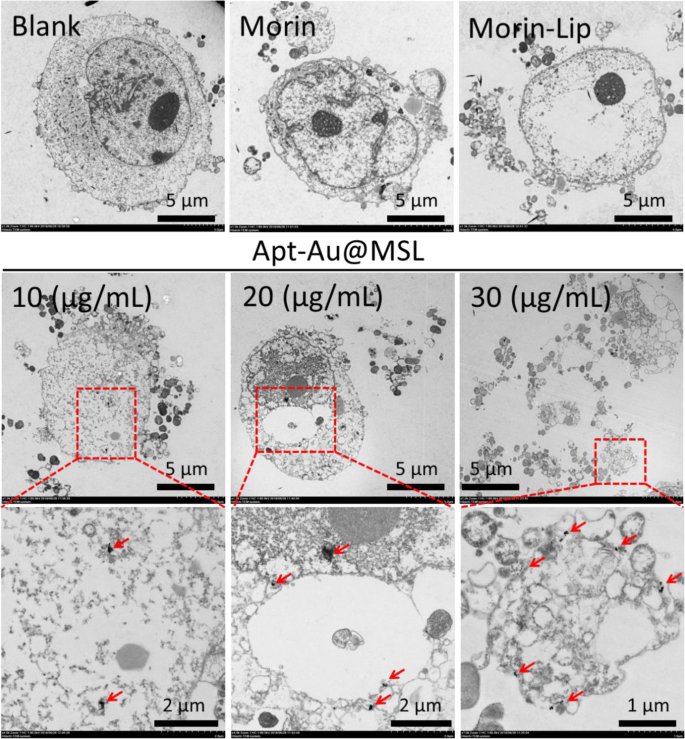
TEM images of SGC-7901 cells treated with different concentration of Apt-Au-MSL (10, 20, and 30 μg/mL). The blank group was PBS. The Morin and Morin–liposome were set as control group. The red square is the enlarge area. The red arrow point to Au NPs
Molecular Mechanism Induced by Apt-Au@MSL
To explore the molecular mechanism of Apt-Au@MSL-induced apoptosis, we detected the expression levels of caspases and PARP. Activation of caspase-3, -8, and -9 was first detected with specific substrates. As shown in Fig. 8a, Apt-Au@MSL treatment induces dose-dependent activation of caspase-3, -8, and -9. Caspase-9 promotes mitochondria-mediated apoptosis more than does caspase-8, indicating that the mitochondria-mediated apoptosis signaling pathway is dominant. Western blot analysis further confirmed the existence of Apt-Au@MSL-induced apoptosis at the protein level. Figures 8b and c show that after cells are treated with Apt-Au@MSL, activation of caspases and cleavage of PARP shows time and dose dependence (Figs. 8b, c). In Fig. 8d, e, the Western blot analysis confirmed our results. In conclusion, Apt-Au@MSL inhibits the growth of SGC-7901 cells mainly by inducing apoptosis.
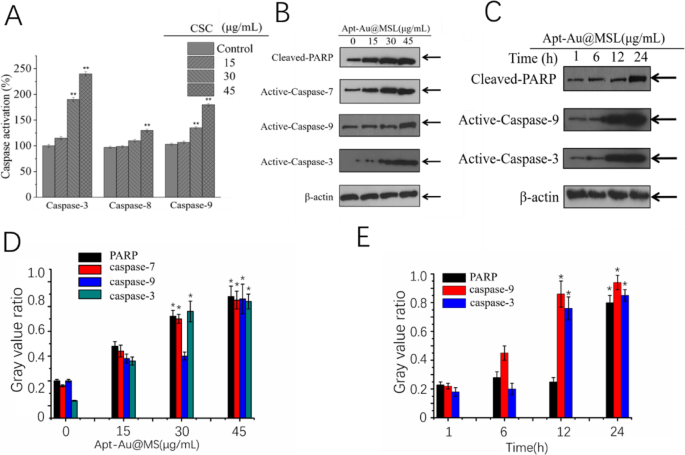
Apt-Au@MSL induced apoptosis in SGC-7901 cells. een SGC-7901 cells were treated with indicated concentrations of Apt-Au@MSL for 24 h. Then, the total protein was extracted and incubated with synthetic Apt-Au@MSL substrates for measuring caspase activities. Dose-dependent (b ) and time-dependent (c ) effects of Apt-Au@MSL on PARP and caspases expression. d , e Quantitative analysis of PARP, caspase-7, caspase-9, and caspase-3 expressions. Data are means ± SD, *P < 0.05, **P < 0.01
Apt-Au@MSL Inhibits Tumor Growth
In Vivo
The in vivo antitumor activities of Apt-Au@MSL were evaluated using an SGC-7901 tumor xenograft model. A comparison of the images of the tumors with those of the control group (Morin and Morin–liposomes) showed that mice treated with Apt-Au@MSL markedly reduced the weight and size of the tumor (Fig. 9a). The relative tumor volume curves and the mice weight curves indicate that the Apt-Au@MSL in vivo exhibits a higher anticancer efficiency (Fig. 9b) than those of the other treatment groups. No significant difference in average tumor volume was indicated between the control group (Morin and Morin–liposomes) and the blank group. The tumor volume of the Apt-Au@MSL group was only nearly a tenth of the blank group and nearly a sixth of the control group. The result indicated that raw Morin and Morin–liposomes at 40 mg/kg exerted no effect on the growth rate of tumors. However, Apt-Au@MSL could inhibit tumor growth. The body weight of mice in the different groups (PBS, Morin, Morin–liposomes, and Au-Apt groups) showed no marked fluctuation (Fig. 9c) during the treatment period. This result suggested that the treatment was tolerated and caused no acute side effects. Notably, we found that the mice with Apt-Au@MSL treatment showed markedly prolonged survival (Fig. 9d). The surviving mice in this group behaved normally, showing no apparent sign of unhealthy condition. These results demonstrated that the administration of Apt-Au@MSL could inhibit tumor growth in xenograft mouse models.
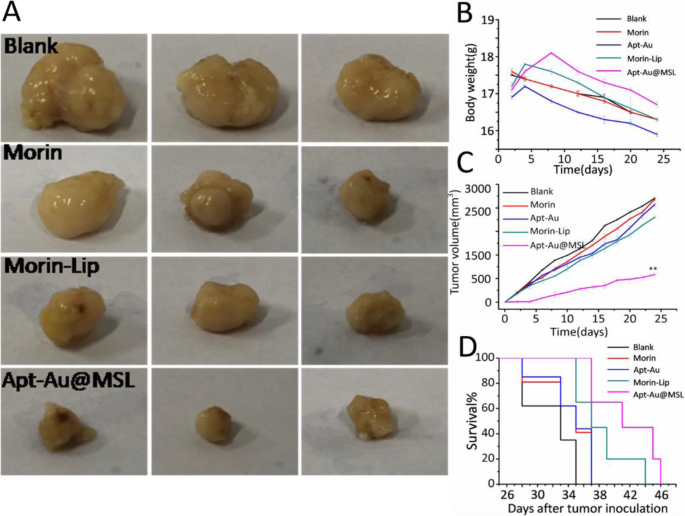
een In vivo applications of Apt-Au@MSL and photographs of the mice tumor taken 24 days. A dosage of 2 mg/kg was administrated intravenously for all mice (n = 6–8). b Tumor weight of mice in different groups after 24 days. c Tumor volume index for the different treatment groups. The tumor sizes were measured at the indicated time points. d Survival rate of the mice in different group after tumor inoculation. Data are means ± SD (n = 6-8). The intravenous injection of PBS was set as blank group (100 μL); the treated by Morin and Morin–liposome were set as control group. In vivo therapeutic effects of Apt-Au@MSL in SGC-7901-bearing mice. Data are means ± SD, *P < 0.05, **P < 0.01
Histological Analysis of Anticancer Activity
H&E staining of tumor tissue and organ samples was conducted after fixation and treatment. Treatment efficacy with respect to tumor cell death was also evaluated by H&E staining of tumor tissue from different groups. In Fig. 10a, the mice treated with Au-Apt, Morin, and Morin–liposomes show the same extent of thermal damage as that of the mice in the blank group. No apparent apoptosis was observed in the blank group. The tumor tissue sections consisted of tightly packed tumor cells. However, Apt-Au@MSL treatment exhibited the most significant damage to the tumor tissue, with moderate cell apoptosis in the tumor. The result suggested anticancer activity in the mouse models treated with Apt-Au@MSL. To further investigate the ratio of apoptotic cells in tumors tissue in vivo, TUNEL assay was performed for the detection of apoptotic cells. As shown in Fig. 10b, the apoptotic cells in tumors can be stained with green fluorescence to indicate apoptosis. The merged images show fewer green fluorescent regions in the blank group and the control group (Morin and Au-Apt), indicating the presence of fewer apoptotic cells. The cells of the mice treated with Morin–liposomes appear partly apoptotic. Moreover, a large number of green fluorescent regions were observed in the group treated with Apt-Au@MSL, indicating a large amount of apoptotic cells. The results were consistent with that of H&E staining, confirming that Apt-Au@MSL can promote tumor apoptosis in vivo.
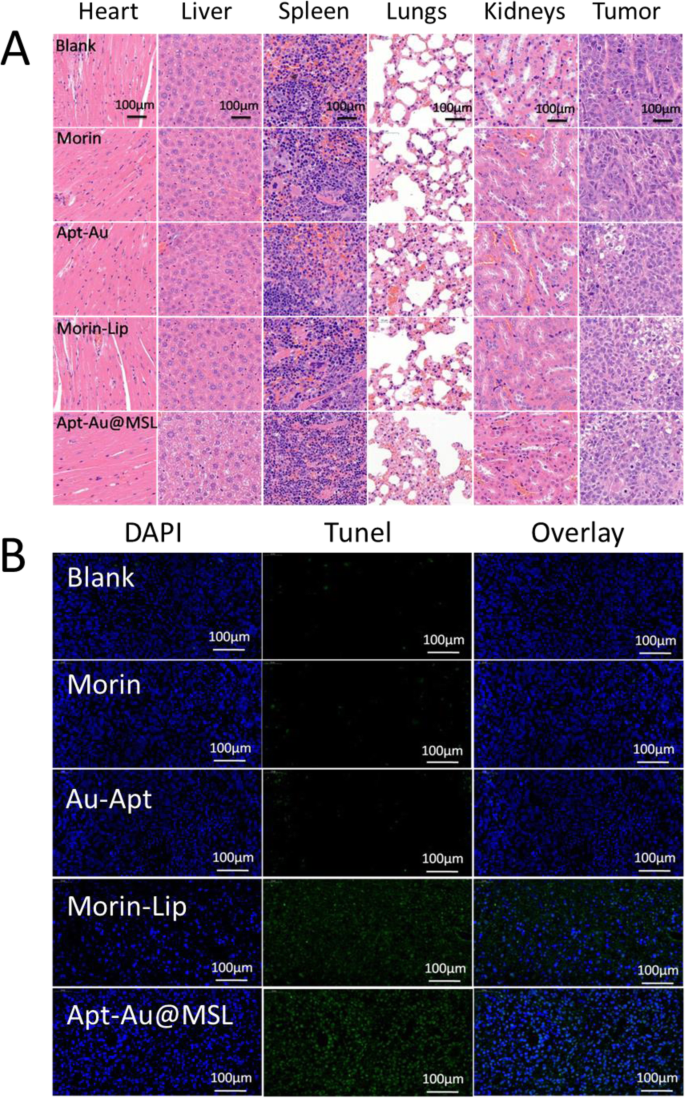
een H&E staining analysis of the tumors in mice. Histological analysis of the tumors in mice following different treatments as PBS, Morin, Morin–liposome, Au-Apt, and Apt-Au@MSL group. b Apoptotic cells were detected by a TUNEL assay (green) and co-stained by nuclear staining DAPI (blue)
In Vivo Toxicity Evaluation
The potential in vivo toxicity is often a significant concern for the clinical application of anticancer medicine. To verify the applicability of Apt-Au@MSL in vivo, the mice were evaluated under different treatments (Morin, Morin–liposomes, Au-Apt, and Apt-Au@MSL). Blood biochemical assays were also conducted to examine possible changes in the biochemistry of mice after treatment. As shown in Fig. 11a, the blood glucose index for blood function of the Apt-Au@MSL groups was similar to those of the blank and control groups. No difference in body weight was found in each group. A steady increase was observed, indicating that the drug exhibited no toxicity (Fig. 11b). H&E staining of organ sections (Fig. 11c) showed no sign of damage or inflammation in the group treated with Apt-Au@MSL, compared with the blank and control group. This finding indicated that PBS, Morin, Morin–liposomes, Au-Apt, and Apt-Au@MSL were negligible side effects in vivo. These results, as well those of H&E staining, further indicate safety in the use of Apt-Au@MSL for tumor treatment.
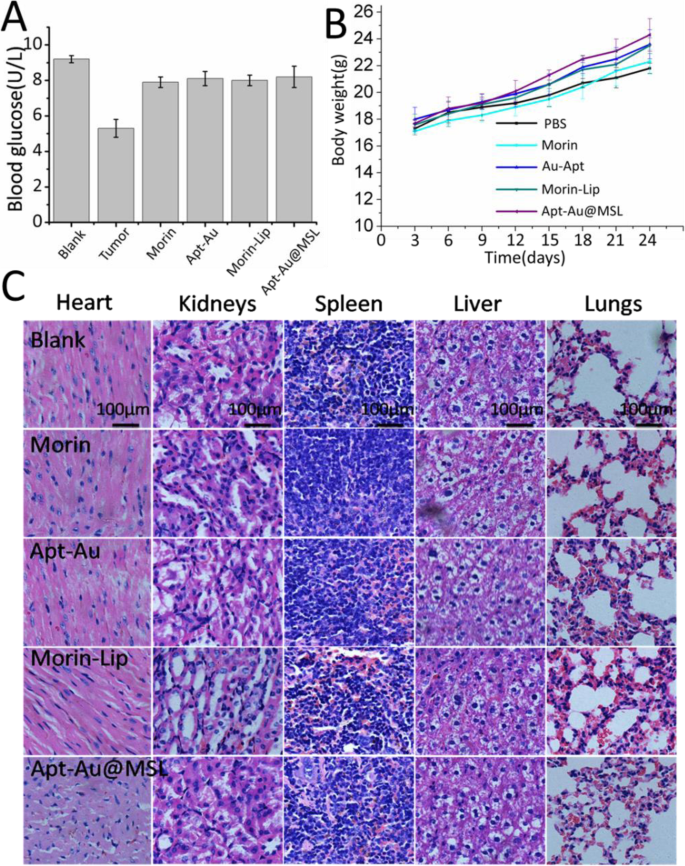
In vivo toxicity evaluation. een Blood glucose data detected in the mouse toxicity model. b Weight of mice in different groups after 24 days. c Images of H&E-stained major organs. Each value represents the mean ± SD (n = 3)
Conclusions
In conclusion, this study presents the synthesis of an antitumor nanomaterial, Apt-Au@MSL. Apt-Au@MSL exhibited excellent monodispersity and tumor-targeting properties. The polarity of Morin was modified, and the antitumor activity was enhanced. The pH of the solution was 5.0, and the release rate of Morin from Apt-Au@MSL was the maximum in the characterization experiments. Apt-Au@MSL showed that the morphology of hybrid vesicles was attributable to Au-Apt modification. The diameter of 150 nm was consistent with the size determined by DLS. We screened our model cancer cell by MTT assay and found that SGC-7901 cells could effectively suppress proliferation. De IC50 of Apt-Au@MSL was 15.6 ± 1.5 μg/mL for the SGC-7901 cells. Fluorescent flow cytometric assays confirmed that Apt-Au@MSL could be used as an effective anticancer material and induced apoptosis in vitro. The Apt-Au@MSL found in the internal cell, as shown in the TEM images, suggested that Apt-Au@MSL could target the cancer cell. The administration of Apt-Au@MSL could inhibit tumor growth in xenograft mouse models, as determined from tumor weight testing. H&E staining and TUNEL assay further confirmed that Apt-Au@MSL could promote tumor apoptosis in vivo. Both blood biochemistry testing and H&E staining suggested that these materials exhibit negligible acute toxicity and good biocompatibility in vivo.
Beschikbaarheid van gegevens en materialen
The authors declare that the materials, data, and associated protocols are promptly available to the readers without undue qualifications in material transfer agreements. All data generated and analyzed during this study are included in this article.
Afkortingen
- Apt:
-
Aptamers
- Apt-Au:
-
Aptamers and Au nanoparticle
- MSL:
-
Morin pH-sensitive liposome
- AuNP's:
-
Gouden nanodeeltjes
- ROS:
-
Reactieve zuurstofsoorten
- Apt-Au@MSL:
-
Aptamers and Au nanoparticle-modified Morin pH-sensitive liposome
- PC:
-
L-α-Phosphatidylcholine
- Chol:
-
Cholesterol
- CHEMS:
-
Cholesteryl hemisuccinate
- PVP:
-
Polyvinylpyrrolidon
- PI:
-
Propidiumjodide
- FT–IR:
-
Fourier-transformatie infrarood spectroscopie
- UV–Vis:
-
Ultraviolet–visible spectroscopy
- TEM:
-
Transmissie-elektronenmicroscopie
- SEM:
-
Scanning elektronenmicroscopie
- DLS:
-
Dynamische lichtverstrooiing
- PDI:
-
Polydispersiteitsindex
- ATCC:
-
American Type Culture Collection
- CLSM:
-
Confocale laser scanning microscopie
- TUNEL:
-
TdT-mediated dUTP Nick-End Labeling
- H&E staining:
-
Hematoxylin-eosin staining
- RTCA:
-
Real-time unlabeled cell analysis
Nanomaterialen
- IBM-wetenschappers demonstreren als eerste Brownian Motors voor nanodeeltjes
- Gouden nanodeeltjes voor chemosensoren
- Nanodeeltjes voor kankertherapie:huidige vooruitgang en uitdagingen
- Op cellen gebaseerde medicijnafgifte voor kankertoepassingen
- Hersengerichte polysorbaat 80-geëmulgeerde Donepezil geneesmiddelgeladen nanodeeltjes voor neuroprotectie
- Elektrospun polymeer nanovezels versierd met edele metalen nanodeeltjes voor chemische detectie
- Folaatreceptor-gerichte bioflavonoïde genisteïne-geladen chitosan-nanodeeltjes voor verbeterd antikankereffect bij baarmoederhalskanker
- Nabehandelingsmethode voor de synthese van monodisperse binaire FePt-Fe3O4-nanodeeltjes
- Aptamer-gemodificeerde magnetische nanosensitizer voor in vivo MR-beeldvorming van HER2-expressie van kanker
- Kationische micel-gebaseerde siRNA-afgifte voor efficiënte gentherapie voor colonkanker
- Milieuvriendelijke biogeconjugeerde gouden nanodeeltjes als efficiënte contrastmiddelen voor door ontsteking geïnduceerde kankerbeeldvorming



