Natuurlijke dissociatieverhouding van door de carboxylgroep gecontroleerde sterk verspreide zilvernanodeeltjes op PSA-microsferen en hun katalytische prestaties
Abstract
De sterk gedispergeerde met zilver nanodeeltjes beladen poly(styreen-co-acrylzuur) nanocomposieten (nAg@PSA) werden bereid en gekarakteriseerd door transmissie-elektronenmicroscopie en thermogravimetrie. De hoeveelheid en verdeling van colloïdaal zilver per deeltje waren gerelateerd aan de dissociatieverhouding van carboxylgroepen in de PSA-bol. De hoeveelheid carboxylgroepen werd geëvalueerd door middel van een geleidbaarheidtitratiecurve. De dissociatie van carboxylgroepen op PSA is echter moeilijk nauwkeurig te bepalen via bestaande methoden omdat de dissociatieverhouding zal toenemen met toenemende onzuiverheidionen tijdens titratie. We hebben een techniek ontwikkeld om de dissociatieverhouding van PSA te bepalen zonder onzuiverheidsionen. Dit maakt gebruik van een nieuw in afstand variabel parallel elektrodesysteem. Zo werd voor het eerst de relatie tussen nanozilververdeling en natuurlijke dissociatie van carboxylgroepen op het oppervlak van de PSA-bolletjes onderzocht. Het nauwkeurig meten en controleren van de dissociatie vergemakkelijkte de productie van PSA-bolletjes die sterk verspreide zilveren nanodeeltjes bevatten. De katalytische prestatie van nAg@PSA-katalysatoren zoals bereid, werd bestudeerd door reductie van 4-nitrofenol. Door de hoeveelheid natuurlijke dissociatieverhouding van carboxylgroep op PSA-bol te regelen, kan dispersie van zilveren nanodeeltjes worden ontworpen en controleerbaar worden bereikt. Ze bieden gemakkelijke synthese, hoge katalytische prestaties en goede recycleerbaarheid.
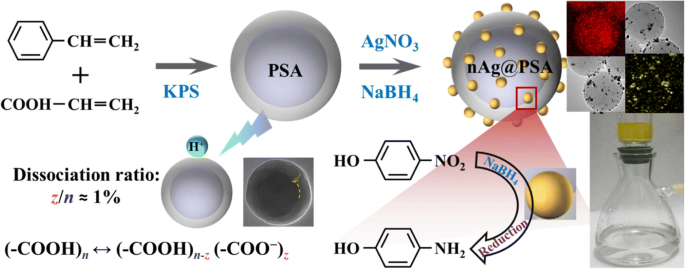
Inleiding
Onlangs heeft de bereiding van kern-schil composiet microbolletjes, bestaande uit een diëlektrische vaste bol die een metalen omhulsel bedekt, veel aandacht getrokken. Deze interesse werd gewekt door hun unieke katalytische en optische eigenschappen. Deze kern-schaalmicrosferen hebben een aanzienlijk potentieel voor een breed scala aan toepassingen, zoals oppervlakteversterkte Raman-verstrooiing (SERS) [1,2,3,4,5], katalyse [6,7,8,9,10], nano-engineering van optische resonanties [11, 12], fotonische kristallen [13,14,15] of biochemie [16, 17] voor toepassingen als chemische sensoren. Vanwege hun nieuwe optische en katalytische eigenschappen [18] zijn veel inspanningen gericht geweest op het maken van kern-schil composiet nanobolletjes met edele metalen omhulsels. Een van de meest bestudeerde systemen zijn samengestelde microsferen met zilveren schelpen. Er zijn verschillende synthetische methoden bestudeerd, waaronder zelfassemblage [19], seeding-plating [18], opeenvolgende ionlaagadsorptie en -reactie (SILAR) [20] en in situ reductiedepositie [21].
Er zijn echter weinig rapporten over de gecontroleerde bereiding van zilveren schelpen op poly(styreen-co) -acrylzuur) microbolletjesoppervlakken. De hoeveelheid zilveren nanodeeltjes ondersteund op poly(styreen-co -acrylzuur) composiet nanobolletjes wordt bepaald door verschillende factoren, waaronder de temperatuur, de hoeveelheid carboxylgroepen en de hoeveelheid gedissocieerde ladingen rond de PSA-bolletjes. Het effect van temperatuur op de afzetting van Ag-nanodeeltjes is onderzocht en beschreven in de literatuur [22]. De hoeveelheid carboxylgroepen is onderzocht met geleidbaarheidtitratiemethoden [19]. Het aantal gedissocieerde ladingen is over het algemeen kleiner dan het stoichiometrische aantal omdat het gedrag van het zwakke zuur afhangt van de ionsterkte. Het toevoegen van elektrolytzouten tijdens elektrochemische metingen verhoogt onmetelijk de dissociatieverhouding van de carboxylgroepen. Bijgevolg is het kwantitatief evalueren van de hoeveelheid van de gedissocieerde ladingen in de latexsuspensies moeilijk. Niettemin beïnvloedt de hoeveelheid gedissocieerde carboxylgroepen per deeltje de afzetting van zilveren nanodeeltjes en werd hier bestudeerd door gebruik te maken van een afstandsvariabel parallel elektrodesysteem. Dit vergemakkelijkt de controleerbare bereiding van zilveren nanodeeltjes.
Enkele toepassingen van met zilver nanodeeltjes geladen poly(styreen-co -acrylzuur) nanosferen zijn gerapporteerd [22,23,24]. Li en medewerkers [22] bereidden met zilver nanodeeltjes gecoat poly(styreen-co) -acrylzuur) composiet nanosferen en gebruikten deze nanosferen vervolgens als oppervlakteversterkte Raman-spectroscopie (SERS)-substraten. Song en medewerkers [24] synthetiseerden met zilver nanodeeltjes geladen poly(styreen-co) -acrylzuur) nanosferen als antibacteriële middelen. Er is echter weinig onderzoek gedaan naar de katalytische toepassingen van met zilver nanodeeltjes beladen poly(styreen-co) -acrylzuur). Verrassend genoeg is er geen rapport over de relatie tussen de dispersie van de Ag-nanodeeltjes en de dissociatieverhouding van carboxylgroepen. Ons eerdere werk [23] heeft een ruwe relatie tussen carboxylgroepen en nanozilverdeeltjes gerapporteerd door thermogravimetrie en TEM-resultaten. Deze keer brengen we een nieuw gezichtspunt naar voren op basis van de natuurlijke dissociatieverhouding van de carboxylgroep door een nieuwe nauwkeurige elektrochemische meting te ontwikkelen.
Dit rapport beschrijft de nauwkeurige karakterisering van de natuurlijke dissociatieverhouding van de carboxylgroep van PSA-bollen via twee draadelektroden om het binnendringen van onzuiverheden te voorkomen. We hebben latexdeeltjes van vier maten gesynthetiseerd om de waarde van de gedissocieerde ladingen te variëren. Vervolgens werd de vorming van goed verdeelde zilveren nanodeeltjes op PSA-nanobolletjes onderzocht. Poly(styreen-co -acrylzuur) nanobolletjes bieden een groot oppervlak voor immobilisatie van zilveren nanodeeltjes en een controleerbare gedissocieerde hoeveelheid carboxyl voor een goede verdeling van zilveren nanodeeltjes. Dit deel lijkt op ons eerdere werk [23]. Er is echter één kritieke vooruitgang in dit werk waarop moet worden gewezen:het is de natuurlijke dissociatieverhouding van de carboxylgroep die fundamenteel het aantal Ag-nanodeeltjes bepaalt in plaats van het totale aantal carboxylgroepen. Deze conclusie kan alleen worden vastgesteld na nauwkeurige meting van de natuurlijke dissociatieverhouding van de carboxylgroep. Dergelijke sterk gedispergeerde zilveren nanodeeltjes op het nAg@PSA-nanocomposiet vertonen hoge katalytische prestaties door de reductie van 4-nitrofenol als modelreactie te gebruiken. Dit heeft interessante mogelijkheden voor toekomstige studies.
Resultaten en discussie
Aantal carboxylgroepen in de PSA-nanosferen
Figuur 1 toont SEM-microfoto's en de bijbehorende deeltjesgrootteverdelingen van vier soorten PSA-nanobolletjes. De deeltjes waren bolvormig met goed gecontroleerde deeltjesgrootteverdelingen. De deeltjesgroottes werden bestudeerd via SEM en het volume van de nanosferen werd berekend. De afmetingen staan vermeld in tabel 1. Het nanobolletjesvolume, de suspensiedichtheid van de PSA-suspensie en het aantal bollen in de voorraadsuspensies werden bepaald met een eerder gepubliceerde methode [23, 25,26,27].
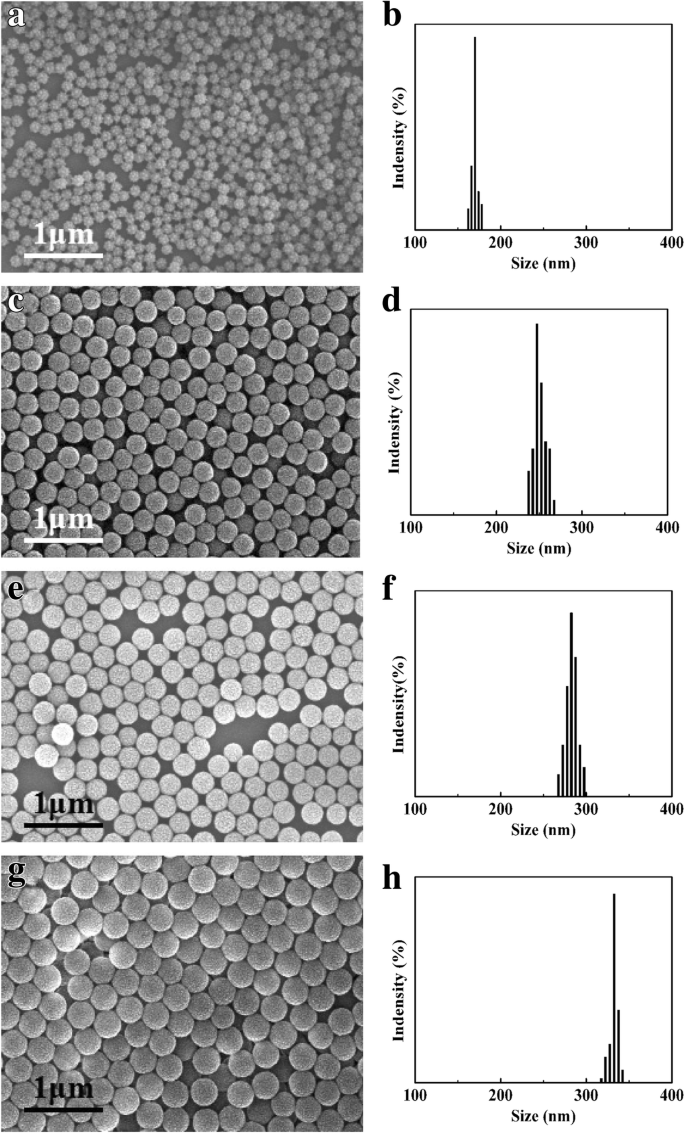
SEM-microfoto's en de histogrammen van de deeltjesgrootteverdeling van PSA-nanosferen:a , b PSA1; c , d PSA2; e , v PSA3; g , u PSA4
De hoeveelheid carboxylgroepen op het deeltje werd bepaald door geleidbaarheidtitratie die eerder werd gerapporteerd [23]. De carboxylbeladingsniveaus (per deeltje) staan vermeld in Tabel 1. Figuur 2 toont een logaritmische grafiek van het totale aantal carboxylgroepen per deeltje met de diameters van de PSA-bol. De grafiek toont een lineair verband met een helling van 2,0. Dit is een bewijs dat de carboxylgroep zich voornamelijk in het bolvormige oppervlak kan bevinden in plaats van in het fasevolume.
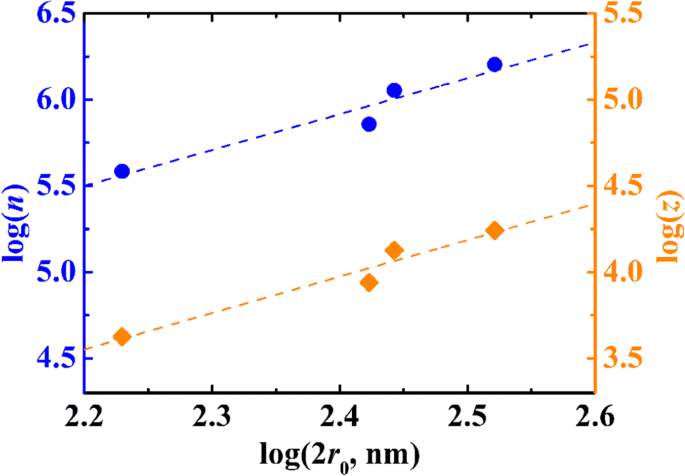
Logaritmische plots van het aantal −COOH en −COO + per deeltje tegen de diameters van PSA-bolletjes
Natuurlijke dissociatieverhouding van carboxylgroepen op PSA-nanosferen
De cel werd gevuld met een PSA-suspensie met een bekende latexconcentratie. Vervolgens werd een AC-spanning van 10 mV toegepast om de AC-impedantie van de ophanging tussen parallelle draadelektroden te verkrijgen. De uitdrukking voor de oplossingsweerstand tussen twee parallelle draden is ongeveer [22]
$$ {R}_S=0.916\frac{\log \left(d/a-1\right)}{Lc\varLambda} $$ (1)Hier, Λ is de molaire geleidbaarheid van de PSA-suspensie met concentratie c , d is de afstand tussen twee elektroden, a is de straal van Pt-draad, en L is de lengte van Pt-draad ondergedompeld in suspensie. Weerstand van de suspensie werd verkregen door Nyquist-plots. Waarden van Z 1 werden uitgezet tegen log(d /een − 1) voor sommige frequenties in Fig. 3. De grafiek voor een bepaalde frequentie viel op een lijn met de gemeenschappelijke helling. Dit vertoont positieve onderscheppingen bij log(d /een − 1) = 0 of d = 2a . De lineaire plot werd gedeeltelijk ondersteund door Vgl. (1), en het voldeed niet aan de evenredigheid van Vgl. (1) in het uiterlijk (positieve waarden van de intercepts). Het intercept betekent dat de weerstand zou verschijnen als de twee elektroden met elkaar in contact zouden komen. Deze weerstand moet zich op het grensvlak bevinden of in de dubbele laag worden opgenomen. De lineariteitshelling die gelijk is aan 0,916/LcΛ , volgens vgl. (1), moet onafhankelijk zijn van de frequentie. De molaire geleidbaarheidswaarden (gebaseerd op molaire concentratie van de PSA-bollen, door een PSA-bol als een enorme ladingsdrager te beschouwen) werden berekend en gemiddeld over frequenties meer dan 150 Hz vanaf de helling; deze staan vermeld in tabel 1. Aangezien één PSA-bol een enorm aantal −COOH bevat, zijn die waarden veel groter dan gewone ionen. Figuur 3 toont de afhankelijkheid van de molaire geleidbaarheid van de diameters van de PSA-bol. Ze liggen op een rechte lijn met een helling van 2,9, wat suggereert dat \( \varLambda ={kr}_0^3 \). Dit houdt in dat de grote deeltjes de molaire geleidbaarheid extreem moeten verbeteren, aangezien de accumulatie van ladingen zich op een enkele bol bevindt.
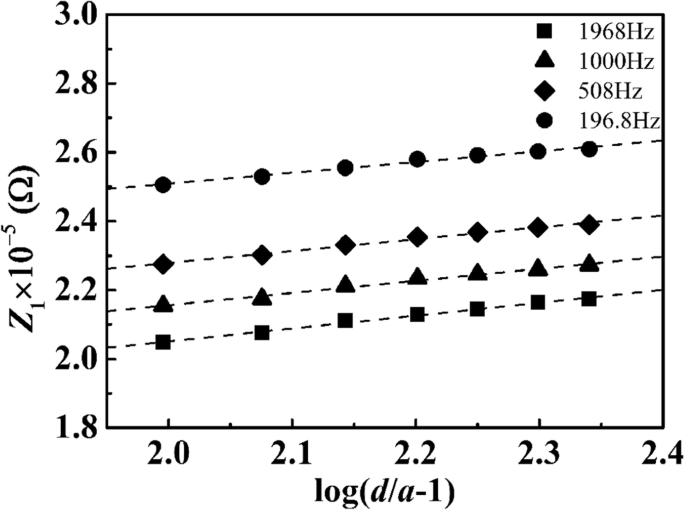
Plot van het reële deel van de AC-impedantie van een typische PSA-suspensie tegen log(d /een − 1) voor frequenties f = 196,8, 508, 1000 en 1968 Hz, respectievelijk
Zoals we eerder beschreven [23, 26], is de molaire geleidbaarheid van de latexsuspensie per N A latexdeeltjes werden gedefinieerd als de som van de molaire geleidbaarheid van z vrije waterstofionen, zλ H , en de geleidbaarheid van N A links z opgeladen −COO — drager PSA bol, λ L :
$$ {\varLambda}_{\mathrm{L}}=z{\lambda}_{\mathrm{H}}+{\lambda}_{\mathrm{L}} $$ (2)Ionische geleidbaarheid wordt weergegeven in termen van de diffusiecoëfficiënt D , via
$$ \lambda =\frac{Dz^2{F}^2}{RT} $$ (3)Wanneer vgl. (3) voor waterstofionen, λ H = F 2 D H /RT , en het latexdeeltje, λ L = F 2 z 2 D L /RT worden ingevoegd in Vgl. (2), we verkrijgen
$$ {\varLambda}_{\mathrm{L}}=\left({F}^2/ RT\right)\left({zD}_{\mathrm{H}}+{z}^2{D }_{\mathrm{L}}\right) $$ (4)Hier, D H en D L vertegenwoordigen de diffusiecoëfficiënten van waterstofionen en −COO — drager PSA bol, respectievelijk. D L werd geschat door de Stokes-Einstein-vergelijking en vervolgens ingevoegd in Vgl. (4) met D H (9,3 × 10 −9 m 2 s −1 ), het oplossen van de vergelijking voor z . De resultaten staan vermeld in Tabel 1. Afbeelding 4 toont de plot van z met diameters van een PSA bol. De helling van de lijn is 2,1, wat bijna gelijk is aan de helling van de lineariteit van n tegen 2r 0 . De waarde van z /n was 0,01. Dit werd berekend volgens tabel 1, die de dissociatie van de carboxyl in een deeltje weergeeft als
$$ {\left(-\mathrm{COOH}\right)}_n\leftrightarrow {\left(-\mathrm{COOH}\right)}_{nz}\ {\left(-{\mathrm{COO}} ^{-}\right)}_z+z{\mathrm{H}}^{+}\ \left(100\leftrightarrow 99:1:1\right) $$ (5A)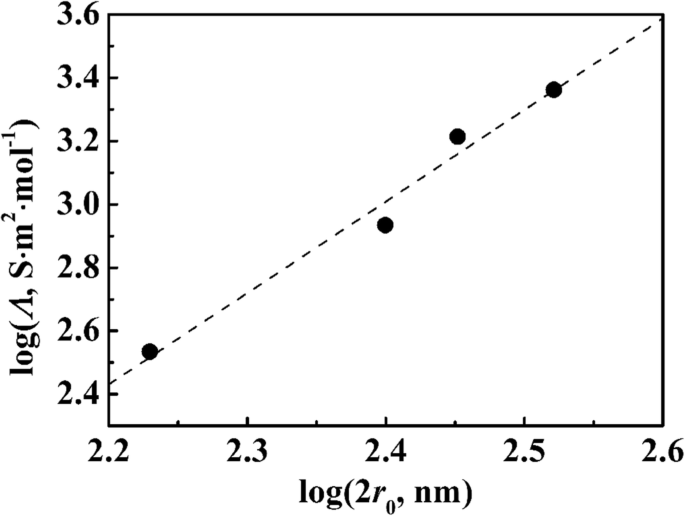
Variatie van de molaire geleidbaarheid met de diameters voor PSA-suspensies op logaritmische schaal
Deze waarde geeft aan dat de natuurlijke dissociatieverhouding van –COOH slechts 1% was. Het andere deel is in de neutrale vorm van –COOH.
Door dit resultaat in te voegen in Vgl. (5A):
$$ {\left(-\mathrm{COOH}\right)}_{100}\leftrightarrow {\left(-\mathrm{COOH}\right)}_{99}{\mathrm{COO}}^{- }+{\mathrm{H}}^{+}. $$ (5B)De geleiding wordt voornamelijk veroorzaakt door de vorming van (AH)99 A − en H + door de reactie (5B).
Om de betrouwbaarheid van deze methoden en de verkregen resultaten te bevestigen, hebben we de berekende waarden van λ uitgezet. L /D tegen z 2 voor de vier latexdeeltjes en monovalente materialen (voor z = 1) op een logaritmische schaal in figuur 5. Zoals verwacht, laat het zien dat een rechte lijn door waarden van eenwaardige materialen gaat. Volgens vgl. (3), de waarden van λ /Dz 2 (=F 2 /RT ) moet constant zijn en onafhankelijk van de diameters of andere eigenschappen van de deeltjes.
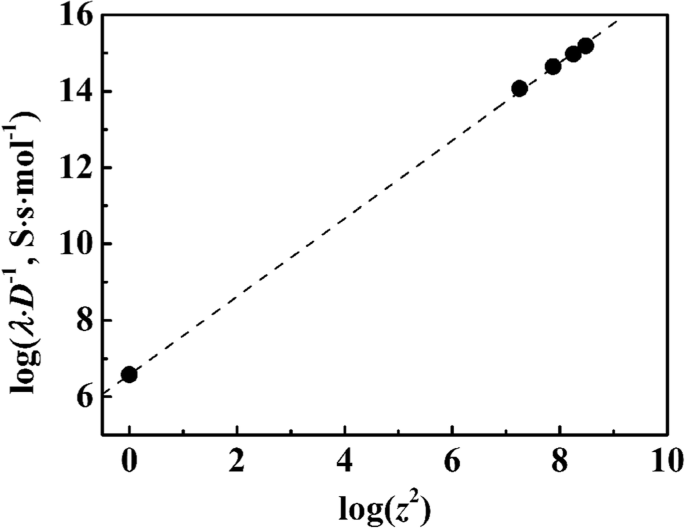
Logaritmische plot van λ ·D −1 tegen z 2 voor de vier PSA-suspensies en halogenide-ionen
Mechanisme van zilveren nanodeeltjes ondersteund op PSA-nanosferen
PSA1-PSA4 werd gekozen als basale sferen om nAg@PSA1-nAg@PSA4-composiet nanosferen te bereiden terwijl alle andere parameters constant werden gehouden (deel "Materialen en methoden"). TEM-microfoto's van nAg@PSA1-nAg@PSA4-nanocomposieten worden getoond in Fig. 6. Uit de microfoto's was PSA bedekt met zilveren nanodeeltjes duidelijk. Naarmate de PSA-nanobolletjes groter werden, werd een toenemend aantal zilveren nanodeeltjes verankerd op de PSA-nanobolletjes. De dekking en uniformiteit van de zilveren nanodeeltjes op de PSA-nanobolletjes namen dienovereenkomstig toe. Figuur 7a toont de microstructuur van Ag-nanodeeltjes bedekt op PSA-nanobolletjes. De roosterafstand van het zilveren nanodeeltje is 0,23 nm, wat overeenkomt met het (111) vlak van het zilverkristal. Dit bevestigde dat Ag-nanodeeltjes met succes werden afgezet. De afzetting van Ag-nanodeeltjes kan ook worden geverifieerd aan de hand van de energiedispersieve röntgenspectroscopie (EDX) -gegevens. EDX-toewijzing van de respectieve Ag- en C-elementen in Fig. 7b toonde de homogene verdeling van deze elementen. Het EDX-spectrum bevestigde de aanwezigheid van Ag, C en O (figuur 7c). De Cu is van het ondersteunende koperen rooster.

TEM-afbeeldingen van nAg@PSA-nanocomposieten. een –d , overeenkomend met nAg@PSA1–nAg@PSA4
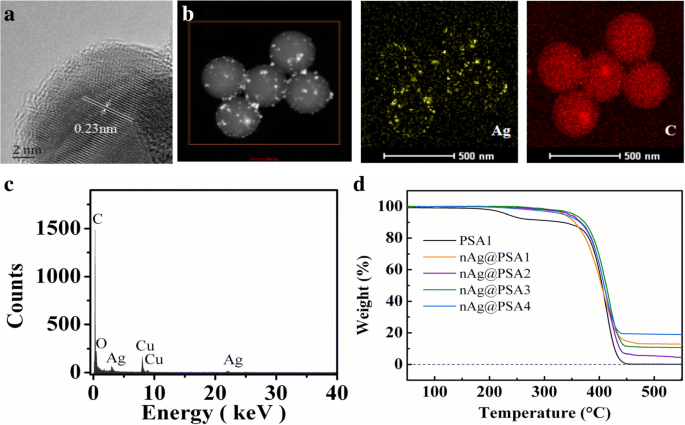
een HRTEM-beeld van Ag op PSA4-nanosferen. b EDX-mapping van nAg@PSA4 composiet nanosferen. c EDX-spectrum van nAg@PSA4 composiet nanosferen. d TG-curven van nAg@PSA1-nAg@PSA-composietbollen
Thermogravimetrische analyse werd gebruikt voor verdere kwantitatieve karakterisering van zilveren nanodeeltjes bedekt op de PSA-nanobolletjes. TG-curven van PSA1-nanosferen en nAg@PSA-composiet-nanosferen verkregen uit PSA1-PSA4-nanosferen worden getoond in Fig. 6d. Met de TG-gegevens konden we de gewichtsbijdrage van de zilveren nanodeeltjes aan de composiet nanosferen berekenen. We zouden dan het aantal zilveren nanodeeltjes kunnen schatten via het gewicht p . De relatie tussen de verdeling van zilveren nanodeeltjes en de dissociatieverhouding van carboxylgroepen wordt getoond in Fig. 8. Het is duidelijk dat het gemiddelde aantal zilverdeeltjes per PSA-deeltje lineair toenam met het aantal gedissocieerde carboxylgroepen. Dit resultaat kan betrekking hebben op de vorming van zilveren nanodeeltjes op het oppervlak van composiet. De negatief geladen carboxylgroepen trekken de positief geladen zilverkationen aan via ionenpaarvorming. De aangehechte zilverionen worden gereduceerd door natriumboorhydride, en dit is een snel reductiemiddel dat de vorming van zilverkernen kan induceren. De resulterende zilveren kernen fungeren als nucleatiecentra; groei vindt plaats door diffusie van zilverionen in de oplossing naar de deeltjesoppervlakken. Deze kunnen worden geïnterpreteerd als heterogene nucleatie-/groeiplaatsen die uiteindelijk zilveren nanodeeltjes vormen. De vorming van zilveren nanodeeltjes wordt sterk bepaald door de balans tussen nucleatiesnelheid en deeltjesgroei.
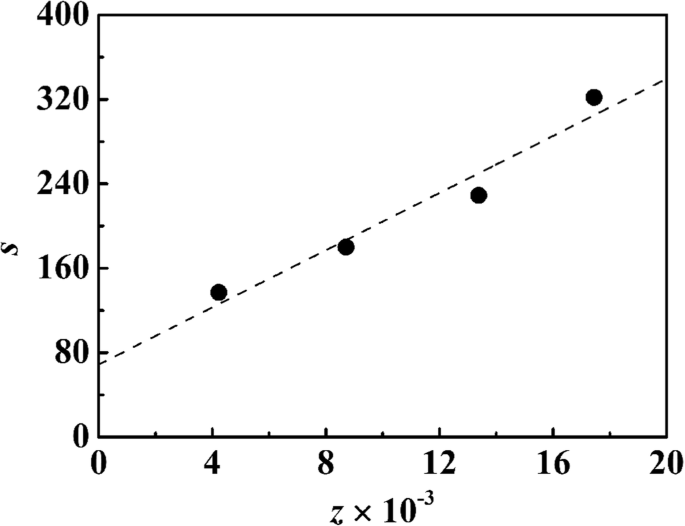
Variatie van de hoeveelheid zilveren nanodeeltjes met het aantal −COO + per deeltje
Katalytische prestaties
De reductie van 4-nitrofenol tot 4-aminofenol is een katalytische modelreactie en werd gebruikt om de katalytische activiteit van nAg@PSA-nanocomposieten te evalueren. De katalytische reactie werd gevolgd met UV-Vis-spectroscopie. Het mengsel van NaBH4 en 4-nitrofenol vertoonde een absorptieband bij 400 nm die overeenkomt met het 4-nitrofenolaat-ion. Figuur 9a-c illustreerde de reductiereactie van 4-nitrofenol die op verschillende tijdstippen werd waargenomen met verschillende nAg@PSA4-hoeveelheden als katalysator. De intensiteit van de absorptieband bij 400 nm nam geleidelijk af en verdween uiteindelijk na verloop van tijd. Dit gaat gepaard met het verschijnen van een nieuwe band rond 300 nm die overeenkomt met 4-aminofenol. Deze gaven de omzetting van 4-nitrofenol in 4-aminofenol aan. Tijdens dit reactieproces worden de totale concentraties van NaBH4 en 4-nitrofenol waren respectievelijk 36 mM en 0,12 mM. De concentratie van 4-nitrofenol is evenredig met de absorptie; de concentratie op reactietijd t (C t ) en tijd t = 0 (C 0 ) zijn gelijk aan de absorptie op reactietijd t (A t ) en tijd t = 0 (A 0 ). Figuur 9d plot ln(A t /A 0 ) versus reactietijd in seconden. De resultaten gaven aan dat ln(A t /A 0 ) nam lineair af met de tijd. Dit volgt op een pseudo-eerste-orde kinetisch gedrag. De snelheidsconstante k bij kamertemperatuur werd berekend uit de helling, en de constanten van nAg@PSA4 met 0,0041 mg Ag, nAg@PSA4 met 0,0054 mg Ag en nAg@PSA4 met 0,0068 mg Ag waren 1,66 × 10 − 3 s −1 , 4,52 × 10 −3 s −1 , en 6,80 × 10 −3 s −1 , respectievelijk. Deze resultaten toonden aan dat hoe groter de hoeveelheid katalysator, hoe hoger de reactiesnelheid. De grootste snelheidsconstante k bij kamertemperatuur is vergelijkbaar met de tegenhanger van eerder gerapporteerde Ag-nanocomposietkatalysatoren, zoals 0,7 × 10 −2 s −1 van G4 -PAMAM-NH2 (Ag12 ) [28], 1,274 × 10 −2 s −1 van Ag10 @SBA-15 [29], 6.2 × 10 −3 s −1 van CNF's/AgNP's [30] en 31,64 × 10 −2 min −1 van [AgCl2 ] − complex [31].
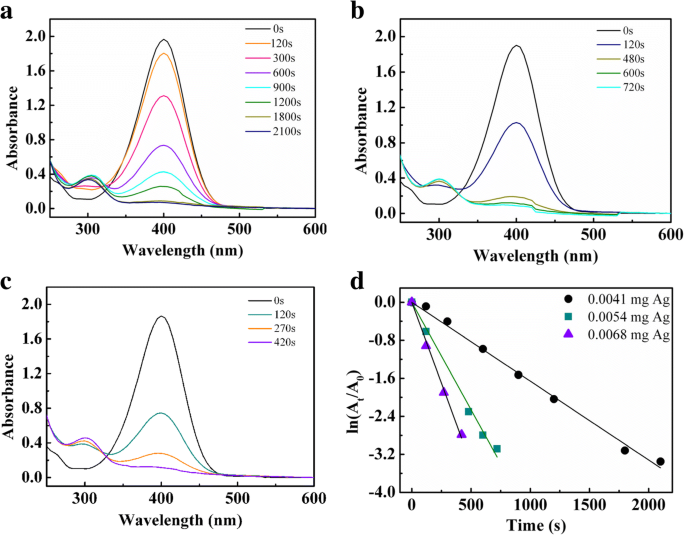
een UV-vis-spectra van 0,12 mM 4-NP met 36 mM NaBH4 in aanwezigheid van nAg@PSA4 nanocomposieten (met 0,0041 mg Ag). b UV-vis-spectra van 0,12 mM 4-NP met 36 mM NaBH4 in aanwezigheid van nAg@PSA4 nanocomposieten (met 0,0054 mg Ag). c UV-vis-spectra van 0,12 mM 4-NP met 36 mM NaBH4 in aanwezigheid van nAg@PSA4 nanocomposieten (met 0,0068 mg Ag). d De plot van ln(At /A0 ) tegen de reactietijd in aanwezigheid van nAg@PSA4 als katalysator
De reductiereacties van 4-nitrofenol, met nAg@PSA2 en nAg@PSA3 als katalysator, worden getoond in Fig. 10a, b. Met dezelfde toevoeging van zilver waren de snelheidsconstanten van nAg@PSA2, nAg@PSA3 en nAg@PSA4 2,92 × 10 3 s −1 , 5.07 × 10 3 s −1 , en 6,80 × 10 3 s −1 , respectievelijk (Fig. 10c). Deze resultaten tonen aan dat de katalytische prestatie van nAg@PSA toeneemt met de toename van de diameter van PSA-nanobolletjes, of het aantal zilverdeeltjes per PSA-deeltje. Met de toename van de diameter van de PSA-bol, zou de als gefabriceerde katalytische film polyporeuzer zijn met de hogere dispersiteit van Ag-nanodeeltjes. Hogere dispersiteit biedt meer kansen voor reactanten die het oppervlak van Ag-nanodeeltjes bereiken. Figuur 10d, e laat zien dat de reactiesnelheden toenamen met respectievelijk toenemende zilverdeeltjesgrootte en hoeveelheid zilver per vierkante centimeter PSA-nanobolletjesoppervlak. Figuur 10f liet zien dat de reactiesnelheid toeneemt met kleinere hoeveelheden nanobolletjes per kubieke centimeter nAg@PSA-suspensie.
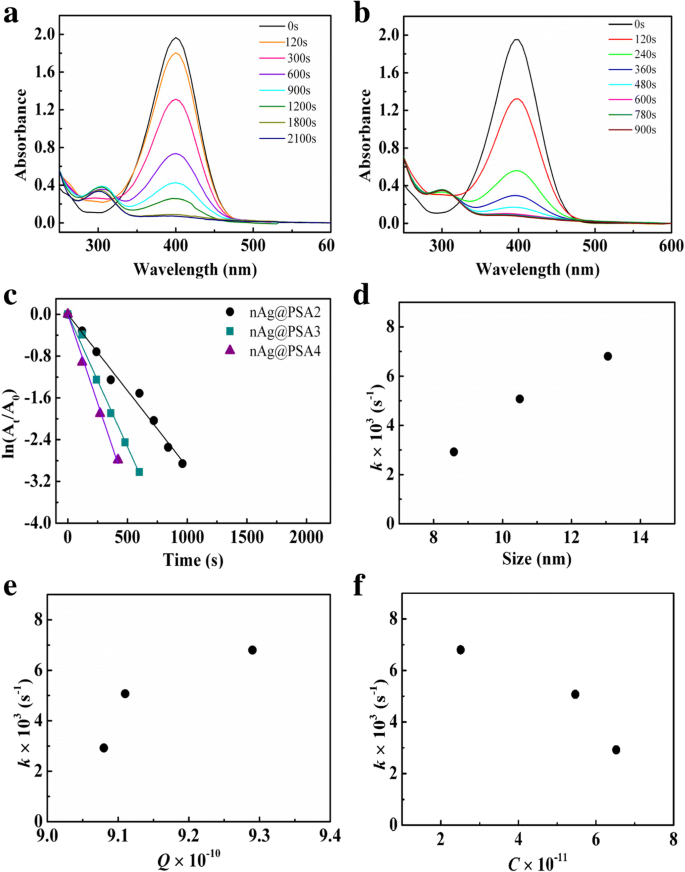
een UV-vis-spectra van 0,12 mM 4-NP met 36 mM NaBH4 in aanwezigheid van nAg@PSA2 nanocomposieten (met 0,0068 mg Ag). b UV-vis-spectra van 0,12 mM 4-NP met 36 mM NaBH4 in aanwezigheid van nAg@PSA3-nanocomposieten (met 0,0068 mg Ag). c Plot van ln(At /A0 ) tegen de reactietijd in aanwezigheid van nAg@PSA-nanocomposieten (met 0,0068 mg Ag) verkregen uit PSA2-PSA4-nanobolletjes. d Effecten van de deeltjesgrootte van zilveren nanodeeltjes op de snelheidsconstante. e Effecten van de hoeveelheid zilver per vierkante centimeter PSA-nanobolletjes op de snelheidsconstante. v Effecten van de hoeveelheid nanobolletjes per kubieke centimeter nAg@PSA-suspensie op de snelheidsconstante
Om de herbruikbaarheid te evalueren, werden nAg@PSA-nanocomposieten afgezet op een glazen zandtrechter om een katalytisch membraan te vormen. Wanneer het reactiemengsel (36 mM NaBH4 en 0,12 mM 4-NP) door het membraan ging, vervaagde de gele kleur in het reactiemengsel, wat een snelle katalytische reactie aantoont (Fig. 11a). De conversieratio van 4-nitrofenol werd bepaald door A t /A 0 bij λ = 400 nm. Volgens figuur 11b was de conversieratio 96% na passage door het katalytische membraan. Bovendien was uit figuur 11c het katalytische membraan actief tot acht cycli van 4-nitrofenolreductie - dit bevestigt de hoge herbruikbaarheid van de katalysator.
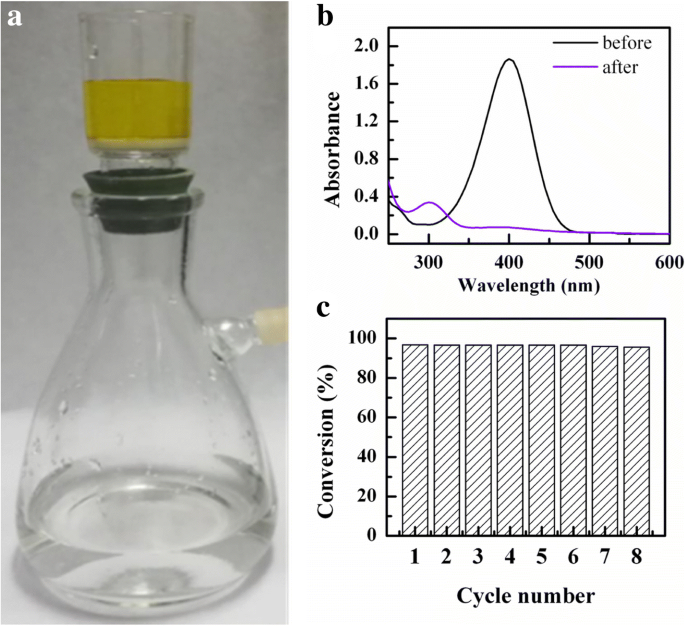
een Foto die de snelle reductie laat zien van 4-NP dat door een nAg@PSA katalytisch membraan gaat. b UV-vis-spectra van 0,12 mM 4-NP met 36 mM NaBH4 voor en na het passeren van het nAg@PSA katalytische membraan. c De conversieratio van 4-NP tijdens de cyclische test
Conclusies
We hebben monodispers poly(styreen-co) gesynthetiseerd -acrylzuur) (PSA) nanobolletjes via zeepvrije emulsiepolymerisatie, en de nAg@PSA composiet nanobolletjes zouden gemakkelijk kunnen worden bereid door de in situ reductie van zilvernitraat via natriumboorhydride in waterige oplossing. SEM-microfoto's van PSA-nanosferen gaven aan dat de PSA-nanosferen bolvormig waren met een smalle deeltjesgrootteverdeling. De grafiek van carboxyl tegen de diameters was lineair met een helling van 2,0. Dit geeft aan dat de carboxylgroepen voornamelijk op het oppervlak van PSA-nanobolletjes zijn verdeeld. Dissociatie moet plaatsvinden op het deeltjesoppervlak in plaats van volumetrisch binnen het deeltje, omdat de hoeveelheid gedissocieerde carboxylgroepen evenredig is met het oppervlak van het latexdeeltje. Het bedrag (z ) van gedissocieerde carboxylgroepen is 1% van de hoeveelheid (n ) van carboxylgroepen. TEM bevestigde de vorming van zilveren nanodeeltjes die op de PSA-nanosferen waren gecoat. De gedissocieerde ladingen op de oppervlakken van PSA-nanosferen hadden een grote invloed op de dekking van Ag-nanodeeltjes op PSA-nanosferen. De katalytische prestatie van nAg@PSA-nanobolletjes werd onderzocht bij het katalyseren van de reductie van 4-nitrofenol. Deze gesynthetiseerde nAg@PSA-nanobolletjes bevatten sterk gedispergeerde zilveren nanodeeltjes met een hoge katalytische activiteit en een goede recyclebaarheid.
Materialen en methoden
Materialen
Acrylzuur (AA), kaliumpersulfaat (KPS), natriumboorhydride (NaBH4 ), zilvernitraat (AgNO3 ) en natriumhydroxide werden gekocht bij Aladdin Chemical Reagent Co., Ltd. (Shanghai, China). Styreen (St) werd geleverd door Tokyo Chemical Industry Co., Ltd. (Tokyo, Japan). Alle chemicaliën waren van analytische kwaliteit en werden gebruikt zoals ontvangen, tenzij anders vermeld.
Synthese van PSA-nanosferen
PSA-nanobolletjes werden bereid volgens de literatuur [22,23,24, 32, 33]. Meestal AA en H2 O (130 mL) werd aanvankelijk in een glazen kolf geladen. Styreen werd toegevoegd na het oplossen van toegevoerd AA. De kolf werd vervolgens onder stikstof onder roeren tot 75°C verwarmd. De polymerisatie werd gestart nadat KPS-oplossing (20 mL) was geïnjecteerd en vervolgens gedurende 12 uur op 75 °C gehouden. Andere bedrijfsparameters worden weergegeven in tabel 2. De producten werden gezuiverd door zeven cycli van centrifugeren en opnieuw dispergeren in gedestilleerd water en vervolgens gedispergeerd in water.
Voorbereiding van nAg@PSA Composite Nanospheres
De typische procedure voor het vervaardigen van nAg@PSA-nanocomposieten [22,23,24] wordt als volgt beschreven:PSA-dispersie (500 mL, 0,3 mg ml −1 ) werd gemengd met een waterige oplossing van AgNO3 (12,5 mL, 10 mM) in de glazen kolf. De mengseldispersie werd geroerd bij 300 r min −1 gedurende 5 uur bij kamertemperatuur. Daarna NaBH4 (12,5 mL, 10 mM) werd aan de dispersie toegevoegd en het resulterende mengsel liet men onder roeren gedurende 2 uur reageren bij 0°C. De suspensie werd gecentrifugeerd (20 min, 12.000 r min −1 ), en het neerslag werd gewassen met gedestilleerd water (30 mL). Deze cyclus van centrifugeren en opnieuw dispergeren werd vier keer herhaald om onzuiverheden te verwijderen.
Katalytische prestatie-experimenten
De reactie van 4-nitrofenol door natriumboorhydride gekatalyseerd met nAg@PSA-nanocomposieten werd uitgevoerd in een waterige oplossing. De reactieprocedure was als volgt:NaBH4 waterige oplossing (4,5 mL, 80 mM) werd gemengd met 4-NP-oplossing (0,5 mL, 2,4 mM) in een Eppendorf-buisje van 10 ml. Vervolgens werden de nAg@PSA-nanocomposieten aan de mengseloplossing toegevoegd en het volume werd met gedestilleerd water op 10 mL gebracht. Onmiddellijk daarna werd een aliquot in een kwartscel met een padlengte van 1 cm geplaatst voor UV-vis-spectroscopie.
De nAg@PSA4-suspensie (die 1,3538 mg Ag bevat) werd gefiltreerd door een glazen zandtrechter uitgerust met een filterconische kolf, afgezet op een filtreerpapier en gewassen met gedestilleerd water (100 mL). De 10 mL oplossing (36 mM NaBH4 en 0,12 mM 4-NP) werd onderworpen aan vacuümfiltratie in de trechter bedekt door het nAg@PSA4-membraan. De opgevangen oplossing in de erlenmeyer werd gekarakteriseerd met UV-Vis-spectroscopie. Om de herbruikbaarheid van de nAg@PSA4-katalysator te evalueren, werd het membraan gewassen met gedestilleerd water en opnieuw gebruikt.
Afstandsvariabele parallelle elektrodensysteem en instrumenten
Afstandsvariabele parallelle elektrodensystemen werden samengesteld door twee platinadraden met een diameter van 0,1 mm en een xz-positioner. Zoals geïllustreerd in Fig. 12, was een van de draden vast en de afstand d werd aangepast door de y . te verplaatsen as van de xz-versteller. De lengte wordt ondergedompeld in oplossing gecontroleerd door de z as van de xz-versteller. AC-impedantie met een andere afstand werd verkregen, volgens onze eerdere werken [25,26,27].
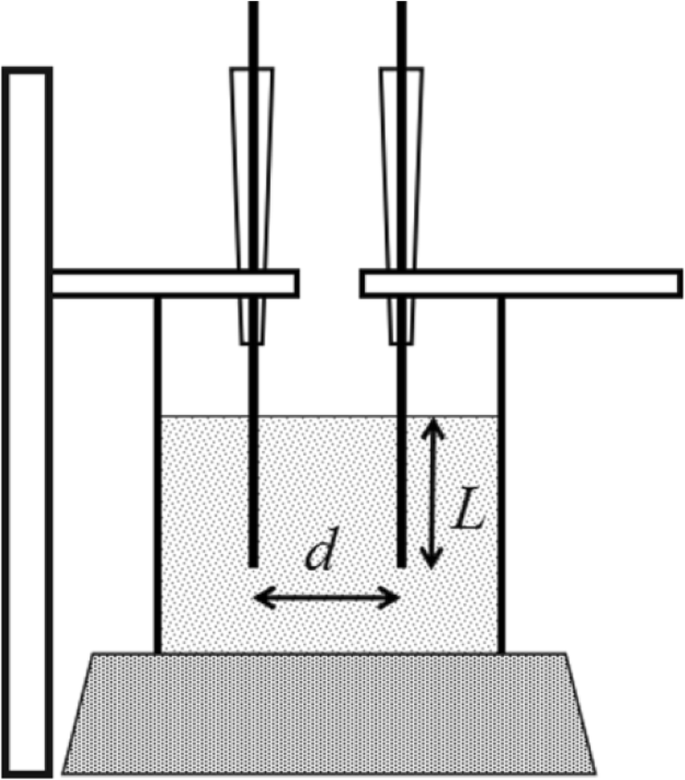
Illustratie van het parallelle afstandsvariabele elektrodensysteem
De kenmerken van nanodeeltjes en de locatie van de zilverdeeltjes op het latexoppervlak werden onderzocht door SEM en TEM (JEOL JEM-2010, JEOL Ltd., Tokyo, Japan). Het gehalte aan zilveren nanodeeltjescoatings op PSA-nanobolletjes werd geanalyseerd door thermogravimetrische analyse (Perkin Elmer Pyris 1, Perkin-Elmer Co., VS). De UV-Vis-spectra werden opgenomen op Shimadzu UV-2550 spectrofotometer (Shimadzu, Kyoto, Japan) bij kamertemperatuur.
Afkortingen
- a :
-
De straal van Pt-draad
- d :
-
De afstand tussen twee elektroden
- D H en D L :
-
The diffusion coefficients of hydrogen ion and −COO — carrier PSA sphere, respectively
- L :
-
The length of Pt wire immersed in suspension
- n :
-
The number of −COOH per PSA microsphere
- nAg@PSA:
-
Silver nanoparticle-loaded poly(styrene-co-acrylic acid) nanocomposites
- PSA:
-
Poly(styrene-co-acrylic acid) nanospheres
- z :
-
The number of –COO — per PSA microsphere
- Λ :
-
The molar conductivity of the PSA suspension with concentration c
Nanomaterialen
- Multifunctionele gouden nanodeeltjes voor verbeterde diagnostische en therapeutische toepassingen:een overzicht
- Voorbereiding van met ICA geladen mPEG-ICA nanodeeltjes en hun toepassing bij de behandeling van door LPS geïnduceerde H9c2-celbeschadiging
- Voorbereiding en verbeterde katalytische hydrogeneringsactiviteit van Sb/Palygorskite (PAL) nanodeeltjes
- De effecten van Li/Nb-verhouding op de voorbereiding en fotokatalytische prestaties van Li-Nb-O-verbindingen
- Synthese en in vitro prestaties van met polypyrrool gecoate ijzer-platina nanodeeltjes voor fotothermische therapie en foto-akoestische beeldvorming
- Zeer verbeterde H2-detectieprestaties van MoS2/SiO2/Si-heterojuncties met weinig lagen door oppervlaktedecoratie van Pd-nanodeeltjes
- Groene bekwaamheid in de synthese en stabilisatie van kopernanodeeltjes:katalytische, antibacteriële, cytotoxiciteits- en antioxidantactiviteiten
- Recente ontwikkelingen in synthetische methoden en toepassingen van zilveren nanostructuren
- Zure peptiserende agent-effect op anatase-rutielverhouding en fotokatalytische prestaties van TiO2-nanodeeltjes
- Platycodon-saponinen van Platycodi Radix (Platycodon grandiflorum) voor de groene synthese van gouden en zilveren nanodeeltjes
- Ronde gouden nanodeeltjes:effect van deeltjesgrootte en concentratie op de wortelgroei van Arabidopsis thaliana



