S-gedopeerd Sb2O3-nanokristal:een efficiënte zichtbaar-lichtkatalysator voor organische afbraak
Abstract
De S-gedoteerde Sb2 O3 nanokristallen werden met succes gesynthetiseerd met behulp van SbCl3 en thioacetamide (TAA) als voorlopers via een gemakkelijke eenstaps hydrothermische methode. De effecten van de pH van de voorloperreactieoplossing op de productsamenstelling en eigenschap werden bepaald. De resultaten gaven aan dat de doteringshoeveelheid S kon worden afgestemd door de pH van de voorloperoplossing aan te passen. Verder ging de S de interstitiële site van Sb2 . binnen O3 kristallen als S 2− , die het absorptiegolflengtebereik van de Sb2 . verbreedde O3 nanokristal. De S-gedoteerde Sb2 O3 vertoonde een uitstekende door zichtbaar licht aangedreven fotokatalytische activiteit bij de ontleding van methyloranje en 4-fenylazofenol. Als laatste, een mogelijk fotokatalytisch mechanisme van de S-gedoteerde Sb2 O3 onder zichtbaar licht werd bestraling voorgesteld.
Achtergrond
De fotokatalytische oxidatie van halfgeleiders is een ideale milieuzuiveringstechniek vanwege het gebruik van zonne-energie, hoge stabiliteit en niet-toxiciteit. Het kan organische verontreinigende stoffen effectief verwijderen, zelfs bij extreem lage concentraties, zonder secundaire vervuiling te veroorzaken [1,2,3,4,5,6]. Onder verschillende soorten halfgeleider-fotokatalysatoren, TiO2 wordt veel onderzocht vanwege zijn uitstekende prestaties onder UV-straling op mineralisatie van een verscheidenheid aan organische verbindingen. De smalle bandafstand van TiO2 (3,2 eV) beperkt het gebruiksrendement van zonne-energie [7, 8]. Daarom is de ontwikkeling van de nieuwe door zichtbaar licht aangedreven fotokatalysatoren van groot belang bij de zuivering van het milieu.
Momenteel kunnen de door zichtbaar licht aangedreven fotokatalysatoren worden voorbereid via twee belangrijke strategieën:de ene is om nieuwe enkelfasige fotokatalysatoren te ontwikkelen, zoals CdS, Sn2 Nb2 O7 , CaBi2 O4 , BiWO4 , en SnIn4 S8 [9,10,11,12,13], en de andere is het modificeren van de UV-actieve fotokatalysatoren. De modificatie kan worden gerealiseerd door vreemde elementen te doteren, UV-actieve fotokatalysatoren te koppelen aan halfgeleiders met smalle bandafstand en door anorganisch-organische hybridisatie te vormen [14,15,16,17,18,19,20,21,22,23, 24,25,26,27,28,29,30]. Zwavel (S), een niet-metalen element, wordt meestal gebruikt om halfgeleiders met een brede bandafstand te doteren, zoals TiO2 [18,19,20], In(OH)3 [21], en Zn2 SnO4 [22], om de gewenste fotokatalysatoren voor zichtbaar licht te verkrijgen. De doteringsconditie kan echter de valentietoestand en vorm van S in de producten aanzienlijk beïnvloeden, wat resulteert in verschillende fotokatalytische activiteiten. Umebayashi et al. bereidde de S-gedoteerde TiO2 door de oxidatie-uitgloeiing van TiS2 , waar de S-atomen de O-atoomplaatsen in TiO2 . bezetten om Ti-S-bindingen te vormen [18]. Ohno et al. gehydrolyseerd titaniumalkoxide in aanwezigheid van thioureum, en het hydrolyseproduct werd in de lucht gecalcineerd om S 4+ op te leveren en S 6+ vervangen TiO2 [19]. Devi et al. bereidde de S-gedoteerde TiO2 door een sol-gelmethode met zwavelpoeder als de S-bron. Ze ontdekten dat S 6+ werd opgenomen in de Ti 4+ rooster van de TiO2 kristal [20]. Met Sanion gedoteerd Zn2 SnO4 werd bereid door het mengsel van thioureum en spinel Zn2 . te calcineren SnO4 onder argonatmosfeer, waarbij S 2− ion ingevoerd in de interstitiële site van Zn2 SnO4 kristal [22].
De oxiden en complexe oxiden van p-blok metaalantimoon, zoals Sb2 O3 [31], M2 Sb2 O7 (M=Ca en Sr) [32, 33], NaSbO3 [32], Sr1.36 Sb2 O6 [34], ZnSb2 O6 [35] en GaSbO4 [36], hebben unieke kristalstructuren en elektronische structuren die de fotogegenereerde ladingsscheiding kunnen bevorderen en de recombinatie van fotogegenereerde elektronen en gaten kunnen verminderen en hebben dus aanzienlijke aandacht getrokken als nieuwe fotokatalytische materialen. De meeste reageren echter alleen op ultraviolet licht, wat hun verdere toepassingen beperkt. In het huidige werk, S 2− -gedoteerde Sb2 O3 nanokristal werd bereid met SbCl3 en thioacetamide (TAA) als de zwavelbron door middel van een hydrothermische synthesemethode. De effecten van de S-doping op de door zichtbaar licht aangestuurde fotokatalytische activiteit van Sb2 O3 voor de afbraak van methyloranje (MO) en 4-fenylazofenol werden ook geëvalueerd. De resultaten gaven aan dat de S 2− doping was in staat om de band gap van Sb2 . effectief te verkleinen O3 en verbeterde zo de door zichtbaar licht aangedreven fotokatalytische activiteit van de Sb2 O3 . Ons werk leverde een haalbare syntheseroute op van de op zichtbaar licht reagerende S-gedoteerde Sb-composietoxide-fotokatalysatoren voor efficiënt gebruik van zonne-energie.
Methoden
Synthese van S-Doped Sb2 O3 Nanokristallen
Alle chemicaliën die in dit werk werden gebruikt, werden gekocht bij Aladdin-reagens en direct gebruikt. De S-gedoteerde Sb2 O3 nanokristallen werden gesynthetiseerd door een hydrothermische methode met behulp van SbCl3 en thioacetamide (TAA) als de voorlopers. In het kort, 3 mmol SbCl3 werd toegevoegd aan een met Teflon beklede roestvrijstalen autoclaafreactor van 100 ml die 70 ml gedeïoniseerd water bevat en 15 minuten mechanisch geroerd. Vervolgens werd onder constant roeren 4 mmol TAA aan de gemengde oplossing toegevoegd. De pH van de voorloperoplossing werd ingesteld op 2, 5, 10, 12 en 14 met behulp van HCl- of NaOH-oplossing. De voorloperoplossing werd gedurende 12 uur in een oven op 120 ° C verwarmd. Het gevormde neerslag werd meerdere keren gewassen met gedestilleerd water en absolute ethanol en aan de lucht gedroogd bij 70 °C. De producten die bij verschillende pH's werden verkregen, werden aangeduid als Sb2 O3 -S-pH (pH = 2, 5, 10, 12 en 14). De pure Sb2 O3 werd bereid in afwezigheid van TAA met gebruikmaking van de vergelijkbare procedure. In het kort, 3 mmol SbCl3 werd opgelost in 50 ml gedeïoniseerd water en 20 ml absolute ethanol in een 100 ml met teflon beklede roestvrijstalen autoclaafreactor onder krachtig roeren en 12 uur verwarmd op 120 ° C. Het gevormde neerslag werd meerdere keren gewassen met gedestilleerd water en absolute ethanol. De verkregen producten werden verkregen na te zijn gedroogd bij 70 °C.
Materiaalkarakterisering
De poederröntgendiffractie (XRD) patronen van de as-prepared Sb2 O3 nanokristallen werden opgenomen op een Bruker D8 Advance röntgendiffractometer met behulp van CuKα straling bedreven bij de versnellingsspanning van 40 kV en de aangelegde stroom van 40 mA. De ultraviolet-zichtbare diffuse reactantiespectra (UV–vis DRS) werden verzameld op een UV–vis spectrometer (Cary 500 Scan Spectrophotometers, Varian, VS) met behulp van BaSO4 als de reflectienorm. De transmissie-elektronenmicroscopie (TEM) en transmissie-elektronenmicroscopie (HRTEM) beelden met hoge resolutie werden vastgelegd met behulp van een JEOL-model JEM 2010 EX-instrument dat werkte bij de versnellingsspanning van 200 kV. Röntgenfoto-elektronspectra (XPS) werden opgenomen op een PHI Quantum 2000 XPS-systeem uitgerust met een monochromatische Al Kα bron en een ladingsneutralisator. Het monsterpoeder werd ultrasoon gedispergeerd in ethanol en een druppel van de suspensie werd op een koolstoffilm gedruppeld die was gecoat op een fijnmazig koperen rooster met een diameter van 3 mm. De C 1s-piek bij 284,8 eV van de oppervlakte-adventieve koolstof werd gebruikt als referentie voor alle bindingsenergieën. Raman-verstrooiingsspectra werden verkregen met een Renishaw inVia Raman-microscoop bij kamertemperatuur.
Metingen van fotokatalytische activiteit
De fotokatalytische activiteit van de monsters werd uitgevoerd in een fotoreactievat. Een 500 W halogeenlamp (Philips Electronics) werd naast het cilindrische reactievat geplaatst met een vlakke zijde als zichtbare lichtbron. Twee scheidingsfilters van 420 en 800 nm werden tussen de lamp en het vat geplaatst om ervoor te zorgen dat alleen zichtbaar licht het vat kon bereiken. Het vat werd op kamertemperatuur gehouden door water te laten circuleren. De fotokatalysator (80 mg) werd verpoederd en toegevoegd aan het vat met 80 ml 3 × 10 −5 mol L −1 MO of p -hydroxyazobenzeen (1,2 × 10 −4 mol L −1 ) waterige oplossing. Het mengsel werd 1 uur in het donker geroerd om het adsorptie/desorptie-evenwicht op de fotokatalysator te bereiken en vervolgens blootgesteld aan het zichtbare licht. Een suspensie van 4 ml werd met bepaalde tijdsintervallen genomen en gecentrifugeerd. Het supernatant werd verzameld en gemeten met een Shimadzu UV-1750 UV-Vis-NIR-spectrofotometer. De absorptie bij de maximale absorptie werd geregistreerd.
Resultaten en discussie
De XRD-patronen van de controle Sb2 O3 en Sb2 O3 -S-pH (pH = 2, 5, 10, 12 en 14) worden getoond in Fig. 1. Alle pieken van zowel controlemonster als Sb2 O3 -S-pH (pH = 10, 12 en 14) werden geïndexeerd op Sb2 O3 (JCPDS-kaart 11-0689). De lage pH's (2 en 5) van de voorloperoplossing verlaagden de kristalliniteit van het product en veroorzaakten de vorming van onzuivere fasen. Deze waarnemingen gaven aan dat de pH van de voorloperoplossing de samenstelling van de producten aanzienlijk zou kunnen beïnvloeden, en de zuivere Sb2 O3 fase kon alleen worden verkregen onder alkalische omstandigheden. De intensiteiten van alle karakteristieke XRD-pieken van Sb2 O3 waren hoger dan die van Sb2 O3 -S-pH (pH = 10, 12 en 14), wat aangeeft dat TAA de groei van Sb2 remde O3 kristalliet.
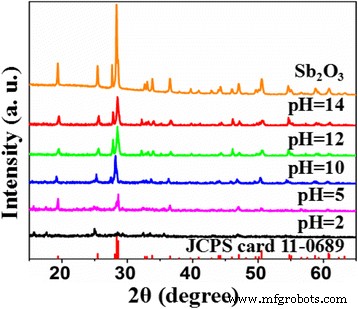
XRD-patronen van Sb2 O3 en S-gedoteerde Sb2 O3 gesynthetiseerd bij verschillende pH's (pH = 2, 5, 10, 12 en 14)
Afbeelding 2 toont de UV–vis diffuse reflectiespectra van Sb2 O3 en Sb2 O3 -S-pH (pH = 10, 12 en 14). De maximale absorptie van Sb2 O3 verscheen om ca. 380 nm, wat suggereert dat Sb2 O3 reageerde alleen op UV-straling. Vergeleken met die van pure Sb2 O3 , de band-gap overgangen van Sb2 O3 -S-pH (pH = 10, 12 en 14) vertoonde duidelijke roodverschuivingen, en de roodverschuiving nam toe met de toename van de pH van de voorloperoplossing. Daarom is het redelijk om aan te nemen dat de vernauwing van de band gap dominant werd toegeschreven aan de S-doping. De S 3p-toestanden gemengd met valentieband (VB), waardoor de breedte van VB werd vergroot en de energieverschuiving in de optische absorptie werd verlaagd [18]. Het is algemeen bekend dat TAA kan worden gehydrolyseerd om S 2− . te genereren in een alkalische oplossing en de verhoogde pH kan de productie van S 2− . bevorderen . Daarom kunnen de toenames in de roodverschuiving van de band-gap-overgang met de pH van de voorloperoplossing worden toegeschreven aan de verhoogde hoeveelheden S gedoteerd in Sb2 O3 bij hogere pH's. Daarom kan de hoeveelheid S-doping worden gecontroleerd door eenvoudig de pH van de voorloperoplossing aan te passen.
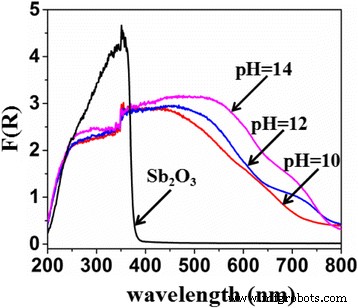
Diffuse reflectie-absorptiespectra van Sb2 O3 en Sb2 O3 -S-pH (pH = 10, 12 en 14)
TEM werd gedaan om de morfologie en kristalstructuur van S-gedoteerde Sb2 te identificeren O3 . Zoals weergegeven in Afb. 3a, is de Sb2 O3 -S-12 was staafvormig met een diameter van ~ 40 nm en een lengte variërend van 100 tot 200 nm. Het HRTEM-beeld onthulde dat de nanostaafjes bestonden uit veel willekeurig geassembleerde nanodeeltjes met een gemiddelde diameter van ~ -5 nm (figuur 3b). Duidelijke diffractiepatronen met interplanaire afstanden van 0,25 en 0,27 nm werden waargenomen in de HRTEM-beelden, die kunnen worden toegewezen aan de (200) en (131) vlakken van Sb2 O3 , respectievelijk. De EDS-analyse (Fig. 3c) onthulde dat Sb-, O- en S-elementen in de monsters aanwezig waren, wat aangeeft dat de S-gedoteerde Sb2 O3 is met succes voorbereid.

een TEM. b HRTEM-afbeeldingen en c EDS-spectrum van Sb2 O3 -S-12
De XPS-spectra en Sb 3d met hoge resolutie en de O 1s XPS-spectra van Sb2 O3 en Sb2 O3 -S-pH (pH = 10 en 12) worden weergegeven in Fig. 4a. De Sb 3d 3/2 piek van Sb2 O3 verscheen bij 539,8 eV en de piek bij 530,5 eV werd toegewezen aan Sb 3d 5/2 en O 1s, wat suggereert dat de oxidatietoestand van Sb + 3 is in plaats van + 5 met iets hogere bindingsenergieën [37, 38]. De S-doping verminderde de bindingsenergieën van Sb 3d, maar vertoonde geen significante effecten op de chemische toestand van Sb. Deze resultaten gaven aan dat de S-doping de chemische omgeving van de Sb-ionen veranderde en de elektronendichtheden rond de Sb-ionen verhoogde vanwege de lagere elektronegativiteit van S [39]. Vergeleken met Sb2 O3 -S-10, Sb2 O3 -S-12 bevatte meer S. De elektronendichtheid rond zijn Sb was hoger dan die van Sb2 O3 -S-10, en dus de Sb 3d bindingsenergie van Sb2 O3 -S-12 verschoof in de richting van lage energie. De S 2p XPS-spectra met hoge resolutie in figuur 4b onthulden twee pieken bij 161,5 en 162,7 eV die werden toegeschreven aan S 2− [22, 40, 41]. De straal van S 2− (184 uur) is veel groter dan die van O 2− (132 uur). Daarom was het moeilijk voor S 2− om de O 2− . te vervangen in Sb2 O3 [22, 42]. Het is zeer waarschijnlijk dat S 2− ingevoerd in de interstitiële site van de Sb2 O3 kristal [18]. XPS-analyse gaf aan dat Sb2 O3 -S-12 bevatte meer S dan Sb2 O3 -S-10, wat verder bevestigt dat de pH van de voorloperoplossing kan worden gebruikt om de hoeveelheid S-doping onder controle te houden.
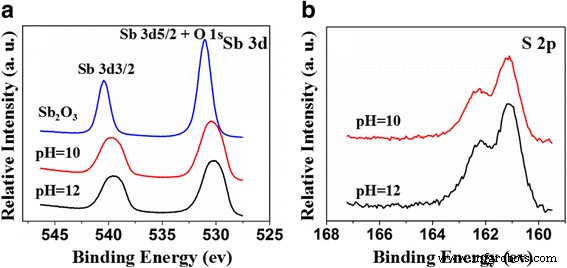
XPS-spectra van Sb2 O3 en Sb2 O3 -S-pH (pH = 10 en 12). een Sb 3d. b S 2p
Afbeelding 5 toont de Raman-spectra van de Sb2 O3 en Sb2 O3 -S-12. Sb2 O3 vertoonde signaal op 216, 257, 293, 442, 498, 593 en 680 cm −1 . Er verscheen een nieuwe piek op 1440 cm −1 in de spectra van Sb2 O3 -S-12, wat het resultaat kan zijn van de S-doping. Bovendien, vergeleken met de pieken van Sb2 O3 , de piekbreedte van de pieken van Sb2 O3 -S-12 nam toe en de symmetrie van hun piekvormen nam af, wat aangeeft dat de S-doping de interne defecten verhoogde [43]. De S gedoteerd in de interstitiële site van Sb2 O3 kristallen veroorzaakten de vervorming van het rooster.
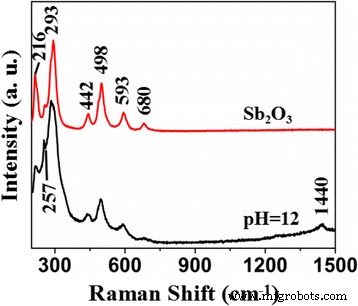
Raman-spectra van Sb2 O3 en Sb2 O3 -S-12
De door zichtbaar licht aangestuurde fotokatalytische activiteiten van pure en S-gedoteerde Sb2 O3 voor de afbraak van MO werden bepaald. De tijdelijke veranderingen in de MO-concentratie werden gevolgd door de UV-vis-absorptie van de MO-oplossing over de fotokatalysator bij 464 nm te meten (figuur 6a). MO lijkt zeer stabiel onder zichtbaar licht met bijna geen degradatie. Sinds de Sb2 O3 kon niet worden geëxciteerd onder zichtbaar licht, de MO-degradatie was verwaarloosbaar in de aanwezigheid van Sb2 O3 . Doping met een bepaalde hoeveelheid S zou de absorptie van zichtbaar licht verbeteren, de interne defecten vergroten en de scheidingssnelheid van de door foto gegenereerde elektron-gatparen bevorderen. Als gevolg hiervan kon de door zichtbaar licht aangedreven fotokatalytische activiteit van de monsters worden verbeterd, wat kan worden aangetoond door de S-gedoteerde Sb2 O3 . Het is opmerkelijk dat de fotokatalytische activiteiten van het S-gedoteerde Sb2 O3 bereid bij verschillende pH's waren verschillend. Sb2 O3 -S-10 vertoonde de laagste door zichtbaar licht aangedreven fotokatalytische activiteit. Het kan worden verklaard dat de hydrolyse van TAA onder zwak alkalische omstandigheden zwak is en minder S 2− produceert. . De Sb2 O3 -S-14 met meer S geproduceerd onder sterk alkalische omstandigheden vertonen een lagere fotokatalytische activiteit vergeleken met de Sb2 O3 -S-12 met relatief minder S, wat kan worden toegeschreven aan de overmatige S-doping die te veel defecten veroorzaakte die de recombinatiecentra waren van het fotogegenereerde elektron-gatpaar. Vergeleken met de tegenhangers, Sb2 O3 -S-12 vertoonde de hoogste door zichtbaar licht aangestuurde fotokatalytische activiteit en was in staat om 99,2% MO in 40 minuten af te breken onder bestraling met zichtbaar licht. Afbeelding 6b toont de spectrale patronen van de absorptie in de tijd van MO tijdens de fotodegradatie over Sb2 O3 -S-12. De absorptie van MO was 464 nm, wat werd toegeschreven aan de -N=N- eenheid. De absorptie-intensiteit nam af naarmate de bestraling met zichtbaar licht vorderde, wat aangeeft dat de -N=N- dubbele bindingen geleidelijk werden afgebroken [44].
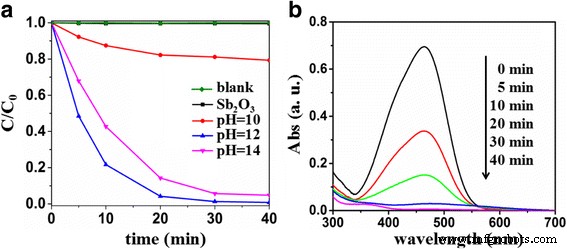
een Tijdelijke veranderingen van de MO-concentratie zoals gevolgd door de UV–vis-absorptiespectra bij 464 nm op Sb2 O3 en Sb2 O3 -S-pH (pH = 10, 12 en 14). b Spectrale absorptiepatronen in de tijd van MO tijdens het fotodegradatieproces over Sb2 O3 -S-12
De fotokatalytische prestaties van Sb2 O3 -S-12 voor de afbraak van p-hydroxyazobenzeen werd ook bepaald. Afbeelding 7a, b geeft de fotokatalytische activiteit van Sb2 . weer O3 -S-12 voor de p-hydroxybenzobenzeenafbraak en de overeenkomstige UV–vis absorptiespectra van p-hydroxybenzobenzeen tijdens de afbraak. Er werd geen p-hydroxyazobenzeenafbraak waargenomen onder de bestraling met zichtbaar licht in afwezigheid van Sb2 O3 -S-12. Daarentegen werd 94,3% p-hydroxyazobenzeen afgebroken onder bestraling met zichtbaar licht gedurende 150 min in aanwezigheid van Sb2 O3 -S-12. Bovendien nam de absorptie van p-hydroxybenzobenzeen bij 347 nm af naarmate de bestraling langer duurde. Deze resultaten gaven aan dat S-gedoteerde Sb2 O3 zou kunnen worden toegepast bij de afbraak van verschillende verontreinigende stoffen.
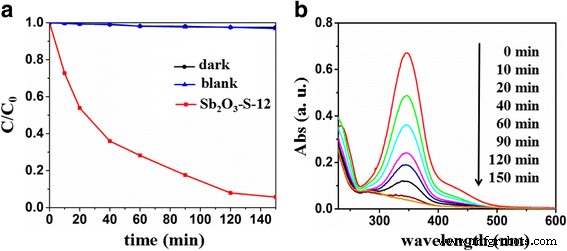
een Tijdelijke veranderingen van de 4-fenylazofenolconcentratie zoals gevolgd door de UV–vis-absorptiespectra bij 347 nm op Sb2 O3 -S-12. b Spectrale absorptiepatronen in de tijd van 4-fenylazofenol tijdens het fotodegradatieproces over Sb2 O3 -S-12
Onderzoek naar het fotokatalytische mechanisme van de S-gedoteerde Sb2 O3 nanokristallen, de belangrijkste oxidatieve soorten in de fotokatalytische reactie, werden gevangen met behulp van p -benzochinon (BZQ, een O2 − · radicalenvanger), dinatriumethyleendiaminetetraacetaat (Na2 -EDTA, een gatenvanger) en tert-butanol (t-BuOH, een OH-radicaalvanger) [39, 45]. Zoals getoond in Fig. 8, vertoonde de toevoeging van t-BuOH geen nadelig effect op de fotokatalytische activiteit van Sb2 O3 -S-12 en de aanwezigheid van BZQ of Na2 -EDTA vertraagde de efficiëntie van de fotokatalytische afbraak van MO en 4-fenylazofenol aanzienlijk. Daarom kan worden geconcludeerd dat h + en O2 − · radicalen waren de dominante oxidatieve soorten van het S-gedoteerde Sb2 O3 fotokatalyse en het OH·-radicaal waren niet betrokken.
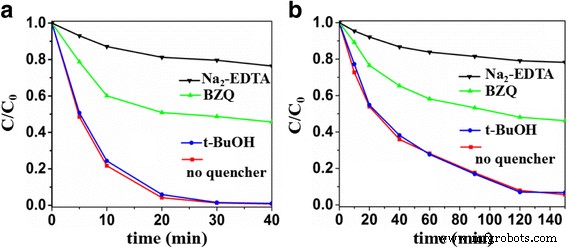
Vangexperiment van actieve soorten over Sb2 O3 -S-12 tijdens de fotokatalytische afbraak van a MO. b 4-Fenylazofenol
Op basis van deze discussies, een mogelijk mechanisme voor fotokatalytische afbraak van MO via S-gedoteerde Sb2 O3 nanokristallen werd als volgt voorgesteld (schema 1). S-gedoteerde Sb2 O3 kan efficiënt worden geëxciteerd om gaten in VB en elektronen in geleidingsband (CB) te creëren onder bestraling met zichtbaar licht. De S-doping verhoogde de VB-breedte van Sb2 O3 . De elektronen zijn lang genoeg om te reageren met geadsorbeerde O2 om O2 . te produceren − · radicalen. De fotogegenereerde h + en O2 − · vertoonde een sterk oxidatiepotentieel dat MO en 4-fenylazofenol direct kan oxideren tot afgebroken producten.
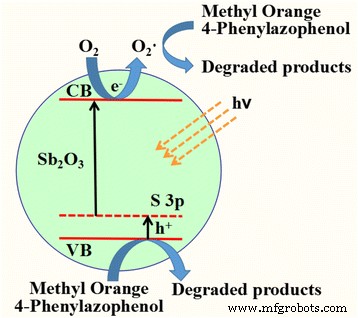
Mogelijk mechanisme van de fotokatalytische afbraak van MO of 4-fenylazofenol over Sb2 O3 -S-12 zichtbaar licht fotokatalysator
Conclusies
De S-gedoteerde Sb2 O3 nanokristallen werden met succes bereid uit SbCl3 en TAA via een gemakkelijke eenstaps hydrothermische methode onder alkalische omstandigheden. S is binnengekomen op de interstitiële site van Sb2 O3 kristallen als S 2− , waardoor het absorptiebereik voor zichtbaar licht werd verbreed. De pH van de voorloperoplossing kan de S-dopinghoeveelheid aanzienlijk beïnvloeden, wat de door zichtbaar licht aangestuurde fotokatalytische activiteit van het S-gedoteerde Sb2 verder afwisselt. O3 nanokristal. Het nanokristal bereid bij pH 12 vertoonde de hoogste door zichtbaar licht aangedreven fotokatalytische activiteit en was in staat om 99,2% MO en 94,3% p-hydroxybenzobenzeen af te breken in respectievelijk 40 en 150 minuten onder bestraling met zichtbaar licht. De fotokatalytische afbraak in zichtbaar licht van MO en p -hydroxyazobenzeen door S-gedoteerde Sb2 O3 zijn behaald door h + en O2 − ·.
Afkortingen
- BZQ:
-
p -Benzochinon
- MO:
-
Methylsinaasappel
- Na2 -EDTA:
-
Dinatriumethyleendiaminetetraacetaat
- S:
-
Zwavel
- TAA:
-
Thioacetamide
- t-BuOH:
-
Tert-butanol
Nanomaterialen
- Gebruik checklists voor een efficiëntere installatie
- S, N co-gedoteerde grafeen Quantum Dot/TiO2-composieten voor efficiënte fotokatalytische waterstofgeneratie
- One-Pot Green-synthese van met Ag versierde SnO2-microsfeer:een efficiënte en herbruikbare katalysator voor reductie van 4-nitrofenol
- Een nieuwe methode zonder organisch oplosmiddel voor gerichte nanodrug voor verbeterde werkzaamheid tegen kanker
- Verkenning van Zr–Metal–Organic Framework als efficiënte fotokatalysator voor waterstofproductie
- Hiërarchische heterostructuur van ZnO@TiO2 holle bollen voor zeer efficiënte fotokatalytische waterstofevolutie
- Op trifenylfosfine gebaseerd functioneel poreus polymeer als een efficiënte heterogene katalysator voor de synthese van cyclische carbonaten uit CO2
- Verbeterde prestaties van een nieuwe anodische PdAu/VGCNF-katalysator voor elektro-oxidatie in een glycerolbrandstofcel
- Een efficiënt en effectief ontwerp van InP-nanodraden voor maximale oogst van zonne-energie
- PtNi-legering Cocatalyst-modificatie van eosine Y-gesensibiliseerde g-C3N4/GO-hybride voor efficiënte zichtbaar-licht fotokatalytische waterstofevolutie
- Richtlijnen voor CNC-programmering voor efficiënt CNC-proces



