Het in kaart brengen van de structurele, elektrische en optische eigenschappen van hydrothermisch gegroeide met fosfor gedoteerde ZnO-nanostaafjes voor opto-elektronische apparaattoepassingen
Abstract
De met fosfor gedoteerde ZnO-nanostaafjes werden bereid met behulp van een hydrothermisch proces, waarvan de structurele modificaties als functie van de doteringsconcentratie werden onderzocht met behulp van röntgendiffractie. De doteringsconcentratie-afhankelijke verbetering in lengte en diameter van de nanostaafjes had de fosfordotering in ZnO-nanostaafjes vastgesteld. De geleidelijke transformatie in het type geleidbaarheid zoals waargenomen uit de variatie van de dragerconcentratie en de Hall-coëfficiënt had de fosfordotering verder bevestigd. De wijziging van de dragerconcentratie in de ZnO-nanostaafjes als gevolg van fosfordoping werd begrepen op basis van de amfotere aard van de fosfor. De ZnO-nanostaafjes vertoonden in afwezigheid van fosfor de fotoluminescentie (PL) in het bereik van de ultraviolette (UV) en zichtbare regimes. De UV-emissie, d.w.z. bijna-band-edge-emissie van ZnO, bleek rood te zijn verschoven na de dotering van fosfor, wat werd toegeschreven aan de vorming van donor-acceptorpaar. De waargenomen emissies in het zichtbare regime waren te wijten aan de diepe emissies die werden opgewekt door verschillende defecten in ZnO. De met Al-gedoteerde ZnO-zaadlaag bleek verantwoordelijk te zijn voor de waargenomen nabij-infrarood (NIR) -emissie. De PL-emissie in UV- en zichtbare regimes kan een breed scala aan toepassingen dekken, van biologische tot opto-elektronische apparaten.
Inleiding
ZnO is een van de meest veelbelovende halfgeleidende materialen, die veel aandacht heeft gekregen vanwege zijn unieke en gemakkelijk afstembare fysische en chemische eigenschappen [1,2,3,4,5,6,7,8,9,10,11]. Het is bekend dat de ZnO een intrinsieke n-type halfgeleider is. De p-type geleidbaarheid in ZnO speelt een sleutelrol bij de vorming van homojunctie, die verschillende toepassingen heeft, waaronder lichtemitterende diodes [12], elektrisch gepompte willekeurige lasers [2] en fotodetectoren [9]. Tot nu toe zijn er verschillende pogingen ondernomen om de p-type geleidbaarheid in de ZnO-matrix te induceren door verschillende elementen zoals antimoon (Sb), arseen (As), stikstof (N), fosfor (P) of andere elementen te doteren [2, 5,6,7,8,9]. Weinig van deze elementen zullen echter waarschijnlijk falen in het induceren van de p-type geleidbaarheid omdat ze diepe acceptoren vormen en daarom niet bruikbaar worden. De schijnbare knelpunten met de p-type doping in ZnO zijn de initiële prestatie en hun reproduceerbaarheid en stabiliteit [7]. Gelukkig kunnen de stabiliteits-/degradatieproblemen worden vermeden in het geval van fosfor in ZnO door de thermische activering met behulp van een snel thermisch gloeiproces [15]. Bovendien bleken de met fosfor gedoteerde ZnO-dunne films tot 16 maanden stabiel te zijn onder omgevingsomstandigheden volgens Allenic et al. [14]. Daarom werd fosfor beschouwd als een van de meest betrouwbare en stabiele voor het induceren van de p-type geleidbaarheid in ZnO onder de bovengenoemde doteermiddelen. Bovendien bleek de fosfor in ZnO-nanostructuren de zuurstofvacature-gerelateerde fotoluminescentie (PL) -emissie in het zichtbare gebied te veroorzaken [8, 16]. Hoewel er verschillende rapporten zijn over de PL-emissiestudie van ZnO-nanostructuren [17,18,19,20,21,22], een systematische studie die de luminescentie in de drie verschillende en belangrijke regimes van de elektromagnetische spectra inclusief ultraviolet ( UV), zichtbare en nabij-infrarood (NIR) regimes samen met hun elektrische en structurele eigenschappen is vrij schaars.
In de huidige studie rapporteren we de succesvolle dotering van fosfor in ZnO-nanostaafjes met behulp van de hydrothermische methode, een van de kosteneffectieve, schaalbare, grootschalige en lage-temperatuurtechnieken. Het fosfor bleek amfoteer van aard te zijn, hetgeen tot stand kwam door een onconventionele variatie van het type geleidbaarheid en dragerconcentratie als functie van de doteringsconcentratie. We demonstreren verder de PL-emissie in de UV-, zichtbare en NIR-regio's door gecontroleerde dotering van fosfor in de ZnO-nanostaafjes gekweekt op Al-gedoteerde ZnO-zaadlaag. Het onderliggende mechanisme van de huidige bevindingen wordt besproken aan de hand van verschillende defecttoestanden in het bestaande systeem. Het meest interessante aspect van de huidige studie is het bereiken van emissie in twee verschillende regimes (UV en zichtbaar) in een enkel systeem door zorgvuldig een geschikte combinatie van de nanostructuren, zaadlaag en doteermiddelen te kiezen.
Methoden
Voorbereiding van de zaadlaag
Een kiemlaag van met Al-gedoteerde ZnO-film van ongeveer 100 nm werd gekweekt met behulp van radiofrequentie (RF) sputterafzetting met een 2% aluminiumoxide ZnO-doelwit op een set gereinigde kwartssubstraten (figuur 1a). De substraten werden gereinigd in aceton en isopropylalcohol met behulp van ultrasone trillingen, waarna de substraten zorgvuldig werden gedroogd met stikstofgas. Het sputteren van de zaadlaag werd gedurende 40 min uitgevoerd met behulp van een RF-vermogen van 90 W en 60 SCCM van Ar-gasstroom. De reden voor het kiezen van de met Al-gedoteerde ZnO-film als kiemlaag was vanwege de betere geleidbaarheid en meer doorlaatbaarheid in vergelijking met pure ZnO-film [23].
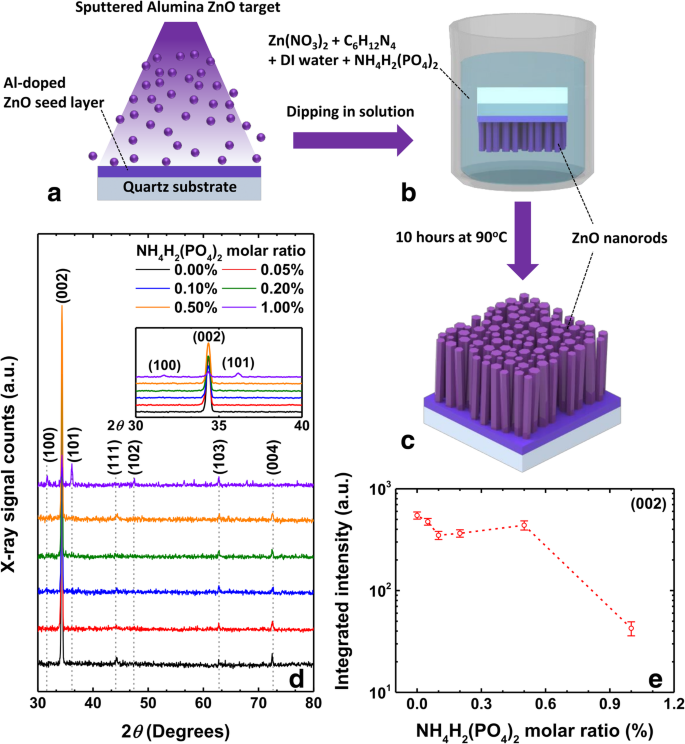
Schematische weergave van de met Al-gedoteerde ZnO-zaadlaag (a ), groeiproces van ZnO-nanostaafjes (b ), en gekweekte ZnO-nanostaafjes (c ). De XRD-patronen (d ) van de ZnO-nanostaafjes die overeenkomen met variërende NH4 H2 (PO4 )2 M-verhouding. De geïntegreerde intensiteit van (002) piek als functies van NH4 H2 (PO4 )2 M-verhouding (e )
Groei van ZnO-nanostaafjes
De ongedoteerde ZnO-nanostaafjes werden gekweekt door hydrothermische methode met behulp van zinknitraathexahydraat (Zn(NO3 )2 , reagenskwaliteit (98%) en hexamethyleentetramine (HMTA, C6 H12 N4 , ≥ 99,0%). Een oplossing van zinknitraat en HMTA van 0,06 M in een volume van 400 ml werd bereid door 2 uur te roeren. De met fosfor gedoteerde ZnO-nanostaafjes werden bereid door toevoeging van ammoniumdiwaterstoffosfaat (NH4 H2 (PO4 )2 , ≥ 98%) aan de bovenstaande chemicaliën in de M-verhoudingen van 0%, 0,05%, 0,1%, 0,2%, 0,5% en 1%. De met zaadlaag afgezette kwartssubstraten werden in deze bekers gedompeld en gedurende 10 uur in de oven bij 90 ° C gehouden (figuur 1b). Vervolgens werden deze monsters gespoeld met gedeïoniseerd water en grondig gedroogd met stikstofgas om bij de verticaal uitgelijnde met fosfor gedoteerde ZnO-nanostaafjes te komen door de resten te verwijderen (Fig. 1c).
Karakterisatiemethoden
De oppervlaktemorfologie van de monsters werd onderzocht met behulp van een scanning elektronenmicroscoop (SEM). Het effect van doping op de structurele eigenschappen van de monsters werd onderzocht met behulp van poedervormige röntgendiffractie (XRD). Hall-effectmetingen werden uitgevoerd op alle monsters om het type geleidbaarheid van de monsters te begrijpen, waarbij het magnetische veld van 0,5 T is toegepast. De PL-metingen bij kamertemperatuur werden uitgevoerd met een excitatiegolflengte van 266 nm (Nd-YAG-gepulseerde laser) en een invallend vermogen van 150 mW.
Resultaten en discussie
Om de structurele veranderingen als gevolg van de opname van fosfor in ZnO-nanostaafjes te begrijpen, hebben we de poedermodus XRD-metingen uitgevoerd, waarvan de grafieken worden weergegeven in Fig. 1d. We merken hier op dat het ongedoteerde monster de diffractiepieken vertoont bij 34,36 °, 44,27 °, 62,80 ° en 72,45 ° overeenkomend met respectievelijk (002), (111), (103) en (004) vlakken van ZnO. De piek die overeenkomt met (002) vlak toont de hoogste intensiteit, en de piekpositie verandert niet ongeacht NH4 H2 (PO4 )2 M-verhouding en de resulterende veranderingen in diameter / lengte van de nanostaafjes. Bij het verhogen van de NH4 H2 (PO4 )2 M-verhouding, de geïntegreerde intensiteit van de hoogste intensiteitspiek, d.w.z. (002) piek, neemt geleidelijk af zoals weergegeven in figuur 1e. Het enige verschil in deze monsters is de variatie van de M-verhouding; daarom kan het worden toegeschreven aan de verminderde kristallijne aard van de ZnO-nanostaafjes [24]. Een ding om hier op te merken is echter de volledige breedte op half maximum (FWHM) van de (002) piek. De FWHM bleek bijna hetzelfde te zijn rond 0,25°, ongeacht de NH4 H2 (PO4 )2 M-verhouding. In deze perspectieven is het ook zeer waarschijnlijk dat de verkeerde uitlijning van de nanostaafjes in c -as kan ook leiden tot de afname van de geïntegreerde (002) piekintensiteit. Wanneer de M-verhouding van NH4 H2 (PO4 )2 bereikt tot 1%, werden drie extra pieken waargenomen onder hoeken van 31,70 °, 36,17 ° en 47,50 °, die respectievelijk verband houden met (100), (101) en (102) pieken van ZnO-kristal. Het verschijnen van deze extra pieken komt ook goed overeen met de bovengenoemde bewering.
De boven- en dwarsdoorsnede van SEM-afbeeldingen van de ongedoteerde en gedoteerde (tot 1%) monsters worden getoond in Fig. 2a-f, waar een uniforme verdeling van de hexagonale nanostaafjes kan worden opgemerkt. Zoals besproken in de bovenstaande paragraaf, bleken de diameter en lengte van de nanostaafjes groter te zijn bij het verhogen van de NH4 H2 (PO4 )2 M-verhouding, die respectievelijk kan worden waargenomen in de inzet (bovenaanzicht) en rechterkant (dwarsdoorsnede) van elk beeld. In het ongedoopte monster (0% van NH4 H2 (PO4 )2 M-verhouding), werd opgemerkt dat de gemiddelde diameter van de nanostaafjes ongeveer 60 nm was, die geleidelijk bleef toenemen tot 145 nm bij het verhogen van de dopingconcentratie zoals weergegeven in de inzet van Fig. 2a-f. Evenzo bleek de lengte van de nanostaafjes ook te worden verhoogd met de dopingconcentratie, hoewel vrij weinig toename, zoals te zien is aan de rechterkant van elke afbeelding. De lengte en diameter van de nanostaafjes zijn uitgezet als functies van NH4 H2 (PO4 )2 M-verhouding in respectievelijk Fig. 3a en b. In de inzet van deze figuren tonen we de schematische illustratie van verticaal gegroeide ZnO-nanostaafjes om hun lengte en diameter aan te geven. Opgemerkt kan worden dat de lengte van deze nanostaafjes ook snel toeneemt van 1,35 m tot 2,5 m bij verhoging van de NH4 H2 (PO4 )2 M-verhouding van 0% tot 0,1% en verzadigt bijna boven deze M-verhouding. Een vergelijkbare trend in de variatie in diameter van de nanostaafjes werd opgemerkt (figuur 3b). De verbeterde lengte en diameter van de nanostaafjes tot 0,1% NH4 H2 (PO4 )2 M-verhouding wordt toegeschreven aan de grotere omvang van de fosfor in vergelijking met zuurstofatomen in het ZnO [12, 13, 25]. Boven de 0,1% M-verhouding kan de aard van de lengte- en diametervariatie worden begrepen op basis van de verzadiging van de oplosbaarheidslimiet van het opnemende fosfor in de ZnO-matrix [26]. Hoewel alle andere parameters constant bleven of vertraagden om toe of af te nemen, behalve de dopingconcentratie, bleken de lengte en diameter van de nanostaafjes nog steeds groter te zijn, wat wijst op de succesvolle opname van fosfor in de ZnO-nanostaafjes [12, 25]. De chemische reacties die verantwoordelijk zijn voor de groei van ZnO en de dotering van fosfor in de ZnO-kristallen kunnen worden begrepen uit de volgende vergelijkingen [16]:

Bovenste (links) en dwarsdoorsnede (rechts) SEM-afbeeldingen van ZnO-nanostaafjes die overeenkomen met NH4 H2 (PO4 )2 M-ratio's 0% (a ), 0,05% (b ), 0,1% (c ), 0,2% (d ), 0,5% (e ), en 1,0% (f ), respectievelijk. Diameter en lengte van de nanostaafjes namen toe als functies van NH4 H2 (PO4 )2 M-verhouding. De verbetering van de volumetrische kenmerken van de nanostaafjes is te danken aan de verhoogde opname van fosfor
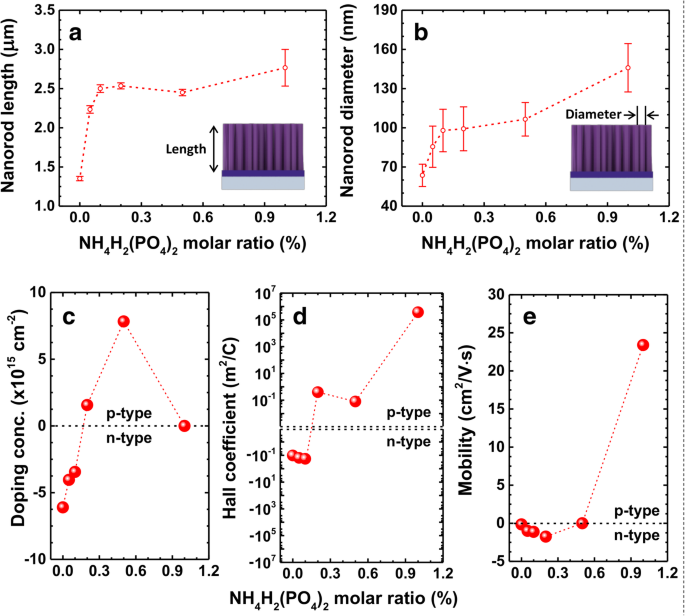
een , b Kwantitatieve weergaven van de lengte en diameter van ZnO-nanostaafjes met een toename van NH4 H2 (PO4 )2 M-verhouding, respectievelijk. c –e De veranderingen in dopingconcentratie, Hall-coëfficiënt en mobiliteit van de nanostaafjes als functies van NH4 H2 (PO4 )2 M-verhouding, respectievelijk. Geleidbaarheid veranderde van negatief naar positief toen NH4 H2 (PO4 )2 M-ratio is hoger dan ongeveer 0,3%. De afname van de doteringsconcentratie van de nanostaafjes die overeenkomt met 1% NH4 H2 (PO4 )2 M-verhouding is te wijten aan het zelfcompensatie-effect voorbij de oplosbaarheidsgrens van fosfor in de ZnO-nanostaafjes
$$ \mathrm{Zn}{\left({\mathrm{NO}}_3\right)}_2\to {\mathrm{Zn}}^{2+}+2{\mathrm{NO}}_3^{ -} $$ (1) $$ {\mathrm{C}}_6{\mathrm{H}}_{12}{\mathrm{N}}_4+10{\mathrm{H}}_2\mathrm{O }\leftrightarrow 6\mathrm{HCHO}+4{{\mathrm{N}\mathrm{H}}_4}^{+}+4{\mathrm{OH}}^{-} $$ (2) $$ {\mathrm{Zn}}^{2+}+2{\mathrm{OH}}^{-}\leftrightarrow \mathrm{Zn}{\left(\mathrm{OH}\right)}_2\to \mathrm {Zn}\mathrm{O}+{\mathrm{H}}_2\mathrm{O} $$ (3) $$ \mathrm{N}{\mathrm{H}}_4{\mathrm{H}}_2 \mathrm{P}{\mathrm{O}}_4+2{\mathrm{O}\mathrm{H}}^{-}\to {{\mathrm{NH}}_4}^{+}+2{ \mathrm{H}}_2\mathrm{O}+{\mathrm{PO}}_4^{3-} $$ (4) $$ 3{\mathrm{Zn}}^{2+}+2{{ \mathrm{PO}}_4}^{3-}\to {\mathrm{Zn}}_3{\left({\mathrm{PO}}_4\right)}_2\downarrow $$ (5)In het hydrothermische proces zou het zinknitraat bij verhoging van de temperatuur in eerste instantie ontleden in Zn 2+ en nitraationen. Aan de andere kant geeft de chemische reactie tussen HMTA en watermolecuul aanleiding tot formaldehyde, ammoniumionen en hydroxylionen zoals hierboven weergegeven in Vgl. (2). Deze hydroxylionen reageren met de Zn 2+ ionen en leiden tot de vorming van ZnO en H2 O moleculen. Bovendien reageert het ammoniumdiwaterstoffosfaat met de reeds aanwezige hydroxylionen in het bekerglas en vormt het samen met ammoniumionen en een watermolecuul fosfaationen. We merken hier op dat deze fosfaationen reageren met de zinkionen om zinkfosfaat te vormen (Zn3 (PO4 )2 ) neerslag, wat schadelijk is voor de opname van fosfor in ZnO-nanostaafjes [16]. Omdat het zinknitraat echter het sterke zuur en het sterke alkalische zout is, heeft het de potentie om de kans op zinkfosfaatprecipitatie te minimaliseren en dus de kans op succesvolle opname van fosfor in ZnO-nanostaafjes [16] te vergroten. Het is bekend dat de fosfordotering in ZnO-nanostaafjes p-type geleidbaarheid induceert vanwege hun inherente n-type geleidbaarheid [7, 27, 28], wat de dotering van fosforatomen verder zal valideren.
Met behulp van de Hall-effectmetingen onderzoeken we het effect van fosfordotering op elektrische eigenschappen zoals het type geleidbaarheid, doteringsconcentratie en mobiliteit van ladingsdragers. Over het algemeen is het meten van Hall-effect van nanostaafjes en/of nanodraden behoorlijk uitdagend vanwege de eendimensionale geometrie. Het is dus duidelijk dat de één-op-één Hall-meting van enkele nanostaafjes waarschijnlijk de meest nauwkeurige is. De methode is echter meestal geldig voor nanostaafjes of nanodraden met een brosse en lage dichtheid, waarvoor uitdagende verwerkingsprocedures vereist zijn [45]. In dit geval wordt Hall-effectmeting mogelijk gemaakt door met Al-gedoteerde ZnO-zaadlaag onder ZnO-nanostaafjes als geleidend medium. Vanwege de elektrische imperfectie van de met Al-gedoteerde ZnO-zaadlaag als medium voor stroom, kan de meting mogelijk de werkelijke elektrische eigenschappen van de ZnO-nanostaafjes onderschatten. Het resultaat kan echter nog laten zien hoe de NH4 H2 (PO4 )2 M-verhouding verandert de elektrische eigenschappen van ZnO-nanostaafjes. De afhankelijkheid van dragerconcentratie, Hall-coëfficiënt en mobiliteit van NH4 H2 (PO4 )2 M-verhouding wordt geïllustreerd in respectievelijk figuur 3c, d en e. De dragerconcentraties voor 0%, 0,05%, 0,1%, 0,2%, 0,5% en 1% M-verhoudingen zijn − 6.1 × 10 15 , − 4.0 × 10 15 , − 3.4 × 10 15 , 1.6 × 10 15 , 7,8 × 10 15 , en 1,67 × 10 9 cm −2 , respectievelijk. Het negatieve teken in de dopingconcentratie van de monsters lager dan 0,2% van de NH4 H2 (PO4 )2 M-verhouding geeft hun n-type geleidbaarheid aan, en het positieve teken in de overige monsters onthult hun p-type geleidbaarheid. ZnO-nanostaafjes vertonen inderdaad intrinsieke n-type geleidbaarheid vanwege de aanwezigheid van zuurstofvacature-gerelateerde defecten en/of Zn-interstitials, maar de details zijn controversieel [7, 27, 28]. Echter, met toenemende NH4 H2 (PO4 )2 M-verhouding worden de ZnO-nanostaafjes geleidelijk getransformeerd in de p-type staafjes door hun intrinsieke negatieve geleidbaarheid te compenseren. De p-type geleidbaarheid door de opname van fosfor wordt ook waargenomen in dunne ZnO-films [29,30,31]. Aan de andere kant, de nanostaafjes die overeenkomen met 1% van NH4 H2 (PO4 )2 M-ratio vertoonde een heel ander gedrag in vergelijking met de vorige rapporten. Zoals weergegeven in figuur 3c, komt het monster overeen met 0,5% NH4 H2 (PO4 )2 M-verhouding toonde de hoogste dragerconcentratie rond 7,8 × 10 15 cm −2 en daalt tot 1,67 × 10 9 cm −2 ineens zodra de NH4 H2 (PO4 )2 M-ratio werd verhoogd tot 1%. We nemen aan dat deze verandering te wijten is aan het amfotere gedrag van fosfor in ZnO [27]. De fosfor fungeert als acceptor of donor, afhankelijk van of de fosfor zuurstofplaatsen vervangt (PO ) of Zn-sites (PZn ), respectievelijk. In [27] wordt gerapporteerd dat de oplosbaarheid van p-type doteermiddelen in ZnO laag is. In deze regimes, door opname van overtollig fosfor boven de oplosbaarheidslimiet, vervangen ze de Zn-plaatsen en compenseren ze zichzelf met PO en kan daardoor de geleidbaarheid van het p-type verliezen. De oplosbaarheidslimiet van fosfor is ongeveer 10 20 cm −3 wanneer Zn3 P2 is gebruikt voor fosfordotering in de ZnO-matrix [27]. We kunnen echter niet duidelijk zeggen hoeveel de oplosbaarheidsgrens van fosfor is als het gaat om het kweken van p-type ZnO met NH4 H2 (PO4 )2 via een hydrothermisch proces, maar we denken dat de oplosbaarheidsgrens ergens rond de 7,8 × 10 15 moet liggen cm −2 . Het is opmerkelijk dat de dragerconcentratie kan worden verhoogd door een postthermisch gloeiproces zoals vermeld in [16]. Het annealingsproces verandert echter niet alleen de dragerconcentraties, maar ook hun diameter, lengte en dichtheid van de nanostaafjes [16]. Het uitgloeien van de nanostaafjes werd dus niet overwogen in het huidige werk. De Hall-coëfficiënten (R H ) voor een halfgeleider kan worden gegeven door R H = 1/n c e [32], waar n c vertegenwoordigt de concentratie van ladingsdragers, waarvan het teken negatief en positief is voor respectievelijk n-type en p-type halfgeleiders, waarbij de ladingsdragers respectievelijk elektronen en gaten zijn. De variatie van R H (getoond in Fig. 3d) bevestigt verder de transformatie van geleidbaarheid van n-type naar p-type in de ZnO-nanostaafjes. Het is bekend dat de Hall-coëfficiënt en mobiliteit verband houden met de vergelijking μ = σR H [32], waarbij σ geeft de elektrische geleidbaarheid weer. Opgemerkt kan worden dat de mobiliteit recht evenredig is met de Hall-coëfficiënten, en daarom volgt de variatie van mobiliteit als functie van de dopingconcentratie ook de aard van R H curve (zoals weergegeven in Afb. 3e).
Figuur 4a toont de genormaliseerde reflectie van de ongedoteerde en met fosfor gedoteerde monsters, die werden gemeten in de diffuse reflectiegeometrie. Het is bekend dat de scherpe daling rond 380 nm in de reflectiespectra de optische bandgap van de ZnO-monsters aangeeft. Het tailing-effect na de doping kan worden opgemerkt in de scherpe daling, die duidt op een verandering in de optische bandgap als gevolg van de dotering van fosfor in ZnO-nanostaafjes. Om de optische bandgap van deze monsters te bepalen, hebben we de Kubelka-Munk (KM) -functie gebruikt, die werd verkregen uit de reflectiespectra. De relatie tussen de KM-functie (F (R )) en reflectie wordt gegeven door F (R ) = (1−R) 2 /2R [33], waarbij R vertegenwoordigt de reflectie van de monsters, waarvan de bijbehorende KM-functie is uitgezet met behulp van de Tauc-relatie (getoond in figuur 4b). De optische bandgaps van alle monsters werden geschat op basis van deze Tauc-plots, die worden getoond in de inzet van figuur 4b. De bandgap van ongedoteerd ZnO-monster bleek 3,28 eV te zijn, wat tot 3,18 eV afneemt tot de NH4 H2 (PO4 )2 M-verhouding van 0,1%, en dan neemt de bandgap toe boven deze concentratie, die 3,26 eV bereikt voor het geval van 1% NH4 H2 (PO4 )2 M-verhouding. We merken hier op dat de bandgap van alle samples binnen het bereik van 3,18 en 3,28 eV ligt. Hoewel de bandgap van de ZnO-nanostaafjes wordt verkregen uit de Tauc-plot, wijkt deze echter af volgens veranderingen in NH4 H2 (PO4 )2 M-verhouding. Inderdaad, het verkrijgen van de bandgap van de Tauc-plot is waarschijnlijk niet de juiste manier voor de monsters die in dit artikel worden onderzocht; dit komt omdat de Tauc-plot het excitonisch effect negeert. Om dit probleem op te lossen, hebben we de PL-metingen uitgevoerd op alle monsters [49].
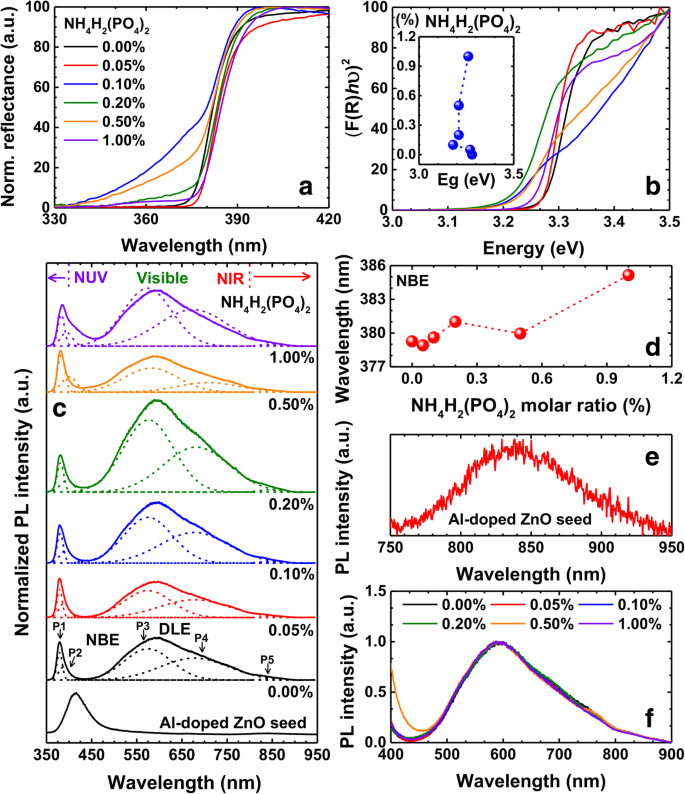
Genormaliseerde reflectie (a ) en bijbehorende Tauc-percelen (b ) voor alle monsters (inzet:NH4 H2 (PO4 )2 M-verhoudingsafhankelijke variatie van optische bandgaps van ZnO-nanostaafjes.). c Genormaliseerde PL-spectra van met Al-gedoteerde ZnO-zaadlaag, niet-gedoteerde ZnO-nanostaafjes en met fosfor gedoteerde ZnO-nanostaafjes. d De PL-piekposities van NBE-emissie als functie van NH4 H2 (PO4 )2 M-verhouding. e De vergrote NIR-emissie van de met Al-gedoteerde ZnO-zaadlaag. v De DLE-emissiepieken van ongedoteerde en gedoteerde ZnO-nanostaafjesmonsters
Figuur 4c toont de genormaliseerde PL-spectra van niet-gedoteerde en met fosfor gedoteerde ZnO-nanostaafjes, evenals met Al-gedoteerde ZnO-zaadlaag. Opgemerkt kan worden dat alle spectra bestaan uit twee prominente pieken, één in het UV-gebied en het andere in het gebied dat zichtbare en NIR-regimes omvat. Het is bekend dat de eerste piek in het UV-gebied verband houdt met de near-band-edge-emissie (NBE) en de andere piek/bult is gerelateerd aan de deep level-emissie (DLE) in de ZnO-nanostaafjes. We merken hier op dat de oorsprong van de emissie op diep niveau in ZnO controversieel is en naar verwachting zal voortkomen uit verschillende soorten defecten en/of vacatures [34,35,36]. Daarom werden de pieken zorgvuldig gedeconvolueerd door rekening te houden met de asymmetrie in deze spectra zoals weergegeven in figuur 4c, wat inzicht geeft in de oorsprong van de waargenomen emissies. Hier moet worden opgemerkt dat de gedeconvolueerde pieken overeenkomen met de UV-, violette, gele, rode en NIR-emissies. De UV-emissie (P1) bij ~ -379 nm in het ongedoteerde ZnO-monster komt overeen met hun bandgap (zoals hierboven besproken). Deze emissie vertegenwoordigt het karakteristieke kenmerk van ZnO, dat ontstaat door vrije excitonische overgangen [14]. Het is opmerkelijk dat de door PL verkregen bandgap 10 meV kleiner is dan die van de Tauc-plot (figuur 4b). De bandgap van ongedoteerde ZnO-nanostaafjes van PL is bijvoorbeeld 3,27 eV, wat overeenkomt met de emissie van 379 nm, en die van de Tauc-plot is 3,28 eV. Dit komt vermoedelijk door de Stokes-shift [48]. Naarmate de dopingconcentratie toeneemt van 0 tot 1%, ondergaat deze emissie een bathochrome verschuiving van 379 naar 384 nm (zoals weergegeven in figuur 4d). Volgens de eerdere rapporten induceert de fosfordoping een emissie bij ~-384 nm, wat te wijten is aan donor-acceptorpaar (DAP) -overgangen [14, 25]. Daarom kan de roodverschuiving in dit geval worden toegeschreven aan de door fosfor geïnduceerde DAP-emissie in de ZnO-nanostaafjes [8, 14]. Het is bekend dat de diameter van de nanostaafjes ook van invloed is op de emissiegolflengte met betrekking tot het oppervlakte-tot-volumeverhouding-afhankelijke getal van het quasi-Fermi-niveau en de verschuiving wordt ernstig zodra de diameter groter is dan 150 nm [44]. De grootste diameter van de onderzochte nanostaafjes is echter ongeveer 150 nm, en de rest is minder dan 150 nm in dit artikel; dus sluiten we het effect van de diameterverandering uit. De violette emissie (P2) waargenomen bij ~-389 nm (in ongedoteerd ZnO-nanostaafjesmonster) is te wijten aan Zn-interstitials, waarvan de emissie ook een roodverschuiving ondergaat, van 389 naar 408 nm, na de doping [37]. De waargenomen gele emissie (P3), binnen het golflengtebereik van 574-587 nm, is te wijten aan de aanwezigheid van interstitiële zuurstofatomen [38, 39]. De aanwezigheid van overmatige zuurstof- of zinkvacatures is verantwoordelijk voor de waargenomen rode emissie (P4) [40, 41], die het golflengtebereik van 678-729 nm bestrijkt (zoals weergegeven in figuur 4c). Geconstateerd kan worden dat de volle breedte op half maximum (FWHM) van de gele en rode emissies veel hoger is in vergelijking met de overige emissies. We merken hier op dat de gemaakte deconvolutie uitsluitend gebaseerd was op de waargenomen asymmetrie van de pieken en het kan gebeuren dat deze twee pieken uit een of meer pieken kunnen bestaan. Daarom kan het bestaan van groene en oranje emissies binnen de bovengenoemde gele respectievelijk rode emissies niet worden uitgesloten. Aan de andere kant bleek de emissie (P5) in het NIR-gebied geen significante verandering te vertonen in zowel de positie als de FWHM van de pieken als een functie van doping, waarvan de variatie binnen de foutbalken ligt (hier niet weergegeven). We merken hier op dat de enige gemeenschappelijke constante factor in al deze monsters de zaadlaag is, die in dit geval Al-gedoteerde ZnO-film is. Bovendien bevestigt het PL-spectrum van alleen de zaadlaag (Fig. 4c, e) de NIR-emissie zoals verwacht, wat kan worden opgemerkt in Fig. 4e. Verder vertoont het PL-spectrum van de zaadlaag een andere emissie bij 425 nm (figuur 4c), wat de karakteristieke NBE-emissie is van de met Al-gedoteerde ZnO-zaadlaag [42]. De reden voor de NIR-emissie van de Al-gedoteerde ZnO-dunne films moet echter nog worden begrepen. Hier moet worden opgemerkt dat de piekposities van emissies op diep niveau geen significante verandering ondergaan als een functie van de dopingconcentratie, terwijl de NBE-emissieveranderingen variëren, zoals weergegeven in figuur 4f. De aanhoudende piekgolflengte ongeacht NH4 H2 (PO4 )2 M-verhouding kan voordelig zijn bij het ontwerpen van apparaten die zichtbaar licht uitstralen die gebruikmaken van de DLE-emissie. Laten we eens kijken naar een eenvoudige structuur van een zichtbaar licht-emitterend apparaat dat is samengesteld uit met fosfor gedoteerde p-type ZnO-nanostaafjes en n-type substraat, de pn-overgang. In dat geval moeten de met fosfor gedoteerde p-type ZnO-nanostaafjes niet alleen een lichtgevend medium zijn, maar ook een injectiemedium voor elektrische dragers. Om een efficiënt injectiemedium voor elektrische dragers te zijn, is het onnodig te zeggen dat de met fosfor gedoteerde ZnO-nanostaafjes sterk gedoteerd moeten zijn. Laten we in een dergelijke omstandigheid aannemen dat de DLE-emissiegolflengte van met fosfor gedoteerde ZnO-nanostaafjes afhangt van de fosforconcentratie en/of de dragerconcentratie. Vervolgens wordt de emissiegolflengte gedwongen om vast te pinnen op een bepaalde emissiegolflengte van zeer met fosfor gedoteerde ZnO-nanostaafjes. Dit komt omdat we geen andere keuze hebben dan de dragerconcentratie zo hoog mogelijk te houden om een efficiënt dragerinjectiemedium te hebben. Helaas kan de emissiegolflengte van zeer met fosfor gedoteerde ZnO-nanostaafjes mogelijk niet overeenkomen met de doelemissiegolflengte die we van de lichtemitterende apparaten verwachten; falen in het ontwerp van lichtgevende apparaten. Ook verandert in de echte wereld de zichtbare DLE-emissiegolflengte van met fosfor gedoteerde ZnO-nanostaafjes niet per dragerconcentratie, zoals weergegeven in figuur 4f. Hoe kunnen we dan de emissiegolflengte afstemmen? Er zijn inderdaad meer parameters waarmee rekening moet worden gehouden bij het ontwerpen van de lichtemitterende apparaten, met andere woorden, de parameters om de DLE-emissiegolflengte aan te passen. Simmol et al. [43] en andere literatuur geven aan dat de ZnO-nanostaafjes bij uitgloeien de emissiegolflengte veranderen en daarom kunnen dienen voor het afstemmen van het emissiespectrum. In dat geval maakt de aanhoudende DLE-emissiegolflengte van met fosfor gedoteerde ZnO-nanostaafjes volgens de dragerconcentratie het ontwerpen van het lichtemitterende apparaat vrij eenvoudig; we hebben maar één parameter (gloeien) waarmee we rekening moeten houden bij het afstemmen van de emissiegolflengte, en een andere (fosforconcentratie of NH4 H2 (PO4 )2 M-verhouding) in elektrische dragerinjectie, afzonderlijk. Een dergelijke benadering zal met fosfor gedoteerde ZnO-nanostaafjes maken als een platform om lichtgevende apparaten a la carte te fabriceren in zichtbaar golflengtebereik met de goedkoopste route samen met het hydrothermale proces. Bovendien merken we hier verder op dat de waargenomen emissies in de belangrijkste regimes van de elektromagnetische spectra, inclusief UV- en zichtbaar emissiebereik, interessant zouden zijn voor een breed scala aan toepassingen, van biologische tot opto-elektronische apparaten. Het is echter opmerkelijk dat de aanhoudende p-type doping in ZnO-nanostaafjes en dunne films nog een uitdaging is voor praktische apparaattoepassingen. Met andere woorden, hoewel een 16 maanden durende p-type geleidbaarheid van met fosfor gedoteerd ZnO behoorlijk persistent is [14], maar niet vergelijkbaar met de andere anorganische kristallijne halfgeleiders zoals GaN:Galliumnitride, GaAs:Galliumarsenide en InP :Indiumfosfide. De onstabiele p-type geleidbaarheid wordt veroorzaakt door intrinsieke natieve defecten [46, 47], en er moet verder onderzoek worden gedaan naar de precieze controle van de defecten.
Conclusies
Samenvattend is de p-type geleidbaarheid in ZnO-nanostaafjes effectief bereikt door het doteren van fosforverontreinigingen erin. De succesvolle dotering van fosfor in ZnO-nanostaafjes vergroot de lengte en diameter van de nanostaafjes. Een ongebruikelijke variatie van dragerconcentratie, mobiliteit en Hall-coëfficiënt als functies van NH4 H2 (PO4 )2 M-ratio, d.w.z. fosforconcentratie, werd opgemerkt, wat werd verklaard op basis van de amfotere aard van fosfor. Deze hydrothermisch gesynthetiseerde ZnO-nanostaafjes gekweekt op Al-gedoteerde ZnO-zaadlaag bleken PL-emissie te vertonen in de drie verschillende regimes, waaronder UV-, zichtbare en NIR-regimes. De waargenomen emissies in UV-, violet-, geel-, rood- en NIR-regimes werden toegeschreven aan respectievelijk NBE-emissie, zinkinterstitials, zuurstofinterstitials, overtollige zuurstof (of zinkvacatures) en kenmerkend kenmerk van met Al-gedoteerde ZnO-zaadlaag. Interessant is dat de dotering van fosfor in deze nanostaafjes leidde tot een verandering in de UV-emissies en geen invloed heeft op de zichtbare en NIR-emissies. Dergelijke ongebruikelijke effecten in ZnO door fosforopname kunnen geschikt zijn voor verschillende opto-elektronische en biologische toepassingen.
Afkortingen
- DLE:
-
Diepe emissie
- HMTA of C6 H12 N4 :
-
Hexamethyleentetramine
- KM-methode:
-
Kubelka-Munk-methode
- NBE:
-
Near-band-edge emission
- Nd-YAG:
-
Neodymium-doped yttrium aluminum garnet
- NH4 H2 (PO4 )2 :
-
Ammonium dihydrogen phosphate
- NIR:
-
Nabij-infrarood
- PL:
-
Fotoluminescentie
- PO :
-
Oxygen sites in ZnO
- PZn :
-
Zinc sites in ZnO
- RF:
-
Radio frequency
- SEM:
-
Scanning elektronenmicroscoop
- UV:
-
Ultraviolet
- XRD:
-
Röntgendiffractie
- Zn(NO3 )2 :
-
Zinc nitrate hexahydrate
- ZnO:
-
Zinkoxide
Nanomaterialen
- Wat zijn de toepassingen en eigenschappen van mangaanstaal?
- De atoomherschikking van op GaN gebaseerde meerdere kwantumbronnen in H2/NH3 gemengd gas voor het verbeteren van structurele en optische eigenschappen
- Eenvoudige synthese en optische eigenschappen van kleine selenium nanokristallen en nanostaafjes
- Optische en elektrische kenmerken van silicium nanodraden bereid door stroomloos etsen
- Effect van gouden nanodeeltjesdistributie in TiO2 op de optische en elektrische kenmerken van kleurstofgevoelige zonnecellen
- Het effect van contactloos plasma op structurele en magnetische eigenschappen van Mn Х Fe3 − X О4 Spinels
- Effecten van dubbellaagse dikte op de morfologische, optische en elektrische eigenschappen van Al2O3/ZnO-nanolaminaten
- De oppervlaktemorfologieën en eigenschappen van ZnO-films afstemmen door het ontwerp van grensvlakken
- De voorbereiding van Au@TiO2 Yolk–Shell Nanostructure en zijn toepassingen voor afbraak en detectie van methyleenblauw
- Structurele en zichtbare infrarood optische eigenschappen van Cr-gedoteerde TiO2 voor gekleurde koele pigmenten
- De structurele, elektronische en magnetische eigenschappen van Ag n V-clusters (n = 1–12) onderzoeken



