NiCo2S4-nanokristallen op met stikstof gedoteerde koolstofnanobuisjes als hoogwaardige anode voor lithium-ionbatterijen
Abstract
In de afgelopen jaren is de ontwikkeling van lithium-ionbatterijen (LIB's) met een hoge energiedichtheid een van de belangrijke onderzoeksrichtingen geworden om te voldoen aan de behoeften van elektrische voertuigen en smart grid-technologieën. Tegenwoordig hebben traditionele LIB's hun limieten bereikt op het gebied van capaciteit, levensduur en stabiliteit, waardoor hun verdere verbetering en ontwikkeling van alternatieve materialen met opmerkelijk verbeterde eigenschappen noodzakelijk is. Een stikstofbevattende koolstof nanobuis (N-CNT) gastheer voor bimetaalsulfide (NiCo2 S4 ) wordt in deze studie voorgesteld als een anode met aantrekkelijke elektrochemische prestaties voor LIB's. De voorbereide NiCo2 S4 /N-CNT nanocomposiet vertoonde verbeterde fietsstabiliteit, snelheidsprestaties en een uitstekende omkeerbare capaciteit van 623,0 mAh g –1 na 100 cycli bij 0,1 A g –1 en handhaafde een hoge capaciteit en fietsstabiliteit van 0,5 A g –1 . De uitstekende elektrochemische prestaties van het composiet kunnen worden toegeschreven aan de unieke poreuze structuur, die de diffusie van Li-ionen effectief kan verbeteren en tegelijkertijd de volume-uitbreiding tijdens de laad-ontlaadprocessen kan verminderen.
Achtergrond
Lithium-ionbatterijen (LIB) is een toonaangevende batterijtechnologie die wordt gebruikt in draagbare elektronische apparaten, elektrische voertuigen en opslag van hernieuwbare energie [1, 2]. Daarom is de ontwikkeling van LIB's met een hoge energiedichtheid een onderzoeksrichting geworden die cruciaal is voor de duurzame ontwikkeling van verschillende sectoren van economie en industrie [3,4,5]. Zo bereikte de specifieke energiedichtheid van commercieel grafietanodemateriaal zijn theoretische capaciteit van 372 mAh g –1 , die niet veel ruimte laat voor verdere verbetering om te voldoen aan de prestatie-eisen van opkomende elektronica en elektrische voertuigtechnologieën [6, 7]. Als gevolg hiervan is het essentieel om alternatieve anodematerialen voor LIB's te ontwikkelen om te voldoen aan de behoeften van de moderne samenleving.
Overgangsmetaalsulfiden (TMS's) bieden een opmerkelijk hogere specifieke capaciteit dan traditionele elektrodematerialen [8,9,10,11,12]. Onlangs zijn TMS's gerapporteerd als anoden met uitstekende geleidbaarheid en katalytische activiteit. Onder hen is binair nikkel-kobaltsulfide (NiCo2 S4 ) vertoont een hoge theoretische specifieke capaciteit (703 mAh g –1 ), een uitstekende elektronische geleidbaarheid (1,26 × 10 6 S m –1 ), en een grotere overvloed aan redoxreactieplaatsen [13,14,15,16,17]. Het gerapporteerde algemene laad-/ontlaadmechanisme van NiCo2 S4 met lithium (Li) gaat gepaard met de volgende reacties:
$${\text{NiCo}}_{2} {\text{S}}_{4} + 8{\text{Li}}^{ + } + 8{\text{e}}^{{- }} \to {\text{Ni}} + {\text{Co}} + 4{\text{Li}}_{2} {\text{S}}$$ (1) $${\text{ Ni}} + x{\text{Li}}_{2} {\text{S}} \leftrightarrow {\text{NiS}}_{x} + 2x{\text{Li}}^{ + } + 2x{\text{e}}^{{-}}$$ (2) $${\text{Co}} + x{\text{Li}}_{2} {\text{S}} \leftrightarrow {\text{CoS}}_{x} + 2x{\text{Li}}^{ + } + 2x{\text{e}}^{{-}}$$ (3)Ondanks de grote Li-opslagcapaciteit van NiCo2 S4 , zijn er nog steeds problemen met betrekking tot de lage omkeerbaarheid van laad- / ontlaadprocessen vanwege de bijbehorende volumevariatie, wat leidt tot materiaaldesintegratie en bijgevolg ernstige capaciteitsvervaging [18]. Een ander ernstig probleem komt voort uit het shuttle-effect van polysulfiden geproduceerd door het oplossen van lithiumpolysulfide (LPS) in de elektrolyt, wat ook resulteert in een lage capaciteitsretentie [19, 20].
Om de problemen van NiCo2 . op te lossen S4 anoden gerelateerd aan de volumeverandering en LPS-oplossing, zijn verschillende benaderingen ontwikkeld, waaronder nanostructurering en het gebruik van koolstofhoudende additieven en op koolstof gebaseerde gastheren, met veelbelovende resultaten. Nanostructurering en de combinatie ervan met koolstof/grafeennetwerken kan het contactoppervlak van de elektrode-elektrolytinterface vergroten en de Li-ion-routes verkorten, wat leidt tot een hogere specifieke capaciteit [18]. Daarom rapporteert deze studie de in situ groei van NiCo2 S4 nanodeeltjes op koolstof nanobuisjes (CNT) structuur met behulp van een hydrothermische methode. Verder werden, om de elektroactiviteit van het elektrodemateriaal te verhogen, de stikstof (N) heteroatomen opgenomen in de CNT-matrix. Een dergelijke verwerking maakt N-CNT bevorderlijker, wat leidt tot de uniforme groei van NiCo2 S4 en zo de kristalliniteit van NiCo2 . te verbeteren S4 /N-CNT-anode. In deze unieke structuur vormt CNT een elastische matrix die de structurele stabiliteit verbetert, de ionische geleidbaarheid van de composiet verbetert en de volumevariatie van NiCo2 vermindert S4 deeltjes. De NiCo2 S4 /N-CNT-materiaal handhaaft een goede capaciteitsretentie tijdens het fietsen en beperkt de spanningsvervaging aanzienlijk. De NiCo2 S4 /N-CNT composietanode heeft een initiële ontladingscapaciteit van 1412,1 mAh g –1 bij 0,1 A g –1 , en de ontlaadcapaciteit blijft op 623,0 mAh g –1 na 100 cycli.
Methoden
Synthese van NiCo 2 S 4
Ten eerste 0,074 g Co(AC)2 ·4H2 O en 0,037 g Ni(Ac)2 ·4H2 O werden opgelost in 40 ml ethanol. De oplossing werd 2 uur op een waterbad bij 80°C en nog eens 2 uur bij kamertemperatuur geroerd. Vervolgens werd 0,078 g thioureum aan het mengsel toegevoegd, dat nog 20 uur continu werd geroerd voordat het reactiemengsel werd overgebracht naar een autoclaaf van 100 ml. De hydrothermische reactie werd 3 uur bij 170 ° C uitgevoerd. Na afkoeling tot kamertemperatuur werd het product meerdere keren gewassen met gedeïoniseerd water en onder verminderde druk gevriesdroogd.
Synthese van NiCo 2 S 4 /N-CNT Nanocomposieten
Eerst werd 68 mg licht geoxideerd CNT ultrasoon gedispergeerd in 40 ml ethanol. Vervolgens 0,074 g Co(AC)2 ·4H2 O en 0,037 g Ni(Ac)2 ·4H2 O werden toegevoegd en het mengsel werd 2 uur op een waterbad bij 80°C geroerd. Vervolgens 2 ml NH3 ·H2 O en 0,078 g thioureum werden aan de oplossing toegevoegd en het reactiemengsel werd 2 uur geroerd. Het reactiemengsel werd overgebracht naar een autoclaaf van 50 ml, gevolgd door een hydrothermische reactie gedurende 3 uur bij 170 ° C. Het product werd afgekoeld tot kamertemperatuur en verschillende keren gecentrifugeerd met gedeïoniseerd water en gevriesdroogd. NiCo2 S4 /CNT werd gesynthetiseerd volgens dezelfde methode maar zonder toevoeging van NH3 ·H2 O.
Karakterisering van materialen
De kristalstructuur van de gesynthetiseerde monsters werd gekenmerkt door poederröntgendiffractie (XRD, D8 Discover Bruker). Röntgenfoto-elektronenspectrometrie (XPS) werd uitgevoerd om de elementaire samenstelling van de monsters te analyseren met behulp van een K-Alpha 1063-analysator. De morfologie van de monsters werd bestudeerd met behulp van een scanning elektronenmicroscoop (SEM, JSM-7100F, JEOL) en een transmissie-elektronenmicroscoop (TEM, JEM-2100F). Het specifieke oppervlak van de monsters werd berekend met behulp van de Brunauer-Emmett-Teller (BET)-methode op basis van de N2 adsorptie-desorptie-isothermen verkregen met behulp van een V-Sorb 2800P. Thermogravimetrische analyse (TGA) is uitgevoerd in lucht met een verwarmingssnelheid van 10 °C min −1 .
Elektrochemische metingen
De elektrochemische prestaties van NiCo2 S4 /N-CNT-monsters werden geëvalueerd in CR 2032-muntcellen. Om de elektrodesuspensie te bereiden, 70 gew.% NiCo2 S4 /N-CNT-composiet, 15 gew.% roet (Super P) en 15 gew.% polyvinylideenfluoride (PVDF) bindmiddel werden gemengd in 1-methyl-2-pyrrolidinon (NMP). De slurry werd gelijkmatig uitgespreid op een Cu-folie met behulp van een rakeltechniek en vervolgens 8 uur aan de lucht bij 70 ° C gedroogd. Cirkelvormige schijfelektroden werden na het drogen gesneden en de cellen werden geassembleerd in een met Ar-gas (99,9995%) gevulde handschoenenkast met hoge zuiverheid (MBraun). De massale belasting van NiCo2 S4 /N-CNT in de elektroden was ongeveer 2 mg cm –2 . Pure Li-folies werden gebruikt als referentie- en tegenelektroden en microporeus polypropyleen Celgard 2300 werd gebruikt als separator. De elektrolyt was 1 mol L –1 LiPF6 (Aladdin, CAS-nummer:21324-40-3) in een mengsel van ethyleencarbonaat (EC, Aladdin, CAS-nummer:96-49-1) en dimethylcarbonaat (DMC, CAS-nummer:616-38-6) met een volume verhouding van 1:1. De galvanostatische ladings-/ontladingsmetingen zijn uitgevoerd met behulp van een meerkanaals batterijtestsysteem (Neware BTS4000) bij een potentiaalvenster van 0,01–3,00 V (vs. Li + /Li). Cyclische voltammetrie (CV) en elektrochemische impedantiespectroscopie (EIS) werden uitgevoerd met behulp van een elektrochemisch werkstation (Princeton, VersaState4).
Resultaten en discussie
Schema 1 toont de bereidingsroute van NiCo2 S4 /N-CNT composiet. Aanvankelijk werd het oppervlak van CNT voorbehandeld met een oplossing van Ni 2+ en Co 2+ . Vervolgens werden de N-atomen via een hydrothermische reactie bij 170 °C in de CNT's gedoteerd, terwijl NiCo2 S4 werd in situ gekweekt op het oppervlak van CNT's. De kristalstructuren van NiCo2 S4 , NiCo2 S4 /CNT en NiCo2 S4 /N-CNT-composieten werden gekenmerkt door XRD (figuur 1a). De karakteristieke diffractiepieken van NiCo2 S4 (JCPDS 20-0728) werden waargenomen in alle drie de monsters. Bovendien zijn de pieken in NiCo2 S4 /N-CNT waren meer uitgesproken en scherper dan die in NiCo2 S4 /CNT [21]. Er wordt aangenomen dat N-CNT kan worden gebruikt als actieve nucleatieplaatsen om de uniforme en dichte groei van NiCo2 te bevorderen S4 [22]. Afbeelding 1b toont de INZET-resultaten voor de NiCo2 S4 /N-CNT nanocomposieten. Het specifieke oppervlak van NiCo2 S4 /N-CNT nanocomposieten is 62,67 m 2 g −1 . Zoals getoond in de TGA-analysegegevens (Fig. 1c), is de NiCo2 S4 /N-CNT nanocomposiet vertoonde een gewichtsverlies bij een temperatuurbereik van 400-600 ° C, dat werd veroorzaakt door de verbranding van CNT's. Daarom is de inhoud van NiCo2 S4 in de NiCo2 S4 /N-CNT-composiet werd bepaald als ~ 30 gew.%.
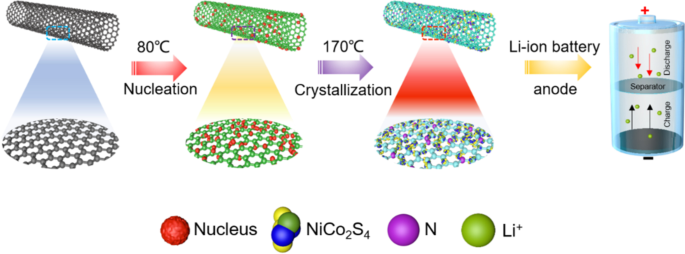
Schematische weergave van NiCo2 S4 /N-CNT composiet
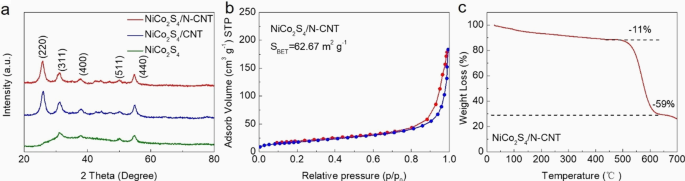
een XRD-patronen van NiCo2 S4 , NiCo2 S4 /CNT en NiCo2 S4 /N-CNT; b N2 adsorptie-desorptie-isothermen van NiCo2 S4 /N-CNT; c TGA van NiCo2 S4 /N-CNT
De SEM-resultaten van de monsters worden getoond in Fig. 2a, b. De gesynthetiseerde NiCo2 S4 nanodeeltjes lijken dichter opeengepakt en geagglomereerd te zijn. Aan de andere kant, door de introductie van CNT en N-CNT, de NiCo2 S4 nanodeeltjes werden uniform verdeeld en afgezet om NiCo2 . te vormen S4 /CNT composiet (Fig. 2c, d) en NiCo2 S4 /N-CNT (Fig. 2e, f), respectievelijk. De dichtheid van NiCo2 S4 nanodeeltjes op het N-CNT-oppervlak in NiCo2 S4 /N-CNT was significant hoger dan die in de NiCo2 S4 /CNT composiet. Dit bevestigt dat de introductie van N-atomen in CNT's de dichtere groei van NiCo2 bevordert S4 nanodeeltjes.

SEM-afbeeldingen van a , b NiCo2 S4; c , d NiCo2 S4 /CNT; en e , v NiCo2 S4 /N-CNT
De TEM-afbeeldingen in Fig. 3a laten zien dat de NiCo2 S4 deeltjes hebben een gemiddelde diameter van ~ 5 nm en zijn gelijkmatig verdeeld over het oppervlak van N-CNT's. In het TEM-beeld (HRTEM) met hoge resolutie van NiCo2 S4 /N-CNT getoond in Fig. 3b, vertonen de nanodeeltjes met een diameter van ongeveer 5 nm een duidelijke roosterrand van 0,35 nm, overeenkomend met het (220) vlak van NiCo2 S4 . Bovendien werden rond de nanodeeltjes veel kromme grafietroosterranden waargenomen. De snelle Fourier-transformatie (FFT) en roosterafstandprofielen in Fig. 3b bevestigden verder de opname van NiCo2 S4 nanodeeltjes in de N-CNT-structuur.
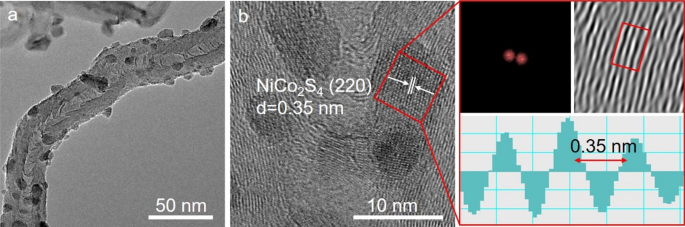
een TEM-afbeelding; b HRTEM-beeld van NiCo2 S4 /N-CNT
Verder werd XPS gebruikt om de bindingseigenschappen en chemische oppervlaktesamenstelling van NiCo2 . te bepalen S4 /N-CNT. De Co 2p spectra (Fig. 4a) kunnen worden verdeeld in twee pieken van 778,8 eV en 793,0 eV, wat overeenkomt met Co 3+ en Co 2+ , respectievelijk [23, 24]. In de N 1s spectrum (Fig. 4b), kunnen de pieken bij 398,3, 399,7 en 400,9 eV worden toegewezen aan respectievelijk de pyridine-, pyrrolische en grafitische N [25, 26]. In het XPS-spectrum van S 2p (Fig. 4c), de S 2p 3/2 en S 2p 1/2 kan duidelijk worden waargenomen bij respectievelijk 161,2 en 163,1 eV, en de piek bij 163,8 eV komt overeen met de metaal-zwavelbinding [27, 28]. Zoals weergegeven in figuur 4d, zijn naast de satellietpieken ook de bindingsenergieën van Ni 2p gecentreerd op 854,6 en 856,9 eV komen overeen met Ni 2p 3/2 , en die bij 871,1 en 875,5 eV komen overeen met Ni 2p 1/2 . Dit duidt op de aanwezigheid van zowel Ni 3+ en Ni 2+ in de steekproef [29, 30]. Zoals weergegeven in figuur 4e, zijn er drie passende pieken aanwezig in het C1s-profiel bij 284,9, 285,7 en 290,4 eV, die respectievelijk kunnen worden toegeschreven aan C-C-, C-N- en -C=O-bindingen. Samengevat, de XPS van NiCo2 S4 /N-CNT duidde op de vorming van een sterk geordende kristalstructuur van NiCo2 S4 en demonstreerde de succesvolle introductie van het N-element in de structuur van verbindingen.
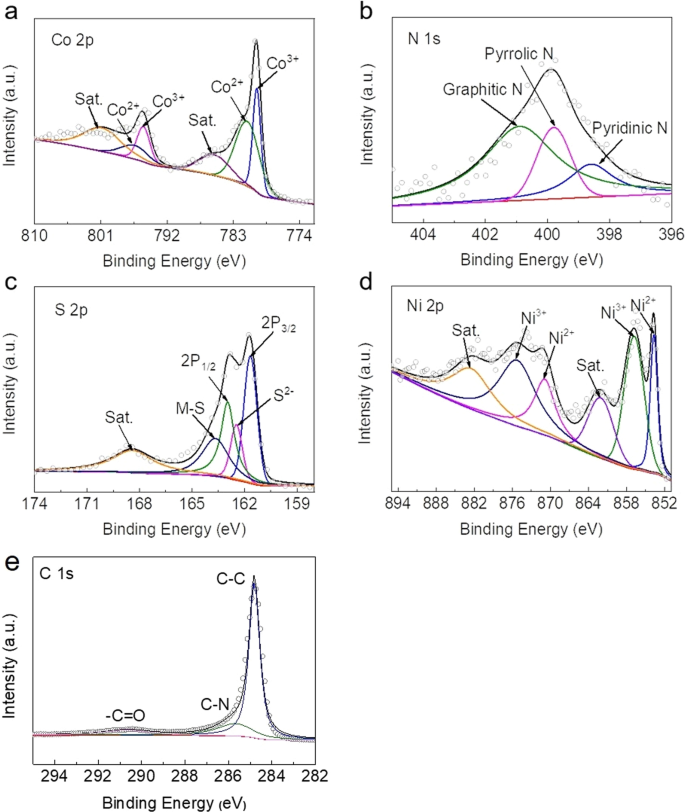
XPS-spectra van a Co 2p , b N 1s , c S 2p , d Ni 2p , en e C 1s in NiCo2 S4 /N-CNT
De elektrochemische eigenschappen van NiCo2 S4 /N-CNT voor Li-opslag werden geëvalueerd door CV en laad-ontlaadcycli, zoals weergegeven in Fig. 5 bij een potentieel bereik van 0,01–3,00 V (vs. Li + /Li). Het kathodische proces bestond uit drie reductiepieken (Fig. 5a) gelegen op 1,71 V, 1,33 V en 0,70 V. De sterkste piek bevindt zich op 1,33 V en twee zwakkere pieken komen overeen met de reductie van NiCo2 S4 naar Ni en Co. Ter vergelijking:de pieken bij 1,71 V en 0,70 V komen overeen met de vorming van Li2 S en de SEI-film, respectievelijk. In het anodische proces kunnen de oxidatiepieken bij 1,33 V en 2,05 V worden toegeschreven aan de oxidatie van metallisch Co tot CoSx . Bovendien is er een intensieve piek bij 2,32 V als gevolg van de oxidatiereacties van metallisch Ni en Co tot NiSx en CoSx , respectievelijk. De vorm van de curve, de piekpositie en de intensiteit van de pieken zijn relatief stabiel in de volgende cycli, wat aangeeft dat NiCo2 S4 /N-CNT heeft een goede stabiliteit en omkeerbaarheid.
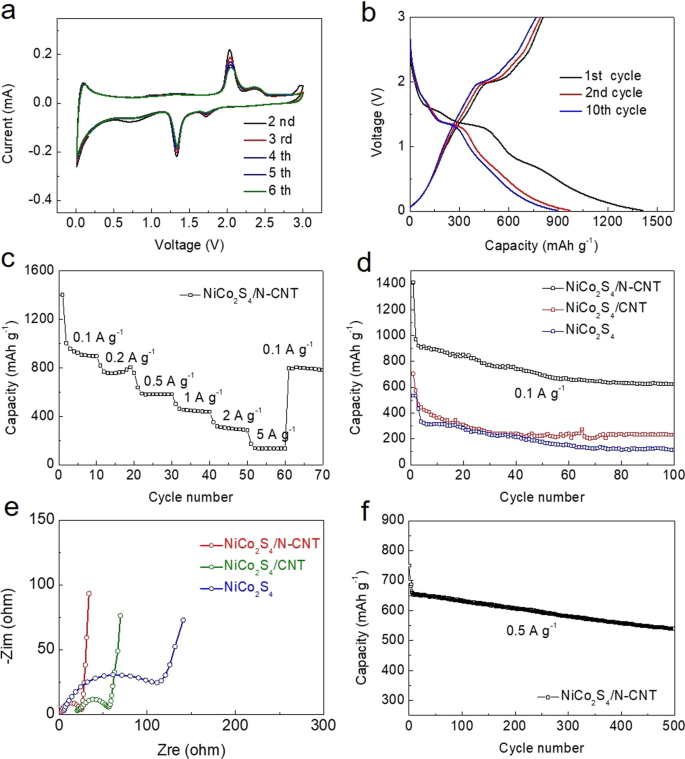
een CV's van NiCo2 S4 /N-CNT met een scansnelheid van 0,1 mV s −1 tussen 0,01 en 3,0 V versus Li + /Li; b laad-/ontlaadcurven van NiCo2 S4 /N-CNT bij 0,1 A g −1 ; c snelheidscapaciteit van NiCo2 S4 /N-CNT-elektroden met verschillende stroomsnelheden; d fietsprestaties van NiCo2 S4 /N-CNT, NiCo2 S4 /CNT en NiCo2 S4 bij 0,1 A g –1 ; e EIS-plots van NiCo2 S4 /N-CNT, NiCo2 S4 /CNT en NiCo2 S4; v fietsprestaties bij een stroomdichtheid van 0,5 A g −1
Afbeelding 5b toont de laad-ontlaadcurven van NiCo2 S4 /N-CNT bij 0,1 A g –1 voor de 1e, 2e en 10e cyclus. De eerste laad- en ontlaadcapaciteiten van de NiCo2 S4 /N-CNT-elektrode bereikte 807,6 en 1412,1 mAh g –1 , respectievelijk, met de initiële coulombefficiëntie van 57,2%. De ontladingscapaciteiten van de 2e en 10e cyclus zijn 970,7 mAh g –1 en 891,1 mAh g –1 , respectievelijk. De omkeerbaarheid van het laad-/ontlaadproces verbeterde met het aantal cycli, vergezeld van een verhoogde coulombefficiëntie. De verkregen CV-profielen komen overeen met de laad-/ontlaadcurven van NiCo2 S4 /N-CNT.
Om de elektrochemische prestatie van NiCo2 . verder te bestuderen S4 /N-CNT, de snelheidscapaciteit werd geëvalueerd bij stroomdichtheden van 0,1 tot 5 A g –1 (Fig. 5c). De resultaten geven aan dat de capaciteit van NiCo2 S4 /N-CNT nam af met de toename van de stroomdichtheid. Toen de stroomdichtheid werd teruggebracht tot 0,1 A g −1 , de capaciteit van NiCo2 S4 /N-CNT keerde terug naar een waarde van 796,1 mAh g –1 , met een capaciteitsbehoud van ongeveer 84% en aantonend dat NiCo2 S4 /N-CNT vertoont uitstekende snelheidsprestaties. De fietsprestatiegegevens van NiCo2 S4 /N-CNT, NiCo2 S4 /CNT en NiCo2 S4 voor 100 cycli bij 0,1 A g –1 worden getoond in Fig. 5d. Gedurende de eerste 50 cycli ondergaat de anode een lichte capaciteitsvervaging. Dan, NiCo2 S4 /N-CNT anode stabiliseerde zijn capaciteit voor de rest van de cycli en toonde een waarde van 623,0 mAh g –1 na 100 cycli. Deze resultaten laten zien dat in vergelijking met de NiCo2 S4 /CNT en NiCo2 S4 elektroden, de NiCo2 S4 /N-CNT-elektrode vertoonde een opmerkelijk hogere ontladingsspecifieke capaciteit en betere cyclusstabiliteit. Afbeelding 5e toont de EIS-gegevens. De hoogfrequente halve cirkels in de Nyquist-grafieken komen overeen met de ladingsoverdrachtsweerstand (R ct ) van de elektroden. De NiCo2 S4 /N-CNT-elektrode vertoont duidelijk de laagste R ct waarden, wat een opmerkelijk verbeterde kinetiek van lading/massa-overdracht suggereert. Afbeelding 5f toont de fietsprestaties van NiCo2 S4 /N-CNT-elektrode bij 0,5 A g −1 meer dan 500 cycli. De NiCo2 S4 /N-CNT-elektrode levert een initiële specifieke ontladingscapaciteit van 750,2 mAh g −1 en behoudt een omkeerbare capaciteit van 539,3 mAh g −1 na 500 cycli, een verdere bevestiging van de uitstekende cyclus- en snelheidscapaciteit van deze anode met hoge capaciteit voor lithiumbatterijen.
Conclusies
Samengevat, een NiCo2 S4 /N-CNT-composiet werd bereid met behulp van een gemakkelijke hydrothermische syntheseroute in één pot. Door de N-atomen in de CNT-structuur te introduceren, uniform verdeeld NiCo2 S4 nanodeeltjes met verminderde deeltjesgrootte werden verkregen. De geassembleerde cellen met de NiCo2 S4 /N-CNT anode vertoonde een hoge specifieke capaciteit van ongeveer 623,0 mAh g –1 en uitstekende fietsstabiliteit bij 0,1 A g –1 na 100 cycli. Bovendien vertoonde deze elektrode een uitstekende cyclische eigenschap bij 0,5 A g −1 meer dan 500 cycli, wat het vermogen bevestigt om zijn hoge prestaties bij verhoogde stroomdichtheden te behouden. Onze studie toont aan dat deze synthesemethode een haalbare manier is om NiCo2 . te laten groeien S4 nanodeeltjes met uniforme verdeling op het oppervlak van een CNT-substraat als een hoogwaardige anode voor LIB's.
Beschikbaarheid van gegevens en materialen
Alle gegevens die tijdens dit onderzoek zijn gegenereerd of geanalyseerd, zijn opgenomen in dit gepubliceerde artikel.
Afkortingen
- LIB's:
-
Lithium-ionbatterijen
- CNT:
-
Koolstof nanobuisje
- NiCo2 S4 :
-
Binair nikkel-kobaltsulfide
- PVDF:
-
Polyvinylideenfluoride
- NMP:
-
N -Methyl-2-pyrrolidon
- XRD:
-
Röntgenpoederdiffractie
- SEM:
-
Scanning elektronenmicroscopie
- CV:
-
Cyclische voltammetrie
- EIS:
-
Elektrochemische impedantiespectroscopie
- N-CNT:
-
Stikstofbevattende koolstofnanobuisjes
- TMS:
-
Overgangsmetaalsulfiden
- LPS:
-
Lithiumpolysulfide
- XPS:
-
Röntgenfoto-elektronenspectrometrie
- TEM:
-
Transmissie elektronenmicroscoop
- HRTEM:
-
Transmissie-elektronenmicroscoop met hoge resolutie
- BET:
-
Brunauer–Emmett–Teller
- TGA:
-
Thermogravimetrische analyse
- EG:
-
Ethyleencarbonaat
- DMC:
-
Dimethylcarbonaat
- FFT:
-
Snelle Fourier-transformatie
- N:
-
Stikstof
- Li:
-
Lithium
Nanomaterialen
- Tinnen nanokristallen voor toekomstige batterij
- Hernieuwbare PVDF-kwaliteiten voor lithium-ionbatterijen
- Mechanische samenstelling van LiNi0.8Co0.15Al0.05O2/Carbon Nanotubes met verbeterde elektrochemische prestaties voor lithium-ionbatterijen
- Eenvoudige synthese van SiO2@C-nanodeeltjes verankerd op MWNT als hoogwaardige anodematerialen voor Li-ionbatterijen
- Weinig gelaagde MoS2/acetyleenzwarte composiet als een efficiënt anodemateriaal voor lithium-ionbatterijen
- Voorbereiding van PPy-Coated MnO2 hybride micromaterialen en hun verbeterde cyclische prestaties als anode voor lithium-ionbatterijen
- Effect van verschillende bindmiddelen op de elektrochemische prestaties van metaaloxide-anode voor lithium-ionbatterijen
- Na4Mn9O18/Carbon Nanotube-composiet als materiaal met hoge elektrochemische prestaties voor waterige natrium-ionbatterijen
- Ingesloten Si/Grafeencomposiet vervaardigd door magnesium-thermische reductie als anodemateriaal voor lithium-ionbatterijen
- Polyaniline-gecoate actieve kool aerogel/zwavelcomposiet voor hoogwaardige lithium-zwavelbatterij
- 3D onderling verbonden V6O13-nanobladen gekweekt op verkoold textiel via een zaad-ondersteund hydrothermisch proces als hoogwaardige flexibele kathodes voor lithium-ionbatterijen



