Verbetering van de cyclusbaarheid van lithiummetaalanode via constructie van atomair interlamellair ionenkanaal voor lithiumzwavelbatterij
Abstract
Uniforme migratie van lithium (Li) -ionen tussen de separator en de lithiumanode is van cruciaal belang voor het bereiken van Li-afzetting van goede kwaliteit, wat van groot belang is voor de werking van lithiummetaalbatterijen, vooral voor Li-zwavel (Li-S) -batterijen. Commerciële separatoren zoals polypropyleen of polyethyleen kunnen worden bereid door natte of droge processen, maar ze kunnen inderdaad overvloedige porositeiten veroorzaken, wat resulteert in ongelijkmatige Li-ionstripping/plating en uiteindelijk de vorming van Li-dendrieten. Daarom hebben we een atomair interlamellair ionenkanaal geconstrueerd door het gelaagde montmorilloniet op het oppervlak van de separator te introduceren om de Li-ionflux te geleiden en stabiele Li-afzetting te bereiken. Het atomaire interlamellaire ionenkanaal met een afstand van 1,4 nm vertoonde een sterke absorptiecapaciteit voor elektrolyten en gereserveerde capaciteit voor Li-ionen, waardoor een snelle overdracht van Li-ionen werd bevorderd en een gelijkmatige afzetting van Li-ionen aan de anode werd bereikt. Wanneer geassembleerd met de voorgestelde separator, was de Coulomb-efficiëntie van Li||Cu-batterijen 98,2% na 200 cycli en stabiel plateren / strippen, zelfs na 800 uur, werd bereikt voor de Li||Li symmetrische batterijen. Belangrijk is dat de voorgestelde separator een specifieke capaciteitstoename van 140% mogelijk maakt na 190 cycli bij gebruik van de Li-S-batterijen.
Inleiding
Met een steeds toenemende vraag naar hoogwaardige elektronische toepassingen zoals elektrische voertuigen en draagbare systemen, heeft het onderzoek gericht op energieopslagapparaten met een hoge energiedichtheid en een lange levensduur uitgebreide aandacht gekregen [1,2,3]. Met name lithium-metaalbatterijen (LMB's) zoals lithiumzwavelbatterijen (Li-S) zijn in staat uitstekende energieopslagprestaties te leveren vanwege de hoge energiedichtheid, toekomstperspectief voor praktische toepassingen [4,5,6]. Met name is Li-metaal gebruikt als een veelbelovend anodemateriaal, omdat het een hoge theoretische opslagcapaciteit heeft (~ 3860 mAh g −1 ), lage standaardpotentiaal (− 3,04 V vs. de standaard waterstofelektrode) en lichtgewicht dichtheid (0,53 g cm −3 ). Desalniettemin kan het bestaan van onregelmatige poriën in commerciële scheiders leiden tot een slechte kwaliteit van afgezet lithium, wat kan resulteren in dendritische vorming en het verbruik van meer lithiummetalen en elektrolyten tijdens de herhaalde galvanisatie-/stripprocessen [7, 8].
Dientengevolge zouden Li-dendrieten het "dode" Li-metaal kunnen vormen wanneer ze gemakkelijk van de geleidende collector kunnen worden afgebroken, wat resulteert in een lage Coulomb-efficiëntie (CE) en onomkeerbaar capaciteitsverlies [9, 10]. Bovendien zouden Li-dendrieten de separator kunnen doorboren en zo kortsluiting van LMB's veroorzaken, wat verder kan leiden tot thermische uitbarsting, brand en zelfs mogelijke explosie van oplaadbare batterijen [11, 12]. Vanwege dergelijke obstakels is het gebruik van LMB's in oplaadbare batterijen de afgelopen 20 jaar inderdaad beperkt geweest. Daarom kan het voorkomen van de vorming van lithiumdendrieten een effectieve benadering zijn om veelbelovende kenmerken van LMB's volledig te benutten [13]. Onlangs hebben onderzoekers verschillende methoden voorgesteld om het bovenstaande probleem op te lossen, waaronder het optimaliseren van de elektrolytsamenstelling [5, 14], het construeren van de kunstmatige vaste elektrolyt-interfase (SEI)-laag op Li-metaalanode [15], en het ontwikkelen van de driedimensionale composiet Li-anode [ 16], en het aanpassen van de collector [17, 18]. Hoewel die strategieën waren ontworpen om de SEI-laag te stabiliseren en/of de effectieve toegepaste stroomdichtheid van lithiummetalen te verminderen, waren ze voornamelijk gericht op lithiummetalen en elektrolyten. Tot op heden zijn er slechts enkele werken uitgevoerd om de dendrietuitdagingen aan te pakken of te verminderen door de separator te wijzigen [19]. Het is duidelijk dat het regelen van de separator een nieuwe en haalbare methode kan zijn om de vorming van lithiumdendriet te remmen.
Van de componenten van LMB's speelt de separator niet alleen een sleutelrol bij het segmenteren van anode- en kathode-elektroden om kortsluiting te voorkomen, maar heeft hij ook een directe invloed op de prestaties van batterijen door Li-ionmigratie toe te staan [9, 20, 21]. Daarom is gemeld dat een eenvoudige wijziging van de separator met behulp van een halfvaste polymeerelektrolyttussenlaag [22], grafeen [23] of een oppervlaktecoating met hoge modulus [24] de vorming van dendrieten effectief kan voorkomen en zo de prestaties van LMB's kan verbeteren. Onder de eerder gerapporteerde benaderingen waren de barrièrelagen echter dik (> 10 m) en hadden ze een hoge massabelasting (enkele milligrammen), wat onvermijdelijk de snelle diffusie van Li-ionen kan belemmeren en de energiedichtheid van LIB's kan verminderen. Bovendien kunnen de meeste LMB's die deze functionele scheidingstekens gebruiken alleen fietsen met lage stroomdichtheden, bijvoorbeeld kleiner dan 2 mA cm −2 . Om de kritische stroomdichtheid van LMB's te verbeteren, kan de toevoeging van anorganische deeltjes in de separator om de poreuze structuur te verbeteren en de kritische stroomdichtheid te verhogen een andere effectieve methode zijn. Een ongelijkmatige porieverdeling in de separator kan echter over het algemeen leiden tot een ongeordende diffusie van Li-ionen tijdens het plateren/strippen, wat leidt tot ongelijkmatige afzetting van Li-ionen en de vorming van Li-dendrieten [7]. Daarom is de microstructuur van de separator met een uniform lithiumoverdrachtskanaal zeer gunstig om het ondervonden probleem van dendriet tijdens de laad-/ontlaadprocessen te elimineren.
In dit werk, met als doel de migratie van Li-ionen gelijkmatig door de separator te leiden, wordt een op Li gebaseerde montmorilloniet (Li-MMT) gemodificeerde composietseparator gefabriceerd via de constructie van atomaire interlamellaire ionkanalen op de PP-separator. De als voorbereide separator ingebed met interlamellaire afstand (~ 1.4 nm) biedt overvloedige actieve plaatsen voor Li-iondiffusie en elektrolytbevochtiging [25]. Zo kan de gemodificeerde separator een uniforme afzetting van Li-ionen op de Li-anode bereiken door de richting van Li-stromen te verenigen, wat de Li-dendrietproblemen in de laad- / ontlaadprocessen effectief kan elimineren. Als resultaat stelt de Li-MMT-scheider de Li||Cu-batterijen in staat om 98,2% CE te leveren, zelfs na 200 cycli en zorgt ervoor dat de Li||Li-symmetrische batterijen een stabiele beplating/stripping realiseren gedurende 800 uur bij 1 mA cm −2 met een capaciteit van 1 mAh cm −2 . Bovendien leveren de batterijen met Li-MMT@PP-scheiders ook een goede cyclusstabiliteit met 140% specifieke capaciteit verhoogd in vergelijking met PP-scheiders na 190 cycli bij 0,5 mA cm −2 met zwavelgehalte van 1,5 mg cm −2 .
Experimentele methoden
Materialen en voorbereidingen
Montmorilloniet (MMT), polyvinylideenfluoride (PVDF) en lithiumhydroxide (LiOH) werden gekocht bij Aladdin. De N-methylpyrrolidon (NMP) en zwavelzuur (H2 SO3 ) werden verkregen van Sinopharm Chemical Reagent Co., Ltd. Zwavelpoeder (S) en acetyleenzwart (aangeduid als C-poeder) werden gekocht bij Alfa Aesar. Celgard 2500 werd gebruikt als afscheider. Het Li-MMT-poeder werd bereid via kationenuitwisseling. Meestal 0,2 M H2 SO3 oplossing werd gebruikt om de kationen in de tussenlaag van MMT om te zetten in ionen en vervolgens werd LiOH-oplossing gebruikt om de oplossing bij PH = 7 te maken en om de waterstofionen naar de Li-ionen te verhullen. Vriesdroogtechnologie werd gebruikt om het Li-MMT-poeder te verzamelen. Voor de bereiding van Li-MMT@PP-scheider werd slechts één kant van de scheider gecoat met de Li-MMT-slurry, zodat Li-MMT en PVDF-poeder met massaverhouding 9:1 uniform waren gedispergeerd in de NMP-oplossing en de gemiddelde massabelading van Li-MMT is slechts ~ 0,15 mg cm −2 .
Karakterisering
Röntgendiffractie (XRD) spectrum met behulp van een UltimaIV-diffractometer met CuKα1-straling (λ = 1.4506 ) werd gebruikt om de kristalstructuur van Li-MMT-poeder te onderzoeken. Transmissie-elektronenmicroscoop met hoge resolutie (HRTEM) werd gebruikt om de tussenlaag van Li-MMT te observeren en de scanning elektronenmicroscoop (SEM, FEI NANOSEI 450) werd gebruikt om de oppervlaktemorfologieën te analyseren.
Elektrochemische metingen
Voor de Li||Cu- en Li||Li-batterijtests werden de Cu-folies meestal eerst drie keer gewassen met gedeïoniseerd water en ethanol om de mogelijke onzuiverheden te verwijderen. Vervolgens werd de lithiumfolie in cirkels gesneden met een oppervlakte van 1 cm −2 te gebruiken als de Li-bronnen. De elektrolyt was 1 M bistrifluormethaansulfonimide lithiumzout (LiTFSI) in een mengsel van 1,3-dioxacyclopentaan (DOL) en 1,2-dimethoxyethaan (DME) (1:1 v/v) met 2 gew.% lithiumnitraat (LiNO3 ) als toevoeging. Voor de Li-S-batterijtests werd de S-kathode bereid via onze vorige methode dat het C- en S-poeder 24 uur werden gemengd en verwarmd op 155 ℃ met een massaverhouding van 8:2 [26]. En vervolgens werden de poeders van C/S-composieten, C en PVDF met een massaverhouding van 8:1:1 uniform gedispergeerd in de NMP-oplossing om de zwavelelektrode te bereiden. De gemiddelde zwavelbelasting is 1,5 mg cm −2 die was gecoat op de met koolstof gecoate aluminiumfolie. De batterijen werden geassembleerd via roestvrijstalen knoopbatterij (CR2025) in een met argon gevuld handschoenenkastje. Als anode werd Li-folie gebruikt. 20 uL elektrolyt werd gebruikt om de lithiumanode te bevochtigen en nog eens 20 µL werd gebruikt om de separator en kathode te bevochtigen. Vóór het testen hadden de geassembleerde Li-S-batterijen 12 uur rust en daarna 0,2 mA cm −2 met 5 cycli werd gebruikt om de batterijprestaties te activeren. Het elektrochemische testsysteem was het CT2001A-batterijtestsysteem (LAND Electronic Co., China). De afsnijspanning was 1,7-2,7 V. Elektrochemische impedantiespectroscopie (EIS) werd getest door een elektrochemisch werkstation (CHI660E, Chenhua Instruments Co., China).
Resultaten en discussie
Om de lithiumionflux over de commerciële PP-scheider te illustreren, worden de schema's getoond in Fig. 1a, b, waarin de ~ 5 µm Li-MMT-laag uniform was gecoat op de PP-scheider om de flux van Li-ionen te geleiden. Het is algemeen bekend dat de commerciële PP-scheider typisch wordt bereid door de droge of natte processen, en dan wordt de scheider uitgerekt om overvloedige lege ruimtes te genereren om Li-ionen door te laten. De commerciële PP-scheider vertoont echter schots en scheefgegroeide paden en willekeurig gestapelde poriën (figuur 1a), en kan dus geen uniforme migratie van Li-ionen realiseren en uiteindelijk Li-dendrieten veroorzaken. Daarom werd het atomaire ionenkanaal Li-MMT gebruikt als de modulator om een gelijkmatige stroom van Li-ionen te leiden (figuur 1b) en een uniforme Li-afzetting te bereiken. De kristalstructuur van MMT is meestal samengesteld uit negatief geladen lagen (NCL's) gescheiden door tussenlaagruimte (> 1 nm), die de uitwisselbare kation-ionen herbergt, zoals Li + , Na + , Mg 2+ , Ca 2+ , enz. Daarom is een kationenuitwisselingsmethode nodig om de gastheerkationen te verbergen voor Li-ionen [25]. De basisstructuur van NCL's is een typische T-O-T-laag, waarbij "T" staat voor de tetraëdrische plaat en "O" voor de octaëdrische plaat [25]. Met de unieke tussenlaagstructuur van Li-MMT kan de elektrolyt effectief doordringen in de Li-MMT-laag, wat resulteert in het ongehinderde transport van Li-ionen, waardoor de efficiënte diffusie van ionen wordt bereikt [7, 25]. De morfologie van Li-MMT wordt getoond in Fig. 1c, d die duidelijk de typische 3D-nanobladstructuur laat zien met nauw en willekeurig gestapelde architectuur. Volgens de HRTEM-afbeelding kan de gelaagde structuur van Li-MMT worden waargenomen en vertoont deze een tussenlaagruimte van ~-1,39 nm.
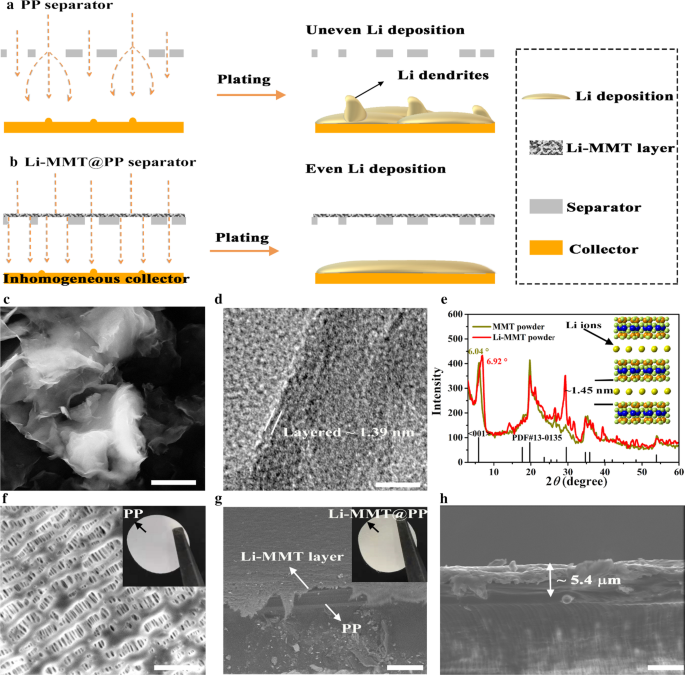
Bereiding en karakterisering van Li-MMT-poeders en Li-MMT@PP-scheider. een , b Schema's van ontwerpconcepten met verschillende scheidingstekens. c SEM-beeld van Li-MMT. d HRTEM-beeld van Li-MMT. e XRD-spectrum. v SEM-afbeelding van PP-scheider, het ingevoegde optische beeld is PP-scheider. g SEM-afbeelding van Li-MMT@PP-scheidingsteken en h overeenkomstige kruisprofiel, de ingevoegde optische afbeelding in g is Li-MMT@PP-scheider. Littekenbalk:c 1,5 µm, d 5 nm, f 2,5 µm, g 25 µm, u 5 µm
De precieze meting van de tussenlaagruimte van Li-MMT wordt getoond in figuur 1e. Raw MMT met de onbepaalde kationen in de tussenlaag vertoont een piek rond 6,04 °. Na ionenuitwisseling kan de piek op 6,92 ° de verandering van onbepaalde kationen naar de Li-ionen bevestigen. Omdat de kationen in onbewerkte MMT zeer variabel zijn in grootte en distributie, terwijl de Li-ionen kleiner zijn dan andere kationen [25], waardoor de afstand tussen de lagen geleidelijk afneemt. Volgens de wet van Bragg kan de tussenlaagafstand van Li-MMT worden geschat op ~-1,4 nm, wat een breed kanaal kan bieden voor Li-ionentransport en elektrolytbevochtiging. De poreuze morfologie van de PP-scheider wordt weergegeven in figuur 1f. Na het coaten van de Li-MMT-laag, kan worden vastgesteld dat de porositeit van de Li-MMT@PP-scheider aanzienlijk is afgenomen (figuur 1g), wat gunstig is voor de reguliere ionenbeweging. In dit werk werd de Li-MMT-slurry gecoat met behulp van een coatingmachine, wat potentieel biedt voor grootschalige productie. De laagdikte is slechts 5 µm (Fig. 1h) met een verwaarloosbare massatoename.
Geprofiteerd van het bovengenoemde atomaire interlamellaire ionenkanaal, is de Li-MMT@PP-scheider effectief voor het reguleren van de Li-afzetting en het onderdrukken van de Li-dendrietgroei op atomaire schaal via het geleiden van de Li-ionenstroom. De Brunner-Emme-Teller (BET) -metingen tonen de poriegrootteverdeling van Li-MMT-poeder binnen het bereik van 1-3 nm (aanvullend bestand 1:Fig. S1). Zoals weergegeven in figuur 2a, werd de Li||Cu-batterij gebruikt om de CE te bestuderen. Het is gebleken dat de Li-MMT@PP-scheider de Li||Cu-batterij kan leveren met een hoge CE en uitstekende stabiliteit, zelfs meer dan 200 cycli bij een stroomdichtheid van 1 mA cm −2 met een capaciteit van 1 mAh cm −2 . Tijdens de tests kan worden waargenomen dat alle CE een opwaartse trend vertonen in de eerste 5 cycli, veroorzaakt door de oppervlaktepassivering van Li-afzetting. Een hogere gemiddelde CE in de eerste 5 cycli van Li-MMT@PP-scheider benadrukt echter de voordelen dat het afgezette Li-metaal een lagere zijreactie ondergaat met de vloeibare elektrolyt in combinatie met Li-MMT@PP-scheider. Met de verdubbelende beplating/stripping wordt de tekortkoming van de PP-scheider geleidelijk aan het licht gebracht dat de geassembleerde Li||Cu-batterij slechts ~ 50 cycli doorstaat en de CE scherp daalt tot 60% en bijna tot nul na 150 cycli. Integendeel, de CE van Li||Cu-batterij geassembleerd met Li-MMT@PP-scheider levert nog steeds stabiele cycli met een lager overpotentiaal (Fig. 2b) en de batterij handhaaft nog steeds 98,2% CE na 200 cycli, wat wijst op de gedeponeerde Li metaal is uniformer en er wordt geen lithiumdendriet geproduceerd na de regulatie van de Li-MMT-laag.
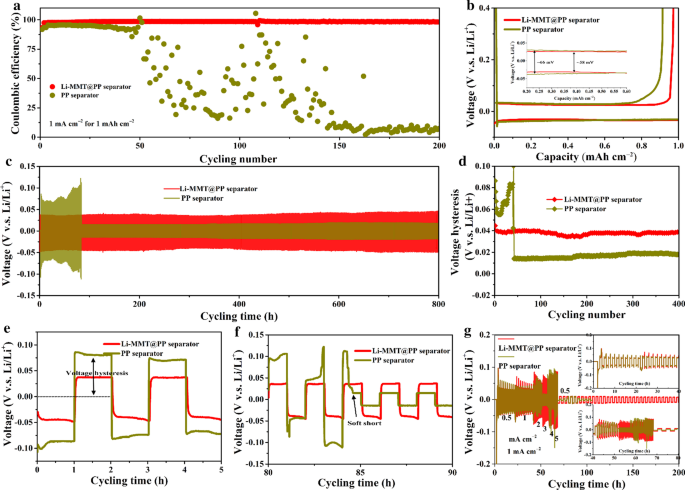
Elektrochemische prestaties van Li||Cu en Li||Li symmetrische batterijen. een CE-curven en b overeenkomstige spanningscurven. c Spanning-tijdprofielen van de Li||Li symmetrische batterijen met Li-MMT@PP of PP-scheider bij 1 mA cm −2 met een capaciteit van 1 mAh cm −2 . d Spanningshysterese van Li||Li symmetrische batterijen. e , v De gedeeltelijke vergrotingsprofielen van c . g De snelheidsprestaties van Li||Li symmetrische batterijen
Om de voordelen van de Li-MMT@PP-scheider in de cyclusstabiliteit van Li-metaalanoden verder te onderzoeken, worden ook symmetrische Li||Li-batterijen met verschillende scheiders gefabriceerd. Zoals weergegeven in Afb. 2c, wanneer de cycluscapaciteit 1 mAh cm −2 is bij een stroomdichtheid van 1 mA cm −2 , levert de batterij met de Li-MMT@PP-scheider een uitstekende cyclusstabiliteit met stabiele spanningsplateaus gedurende 400 cycli (900 uur) (Fig. 2d). In scherp contrast vertoont de batterij met de PP-scheider in de beginfase een sterke spanningshysterese. De overpotentiaal is bijna twee keer zo groot als die van Li-MMT@PP-scheider (Fig. 2e). Na Li-plating/stripping gedurende 84 uur wordt een plotselinge spanningsval waargenomen voor de batterij met de PP-scheider (Fig. 2f), die kan worden toegeschreven aan de elektrische verbinding tussen de elektroden, wat resulteert in de "zachte kortsluiting". Daarom werden de snelheidsprestaties van de Li-symmetrische batterij verder gebruikt om de stroomdichtheid te beoordelen bij het onderdrukken van de Li-dendrieten. Zoals getoond in Fig. 2g, de Li-MMT@PP-scheider onder de stroomdichtheid zelfs zo hoog als 5 mA cm −2 vertoont nog steeds normale galvanisatie-/striping-gedragingen. De PP-scheider vertoont significante spanningsfluctuaties naarmate de stroomdichtheid nadert tot 3 mA cm −2 . Vooral wanneer de stroomdichtheid wordt verhoogd tot 5 mA cm −2 , wordt de spanning extreem onstabiel, wat aangeeft dat het Li-anode-oppervlak ernstige Li-dendrieten heeft. In vergelijking met eerdere werken (aanvullend bestand 1:tabel S1), vertoont de gemodificeerde Li-MMT-scheider concurrentievoordelen om de Li-dendrieten effectief te onderdrukken.
De correlatie van Li-ionen over de separator voor en na het coaten van de Li-MMT-laag wordt voorgesteld in figuur 3a. Na kationenuitwisseling levert de tussenlaag van Li-MMT de actieve plaats voor Li. De tussenlaagafstand van 1,4 nm dient als een uniek Li-ionkanaal om de regelmatige flux van Li-ionen mogelijk te maken tijdens het plateren/strippen. Voor de PP-scheider zullen de schots en scheefstaande paden (Fig. 3b) en willekeurig gestapelde poriën echter de uniforme migratie van Li-ionen over de separator niet mogelijk maken, wat leidt tot de heterogene afzetting van Li-ionen in de elektrochemische processen, en waardoor er lithiumdendrieten ontstaan. Zo worden de morfologieën van Li-metaalanoden na 20 cycli onderzocht om het effect van Li-MMT@PP-scheider op de onderdrukking van Li-dendrieten verder te verduidelijken. Zoals getoond in Fig. 3c, e, wordt na het coaten van de Li-MMT-laag een uniforme en dichte Li-afzetting gerealiseerd en wordt geen vorming van Li-dendriet waargenomen op het anode-oppervlak, zelfs niet na 20 cycli. Belangrijk is dat de Li-metaalanode nog steeds een relatief dichte en compacte structuur behoudt met een dendrietvrij oppervlak, wat de voordelen van de Li-MMT-laag benadrukt voor een gunstig dendrietvrij Li-plating / stripgedrag. Voor de cel met PP-scheider vertoont de Li-metaalanode echter duidelijke draadvormige Li-dendrieten na cycli (figuur 3d) en stapelt bemoste Li losjes met een zeer poreuze structuur (figuur 3f).
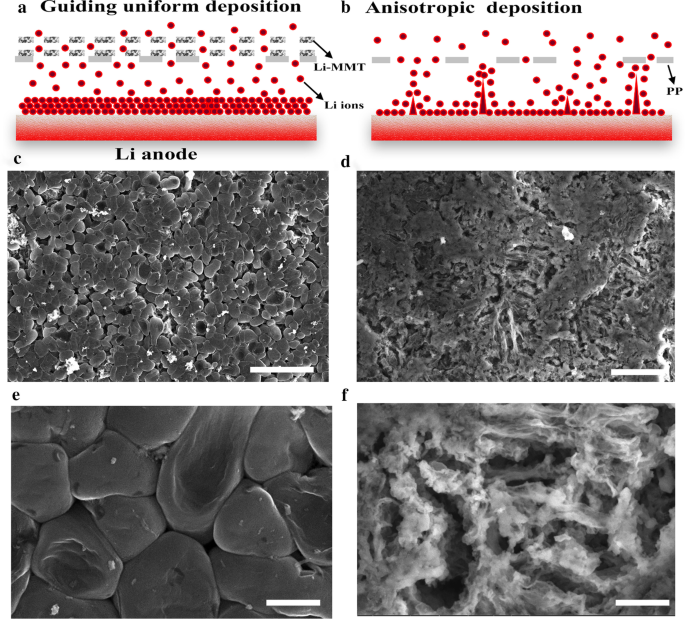
SEM-beelden van Li-anode gekoppeld aan Li-MMT@PP of PP-scheider na 20 cycli bij 1 mA cm −2 met een capaciteit van 1 mAh cm −2 . een , b Mechanisme illustratie van Li-MMT@PP of PP afscheiders. c , e Li-MMT@PP-scheider. d , v PP-scheider. Schaalbalken:c 25 µm, d 10 µm, e , v 2,5 µm
Om het potentieel van Li-MMT@PP-scheider in de praktische toepassing van Li-metaalbatterijen te demonstreren, de S-kathode met S-lading van 1,5 mg cm −2 werd als elektrode gebruikt. De elektrochemische interface samengesteld met verschillende separatoren werd onderzocht door de elektrochemische impedantiespectroscopie (EIS) meting. Zoals te zien is in figuur 4a, vertonen alle scheiders typisch depressieve halve cirkels bij hoge frequenties, die overeenkomen met de weerstand van de grensvlakladingoverdracht. Hoewel we kunnen zien dat de ladingsoverdrachtsweerstand van de batterij die is geassembleerd met Li-MMT@PP-scheider iets groter is dan die van PP-scheider, werden de prestaties van de batterij niet beïnvloed na activering met lage stroomdichtheid, wat in het experimentele gedeelte is geclaimd. Tijdens de laagfrequente gebieden presenteren de hellende lijnen de lithiumiondiffusie in de actieve materialen. Afbeelding 4b toont de spanningsplateaus van de C/S-composietkathode gemonteerd met Li-MMT@PP- of PP-scheiders tussen 1,7 en 2,8 V (V.S. Li/Li + ). De cyclische voltammetrie (CV) tests werden uitgevoerd en gepresenteerd in Aanvullend bestand 1:Fig. S2. Hoewel de grotere concentratie polysulfiden slechts een iets grotere concentratiepolarisatie genereert dan de PP-scheider, is het piekoppervlak van de Li-MMT@PP-scheider veel groter dan dat van de PP-scheider, wat aangeeft dat er meer polysulfiden worden gegenereerd bij gebruik van de Li-MMT-coatinglaag . Volgens de reactiemechanismen van de S-kathode vertoont de Li-S-batterij twee typische plateaus tijdens de laad- / ontlaadprocessen. In de eerste fase voor het kniepunt levert de Li-MMT@PP-scheider een hoge ontlaadcapaciteit van ~ 400 mAh g −1 met verwaarloosbare spanningshysterese. Voor de PP-scheider geldt echter alleen ~ 210 mAh g −1 capaciteit wordt waargenomen, wat aangeeft dat gedeeltelijk vrijgekomen polysulfiden met lange keten (vooral voor de Li2 S8 ) zijn niet betrokken bij de daaropvolgende redoxreactie om de capaciteit bij te dragen. De hogere ontladingscapaciteit tijdens het eerste plateau houdt in dat de Li-MMT-laag de shuttle van oplosbare polysulfiden met lange keten naar het Li-anode-oppervlak effectief kan vermijden. Bij de tweede conversiestappen worden voor de PP-scheider uiteraard kleine hoeveelheden korte-keten polysulfiden gevormd vanwege het bestaan van een shuttle-effect in de op ether gebaseerde elektrolyt, wat is bevestigd door ons eerdere werk [26]. Daarentegen is de Li-MMT@PP-scheider rationeel ontworpen dat het Li-MMT-oppervlak een sterk verankeringsvermogen heeft voor polysulfiden om de shuttle van polysulfiden te vermijden [25]. De uitstekende adsorptie-eigenschappen zorgen ervoor dat wordt voorkomen dat de polysulfiden het Li-anode-oppervlak verspreiden en het Li-oppervlak passiveren, waardoor de Li-S-batterij geassembleerd met Li-MMT@PP-scheider een hoge ontladingscapaciteit heeft van 1283 mAh g −1 . Langetermijncycli met een goede stabiliteit zijn de primaire doelen voor de commerciële batterijen. De recyclebaarheid op lange termijn van Li-MMT@PP-scheiders wordt getoond in figuur 4c. In de vroege 20 cycli kan worden vastgesteld dat de capaciteiten van Li-MMT@PP en PP-scheider een typische dalende trend vertonen. Dit komt omdat in het vroege ontladingsproces overvloedige polysulfiden zouden neerslaan uit het binnenste van het C/S-kathodemateriaal en zich zouden afzetten op het oppervlak van het kathodemateriaal [26], wat zou leiden tot capaciteitsverlies. Echter, na stabilisatie van de lithiummetaalanode, komen de voordelen van Li-MMT@PP-scheider naar voren dat het behoud van ontlaadcapaciteit 100% blijft tijdens de volgende cycli en de CE ook 100% is.
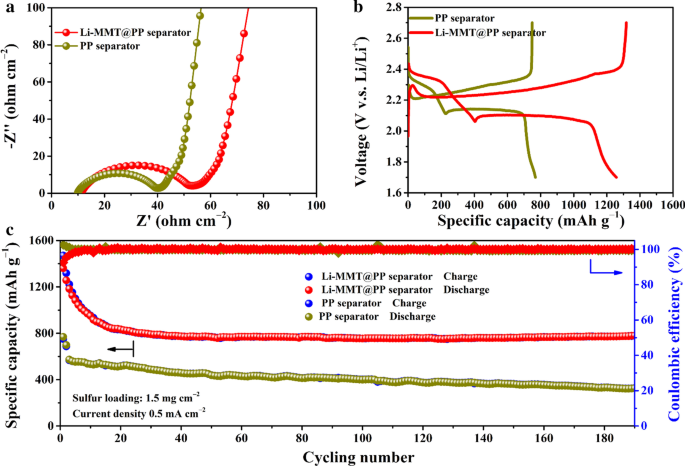
Elektrochemische prestaties van Li-S-batterijen met verschillende separator. een EIS resultaten. b De laad-/ontlaadplateaus met Li-MMT@PP of PP afscheider. c Fietsprestaties op lange termijn bij 0,5 mA cm −2 met zwavelgehalte van 1,5 mg cm −2
Conclusies
Samenvattend werd het interatomaire ionenkanaal (Li-MMT) geconstrueerd op de poreuze PP-scheider om de Li-ionenflux te moduleren en vervolgens de gelijkmatige afzetting van Li-ion op de Li-anode te begeleiden tijdens het galvaniseren/strippen. Vanwege de brede tussenlaagruimte (~-1,4 nm) van Li-MMT, zorgt de Li-MMT@PP-scheider in hoge mate voor de recycleerbaarheid van Li-metaalanode door de stroomrichting van lithiumionen te verenigen, wat resulteert in de uniforme afzetting van Li-ionen op de anodeoppervlak, waardoor een dendritische vrije lithiumanode wordt gevormd. Zoals geassembleerd met de Li-MMT@PP-scheider, vertoont de Li-S-batterij een opmerkelijke omkeerbare capaciteit van 776 mAh g −1 (bijna 1,4 keer groter dan PP-scheider) met een 100% CE na 190 cycli bij een stroomdichtheid van 0,5 mA cm −2 met de zwavelbelasting van 1,5 mg cm −2 .
Beschikbaarheid van gegevens en materialen
Alle gegevens zijn onbeperkt beschikbaar.
Afkortingen
- Li:
-
Lithium
- Li–S:
-
Lithiumzwavel
- PP:
-
Polypropyleen
- PE:
-
Polyethyleen
- MMT:
-
Montmorilloniet
- CE:
-
Coulomb efficiëntie
- LMB's:
-
Lithium-metaalbatterijen
- SEI:
-
Vaste elektrolyt interfase
- Li-MMT:
-
Montmorilloniet op basis van Li
- PVDF:
-
Polyvinylideenfluoride
- LiOH:
-
Lithiumhydroxide
- NMP:
-
N-methylpyrrolidon
- H2 SO3 :
-
Zwavelzuur
- C:
-
Acetyleen zwart
- XRD:
-
Röntgendiffractie
- HRTEM:
-
Transmissie-elektronenmicroscoop met hoge resolutie
- LiTFSI:
-
Bistrifluormethaansulfonimide lithiumzout
- DOL:
-
1,3-Dioxacyclopentaan
- DME:
-
1,2-dimethoxyethaan
- LiNO3 :
-
Lithiumnitraat
- EIS:
-
Elektrochemische impedantiespectroscopie
- NCL's:
-
Negatief geladen lagen
- BET:
-
Brunner–Emmet–Teller
- CV:
-
Cyclische voltammetrie
Nanomaterialen
- Tinnen nanokristallen voor toekomstige batterij
- Nano- en batterijanode:een recensie
- De atoomherschikking van op GaN gebaseerde meerdere kwantumbronnen in H2/NH3 gemengd gas voor het verbeteren van structurele en optische eigenschappen
- Onderzoek naar de sorptie van zware metalen met behulp van nanocomposieten van met ijzer gemodificeerde biochar
- Effect van verschillende bindmiddelen op de elektrochemische prestaties van metaaloxide-anode voor lithium-ionbatterijen
- Polyaniline-gecoate actieve kool aerogel/zwavelcomposiet voor hoogwaardige lithium-zwavelbatterij
- Transformatie van slib Si naar nano-Si/SiOx-structuur door diffusie van zuurstof naar binnen als voorloper voor hoogwaardige anoden in lithium-ionbatterijen
- Humaat-geassisteerde synthese van MoS2/C-nanocomposieten via co-precipitatie/calcineringsroute voor hoogwaardige lithium-ionbatterijen
- Review:poreuze metalen filters en membranen voor olie-waterscheiding
- Een nieuwe flexibele full-cell lithium-ionbatterij op basis van elektrospun koolstofnanovezels via een eenvoudige plastic verpakking
- CNC-draaibanken voor metaal



