Kobaltfosfide (Co2P) met opmerkelijke elektrokatalytische activiteit Ontworpen voor gevoelige en selectieve enzymloze bioanalyse van waterstofperoxide
Abstract
In dit werk worden kobaltfosfide nanodeeltjes (Co2 P NP's) werden bereid met een eenvoudige en milde hydrothermische methode zonder het gebruik van een schadelijke fosforbron. De morfologische structuur en oppervlaktecomponent van Co2 P werden gekenmerkt door transmissie-elektronenmicroscopie, röntgendiffractie en röntgenfoto-elektronspectroscopiemetingen. Gezien de uitstekende elektrokatalytische reductie-activiteit en goede elektrische geleidbaarheid van overgangsmetaalfosfide, hebben we Co2 gefabriceerd P NP's op indiumtinoxide (ITO) substraat (Co2 P/ITO) voor H2 O2 detectie. De Co2 De P/ITO-transducer vertoonde een snelle amperometrische respons van minder dan 5 s, een breder responsbereik van 0,001 tot 10,0 mM en een lage detectielimiet van 0,65 μM. Bovendien is de niet-enzymatische Co2 P/ITO-sensor toonde uitstekende selectiviteit, reproduceerbaarheid, herhaalbaarheid en stabiliteit, die allemaal de Co2 kwalificeerden P/ITO-elektrode voor een vrij betrouwbare en veelbelovende biosensor voor H2 O2 voelen.
Inleiding
Waterstofperoxide (H2 O2 ) is een representatieve reactieve zuurstofsoort in levende organismen en speelt een cruciale rol in de normale fysiologische functie [1]. De concentratie van H2 O2 in levende cellen hangt nauw samen met de celfysiologische balans [2]. Talrijke onderzoeken zijn ook gemeld dat kanker, de ziekte van Alzheimer, de ziekte van Parkinson en sommige ernstige ziekten kunnen worden veroorzaakt door een abnormale concentratie van H2 O2 [3,4,5]. Het ontwikkelen van nauwkeurige, gevoelige, snelle en selectieve methoden om de concentratie van H2 . te detecteren O2 , een normale biomarker voor oxidatieve stress, zal ongetwijfeld gunstig zijn voor de vroege diagnose. Tot nu toe zijn een groot aantal analytische methoden zoals spectroscopie [6], colorimetrie [7], fluorescentie [8, 9] en elektrochemische methoden [10,11,12] toegepast in H2 O2 bepaling. Elektrochemische methode, met name amperometrische test, wordt geleidelijk een van de meest eenvoudige en effectieve detectiemethoden voor H2 O2 biologische analyse tussen verschillende detectiemethoden vanwege de voordelen zoals hoge gevoeligheid, uitstekende selectiviteit en lage kosten.
Enzymatische elektrochemische sensoren zijn bewezen effectieve instrumenten voor het detecteren van H2 O2 . De grootschalige praktische toepassing van op enzymen gebaseerde sensoren wordt echter beperkt door gecompliceerde immobilisatie, instabiliteit van de omgeving en lage reproduceerbaarheid. Daarom is het ontwikkelen van niet-enzymatische elektrochemische H2 O2 sensoren is zeer onmisbaar.
De afgelopen jaren is een groeiend aantal sensoren op basis van edelmetaal [13,14,15], niet-edelmetaal en hun overeenkomstige verbindingen [16,17,18,19] of koolstofmaterialen [20, 21] gebruikt voor elektrochemische H2 O2 detectie. Als elektrochemisch actieve materialen voor het vervaardigen van niet-enzymatische biosensoren, hebben overgangsmetaalverbindingen steeds meer belangstelling gekregen. Overgangsmetaalfosfiden (TMP's) zijn een klasse van nieuw ontwikkelde materialen met uitstekende elektrokatalytische activiteit, goede elektrische geleidbaarheid en tal van uitstekende eigenschappen. Ze zijn dus uitgebreid bestudeerd voor toepassingen in watersplitsing [22, 23], hydro-ontzwaveling [24] en supercondensatorelektroden [25]. Recent onderzoek geeft aan dat CoP, Ni2 P en Cu3 P [26,27,28] kan ook worden gebruikt als efficiënte elektrokatalysator voor niet-enzymatisch H2 O2 detectie. Het aantal onderzoeken naar de toepassing van TMP's in de bioanalyse is tegenwoordig echter nog beperkt. Bovendien kan het gebruik van trifenylfosfine [29, 30], witte fosfor [31, 32] of een andere milieugevaarlijke fosforbron [33] het operationele risico bij de bereiding van TMP's verhogen. Daarom is enig onderzoekswerk voor de ontwikkeling van een groene methode bij de voorbereiding van TMP de moeite waard om op dit gebied te worden aangevuld.
In dit werk worden kobaltfosfide nanodeeltjes (Co2 P NP's) werden bereid door een eenstaps hydrothermische methode met kobaltacetaat en rode fosfor als grondstoffen. Hierin hebben we Co2 . gefabriceerd P NP's op indiumtinoxide (ITO)-substraat door middel van drop-casting-methode voor H2 O2 detectie. Co2 P vertoonde uitstekende elektrokatalytische activiteit in de richting van H2 O2 afname. Bovendien onthulde het een gunstige selectiviteit, uitstekende reproduceerbaarheid en goede stabiliteit, wat daarom zijn potentiële toepassing als een gevoelig platform voor H2 vertoonde. O2 detectie.
Experimentele sectie
Reagentia en materialen
Alle reagentia waren van analytische kwaliteit en werden zonder verdere zuivering gebruikt. Kobalt(II)acetaattetrahydraat (Co(Ac)2 ·4H2 O), kobaltchloridehexahydraat (CoCl2 ·6H2 O), D-(+)-glucose, L-Glycine (L-Gly), ascorbinezuur (AA), urinezuur (UA), ureum, NaCl, KCl, NaH2 PO4 , Na2 HPO4 , waterstofperoxide (30% H2 O2 ), ethanol en aceton werden gekocht bij Sinopharm Chemical Reagent Co., Ltd. China. D-(–)-fructose, L-arginine (L-Arg), L-lysine (L-Lys), dopamine (DA), paracetamol (APAP), aminotrimethyleenfosfonzuur (ATMP, 50 gew.%) werden gekocht bij Aladdin Ltd. Commerciële rode fosfor (98,5%, 100 mesh) werd gekocht bij Energy Chemical Technology (Shanghai) Co., Ltd. Nafion PFSA-polymeerdispersie (5%) werd gekocht bij Beijing Honghaitian technology Co., Ltd. Gedeïoniseerd water werd gebruikt in alle experimenten. Het indiumtinoxide (ITO) glas (10 × 20 × 1.1 mm met een ITO-film van 185 ± 2 nm en een plaatweerstand van 6.6 ± 0.1 ) werd geleverd door Shenzhen South Xiangcheng Technology Co., Ltd.
Synthese van Co2 P Nanodeeltjes
Commerciële rode fosfor (2 g) werd gedispergeerd in 15 ml H2 O onder sonificatie en hydrothermisch behandeld bij 200 ° C gedurende 12 uur in een met teflon beklede roestvrijstalen autoclaaf van 50 ml om oxidelagen te verwijderen [34]. Vervolgens werd de hydrothermisch behandelde rode fosfor gedroogd in een vacuümoven. Na het beëindigen van de voorbehandeling van rode fosfor, 1 mmol Co(Ac)2 ·4H2 O werd opgelost in 30 ml gedestilleerd water om een waterige oplossing te verkrijgen. Vervolgens werd de hydrothermisch behandelde rode fosfor gedurende 15 minuten onder ultrasone trillingen aan de oplossing toegevoegd met de molaire verhouding van Co/P 1/10. De bereide suspensie werd snel in een met teflon beklede autoclaaf van 50 ml gegoten. Vervolgens werd de autoclaaf in een elektronische oven geplaatst en gedurende 12 uur hydrothermisch behandeld bij 160, 200, 240 ° C. Vervolgens werd het product verzameld door centrifugeren en driemaal gewassen met respectievelijk gedestilleerd water en ethanol. Tot slot Co2 P NP's werden 3 uur aan de lucht bij 60 ° C gedroogd.
Synthese van Co(PO3 )2
De bereidingswijze van Co(PO3 )2 werd verwezen naar het vorige rapport [35]. 0,1 M CoCl2 ·6H2 Eerst werd een methanoloplossing bereid. Daarna 2 ml ATMP (50 w t%) werd druppelsgewijs toegevoegd aan 20 ml van de bovenstaande paarse oplossing en 30 minuten geroerd. Het onoplosbare kobalt-metafosfaat-coördinatiepolymeer vormde zich vervolgens in de oplossing. Het verkregen roze poeder werd verder verwarmd tot 900 °C onder Ar-stroom met een verwarmingssnelheid van 5 °C·min −1 en vervolgens 2 uur vastgehouden. Na afkoeling tot kamertemperatuur werd het zwarte product verzameld en gedurende 4 uur opnieuw verwarmd bij 650 °C in lucht om het verkoolde organische ligand te verwijderen. Eindelijk, het lichtpaarse poeder van Co(PO3 )2 werd verkregen.
Vervaardiging van Co2 P/ITO-elektrode
Ten eerste werd het ITO-glas (1 cm × 2 cm) gedurende respectievelijk 10 minuten gereinigd in aceton, ethanol en gedeïoniseerd water door middel van sonicatie. Daarna werd het behandelde ITO gedroogd onder vegen met stikstof. Voor de wijziging van de elektrode, 5 mg van de Co2 P NP's werden gedispergeerd in 1 ml gedeïoniseerd water om 5 mg ml −1 te vormen Co2 P-ophanging. Vervolgens werd 5 L 5% Nafion-oplossing aan de suspensie toegevoegd en het mengsel werd gedurende 15 minuten aan ultrasone trillingen onderworpen om een uniforme inktachtige suspensie te verkrijgen. De Co2 P/ITO-elektrode werd bereid door 100 L Co2 . te drop-casten P-suspensie op het ITO-oppervlak en aan de lucht gedroogd als werkelektrode. Het schematische voorbereidingsproces van Co2 P/ITO-elektrode wordt getoond in Schema 1.
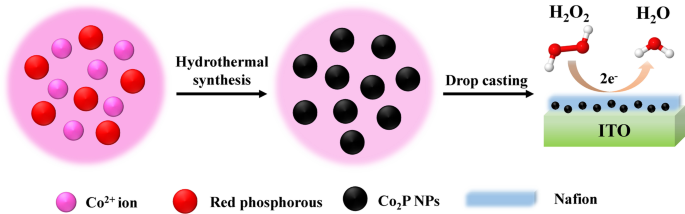
Schematische voorbereiding van Co2 P/ITO-elektrode en H2 O2 voelen
Karakteriseringen
De röntgendiffractiegegevens (XRD) werden geanalyseerd met een D8 ADVANCE-diffractometer met Cu Ka-straling. De transmissie-elektronenmicroscopie (TEM)-meting werd uitgevoerd met behulp van een Tecnai G2 F20 met een energieverspreid-spectrumdetector. Röntgenfoto-elektronspectroscopie (XPS) spectra werden gemeten op een Thermo ESCALAB 250XI-spectrometer.
Elektrochemische metingen
Voltammetriemetingen werden uitgevoerd door CHI 660E elektrochemisch werkstation in een systeem met drie elektroden, waarbij gebruik werd gemaakt van Co2 P/ITO-elektrode als werkelektrode, een platinafolie (1 cm × 1 cm) als tegenelektrode en Ag/AgCl met 3 M KCl-oplossing als referentie-elektrode om de elektrochemische activiteiten van de gesynthetiseerde monsters voor H2 O2 detectie. Fosfaatbufferzoutoplossing (PBS; 0,1 M, pH 7,4) werd gebruikt als elektrolyt om het fysiologische medium in het menselijk lichaam te simuleren. De voelprestaties van Co2 P/ITO-elektrode naar H2 O2 detectie werden onderzocht door middel van cyclische voltammetrie (CV) en amperometrie (I-t). Alle detectie-experimenten werden uitgevoerd onder 100 rpm roeren bij kamertemperatuur. Er werden elektrochemische impedantietests uitgevoerd op een elektrochemisch werkstation van de VersaSTAT 3F en er werd een ferricyanide-oplossing gebruikt als elektrolyt voor de impedantiemeting.
Resultaten en discussie
Karakterisering van Co2 P NP's
De kristalstructuur van Co2 P NP's werden bevestigd door XRD-meting. Afbeelding 1a toont de XRD-patronen van Co2 P-monsters bereid bij 160, 200 en 240 ° C gedurende 12 uur. De Co2 P-monster bereid bij 200 ° C vertoont diffractiepieken bij ongeveer 40,7 °, 40,9 °, 52,0 ° en 56,2 ° die overeenkomen met de karakteristieke diffractievlakken op (121), (201), (002) en (320) voor de orthorhombische fase van Co2 P (JCPDS nr. 32-0306). Wanneer de temperatuur varieerde van 160 tot 200 °C, namen de intensiteiten van de diffractiepieken toe en werden de pieken smaller en scherper, wat aangeeft dat de producten een hogere kristalliniteit hadden bij 200 °C. Toen de temperatuur echter 240 °C bereikte, werden enkele onzuiverheden gevormd en de diffractiepieken bij 29,7 ° werden toegeschreven aan het diffractievlak bij (-222) van Co(PO3 )2 (JCPDS nr. 27-1120). De invloed van synthetische tijd op de bereiding van Co2 P onder 200 °C wordt weergegeven in aanvullend bestand 1:Fig. S1. Wanneer de tijdsduur binnen 12 uur werd gecontroleerd, werd de verkregen Co2 P NP's vertoonden de laagste waarde van de volledige breedte bij het halve maximum van (121) piek, wat een betere kristalliniteit suggereert. Bovendien waren er geen onzuiverheden in het monster toen de reactietijd varieerde van 6 tot 24 uur. Volgens de Scherrer-formule is de berekende korrelgrootte van Co2 P NP's bereid bij 200 °C gedurende 12 uur waren 14,2 nm.
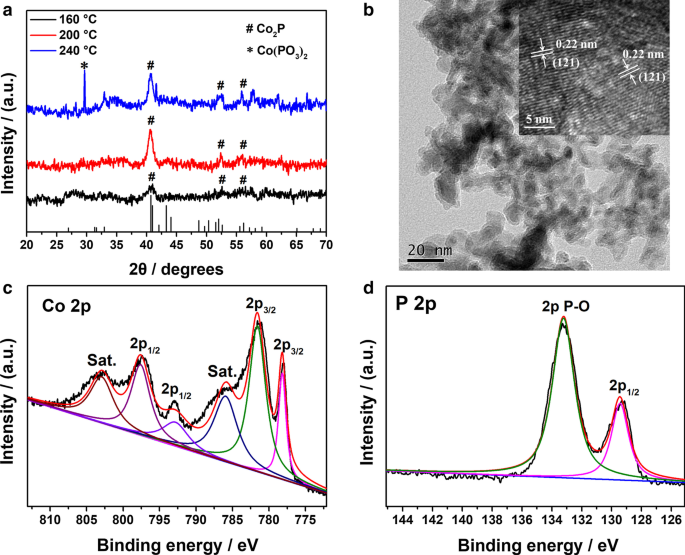
een XRD-patronen van Co2 P NP's bereid bij verschillende temperaturen gedurende 12 uur. b Transmissie-elektronenmicroscopisch beeld en transmissie-elektronenmicroscopisch beeld met hoge resolutie (inzet) van Co2 P NP's. XPS-spectra van Co2 P in de c Co 2p regio en d P 2p regio
De morfologie van Co2 P NP's werden beoordeeld door TEM-metingen. Zoals getoond in Fig. 1b, is het product bereid bij 200 ° C samengesteld uit onregelmatige nanodeeltjes met een diameter van ongeveer 10-20 nm en twee roosterranden zijn duidelijk te zien in het TEM-beeld (HRTEM) met hoge resolutie (inzet in Fig. 1b). De afstand tussen de aangrenzende vlakken is 0,22 nm, wat overeenkomt met de (121) facetten van Co2 P, wat verder bevestigt dat de vorming van TMP Co2 . is P.
De XPS-techniek werd gebruikt bij het analyseren van de chemische samenstellingen op het oppervlak van de Co2 P. Aanvullend bestand 1:Fig. S2 toont het XPS-onderzoeksspectrum van Co2 P. Co-, P- en O-elementen worden gedetecteerd in het monster, wat het bestaan van Co2 . bevestigt P en sommige geoxideerde producten. Energie-dispersieve röntgenspectroscopie (EDX) spectra van Co2 P (Aanvullend bestand 1:Fig. S3) bevestigt verder het naast elkaar bestaan van drie elementen (Co, P, O) in het monster. De XPS-spectra met hoge resolutie van Co 2p en P 2p worden respectievelijk getoond in Fig. 1c, d. In het Co 2p-spectrum kunnen de pieken bij 781,1 en 797,6 eV worden toegeschreven aan de bindingsenergieën (BE's) van Co 2+ 2p 3/2 en Co 2+ 2p 1/2 , respectievelijk [26, 36]. De pieken van 786,0 en 803,1 eV zijn twee schijnbare pieken in de satelliet. De Co 2p BE van 778,2 eV verschuift positief ten opzichte van die van metallisch Co (777,9 eV), wat suggereert dat Co in Co2 P heeft een gedeeltelijke positieve lading (δ + ) met een kleine waarde (0 < δ < 2) [37]. Integendeel, de P 2p BE van 129,4 eV verschuift negatief van die van elementair P (130,2 eV) zodat de P een gedeeltelijke negatieve lading heeft (δ − ) in Co2 P. De veranderingen van BE in Co- en P-element vergeleken met respectievelijk hun elementaire substantie, onthullen dat de overdrachtsrichting van elektronendichtheid in Co2 P is van Co tot P [38]. Oppervlakkige oxidatie van Co2 P genereert enkele geoxideerde P-soorten in het monster. Daarom worden de pieken bij 133,2 eV in het hoge BE-bereik toegewezen aan de oxiden [39].
Elektrochemische detectie van H2 O2 op Co2 P/ITO-elektrode
Onderzoek naar de elektrokatalytische activiteit van Co2 P NP's in H2 O2 reductie, ontwierpen we een niet-enzymatische H2 O2 elektrode door druppelgieten van Co2 P NP's ophanging op een kaal ITO-oppervlak. Afbeelding 2a toont de CV-curven van kale ITO en Co2 P/ITO in 0,1 M PBS bij pH 7,4 met en zonder 5,0 mM H2 O2 , respectievelijk. De streepjeslijnen geven aan dat de reactie van kale ITO op H2 O2 vermindering is verwaarloosbaar. Echter, de Co2 P/ITO-elektrode vertoont een opmerkelijke reductiepiek bij − 0,5 V in aanwezigheid van H2 O2 , die de prominente elektrokatalytische activiteit van Co2 . aantoont P NP's richting H2 O2 afname. Afbeelding 2b geeft de CV-curven van Co2 . weer P/ITO bij verschillende scansnelheden (van 30 tot 100 mV s −1 ) met 2,5 mM H2 O2 . Bij het verhogen van de scansnelheid nam de reductiepiekstroom toe en verschoof het piekpotentiaal naar de meer negatieve potentiaalzijde, wat wijst op de reductie in H2 O2 op Co2 P/ITO was een onomkeerbare reactie. De corresponderende kalibratiecurve (inzet, Fig. 2b) laat zien dat de reductiepiekstroomdichtheden lineair toenemen met de scansnelheid, wat suggereert dat de elektrochemische reductie van H2 O2 op het oppervlak van Co2 P/ITO-elektrode is een oppervlaktegestuurd proces [40].
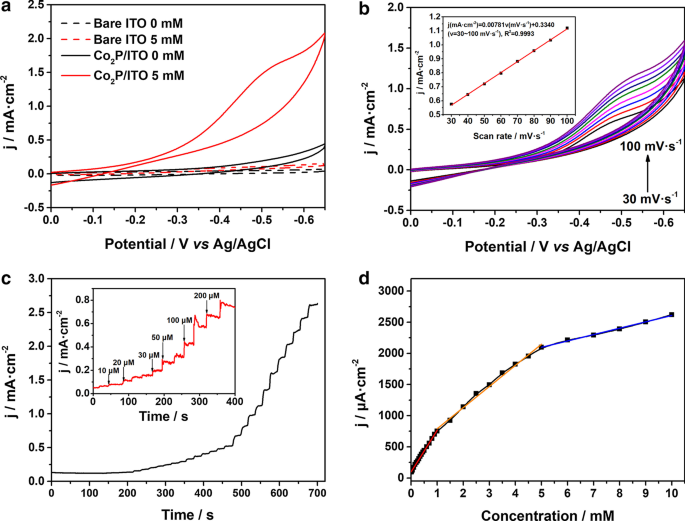
een CV-curven van kale ITO en Co2 P/ITO-elektrode in 0,1 M PBS met en zonder 5,0 mM H2 O2 met een scansnelheid van 100 mV s −1 . b CV-curven van Co2 P/ITO-elektrode in 2,5 mM H2 O2 bij scansnelheden van 30 tot 100 mV s −1 . Inzet:De overeenkomstige grafiek van stroom versus de scansnelheid. c Amperometrische reacties van Co2 P/ITO-elektrode met opeenvolgende toevoeging van H2 O2 in 0,1 M PBS. d De kalibratiecurve van constante stroom versus de concentratie van H2 O2
Afbeelding 2c, d toont de amperometrische respons en de kalibratiecurve van Co2 P/ITO-elektrode na de opeenvolgende toevoeging van H2 O2 onder roeren in de 0,1 M PBS bij − 0,5 V. De Co2 P/ITO-elektrode vertoonde een snelle reactie op de toevoeging van H2 O2 en bereikte de stationaire stroom binnen 5 s. De kalibratiecurve in Fig. 2d laat zien dat de transducer een multilineair bereik van H2 weergeeft O2 concentratie van 0,001 tot 1,0 mM, 1,0-5,0 mM en 5,0-10,0 mM. De gevoeligheid van de sensor verandert met de toenemende concentratie van H2 O2 , als gevolg van de verandering van de elektrokatalytische reductiekinetiek van H2 O2 op het elektrodeoppervlak. Volgens eerdere rapporten is de snelheidsbepalende stap van H2 O2 reductie wordt gedomineerd door H2 O2 adsorptie bij lage concentratie, terwijl de activering van H2 O2 is de belangrijkste determinant bij hoge concentraties. In het middelste gebied is de reductiekinetiek van H2 O2 wordt gecontroleerd door adsorptie en activering tegelijkertijd [10]. Een groot aantal analisten zal adsorberen op het oppervlak van Co2 P en bedek de actieve plaatsen in de hoge concentratie, wat leidt tot een afname van de gevoeligheid [41].
De vergelijking op H2 O2 uitvoeringen van de voorbereide Co2 . waarnemen P-monster bij verschillende reactietemperaturen en -tijden wordt getoond in aanvullend bestand 1:Fig. S4, S5 en Tabel S1, wat aangeeft dat de Co2 P-monster bereid bij 200 °C gedurende 12 uur geeft de beste H2 . weer O2 optredens voelen. Toen de reactietemperatuur tot 240 °C steeg, vormde de gevormde Co(PO3 )2 in Co2 P zou als onzuiverheid kunnen worden beschouwd. Om de invloed van Co(PO3 .) verder te verduidelijken )2 op H2 O2 detectie, de elektrochemische eigenschappen van Co(PO3 )2 werd onderzocht. Zoals getoond in Aanvullend bestand 1:Fig. S6, Co(PO3 )2 vertoont een verwaarloosbare elektrochemische respons op H2 O2 en zijn geleidbaarheid is inferieur aan Co2 P, die het huidige signaal van Co2 . afwijst P/ITO in amperometrische test. Daarom is de hogere zuiverheid en betere kristalliniteit van Co2 P-sample kan bijdragen aan de verbetering van de waarnemingsprestaties. Daarom kiezen we voor de Co2 P-monster bereid bij 200 °C en 12 uur als de beste H2 O2 tast materiaal. De kalibratie I –t curve vertoont ook een goede lineaire relatie in de concentratie van 1,0-50 μM, het fysiologische bereik van H2 O2 concentratie in het biosysteem (Fig. S7) [28], wat nuttig zou kunnen zijn om de mogelijkheid van praktische toepassingen van deze sensor te verbeteren. Bovendien is de detectielimiet (LOD) van de H2 O2 sensor kan worden berekend als 0,65 μM bij een signaal-ruisverhouding van 3. Vergeleken met de eerder gerapporteerde H2 O2 sensor, de uitgebreide elektrochemische prestaties van onze Co2 P/ITO-transducers zijn superieur aan die met een gunstige gevoeligheid, lineair bereik en LOD, zoals weergegeven in tabel 1.
Na detectie van 1,0 mM H2 O2 herhaaldelijk 35 keer (Fig. 3a, b), de XPS-spectra in Co 2p en P 2p regio van Co2 P worden geanalyseerd om het detectiemechanisme verder te onderzoeken. Er is geen significante verandering in de positie van de pieken in P 2p regio voor en na H2 O2 detectie. De pieken bij 778,2 en 793,0 eV in Co 2p spectrum verdween na meerdere metingen. Aangezien de piek van 778,2 eV het bestaan aangeeft van gereduceerde Co-soorten in Co2 P-monster [37], het verdwijnen van deze twee pieken toont aan dat de gereduceerde Co-soort met een lage valentie in Co2 P kan worden geoxideerd door H2 O2 tijdens het detectieproces, vooral bij hoge concentraties H2 O2 . De restpieken in Co 2p regio (782.1 en 798.3 eV) worden toegeschreven aan Co 2+ 2p 3/2 en Co 2+ 2p 1/2 , wat het exclusieve bestaan van Co(II)-soorten in Co2 . suggereert P na meerdere metingen. Volgens eerdere rapporten over het gebruik van op kobalt gebaseerde elektrokatalysatoren in H2 O2 detectie, Co 2+ soorten zijn aangetoond als de katalytische actieve plaatsen voor H2 O2 vermindering [46,47,48]. Over het algemeen is de elektrochemische reductie in H2 O2 doorloopt twee stappen in PBS [49, 50], zoals hieronder weergegeven.
$${\text{H}}_{{2}} {\text{O}}_{{2}} + {\text{ e}}^{ - } \to {\text{OH}}_ {{{\text{ad}}}} + {\text{ OH}}^{ - }$$ (1) $${\text{OH}}_{{{\text{ad}}}} + {\text{ e}}^{ - } \to {\text{OH}}^{ - }$$ (2) $${\text{2OH}}^{ - } + {\text{ 2H}} ^{ + } \to {\text{2H}}_{{2}} {\text{O}}$$ (3)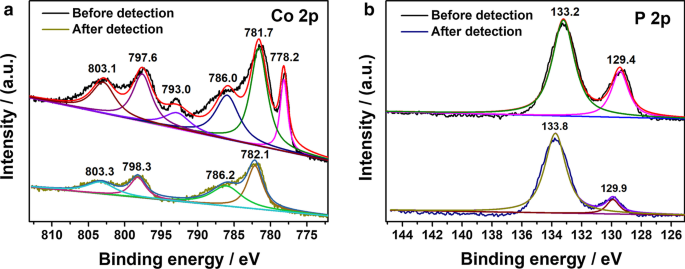
De vergelijking van XPS-spectra in a Co 2p regio en b P 2p regio van Co2 P voor en na detectie
In de eerste stap, H2 O2 verkrijgt een elektron om geadsorbeerd OH te vormen − (OHadvertentie ). Wanneer de tussenliggende OHadvertentie verkrijgt een extra elektron, het uiteindelijke reductieproduct van H2 O2 , H2 O, wordt gegenereerd. Als de redoxpotentiaal van H2 O2 /H2 O is hoger dan Co 3+ /Co 2+ , de Co(II)-soort in Co2 P kan worden geoxideerd tot Co(III) in het elektronenoverdrachtproces en H2 O2 wordt teruggebracht tot H2 O onomkeerbaar. Tijdens de amperometrische test is de toegepaste bias − 0,5 V versus Ag/AgCl (gelijk aan 0,14 V versus . NHE), die lager is dan het standaard redoxpotentieel van Co 3+ /Co 2+ . Hierdoor kan het geoxideerde Co(III) gereduceerd worden tot Co(II) en worden deze katalytisch actieve plaatsen van Co(II) weer geregenereerd. Daarom kan worden geconcludeerd dat de katalytische cyclus van Co (II) soorten plaatsvindt tijdens elektrochemische detectie van H2 O2 en de gereduceerde Co-soorten met lage valentie worden geoxideerd door H2 O2 na herhaalde metingen.
Selectiviteit, stabiliteit, reproduceerbaarheid en herhaalbaarheid van Co2 P/ITO-elektrode
Anti-interferentieprestaties zijn een andere belangrijke eigenschap van biosensor. Stikstof met een hoge zuiverheid werd gebruikt om de invloed van opgeloste zuurstof in oplossing te vermijden, omdat zuurstof kon worden gereduceerd bij een vergelijkbaar potentiaal dat werd toegepast in de amperometrische test [51]. Vergelijking van de CV-curven van Co2 P/ITO in 0,1 M PBS met of zonder stikstofspoeling, het reductiepotentieel en de huidige respons van 2,5 mM H2 O2 zijn vergelijkbaar, zoals weergegeven in Fig. S8, wat daarom suggereert dat de interferentie van opgeloste zuurstof kan worden verwaarloosd. Selectiviteit van Co2 P/ITO is ook getest met veelvoorkomende stoffen en andere kleine moleculen in lichaamsvloeistof, zoals sommige anorganische zouten, sacchariden, aminozuren en reductieve biomoleculen. Zoals getoond in Fig. 4a, kan de huidige respons na toevoeging van de bovenstaande interferenten worden verwaarloosd in vergelijking met de respons van 1,0 mM H2 O2 . Als beide twee O-atomen van H2 O2 kan worden gebonden met een of twee Co-atomen [52], de H2 O2 molecuul zou chemisch adsorberen op Co(II)-soorten in Co2 P specifiek. Bovendien kan de interferentie van willekeurige oxidatie van sommige reductieve verbindingen in echte biologische monsters met een hoog potentieel ook aanzienlijk worden verminderd bij een lager biaspotentiaal [53]. Daarom is de gunstige selectiviteit van Co2 P richting H2 O2 profiteert voornamelijk van de Co(II)-soort als specifieke adsorptieplaatsen en het toegepaste negatieve biaspotentieel tijdens het detectieproces.
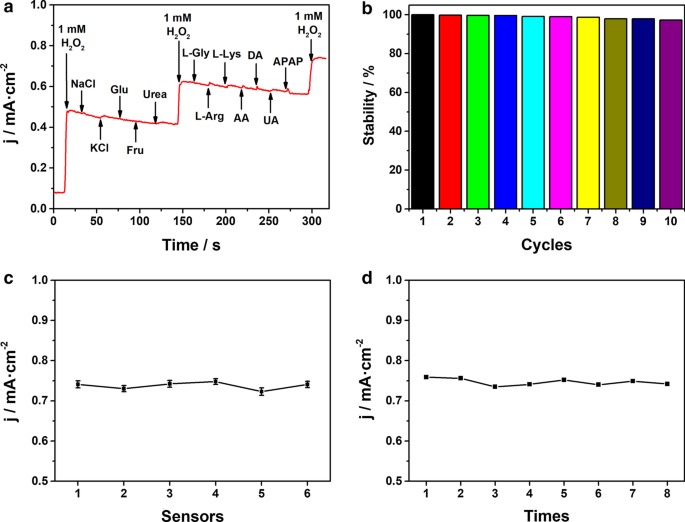
een Amperometrische reacties van Co2 P/ITO-elektrode met toevoeging van 1 mM H2 O2 en andere interfererende soorten (10 mM NaCl, KCl, Glu, Fru, ureum, L-Gly, L-Arg, L-Lys, AA; 1 mM DA, UA; 0,5 mM APAP) in 0,1 M PBS. b De kathodische piekstromen van tien opeenvolgende scanning-CV-curven in 50 μM H2 O2 . c Reproduceerbaarheid van zes Co2 P/ITO-elektroden voor detectie van 1,0 mM H2 O2 . d Herhaalbaarheid van Co2 P/ITO-elektrode voor detectie van 1,0 mM H2 O2 acht keer
Bovendien is de stabiliteit, reproduceerbaarheid en herhaalbaarheid van de Co2 P/ITO-transducers werden ook geëvalueerd. De reductiepiekstromen van tien opeenvolgende scanning-CV-curven in 50 μM H2 O2 wordt getoond in Fig. 4b. Na tien cycli daalde de piekstroom van de elektrode slechts met 2,7%. Bovendien bleef de sensor ongeveer 98,2% van zijn aanvankelijke huidige respons na een maand in de lucht te hebben gestaan (Fig. S9), wat een ideale detectiestabiliteit en uitstekende duurzaamheid op lange termijn aantoont. De reproduceerbaarheid van elektrode tot elektrode wordt onderzocht door de relatieve standaarddeviatie (RSD) van H2 te berekenen O2 huidige reacties. Om de potentiële fout van de fabricage van de elektroden zo veel mogelijk te elimineren, moet de constante stroomdichtheid in aanwezigheid van H2 O2 wordt afgetrokken van het initiële achtergrondsignaal van de individuele elektrode en de verkregen verschilwaarde wordt beschouwd als de elektrochemische respons van elke elektrode. Zes Co2 P/ITO-elektroden werden onder dezelfde omstandigheden vervaardigd voor gecontroleerde experimenten en de RSD van stroomresponsen was 1,24%, zoals weergegeven in figuur 4c, wat de relatief uitstekende reproduceerbaarheid van Co2 aangeeft. P/ITO. Ondertussen werd de herhaalbaarheid gemeten in één elektrode door 1,0 mM H2 . te detecteren O2 acht keer, en de RSD van 1,14% werd bereikt (figuur 4d). De bovenstaande resultaten illustreren de bevredigende stabiliteit, reproduceerbaarheid en herhaalbaarheid van de elektrode voor niet-enzymatische elektrochemische detectie van H2 O2 .
Conclusie
Samengevat, Co2 P NP's werden met succes gesynthetiseerd door de hydrothermale methode. Verder is de Co2 P NP's bereid bij 200 °C gedurende 12 uur zijn bewezen als een efficiënte katalysator voor elektrochemische reductie van H2 O2 in pH 7,4 PBS. Als een niet-enzymatische H2 O2 sensor, de Co2 De P/ITO-elektrode vertoonde een snelle amperometrische respons van minder dan 5 s, een breder responsbereik van 0,001 tot 10,0 mM en een lage detectielimiet van 0,65 μM, evenals bevredigende selectiviteit, reproduceerbaarheid en stabiliteit. Dit werk heeft tot doel het onderzoek naar de toepassing van overgangsmetaalfosfide in elektrochemische detectie van kleine biomoleculen en onze Co2 P/ITO-sensor kan worden ontworpen als een nieuw niet-enzymatisch platform voor H2 O2 detectie.
Beschikbaarheid van gegevens en materialen
Alle gegevens en materialen zijn volledig en onbeperkt beschikbaar.
Afkortingen
- NP's:
-
Nanodeeltjes
- ITO:
-
Indiumtinoxide
- TEM:
-
Transmissie-elektronenmicroscopie
- HRTEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- XRD:
-
Röntgendiffractie
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- EDX:
-
Energie-dispersieve röntgenspectroscopie
- CV:
-
Cyclische voltammetrie
- I-t:
-
Amperometrie
- Gly:
-
Glycine
- AA:
-
Ascorbinezuur
- UA:
-
Urinezuur
- Arg:
-
Arginine
- Lys:
-
Lysine
- DA:
-
Dopamine
- APAP:
-
paracetamol
- ATMP:
-
Trimethyleenfosfonzuur
- PBS:
-
Fosfaatbuffer
- LOD:
-
Detectielimiet
- RSD:
-
Relatieve standaarddeviatie
Nanomaterialen
- Demonstratie van een flexibele op grafeen gebaseerde biosensor voor gevoelige en snelle detectie van eierstokkankercellen
- MoS2 met gecontroleerde dikte voor elektrokatalytische waterstofevolutie
- Koolstofnanodots als dual-mode nanosensoren voor selectieve detectie van waterstofperoxide
- Vervaardiging, karakterisering en biologische activiteit van avermectine nano-afgiftesystemen met verschillende deeltjesgroottes
- Silica diatomeeënschalen op maat gemaakt met Au-nanodeeltjes maken gevoelige analyse van moleculen mogelijk voor biologische, veiligheids- en milieutoepassingen
- Een gemakkelijke methode voor de bereiding van Cu2O-TiO2 NTA heterojunctie met zichtbare fotokatalytische activiteit
- Een nieuwe nanocone-clustermicrostructuur met antireflectie en superhydrofobe eigenschappen voor fotovoltaïsche apparaten
- Plasmonische ELISA voor gevoelige detectie van ziektebiomarkers met een smartphonelezer
- De invloed van materialen, heterostructuur en oriëntatie voor nanohybriden op fotokatalytische activiteit
- Gereduceerde grafeenoxide-gecoate Si-nanodraden voor zeer gevoelige en selectieve detectie van formaldehyde binnenshuis
- Draaibank ontworpen voor precisie en snelheid



