Synthese van verschillende grootte gouden nanodeeltjes door middel van chemische reductiemethode met verschillende oplosmiddelpolariteit
Abstract
Gecompliceerde en strikte protocollen worden gevolgd om de grootte van gouden nanodeeltjes (BNP's) in chemische synthesemethoden af te stemmen. In deze studie behandelen we de polariteit van oplosmiddelen als een hulpmiddel voor het afstemmen van de grootte van BNP's in de chemische reductiemethode. De effecten van variërende polariteitsindex van het reactiemedium op het synthetiseren van gouden nanodeeltjes door middel van chemische reductiemethode zijn onderzocht. Ethanol als polair oplosmiddel, ethanol-watermengsel als reactiemedium, L-ascorbinezuur als reductiemiddel en polyvinylpyrrolidon als stabilisator werden gebruikt om BNP's te synthetiseren. De polariteitsindex van het reactiemedium werd aangepast door de volumeverhouding van ethanol tot water te veranderen. Karakteriseringen van UV-Vis, dynamische lichtverstrooiing (DLS) en transmissie-elektronenmicroscopie (TEM) laten zien dat de groei van nanodeeltjes geleidelijk toenam (~ 22 tot 219 nm hydrodynamische diameter) met afnemende waarde van de polariteitsindex van het reactiemedium (~ 8,2 tot 5.2). Bovendien produceerde de hoge polariteitsindex van het reactiemedium kleinere en sferische nanodeeltjes, terwijl een lagere polariteitsindex van het reactiemedium resulteert in grotere BNP's met verschillende vormen. Deze resultaten impliceren dat de mechanistiek van de groei-, assemblage- en aggregatieverschijnselen van ligand- of stabilisator-afgetopte BNP's sterk afhankelijk zijn van de polariteit van oplosmiddelmoleculen. Met behulp van de voorgestelde methodologie kan een breed scala aan BNP's met verschillende morfologiegroottes worden gesynthetiseerd door eenvoudig het volumepercentage organisch oplosmiddel in het reactiemedium te moduleren.
Inleiding
Gouden nanodeeltjes (BNP's) worden erkend als een potentiële kandidaat in veel gebieden van wetenschappelijke en technische toepassingen, waaronder medische therapie [1], medicijnafgifte [2], chemische detectie [3, 4], katalysatie [5] en elektronische [6] toepassingen vanwege de grootte- en vormafhankelijke oppervlakteplasmonresonantie (SPR) [7], affiniteit met organische soorten en hoge elektrische geleidbaarheidseigenschappen [8] van BNP's. Gezien de exponentieel toenemende vraag naar BNP's, wordt veel meer aandacht besteed aan het synthetiseren van monodisperse nanodeeltjes met regelbare grootte en morfologie. Er zijn talloze ontwerpprincipes voorgesteld om de eigenschappen van BNP's te beheersen door verschillende reactanten, stabilisatoren of liganden [9], reactieomstandigheden waaronder temperatuur, pH en concentratie [4] en gedispergeerd medium (zoals verschillende soorten oplosmiddel) op te nemen. [10].
Bij de chemische synthese van BNP's is de Turkevich-methode een veelbelovende methode in vergelijking met andere. In de Turkevich-methode, Au 3+ ionen worden gereduceerd door een mild reductiemiddel zoals citraat [11], ascorbinezuur [12] en looizuur [13] in een waterig medium. In dit proces worden relatief kleine en biocompatibele BNP's geproduceerd. Het belangrijkste nadeel van deze methode is echter het zeer controleerbare procesprotocol (temperatuur, concentratie en pH) dat strikt moet worden gevolgd om monodisperse deeltjes met gewenste afmetingen te produceren. Bovendien is labeling van BNP's door organische geneesmiddelmoleculen en oppervlaktemodificatie met verschillende liganden in een zuiver waterig medium moeilijk vanwege de minder oplosbaarheid en hydrofobiciteit van de organische component in water [14]. Er wordt dus aandacht besteed aan het overwinnen van deze beperkingen van de Turkevich-methode door het reactiemedium te optimaliseren dat de eigenschappen van oplosmiddel aanzienlijk controleert.
Oplosmiddel speelt een belangrijke rol bij de groei en assemblage van nanodeeltjes in het colloïdale syntheseproces. Interactie tussen het oppervlak van nanodeeltjes en oplosmiddelmoleculen of interactie tussen de oplosmiddelmoleculen en ligandmoleculen heeft een aanzienlijke invloed op de uiteindelijke deeltjesgrootte en morfologie [15, 16]. In het algemeen wordt, bij afwezigheid van de passieve liganden of het afdekmiddel, de sterkte van de elektrische dubbele laag die de deeltjesgroei regelt dominant bepaald door de aard van oplosmiddelmoleculen. Bij een hoge polariteitsindex van gedispergeerd medium worden grote hoeveelheden geladen ionen geadsorbeerd door het oppervlak van nanodeeltjes, waardoor zich een sterke elektrische dubbele laag vormt rond de colloïdale deeltjes [17]. Als gevolg hiervan neemt de zeta-potentiaal van deeltje toe en wordt voorkomen dat de deeltjes aggregeren door elkaar af te stoten. De oppervlaktelading rond de nanodeeltjes kan echter worden gemanipuleerd door de polariteit van het oplosmiddel, en de interactie tussen de deeltjes wordt gecontroleerd voordat de grootte en vorm worden geoptimaliseerd [18]. Bijvoorbeeld Song et al. produceerde een bereik van 1-6 nm van thiol-afgetopte BNP's in verschillende polariteiten van organisch oplosmiddel [19]. Hoewel er weinig werken zijn voorgesteld om de grootte van BNP's in verschillende polariteiten van oplosmiddelen te optimaliseren, ligt de grootte van de uiteindelijke deeltjes tussen een klein bereik (minder dan 20 nm) dat niet volledig kan voldoen aan de belangrijkste toepassingen van BNP's, zoals voor therapeutische en medicijnafgifte .
Aan de andere kant, in aanwezigheid van liganden in het reactiemedium, beïnvloeden interacties tussen oplosmiddelmoleculen en liganden de groei en assemblage van nanodeeltjes aanzienlijk. Vergelijkbare onderzoeken tonen aan dat het niet-waterige medium organische ligandmoleculen in de colloïdale oplossing solvateert, nanodeeltjes in hoge mate beschermen tegen verdere groei en aggregatie [20, 21]. Onder bepaalde omstandigheden, zoals bij hogere concentraties, kan een hoger molecuulgewicht en een grote lengte van liganden echter aggregatie of sterke groei van colloïdale nanodeeltjes veroorzaken. Met name verschillende zwellings- en verlengingssnelheden van ligandmoleculen in verschillende polariteit van de oplosmiddelen veroorzaken gemakkelijk de groei en assemblage van nanodeeltjes in colloïdale synthese [22]. Dit negatieve effect kan echter worden gebruikt als een hulpmiddel om nanodeeltjes met een beheersbare grootte te laten groeien. Meer dan de directe betrokkenheid van oplosmiddel bij de groei van nanodeeltjes, kan het concept van het regelen van de eigenschappen van liganden met behulp van oplosmiddel het mogelijk maken om BNP's te synthetiseren met een breed scala aan schaalgroottes.
Rekening houdend met de bovengenoemde propositie, stelt deze studie een methode voor om de grootte en morfologie van het BNP te optimaliseren door het ligand of de stabilisator en de oppervlakteladingen te regelen met behulp van de polariteitsindex van het reactiemedium als hulpmiddel. In deze studie werden BNP's gesynthetiseerd via een chemische reductiemethode met L-ascorbinezuur als reductiemiddel en PVP als stabilisator. In vergelijking met watermoleculen is de polariteitsindex van ethanol (geselecteerd polair organisch oplosmiddel in deze studie) minder. Daarom werd de polariteitsindex van het reactiemedium gemanipuleerd door ethanol toe te voegen aan water in verschillende volumeverhoudingen. In tegenstelling tot de conventionele Turkevich-methode, wordt verwacht dat het BNP's met een breed scala aan BNP's van voorkeursgrootte zal synthetiseren met behulp van deze voorgestelde techniek in een enkele stap met het minimale protocol.
Methoden
Materiaal
HAuCl4 ∙3H2 O (≥ 99% sporenmetaalbasis), kristallijn L-ascorbinezuur, polyvinylpyrrolidon (PVP) K60 en natriumhydroxide (NaOH) pellets werden gekocht bij Sigma-Aldrich (Missouri, VS). Ethanol (99,90% test) werd verkregen van J-Kollin Chemicals (VK) en dubbel gedestilleerd water (ddH2 O) werd verkregen van het laboratorium (Faculteit Chemische Technologie, UiTM, Maleisië).
Voorbereiding van gouden nanodeeltjes (BNP's)
Colloïdale BNP's werden bereid met behulp van een gemodificeerde Turkevich-benadering met ascorbinezuur [23]. Bij deze methode werd L-ascorbinezuur als reductiemiddel gebruikt en polyvinylpyrrolidine (PVP) als stabilisator. De reductiemiddeloplossing werd bereid door L-ascorbinezuur op te lossen in absolute ethanol of 20%, 50% en 80% volumeverhoudingen van ethanol tot water binair oplosmiddelmengsel. Het totale volume water dat aan het mengsel van ethanol tot water binair oplosmiddel werd toegevoegd, werd bepaald volgens Vgl. (1). Bovendien werd PVP direct opgelost in het L-ascorbinezuur/ethanol tot wateroplosmiddelmengsel tot de eindconcentratie van 1% (w/v) onder lage decibelsonicatie. Ten slotte werd de pH van de reductiemiddeloplossing ingesteld op 10,5 vanaf de beginwaarde door druppelsgewijs 2 M NaOH toe te voegen.
$$ Volume\ percentage\ van\ water\ in\ oplosmiddel\ mengsel\ \left(\%\right)=\frac{V_w+{V}_{GC}}{V_R}\times 100\kern0.5em $$ ( 1)waarbij het watervolume V . is W , volume goudchloride is V GC , en het totale volume van het reactiemengsel is V R .
Het BNP-vormende reactiemengsel werd bereid door snel 5 mM HAuCl4 . te injecteren waterige oplossing tot de reductiemiddeloplossing. Het totale volume van het reactiemengsel werd op 20 ml HAuCl4 . gehouden en L-ascorbinezuuroplossingen. De initiële concentratie van de HAuCl4 en L-ascorbinezuur in het uiteindelijke reactiemengsel werd ingesteld op respectievelijk 0,15 mM en 1,5 mM met een molaire verhouding van HAuCl4 tot L-ascorbinezuur van 1:10. Het reactiemengsel werd krachtig geroerd met 800 rpm gedurende 30 min bij omgevingstemperatuur, en het resulterende BNP-colloïde werd gefiltreerd met behulp van Whatman laboratoriumfilterpapier vóór opslag bij 4 °C om een continue reactie te voorkomen.
Karakterisering en instrumentatie
UV–vis-karakterisering
UV-zichtbare extinctiespectra van elk BNP-monster werden gemeten bij omgevingstemperatuur (25°C) met behulp van een Agilent Cary 60 UV-Vis-spectrofotometer. De maximale oppervlakteplasmonresonantie (SPR) golflengte van de resulterende BNP's werd bepaald uit de verkregen UV-Vis-gegevens om de deeltjesgrootte te vergelijken.
Verdeling van deeltjesgrootte en zeta-potentieel
De gemiddelde deeltjesgrootte, grootteverdeling, polydispersiteitsindex (PDI) en zeta-potentiaal van BNP's werden gemeten met behulp van een Malvern Zetasizer nanoZS-instrument. De PDI-waarde werd berekend uit grafieken van intensiteitsdeeltjesgrootteverdeling (PSD) van dynamische lichtverstrooiing (DLS) metingen met behulp van Vgl. (2) [24]:
$$ PDI={\links(standaard\deviatie/gemiddelde\deeltjes\grootte\rechts)}^2 $$ (2)Polariteitsindexanalyse van gemengd oplosmiddel
De polariteit van het reactiemedium werd geoptimaliseerd door verschillende volumetrische verhoudingen van water en organisch oplosmiddel te mengen. Verder is de netto polariteitsindex van het resulterende mengsel van organisch oplosmiddel en water, P ′, kan worden gegeven door Vgl. (3) [25].
$$ {P}^{\prime }=\sum {p}_i^{\prime }{\varnothing}_i $$ (3)waarbij \( {p}_i^{\prime } \)de polariteitsindex is van oplosmiddel i , en ∅i is de volumefractie van oplosmiddel i in het mengsel. De polariteitsindex van gedestilleerd water en absolute ethanol was respectievelijk 9,0 en 5,2.
Transmissie-elektronenmicroscopie (TEM) en deeltjesgrootteverdeling
BNP-monsters werden voorafgaand aan TEM-meting gesoniceerd. Druppeltjes van de gesoniceerde suspensies/colloïden werden vervolgens op 200 mesh Formvar koperen rooster gedruppeld. Het raster werd in een "single tilt" -monsterhouder geplaatst, gevolgd door het in een 200 kV FEI, Tecnai G2 20 Twin Transmission Electron Microscope te plaatsen voor beeldvorming. Bovendien werd kwantitatieve analyse van deeltjesgrootte en grootteverdeling van TEM-afbeeldingen geanalyseerd met behulp van de ImageJ-beeldverwerkingssoftware.
Resultaten en discussie
Figuur 1 toont de UV-Vis-spectra van gesynthetiseerde colloïdale BNP's in verschillende volumetrische verhoudingen van ethanol tot wateroplosmiddelmengsel. Typisch, maximale SPR-absorptiegolflengte (λm ) van het BNP is afhankelijk van grootte en vorm [26, 27]. Zoals getoond in Fig. 1, maximaal λm van de gesynthetiseerde colloïdale BNP-verschuiving naar rechts, wat impliceert dat de grootte van gesynthetiseerde BNP's toenam met een toenemende volumetrische verhouding van ethanol in water. De maximale λm van de colloïdale BNP's die zijn gesynthetiseerd in reactiemengsels die ethanol bevatten met 20% en 50% volumetrisch percentage verschijnt in het kortere gebied van absorptiegolflengten (514 nm en 520 nm), wat impliceert dat kleine BNP's werden geproduceerd in een laag volumepercentage ethanol. Bovendien is de maximale λm van BNP's gesynthetiseerd in ethanol tot water met 80% volumetrisch percentage of absolute ethanol verschoven naar de hogere golflengtegebieden bij respectievelijk 575 nm en 561 nm. Deze verschuivingen duiden op de vorming van een grotere omvang en een brede trend van de grafieken die de ongelijke vormen van het BNP impliceren.
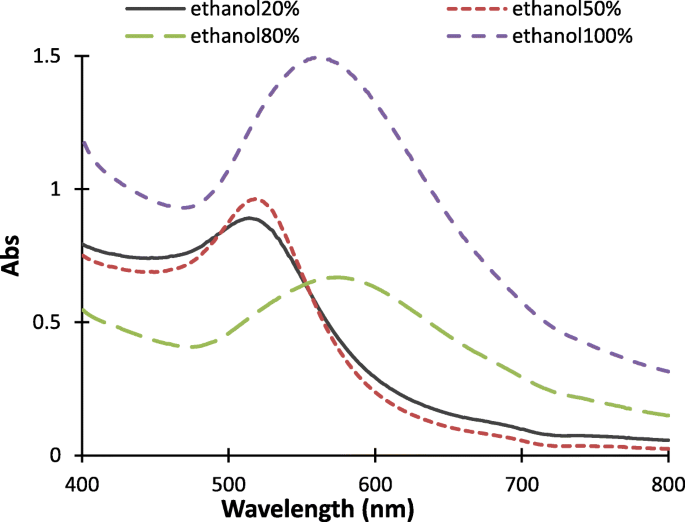
UV–Vis-spectra van BNP's in 20%, 50%, 80% en 100% volumepercentage van ethanol tot water binair oplosmiddelmengsel
De gesynthetiseerde BNP's in verschillende volumetrische percentages van ethanol tot watermengsels met verschillende polariteitsindexen werden gekwantificeerd met behulp van DLS, en de verkregen grootteverdeling van BNP's wordt getoond in Fig. 2. Bovendien worden de gemiddelde deeltjesgrootte, PDI-waarden van BNP's en polariteit indexen van ethanol-watermengsels van geproduceerde BNP's zijn samengevat in Tabel 1. Figuur 2 laat zien dat de DLS-grootteverdeling toeneemt met een toenemend volumetrisch percentage ethanol. De gemiddelde hydrodynamische diameters van BNP's in mengsels van oplosmiddelen die absolute ethanol, 80%, 50% en 20% ethanol tot water volumetrisch percentage bevatten, waren respectievelijk 154 ± 56,7, 219 ± 84,9, 28 ± 10,5 en 22 ± 4,6 nm (zie tabel 1). Deze DLS-resultaten zijn vergelijkbaar met de UV-Vis-bevindingen van deze studie, waarbij kleine deeltjes werden geproduceerd in een hoge polariteitsindex van het ethanol-watermengsel en vice versa.
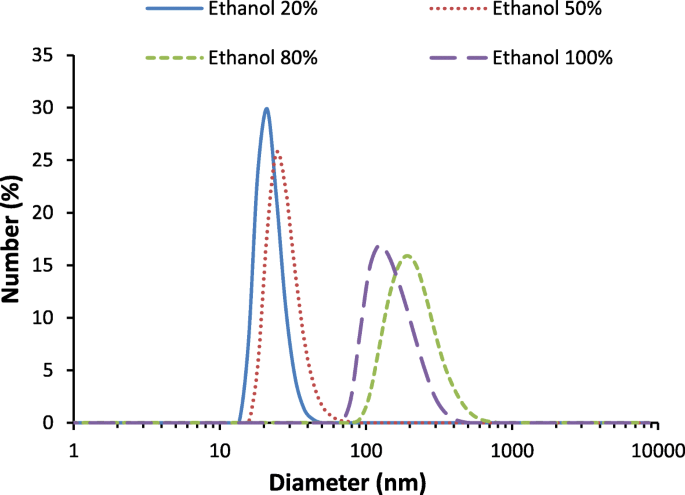
DLS-grootteverdelingstrends van BNP-deeltjes in 20%, 50%, 80% en 100% volumepercentage van ethanol tot water binair oplosmiddelmengsel
De berekende polariteitsindexwaarden van verschillende volumepercentages van ethanol tot wateroplosmiddelmengsels worden gegeven in Tabel 1. De polariteitsindex van binair oplosmiddelmengsel neemt af met een toenemend volumetrisch percentage ethanol (organisch oplosmiddel) in het oplosmiddelmengsel. Hierin onthullen UV-Vis- en DLS-resultaten van deze studie dat de kleinere omvang van BNP's werd geproduceerd in een hoge polariteitsindex van reactiemedium, terwijl grotere omvang van BNP's werd geproduceerd in een lage polariteitsindex van reactiemedium. Het is goed bestudeerd dat zowel oplosmiddelen als liganden een belangrijke rol spelen bij het beheersen van de groei en assemblage van nanodeeltjes in het colloïdale syntheseproces van nanodeeltjes. Tijdens de vorming van nanodeeltjes controleren en vertragen oplosmiddelmoleculen en ligandmoleculen de deeltjesgroei door de bindingsplaatsen aan het oppervlak te blokkeren. In bepaalde omstandigheden, zoals verschillende polariteit van het oplosmiddelmengsel, kunnen de oplosmiddelmoleculen en ligandmoleculen echter ook de groei en assemblage van nanodeeltjes in colloïdale oplossingen veroorzaken. In overeenstemming met deze verklaring laten UV-Vis- en DLS-resultaten zien dat de groei en assemblage van PVP-afgetopte BNP's toenam met een toenemend volumepercentage ethanol in binair oplosmiddelmengsel. Om deze bevindingen te valideren, kan het corresponderende mechanisme voor de groei van PVP-afgetopte BNP's in ethanol-water binair oplosmiddelmengsel worden geïnterpreteerd in twee fasen (zoals getoond in Fig. 3), namelijk door oplosmiddel veroorzaakte groei en door ligand geïnduceerde groei.
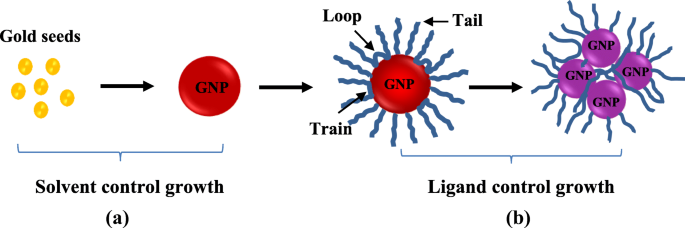
Groeistadia van BNP's in colloïdale oplossing in aanwezigheid van ligandmoleculen met lange polymeerketens waarbij de groei van BNP's wordt bepaald door (a ) oplosmiddelmoleculen en (b ) ligand moleculen
In de eerste fase, na kiemvorming van monomeren, werd de groei van BNP's bepaald door de oplosmiddelmoleculen. In colloïdale oplossingen verdelen hoogpolaire oplosmiddelmoleculen een hoge oppervlaktelading op het oppervlak van de nanodeeltjes en bouwen ze een sterke elektrische dubbele laag op die voorkomt dat deeltjes verder groeien, terwijl oplosmiddelmoleculen met een lage polariteitsindex een zwakke elektrische dubbele laag rond de deeltjes vormen, wat resulteert in een hogere groei of aggregatie [28]. De correlatie tussen de oppervlaktelading en de polariteitsindex van de reactie kan worden verklaard met behulp van de vergelijking van Poisson in Vgl. (4) [29].
$$ \varepsilon {\varepsilon}_o\frac{d^2\psi (x)}{d{x}^2}=-\rho (x)\kern4em $$ (4)waar ρ is de ladingsdichtheid, ψ is de elektrische potentiaal, ε is de permittiviteit van vacuüm, ε o is de diëlektrische constante, en x is de afstand tussen het deeltjesoppervlak.
Volgens vgl. (4), ladingsdichtheid op het oppervlak van nanodeeltjes (ρ ) is evenredig met de diëlektrische constante (ε o ) van de omgeving die wordt bepaald door de polariteitsindex van het medium. In deze studie kan de polariteitsindexwaarde van overeenkomstige oplosmiddelen worden gerangschikt als water> ethanol. Daarom kan gedispergeerd medium met een hoger volumetrisch percentage water een hogere oppervlaktelading aan het BNP-oppervlak bieden vanwege de hoge polariteit. Bovendien werkt ascorbinezuur als een reductiemiddel om het elektron aan het metaalzout te doneren om een gouden nanodeeltje te vormen. Ascorbinezuur heeft een hogere oplosbaarheid in zuiver water dan absolute ethanol, waardoor er meer waterstofbinding tot stand komt met watermoleculen. Ook zou de hogere oplosbaarheid meer vrije elektronenoverdracht kunnen bevorderen voor snelle nucleatie van Au 0 monomeren die leiden tot langzame groei van BNP's [30]. Vanwege deze feiten was de groeisnelheid van het BNP omgekeerd aan de polariteitsindexwaarde van het ethanol-wateroplosmiddelmengsel.
In de tweede fase werd verondersteld dat de groei en assemblage van BNP's voornamelijk werden bepaald door ligandmoleculen (PVP) (zie figuur 3(b)). In aanwezigheid van ligandmoleculen in de colloïdale oplossing worden de liganden geadsorbeerd of covalent gehecht aan het oppervlak van nanodeeltjes en voorkomen ze verdere groei en assemblage van de nanodeeltjes door de grensvlakenergie tussen het deeltjesoppervlak en het oplosmiddel te regelen of afstotende krachten te creëren tussen soortgelijke met ligand gecoate deeltjes [28]. Als geadsorbeerde ligandmoleculen echter een hoge concentratie, een lange polymeerketen of een hoog molecuulgewicht hebben, vormen ze een staart, trein en lus in de colloïdale oplossing. Zoals weergegeven in Fig. 3 (b), overbruggen deze uitstekende staarten, treinen en lussen van de ligandketens de nanodeeltjes en induceren ze flocculatie in colloïden [31]. Deze overbruggende uitvlokking in nanodeeltjes kan de secundaire zaadgemedieerde groei in nanodeeltjes bevorderen, waardoor deeltjes gemakkelijk kunnen worden gekweekt. In deze studie werd 1% (w/v) PVP gebruikt om de BNP's in colloïdale oplossing te stabiliseren. PVP is een amfifiel molecuul met een hydrofiele kop (die bestaat uit C =O- en N-soorten) en een zeer hydrofobe koolwaterstofachterketen. In polair organisch oplosmiddel hebben organische moleculen een grote affiniteit met zowel de carboxylgroep als de koolwaterstofstaart van de ruggengraat van PVP, zoals weergegeven in figuur 4 (a). Alleen in een waterig medium kunnen watermoleculen echter alleen binden met de carboxylkop van PVP via waterstofbinding, en hydrofobe staarten blijven onafhankelijk in de suspensie, zoals weergegeven in figuur 4 (b). PVP-moleculen worden dus in een hogere mate gesolvateerd en gezwollen in een organisch oplosmiddel dan zuiver waterig medium [21]. Als bewijs hebben Guettari et al. onderzocht het gedrag van PVP-polymeer in verschillende volumetrische percentages van ethanol tot wateroplosmiddelmengsel. Experimentele resultaten met effectieve oplosmiddelinteractie met polymeer (ESIP) modellering van dit werk bevestigen dat de hydrodynamische straal en polymeer-polymeerinteractie van PVP-moleculen toenemen met toenemende molaire fractie van ethanol [32]. Deze toenemende bolvormige grootte van de PVP-moleculen in een hoger volumepercentage ethanol verbetert de overbrugging van BNP's, wat resulteert in een hoge groei of assemblage. Daarom werd geconcludeerd dat sterk verlengde 1% (w/v) PVP-ketens de deeltjes uitvlokten en de verschillende vormen van assemblage of aggregatie van BNP's vormden die een hoge groei veroorzaken in een hoge volumetrische verhouding van ethanol [33,34,35] .
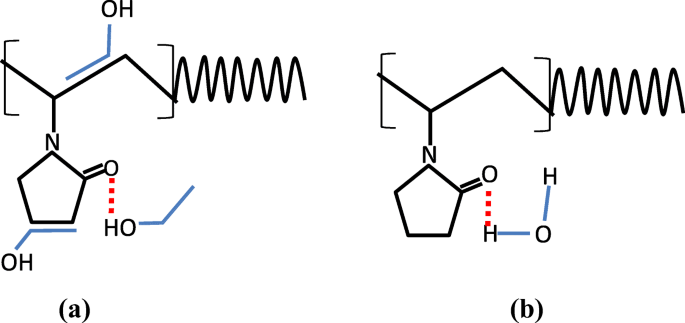
(een ) Interactie tussen ethanolmoleculen en PVP-moleculen en (b ) Interactie tussen H2 O-moleculen en PVP-moleculen
Verder werd de invloed van ligandmoleculen op de groei en assemblage van nanodeeltjes in variërende polariteitsindex van ethanol-wateroplosmiddelmengsel geanalyseerd door de zeta-potentiaal van de resulterende BNP's. De zeta-potentiaalwaarden van BNP's die werden gesynthetiseerd in een andere volumetrische verhouding van ethanol tot water, worden getoond in Fig. 5. De verkregen resultaten laten zien dat de zeta-potentiaalwaarden van PVP-gestabiliseerde BNP's afnemen met een toenemend volumepercentage ethanol. In het algemeen verdringt het polymeer het glijvlak van de elektrische dubbele laag van de deeltjes, wat de zeta-potentiaalwaarde kan veranderen. De veranderingen in de waarde van de zeta-potentiaal hangen af van de grensvlaklading en de hoeveelheid geadsorbeerd polymeer [22]. Vergelijkbare onderzoeken hebben aangetoond dat de zeta-potentiële waarde van volledig PVP-afgetopte BNP's ongeveer - 6 mV is [23, 36]. Bovendien kan deze negatieve zeta-potentiaalwaarde toenemen met afnemende adsorptiehoeveelheid PVP op het BNP-oppervlak [22]. Daarom geeft de verkregen laagste waarde van zeta-potentiaal (-5,53 mV) in absolute ethanol aan dat de gesynthetiseerde BNP's volledig werden omringd door PVP-moleculen. Aan de andere kant namen de zeta-potentiaalwaarden af met toenemende volumetrische verhouding van ethanol, impliciet dat de PVP in hoge mate geadsorbeerd werd in een hoge volumetrische verhouding van organisch oplosmiddel (ethanol).
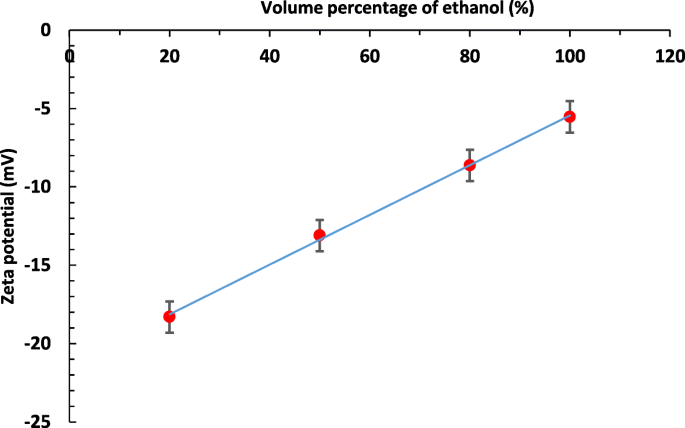
Zeta-potentiële waarden van PVP-gestabiliseerde BNP's in 20%, 50%, 80% en 100% volumepercentage van ethanol tot water binair oplosmiddelmengsel
TEM-afbeeldingen van de gesynthetiseerde BNP's in verschillende polariteitsindexen van ethanol tot wateroplosmiddelmengsels worden getoond in Fig. 6. Figuren 6 (a) en (b) laten zien dat 9,7 nm en 13,9 nm van bijna bolvormige nanodeeltjes werden geproduceerd in 20% en 50 % volumetrisch percentage ethanol tot wateroplosmiddelmengsel respectievelijk. Aan de andere kant toont Fig. 6 (c) de typische afbeeldingen van BNP's in 80% volumetrisch percentage ethanol tot watermengsel. TEM-afbeeldingen laten zien dat een onregelmatige vorm [37] en grotere afmetingen (ongeveer 53,1 nm) van BNP's werden gevormd in 80% volumetrisch percentage ethanoloplossing, en deze deeltjes werden geaggregeerd in de colloïdale oplossing. Evenzo werd een gemiddelde diameter van 37,2 nm met een relatief grotere en onregelmatige vorm van BNP's ook in absolute ethanol geproduceerd. Deze resultaten komen overeen met de eerdere UV-Vis- en DLS-resultaten van deze studie, waarin de grotere deeltjesgrootte werd gevormd vanwege de lage waarde van de polariteitsindex van het reactiemedium, wat de groei van deeltjes en assemblage veroorzaakt door de sterk uitgebreide PVP tot gevolg had. polymeerketen in lage polariteitsindex van ethanol-oplosmiddelmengsel.
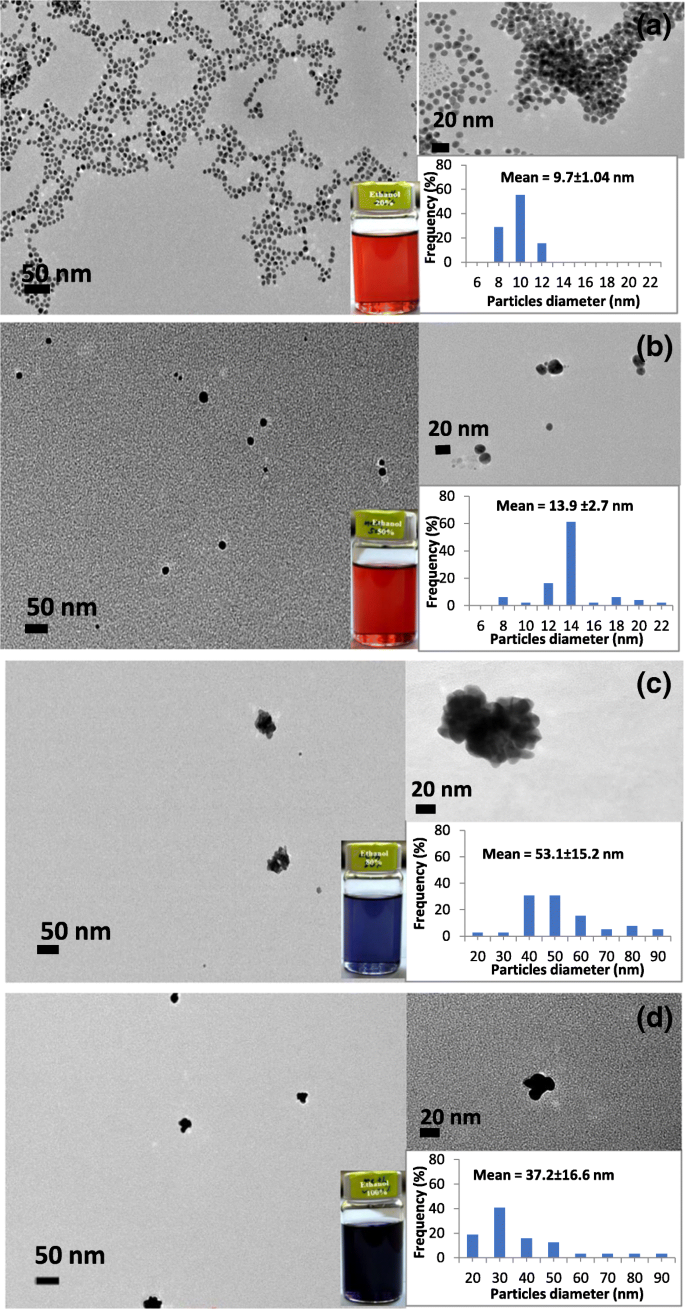
Kleuren, TEM-afbeeldingen en grootteverdeling van de geproduceerde BNP-suspensie in verschillende volumepercentages ethanol tot water met (a ) 20%, (b ) 50%, (c ) 80%, en (d ) 100% ethanol
Het is de moeite waard om te informeren dat de grootte van het BNP in 80% volumetrisch percentage ethanol tot water groter is dan de grootte van het BNP in absolute ethanol.
Figuren 7 (a) en (d) vergelijken de TEM-afbeeldingen van BNP's in respectievelijk 80% volumetrische verhouding van ethanol tot water en absolute ethanol. De BNP's werden geaggregeerd als clusters (Fig. 7 (a-c)) en lineair uitgelijnd (Fig. 7 (a) en (b)) in 80% volumetrische verhouding van ethanol, terwijl BNP's in absolute ethanol als afzonderlijke deeltjes bleven met minder aggregatie (Fig. 7d). We veronderstelden dat de samenstelling van 80% ethanol tot water de oppervlakte-energie van primaire BNP-deeltjes snel verhoogde vanwege de asymmetrische interactie van water- en ethanolmoleculen met PVP-polymeerketen- en nanodeeltjesoppervlakken. Daarom vormden deeltjes geaggregeerd door een georiënteerd-bevestigingsmechanisme grotere nanoclusters om deze oppervlakte-energie te minimaliseren [38, 39]. Bovendien werd de lineaire uitlijning van BNP's in 80% ethanol ten opzichte van water toegeschreven aan de dipool-dipool-interactie van de deeltjes die werd veroorzaakt door de asymmetrische interactie van water- en ethanolmoleculen met de PVP-polymeerketen [40]. Bovendien werd waargenomen dat de gemiddelde hydrodynamische diameter van BNP's verkregen met behulp van DLS hoger was dan de grootte berekend op basis van TEM-afbeeldingen. In deze studie werden BNP's gesynthetiseerd in een overmatige hoeveelheid PVP-polymeeroplossing. Daarom mat de DLS-techniek niet alleen de diameter van de deeltjes, maar ook de afdekpolymeerlaag met langwerpige polymeerstaart, trein en lus. Bovendien kan DLS de grootte van vlokken meten in plaats van individuele deeltjes (bijv. 80% ethanol tot water BNP-monster). Bijgevolg was de gemiddelde grootte van het BNP gemeten met DLS hoger dan met TEM.

TEM-afbeeldingen van BNP's (a ), (b ) en (c ) geaggregeerde deeltjes in 80% volumetrisch percentage ethanol (d ) discrete deeltjes in 100% ethanol
Conclusie
In deze studie is de synthese van grootteselectieve BNP's besproken met behulp van de polariteit van organisch oplosmiddel als variabele. Invloed van oplosmiddelpolariteit in BNP-groei is onderzocht door PVP-afgetopte BNP's te synthetiseren in ethanol en ethanol-watermengsels in L-ascorbinezuur. UV-vis-spectra en DLS-metingen bevestigden dat de deeltjesgrootte toeneemt met afnemende polariteitsindex van het oplosmiddel. Op basis van deze resultaten werd de groei van het BNP in twee fasen gecontroleerd tijdens het chemische reductieproces. De deeltjesgroei werd aanvankelijk gecontroleerd door de oplosmiddelmoleculen door een sterke dubbele laag rond het nanodeeltje te vormen. Vervolgens worden de assemblage en stabiliteit van BNP's bepaald door de stabilisator- of ligandmoleculen in de tweede fase. De groei van BNP's neemt echter in beide stadia toe met afnemende polariteitsindex van het reactiemedium. De uiteindelijke kleuren van gesuspendeerde BNP's en TEM-afbeeldingen impliceren de morfologieën van de geproduceerde BNP's. Met name resulteerde een hoge polariteit van het oplosmiddelmengsel in bolvormige BNP's en een omgeving met een lage polariteitsindex resulteerde in een onregelmatige vorm van BNP's. Dit onderzoek richtte zich op een nieuwe benadering om verschillende groottes en vormen van BNP's in één enkele stap te synthetiseren door gebruik te maken van de oplosmiddelpolariteitsindex-afhankelijke deeltjesgroei en assemblage.
Beschikbaarheid van gegevens en materialen
Alle gegevens die tijdens dit onderzoek zijn gegenereerd of geanalyseerd, worden in dit onderzoek meegenomen. De ruwe dataset die tijdens het experimentele werk is verkregen en geanalyseerd, is op redelijk verzoek verkrijgbaar bij de corresponderende auteur.
Afkortingen
- BNP:
-
Gouden nanodeeltjes
- NP's:
-
Nanodeeltjes
- PVP:
-
Polyvinylpyrrolidon
- TEM:
-
Transmissie-elektronenmicroscopie
- DLS:
-
Dynamische lichtverstrooiing
- PDI:
-
Polydispersiteitsindex
Nanomaterialen
- Plasmonische nanodeeltjes
- Gouden nanodeeltjes voor chemosensoren
- Elektrospun polymeer nanovezels versierd met edele metalen nanodeeltjes voor chemische detectie
- Eenvoudige synthese van gekleurd en geleidend CuSCN-composiet gecoat met CuS-nanodeeltjes
- Eenvoudige synthese van zilveren nanodraden met verschillende beeldverhoudingen en gebruikt als hoogwaardige flexibele transparante elektroden
- Verbeterde stabiliteit van gouden magnetische nanodeeltjes met poly(4-styreensulfonzuur-co-maleïnezuur):op maat gemaakte optische eigenschappen voor eiwitdetectie
- Nabehandelingsmethode voor de synthese van monodisperse binaire FePt-Fe3O4-nanodeeltjes
- Gemodificeerd hypervertakte polyglycerol als dispergeermiddel voor groottecontrole en stabilisatie van gouden nanodeeltjes in koolwaterstoffen
- Effect van de synthesemethode van La1 − xSr x MnO3 manganite nanodeeltjes op hun eigenschappen
- Bevordering van SH-SY5Y-celgroei door gouden nanodeeltjes gemodificeerd met 6-mercaptopurine en een neuron-penetrerend peptide
- Gecontroleerde synthese van BaYF5:Er3+, Yb3+ met verschillende morfologie voor de verbetering van upconversie-luminescentie



