Stapsgewijze synthese van Au@CdS-CdS Nanoflowers en hun verbeterde fotokatalytische eigenschappen
Abstract
Fabricage van hybride nanostructuren met complexe morfologieën en hoge fotokatalytische activiteit is een moeilijke uitdaging omdat deze deeltjes extreem hoge preparatievaardigheden vereisen en niet altijd praktisch zijn. Hier zijn hiërarchische bloemachtige Au@CdS-CdS-nanodeeltjes (Au@CdS-CdS-nanobloemen) gesynthetiseerd met behulp van een stapsgewijze methode. De Au@CdS-CdS nanoflowers bestaan uit Au core, CdS shell en CdS nanorods. Het UV-Vis-absorptiebereik van de Au@CdS-CdS nanoflowers reikt tot 850 nm, wat het hele zichtbare bereik dekt (400-760 nm). Foto-geïnduceerde ladingsoverdrachtseigenschap van Au@CdS-CdS nanoflowers werd aangetoond met behulp van fotoluminescentie (PL) spectroscopie. Vergeleken met CdS-tegenhangers en Au@CdS-tegenhangers, vertoonden Au@CdS-CdS nanoflowers de hoogste fotokatalytische afbraaksnelheid onder bestraling van respectievelijk λ = 400-780 nm en λ = 600-780 nm. Op basis van structuur- en morfologieanalyses hebben we een mogelijk vormingsmechanisme van de hybride nanostructuur voorgesteld dat kan worden gebruikt om het ontwerp van andere metaal-halfgeleider nanostructuren met complexe morfologieën te sturen.
Inleiding
Zonne-energie wordt momenteel erkend als de meest schone en overvloedige energiebron. De omzetting van zonne-energie in andere energievormen met behulp van halfgeleiderfotokatalysatoren wordt beschouwd als een ideale manier om de energiecrisis en de vervuiling van het milieu op te lossen [1, 2]. Om volledig gebruik te maken van zonne-energie zijn er veel op halfgeleiders gebaseerde fotokatalysatoren ontworpen en ontwikkeld [3, 4]. Onder hen is CdS, met een geschikte bandafstand van ongeveer 2,4 eV voor effectieve absorptie van zichtbaar licht door zonlicht, een van de weinige door zichtbaar licht aangedreven fotokatalysatoren [5]. De hoge recombinatiesnelheid van ladingsdragers en fotocorrosie belemmeren echter de fotokatalytische efficiëntie van CdS ernstig.
In de afgelopen jaren hebben hybride nanostructuren veel aandacht getrokken vanwege hun fysisch-chemische eigenschappen [6,7,8,9]. Vergeleken met de overeenkomstige individuele component, vertonen op CdS gebaseerde hybride nanostructuren betere prestaties in bepaalde toepassingen vanwege het verbeterde lichtabsorptiebereik en verbeterde ladingsscheiding. Yu et al. hebben een uniek ternair sulfide geconstrueerd -[ZnS-CdS-Cu2-x S]-ZnS-heteronanorod die een uitgebreid absorptiegebied en efficiënte ladingsscheiding vertoont, wat leidt tot verbeterde prestaties bij de omzetting van zonne-energie [10]. Xu et al. hebben bolvormige en staafvormige CdS@TiO2 . gesynthetiseerd core-shell nanodeeltjes (CSN's) die uitstekende fotokatalytische prestaties vertonen voor selectieve redoxreacties onder bestraling met zichtbaar licht [11, 12]. Het Z-schema in CdS-Au-TiO2 driecomponenten nanojunctiesystemen vertoonden een hogere fotokatalytische activiteit dan die van een- en tweecomponentensystemen, vanwege de overdracht van elektronen langs de ontworpen route [13]. Hoewel er veel op CdS gebaseerde hybride nanostructuren zijn gesynthetiseerd, blijft de gecontroleerde synthese van hybride nanostructuren met gewenste componenten, structuren en kristalfasen een opmerkelijke uitdaging.
Als een belangrijke tak van hybride nanostructuren zijn metaal-halfgeleider nanostructuren op grote schaal bestudeerd als een nieuw type geavanceerd functioneel materiaal [14,15,16,17,18,19]. Onder hen hebben Au-CdS hybride nanostructuren steeds meer aandacht getrokken vanwege de interactie tussen plasmon en exciton. Plasmonische nanostructuren hebben een aanzienlijk vermogen om lichtenergie op nanoschaal te concentreren, wat voortkomt uit hun aard als een collectieve oscillatie van oppervlakte-elektronen van het metaal met invallend licht op overeenkomende frequenties [20]. Wanneer metalen worden gehybridiseerd met halfgeleiders, zou een dergelijk lichtbeheersvermogen op nanoschaal van plasmonica kunnen worden gebruikt om de efficiëntie van foto-excitatie in de halfgeleiders te verbeteren [21]. In nanowetenschappelijk onderzoek is het ontwerpen van complexe nanostructuren door de grootte en vorm van nanokristallen te regelen van cruciaal belang voor het verkennen van hun nieuwe eigenschappen [22,23,24,25]. Tot nu toe zijn verschillende vormen van Au-CdS hybride nanostructuren voorbereid en toegepast op optische componenten, sensoren, fotovoltaïsche en fotokatalytische apparaten [26,27,28,29,30]. De hiërarchische 3D-structuur van Au-CdS-nanocomposieten met een goed gedefinieerde morfologie is echter zelden gemeld. De synthese van complexe nanocomposieten is een zeer moeilijke uitdaging omdat deze nanodeeltjes extreem hoge voorbereidingsvaardigheden vereisen en niet altijd praktisch zijn.
Hierin construeren we een bloemachtige Au@CdS-CdS nanodeeltjes (Au@CdS-CdS nanoflowers) door middel van een stapsgewijze synthesestrategie. Die hiërarchische heterostructuren heeft die zijn geconstrueerd door epitaxiale groei van 1D CdS-nanostaafjes op de oppervlakken van Au@CdS CSN's en een heterogene structuur tussen Au en CdS. De gesynthetiseerde Au@CdS-CdS-nanobloemen vertonen een uitgebreid absorptiegebied dat tot 850 nm reikt en het hele zichtbare bereik bestrijkt. Au@CdS-CdS-nanobloemen vertonen verbeterde fotokatalytische activiteit in vergelijking met Au@CdS CSN's en CdS-tegenhangers onder de zichtbare bestraling. Op basis van zijn grootte, morfologie en structuur hebben we een haalbaar groeimechanisme voorgesteld, dat waarschijnlijk nuttig zal zijn voor onderzoekers op uiteenlopende gebieden als geneeskunde, energie en elektronica, die vaak complexe nanodeeltjes ontwerpen waarvan wordt voorspeld dat ze nuttige functies hebben.
Methoden
Synthese van Au@CdS-CdS Nanoflowers
Alle chemicaliën die van Aladdin werden ontvangen, waren reagentia van analytische kwaliteit en werden zonder verdere zuivering gebruikt. Au-colloïden met een gemiddelde diameter van 50 nm werden gesynthetiseerd met de traditionele Frens-methode [31] en Au@CdS CSN's werden bereid met behulp van een gepubliceerde hydrothermale methode [32]. Gewoonlijk werd een waterige oplossing van l-cysteïne (Cys, 99%) gemengd met cadmiumnitraattetrahydraat (99%) in een verhouding van 2:1 M van Cys tot Cd 2+ . 2 ml l-cysteïne-cd 2+ (Cys/Cd 2+ ) mengsel werden toegevoegd aan 10 ml Au-colloïden en 15 minuten geroerd, waarna de verkregen Au-(Cys/Cd 2+ ) werden met water verdund tot 50 ml en overgebracht in een met Teflon beklede roestvrijstalen autoclaaf (capaciteit van 100 ml). Na verzegeling werd de autoclaaf verwarmd en 6 uur op 130°C gehouden. Om dikke CdS-omhulsel op Au-nanodeeltjes te coaten, 10 ml Cys/Cd 2+ mengsel werden toegevoegd aan Au-colloïden (10 ml) terwijl de andere reactieomstandigheden ongewijzigd waren.
Au@CdS-CdS nanoflowers werden vervolgens als volgt gesynthetiseerd:de resulterende Au@CdS CSNs-colloïden (10 ml), 1 ml 10 mM Cys/Cd 2+ mengsel en 20 ml ethyleendiamine (En,> 99%) werden gemengd en gedurende 15 minuten geroerd en vervolgens overgebracht in een met Teflon beklede roestvrijstalen autoclaaf (capaciteit van 50 ml). De afgesloten autoclaaf werd tot 180°C verwarmd en gedurende 10 uur op deze temperatuur gehouden, waarna men hem liet afkoelen tot kamertemperatuur. Het product werd verzameld en meerdere keren gewassen met gedestilleerd water en ethanol om resterende ionen en onzuiverheden te verwijderen.
CdS-tegenhangers werden als volgt gesynthetiseerd:4 ml Cys/Cd 2+ mengsel en 20 ml water werden aan de reactor toegevoegd en 15 min geroerd, vervolgens afgesloten en 6 uur verwarmd tot 130°C. De producten werden op natuurlijke wijze afgekoeld tot kamertemperatuur en meerdere keren gewassen met gedestilleerd water en ethanol. Ten slotte werden de monsters gedispergeerd in absolute ethanol.
Materiaalkarakteriseringen
De röntgendiffractie (XRD) metingen van de monsters werden uitgevoerd op een Bruker D8 geavanceerde diffractometer en de UV-Vis absorptiespectra werden getest op een PerkinElmer Lambda 35 fotometer. Veldemissie scanning elektronenmicroscoop (FE-SEM) beelden en energie dispersieve röntgenspectrometer (EDS) werden verkregen op een JSM-7001F apparaat. Het transmissie-elektronenmicroscoop (TEM) -model is JEM-2010 en de bedrijfsspanning is 200 kV. Hoge resolutie transmissie-elektronenmicroscoop (HR-TEM) beelden werden ook getest op JEM-2010 met een bedrijfsspanning van 200 kV. Fotoluminescentie (PL) spectra werden gemeten op een Perkin-Elmer LS-55 met een excitatiegolflengte van 400 nm. Fotostroommetingen (i-t-curven) werden uitgevoerd in een conventioneel celsysteem met drie elektroden met behulp van een CHI660C elektrochemisch station zonder voorspanning onder een 300 W Xe-booglamp als lichtbron. Het gereinigde ITO-glas afgezet met fotokatalysatoren, Pt-vlok en een Ag/AgCl-elektrode werden respectievelijk gebruikt als werkelektroden, tegenelektrode en referentie-elektrode. Na2 SO4 (0,2 M) werd gebruikt als elektrolyt.
Meting van fotokatalytische activiteit
Het optische systeem dat voor de fotokatalytische reactie werd gebruikt, bestond uit een xenonlamp (300 W) en twee banddoorlaatfilters (met een bandbreedte van 400-780 nm en 600-780 nm) die zorgen voor de bestraling in het zichtbare bereik. Vier soorten fotokatalysatoren, waaronder Au-nanodeeltjes, CdS-tegenhanger, Au@CdS dik en Au@CdS-CdS nanobloemen werden gebruikt om rhodamine 6G (R6G) -oplossing af te breken. Meestal werd 6 mg fotokatalysator toegevoegd aan 20 ml R6G-oplossing (1,0 × 10 −5 M) en gedurende 30 minuten in het donker geroerd om adsorptie-evenwicht te bereiken vóór bestraling. De fotokatalytische experimenten werden uitgevoerd onder twee bestralingsbereiken, respectievelijk 400-780 nm en 600-780 nm. Vervolgens werd elke 10 minuten 2,5 ml oplossing geëxtraheerd en gecentrifugeerd om de fotokatalysator te verwijderen. De UV-Vis-absorptiespectra van filtraten werden geregistreerd met behulp van een PerkinElmer Lambda 35-fotometer om de katalytische reactie te volgen. Alle fotokatalyse-experimenten werden uitgevoerd bij kamertemperatuur in lucht. Afbraak van R6G werd als volgt gedefinieerd:
Degradatie (%) = [(C 0 -C t ) / C 0 ] × 100.
waar C 0 is de beginconcentratie van R6G, C t is de concentratie van R6G op een bepaald moment na de fotokatalytische reactie.
Resultaten en discussie
Het synthesemechanisme van nanobloemen
Het stapsgewijze syntheseproces voor de Au@CdS-CdS-nanobloemen is weergegeven in Fig. 1. Eerst worden Au-nanodeeltjes gesynthetiseerd met een gemiddelde grootte van ongeveer 50 nm. De CdS-laag wordt afgezet op het oppervlak van de Au-nanodeeltjes door een hydrothermische reactie om Au@CdS CSN's te produceren. Vervolgens worden de CdS-nanostaafjes op het oppervlak van Au@CdS CSN's gekweekt via een gemengde solvothermische methode om de hiërarchische Au@CdS-CdS-nanostructuren te produceren. l-cysteïne en ethyleendiamine spelen een belangrijke rol bij de synthese van Au@CdS-CdS-nanobloemen. l-cysteïne, met drie functionele groepen (SH, COOH, NH2 ), dient zowel als zwavelbron als als verbindingsmiddel om de roostermismatch tussen Au- en CdS-kristallen te compenseren [32]. De kristalfase zou kunnen worden gecontroleerd door ethyleendiamine in te voeren als een structuurgeleidend reagens in de groei van CdS-nanostaafjes [33]. Bovendien is het voor ons erg moeilijk om Au@CdS-CdS nanoflowers te synthetiseren door Au-colloïden, Cys/Cd 2+ toe te voegen. mengsel en ethyleendiamine samen onder dezelfde omstandigheden. Daarom is het tussenproduct van Au@CdS CSN's noodzakelijk voor de synthese van Au@CdS-CdS-nanobloemen, omdat het oppervlak van de CdS-schaal niet glad is en deze uitstulpingen de "groeiplaatsen" worden voor de epitaxiale groei van CdS-nanostaafjes.
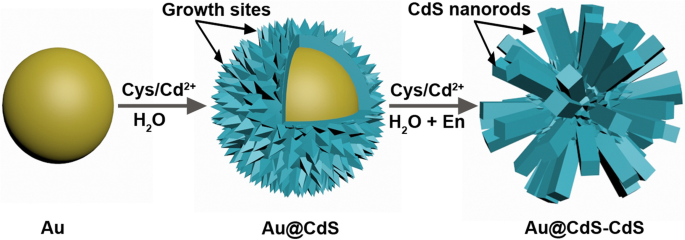
Schematische weergave van de syntheseprocessen van Au@CdS-CdS nanoflowers
Voorbeeld morfologie en structuur
De SEM-afbeeldingen van de nanodeeltjes in elke procedure werden getoond in Fig. 2a-c. Au-nanodeeltjes toonden aan dat ze uniform van grootte waren en goed verspreid waren. Au@CdS CSN's werden getoond in Fig. 2b waarin enkele Au- of CdS-nanodeeltjes zelden werden waargenomen. Het oppervlak van de CdS-schaal was gekarteld en de uitstulpingen konden worden waargenomen in de insert TEM-afbeelding. Zoals getoond in Fig. 2c, presenteerden de Au@CdS-CdS-nanokristallen zich als goed gedefinieerde bloemachtige nanodeeltjes met een goede dispersie. Afbeelding 2d toonde het TEM-beeld van Au@CdS CSN's met een dikke CdS-schaal (aangeduid als Au@CdS dik). Figuur 2e toonde het TEM-beeld van Au@CdS-CdS nanoflowers. Het is te zien dat 1D CdS-nanostaafjes epitaxiaal werden gekweekt op het oppervlak van Au@CdS CSN's. De diameter en de lengte van de CdS-nanostaaf was respectievelijk ongeveer 16 nm en 40 nm. Het HR-TEM-beeld van Au@CdS-CdS-nanobloemen werd getoond in Fig. 2f. De roosterafstand van 0,34 nm in nanostaafjes kwam overeen met de (002) kristalvlakken van wurtziet-CdS. De bereide CdS-nanostaafjes waren eenkristallen met een preferentiële groeirichting van [001], de c-as [34]. De EDS-analyse bevestigde verder de elementaire samenstelling van de Au@CdS-CdS-nanobloemen, zoals weergegeven in Fig. 2g, die de aanwezigheid van de elementen Cd, S en Au aangaf. CdS-nanokristallen met uniforme grootte werden getoond in figuur 2h. Bovendien waren de kleuren van de oplossing van Au-colloïden, Au@CdS dun, Au@CdS-CdS nanoflowers, CdS-tegenhangers en Au@CdS dik respectievelijk rode wijn, paars, groen, geel en groen, weergegeven in Fig. . 2i.

een , b , u SEM-afbeeldingen van respectievelijk Au-nanodeeltjes, Au@CdS met dunne schaal en CdS-tegenhangers. d TEM-afbeeldingen van Au@CdS met dikke schaal. c , e , v , g SEM-, TEM-, HR-TEM-beeld en EDS-profiel van Au@CdS-CdS nanoflowers. ik Foto's van hun oplossingskleuren
De XRD-patronen van de monsters verkregen in het syntheseproces van Au@CdS-CdS-nanaoflowers werden getoond in Fig. 3. XRD-pieken van Au-nanodeeltjes werden waargenomen en de pieken bij 2θ = 38,2, 44,2 en 64,75 waren te wijten aan de (111 ), (200) en (220) vlakken, respectievelijk van het fcc Au-kristal (JCPDS 04-0784). Voor CdS-kristallen waren de pieken bij 2θ = 25, 26,5, 28,2, 43,8, 47,8 en 51,9 te wijten aan (100), (002), (101), (110), (103) en (112) vlakken van het wurtziet CdS kristal (JCPDS 41-1049). Zowel fcc Au- als wurtziet-CdS-kristaldiffractiepieken werden waargenomen in de XRD-patronen van respectievelijk Au@CdS CSN's en Au@CdS-CdS nanoflowers. Opgemerkt moet worden dat de diffractiepiekintensiteit van het (002) kristalvlak veel hoger was dan andere pieken in Au@CdS-CdS-nanokristallen. Dit gaf aan dat de diffractiepiek van het (002) kristalvlak prominent aanwezig is en dat de CdS-nanostaafjes in de [001]-richting zijn gegroeid, wat in overeenstemming was met het HR-TEM-resultaat.
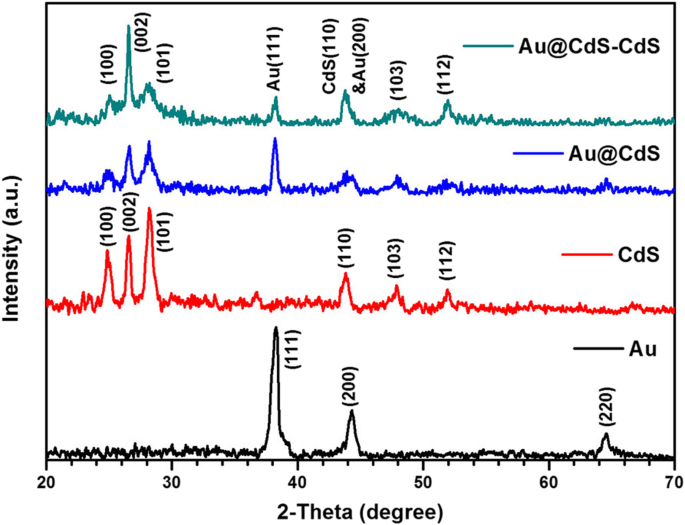
XRD-patronen van Au, CdS, Au@CdS CSN's en Au@CdS-CdS nanoflowers
Optische eigenschappen van het monster
De optische eigenschappen van de vijf monsters werden geanalyseerd door UV-Vis-metingen, zoals weergegeven in Fig. 4. De bandrandpositie van CdS-colloïden was minder dan 500 nm. De 50 nm Au-colloïden vertonen een oppervlakteplasmonresonantie (SPR) -absorptie gecentreerd op 530 nm. Het coaten van de Au-nanosferen met een dunne CdS-laag resulteerde in een roodverschuiving van de plasmonpiek naar 568 nm. Naarmate de dikte van de CdS-schaal toenam, verschoof de SPR-positie verder naar rood naar 623 nm en 635 nm in respectievelijk de Au@CdS-dikke en Au@CdS-CdS-nanobloemen. De experimentele resultaten toonden aan dat met de toename van de dikte van de CdS-schaal, de SPR-absorptiepiek van de Au-nanodeeltjes een continue roodverschuiving vertoonde, omdat de SPR-positie van het metaal afhing van de metaalgrootte, vorm en omringende media. Soortgelijke verschijnselen werden waargenomen in Au@SiO2 , Au@Cu2 O, en Au-Fe3 O4 hybride nanostructuursystemen [35,36,37]. De positie van de bandrand van Au@CdS-CdS nanoflowers reikte tot 850 nm, wat het zichtbare gebied van het zonlicht (400-760 nm) beter zou kunnen oogsten om de fotokatalytische activiteit te verbeteren.
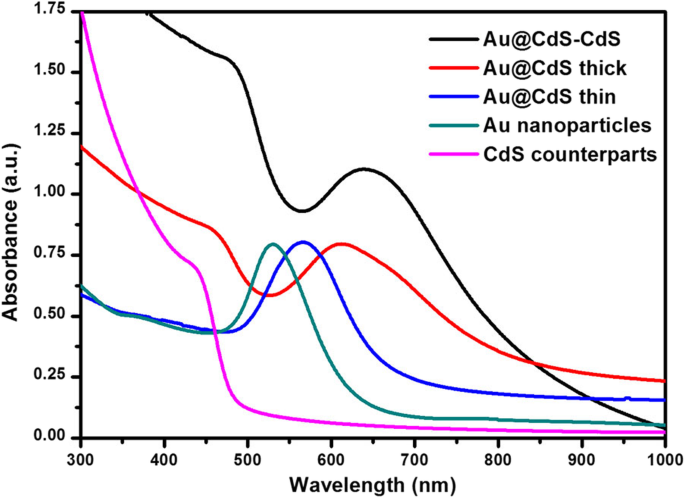
De UV-Vis-absorptiespectra van monsters:respectievelijk CdS-tegenhangers, Au-nanodeeltjes en Au@CdS CSN's en Au@CdS-CdS nanobloemen
Eigenschappen voor door licht veroorzaakte overdracht van kosten
De fotoluminescentie (PL) spectra van de gesynthetiseerde Au@CdS-CdS nanoflowers, Au@CdS CSN's, CdS-tegenhangers en Au-colloïden werden getoond in Fig. 5a. De gouden colloïden hadden een zwakke PL-piek bij ~ -600 nm. Het PL-spectrum van de CdS-tegenhangers vertoonde een dominante emissieband bij 530 nm en een kleinere schouderpiek bij 598 nm. De band bij 530 nm kan worden toegeschreven aan de typische excitonische band-bandemissie van CdS. De schouder bij 598 nm kan te wijten zijn aan ingesloten emissie die is ontstaan door structurele defecten in het CdS-kristal. De PL-spectrale intensiteit van de hybride structuur was echter significant verminderd en de stralingsemissie van de CdS in Au@CdS-CdS nanoflowers werd meer gedoofd dan die in Au@CdS CSN's. Omdat het Fermi-niveau van Au zich op +-0,5 V ten opzichte van de genormaliseerde waterstofelektrode (NHE) bevond, was het lager dan het geleidingsbandniveau van CdS (-1,0 V vs. NHE). Nadat CdS is geëxciteerd, zouden de vrije elektronen in de geleidingsband worden overgedragen naar de Au-kern vanwege het energieverschil [32, 38]. Het foto-geïnduceerde ladingsoverdrachtsmechanisme leidde tot een afname van de elektron-gat-recombinatiekans en onderdrukking van excitonemissie in CdS. De kans op recombinatie van fotogegenereerd elektron en gat was groter in de Au@CdS CSN's, waarschijnlijk vanwege het hoge gehalte aan CdS. Bloemachtige Au@CdS-CdS hybride nanostructuren bieden een ideaal onderzoeksplatform voor de studie van foto-geïnduceerde ladingsoverdrachtsmechanismen voor metaal-halfgeleider heterojunctie. De resultaten van de tijdelijke fotostroomrespons verkregen van Au@CdS-CdS nanoflowers, Au@CdS dik en CdS-tegenhangers werden getoond in Fig. 5b. Het was gemakkelijk waar te nemen dat de fotostroom over Au@CdS-CdS sterk verbeterd was in vergelijking met die van Au@CdS dik en CdS-tegenhangers. De verbeterde fotostroom over het Au@CdS-CdS-nanocomposiet impliceerde een efficiëntere scheiding van de foto-geïnduceerde elektron-gatparen en een langere levensduur van de fotogegenereerde ladingsdragers dan die van blanco-CdS, wat gunstig was voor de fotokatalytische activiteit.
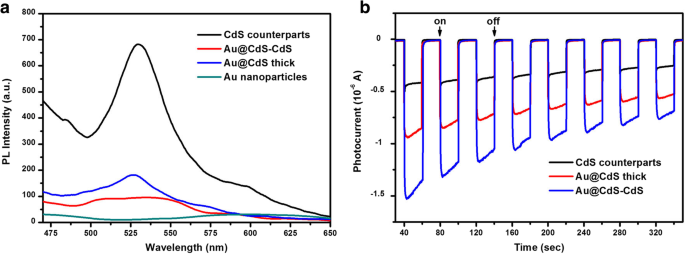
een De PL-spectra van respectievelijk Au-colloïden, Au@CdS dik, Au@CdS-CdS en CdS-tegenhangers. b Vergelijking van tijdelijke fotostroomrespons van de Au@CdS-CdS nanoflowers, Au@CdS dikke en CdS-tegenhangers bestraald met zichtbaar licht van λ ≥ 400 nm in 0,2 M Na2 SO4 waterige oplossing zonder bias versus Ag/AgCl
Toepassing van materialen
Au@CdS-CdS-nanobloemen hebben een verbeterd vermogen om zichtbaar licht op te vangen en foto-geïnduceerde ladingsscheidingseigenschappen, die bij bepaalde toepassingen potentiële waarde hebben. De fotokatalytische activiteit van Au@CdS-CdS onder 400-780 nm bestraling werd gedetecteerd met behulp van kleurstof Rhodamine 6G als fotodegradatiedoelwit. Ter vergelijking werden ook Au-nanodeeltjes, CdS-tegenhangers en Au@CdS dik onder dezelfde omstandigheden getest. Figuur 6a was de UV-Vis-absorptiespectra van de R6G-oplossingen onder verschillende bestralingstijden met behulp van Au@CdS-CdS-nanobloemen. De intensiteit van de absorptiepiek van de R6G-oplossing nam snel af met de verlichtingstijd, en de karakteristieke absorptiepiek verschoof ook van 528 nm naar 507 nm. Na 40 min was de concentratie van R6G bijna niet veranderd, wat suggereert dat de afbraakreactie voltooid was. Figuur 6b toonde de genormaliseerde verandering van de concentratie van R6G-oplossingen met Au-nanodeeltjes, CdS-tegenhangers en Au@CdS-dikke en Au@CdS-CdS-nanobloemen. Zonder katalysator zou de verandering in de concentratie van R6G verwaarloosbaar kunnen zijn. Van de katalysatoren was de fotodegradatiesnelheid van Au@CdS-CdS-nanobloemen aanzienlijk sneller dan die van andere materialen. Na 40 min was 86% van de R6G-oplossing afgebroken in het Au@CdS-CdS nanoflowers-systeem, terwijl slechts 71%, 46% en 12% van de R6G-oplossing was afgebroken in de Au@CdS dikke, CdS-tegenhangers, en Au nanodeeltjessysteem, respectievelijk.
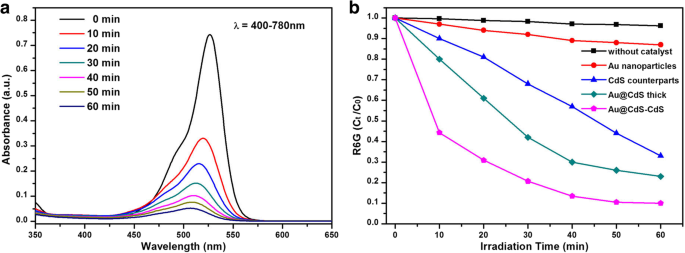
een Absorptiespectra van R6G-oplossingen bij verschillende bestralingstijden met behulp van Au@CdS-CdS nanoflowers als fotokatalysator onder bestraling van 400-780 nm. b C t /C 0 versus bestralingstijdgrafieken voor R6G-fotodegradatie in aanwezigheid van verschillende fotokatalysatoren
Zoals te zien is in figuur 6b, vertoonden hybride nanostructuren superieure fotokatalytische activiteit in vergelijking met overeenkomstige ééncomponentige. Het inbedden van plasmonische metalen nanokristallen in halfgeleider nanostructuren verbeterde de fotokatalytische prestaties van de laatste aanzienlijk door de LSPR van de eerste [39, 40]. Het geconcentreerde en verstrooide licht van gouden nanodeeltjes droeg bij aan het verhogen van de lichtabsorptie van CdS, wat leidde tot het genereren van meer excitonen. De heterojunctie tussen Au en CdS zou ladingsscheiding en -overdracht bevorderen. Bovendien was de fotokatalytische snelheid van Au@CdS-CdS-nanobloemen duidelijk hoger dan die van Au@CdS dik, hoewel ze dezelfde grootte en een vergelijkbaar spectraal absorptiebereik hadden. Dit kan te maken hebben met de speciale morfologie van Au@CdS-CdS-nanobloemen, die een groter specifiek oppervlak hadden, wat betekent dat het meer reactieplaatsen zou kunnen bieden. Bij dezelfde massa was het oppervlak van nanobloemen meer dan 4,67 keer dat van nanosferen. Gedetailleerde berekeningen zijn weergegeven in het aanvullende bestand 1. Daarom hebben Au@CdS-CdS-nanobloemen een uitstekende fotokatalytische activiteit bij alle monsters.
Er zijn verschillende primaire mechanismen zoals near-field-mechanisme, lichtverstrooiing en hete elektroneninjectie die kunnen worden beschreven voor plasmon-versterkte fotokatalytische reactie. Om het uitgebreide absorptiebereik van Au@CdS-CdS-nanobloemen te testen, ongeacht of de fotokatalytische activiteit werd verbeterd of niet, hebben we fotokatalytische tests uitgevoerd onder de verlichting van λ =-600-780 nm. Figuur 7a toonde de UV-Vis-absorptie van R6G afgebroken door Au@CdS-CdS nanoflowers onder de verlichting van λ = 600-780 nm. De fotokatalytische activiteit voor het afbreken van R6G door vier fotokatalysatoren werd getoond in figuur 7b. Na 60 minuten bestraling was de afbraak van Au-nanodeeltjes, CdS-tegenhangers, Au@CdS dik en Au@CdS-CdS nanobloemen respectievelijk 9,8%, 15%, 34% en 45%. De snelheid van fotodegradatie in hybride nanostructuren-systemen was sneller dan die van kristallen met één component. De fotokatalytische activiteit van de hybride nanostructuren werd verbeterd door het uitgebreide absorptiebereik omdat CdS niet werd geëxciteerd bij invallend licht boven 516 nm. Terwijl de SPR-absorptiepiek van Au-nanodeeltjes in Au@CdS-CdS-nanobloemen ongeveer 650 nm was. Onder de verlichting van 600-780 nm werden hete elektronen gegenereerd uit Au en zouden tijdens relaxatie worden overgebracht naar de geleidingsband van CdS [41, 42]. Om de duurzaamheid en herbruikbaarheid van deze fotokatalysatoren verder te evalueren, werd hetzelfde monster gecentrifugeerd en opnieuw gedispergeerd in 20 ml H2 O met 10 −5 M R6G voor meerdere fietstesten. Figuur 8a toonde aan dat de efficiëntie van fotodegradatie van R6G vrijwel onveranderd blijft tijdens de drie opeenvolgende testcycli, wat wijst op de hoge stabiliteit van Au@CdS-CdS-nanostructuren.
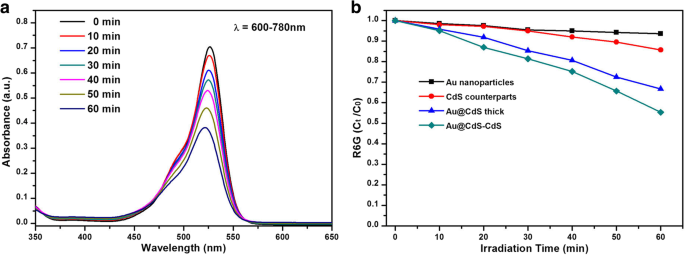
een Absorptiespectra van R6G-oplossingen bij verschillende bestralingstijden met behulp van Au@CdS-CdS nanoflowers als fotokatalysator onder bestraling van 600-780 nm. b C t /C 0 versus bestralingstijdgrafieken voor R6G-fotodegradatie in aanwezigheid van verschillende fotokatalysatoren
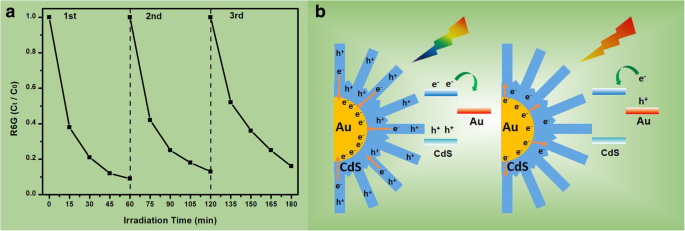
een De cyclus loopt voor de fotokatalytische afbraak van R6G-kleurstof over de Au@CdS-CdS-nanobloemen onder bestraling met zichtbaar licht (400-780 nm). b Twee ladingsscheidingsmechanismen voor Au@CdS-CdS nanoflowers onder respectievelijk 400-780 nm en 600-780 nm bestraling
Zowel plasmonische Au als halfgeleider CdS met smalle bandgap zijn gevoelig voor zichtbaar licht in Au-CdS-nanostructuur. Er wordt dus verwacht dat er twee verschillende foto-geïnduceerde ladingsscheidings- en overdrachtsmechanismen in Au@CdS-CdS-nanobloemen bestaan, afhankelijk van de invallende excitatie-energie, zoals weergegeven in figuur 8b. Voor een specifiek geval, als alleen de CdS wordt geëxciteerd, zullen de elektronen worden overgedragen van de geleidingsband van CdS naar de Au. Evenzo, als alleen Au wordt geëxciteerd, zullen de elektronen van de oppervlakteplasmontoestand van Au naar de geleidingsband van CdS springen. Maar de zaak wordt ingewikkelder wanneer zowel Au als CdS samen opgewonden zijn. De overdracht van elektronen op beide manieren is mogelijk, hoewel waarschijnlijker de overdracht van halfgeleider naar metaal is [43,44,45]. De verhoogde kans op ladingsscheiding zal de fotokatalytische activiteit van metaal-halfgeleider hybride nanostructuren verbeteren, omdat gescheiden elektronen en gaten een hoge kans hebben om deel te nemen aan katalytische reacties. Gewoonlijk kunnen de gaten de organische verontreinigingen of watermoleculen oxideren om · te vormen OH, en tegelijkertijd worden de door foto gegenereerde elektronen gemakkelijk opgevangen door de oxiderende stoffen of andere actieve stoffen om O2 te produceren ·- . De O2 ·- en · OH heeft een hoge oxidatie-efficiëntie en uitstekende chemische activiteiten, die de overgrote meerderheid van organische kleurstoffen kunnen oxideren. De synthese van hiërarchische Au@CdS-CdS-nanobloemen zal een nieuw perspectief bieden voor rationeel ontwerp en gecontroleerde synthese van hybride nanostructuren met hoge fotokatalytische eigenschappen.
Conclusie
Hiërarchische Au@CdS-CdS-nanobloemen werden met succes stapsgewijs bereid. In de verkregen nanohybriden werden CdS-nanostaafjes epitaxiaal gekweekt op het oppervlak van Au@CdS CSN's. De Au@CdS-CdS nanoflowers vertoonden uitstekende fotokatalytische activiteit tegen de afbraak van R6G onder de bestraling van respectievelijk λ = 400-780 nm en λ = 600-780 nm. Hiërarchische Au@CdS-CdS nanoflowers hadden drie voordelen:ten eerste verbeterde heterostructuur de scheiding en overdracht van fotogegenereerde elektron-gatparen; ten tweede zorgt de hiërarchische structuur voor meer reactieplaatsen; en ten derde verbeterde het uitgebreide absorptiebereik het vermogen om licht op te vangen. Verder hebben we een mogelijk mechanisme voorgesteld voor de stapsgewijze synthese van Au@CdS-CdS-nanobloemen, dat kan worden gebruikt om andere metaal-halfgeleider-nanohybriden met complexe morfologie voor te bereiden voor toekomstige velden voor schone energie en milieuherstel.
Afkortingen
- CSN's:
-
Kern-schaal nanodeeltjes
- Cys:
-
l-cysteïne
- Cys/Cd 2+ :
-
l-cysteïne-Cd 2+
- EDS:
-
Energiedispersieve spectrometer
- Nl:
-
Ethyleendiamine
- FE-SEM:
-
Veldemissie scanning elektronenmicroscoop
- HR-TEM:
-
Transmissie-elektronenmicroscoop met hoge resolutie
- NP's:
-
Nanodeeltjes
- PL:
-
Fotoluminescentie
- TEM:
-
Transmissie-elektronenmicroscoop
- UV-Vis:
-
Ultraviolet zichtbaar
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Eenvoudige synthese en optische eigenschappen van kleine selenium nanokristallen en nanostaafjes
- Nanogestructureerde Silica/Gold-Cellulose-Bonded Amino-POSS Hybrid Composite via Sol-Gel Process en zijn eigenschappen
- Hydrothermische synthese van In2O3 nanodeeltjes hybride tweeling hexagonale schijf ZnO heterostructuren voor verbeterde fotokatalytische activiteiten en stabiliteit
- Synthese van in water oplosbare antimoonsulfide Quantum Dots en hun foto-elektrische eigenschappen
- Gemakkelijke synthese van wormgatachtig mesoporeus tinoxide via verdamping-geïnduceerde zelfassemblage en de verbeterde gasdetectie-eigenschappen
- Effect van de synthesemethode van La1 − xSr x MnO3 manganite nanodeeltjes op hun eigenschappen
- One-Pot-synthese van Cu2ZnSnSe4-nanoplaten en hun door zichtbaar licht aangedreven fotokatalytische activiteit
- Eenstaps sonochemische synthese en fotokatalytische eigenschappen van grafeen/Ag3PO4 Quantum Dots Composites in één stap
- Afhankelijkheid van de toxiciteit van nanodeeltjes van hun fysische en chemische eigenschappen
- Eigenschappen van zinkoxide-nanodeeltjes en hun activiteit tegen microben
- Soorten metalen en hun eigenschappen



