De invloed van materialen, heterostructuur en oriëntatie voor nanohybriden op fotokatalytische activiteit
Abstract
In dit werk worden verschillende structuren op basis van elektrolytisch afgezette n-type ZnO-nanostaafjes en p-type Cu2 O-, CuSCN- en NiO-nanostructuren zijn gefabriceerd voor de afbraak van methyloranje (MO). De invloed van materialen, heterostructuur en oriëntatie van nanohybriden op fotokatalytische activiteit wordt voor het eerst besproken. De heterojunctiestructuren vertonen een opmerkelijke verbetering in vergelijking met de kale halfgeleider. De morfologie van nanostructuur heeft vooral een invloed op de fotokatalytische activiteit. NiO heeft de hoogste katalytische activiteit van de vier ongerepte halfgeleider nanostructuren van ZnO, Cu2 O, CuSCN en NiO. De grootste verbetering van de fotokatalytische activiteit wordt verkregen met behulp van een ZnO/NiO (1 min) heterostructuur toegeschreven aan de heterojunctiestructuur en een extreem hoger specifiek oppervlak, dat MO (20 mg/L) binnen 20 min kan degraderen tot kleurloos met de snelste fotokatalytische snelheid tussen homogene heterojunctiestructuren. Ondertussen zullen de hierin beschreven methodologie en gegevensanalyse dienen als een effectieve benadering voor het ontwerp van hybride nanostructuren voor toepassing van zonne-energie, en de geschikte nanohybriden zullen een aanzienlijk potentieel hebben om de milieu- en energieproblemen op te lossen.
Achtergrond
Hybride nanomaterialen met uitstekende optische, elektronische en magnetische eigenschappen hebben de afgelopen jaren veel belangstelling getrokken vanwege hun wijdverbreide toepassingen in milieusanering [1, 2] en conversie van zonne-energie [3, 4]. In de afgelopen jaren zijn er verschillende soorten nanohybriden ontwikkeld, bijvoorbeeld grafeenoxide-nanocomposieten [5], TiO2 /BiVO4 nanocomposieten [6], 3D-geprinte hydrogel nanocomposieten [7] en Ru/Li2 O nanocomposieten [8]. Onder de verschillende soorten nanomaterialen hebben heterojuncties op basis van verschillende nano-halfgeleiders zich ontwikkeld tot een belangrijk onderzoeksgebied vanwege hun aantrekkelijke fotokatalytische [9,10,11] en de fotovoltaïsche [12,13,14] eigenschappen. Onlangs zijn er verschillende onderzoeken gedaan naar verschillende katalytische toepassingen van kleurstofafbraak, zoals nanohybride membraanorganokatalysator [15], bio-anorganische nanohybride katalysator [16] en groene nanohybride katalysator [17]. Vanwege de toxiciteit vormen de organische kleurstoffen in het afvalwater een ernstige bedreiging voor de menselijke gezondheid [18, 19]. De omzetting van organische kleurstoffen in onschadelijke stoffen is dus essentieel voor het menselijk leven en duurzame ontwikkeling. Een verscheidenheid aan anorganische halfgeleidermaterialen met verschillende morfologieën zijn onderzocht als fotokatalysatoren voor afvalwaterzuivering onder UV- of zichtbaar lichtbestraling [20,21,22], met name zinkoxide (ZnO) en titaniumdioxide (TiO2 ) eendimensionale (1D) nanomaterialen. Tot nu toe hebben ZnO-nanomaterialen het meest uitgebreide onderzoek onder verschillende halfgeleiders verkregen, wat kan worden toegeschreven aan hun efficiënte elektronenoverdrachtsprestaties [23], door fotogegenereerde gaten te bieden voor sterke oxidatie, betere milieuvriendelijke eigenschappen, niet-toxiciteit, lage kosten en goede stabiliteit en wijdverbreid op aarde [24, 25]. De fotokatalytische activiteit van ZnO wordt echter ernstig beperkt door zijn interne defecten:een smallere respons van het UV-zichtbare gebied vanwege de grote bandgap en de hoge kans op recombinatie van door foto gegenereerde elektron-gatparen [26, 27]. Om deze beperkingen te overwinnen zijn er tal van maatregelen genomen, zoals doping [28], samengestelde edelmetalen, zoals Au [29, 30] en Ag [31]; en combineren met andere halfgeleiders, zoals CdS [32], ZnSe [33], CdSe [34, 35] en PbS [36, 37]. Het is bewezen dat het verkrijgen van heterojuncties op basis van ZnO en andere halfgeleiders een haalbare manier is om de respons op zichtbaar licht en de efficiëntie van de afbraak van afvalwater te verbeteren. Onlangs zijn verschillende heterojuncties ontwikkeld op basis van ZnO-nanomateriaal en p-type nano-halfgeleider op degradatie. Onlangs heeft de Cu2 O-ZnO heterostructuren op fotokatalyse werden gerapporteerd door Wang et al. [38] en Yu et al. [39]. Luo en collega's rapporteerden de ZnO/CNF/NiO-heteroarchitectuur voor hoogwaardige fotokatalyse [40]. Liu et al. gerapporteerde elektrospun nanovezel NiO / ZnO heterojuncties met verbeterde fotokatalytische activiteit [41]. ZnO/CdS-structuur heeft ook een hogere fotokatalytische activiteit dan ongerepte materialen [42]. Deze rapporten geven aan dat de heterostructuren een hogere fotokatalytische activiteit van kleurstofontleding bezaten dan ongerepte halfgeleiders. De efficiëntie van fotokatalytische afbraak van methyloranje (MO) moet echter verder worden verbeterd. Ook moet het ontwerp van de heterojunctiestructuur nader worden onderzocht, bijvoorbeeld om de kosten te verlagen door edelmetaal te verwijderen en een eenvoudige methode te gebruiken, zoals elektrodepositie en lagere reactietemperatuur. In deze studie, ZnO, Cu2 O-, CuSCN- en NiO-nanostructuren worden bereid door een goedkope, eenvoudige elektrodepositiemethode bij kamertemperatuur. Heterojunctiestructuren van verschillende materialen en verschillende oriëntaties worden gefabriceerd op basis van n-type ZnO-nanostaafjes en p-type Cu2 O, CuSCN en NiO nanostructuren. De heterostructuren vertonen veel betere fotokatalytische prestaties voor fotokatalytische afbraak van MO dan ongerept n-type materiaal of p-type materiaal. De invloed op de oriëntatie van de heterojunctie is afhankelijk van de kristalkwaliteit van het bovenmateriaal van de heterojunctie. De invloed op het materiaal van verschillende reactieomstandigheden is afhankelijk van de morfologie en kwaliteit van de nanostructuren. Van de drie p-type materialen die in ons werk worden gebruikt, heeft NiO de meest uitstekende fotokatalytische prestaties. De ZnO/NiO (1 min) kan de MO (20 mg/L) waterige oplossing binnen 20 min ontleden van oranje tot kleurloos. Het laat zien dat het materiaal en de oriëntatie beide een effect kunnen hebben op de fotokatalytische prestatie, wat van groot belang is voor de afbraak van organische verontreinigende stoffen; bovendien is deze studie de eerste grondige studie van de invloed van materialen, oriëntatie en heterostructuur op fotokatalytische activiteit en kan het verder onderzoek naar meer nanohybriden bevorderen om een hogere fotokatalytische efficiëntie te verkrijgen.
Methoden
Experimentele materialen
Met indiumtinoxide (ITO) gecoat glas (CSG Holding Co., Ltd., 15 Ω/sq), zinknitraat (Zn(NO3) )·6H2 O), hexamethyleentetramine (HMT), koper (II) sulfaatpentahydraat, natriumhydroxide, melkzuur, kaliumthiocyanaat, ethyleendiaminetetra-azijnzuur, triethanolamine en nikkelnitraathexahydraat worden allemaal gekocht bij Sinopharm Chemical Reagent Co., Ltd. Al deze materialen zijn van analytische kwaliteit en gebruikt zoals ontvangen zonder verdere zuivering.
Voorbereiding van nanostructuren
De kosteneffectieve elektrodepositiemethode wordt in dit werk gebruikt voor de voorbereiding van het grote gebied van nanostructuren vanwege de verwerking bij lage temperatuur, willekeurige substraatvormen en nauwkeurige controle van de grootte van nanostructuren [43]. Alle afzettingen worden uitgevoerd in een geconfigureerde glazen cel waarin een ITO-substraat, een platinaplaat en een Ag/AgCl-elektrode in verzadigde KCl of verzadigde calomelelektrode (SCE) dienen als de werkelektrode, de tegenelektrode en de referentie-elektrode , respectievelijk. De gedetailleerde reactieomstandigheden voor de fabricage van alle nanostructuren door elektrodepositie worden weergegeven in tabel 1. De pH-waarde van Cu2 O reactie-oplossing wordt geregeld van 10 tot 12 door NaOH. De pH-waarde van CuSCN-reactieoplossing ligt rond de 1,5. Ten slotte worden alle hierboven afgezette monsters gespoeld met gedeïoniseerd water om de elektrolyt te verwijderen en op natuurlijke wijze aan de lucht gedroogd. Er wordt geen gloeiing na depositie toegepast.
Karakteriseringen
Röntgendiffractiepatronen (XRD) worden gemeten met een Rigaku D/Max-2500-diffractometer met behulp van Cu Kα-straling (λ = 1.54 Å) bij kamertemperatuur. De scansnelheid is 10°/min. De spanning en stroom zijn 40 kV en 40 mA. Oppervlakte- en dwarsdoorsnedestructuur van de monsters worden gekenmerkt door scanning elektronenmicroscopie (SEM) met behulp van een Philips-FEI XL 30-SFEG bij kamertemperatuur zonder enige oppervlaktecoating. De versnellingsspanning is 10–20 kV. De optische eigenschappen van de monsters worden onderzocht met UV-vis diffuse reflectiespectrometrie (UV-vis DRS) met een Shimadzu UV-3101PC UV-vis spectrofotometer bij kamertemperatuur.
Fotokatalytische ontledingsexperimenten
Fotokatalytische activiteiten van bereide monsters worden beoordeeld op de afbraak van MO in waterige oplossing. Een Xe-lamp van 500 W is een lichtbron van fotokatalytische reactieapparaten. Bij een fotodegradatieproces wordt het monster in een kwartsreactor geplaatst die is gevuld met 3 mL MO (20 mg/L) waterige oplossing. Vóór de bestraling wordt de waterige oplossing 60 min in het donker gehouden om het adsorptie-evenwicht van MO te bereiken. Na een specifieke bestralingstijd worden de fotokatalytische ontledingsprestaties geanalyseerd door de absorptie van MO-oplossing bij zijn karakteristieke golflengte (465 nm) te meten met een UV-vis-spectrofotometer. Alle monsters worden uitgevoerd in onafhankelijke experimenten en bij kamertemperatuur uitgevoerd.
Resultaten en discussie
Voorbereiding van nanostructuren en samenstellingsanalyse
Alle ZnO, Cu2 O-, CuSCN- en NiO-nanostructuren worden gesynthetiseerd door de kosteneffectieve elektrodepositiemethode bij kamertemperatuur. De elektrodepositie wordt uitgevoerd in een standaard elektrochemische cel met drie elektroden in de potentiostatische modus. De kristalstructuren van ZnO, Cu2 O-, CuSCN- en NiO-nanostructuren worden gekarakteriseerd via XRD-profielen. De XRD-beelden van ZnO, Cu2 O-, CuSCN- en NiO-nanostructuren bereid door de elektrodepositiemethode worden getoond in Fig. 1. Een reeks pieken in Fig. 1a verschijnt bij 2θ van ca. 34,36 °, 36,12 ° en 47,48 ° voor de ZnO-nanostaafjes, die respectievelijk zijn toegewezen aan de (002), (101) en (102) van ZnO-kristallen. Alle pieken in de ZnO-nanostaafjes kunnen worden geïndexeerd met de hexagonale wurtzietstructuur van ZnO, en er zijn geen andere detecteerbare fasen in de ZnO-nanostructuren, die vergelijkbaar zijn met XRD-profielen in Ref. [39]. Bovendien geeft de sterke ZnO (002)-piek aan dat georiënteerde nanostaafjes met een hoge kristalliniteit worden verkregen. Drie pieken in Fig. 1b bij 2θ van ca. 29,78°, 36,81° en 42,89° worden waargenomen voor de elektrolytisch afgezette Cu2 O film op ITO-substraat, die zijn toegewezen aan de (110), (111) en (200) van Cu2 O-kristallen, wat aangeeft dat Cu2 O heeft de pure cupri-kubusstructuur met een (111) voorkeursoriëntatie, die hetzelfde is als XRD-profielen in Ref. [38]. De diffractie van pieken in Fig. 1c verschijnt bij 2θ van ca.16.21°, 27.20° en 32.69° en kan respectievelijk worden toegewezen aan de (003), (101) en (006) vlakken van CuSCN-kristallen, die kunnen worden geïndexeerd aan een rhomboëdrische structuur β -CuSCN [44]. De XRD-patronen in figuur 1d zijn toegewezen aan de drie belangrijkste NiO-pieken op 37,52 °, 43,26 ° en 62,86 °, die respectievelijk verwijzen naar de vlakken (111), (200) en (220), die vergelijkbaar zijn met XRD profielen in ref. [39]. Alle XRD-patronen laten zien dat geen van de andere fasen wordt gedetecteerd en dat de nanostructuren vrij zijn van onzuiverheden. Figuur 1e toont de absorptiespectra van ZnO, Cu2 O-, CuSCN- en NiO-nanostructuren bereid door de elektrodepositiemethode. Zoals weergegeven in figuur 1e, kunnen ZnO-nanostaafjes alleen het hoogenergetische licht absorberen met een golflengte korter dan 370 nm. Een absorptiebandrand bij 600 nm kan worden waargenomen voor Cu2 O, zoals weergegeven in Fig. 1e, wat consistent is met de bandafstand van Cu2 O (2,1 eV). Zoals weergegeven in figuur 1e, heeft CuSCN een lage en brede absorptie met een golflengte langer dan 350 nm en heeft NiO een absorptie tussen 350 en 500 nm, maar een lage absorptie met een golflengte langer dan 500 nm. Alle absorptie van ZnO, Cu2 O-, CuSCN- en NiO-nanostructuren bevinden zich in het ultraviolette en zichtbare bereik, en dit garandeert de absorptie van het ultraviolette licht onder Xe-lampbestraling in de fotokatalytische ontledingsexperimenten en de daaruit voortvloeiende vorming van elektron-gatparen.
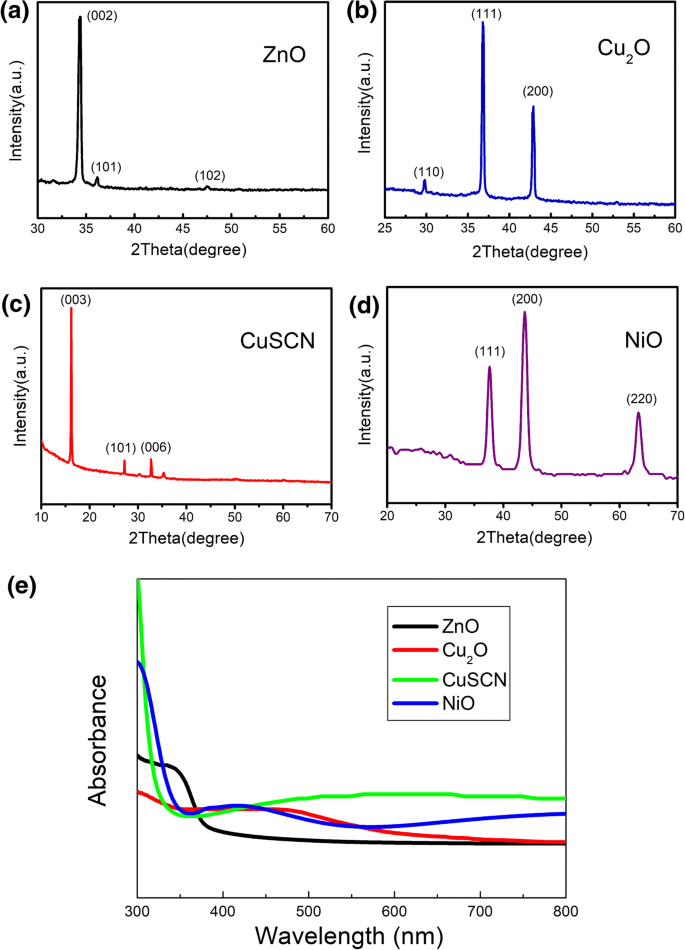
Röntgenfoto-elektronenspectra van ZnO (a ), Cu2 O (pH 10, 20 min) (b ), CuSCN (3D) (c ), en NiO (1 min) (d ) nanostructuren bereid door elektrodepositiemethode en de absorptiespectra (e ) van ZnO, Cu2 O (pH 10, 20 min), CuSCN(3D) en NiO(1 min) nanostructuren bereid door elektrodepositiemethode
Ontwerp en morfologie van de heterostructuren
Verschillende heterojuncties op basis van n-type ZnO-nanostaafjes en p-type Cu2 O-, CuSCN- en NiO-nanostructuren met verschillende oriëntatie worden gefabriceerd. Ten eerste, de ZnO, Cu2 O, ZnO/Cu2 O, en Cu2 O/ZnO worden voorbereid voor fotokatalytische afbraak van MO. Afbeelding 2 toont het bovenaanzicht SEM-beeld van ZnO-nanostaafjes (a), ZnO/Cu2 O (pH 12, 20 min) heterojunctie (b), Cu2 O (pH 12, 20 min) (c), en Cu2 O (pH 12, 20 min)/ZnO heterojunctie (d). Aanvullend bestand 1:Afbeelding S1 toont de dwarsdoorsnede van deze vier structuren. Afbeelding 3 toont het bovenaanzicht SEM-beeld van ZnO/Cu2 O (pH 10, 20 min) heterojunctie (a), ZnO/Cu2 O (pH 10, 40 min) heterojunctie (b), Cu2 O (pH 10, 20 min)/ZnO heterojunctie (c), Cu2 O (pH 10, 40 min)/ZnO heterojunctie (d), Cu2 O (pH 10, 20 min) (e), en Cu2 O (pH 10, 40 min) (f). Aanvullend bestand 1:Afbeelding S2 toont de dwarsdoorsnede van deze zes structuren. Zoals te zien is in het bovenaanzicht in figuur 2a en de dwarsdoorsnede in aanvullend bestand 1:figuur S1 (a), hebben de ZnO-nanostaafjes verkregen door de elektrodepositiemethode bijna de structuur van een hexagonaal prisma. De diameter en de lengte van de nanostaafjes liggen in het bereik van respectievelijk 200-300 nm en 800-1200 nm. Zoals getoond in Fig. 2c en 3e en f, kan worden opgemerkt dat de Cu2 O-kristallen groeien van kubussen tot octaëders wanneer de pH-waarde van de elektrodepositie-oplossing verandert van 10 tot 12. De kristallen verkregen bij pH ~-10 met een reactietijd van 20 en 40 min zijn niet allemaal de perfecte kubussen vanwege de verschillende oplossing van de kristal in de reactieoplossing [45]. Het is ook duidelijk te zien dat de Cu2 O-kristallen worden groter en dichter naarmate de tijd langer duurt, en de Cu2 O-kristallen zullen samenklonteren en samenklonteren als de reactietijd langer is. In het aggregatieproces, de Cu2 O-kristallen raken uit vorm vanwege de grote dichtheid. Zoals getoond in Fig. 2b en 3a en b, kan worden geconcludeerd dat Cu2 O-kristallen die op de ZnO-nanostaafjes zijn gegroeid, zijn net zo compact als de Cu2 O-kristallen gegroeid op het kale ITO-glassubstraat en zijn sommige kleiner dan de Cu2 O-kristallen gekweekt op ITO-glas vanwege het verschillende kiemvormingspunt. Wanneer de pH-waarde van de reactieoplossing 10 is, groeien de ZnO-nanostaafjes op de Cu2 O-kristallen zijn compacter dan de ZnO-nanostaafjes die op ITO-glas zijn gekweekt, en de diameter en de lengte van de ZnO-nanostaafjes die op de Cu2 O-kristallen zijn bijna hetzelfde met de ZnO-nanostaafjes die op ITO-glas zijn gegroeid, zoals weergegeven in Fig. 3c en d. De ZnO-nanostaafjes gekweekt op de Cu2 O-kristallen (pH 10, 40 min) zijn iets dichter dan de ZnO-nanostaafjes die op de Cu2 O-kristallen (pH 10, 20 min) en veel grotere ZnO-staafjes verschijnen op de laag van de ZnO-nanostaafjes. Zoals getoond in Fig. 2d, zijn de ZnO-nanostaafjes gegroeid op de Cu2 O-kristallen (pH 12, 20 min) zijn veel schaarser dan de ZnO-nanostaafjes die op het ITO-glas zijn gegroeid. De diameter en de lengte van de ZnO-nanostaafjes gekweekt op de Cu2 O-kristallen (pH 12, 20 min) zijn niet homogeen in een groot bereik.

Het bovenaanzicht SEM-beeld van ZnO-nanostaafjes (a ), ZnO/Cu2 O (pH 12, 20 min) heterojunctie (b ), Cu2 O (pH 12, 20 min) (c ), en Cu2 O (pH 12, 20 min)/ZnO heterojunctie (d )

Het bovenaanzicht SEM-beeld van ZnO/Cu2 O (pH 10, 20 min) heterojunctie (a ), ZnO/Cu2 O (pH 10, 40 min) heterojunctie (b ), Cu2 O (pH 10, 20 min)/ZnO heterojunctie (c ), Cu2 O (pH 10, 40 min)/ZnO heterojunctie (d ), Cu2 O (pH 10, 20 min) (e ), en Cu2 O (pH 10, 40 min) (f )
Ten tweede worden ZnO, CuSCN, ZnO/CuSCN en CuSCN/ZnO voorbereid voor fotokatalytische afbraak van MO. Twee verschillende CuSCN-nanostructuren, hexagonale prisma-achtige (3D) en nanodraad (NW) structuren, worden bereid door de elektrodepositiemethode. Figuur 4 toont het bovenaanzicht SEM-beeld van ZnO/CuSCN (3D) heterojunctie (a), ZnO/CuSCN (NWs) heterojunctie (b), CuSCN (3D)/ZnO heterojunctie (c), CuSCN (NWs)/ZnO heterojunctie ( d), CuSCN (3D) (e) en CuSCN (NW's) (f). Aanvullend bestand 1:Afbeelding S3 toont de dwarsdoorsnede van deze zes structuren. De CuSCN (3D) en CuSCN (NWs) structuren die elektrolytisch zijn afgezet op ZnO-nanostaafjes zijn dichter dan die op ITO-glas, zoals weergegeven in Fig. 4a en b. De ZnO-nanostaafjes onder CuSCN (3D)-structuren zijn gedeeltelijk geëtst door de CuSCN-reactieoplossing met een erosieve pH van 1,5, zoals weergegeven in figuur 4a en aanvullend bestand 1:figuur S3(a). De ZnO-nanostaafjes onder CuSCN (NW's) -structuren worden voornamelijk geëtst door de CuSCN-reactieoplossing met een pH van 1,5, maar de omtrek van ZnO-nanostaafjes blijft behouden na de elektrodepositie van CuSCN (NW's) -structuren, zoals weergegeven in Fig. 4b en aanvullend bestand 1:Figuur S3(b). De CuSCN (3D) op de ZnO-nanostaafjes is veel intensiever dan de CuSCN (NWs)-structuren op de ZnO-nanostaafjes, en de ZnO-nanostaafjes onder CuSCN (NWs)-structuren verdwijnen bijna en blijven alleen het overblijfsel van het ZnO-zeskantprisma. De ZnO-nanostaafjes die op de laag CuSCN zijn geprepareerd, zijn compacter dan de ZnO-nanostaafjes die op ITO-glas zijn gekweekt, en de diameter en de lengte van de ZnO-nanostaafjes die op CuSCN zijn gekweekt, zijn kleiner dan de ZnO-nanostaafjes die op ITO-glas zijn gekweekt vanwege het verschillende kiemvormingspunt , zoals weergegeven in Fig. 4c en d. De CuSCN- (3D) en CuSCN (NW's)-structuren die zijn vervaardigd door de elektrodepositiemethode op ITO-glas, zijn georiënteerd met een hoge dichtheid en bijna verticaal op het substraat met een diameter van respectievelijk ongeveer 100 nm en 80 nm, zoals weergegeven in Fig. 4e en v.

Het bovenaanzicht SEM-beeld van ZnO/CuSCN (3D) heterojunctie (a ), ZnO/CuSCN (NWs) heterojunctie (b ), CuSCN (3D)/ZnO heterojunctie (c ), CuSCN (NWs)/ZnO heterojunctie (d ), CuSCN (3D) (e ), en CuSCN (NWs) (f )
Ten slotte worden de ZnO, NiO, ZnO/NiO en NiO/ZnO voorbereid voor fotokatalytische afbraak van MO. Figuur 5 toont het bovenaanzicht SEM-beeld van ZnO/NiO (1 min) heterojunctie (a), ZnO/NiO (10 min) heterojunctie (b), NiO (1 min)/ZnO heterojunctie (c), NiO (10 min) /ZnO heterojunctie (d), NiO (1 min) (e) en NiO (10 min) (f). Aanvullend bestand 1:Afbeelding S4 toont de dwarsdoorsnede van deze zes structuren. De NiO-nanostructuur die gedurende 1 min elektrolytisch op ZnO-nanostaafjes is afgezet, is een maaswerk dat is doorsneden met ZnO-nanostaafjes, zoals weergegeven in figuur 5a en aanvullend bestand 1:figuur S4(a). De ZnO-nanostaafjes die elektrolytisch op de NiO-nanostructuur (1 min) zijn afgezet, worden gedeeltelijk blootgesteld aan het groeien door het netwerk van NiO (1 min), en het resterende deel van de ZnO-nanostaafjes blijft in het netwerk dat niet te zien is in de SEM-afbeeldingen van het bovenaanzicht, zoals weergegeven in figuur 5c en aanvullend bestand 1:figuur S4(c). De NiO-nanostructuur die gedurende 1 min op ITO-glas is aangebracht, is het meerlagige verweven netwerk dat gelijkmatig is verdeeld over het ITO-glas met een hoog specifiek oppervlak, zoals weergegeven in figuur 5e en aanvullend bestand 1:figuur S4 (e). De NiO-nanostructuur die gedurende 10 min elektrolytisch op ZnO-nanostaafjes is afgezet, bestaat uit veel deeltjes, zoals weergegeven in figuur 5b en aanvullend bestand 1:figuur S4 (b). De NiO-nanostructuur die gedurende 10 min elektrolytisch op ITO-glas is afgezet, bestaat uit veel NiO-deeltjes die een compacte laag op het ITO-glas en een deeltjeslaag op de compacte laag kunnen vormen, zoals weergegeven in figuur 5f en aanvullend bestand 1:figuur S4 (f ). Uit de dwarsdoorsnede van SEM in aanvullend bestand 1:figuur S4(f) kunnen enkele scheuren worden gevonden in de compacte laag op het ITO-glas als gevolg van de extrusiekracht die wordt gegenereerd door NiO-deeltjes. Wanneer ZnO elektrolytisch wordt afgezet op NiO (10 min), groeien de kleinere ZnO-nanostaafjes (vergeleken met die op het ITO-glas) op de NiO-deeltjeslaag, en de vorm van de NiO-deeltjes verdwijnt alleen de morfologie van de ZnO-nanostaafjes, zoals weergegeven in figuur 5d en aanvullend bestand 1:figuur S4(d). De scheuren in de compacte NiO-laag op het ITO-glas zijn ook te zien in aanvullend bestand 1:figuur S4(d), en sommige scheuren in de structuur van ZnO-nanostaafjes worden veroorzaakt door de scheuren in de compacte laag.

Het bovenaanzicht SEM-beeld van ZnO/NiO (1 min) heterojunctie (a ), ZnO/NiO (10 min) heterojunctie (b ), NiO (1 min)/ZnO heterojunctie (c ), NiO (10 min)/ZnO heterojunctie (d ), NiO (1 min) (e ), en NiO (10 min) (f )
Fotokatalytische activiteit
De fotokatalytische eigenschappen worden onderzocht via de afbraak van MO, een veel voorkomende organische verontreinigende stof [46, 47]. Drie systemen van ZnO/Cu2 O, ZnO/CuSCN en ZnO/NiO worden besproken, inclusief ongerept ZnO, ongerept Cu2 O (of CuSCN of NiO), ZnO/Cu2 O (of CuSCN of NiO), en Cu2 O (of CuSCN of NiO) met vier structuren in elk systeem. Hoewel de elektrodepositiemethode die in dit werk voor de voorbereiding van de nanostructuren wordt gebruikt, groen en milieuvriendelijk is, kan de voorbereidingsmethode een aanzienlijke hoeveelheid ongewenste chemicaliën vereisen, wat de groenheid van de methoden ondermijnt. Het probleem, zoals de duurzame membraanterugwinning van chemicaliën, kan worden opgelost door een continu hybride proces dat bestaat uit een stroomreactor en een daaropvolgende nanofiltratie-eenheid voor in situ recycling van oplosmiddelen en reagens, ontwikkeld door Szekely et al. [48]. Aanvullend bestand 1:figuur S5 en figuur S6 tonen de concentratieveranderingen van MO in afwezigheid en in aanwezigheid van verschillende fotokatalysatoren. Het is duidelijk dat het MO-gehalte weinig verandert in afwezigheid van de katalysator in vergelijking met de toevoeging van de katalysator. Bij bestraling met zichtbaar licht wordt slechts 15% van de MO ontleed na 40 min in afwezigheid van de katalysator, zoals weergegeven in aanvullend bestand 1:figuur S5(a). Ongerepte ZnO-nanostaafjes vertonen een zekere mate van fotokatalytische activiteit voor de afbraak van MO. Vanwege de beperkingen van interne defecten (grote bandafstand en gemakkelijke recombinatie van elektron-gat-paren) en specifiek oppervlak, zijn de fotokatalytische prestaties echter nog steeds slecht, zoals weergegeven in aanvullend bestand 1:Afbeelding S6(a), Afbeelding S6( b) en figuur S6 (c). De vergelijking van het specifieke oppervlak van de nanostructuren wordt vermoed uit de grootte en dichtheid van het oppervlak door SEM-afbeelding [49,50,51]. De concentratieveranderingen van MO met ZnO, Cu2 O (pH 10, 20 min), Cu2 O (pH 10, 40 min), Cu2 O (pH 12, 20 min), ZnO/Cu2 O (pH 10, 20 min), ZnO/Cu2 O (pH 10, 40 min), ZnO/Cu2 O (pH 12, 20 min), Cu2 O (pH 10, 20 min)/ZnO, Cu2 O(pH 10, 40 min)/ZnO, en Cu2 O (pH 12, 20 min)/ZnO zoals de katalysatoren worden getoond in aanvullend bestand 1:Figuur S6(a). De intensiteit van de absorptiepiek wordt geleidelijk verminderd en blauw verschoven naarmate de bestralingstijd toenam van 0 tot 40 min. De blauwe verschuiving kan worden toegeschreven aan dealkylering [52]. De fotokatalytische prestaties van drie verschillende Cu2 O, Cu2 O (pH 10, 20 min), Cu2 O (pH 10, 40 min) en Cu2 O (pH 12, 20 min), is vergelijkbaar vanwege de vergelijkbare morfologie en het specifieke oppervlak, zoals weergegeven in Fig. 2c en 3a en b. De fotokatalytische prestaties van ongerepte Cu2 O is armer dan die van ongerepte ZnO-nanostaafjes vanwege een grotere kristalgrens, lagere dragermobiliteit, kleiner specifiek oppervlak en gemakkelijkere recombinatie van elektronen en gaten. De fotokatalytische prestaties van ZnO/Cu2 O (pH 10, 20 min), ZnO/Cu2 O (pH 10, 40 min) en ZnO/Cu2 O (pH 12, 20 min) is bijna hetzelfde vanwege de vergelijkbare morfologie en het specifieke oppervlak van de bovenste laag Cu2 O, zoals getoond in Fig. 2b en 3e en f. De fotokatalytische prestatie van drie heterojuncties van ZnO/Cu2 O is lager dan die van ongerepte ZnO-nanostaafjes vanwege het kleinere specifieke oppervlak van de bovenste laag Cu2 O als een directe verbinding met de MO-oplossing, maar is hoger dan die van ongerepte Cu2 O vanwege het effect van heterojunctie van ZnO en Cu2 O. De fotokatalytische prestatie van Cu2 O/ZnO-architectuur is de hoogste in de ZnO/Cu2 O-systeem vanwege hun heterojunctiestructuur en groter specifiek oppervlak van de bovenste laag ZnO. Vergeleken met de schaarse ZnO-nanostaafjes op Cu2 O (pH 12, 20 min) en te veel grote ZnO-nanostaafjes op Cu2 O (pH 10, 40 min), Cu2 O (pH 10, 20 min)/ZnO heeft de beste fotokatalytische prestatie van drie Cu2 O/ZnO-architecturen als resultaat van perfecte ZnO-nanostructuren gekweekt op Cu2 O (pH 10, 20 min), zoals getoond in Fig. 2d en 3c en d. De invloed op de reactie-pH, reactietijd en oriëntatie van de heterojunctie wordt besproken, en tot slot heeft de reactietijd weinig effect op de fotokatalytische prestatie in de ZnO/Cu2 O-systeem. Samengevat, in de ZnO/Cu2 O-systeem, Cu2 O (pH 10, 20 min)/ZnO heeft de beste fotokatalytische prestatie.
De concentratieveranderingen van MO met ZnO, CuSCN (3D), CuSCN (NWs), ZnO/CuSCN (3D), ZnO/CuSCN (NWs), CuSCN (3D)/ZnO en CuSCN (NWs)/ZnO als katalysatoren weergegeven in Aanvullend bestand 1:Afbeelding S6(b). De fotokatalytische prestatie van ongerept CuSCN is slechter dan die van ongerepte ZnO-nanostaafjes vanwege een kleiner specifiek oppervlak, lagere mobiliteit van de drager en gemakkelijkere recombinatie van elektronen en gaten. De fotokatalytische prestaties van CuSCN (NW's) zijn beter dan die van CuSCN (3D) vanwege het grotere specifieke oppervlak van de CuSCN-nanostructuren, zoals weergegeven in Fig. 4e en f. De fotokatalytische prestaties van CuSCN (3D)/ZnO en CuSCN (NWs)/ZnO zijn beter dan die van ZnO vanwege hun heterojunctiestructuur en groter specifiek oppervlak. CuSCN (NWs)/ZnO heeft betere fotokatalytische prestaties dan CuSCN (3D)/ZnO vanwege de kleinere en beter verdeelde ZnO-nanostaafjes die op CuSCN-nanostructuur zijn gegroeid en het daaruit voortvloeiende grotere specifieke oppervlak. In het ZnO/CuSCN-systeem heeft de ZnO/CuSCN-architectuur de beste fotokatalytische prestaties van ZnO, CuSCN, ZnO/CuSCN en CuSCN/ZnO als gevolg van de heterojunctiestructuur, een groter specifiek oppervlak van het bovenste materiaal van de heterojunctie, en het grotere contactoppervlak met de MO-oplossing. De ZnO-nanostaafjes onder CuSCN (3D)-structuren worden gedeeltelijk geëtst door de CuSCN-reactieoplossing met een erosieve pH, en de ZnO-nanostaafjes onder CuSCN (NWs) -structuren worden voornamelijk geëtst door de CuSCN-reactieoplossing met een pH van 1,5 waarbij alleen de omtrek en een paar overblijfselen van ZnO-nanostaafjes zoals weergegeven in Fig. 4a en b en Aanvullend bestand 1:Figuur S3 (a, b). Hoewel de ZnO-nanostaafjes onder CuSCN (3D)-structuren gedeeltelijk zijn geëtst, wordt de tussenruimte tussen de nanostaafjes groter dan die tussen de ongerepte ZnO-nanostaafjes met als gevolg een groter specifiek oppervlak en is het helderder en netter dan de ZnO-nanostaafjes onder CuSCN (NWs) -structuren met bijna volledige ets. De fotokatalytische prestatie van ZnO/CuSCN (3D) is dus beter dan die van ZnO/CuSCN (NWs). De invloed op de morfologie van de nanostructuur en de oriëntatie van de heterojunctie worden besproken, en beide kunnen de fotokatalytische prestaties in het ZnO/CuSCN-systeem beïnvloeden. Samengevat heeft ZnO/CuSCN (3D) de beste fotokatalytische prestaties in het ZnO/CuSCN-systeem.
Aanvullend bestand 1:Figuur S6(c) toont de concentratieveranderingen van MO met ZnO, NiO (1 min), NiO (10 min), ZnO/NiO (1 min), ZnO/NiO (10 min), NiO (1 min )/ZnO en NiO (10 min)/ZnO als katalysator. De fotokatalytische prestaties van ongerept NiO (10 min) zijn slechter dan die van ongerepte ZnO-nanostaafjes vanwege de grotere nanostructuur, het daaruit voortvloeiende kleinere specifieke oppervlak, lagere dragermobiliteit en gemakkelijkere recombinatie van elektronen en gaten. De fotokatalytische prestaties van NiO (1 min) zijn beter dan NiO (10 min) en ZnO vanwege het veel grotere specifieke oppervlak van de NiO-nanostructuren, zoals weergegeven in Fig. 5e en f. De fotokatalytische prestatie van NiO (10 min)/ZnO is slechter dan die van ZnO als gevolg van de nog grotere nanostructuur van de bovenste laag NiO (10 min) en het kleinere specifieke oppervlak. As shown in Fig. 5c, ZnO nanorods are partially exposed growing through the meshwork of NiO (1 min) and the remnant part of the ZnO nanorods are remained in the meshwork. NiO (1 min) nanostructures are the multi-layer interspersed meshwork uniformly distributed on the ITO glass with much higher specific surface area, as shown in Fig. 5e. So, NiO (1 min)/ZnO has a little better photocatalytic performance than ZnO and a lower photocatalytic action than NiO (1 min). The photocatalytic performance of ZnO/NiO (1 min) and ZnO/NiO (10 min) is better than others due to their heterojunction structure and larger specific surface area. ZnO/NiO(1 min) architecture has the best photocatalytic performance in the ZnO/NiO system as a result of the heterojunction structure, extremely higher specific surface area of the upper material in the heterojunction, and the consequent larger contact area with the MO solution. The influence on reaction time and orientation of the heterojunction are discussed and both will give an effect on the photocatalytic performance in the ZnO/NiO system. In summary, ZnO/NiO (1 min) has the best photocatalytic performance in the ZnO/NiO system.
Figure 6a and b show the concentration changes of MO and the UV-vis absorption spectra of MO aqueous solution with ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO (1 min) as the catalysts. Among the four semiconductor nanostructures ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), and NiO (1 min), NiO has the most excellent photocatalytic performance owing to the multi-layer interspersed meshwork uniformly distributed and the consequent extremely higher specific surface area. ZnO has the bigger mobility and bigger specific surface area than Cu2 O and CuSCN so that ZnO has the better photocatalytic performance. Cu2 O has the better photocatalytic performance than CuSCN due to the bigger specific surface area. ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the heterostructures based on n-type ZnO and p-type Cu2 O, CuSCN, and NiO. It is owing to more charge transfer caused by heterojunction structure, more photo-generated carrier as a result of higher specific surface area caused by the meshwork nanostructure of the upper NiO directly contacting to MO, and less carrier recombination caused by more compact contact of NiO/ZnO than Cu2 O/ZnO and CuSCN/ZnO, as shown in Additional file 1:Figure S2(c), Figure S3(a), and Figure S4(a). In summary, NiO is the most suitable material for photocatalytic degradation of MO among the four semiconductor nanostructures of ZnO, Cu2 O, CuSCN, and NiO. The photocatalytic performance of the semiconductor can be affected both by the mobility and the specific surface caused by the nanostructure. ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the architectures based on ZnO, Cu2 O, CuSCN, and NiO. Influencing factor on the photocatalytic performance of all these architectures can be summarized as the inherent mobility of the material, the heterojunction architecture, and the morphology of nanostructure. The scheme of the photocatalysis mechanism using heterostructure photocatalyst is shown in Additional file 1:Figure S7. The mechanisms for improved photocatalytic properties are demonstrated in Additional file 1. To further assess the photocatalytic activity, we have compared the degradation ability of our best heterojunction in every system with other nanohybrids in Table 2. Compared with other catalysts, ZnO/NiO (1 min) demonstrated the best photocatalytic performance.
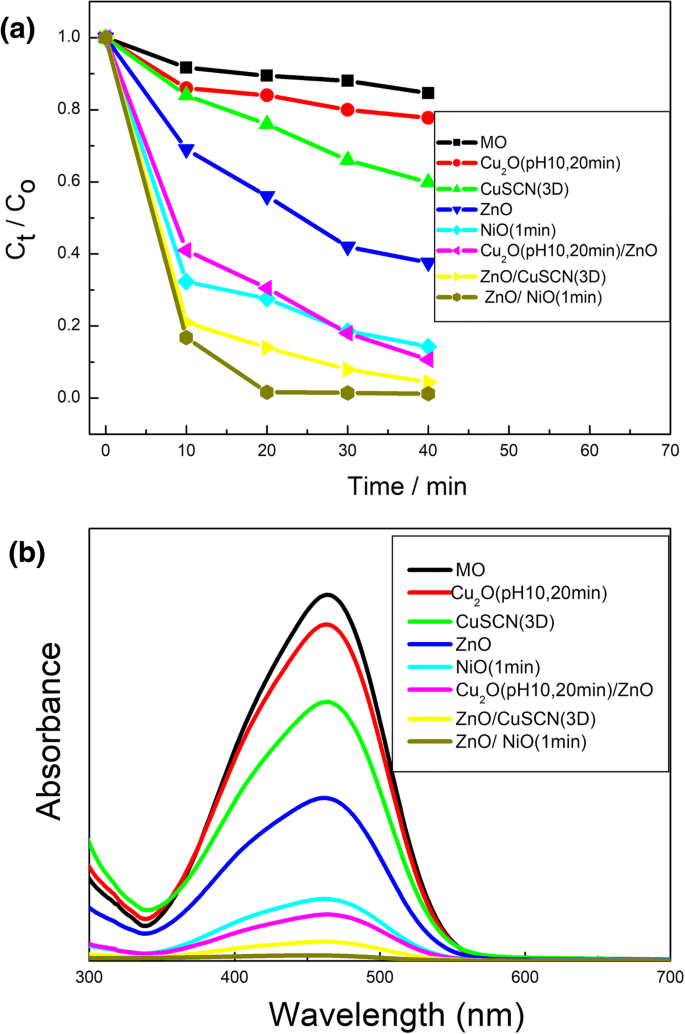
een The relative concentration (Ct /C0 ) of MO versus time under light irradiation in the absence and presence of various photocatalysts:ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO(1 min); b The UV-vis absorption spectra of MO aqueous solution with different photocatalysts:ZnO, Cu2 O (pH 10, 20 min), CuSCN (3D), NiO (1 min), Cu2 O (pH 10, 20 min)/ZnO, ZnO/CuSCN (3D), and ZnO/NiO(1 min)
Conclusies
In summary, different heterojunctions based on n-type ZnO nanorods and p-type Cu2 O, CuSCN, and NiO nanostructures with different orientations are fabricated. All these structures exhibit certain photocatalytic activity for the degradation of MO. Several conclusions can be summarized with analysis of these photocatalytic data as follows:the morphology of nanostructure has significant influence on photocatalytic activity; the photocatalytic activity of heterojunction structure is better than pristine semiconductor except consideration of the influence of the nanostructure morphology; the orientation of the heterojunction has no remarkable influence on photocatalytic activity; NiO has the best photocatalytic activity among the four pristine semiconductor nanostructures ZnO, Cu2 O, CuSCN, and NiO; and ZnO/NiO (1 min) heterostructure has the most excellent photocatalytic performance among all the architectures. The great enhancement of the photocatalytic activity is obtained using ZnO/NiO (1 min) heterostructure attributed to the heterojunction structure and extremely higher specific surface area. The study on the influence of materials, nanostructure morphology, and orientation in heterostructure on photocatalytic activity can provide a theoretical direction for the photocatalyst research with application in the energy and environment fields, and it can be concluded with a perspective on the future photocatalyst and a bright prospect of these controllable nanohybrid materials.
Afkortingen
- 1D:
-
Eendimensionaal
- EDTA:
-
Ethyleendiaminetetra-azijnzuur
- HMT:
-
Hexamethylenetetramine
- MO:
-
Methylsinaasappel
- NW:
-
Nanodraad
- SCE:
-
Verzadigde calomelelektrode
- SEM:
-
Scanning elektronenmicroscopie
- UV-vis DRS:
-
UV-vis diffuse reflectance spectrometry
- XRD:
-
Röntgendiffractie
Nanomaterialen
- De evolutie van SLS:nieuwe technologieën, materialen en toepassingen
- De perfecte formule om operaties en onderhoud op elkaar af te stemmen
- De beste metalen 3D-printmaterialen voor additieve productie
- Onthulling van de atomaire en elektronische structuur van gestapelde koolstof nanovezels
- Invloed van water op de structuur en diëlektrische eigenschappen van microkristallijne en nano-cellulose
- One-Pot-synthese van Cu2ZnSnSe4-nanoplaten en hun door zichtbaar licht aangedreven fotokatalytische activiteit
- PCB-materialen en ontwerp voor hoogspanning
- De beste materialen voor voedselveilige prototypes
- De beste materialen voor uw medische prototypes
- Een schaalbare methode voor de integratie van 2D-materialen op grote oppervlakken
- Remmen, koppelingen en wrijvingsmaterialen voor de olie- en gasindustrie



