Verbeterd effect van combinatie van chlorogeenzuur op seleniumnanodeeltjes bij het remmen van amyloïde β Aggregatie en vorming van reactieve zuurstofsoorten in vitro
Abstract
De afzetting van amyloïde-β (Aβ) plaques en de vorming van neurotoxische reactieve zuurstofsoorten (ROS) is een significant pathologisch kenmerk van de ziekte van Alzheimer (AD). Hierin wordt een nieuwe strategie gerapporteerd voor het combineren van de unieke Aβ-absorptie-eigenschap van seleniumnanodeeltjes met het natuurlijke antioxidant chlorogeenzuur (CGA) om CGA@SeNP's te vormen. De in vitro biologische evaluatie onthulde dat CGA de door Aβ40-aggregaten geïnduceerde ROS kon verwijderen, maar de Aβ40-aggregatie en celmembraanbeschadiging die ook door Aβ40-aggregaten werden veroorzaakt, niet remde. Interessant is dat CGA@SeNP's een versterkt remmend effect op Aβ40-aggregatie laten zien en, nog belangrijker, PC12-cellen beschermen tegen door Aβ-aggregatie geïnduceerde celdood. Er wordt aangenomen dat CGA@SeNP's efficiënter zijn dan CGA bij het verminderen van het toxische Aβ40 bij langdurig gebruik.
Achtergrond
De ziekte van Alzheimer (AD) is een onomkeerbare progressieve neurodegeneratieve ziekte die wordt gekenmerkt door progressieve cognitieve stoornissen en neuronaal verlies [1]. Het wordt nu algemeen aanvaard dat de accumulatie van extracellulaire amyloïdale plaques in de hersenen een veelvoorkomend pathologisch kenmerk is bij AD [2, 3]. De plaques bevatten de verkeerde vouwing en aggregatie van het amyloïde-β (Aβ)-eiwit [4]. Hoewel de exacte rol van Aβ-protofibrillen of oligomeer in de pathogenese van AD niet volledig wordt begrepen, suggereert toenemend bewijs dat de meeste van hen toxische soorten zijn die verantwoordelijk zijn voor neurondisfunctie en dood [5,6,7,8]. Bovendien bestaan de Aβ-aggregaten al in de hersenen van een AD-patiënt. Deze aggregaten zullen doorgaan met het vormen van neurotoxine-reactieve zuurstofsoorten (ROS), die een reeks schade aan cellulaire componenten zoals DNA, lipiden en eiwitten zullen veroorzaken en de oxidatieve stress in AD zullen veroorzaken [9]. Schade aan het neuron resulteert meestal in leer- en geheugentekorten. Daarom wordt verwacht dat het remmen van amyloïde β-aggregatie en de vorming van reactieve zuurstofsoorten veelbelovende therapeutische doelen kunnen zijn voor het voorkomen of verlichten van de pathologie van AD.
Nanomaterialen hebben unieke fysisch-chemische eigenschappen zoals kleine afmetingen, groot oppervlak en hoge reactiviteit. Onlangs heeft onderzoek benadrukt dat met de juiste oppervlaktemodificaties nanodeeltjes (NP's) kunnen worden gebruikt als hulpmiddelen voor medicijnafgifte, beeldvorming en therapeutische toepassingen in AD [10,11,12]. Over het algemeen hebben NP's een groot oppervlak dat grote adsorptiecapaciteiten met zich meebrengt. In het bijzonder kan Aβ aan sommige NP's binden om de fibrillatieprocessen van Aβ te vertragen. De binding van een Aβ-monomeer aan polyoxometalaten zou bijvoorbeeld de concentratie van vrije monomeren verlagen en het evenwicht verschuiven van fibrillatie [13]. Onder deze nanomaterialen vertonen selenium-nanodeeltjes (SeNP's) verschillende kenmerken die ze zeer geschikt maken voor biomedische toepassingen, zoals ongecompliceerde voorbereiding en stabiliteit. Selenium is een essentieel sporenelement dat een belangrijke rol speelt bij cellulaire redoxregulatie, ontgifting en bescherming van het immuunsysteem [14]. Daarom hebben SeNP's, in vergelijking met anorganische en organische seleniumverbindingen, een betere biocompatibiliteit en een lagere toxiciteit [15]. Tegenwoordig vergemakkelijken oppervlaktemodificaties van NP's de bindingsaffiniteit tussen NP's en Aβ en helpen ze de biochemische eigenschappen van de geconjugeerde moleculen te verhelpen. Onze eerdere studie vond dat de anti-amyloïde capaciteit van SeNP's verder kon worden verbeterd door een anti-amyloïde peptide (LPFFD) op een SeNP-oppervlak te enten [12]. De meeste van deze onderzoeken waren echter niet gericht op het anti-oxidatievermogen van NP's na oppervlaktemodificaties.
Chlorogeenzuur (CGA) is het belangrijkste polyfenolbestanddeel in fruit zoals appel, peren en bessen en komt vooral veel voor in koffie [16]. CGA heeft een aantal farmacologische eigenschappen, zoals antikanker, ontstekingsremmend en antibacterieel [16]. Vooral CGA heeft anti-oxidatieve en neuroprotectieve activiteiten, waardoor het kan worden toegepast om de ziekte van Alzheimer te behandelen [17, 18]. Het effect van CGA op Aβ-aggregatie is echter nooit gerapporteerd. Bovendien wordt het gebruik van CGA beperkt door de lage biologische beschikbaarheid en stabiliteit, en bereikt slechts een derde van het CGA dat uit het maagdarmkanaal wordt geabsorbeerd de bloedsomloop [19]. Een aantal studies hebben gemeld dat vanwege de kleine omvang van NP's, ze rechtstreeks in de bloedbaan kunnen komen via inademing, inname en transport door de bloedsomloop naar vele organen. Om dit probleem op te lossen, hebben we daarom de binding van CGA aan SeNP's (CGA@SeNP's) onderzocht om de potentiële therapeutische werkzaamheid van CGA te verbeteren. In deze context was het doel van deze studie om de potentiële therapeutische werkzaamheid van CGA@SeNP's bij anti-Aβ-aggregatie en anti-oxidatie te onderzoeken. Voor zover wij weten, is er geen eerder rapport over het gebruik van CGA@SeNP's voor AD-therapie.
Methoden/experimenteel
Materialen en cellijnen
Aβ40 werd gesynthetiseerd bij GL Biochem Ltd. (Shanghai, China). Seleniumdioxide (Na2 SeO3 ), NaBH4 , thiazolylblauw tetrazoliumbromide (MTT), thioflavine T en 2',7'-dichloordihydrofluoresceïnediacetaat (DCFH-DA) waren van Sigma (St. Louis, MO, VS). CGA werd gekocht van Aladdin (Shanghai, China). Dulbecco's gemodificeerd Eagle-medium (DMEM), foetaal runderserum (FBS) en paardenserum werden verkregen van Gibco (Life Technologies AG, Zwitserland). PC12-cellen (rattenfeochromocytoom, American Type Culture Collection) werden gekweekt in DMEM-medium aangevuld met 5% FBS en 10% paardenserum bij 37 ° C in een 5% CO2 vochtige omgeving bij 37 °C.
Voorbereiding van CGA@SeNP's
Eerst voorraadoplossingen van 25 mM CGA, 0,1 M Na2 SeO3 , en 0,1 M NaBH4 waren voorbereid. Vervolgens 200 μL aliquot van Na2 SeO3 oplossing werd gemengd met verschillende volumes CGA en de reactantconcentratieverhoudingen van Na2 SeO3 naar CGA waren 1:1, 1:2, 1:4, 1:6 en 1:8. Daarna 200 μL 0,1 M NaBH4 werd aan het mengsel toegevoegd en gedurende 30 minuten geroerd. De kleur van de oplossing werd veranderd in rood. Overtollige CGA en Na2 SeO3 werden verwijderd door dialyse. We ontdekten dat de beste concentratieverhouding van Na2 SeO3 naar CGA was 1:6.
Karakterisering van CGA@SeNP's
De als voorbereide CGA@SeNP's werden gekarakteriseerd door transmissie-elektronenmicroscoop (TEM; Hitachi, H-7650), Fourier-transformatie-infraroodspectroscopie (FT-IR; Equinox 55 IR-spectrometer) en UV-vis-spectroscopie (Carry 5000-spectrofotometer). De grootteverdeling werd bepaald door Zetasizer Nano ZS deeltjesanalysator (Malvern Instruments Limited). De fluorescentie van nanodeeltjes werd uitgevoerd met een JASCO FP6500 spectrofluorometer (λ ex =350 nm).
H2 O2 Generatietest
De hydroxylradicaal, 2,29-azinobis-(3-ethylbenzothiazoline-6-sulfonzuur) (ABTS + ), en superoxide-anion-opruimactiviteiten van CGA en CGA @ SeNP's werden geanalyseerd door commerciële kits (Nanjing Jiancheng Bioengineering Institute, Nanjing, China). Het reducerende vermogen van de monsters werd als volgt gemeten:2 ml CGA of CGA@SeNP's werd geïncubeerd met 2 ml fosfaatbuffer (0,2 mol/L, pH 6,6) en 2 ml K3 Fe(CN)6 (1%, w /v ) bij 50 °C gedurende 20 minuten. Daarna werd de reactie gestopt door 2,5 ml trichloorazijnzuur toe te voegen (10%, w /v ) en gedurende 10 minuten bij 3000 tpm gecentrifugeerd. Twee milliliter van het supernatant werd gemengd met 2 ml gedestilleerd water en 1 ml FeCl3 (0,1%, w /v ) bij kamertemperatuur gedurende 10 min. Ten slotte werd de absorptie gemeten bij 700 nm. Vitamine c (Vc) werd gebruikt als een positieve controle in de anti-oxidatie-activiteitstest.
De H2 O2 generatie in Aβ40 werd geanalyseerd door DCFH-DA. DCFH-DA-voorraadoplossing (1 mM) gekocht bij Beyotime Institute of Biotechnology (Shanghai, China). Vier micromolair mierikswortelperoxidase (HRP) werd bereid in buffer (20 mM Tris-HCl/150 mM NaCl, pH 7,4). Monsteroplossingen met 35 μM Aβ40 met of zonder 20, 40 en 60 μg/ml CGA@SeNPs/CGA werden 3 dagen bij 37 °C geïncubeerd. Ascorbaat (10 μM) werd aan elk monster toegevoegd en gedurende 1 uur verder geïncubeerd. Monsteranalyses werden uitgevoerd door DCFH-DA (20 L, 100 μM) en HRP (2 L, 0,04 M) aan de monsteroplossing (10 L) toe te voegen. Fluorescentiespectra met excitatie- en emissiegolflengten van 488 en 525 nm werden gemeten met een JASCO FP6500-spectrofluorometer.
Thioflavine T-fluorescentiemetingen
De kinetiek van Aβ40-fibrillatie werd gedetecteerd met behulp van de kleurstof thioflavine T (ThT). In het kort werd 35 μM Aβ40 geïncubeerd met 20, 40 en 60 μg/ml CGA@SeNPs/CGA bij 37 °C van 0 tot 5 dagen. Elke dag werd 50 L oplossing eruit gehaald en toegevoegd aan 200 μL ThT-oplossing (15 μM ThT in 50 mM PBS, pH 7,4). Vervolgens was de excitatie van ThT 440 nm en werd de emissiegolflengte van 490 nm geregistreerd.
TEM
Morfologieën van Aβ40 in aanwezigheid of afwezigheid van CGA@SeNPs/CGA werden waargenomen door TEM (Hitachi, H-7650). De monsters werden op dezelfde manier bereid als in de ThT-fluorescentietest. Na 3 dagen incubatie werd 10 μL monsteroplossing gedurende 10 minuten op de met koolstof beklede koperen roosters gespot. Vervolgens werd elk raster gekleurd met 1,5% (w /v ) fosfowolfraamzuur (pH 7,4) en laat drogen.
Binding van nanodeeltjes aan Aβ40 werd ook bevestigd door TEM. Eerst werd 35 μM Aβ40 3 dagen geïncubeerd om de vezels te formatteren. Vervolgens werden 20 μg / ml nanodeeltjes toegevoegd aan de voorgeïncubeerde oplossing en nog eens 6 uur geïncubeerd. Daarna is dit monster onderzocht op TEM.
Resonantie lichtverstrooiingsmetingen
De resonantie lichtverstrooiing (RSL) werd gemeten volgens de methode van Yu et al. [20] met enkele aanpassingen. Een bepaalde hoeveelheid Aβ40-dispersie werd verdund tot 1 ml met H2 O, terwijl de eindconcentratie van CGA@SeNP's varieerde van 0,05 tot 0,45 μg/ml. Het mengsel werd 10 minuten geïncubeerd. De RLS-intensiteiten werden geregistreerd op de Cary Eclipse-fluorspectrofotometer (Agilent-technologieën, VS) door de excitatie- en emissiemonochromatoren synchroon te scannen (Δλ = 0 nm) tussen 200 en 800 nm. Zowel de excitatie- als de emissiespleetbreedte waren ingesteld op 5 nm.
Cytotoxiciteitstest
De levensvatbaarheid van de cellen werd geanalyseerd met behulp van de MTT-assay. PC12-cellen werden uitgeplaat met een dichtheid van 5000 cellen per putje op platen met 96 putjes in vers medium zonder FBS. Aβ (35 μM) werd gedurende 3 dagen gelijktijdig geïncubeerd met of zonder 60 μg/ml CGA@SeNPs/CGA. Daarna werden de cellen nog 72 uur met deze monsters behandeld. Na incubatie werden de cellen behandeld met 10 μL MTT per putje, volgens de handleiding van Cell Titer 96 Aqueous One Solution Cell Proliferation assay (Promega). De afgifte van lactaatdehydrogenase (LDH) werd getest met behulp van de commerciële detectiekit. De PC12-cellen werden behandeld zoals hierboven. Aan het einde van de behandelingen werd de plaat met 96 putjes gecentrifugeerd bij 1500×g gedurende 10 min. De LDH-activiteit in supernatanten werd gemeten volgens de instructies van de fabrikant.
Intracellulaire ROS-generatie
De effecten van CGA@SeNPs/CGA op Aβ40-geïnduceerde intracellulaire ROS-generatie werden gevolgd door DCFH-DA-assay. De PC12-cellen (1 × 10 5 per putje) werden op dezelfde manier behandeld als in de MTT-assay. Vervolgens werden de cellen tweemaal gewassen met PBS en 30 minuten bij 37 ° C geïncubeerd met DCFH-DA (10 mM). Het intracellulaire ROS-niveau werd onderzocht onder een fluorescentiemicroscoop (vergroting x 200) met de excitatie- en emissiegolflengten bij respectievelijk 488 nm en 525 nm. Om het intracellulaire ROS-niveau te meten, werden de cellen op dezelfde manier behandeld en geoogst door centrifugeren, opnieuw gesuspendeerd in PBS. Vervolgens werden de cellen geanalyseerd met flowcytometrie.
TUNEL-DAPI co-kleuring-assay
De PC12-cellen werden op dezelfde manier behandeld als in de MTT-assay. Daarna werden cellen in kamerglaasjes gefixeerd met 3,7% form-aldehyde en gepermeabiliseerd met 0,1% Triton X-100 in PBS. De kleuringstest werd uitgevoerd met behulp van terminal transferase dUTP nick end labeling (TUNEL) testkit (KeyGen BioTECH, Nanjing, China) volgens het protocol van de fabrikant. Afbeeldingen zijn gemaakt met behulp van een fluorescentiemicroscoop (vergroting × 200).
Statistieken
Statistische significantie werd geschat met behulp van eenrichtingsanalyse van variantie (ANOVA) gevolgd door Bonferroni's post hoc-test. Statistische significantie werd vastgesteld op P < 0.05.
Resultaten en discussie
Karakterisering van CGA@SeNP's
In deze studie gebruiken we een eenvoudige methode om CGA@SeNP's te synthetiseren door een mengsel van CGA en Na2 te reduceren. SeO3 met NaBH4 . Nanodeeltjes met een grootte variërend van 30 tot 150 nm waren gunstiger voor cellulaire opname [21]. TEM toonde aan dat CGA@SeNP's een bolvormige structuur hebben met een diameter van ongeveer 100 nm (figuur 1a), wat suggereert dat de grootte van CGA@SeNP's geschikt was voor de biologische toepassing. Elementaire samenstellingsanalyse toonde aan dat Se, C en O gemakkelijk te vinden zijn in de energiedispersieve röntgenspectroscopie (EDX) -grafiek van CGA @ SeNP's (figuur 1b). Het signaal van de Se-atomen was 30,00%, samen met het sterke C-atoomsignaal (52,60%) en O-atoomsignaal (1,50%) van CGA, wat aangeeft dat we de CGA@SeNP's met succes hebben voorbereid.
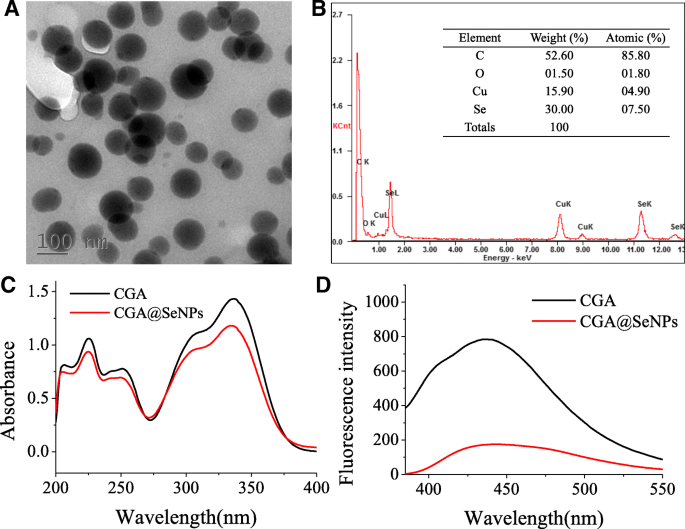
Karakterisering van CGA@SeNP's. een TEM-afbeeldingen van CGA@SeNP's. b EDX-analyse van CGA@SeNP's. c UV-vis absorptiespectrum van CGA@SeNP's. d Het emissiespectrum van CGA@SeNP's
Het UV-vis-absorptiespectrum van CGA vertoont een karakteristieke absorptiepiek bij 334 nm (figuur 1c). Er werd echter een kleine verschuiving waargenomen in het UV-vis-absorptiespectrum van CGA@SeNP's en de absorptiepiek werd veranderd in 337 nm. De emissiegolflengten van CGA en CGA@SeNP's werden gedetecteerd met een fluorescentiespectrofotometer. De emissiegolflengte van CGA was 442,9 nm, die werd verschoven naar 437,5 nm in CGA@SeNP's (figuur 1d). Deze resultaten bevestigden de aanwezigheid van CGA op het oppervlak van SeNP's. Het FT-IR-spectrum van CGA@SeNP's geeft aan dat CGA een deel van het nanocomposiet heeft gevormd. De O–H-rekfrequentie bevindt zich op 3353,99 cm −1 in het FT-IR-spectrum van CGA (aanvullend bestand 1:figuur S1); deze karakteristieke piek in CGA@SeNP's is echter gewijzigd in 3419,00 cm −1 . De verschuiving bevestigde dat CGA via de −OH-groep aan het oppervlak van SeNP's was geconjugeerd.
De stabiliteit van CGA@SeNP's onder fysiologische omstandigheden is belangrijk voor het evalueren van hun toekomstige toepassingen. Zo werd de grootteverdeling van CGA@SeNP's in PBS (pH 7,4) gedurende 7 dagen bij kamertemperatuur gevolgd. Zoals weergegeven in Aanvullend bestand 1:Afbeelding S2, bleef de grootte van CGA@SeNP's stabiel met een gemiddelde grootte van ongeveer 100 nm, en CGA@SeNP's behielden binnen 7 dagen een goede waterdispergeerbaarheid in PBS. De gunstige stabiliteit van CGA@SeNP's ondersteunt hun potentiële toepassing op medisch gebied.
Remming van ROS-generatie
Het afgezette Aβ kan microglia activeren en microglia stimuleren om neurotoxinen te produceren, zoals ROS, die verder ernstige neuronale schade in de hersenen kunnen veroorzaken [22]. Trouwens, ROS zoals waterstofperoxide (H2 O2 ) kan ook worden gegenereerd door Aβ-aggregaten [23]. Zo onderzochten we de antioxidantactiviteiten van CGA@SeNP's en het effect van CGA@SeNP's op Aβ-aggregaat-geïnduceerde H2 O2 vorming. Zoals te zien is in Aanvullend bestand 1:Afbeelding S3, hebben de CGA@SeNP's sterke afvangende activiteiten tegen radicalen op een concentratieafhankelijke manier. Toen de concentratie 60 μg/ml bereikte, werd de hydroxylradicaal ABTS + , en de activiteiten voor het opruimen van superoxide-anionen bereikten respectievelijk 70,3%, 95,2% en 95,1%. Het is duidelijk dat het reducerende vermogen van CGA@SeNP's toenam met toenemende concentraties. Van alle monsters vertoonden CGA@SeNP's een sterk reducerend vermogen en wegvangende capaciteiten op hydroxylradicaal, ABTS + , en superoxide-anion dan Vc en CGA. Deze resultaten suggereerden dat CGA@SeNP's een hogere antioxidantactiviteit vertoonden, wat kan helpen bij het opruimen van actieve zuurstof bij AD. Het punt dat moet worden opgemerkt is dat de wijziging van CGA op SeNP's een synergetisch effect heeft op de antioxidantactiviteit.
Het effect van CGA@SeNP's op de Aβ-gemedieerde H2 O2 generatie werd onderzocht met een DCFH-DA-assay [24], wat de generatie van H2 kan aangeven O2 van de Aβ in aanwezigheid of afwezigheid van CGA@SeNP's. Zoals weergegeven in Afb. namen CGA@SeNP's en CGA af H2 O2 op een dosisafhankelijke manier. Belangrijker is dat de Aβ-samples die CGA@SeNP's bevatten minder H2 . vertonen O2 dan die met CGA, waaruit blijkt dat de hoge antioxidantactiviteit van CGA@SeNP's meer effect vertoonde dan CGA bij het verminderen van de door Aβ geïnduceerde H2 O2 generatie.
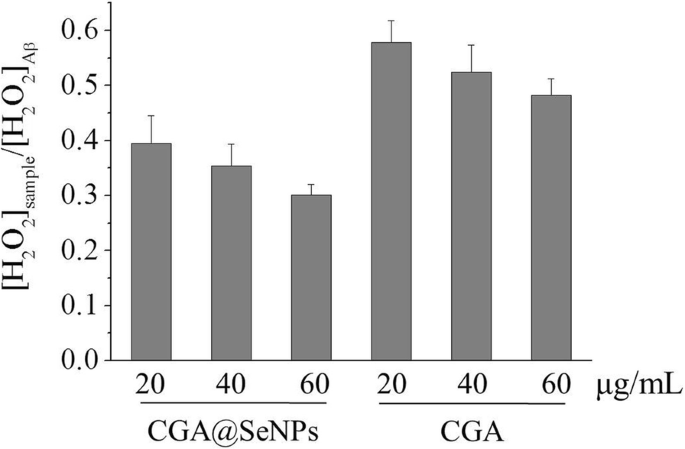
H2 O2 generatie van reacties van Aβ40 in aanwezigheid of afwezigheid van nanodeeltjes. Aβ =35 μM, nanodeeltjes/CGA =20, 40 en 60 μg/ml
Remming van Aβ-aggregatie door CGA@SeNPs
Hoewel de antioxiderende activiteit van CGA een bekende eigenschap is, is de anti-amyloïde aggregatieactiviteit van CGA nog onbekend. Om de haalbaarheid van de CGA@SeNP's voor AD-therapeutische toepassingen te verifiëren, werd het remmende effect van CGA@SeNP's op Aβ-aggregatie eerst onderzocht met een op ThT gebaseerde fluorometrische test, een gevestigde methode om de vorming van β-sheets onder continue tijd [25]. Zoals getoond in Fig. 3a, aggregeerde Aβ40 spontaan en de fluorescentie van Aβ-fibrillen nam geleidelijk toe totdat het een plateau bereikte na 3 dagen incubatie. We hebben waargenomen dat CGA@SeNP's in staat waren om langzaam amyloïde-eiwitten te aggregeren met toenemende concentratie. Fluorescentie-intensiteit van Aβ40-vezels ongeveer twee keer meer dan die van Aβ40 geïncubeerd met 60 g / ml CGA@SeNP's. Er werd echter weinig of geen verandering in de ThT-fluorescentie-intensiteit waargenomen in CGA, wat suggereert dat CGA de Aβ40-aggregatie slechts in geringe mate remde.
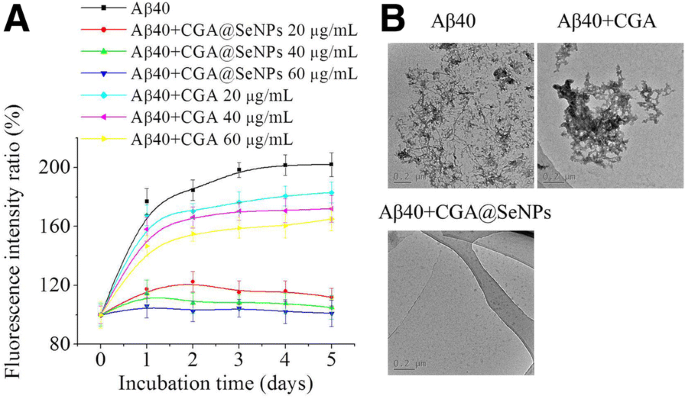
Remmingseffect van CGA@SeNP's op Aβ40-fibrillatie. een ThT-fluorescentie van Aβ40-fibrilvorming in aanwezigheid of afwezigheid van nanodeeltjes/CGA van 0 tot 5 dagen. Aβ40 =35 μM, nanodeeltjes/CGA =20, 40 en 60 g/ml. b Morfologie van Aβ40 geïncubeerd met of zonder nanodeeltjes of CGA gedurende 3 dagen. Aβ40 =35 μM, nanodeeltjes/CGA =60 μg/ml
De morfologische veranderingen van Aβ40 geïncubeerd met of zonder CGA of CGA@SeNP's worden getoond in figuur 3b. Aβ40 geïncubeerd in 3 dagen vormde overvloedige fibrillen, terwijl in aanwezigheid van CGA@SeNP's (60 μg/ml), geen fibrillen werden gevormd. Zoals verwacht remde CGA de Aβ-fibrillogenese niet significant, terwijl grote hoeveelheden aggregaten werden waargenomen in de oplossing van met CGA behandeld Aβ40, wat consistent was met de ThT-fluorometrische test. Deze resultaten gaven aan dat het na wijziging van CGA op SeNP's duidelijk de vorming van β-sheets zou kunnen verminderen.
Bindactiviteit van CGA@SeNP's aan Aβ40
Om een beter begrip te krijgen van de remmende activiteit van CGA@SeNP's op Aβ-aggregatie, hebben we de bindingsaffiniteit van CGA@SeNP's voor Aβ40 onderzocht. Ten eerste, om de binding van nanodeeltjes aan Aβ40-vezels op ultrastructureel niveau te evalueren, werden Aβ40-vezels geïncubeerd met CGA@SeNP's. We hebben waargenomen dat de fibrillen specifiek aan het oppervlak van SeNP's bonden zonder de aanwezigheid van vrije niet-geassocieerde gesuspendeerde nanodeeltjes (Fig. 4a).
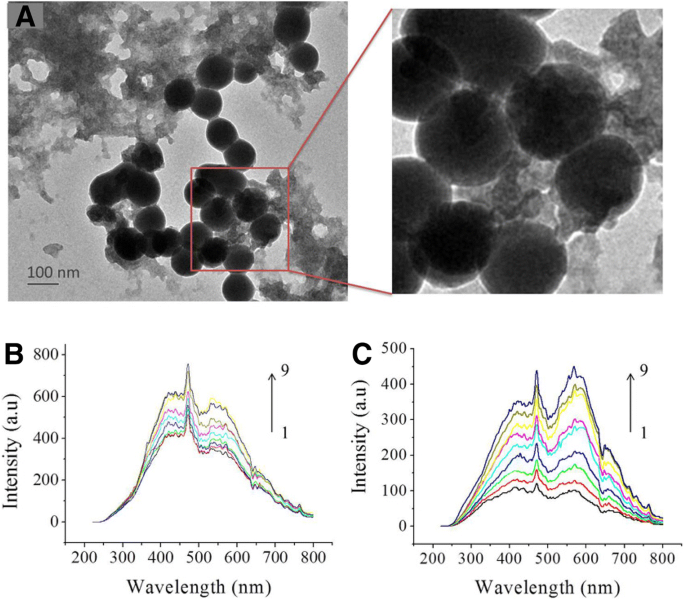
Affiniteit van CGA@SeNP's voor Aβ40. een De bindingscapaciteit van CGA@SeNP's op Aβ40-vezels. De uitgevoerde vezels van Aβ40 werden geïncubeerd met CGA@SeNP's en onderzocht op TEM. Aβ40 =35 μM, CGA@SeNPs =60 μg/ml. b Affiniteit en specificeer van CGA@SeNP's voor Aβ40-monomeer. De RLS-spectra van Aβ40-monomeer in aanwezigheid van verschillende concentraties CGA@SeNP's. Aβ40 =600 nM, nanodeeltjesconcentratie, 1–9:0, 0,05, 0,1, 0,15, 0,2, 0,25, 0,3, 0,35 en 0,4 μg/ml. c De RLS-spectra van CGA@SeNP's, nanodeeltjesconcentratie, 1–9:0,05, 0,1, 0,15, 0,2, 0,25, 0,3, 0,35, 0,4 en 0,45 μg/ml
Resonantielichtverstrooiing (RLS) is een krachtige optische techniek gebaseerd op elastische lichtverstrooiing en is op grote schaal toegepast om de grootte, vorm en verdeling van nanodeeltjes in oplossing te bestuderen [26]. Daarom hebben we vervolgens RLS gebruikt om de interactie tussen Aβ40-monomeer en CGA@SeNP's te analyseren. Zoals getoond in Fig. 4b, c, is de RLS-intensiteit van NP's veel lager dan die van NP's die zijn geïncubeerd met 600 nM Aβ40-monomeer in dezelfde concentratie. Toen de CGA@SeNP's eenmaal waren blootgesteld aan Aβ-moleculen, wordt aangenomen dat Aβ aan het oppervlak van SeNP's bindt via N-donoren die zijketens van aminozuren bevatten om een Se-N-binding te vormen [27]. De vorming van conjugaten van Aβ-moleculen op CGA @ SeNP's resulteert in het vergroten van de verstrooiing, wat de RLS-intensiteit van het systeem verhoogde (figuur 4b). Gecombineerd met het resultaat van ThT-assay en TEM, wordt gespeculeerd dat de interacties tussen het grote CGA@SeNP-oppervlak en Aβ40-monomeer zouden kunnen resulteren in ongunstige omstandigheden voor nucleatie en fibrilgroei door het blokkeren van direct contact tussen monomeren. Dus CGA@SeNP's oefenen meer effect uit dan CGA bij het remmen van de Aβ40-aggregatie.
Remming van Aβ40-neurotoxiciteit
De cytotoxiciteit van Aβ40 in aanwezigheid of afwezigheid van CGA@SeNP's in PC12-cellen werd onderzocht met MTT-assay. Figuur 5a laat zien dat Aβ40-vezels giftig waren voor de PC12-cellen, wat de levensvatbaarheid van de cellen verminderde tot 53%. In aanwezigheid van CGA@SeNP's nam de overleving van de cellen toe tot ongeveer 95%. Voorbehandeling van de cellen met CGA verhoogde de overleving van de cellen echter slechts in geringe mate tot 66%. Bovendien waren de CGA@SeNP's niet-toxisch voor PC12-cellen (aanvullend bestand 1:Afbeelding S4), wat suggereert dat CGA@SeNP's de neurotoxiciteit van Aβ40 zouden kunnen remmen.
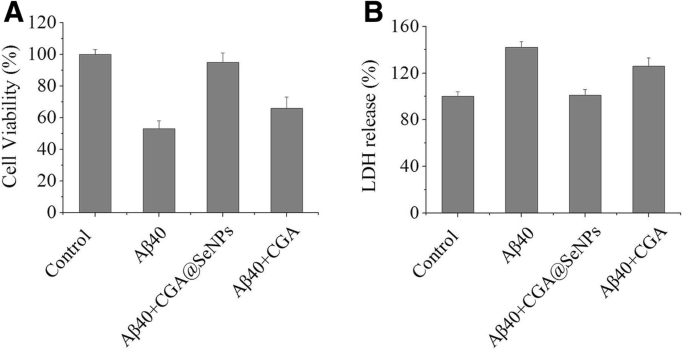
De neurotoxiciteit van Aβ40 geïncubeerd met of zonder CGA@SeNPs/CGA. een De levensvatbaarheid van PC12-cellen in de richting van Aβ40 in aanwezigheid van CGA@SeNP's of CGA getest met MTT-assay. b De afgifte van LDH in het kweekmedium. Aβ40 =35 μM, CGA@SeNPs/CGA =60 μg/ml
Er is gemeld dat Aβ bij voorkeur geïmmobiliseerd werd op het celoppervlak en de celmembraanbeschadiging veroorzaakte [28]. Om de integriteit van het celmembraan te bepalen na blootstelling aan Aβ40 in de aanwezigheid of afwezigheid van NP's/CGA, hebben we daarom de extracellulaire LDH-niveaus in celkweekmedium gemeten. In deze test weerspiegelt het hoge LDH-niveau de schade aan het celmembraan. Zoals weergegeven in figuur 5b, nam de LDH-afgifte in vergelijking met de controle na blootstelling aan Aβ40 toe tot 142%. In overeenstemming met het resultaat van MTT, werd de LDH-afgifte in aanwezigheid van CGA@SeNP's teruggebracht tot een normaal niveau. Interessant is dat we hebben waargenomen dat CGA de LDH-concentratie niet verlaagde, wat suggereert dat CGA PC12-cellen niet kan voorkomen van celmembraanbeschadiging veroorzaakt door Aβ-aggregaten.
Preventie van Aβ40-geïnduceerde ROS-generatie in PC12-cellen
Aβ-aggregaten zijn in staat ROS te produceren die oxidatieve stress in AD zou kunnen veroorzaken [29]. Vanwege de anti-oxidatie- en anti-aggregatie-eigenschappen van CGA @ SeNP's, veronderstelden we dat het in staat zou zijn om Aβ40-geïnduceerde ROS-generatie in PC12-cellen te verminderen. Het effect van NP's op de Aβ40-aggregaat-geïnduceerde ROS-generatie werd dus gemeten met DCFH-DA. DCF is een fluorescerende marker die is afgeleid van de reactie van niet-fluorescerende DCFH-DA met ROS, wat kan wijzen op de vorming van ROS die wordt geïnduceerd door Aβ40-aggregaten. Zoals weergegeven in Aanvullend bestand 1:Afbeelding S5, veroorzaakte behandeling met Aβ40-aggregaten een meer dan 1,5-voudige toename van het ROS-gehalte in vergelijking met onbehandelde cellen. CGA@SeNP-behandeling verminderde de DCF-fluorescentie-intensiteit in PC12-cellen, wat aangeeft dat de CGA@SeNP's de door Aβ-fibrillen geïnduceerde ROS tot een normaal niveau verlaagden. Interessant is dat CGA ook de ROS-generatie in PC12-cellen verminderde, maar niet zo duidelijk als CGA@SeNP's.
Preventie van door Aβ40 geïnduceerde celapoptose in PC12-cellen
Er is gemeld dat de dood van neuronale cellen veroorzaakt door Aβ-fibril een kritieke gebeurtenis is in AD-pathologie [30]. Om de cytotoxiciteit van Aβ40-fibrillen verder te bestuderen, hebben we TUNEL-DAPI co-kleuring uitgevoerd om het effect van NP's of CGA in Aβ40-geïnduceerde celapoptose te bepalen. DNA-fragmentatie is een kenmerk van celapoptose, die in de vroege stadia van apoptose kon worden gedetecteerd met behulp van TUNEL [31]. Zoals getoond in Fig. 6, werden de apoptotische kernen gekleurd in helder fluorescerend groen door TUNEL. Aβ40 verhoogde het aantal TUNEL-gekleurde kernen dramatisch, terwijl CGA@SeNP-behandeling een afname van TUNEL-positieve kernen veroorzaakte, wat aantoont dat CGA@SeNP's neuronen kunnen beschermen tegen Aβ40-geïnduceerde PC12-celapoptose. Anders nemen hoge niveaus van ROS in cellen ook deel aan apoptose [32]. Deze resultaten duidden er dus op dat door Aβ40 opgewekte apoptose kan worden toegeschreven aan het genereren van ROS. Het is vermeldenswaard dat CGA ook de door Aβ40 geïnduceerde celapoptose kan verminderen. Uit de MTT- en LDH-assay verbeterde CGA de overleving van de cel niet en verminderde de door Aβ-aggregaat geïnduceerde celmembraanbeschadiging niet. Gecombineerde resultaten van de TEM- en ThT-assay, we ontdekten dat CGA een anti-oxidatie-eigenschap heeft die actieve zuurstof kan verwijderen tijdens het proces van Aβ-aggregatie, maar het kan de Aβ-aggregatie niet volledig remmen. Daarom zou CGA de ROS-generatie in incubatieoplossing en PC12-cellen kunnen verminderen, waardoor ROS-geïnduceerde celapoptose wordt beschermd, maar het kan de door Aβ-aggregaat geïnduceerde celmembraanbeschadiging niet verminderen. De celmembraanbeschadiging zal resulteren in het lekken van intracellulaire inhoud in het omringende weefsel, wat kan leiden tot weefselbeschadiging en ontsteking [33]. Zo kan een combinatie van geremde Aβ-aggregatie en vorming van reactieve zuurstofsoorten worden beschouwd als een nieuwe therapeutische methode.
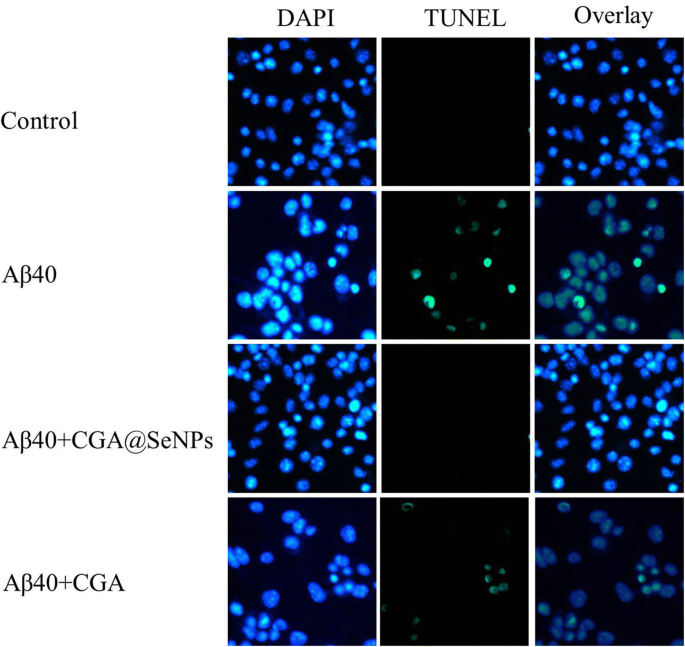
CGA@SeNP's voorkomen door Aβ40 geïnduceerde celapoptose in PC12-cellen. Celapoptose werd gedetecteerd door TUNEL-DAPI co-kleuring-assay. De normale celkern werd blauw gekleurd en het DNA-fragment werd groen gekleurd. Aβ40 =35 μM, CGA@SeNPs/CGA =60 μg/ml
Conclusies
Samengevat heeft CGA een farmacologische eigenschap tegen oxidatie, maar het heeft geen effect op het remmen van Aβ-fibrillatie. Oppervlaktemodificatie van CGA op SeNP's geeft het een nieuwe anti-aggregatie-eigenschap. Aβ40 zou kunnen binden aan het oppervlak van CGA@SeNP's, wat resulteert in ongunstige omstandigheden voor nucleatie en fibrilgroei door het blokkeren van direct contact tussen monomeren. In dat geval remden CGA@SeNP's Aβ40-aggregatie, maakten de ROS vrij en beschermden PC12-cellen tegen de celmembraanverstoring en ROS-gemedieerde apoptose geïnduceerd door Aβ40-aggregaten. In de CGA-groep werden de Aβ-aggregaten echter geïmmobiliseerd op het celoppervlak en veroorzaakten ze de celmembraanbeschadiging, wat ook leidde tot celdood. Over het algemeen zijn CGA@SeNP's efficiënter dan CGA bij het verminderen van het toxische Aβ40 bij langdurig gebruik.
Afkortingen
- ABTS + :
-
2, 29-Azinobis-(3-ethylbenzothiazoline-6-sulfonzuur)
- AD:
-
Ziekte van Alzheimer
- Aβ:
-
Amyloïde-β
- CGA:
-
Chlorogeenzuur
- DCFH-DA:
-
2′,7′-dichloordihydrofluoresceïnediacetaat
- DMEM:
-
Dulbecco's gemodificeerde Eagle-medium
- EDX:
-
Energie-dispersieve röntgenspectroscopie
- FBS:
-
Foetaal runderserum
- FT-IR:
-
Fourier-transformatie infraroodspectroscopie
- HRP:
-
Mierikswortelperoxidase
- LDH:
-
Lactaatdehydrogenase
- MTT:
-
Thiazolylblauwtetrazoliumbromide
- ROS:
-
Reactieve zuurstofsoorten
- RSL:
-
Resonantie lichtverstrooiing metingen
- SeNP's:
-
Selenium nanodeeltjes
- TEM:
-
Transmissie-elektronenmicroscoop
- ThT:
-
Thioflavine T
- TUNEL:
-
Terminal transferase dUTP nick einde labeling
- Vc:
-
Vitamine c
Nanomaterialen
- De toxiciteit van reactieve zuurstofsoorten afstemmen op geavanceerde tumortherapie
- Eenvoudige synthese en optische eigenschappen van kleine selenium nanokristallen en nanostaafjes
- Voorbereiding en verbeterde katalytische hydrogeneringsactiviteit van Sb/Palygorskite (PAL) nanodeeltjes
- De verbeterde foto-elektrochemische detectie van urinezuur op Au Nanodeeltjes gemodificeerde glasachtige koolstofelektrode
- Nanodeeltjes als effluxpomp en biofilmremmer om het bacteriedodende effect van conventionele antibiotica te verjongen
- Folaatreceptor-gerichte bioflavonoïde genisteïne-geladen chitosan-nanodeeltjes voor verbeterd antikankereffect bij baarmoederhalskanker
- In vitro onderzoek naar de invloed van Au-nanodeeltjes op HT29- en SPEV-cellijnen
- Synthese en in vitro prestaties van met polypyrrool gecoate ijzer-platina nanodeeltjes voor fotothermische therapie en foto-akoestische beeldvorming
- Synergetisch effect van Dy2O3 en Ca-co-doteerstoffen op verbeterde coërciviteit van zeldzame aarde overvloedige RE-Fe-B-magneten
- Zure peptiserende agent-effect op anatase-rutielverhouding en fotokatalytische prestaties van TiO2-nanodeeltjes
- Vergelijking tussen foliumzuur en op gH625 peptide gebaseerde functionalisering van Fe3O4 magnetische nanodeeltjes voor verbeterde celinternalisatie



