Eenvoudige synthese van oppervlaktegefunctionaliseerde magnetische nanocomposieten voor effectieve selectieve adsorptie van kationische kleurstoffen
Abstract
Een nieuw magnetisch nano-adsorbens, polycatechol gemodificeerd Fe3 O4 magnetische nanodeeltjes (Fe3 O4 /PCC MNP's) werden bereid door een gemakkelijke chemische coprecipitatiemethode met ijzerzouten en catechol-oplossing als voorlopers. Fe3 O4 /PCC MNP's bezaten een negatief geladen oppervlak met zuurstofbevattende groepen en vertoonden een sterke adsorptiecapaciteit en snelle adsorptiesnelheden voor de verwijdering van kationische kleurstoffen in water. De adsorptiecapaciteit van methyleenblauw (MB), kationisch turkooisblauw GB (GB), malachietgroen (MG), kristalviolet (CV) en kationisch roze FG (FG) was 60,06 mg g − 1 , 70,97 mg g − 1 , 66,84 mg g − 1 , 66,01 mg g − 1 en 50,27 mg g − 1 , respectievelijk. Het adsorptiemechanisme werd voorgesteld door de analyses van de adsorptie-isothermen en adsorptiekinetiek van kationische kleurstoffen op Fe3 O4 /PCC MNP's. Bovendien werden ook de kationische kleurstoffen die op de MNPs werden geadsorbeerd als functie van contacttijd, pH-waarde, temperatuur, naast elkaar bestaande kationische ionen en ionsterkte onderzocht. Deze resultaten suggereerden dat de Fe3 O4 /PCC MNP's belooft te worden gebruikt als magnetisch adsorbens voor selectieve adsorptie van kationische kleurstoffen in afvalwaterzuivering.
Achtergrond
Anorganisch en organisch afval geproduceerd door menselijke activiteiten heeft geleid tot grote hoeveelheden verontreinigd water dat een bedreiging vormt voor de gezondheid van mensen en andere levende organismen [1]. Watervervuiling is tegenwoordig een van de ernstigste milieuproblemen, die de ontwikkeling van de menselijke samenleving belemmert [2, 3]. Vooral kleurstofverontreinigende stoffen hebben grote bezorgdheid gewekt bij het publiek vanwege de hoge zichtbaarheid en de toxische impact op biologische organismen en de ecologie [4]. Organische kleurstoffen zijn op grote schaal gebruikt in verschillende branches, zoals textiel, papier, drukkerijen, kleurenfotografie, farmaceutische industrie, leer, cosmetica, plastic en andere industrieën, die de belangrijkste industriële afvalwaterbronnen zijn geweest [5]. De hoeveelheid kleurstofafvalwater is extreem groot, over het algemeen is het volume van het geloosde afvalwater van elke stap van een textielbewerking ongeveer tussen de 40 L/kg en 65 L/kg van het product [6]. Bovendien zijn kleurstoffen niet-biologisch afbreekbare stoffen die onder verschillende omstandigheden stabiel blijven vanwege hun synthetische oorsprong en complexe aromatische structuren [7]. Daarom is het noodzakelijk om een geschikte methode te selecteren om kleurstoffen uit afvalwater te verwijderen voordat het in het milieu wordt geloosd.
In de afgelopen jaren is een verscheidenheid aan technieken gebruikt om kleurstofafvalwater te behandelen, waaronder fotokatalytische afbraak [8], coagulatie [9], elektrochemische processen [10], chemische oxidatie [11], membraanfiltratie [12], biologische behandeling [13] en adsorptie [14]. Van deze kleurstofafvalwaterbehandelingstechnieken is adsorptie op grote schaal gebruikt vanwege hun verdiensten van eenvoud, hoge efficiëntie en zuinigheid [15, 16]. Van veel adsorbentia, zoals actieve kool, kaolien, montmorillonietklei, rode modder, vollere aarde en gebakken klei is gemeld dat ze afvalwater ontkleuren [17, 18]. Vooral magnetische nanodeeltjes (MNP's) hebben veel aandacht getrokken als adsorberende materialen voor organische kleurstoffen en zware metalen, vanwege hun unieke magnetische eigenschappen, lage kosten, biocompatibel, gemakkelijk te synthetiseren, gemakkelijk te recyclen, in het bijzonder economisch en milieuvriendelijk [19]. Er zijn verschillende methoden ontwikkeld om magnetische Fe3 . te synthetiseren O4 nanodeeltjes, waaronder i) coprecipitatie van ferro- en ferri-waterige oplossing in aanwezigheid van een base [20]; ii) thermische ontleding van een ijzercomplex [21]; iii) sonochemische benadering [22].
Vanwege hun hoge oppervlakte-energieën en intrinsieke magnetische interacties, gemakkelijke aggregatie van Fe3 O4 MNP's zouden hun oppervlakte/volume-verhouding en dispersiestabiliteit in waterige oplossing verminderen [23]. De stabilisatoren zoals oppervlakteactieve stoffen, dragers, oxiden of polymere verbindingen zijn gebruikt om Fe3 te modificeren. O4 MNP's om hun stabiliteit te vergroten en hun dispersiteit te verbeteren. Zhang et al. gesynthetiseerd magnetisch Fe3 O4 /C core shell nanodeeltjes en gebruikt als absorptiemiddelen met een goede adsorptiecapaciteit voor kleurstofverwijdering [24]. Wang et al. voorbereid Fe3 O4 nanodeeltjes met cetyltrimethylammoniumbromide (CTAB)-assistent voor adsorptieverwijdering van Congorood (CR) en methyleenblauw (MB) [25]. Verder is de adsorptiecapaciteit van kale Fe3 O4 MNP's zijn niet sterk genoeg.
Om de adsorptie-eigenschap te verbeteren, oppervlaktefunctionalisering van Fe3 O4 MNP's is onderzocht. Zhang et al. gewijzigde Fe3 O4 MNP's met 3-glycidoxypropyltrimethoxysilaan (GPTMS) en glycine (Gly), de magnetische nanocomposieten zouden uitstekend zowel anionische als kationische kleurstoffen kunnen verwijderen in een ernstige omgeving (zeer zuur of sterk alkalisch) [26]. Bovendien kan selectieve adsorptie sterk worden verbeterd voor de verrijking van polluenten door de introductie van grote aantallen actieve sites. Pourjavadi et al. rapporteerde een nieuwe gefunctionaliseerde magnetische nanocomposiet van poly(methylacrylaat) voor de efficiënte verwijdering van anionische kleurstoffen uit waterige media [27]. Polycatechol, het resultaat van de polymerisatie van catechol gekatalyseerd door Fe(III) [28,29,30], is gebruikt in oppervlaktemodificaties als kleefstoffen en coatings over een breed scala van zowel organische als anorganische materialen vanwege hun unieke thermische, structurele eigenschappen , en het vermogen om stabiele complexen te vormen met metaaloxiden [31, 32]. Het betekent dat Fe3 O4 MNP's gemodificeerd met polycatechol zullen het adsorptievermogen van Fe3 . aanzienlijk verhogen O4 MNP's. Er is echter geen rapport over polycatechol-gemodificeerd Fe3 O4 MNP's verreweg als een absorptiemiddel voor het verwijderen van kleurstoffen.
In dit werk gemodificeerde polycatechol Fe3 O4 MNP's (Fe3 O4 /PCC MNP's) werden bereid met een gemakkelijke coprecipitatiemethode en gebruikt als adsorbentia voor het verwijderen van kleurstoffen. Het absorptiemiddel werd gekarakteriseerd met behulp van magnetische hysteresislussen, thermogravimetrische analyse en zeta-potentiaalanalysetechniek. Vijf soorten kationische kleurstoffen, waaronder methyleenblauw (MB), kationisch turkooisblauw GB (GB), malachietgroen (MG), kristalviolet (CV) en kationisch roze FG (FG), werden gekozen als modelverbindingen om de adsorptie bloot te leggen. gedrag van Fe3 O4 /PCC MNP's. De adsorptiekinetiek, isothermanalyses en het effect van verschillende experimentele omstandigheden op de verwijdering van kationische kleurstoffen werden ook onderzocht.
Methoden
Materialen
IJzerchloride (FeCl3 ·6H2 O), ferrosulfaat (FeSO4 ·7H2 O), ammoniumhydroxide (NH3 ·H2 O, 25%), MB, GB, MG, CV, FG, Orange ΙΙ, Fuchsin, methyloranje (MO) en catechol werden verkregen van Chuandong Chemical Inc., Chengdu, Sichuan, China. Alle chemicaliën waren van analytische kwaliteit en werden zonder verdere zuivering gebruikt en alle oplossingen en suspensies werden bereid met gedeïoniseerd water. De structuren van vijf kationische kleurstoffen, waaronder MB, GB, MG, CV en FG, zijn weergegeven in figuur 1.
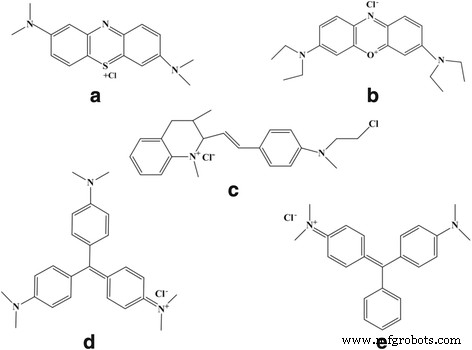
Moleculaire structuren van (a ) MB (b ) GB (c ) MG (d ) CV (e ) FG. Zoals weergegeven in Fig. 1, wordt de structuur van vijf soorten kationische kleurstoffen beschreven
Voorbereiding en karakterisering van Fe3 O4 /PCC MNP's
Fe3 O4 /PCC MNP's werden bereid door een gemakkelijke chemische coprecipitatiemethode met ijzerzouten en catechol als voorlopers [23]. Het hele syntheseproces werd uitgevoerd bij omgevingsatmosfeer. In het kort, FeCl3 ·6H2 O (10 mmol) en FeSO4 ·7H2 O (5 mmol) werd opgelost in 75 ml gedeïoniseerd water en vervolgens voldoende gemengd met 75 ml catechol (20 mM). Wanneer catechol werd gemengd met ijzeroplossing (pH 2,87), werd de polymerisatie van catechol gekatalyseerd door Fe 3+ gebeurde, waarbij polycatechol werd gevormd, wat zwarte grove precipitaten waren [30]. Tegelijkertijd Fe 3+ ionen werden chemisch geadsorbeerd op polycatechol door complexering en dienden als nucleatievoorlopers. Het mengsel bleef 30 min staan en werd daarna snel toegevoegd aan 100 ml ammoniumhydroxide (3,3 M), onder krachtig roeren 120 min verouderen. De magnetische nanodeeltjes groeiden in situ tot aggregaties op het oppervlak van polycatecholketens. Koppels van Fe3 O4 /PCC-ketens stevig met elkaar gecombineerd om Fe3 . te vormen O4 /PCC MNP's. De hele syntheseprocessen werden uitgevoerd bij omgevingsatmosfeer, zonder enige beschermende atmosfeer. De zwarte magnetische nanodeeltjes werden gescheiden door een externe magneet en gewassen met gedeïoniseerd water tot neutrale pH en 24 uur in een vacuümoven bij 50°C gedroogd. Fe3 O4 MNP's werden gesynthetiseerd met dezelfde procedures als hierboven vermeld zonder catechol toe te voegen. Alle producten werden bewaard in een exsiccator onder omgevingstemperatuur voor verdere experimenten.
Magnetische eigenschappen werden gemeten bij kamertemperatuur op een meetsysteem voor magnetische eigenschappen (MPMS XL-7, Quantum Design, Amerika). Thermogravimetrische analyse (TGA) werd uitgevoerd voor poedermonsters met behulp van een TGA/DSC 1 thermogravimetrische analysator (TGA) (Mettler-Toledo, Zwitserland) onder N2 omgeving met een verwarmingssnelheid van 5 °C min − 1 . De zeta-potentialen van katalysatorsuspensies bij verschillende pH's werden bepaald met een Malvern 3000 Zetasizer.
Batch adsorptie-experimenten
Experimenten met sorptie-isothermen werden uitgevoerd door 25 mg Fe3 . te schudden O4 /PCC MNP's in 25 ml oplossing met gevarieerde adsorbaten, met initiële adsorbaatconcentratie variërend van 0,02 mM tot 0,4 mM. Het mengsel werd continu geschud op een schudder bij 180 rpm onder een gecontroleerde temperatuur van 30 °C totdat evenwicht werd bereikt. De pH van de oplossing is aangepast met 1,0 M H2 SO4 of 1,0 M NaOH-oplossingen. Na adsorptie werd het adsorbens onder magnetisme van de oplossing gescheiden en vervolgens werd de bovenstaande vloeistof gemeten bij de maximale absorptie van elke kleurstof met een UV-vis-spectrofotometer.
Verder werd de adsorptiekinetiek van de processen bestudeerd. 100 mg Fe3 O4 /PCC MNP's werden gesuspendeerd in 100 ml 0,1 mM oplossingen van adsorbaten en vervolgens geschud bij 180 tpm onder pH 6,0 en 30 ° C. Met verschillende tijdsintervallen werd 0,5 ml suspensiemonster genomen en onmiddellijk gescheiden door een extern magnetisme en de bovenstaande vloeistof werd verzameld voor analyse.
De invloeden van pH-waarde en temperatuur op de adsorptie van kationische kleurstoffen werden ook bestudeerd. Het typische batchadsorptie-experiment werd als volgt uitgevoerd:50,0 mg Fe3 O4 /PCC MNP's werd gedispergeerd in 50,0 ml kationische kleurstofoplossing en vervolgens geschud op een shaker met een snelheid van 180 tpm.
Alle adsorptie-experimenten werden in duplo uitgevoerd. De adsorptiecapaciteit van elke kleurstof in het adsorptiesysteem, qe , werd berekend volgens Vgl. (1):
$$ {q}_e=\left({C}_i-{C}_e\right)\ V/{M}_s $$ (1)Waar q e (mg g − 1 ) is de adsorptiecapaciteit, C e (mM) is de evenwichtsconcentratie in de waterige fase, Ci (mM) is de initiële concentratie in de waterige fase, V (L) is het volume van de oplossing en M s (g) is de massa van vast adsorbens.
Resultaten en discussie
Karakterisering van Fe3 O4 /PCC MNP's
Afbeelding 2a toont de magnetische hysteresislussen bepaald bij kamertemperatuur voor Fe3 O4 en Fe3 O4 /PCC MNP's. De verzadigingsmagnetisatiewaarden van Fe3 O4 /PCC MNP's waren 53,5 emu g − 1 , hoger dan die van Fe3 O4 (49.6 emu g − 1 ), wat suggereert dat ze gemakkelijk kunnen worden gescheiden door een extern magnetisch veld [33]. De deeltjesgrootte, het spin-kantelingsverschijnsel, het grootte-effect en andere zijn gerelateerd aan de verzadigingsmagnetisatie van de ferriet-nanodeeltjes [34]. De modificatie van polycatechol maakt de Fe3 O4 /PCC MNP's met veel hogere kristallisatie en kleinere deeltjesgrootte dan Fe3 O4 MNP's, wat zou kunnen resulteren in de hogere verzadigingsmagnetisatie van Fe3 O4 /PCC MNP's dan Fe3 O4 MNP's. Verder hogere verzadigingsmagnetisatie van het bereide Fe3 O4 /PCC MNP's kunnen ook worden toegeschreven aan het oppervlakte-effect, soms het "dode oppervlak" genoemd. Het dode oppervlak wordt geassocieerd met wanorde van de oppervlaktespin [35].
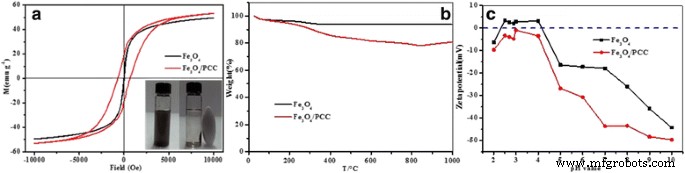
een Magnetisatiegedrag van Fe3 O4 MNP's en Fe3 O4 /PCC MNP's bij kamertemperatuur. b Thermogravimetrie (TGA) curven van Fe3 O4 MNP's en Fe3 O4 /PCC MNP's. c zeta-potentialen van Fe3 O4 /PCC magnetische nanodeeltjes. In Fig. 2 vertegenwoordigen de lege regels de aard van Fe3 O4 MNP's en de rode lijnen zijn namens het eigendom van Fe3 O4 /PCC MNP's
Het thermische gedrag van Fe3 O4 en Fe3 O4 / PCC MNP's werden verder onderzocht door thermogravimetrische analyse (TGA) (figuur 2b). Voor de TGA-curve van Fe3 O4 MNP's, was het gewichtsverlies (6,5%) onder 150 ° C te wijten aan het verlies van fysiek geadsorbeerd water. Voor de curve van Fe3 O4 /PCC MNP's, het gewichtsverlies (5,2%) onder 150 °C was te wijten aan het verlies van fysiek geadsorbeerd water, het gewichtsverlies (9,4%) van 150 °C tot 400 °C werd toegeschreven aan het verlies van zuurstofhoudende functionele groepen werd het gewichtsverlies (6,8%) van 400 °C naar 800 °C voornamelijk toegeschreven aan de verbranding van koolstof, en een lichte gewichtstoename (2,3%) boven 800 °C werd veroorzaakt door de oxidatie van Fe3 O4 tot γ-Fe2 O3 [36]. De Fe3 O4 /PCC MNP's vertoonden een lagere thermische stabiliteit dan Fe3 O4 , vanwege de wijziging van polycatechol [37].
Afbeelding 2c toont de zeta-potentialen van de Fe3 O4 en Fe3 O4 /PCC-suspensies bij verschillende pH-waarden. Zoals getoond in Fig. 2c, is het iso-elektrische punt van Fe3 O4 was 4,2, terwijl het oppervlak van Fe3 O4 /PCC MNP's hadden negatieve ladingen in het pH-bereik van 3,0-10,0, wat te wijten zou kunnen zijn aan de elektronegativiteit van de fenolische hydroxylgroep in polycatechol. Bovendien is de oppervlakteladingsdichtheid van Fe3 O4 /PCC MNP's namen toe naarmate de pH toenam van 3,0 naar 10,0. De negatieve ladingen van Fe3 O4 /PCC MNP's verhinderden ook agglomeratie van nanodeeltjes.
Selectieve adsorptie van Fe3 O4 /PCC MNP's
De adsorptie-eigenschappen van de Fe3 O4 /PCC MNP's naar kationische kleurstoffen, anionische kleurstoffen en fenol uit waterige oplossing werden in detail onderzocht. Afbeelding 3 toont de verwijderingsefficiëntie van MB als een soort kationische kleurstof, MO als een soort anionische kleurstof en fenol geadsorbeerd op Fe3 O4 /PCC MNP's. Er werd waargenomen dat de verwijderingsefficiëntie van MB 75,7% was. De verwijderingsefficiëntie van MO was echter slechts 10,9% en de verwijderingsefficiëntie van fenol was slechts 1,5%. De resultaten gaven aan dat de Fe3 O4 /PCC MNP's adsorbeerden selectief kationische kleurstof, vanwege de elektrostatische interactie (Fig. 2c).
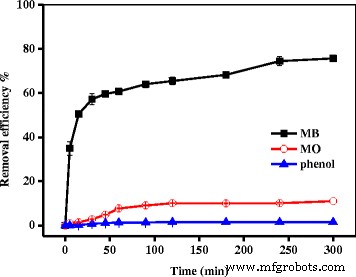
De verwijderingsefficiëntie van MB, MO en telefoon geadsorbeerd door Fe3 O4 /PCC MNP's. Zoals weergegeven in Fig. 3, staat de lege lijn voor de verwijderingsefficiëntie van MB, de rode lijn voor de verwijdering van MO en de blauwe lijn voor de verwijdering van phonel
Adsorptiekinetiek van kationische kleurstoffen
Adsorptiekinetiek van vijf kationische kleurstoffen op Fe3 O4 /PCC MNP's werden bestudeerd met behulp van twee kinetische modellen, namelijk het pseudo-eerste-ordemodel en het pseudo-tweede-ordemodel (Fig. 3). In het pseudo-eerste-orde kinetische model wordt de snelheidsconstante van de adsorptie van kleurstoffen uitgedrukt als [38]:
$$ Ln\left({q}_e-{q}_t\right)=\mathit{\ln}\left({q}_e\right)\hbox{--} {k}_1\ t $$ ( 2)waar q e en q t zijn de hoeveelheden geadsorbeerde kleurstoffen (mg g − 1 ) bij evenwicht en op elk moment t (min), respectievelijk, en k 1 is de snelheidsconstante van pseudo-eerste-orde adsorptie (min − 1 ).
Het pseudo-tweede-orde kinetische model wordt beschreven door de formule [39]:
$$ t/{q}_t=1/{k}_{ad}\ {q_e}^2+ 1/{q}_e $$ (3)Waar q e en q t zijn respectievelijk de hoeveelheid geadsorbeerde kleurstoffen op het evenwichts- en tijdstip t (mg g − 1 ); en k advertentie is de pseudo-tweede-orde snelheidsconstante voor het adsorptieproces (mg g − 1 min − 1 ). De parameterwaarden voor elk model zijn berekend op basis van de lineaire kleinste-kwadratenmethode en de correlatiecoëfficiënten zijn weergegeven in tabel 1. De resultaten toonden aan dat alle adsorptiekinetiek van deze vijf kationische kleurstoffen op Fe3 O4 /PCC MNP's kunnen goed worden beschreven door een pseudo-tweede-orde kinetiekmodel met een hoge correlatiecoëfficiënt (R 2 > 0.997) en de snelheidsconstanten (k advertentie ) werden berekend op 0,043, 0,047, 0,051, 0,057, 0,052 g mg − 1 ml − 1 , overeenkomend met respectievelijk MB, GB, MG, CV en FG (Fig. 4 en Tabel 1). Bovendien is de adsorptiecapaciteit van MB op Fe3 O4 /PCC MNP's waren significant verbeterd, vergeleken met die van Fe3 O4 MNP's (aanvullend bestand 1:figuur S1). De belangrijkste reden was de elektrostatische aantrekkingskracht tussen de positieve lading van kationische kleurstoffen en de negatieve lading van Fe3 O4 /PCC MNP's.
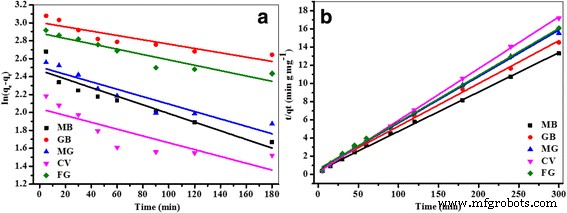
Adsorptie van kationische kleurstoffen op Fe3 O4 /PCC MNP's (a ) pseudo-tweede-orde kinetiek (b ) pseudo-eerste-orde kinetiek. Zoals weergegeven in Fig. 4, vertegenwoordigen de lege lijn de adsorptie van MB, de rode lijn de adsorptie van GB, de blauwe lijn de adsorptie van MG, de magenta representeert CV-adsorptie en de olijf is namens de adsorptie van FG
Adsorptie-isothermen van verschillende kationische kleurstoffen
De adsorptie-isotherm speelde een belangrijke rol bij het evalueren van de adsorptie-eigenschappen van Fe3 O4 /PCC MNP's [40]. Om het adsorptieproces grondig weer te geven, werden twee bekende isothermvergelijkingen, de Langmuir- en Freundlich-vergelijkingen (Vgl. (4) en (5)), toegepast [41].
Langmuir-vergelijking:
$$ {C}_e/{q}_e={C}_e/{q}_m+ 1/{K}_L\ {q}_m $$ (4)waar q e (mg g − 1 ) is de evenwichtsadsorptiecapaciteit van kleurstof op het adsorbens; C e (mg L − 1 ) is de evenwichtskleurstofconcentratie in oplossing; q m (mg g − 1 ), de maximale capaciteit van het adsorbens; en K L (L mg − 1 ), de constante van Langmuir.
Freundlich-vergelijking:
$$ {q}_e={K}_F\ {C_e}^{1/n} $$ (5)Waar q e en C e zijn gedefinieerd als hetzelfde als hierboven; K F (L mg − 1 ) is de constante van Freundlich; en n is de heterogeniteitsfactor.
Afbeelding 5 toont de adsorptie-isothermen van kationische kleurstoffen op Fe3 O4 /PCC MNP's. De resultaten gaven aan dat de adsorptie van de vijf kationische kleurstoffen volgens de correlatiecoëfficiënten allemaal beter paste bij de Langmuir-vergelijking dan bij de Freundlich-vergelijking. De maximale adsorptiecapaciteiten (q m ) voor deze kleurstoffen werden uitgewerkt met de Langmuir-vergelijking die in tabel 2 staat vermeld. De q m voor kationische kleurstoffen:MB, GB, MG, CV en FG waren 60,06, 70,97, 66,84, 66,01 en 50,27 mg g − 1 , respectievelijk. Het gefitte Langmuir-model ging ervan uit dat de enkele verontreinigende stof zich hechtte aan een enkele plaats op het adsorbens en dat alle oppervlakteplaatsen op de adsorbentia dezelfde affiniteit hadden voor verontreinigende stof en geen interacties tussen verontreinigende stof [42].
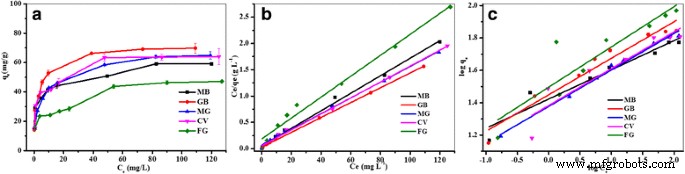
een Isothermen van kationische kleurstoffen adsorptie op Fe3 O4 /PCC MNP's (b ) Langmuir en (c ) Freundlich-adsorptie-isothermmodellen voor organische kleurstoffen door Fe3 O4 /PCC MNP's. Zoals weergegeven in Fig. 5, vertegenwoordigt de lege lijn de adsorptie van MB, de rode lijn de adsorptie van GB, de blauwe lijn de adsorptie van MG, de magenta lijn de CV-adsorptie en de olijflijn is namens de adsorptie van FG
Effect van temperatuur op de adsorptie van kationische kleurstoffen
Het effect van temperatuur op de adsorptie van kationische kleurstoffen werd getoond in Fig. 6. Zoals te zien is, nam de verwijderingsefficiëntie van MB toe met stijgende temperatuur (30-45 ° C) en bereikte deze tot 84% bij 45 ° C , wat suggereerde dat de adsorptie van MB op Fe3 O4 /PCC was een endotherm proces. Terwijl de verwijderingsefficiëntie van GB en CV afnam met stijgende temperatuur, wat wijst op een exotherme reactie voor de adsorptie van GB en CV, wat aangaf dat de sorptieprocessen voornamelijk fysieke adsorptie waren. Verder had de reactietemperatuur weinig invloed op de adsorptie van WG en FG. Het effect van de reactietemperatuur op de adsorptie van vijf kationische kleurstoffen was anders, voornamelijk vanwege de verschillende structuur van kleurstoffen en het gat van de MNP's. Wanneer de gaten van de MNP's te klein zijn om in te komen, moeten de adsorbaatmoleculen over de hoge barrière gaan om in het gat te komen. Omdat de gaten klein zijn en de diffusie wordt geblokkeerd, is het adsorptieproces onstabieler, wat resulteert in hogere energie en het proces is endotherm. Anders is het proces exotherm.
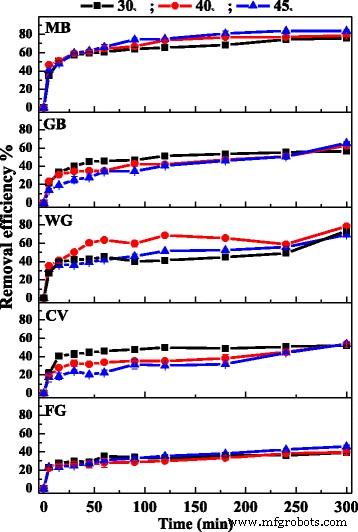
Effect van temperatuur op de adsorptie van kationische kleurstoffen op Fe3 O4 /PCC MNP's. Zoals weergegeven in Fig. 6, geeft de lege lijn aan dat de temperatuur 30 °C is, de rode lijn geeft aan dat de temperatuur 40 °C is en de blauwe lijn geeft aan dat de temperatuur 45 °C is
Effect van pH op adsorptie van kationische kleurstoffen
De pH van de waterige oplossing was een belangrijke factor die het kleurstofadsorptieproces beïnvloedt, omdat het de oppervlaktelading van een adsorbens en het ionisatiegedrag van zowel het adsorbens als de kleurstof beïnvloedde [43]. Het effect van pH op de verwijdering van kationische kleurstoffen werd bestudeerd bij een kleurstofconcentratie van 0,1 mM bij 30 °C en bij pH-waarden van 3,0 tot 9,0. Zoals getoond in Fig. 7, nam de verwijderingsefficiëntie van kationische kleurstoffen toe met toenemende pH-waarde. Omdat de Fe3 O4 /PCC MNP's hadden een negatieve lading en hun oppervlakteladingsdichtheid nam toe met hogere pH (Fig. 2c), kationische kleurstoffen werden geadsorbeerd op Fe3 O4 /PCC MNP's door de elektrostatische aantrekkingskracht tussen de positieve lading van kationische kleurstofmoleculen en de negatieve lading van Fe3 O4 /PCC MNP's. Naarmate de pH toeneemt, neemt de elektrostatische aantrekking tussen het negatief geladen oppervlak van de Fe3 O4 /PCC composiet en kationische kleurstoffen molecuul verhoogd, wat resulteert in de toename van de adsorptiecapaciteit van kationische kleurstoffen. Daarom hielp de verhoogde pH bij het verwijderen van kationische kleurstoffen door Fe3 O4 /PCC MNP's.
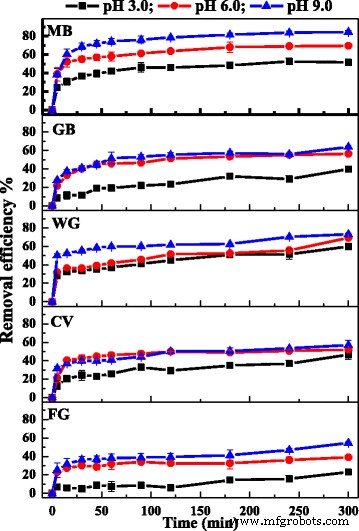
Effect van initiële pH op de verwijdering van kationische kleurstoffen op Fe3 O4 /PCC MNP's is de temperatuur 30 °C. Zoals weergegeven in Fig. 7, geeft de lege lijn aan dat de pH van de oplossing 3,0 is, de rode lijn geeft aan dat de pH van de oplossing 6,0 is en de blauwe lijn geeft aan dat de pH van de oplossing 9,0 is
Effect van naast elkaar bestaande kationen op MB-adsorptie
Kleurstofeffluenten bevatten altijd een grote verscheidenheid aan naast elkaar bestaande ionen, die het kleurstofadsorptieproces zouden kunnen beïnvloeden [4]. In deze studie werden drie vaak naast elkaar bestaande zouten, NaCl, MgSO4 en FeCl3 werden geselecteerd om het effect van naast elkaar bestaande kationen en hun ionsterkte op MB-adsorptie op Fe3 te bestuderen O4 /PCC MNP's met de resultaten weergegeven in Fig. 8. Zoals te zien is, Na + , Mg 2+ en Fe 3+ alle onderdrukten MB-adsorptie vanwege de competitie-adsorptie tussen kationen en MB op de adsorptieplaatsen van Fe3 O4 /PCC MNP's. Bovendien daalde de verwijderingsefficiëntie van MB van 63% naar 20% met Fe 3+ concentratie stijgt van 0,1 mM tot 0,5 mM. Een dergelijke competitieve adsorptie werd breed uitgemeten in de literatuur [44]. De resultaten bevestigden verder de elektrostatische adsorptie van MB op Fe3 O4 /PCC MNP's.
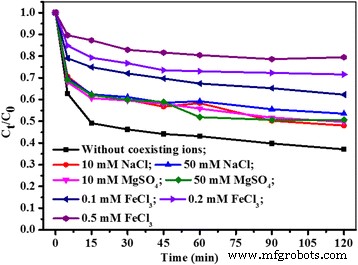
Effect van naast elkaar bestaande kationen en ionsterkte op de adsorptie van MB op Fe3 O4 /PCC MNP's. Zoals weergegeven in Fig. 8, geeft de lege lijn de adsorptie van MB weer zonder enige naast elkaar bestaande ionen, de rode lijn geeft het effect weer op MB-adsorptie met 10 mM NaCl, de blauwe lijn geeft het effect weer op MB-adsorptie met 50 mM NaCl, de magenta lijn geeft het effect op MB-adsorptie weer met 10 mM MgSO4 , de olijflijn geeft het effect op MB-adsorptie weer met 50 mM MgSO4 , de marinelijn weerspiegelt het effect op MB-adsorptie met 0,1 mM FeCl3 , de violette lijn geeft het effect op MB-adsorptie weer met 0,2 mM FeCl3 , geeft de paarse lijn het effect op MB-adsorptie weer met 0,1 mM FeCl3
Recycling van het adsorbens
Na adsorptie, Fe3 O4 /PCC MNP's kunnen gedurende 12 uur worden geregenereerd met ethanoldesorptie bij pH 4,0 en worden gewassen met gedeïoniseerd water tot een neutrale toestand. De Fe3 O4 /PCC MNP's kunnen vijf keer worden geregenereerd en hergebruikt. Afbeelding 9 toont de adsorptieprestaties van het geregenereerde Fe3 O4 /PCC MNP's voor kationische kleurstoffen. De verwijderingsefficiëntie van kationische kleurstoffen nam geleidelijk af tijdens de eerste adsorptie-desorptiecyclus tot de vijfde cyclus. Bij de zesde cyclus nam de verwijderingsefficiëntie van MB, GB, MG, CV en FG dramatisch af tot respectievelijk 27%, 23%, 37%, 43% en 39%. Met name de aanwezigheid van magnetische nanodeeltjes vergemakkelijkte de scheiding en terugwinning van het adsorbens. Het geeft aan dat de Fe3 O4 /PCC MNPs heeft een zekere economische haalbaarheid.
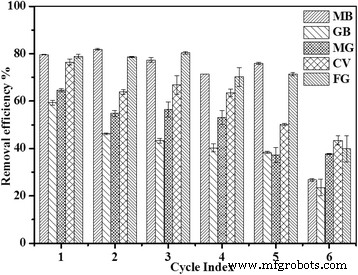
Het histogram van verwijderingsefficiëntie van kationische kleurstoffen door Fe3 O4 /PCC MNP's adsorptie ([Fe3 O4 /PCC] = 1.0 g L − 1 , [kleurstoffen]0 = 0,1 mM, pH 6,0, t = 300 min)
Conclusie
Concluderend kan een nieuw magnetisch nano-adsorbens (Fe3 O4 /PCC MNP's) werd met succes bereid met actieve adsorptieplaatsen voor het verwijderen van kationische kleurstoffen uit waterige oplossing. De introductie van polycatechol in de structuur van Fe3 O4 /PCC MNP's hadden verbazingwekkende voordelen, waaronder het voorkomen van agglomeratie van nanodeeltjes en het verbeteren van het adsorptiegedrag van de MNP's. De elektrostatische interactie bleek de belangrijkste kracht te zijn van het adsorptiegedrag van de kationische kleurstoffen. Het adsorptieproces werd goed beschreven door respectievelijk pseudo-tweede-orde kinetiek en Langmuir-isothermmodellen. De resultaten toonden aan dat Fe3 O4 /PCC MNP's toonden potentiële toepassing voor het verwijderen van kationische kleurstoffen in industrieel afvalwater.
Afkortingen
- CR:
-
Congorood
- CTAB:
-
Cetyltrimethylammoniumbromide
- Fe3 O4 /PCC:
-
Fe3 O4 /polycatechol
- Gly:
-
Glycine
- GPTMS:
-
3-glycidoxypropyltrimethoxysilaan
- MB:
-
Methyleenblauw
- MNP's:
-
Magnetische nanodeeltjes
- PCC:
-
Polycatechol
- TGA:
-
Thermogravimetrische analyse
Nanomaterialen
- Verven voor textiel
- Nanodiamanten voor magnetische sensoren
- Vooruitgang en uitdagingen van fluorescerende nanomaterialen voor synthese en biomedische toepassingen
- Eenvoudige synthese en optische eigenschappen van kleine selenium nanokristallen en nanostaafjes
- Eenvoudige synthese van heterogestructureerde WS2/Bi2MoO6 als krachtige, zichtbaar licht-gedreven fotokatalysatoren
- Eenvoudige synthese van SiO2@C-nanodeeltjes verankerd op MWNT als hoogwaardige anodematerialen voor Li-ionbatterijen
- Koolstofnanodots als dual-mode nanosensoren voor selectieve detectie van waterstofperoxide
- Onderzoek naar de sorptie van zware metalen met behulp van nanocomposieten van met ijzer gemodificeerde biochar
- Nabehandelingsmethode voor de synthese van monodisperse binaire FePt-Fe3O4-nanodeeltjes
- Magnetisch poly(N-isopropylacrylamide) nanocomposieten:effect van bereidingsmethode op antibacteriële eigenschappen
- Synthese en karakterisering van gemodificeerde BiOCl en hun toepassing bij adsorptie van kleurstoffen met een lage concentratie uit een waterige oplossing



