Bereiding van palladium(II)-ion-imprinted polymere nanosferen en de verwijdering van palladium(II) uit waterige oplossing
Abstract
Drie soorten functionele monomeren, 4-vinylpridine(4-VP), 2-(allylthio)nicotinezuur(ANA) en 2-acetamidoacrylzuur(AAA), werden gebruikt om met palladium(II)-ionen bedrukt polymere nanosferen (Pd (II) IIP's) via precipitatie-polymerisatiemethode om de effecten van verschillende functionele monomeren op de adsorptie-eigenschappen van met ionen bedrukt materiaal te bestuderen. De resultaten van UV-spectra om de interactie tussen template-ion PdCl4 . te bestuderen 2− en functionele monomeren toonden aan dat er grote verschillen in structuur waren nadat de matrijs reageerde met drie functionele monomeren, 4-VP en ANA veroorzaakten een grote structurele verandering, terwijl AAA in principe niet veranderde. Verdere resultaten over de adsorptieprestaties van Pd(II) IIP's op Pd(II) bevestigden dat 4-VP de meest veelbelovende kandidaat was voor de synthese van Pd(II) IIP's met een adsorptiecapaciteit van 5,042 mg/g in vergelijking met ANA en AAA . De invloed van bedrijfsparameters op de prestaties van Pd(II) IIP op Pd(II)-adsorptie werd onderzocht. Er was een toename in de adsorptiecapaciteit van Pd(II) IIP's bij hogere pH, temperatuur en initiële concentratie van Pd(II). De resultaten van competitieve adsorptie-experimenten met meerdere metalen toonden aan dat Pd(II) IIP's selectiviteit hadden voor Pd(II). Na 180 min kon een adsorptie-evenwicht worden bereikt. Kinetische analyse toonde aan dat de adsorptietestgegevens het beste pasten bij het pseudo-tweede-orde kinetische model, en de theoretische evenwichtsadsorptiecapaciteit was ongeveer 5,085 mg/g. De adsorptie-isothermen van Pd(II) door Pd(II) IIP's kwamen goed overeen met de Freundlich-vergelijking, wat wijst op een gunstige adsorptiereactie onder optimale omstandigheden. Deze resultaten toonden aan dat Pd(II) IIP's potentieel kunnen worden toegepast bij de verwijdering van Pd(II) uit waterige oplossingen en mogelijk enige informatie verschaffen voor de selectie van functionele monomeren bij de bereiding van Pd(II) IIP's.
Achtergrond
Palladium met unieke fysische en chemische eigenschappen wordt veel gebruikt in galvaniseermaterialen, katalysatoren, tandheelkundige legeringen en soldeerlegeringen [1, 2]. Met de toenemende toepassing van palladium op verschillende gebieden kan een aanzienlijke hoeveelheid palladiumhoudend afvalwater worden geproduceerd. De lozing van het afvalwater dat palladium bevat, kan niet alleen leiden tot ernstige verspilling van hulpbronnen, maar ook tot grote vervuiling van het milieu en schade aan de menselijke gezondheid [3,4,5,6]. Scheiding en verrijking in sommige onderzoeken kunnen deze problemen oplossen, de gebruikelijke verrijkings- en scheidingsmethoden omvatten co-precipitatie [7], adsorptie [8] en ionenuitwisseling [9], vloeistof-vloeistofextractie [10] en vastefase-extractie [11] , microvloeistofextractie [12] en troebelingspuntextractie [13]. Er zijn veel onderzoeken naar de verrijking en scheiding van palladium [14,15,16,17,18]; onder hen wordt de adsorptiemethode op veel manieren veel gebruikt omdat het eenvoudig, handig en efficiënt is. De prestaties van gebruikelijke adsorbentia omvatten actieve kool, maar zijn niet erg selectief voor het sequestreren van palladiumionen uit waterige oplossingen die verschillende metalen bevatten. Daarom is de ontwikkeling van palladiumscheidingsmateriaal met een hoge selectiviteit voor het verwijderen, terugwinnen en recyclen van palladiumionen uit de afvaloplossing van groot belang.
Met ionen bedrukt polymere nanobolletjes met hoge selectiviteit voor de scheiding van metalen uit waterige oplossing in vergelijking met andere gebruikelijke adsorbentia is de afgelopen jaren een van de onderzoekshotspots geworden [19,20,21,22,23]. Bij de bereiding van met ionen bedrukt polymere nanosferen is de stabiliteit van chelaten gevormd door functionele monomeren met verschillende functionele groepen en metaalionen door ionenbinding of coördinatiebinding afhankelijk van de interactiesterkte tussen het functionele monomeer en metaalionen, hoe sterker de interactie, hoe sterker het vermogen van met ionen bedrukt polymeer om metaalionen te cheleren en hoe groter de adsorptieprestaties. Het is dus belangrijk om functionele monomeren te selecteren [24].
Veel studies gebruikten 4-VP als het functionele monomeer bij de bereiding van Pd(II) IIP's, terwijl weinig studies betrekking hadden op de vergelijking van 4-VP met andere functionele monomeren [25,26,27,28,29,30]. In deze studie werden twee soorten ongewone functionele monomeren ANA en AAA gebruikt om te vergelijken met gewone 4-VP. De interactie tussen PdCl4 2− en functioneel monomeer werd geanalyseerd door middel van UV-scanning met volledige golflengte. Vervolgens werd het beste functionele monomeer geselecteerd door het adsorptie-effect van Pd (II) IIP's die overeenkomen met drie functionele monomeren op palladium (II) te vergelijken. Door middel van batch-adsorptie-experimenten werden de adsorptieprestaties van Pd(II) IIP's voor palladium(II)-ionen in waterige oplossingen geëvalueerd. Verschillende karakteriseringsmiddelen van FTIR, SEM en TGA werden gebruikt om het overeenkomstige mechanisme van Pd(II)-adsorptie op Pd(II) IIP's verder te onderzoeken.
Methoden
Materialen
De volgende chemicaliën K2 PdCl4 , 4-vinylpyridine (4-VP, 96%), 2-allylsulfhydryl-nicotinezuur (ANA, 98%), 2-acetamidoacrylzuur (AAA, 99%) en ethyleenglycoldimethacrylaat (EGDMA, 98%) werden gekocht van het Alfa-bedrijf in de VS. Azo-isobutyronitril (AIBN, 99%) werd gekocht bij Shanghai zhongfugang Co. Ltd. Palladium-standaardoplossing met één element werd gekocht bij het Chinese nationale standaardmateriaalnetwerk. Alle chemicaliën waren van analytische reagenskwaliteiten en werden zonder verdere modificatie gebruikt. Ultrapuur water werd gebruikt om alle oplossingen te bereiden. Al het glaswerk werd schoongemaakt en gespoeld met Milli-Q-water en vervolgens een nacht in een oven gedroogd voor gebruik.
Voorbereiding van palladium(II)-ion-imprinted polymere nanosferen
De met palladium (II) ionen bedrukt polymere nanosferen werden gesynthetiseerd door middel van een precipitatie-polymerisatiemethode. In de precipitatieprocedure werden Pd(II) IIP's bereid volgens de verhouding van de matrijs (PdCl4 2− ), functionele monomeren (4-VP, ANA, AAA) en verknopend monomeer bij 1:4:40. In de polymerisatieprocedure werd ethyleenglycoldimethacrylaat (EGDMA) gebruikt als het verknopende monomeer, het polymerisatiemengsel omvatte ook 2,2-azobisisobutyronitril (AIBN, initiator) en methanol (Porogen). De gedetailleerde werking is als volgt:
Ten eerste 0,1 mmol K2 PdCl4 werd opgelost in 20 ml methanol in een glazen kolf van 50 ml, vervolgens werd 0,4 mmol 4-VP toegevoegd en gedurende 3 uur in een thermostatische oscillator bij 25 ° C geroerd. Ten tweede werden 4 mmol EGDMA en 36,13 mg AIBN aan de glazen kolf toegevoegd en de verkregen oplossing werd overgebracht in dikwandige drukflessen. De zuurstof van de monsteroplossing werd verwijderd door gedurende 10 minuten stikstofgas door het monster te laten borrelen. Polymerisatie werd uitgevoerd in een waterbad bij 60°C gedurende 24 uur onder roeren bij 180 rpm. Het bereide polymeer werd meerdere keren gewassen met 1:4 (v /v ) methanol/water om de niet-gereageerde materialen te verwijderen, en vervolgens palladiumionen (PdCl4 2− ) werd uit het polymeermateriaal geloogd door 24 uur te roeren met 4 x 50 ml 1:1 HC1 totdat de wasoplossing vrij was van palladiumionen. Ten slotte werd het gewassen met gedeïoniseerd water totdat het een neutrale pH bereikte. De polymeren werden onder vacuüm in een exsiccator gedroogd. Op dezelfde manier werden de niet-bedrukte polymeren (NIP's) bereid, maar zonder palladiumionen te doteren.
Karakteriseringen
Ultraviolet zichtbare spectrofotometer (UV-2600, Shimadzu, Japan) werd gebruikt om de interactie tussen PdCl4 2− en functioneel monomeer. Veldemissie scanning elektronenmicroscoop (SU8040, Hitachi, Japan) werd gebruikt om de morfologieveranderingen van met ionen bedrukt polymeer voor en na elutie en niet-ionen bedrukt polymeer te observeren. Fourier-transformatie-infraroodspectra (FTIR) van de Pd(II) IIP's voor en na elutie, en NIP's werden geanalyseerd met FTIR-spectrometer (Nicolet 6700, Thermo-Nicolet, VS) met KBr-pellets in het bereik van 4000 ~ 400 cm −1 . Brunauer, Emmett, Teller's test (BET, TriStarII3020) werd gebruikt om het specifieke oppervlak te analyseren. Thermogravimetrie-analyse (TGA) werd uitgevoerd met Netzsch STA-409PC (Duitsland) van 313 tot 873 K onder een atmosfeer van gedroogde stikstof en de verwarmingssnelheid was 10 K/min.
Batch adsorptie-experimenten
De concentratie van Pd (II) werd bepaald door vlam-atomaire absorptiespectrofotometrie (FAAS, TAS-990, Persee, China). Alle batchadsorptie-experimenten werden uitgevoerd met behulp van een thermostatische oscillator bij 180 tpm met 10 mg adsorbens in een 50 ml plastic centrifugebuis met 10 ml metaaloplossing. Monsters werden in drievoud genomen voor alle batchexperimenten. Het effect van temperatuur op de adsorptie van Pd(II) op Pd(II) IIP's werd geëvalueerd bij 15, 25, 35, 45 en 55 °C. Vier interfererende metaalionen, waaronder Pt(II), Zn(II), Cu(II) en Ni(II) met een beginconcentratie van 10 mg/L, werden gekozen om het effect van meerdere metalen op de adsorptie van Pd(II) te bestuderen. .
Isotherme adsorptie-experimenten werden uitgevoerd met een constante dosering van adsorbentia en variërende concentratie van Pd(II) in het bereik van 1~80 mg/L bij 25°C (pH 2). Kinetische adsorptie-experimenten werden uitgevoerd door de oplossing met vooraf bepaalde tijdsintervallen te verzamelen (de bemonsteringstijd was ingesteld op 5, 8, 10, 15, 20, 25, 30, 40, 60, 120, 180, 240 en 300 min) en de uiteindelijke analyse te analyseren. metaalconcentratie in de waterige oplossingen.
Het verwijderingspercentage van Pd(II) en de adsorptiecapaciteit van de Pd(II) IIP's voor Pd(II)-ionen kunnen worden berekend volgens de volgende vergelijkingen:
$$ r=\left({c}_0-{c}_e\right)/{c}_0\times 100\% $$ (1) $$ q=\left({c}_0-{c}_e \right)\times V/m $$ (2)waarin r (%) is de verwijderingsefficiëntie van Pd(II), q (mg/g) is de capaciteit van Pd(II) geadsorbeerd op het adsorbens van Pd(II) IIP's, c e (mg/L) is de concentratie van Pd(II) in oplossing bij evenwicht, c 0 (mg/L) is de beginconcentratie van Pd(II) in oplossing, V (mL) is het volume van de Pd(II)-oplossing, en m (mg) is de massa van het adsorbens.
De isothermmodellen van Langmuir (Vgl. 3) en Freundlich (Vgl. 4) kunnen wiskundig worden weergegeven door de volgende vergelijkingen:
$$ \frac{c_e}{q_e}=\frac{1}{bq_m}+{c}_e\frac{1}{q_m} $$ (3) $$ \ln {q}_e=\ln {K }_f+\frac{1}{n}\times \ln {c}_e $$ (4)waar q e is de hoeveelheid Pd(II) geadsorbeerd aan adsorbentia bij evenwicht (mg/g), q m is de theoretische maximale adsorptiecapaciteit van adsorbentia onder bepaalde omstandigheden (mg/g), c e is de concentratie van Pd(II) in waterige oplossingen bij evenwicht (mg/L), b is de Langmuir-constante verbonden met de affiniteit tussen de Pd(II) en de adsorbentia (L/mg), K f is de Freundlich-constante gerelateerd aan de adsorptiecapaciteit van adsorbentia, en 1/n is de heterogeniteitsfactor variërend van 0 tot 1.
Om de dynamiek en het snelheidscontrolemechanisme voor het adsorptieproces verder te verduidelijken, werden twee veelgebruikte kinetiekmodellen, namelijk de pseudo-eerste-orde-kinetiek en de pseudo-tweede-orde-kinetiek, gebruikt om de experimentele adsorptiegegevens te simuleren. De pseudo-eerste-orde (Vgl. 5) en de pseudo-tweede-orde (Vgl. 6) kinetiek kan wiskundig worden uitgedrukt als:
$$ {q}_t={q}_e\left(1-{e}^{\left(-{k}_1t\right)}\right) $$ (5) $$ {q}_t=\frac {q_e^2{k}_2t}{1+{q}_e{k}_2t} $$ (6)waar q e is de hoeveelheid Pd(II) geadsorbeerd aan adsorbentia bij evenwicht (mg/g), t is de contacttijd tijdens het adsorptieproces, q t is de hoeveelheid Pd(II) geadsorbeerd op adsorbentia op enig moment t (mg/g), k1 is de snelheidsconstante van het pseudo-eerste-orde-model (min −1 ), en k 2 is de snelheidsconstante van het pseudo-tweede-ordemodel (g/mg min).
Resultaten en discussie
De optimalisatie van functioneel monomeer
De UV-spectra van PdCl4 2− en 4-VP, en ANA en AAA in methanol voor en na de interactie worden getoond in Fig. 1. Uit de figuur is te zien dat PdCl4 2− heeft twee absorptiepieken bij 219,4 en 242,4 nm, en de absorptiepieken worden verschoven wanneer verschillende functionele monomeren worden toegevoegd. Wanneer functioneel monomeer van 4-VP wordt gedoseerd (Fig. 1a), is er een hypochroom effect op PdCl4 2− verscheen bij 219,4 en 242,4 nm, en een nieuwe absorptiepiek vormde zich rond 275 nm als gevolg van hyperchroom effect vergeleken met die bij 219,4 nm, wat duidt op de duidelijke veranderingen in de structuur van PdCl4 2− en 4-VP in de buurt van 275 nm. Toen ANA werd toegevoegd in PdCl4 2− methanoloplossing als functioneel monomeer (Fig. 1b), PdCl4 2− verscheen roodverschuivingsverschijnsel bij 219,4 en 242,4 nm, en twee nieuwe absorptiepieken ontstonden in de buurt van 285 en 347 nm in vergelijking met de absorptiepiek bij 219,4 nm, de twee nieuw gevormde pieken kunnen worden toegeschreven aan het hypochrome effect, wat aangeeft dat beide PdCl4 2− en ANA hebben enig verschil in hun structuren in de buurt van 285 en 347 nm. Uit figuur 1c blijkt dat de toevoeging van AAA geen roodverschuiving of blauwverschuiving geeft aan de absorptiepiek van PdCl4 2− bij zowel 219,4 als 242,4 nm, en er is geen nieuwe absorptiepiek, wat wijst op de verwaarloosbare verandering in de structuur van PdCl4 2− en AAA.
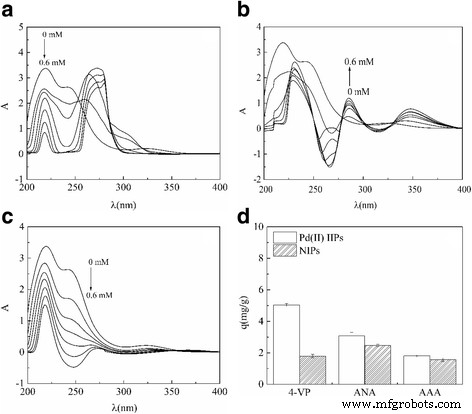
Ultraviolette spectra van de interacties tussen PdCl4 2− en (een ) 4-VP, (b ) ANA, (c ) AAA in methanol en (d ) adsorptie-eigenschappen van Pd(II) IIP's gesynthetiseerd door verschillende functiemonomeren
Om het adsorptie-effect van Pd(II) op Pd(II) IIP's en NIP's bereid door 4-VP, ANA en AAA verder te bestuderen, werd de adsorptie van Pd(II) op elk materiaal gemeten. Zoals getoond in Fig. 1d, was de hoeveelheid Pd(II)-ionen geadsorbeerd op Pd(II) IIP's groter dan die op de overeenkomstige NIP's. Bovendien werd volgens de BET-methode het oppervlak van IIP's en NIP's berekend (Tabel.1):het oppervlak van IIP's bereid door 4-VP is 23,74 m 2 /g overschrijdt NIP's (0,46 m 2 /G). Het betekent dat een soort polymere nanosferen Pd(II) IIP's met een groter oppervlak werd geproduceerd na toevoeging van het ingeprinte ion. Deze waarneming kan worden geïnterpreteerd door de significante verschillen in de ruimtelijke structuur van Pd(II) IIP's en NIP's met dezelfde soort functionele monomeren. Tijdens het proces van de vorming van Pd(II) IIP's vormden het functionele monomeer en het Pd(II)-ion, als gevolg van de toevoeging van bedrukt Pd(II)-ion een coördinatiecomplex met de inprentingsholten en het gat van het Pd(II)-ion. ) ion presenteert een "geheugen", wat leidt tot meer adsorptiehoeveelheid Pd(II)-ionen op Pd(II) IIP's dan op NIP's. Bovendien liet Tabel 1 zien dat de Pd(II)-adsorptiecapaciteit van de drie soorten polymeren toenam met een volgorde als 4-VP> ANA> AAA, wat aangeeft dat de Pd(II) IIP's bereid door 4-VP de beste waren. De resultaten werden veroorzaakt door de lone pair elektronen van N-atomen in de structuur van 4-VP die niet alleen kunnen worden gecheleerd met metaalionen, maar ook waterstofbruggen kunnen vormen met functionele groepen zoals carboxyl- en hydroxylgroepen. Bovendien kunnen de vinylgroepen in de structuur reageren met het verknopingsmiddel, zodat het atoom N aan de keten van het polymeer wordt gehangen om een zwak alkalisch polyelektrolyt te vormen.
Door de structuur van deze drie soorten functionele monomeren (figuur 2) en de adsorptietestresultaten te vergelijken, ontdekten we dat het adsorptie-effect van 4-VP-bevattende stikstofheterocycli het beste was, gevolgd door ANA dat zowel stikstofheterocycli als carboxylgroepen bevat, en het ergste was AAA dat carboxylgroepen bevatte. Daarom speculeerden we dat de binding van Pd(II)-ionen en functionele monomeren die stikstofheterocycli bevatten sterker zijn dan die met carboxylgroepen, en dat de aanwezigheid van carboxylgroepen de binding van Pd(II)-ionen en functionele monomeren die beide stikstofheterocycli bevatten, kan verzwakken. en carboxylgroepen.
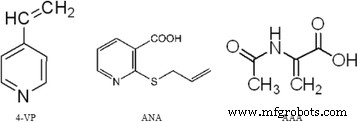
Structuurformule van drie functionele monomeren
De Pd(II) IIP's die in de volgende onderzoeken worden genoemd, zijn allemaal bereid met 4-VP als het functionele monomeer.
Kenmerken van Pd(II) IIP's en NIP's
De microscopische morfologie van uitgeloogde Pd(II) IIP's, niet-uitgeloogde Pd(II) IIP's en NIP's werd waargenomen. Uit Fig. 3a, d blijkt dat er geen veranderingen zijn in de morfologie van noch niet-uitgeloogde Pd(II) IIP's noch uitgeloogde Pd(II) IIP's; bovendien toonde de BET-methode aan dat het specifieke oppervlak van Pd(II) IIP's (23,74 m 2 /g) was vergelijkbaar met de ongeloogde Pd(II) IIP's (22,49 m 2 /g), kan het kleine verschil worden genegeerd, zodat kan worden geconcludeerd dat de elutie geen effect heeft op de morfologie van de Pd(II) IIP's. Het oppervlak van het polymeer wordt relatief ruw na toevoeging van het PdCl4 2− sjabloon, wat te wijten is aan de vorming van bedrukte gaten. Ter vergelijking:de NIP's vertonen een gladder oppervlak (Fig. 3e) met een veel grotere deeltjesgrootte van 2 m dan die van niet-uitgeloogde Pd(II) IIP's en uitgeloogde Pd(II) IIP's (ongeveer 200 nm) onder dezelfde vergroting. Deze bevinding gaf aan dat de toevoeging van template PdCl4 2− oefent een grote invloed uit op de morfologische eigenschappen van met palladium(II)-ionen bedrukt polymeer.

SEM van (een ) 4-VP - uitgeloogde IIP's, (b )ANA - uitgeloogde Pd(II) IIP's, (c ) AAA-uitgeloogde Pd(II) IIP's, (d ) 4-VP - Unleached IIP's, (e ) 4-VP - uitgeloogde NIP's. (Alle afbeeldingen onder dezelfde vergroting in 20.000X)
Verschillend ontledingsgedrag kan worden waargenomen aan de hand van de thermogravimetrische curven van niet-uitgeloogde Pd (II) IIP's, uitgeloogde Pd (II) IIP's en NIP's (figuur 4a). Bij een lagere temperatuur van 40 ~ 100 ° C is de thermische ontledingssnelheid relatief laag. Het gewichtsverlies wordt voornamelijk toegeschreven aan de verdamping van vrije en/of gebonden watermoleculen. De belangrijkste samenstelling van monsters is nog niet begonnen met ontleden bij een temperatuur van 100~250 °C. Bij een temperatuur hoger dan 250 °C beginnen de monsters snel af te vallen; dit komt voornamelijk door de ontleding van organische stoffen in de polymeren met toenemende temperatuur. Toen de temperatuur tot boven 440 ° C steeg, zijn de organische stoffen in de polymeren volledig ontleed, waardoor een staat van thermische stabiliteit is bereikt. Wanneer de temperatuur tot 600 ° C stijgt, komt het residumassapercentage van ongeloogde Pd(II) IIP's uit op ongeveer 6%. De reststoffen zouden voornamelijk uit anorganisch palladium bestaan.
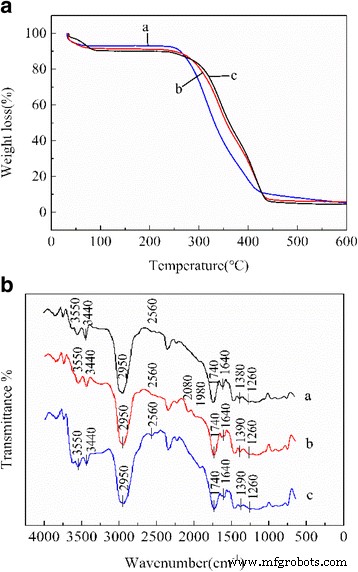
een TGA-curven van a:niet-uitgeloogde Pd(II) IIP's, b:uitgeloogde Pd(II) IIP's, c:NIP's; (b ) FTIR-spectra van a:niet-uitgeloogde Pd(II) IIP's, b:uitgeloogde Pd(II) IIP's, c:NIP's
Op basis van de absorptiepieken en banden op FTIR-spectra kunnen veel functionele groepen op het oppervlak van absorberend materiaal worden afgebeeld en gekarakteriseerd voor niet-uitgeloogde Pd (II) IIP's, uitgeloogde Pd (II) IIP's en NIP's (figuur 4b). Uit de figuur blijkt dat de banden die zijn waargenomen op 3440 en 1640 cm −1 worden toegewezen aan de strektrillingsfrequentie van respectievelijk C-N en -CONH- in amide. De pieken op 3550, 2950, 2560, 2350, 1740 en 1260 cm −1 worden toegeschreven aan de strektrillingsfrequentie van respectievelijk −OH, C-H, S-H, C=O in esters en C-O. Er is geen verschuiving tussen deze trillingsabsorptiepieken in de drie FTIR-curven vanwege geen coördinatie. Zoals weergegeven in curve b en curve c, verschoof de piek toegeschreven aan C-N van 1390 naar 1380 cm −1 na toevoeging van matrijsion Pd(II), wat aangeeft dat de coördinatie plaatsvond tussen het matrijsion Pd(II) en functioneel monomeer. Bovendien verschenen er nieuwe absorptiepieken op 2080 en 1980 cm −1 in curve b kan worden veroorzaakt door het elutieproces van Pd(II) wat kan leiden tot enkele veranderingen in groepen.
Batch adsorptie-experimenten
Het effect van de initiële concentratie van Pd(II)-ionen op de adsorptiecapaciteit van Pd(II)IIP's wordt getoond in figuur 5a. Wanneer de dosering van Pd(II) IIP's vastligt, neemt de adsorptiecapaciteit van Pd(II) IIP's voor Pd(II)-ionen toe met de toenemende initiële concentratie van adsorbationen, terwijl de verwijderingsefficiëntie dienovereenkomstig afneemt. Dit komt door de beperkte adsorptieplaatsen die worden geboden door Pd (II) IIP's in oplossing. Bij een lagere Pd(II)-concentratie is de hoeveelheid actieve adsorptieplaatsen overvloedig om de meeste Pd(II)-ionen in oplossing te absorberen. Naarmate de initiële concentratie van Pd(II)-ionen toenam, werd het beschikbare aantal actieve adsorptieplaatsen echter beperkt door de vaste dosering van het adsorbens. Er zijn geen verdere actieve plaatsen om de overtollige Pd(II)-ionen bij hogere concentratie te combineren. Samen met de geleidelijke verzadiging van de adsorptiecapaciteit van Pd(II) IIP's, is er een constante afname van de efficiëntie van Pd(II)-verwijdering.
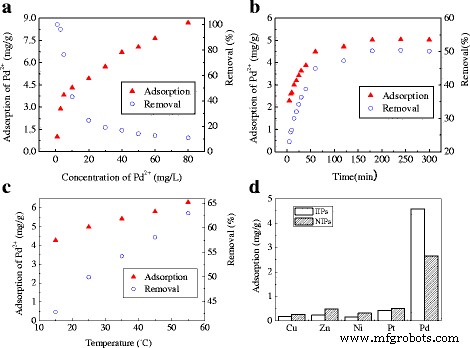
Effecten van (a ) aanvankelijke concentratie, (b ) contacttijd, (c ) temperatuur en (d ) meerdere metalen bij adsorptie van Pd(II) op Pd(II) IIP's
Het effect van contacttijd op adsorptiecapaciteit en verwijderingsefficiëntie van Pd (II) IIP's voor Pd (II) -ionen wordt getoond in Fig. 5b. In een vroege testperiode van 60 minuten nemen zowel de adsorptiecapaciteit als de verwijderingsefficiëntie van Pd(II) IIP's voor Pd(II) snel toe naarmate de contacttijd van de reactie langer wordt. Helemaal aan het begin van de reactie is een groot aantal bindingsplaatsen beschikbaar op Pd(II) IIP's voor Pd(II)-adsorptie, samen met de relatief hoge concentratie van Pd(II)-ionen, bestaat er een sterke drijvende kracht om de massa te bevorderen overdracht van adsorbationen van bulkoplossing naar de onbezette bindingsplaatsen. Als gevolg hiervan is het bevorderlijk voor Pd(II) IIP's die fungeren als een efficiënt adsorbens om in de eerste 3 uur zware metalen uit afvalwater te verwijderen. Naarmate de contacttijd echter langer werd, namen de meeste actieve plaatsen van Pd(II) IIP's in combinatie met Pd(II)-ionen af en namen de beschikbare actieve plaatsen af. Na 180 min blijven de adsorptiecapaciteit en verwijderingsefficiëntie van Pd(II) IIP's onveranderd en bereikt een evenwichtstoestand. Daarom werd 180 min ingesteld als de optimale contacttijd voor het adsorptieproces.
Afbeelding 5c geeft het effect weer van de bedrijfstemperatuur op de adsorptiecapaciteit en verwijderingsefficiëntie van Pd(II) IIP's voor Pd(II). We ontdekten dat de adsorptiecapaciteit en verwijderingsefficiëntie van Pd(II) IIP's voor Pd(II) toeneemt met de temperatuurstijging, wat wijst op een endotherm proces voor de adsorptiereactie. Een hogere temperatuur is gunstig om de adsorptiecapaciteit van absorptiemiddelen te bevorderen. Over het algemeen kunnen Pd(II) IIP's bij een normale technische temperatuur tussen 25 en 35 °C goede prestaties leveren in praktische toepassingen.
De invloed van meerdere metalen op de adsorptie van Pd (II) door Pd (II) IIP's en NIP's wordt getoond in Fig. 5d. In het naast elkaar bestaande systeem van meerdere metalen is de adsorptiecapaciteit van Pd(II) IIP's en de bijbehorende NIP's op Pd(II) het grootst, gevolgd door Pt, Zn, Ni en Cu. De adsorptiecapaciteit van Pd(II) IIP's op Pd(II) was respectievelijk 26,7, 21,5, 31,8 en 10,4 keer hoger dan die van Cu(II), Zn(II), Ni(II) en Pt(II). . De resultaten gaven aan dat Pd (II) IIP's zeer efficiënt en selectief waren voor Pd (II). De adsorptiecapaciteit van Pd(II) IIP's op Pt(II) was groter dan die op Cu(II), Zn(II) en Ni(II), mogelijk vanwege de chemische gelijkenis van Pt(II) met Pd( II) en concurrerende adsorptieplaatsen vergeleken met andere metalen. De adsorptiecapaciteit van NIP's op Cu(II), Zn(II), Ni(II) en Pt(II) was groter dan die van Pd(II) IIP's, terwijl Pd(II) precies het tegenovergestelde is, wat aangeeft dat beter adsorptie-effect van Pd(II) IIP's op Pd(II) dan dat van NIP's wordt niet veroorzaakt door een groot specifiek gebied, maar door de vorming van de herkenningsadsorptieplaatsen voor Pd(II) in het bereidingsproces.
Isotherme en kinetische studies
Om het adsorptievermogen van Pd (II) IIP's te onderzoeken, werden twee typische adsorptie-isothermmodellen, d.w.z. de Langmuir- en Freundlich-adsorptie-isothermmodellen (figuur 6a), gebruikt om het adsorptiemechanisme te onderzoeken. De experimentele gegevens worden vervolgens uitgerust met de pseudo-eerste-orde en de pseudo-tweede-orde kinetische modellen (figuur 6b). De isotherme en kinetische parameters voor de respectievelijke modellen zijn samengevat in tabel 2.
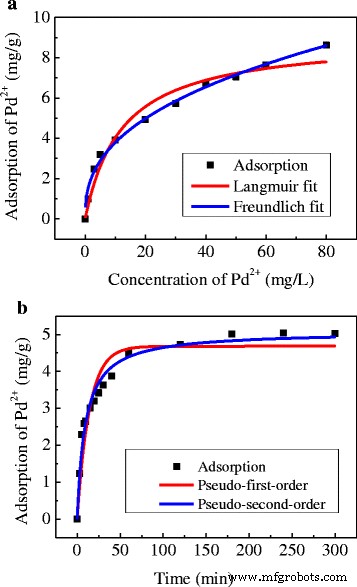
een Adsorptie isotherm en (b ) kinetische aanpassingscurven van Pd(II) op Pd(II) IIP's
In de isothermstudie is de correlatiecoëfficiënt van het Freundlich-isothermmodel (R ^2 = 0.991) is veel dichter bij 1 in vergelijking met dat van het Langmuire-model (R ^2 = 0.946), wat suggereert dat het Freundlich-isothermmodel geschikter is om het adsorptieproces van Pd(II)-ionen op Pd(II) IIP's te beschrijven. Freundlich-model is een empirische vergelijking, algemeen wordt aangenomen dat het omgekeerde van de constante van Freundlich n is negatief gecorreleerd met de adsorptieprestatie [27]. Wanneer 1/n is tussen 0,1 ~ 0,5, het is gemakkelijk te adsorberen; wanneer 1/n groter is dan 2, is het moeilijk te adsorberen. De 1/n waarde verkregen uit dit experiment is ongeveer 0,39, wat aangeeft dat Pd(II)-ionen gemakkelijk kunnen worden geadsorbeerd door Pd(II) IIP's.
In de kinetische studie komt het fittingresultaat beter overeen met het pseudo-tweede-orde kinetische model (R 2 = 0.971) dan met het pseudo-eerste-orde kinetische model (R 2 =0,896). Met een theoretische evenwichtsadsorptiecapaciteit van 5,085 mg/g die dichter bij de experimentele waarde van 5,042 mg/g ligt, wordt de adsorptie van Pd(II)-ionen op Pd(II)-IIP's geacht meer in overeenstemming te zijn met de pseudo-seconde -Order kinetisch model. Het pseudo-tweede-orde kinetische model gaat ervan uit dat de snelheidsregulerende stappen voornamelijk chemische adsorptieprocessen zijn tussen zware metaalionen en de adsorptieplaatsen op absorbentia [31]. Daarom wordt de adsorptie van Pd(II)-ionen op Pd(II) IIP's voornamelijk bijgedragen door chemische reacties, waardoor de vorming van ingeprinte herkenningsplaatsen wordt bevestigd.
Conclusie
Studies naar drie soorten functionele monomeren tijdens de synthese van Pd(II) IIP's lieten significant verschillende imprinting-effecten zien. De UV-spectra toonden aan dat 4-VP en ANA een grote structurele verandering veroorzaakten nadat de template reageerde met drie functionele monomeren, terwijl AAA in principe niet veranderde. Volgens de batch-adsorptie-experimenten presteerde 4-VP als het meest veelbelovende kandidaat-functionele monomeer met een hogere Pd(II)-adsorptiecapaciteit dan ANA en AAA. De vorming van ingeprinte herkenningsplaatsen, wat gunstig was voor de adsorptie van Pd (II) IIP's voor Pd (II) -ionen, werd aangetoond door de FTIR-spectra. Onder optimale werkomstandigheden werd een theoretische evenwichtsadsorptiecapaciteit van 5,085 mg/g verkregen voor Pd(II)-ionen door de gesynthetiseerde Pd(II) IIP's. Vergeleken met Cu(II), Zn(II), Ni(II) en Pt(II), vertoonden Pd(II) IIP's een hoge selectiviteit voor Pd(II)-ionen. De isotherme resultaten suggereerden dat het Freundlich-isothermmodel een betere pasvorm voor het adsorptieproces van Pd(II) op Pd(II) IIP's aantoonde dan het Langmuir-isothermmodel. Kinetische studies hebben aangetoond dat het adsorptieproces het best kan worden beschreven met het pseudo-tweede-orde kinetische model.
Afkortingen
- 4-VP:
-
4-Vinylpridine
- AAA:
-
2-Acetamidoacrylzuur
- ANA:
-
2-(allylthio)nicotinezuur
- BET:
-
(Brunauer, Emmett, Teller's test)
- FAAS:
-
Vlam atomaire absorptiespectrofotometrie
- FTIR:
-
Fourier-transformatie infraroodspectroscopie
- NIP's:
-
Niet-ion-geprinte polymere nanobolletjes
- Pd(II) IIP's:
-
Met palladium(II)-ionen bedrukt polymere nanobolletjes
- SEM:
-
Veldemissie scanning elektronenmicroscoop
- TGA:
-
Thermogravimetrie-analyses
- UV:
-
Ultraviolet zichtbaar
Nanomaterialen
- Adsorberende verwijdering van koper(II)-ionen uit waterige oplossing met behulp van een magnetiet nano-adsorbens uit afval van walshuid:synthese, karakterisering, adsorptie en kinetische modellering O…
- Preparatie en magnetische eigenschappen van kobalt-gedoteerde FeMn2O4-spinel-nanodeeltjes
- Op weg naar TiO2-nanovloeistoffen:deel 1:voorbereiding en eigenschappen
- Bereiding van aluminiumoxide nanostaafjes uit chroomhoudend aluminiumoxide slib
- De voorbereiding van Au@TiO2 Yolk–Shell Nanostructure en zijn toepassingen voor afbraak en detectie van methyleenblauw
- Voorbereiding en fotokatalytische prestaties van LiNb3O8-fotokatalysatoren met holle structuur
- Synthese en karakterisering van gemodificeerde BiOCl en hun toepassing bij adsorptie van kleurstoffen met een lage concentratie uit een waterige oplossing
- Voorbereiding van hiërarchische poreuze Silicalite-1 ingekapselde Ag NP's en zijn katalytische prestaties voor 4-nitrofenolreductie
- Verwijdering van antibiotica uit water met een koolstofvrij 3D-nanofiltratiemembraan
- Een hydrothermische synthese van Fe3O4@C hybride nanodeeltjes en magnetische adsorptieprestaties om zware metaalionen in waterige oplossing te verwijderen
- Bereiding van glycyrrhetinezuur-liposomen met behulp van vriesdrogen Monofase-oplossingsmethode:voorformulering, optimalisatie en in-vitro-evaluatie



