De effecten van Li/Nb-verhouding op de voorbereiding en fotokatalytische prestaties van Li-Nb-O-verbindingen
Abstract
De effecten van de Li/Nb-verhouding op de bereiding van Li-Nb-O-verbindingen door middel van een hydrothermische methode werden diepgaand bestudeerd. Li/Nb-verhouding heeft een grote invloed op de vorming van LiNbO3; de verhouding kleiner dan 3:1 is gunstig voor de vorming van LiNbO3 , hoewel groter dan 3:1, vormt geen LiNbO3 helemaal niet en de morfologie en chemische binding van Nb2 O5 grondstof zijn totaal gewijzigd door Li ionen. De reden kan worden toegeschreven aan het grote gehalte aan LiOH, wat gunstig is voor de vorming van Li3 NbO4 niet LiNbO3 , en ook, zelfs als LiNbO3 deeltje vormt zich lokaal, het wordt gemakkelijk opgelost in LiOH-oplossing met een sterke alkaliteit. Pure LiNb3 O8 poeders worden verkregen met twee absoluut tegengestelde Li/Nb-verhoudingen:8:1 en 1:3; de eerste vertoont een unieke poreuze en holle structuur, heel anders dan de deeltjesaggregatie (de laatste vertoont). Vergeleken met Li/Nb = 1:3, de 4,2 keer hogere fotokatalytische prestatie van LiNb3 O8 (Li/Nb = 8:1) worden waargenomen en dit kan worden toegeschreven aan de unieke poreuze en holle structuur, die zorgt voor een hoge dichtheid aan actieve plaatsen voor de afbraak van MB. Vergeleken met LiNbO3 , de verbeterde fotokatalytische prestaties van LiNb3 O8 kan worden toegeschreven aan het gelaagde structuurtype met de verminderde symmetrie die de scheiding van elektronen en gaten verbetert.
Achtergrond
Niobiumverbindingen, een zeer veelzijdige groep materialen, waaronder niobiumoxiden, alkaliniobaten en columbietniobaten, vertonen veel interessante fysische eigenschappen en zijn op veel gebieden uitgebreid bestudeerd, zoals katalyse [1,2,3], memristors [4] , kleurstofgevoelige zonnecellen [5], optische apparaten en andere [6, 7]. LiNbO3 , als een van de meest bekende alkaliniobaten, presenteert prominente eigenschappen zoals elektro-optisch en niet-lineair optisch gedrag, pyro-elektriciteit en piëzo-elektriciteit, en het wordt voornamelijk gebruikt als optische modulatoren, golfgeleiders, akoestische golftransducers, et al. in optische apparaten.
Voor milieusanering en schone energietoepassingen, niobaten, zoals (Na, K)NbO3 [8], BiNbO4 [9], LiNbO3 [10], en LiNb3 O8 [11], zijn grondig onderzocht vanwege hun speciale vervormde [NbO6 ] octaëdrische structuren die een mogelijke delokalisatie van ladingsdragers bevorderen [12]. Ten tweede, de geleidingsbanden bestaande uit Nb4d-orbitalen die zich in een meer negatieve staat van redoxpotentiaal van H+/H2 bevinden bevorderen de scheiding en overdracht van foto-geïnduceerde ladingsdragers en resulteren in hoge fotokatalytische activiteiten [13]. Van deze materialen is LiNb3 O8 unieke optredens laat zien. Als een nieuw lithium-ionbatterij (LIB) anodemateriaal, is de theoretische capaciteit van LiNb3 O8 is 389 mAh/g uitgaande van overdracht van twee elektronen (Nb 5+ → Nb 3+ ), groter dan veel andere anodematerialen, zoals Li4 Ti5 O12 [14, 15]. Gebruikt voor apparaten met supercondensatoren, LiNb3 O8 nanovlokken vertonen een uitstekende cyclusstabiliteit met een verwaarloosbare afname van de specifieke capaciteit, zelfs na 15.000 cycli [16]. Het wordt ook gebruikt als een efficiënte fotokatalysator bij de toepassingen van waterstofopwekking en afbraak van organische verontreinigende stoffen. Pure LiNb3 O8 is een zeer actieve UV-fotokatalysator voor waterreductie die 83,87 μmol waterstof produceert in 1 uur, en het produceert geen waterstof onder bestraling met zichtbaar licht vanwege de grote bandafstand (dwz 3,9 eV) en het onvermogen om zichtbaar licht te absorberen [17 , 18]. LiNb3 O8 nanovlokken vertonen snelle ontkleuring van toluidineblauw O (TBO) kleurstof onder UV-licht in vergelijking met commercieel TiO2 poeders [13].
Meestal is het uiterlijk van LiNb3 O8 wordt herkend als een onzuiverheidsfase tijdens de bereiding van LiNbO3 , vooral in filmmonsters, vanwege de hoge gloeitemperatuur of inhomogene verdeling van Li-element in voorlopers [19, 20]. Vanwege de moeilijkheid om een zuivere fase te bereiden, is LiNb3 O8 is zelden onderzocht, terwijl voor LiNbO3 poeders, de bereidingstechnologieën zijn divers, zoals sol-gel [19], hydrothermale [21] en laserbestralingsmethoden [22]. Hydrothermische methode wordt veel gebruikt om nanomaterialen te synthetiseren met voordelen zoals lage temperatuur, milieuvriendelijkheid en homogene deeltjesgrootteverdeling, die de variatie van de Li / Nb-molverhouding efficiënt kan vermijden zonder door hoge temperaturen te gaan. Wat de hydrothermische methode betreft, spelen de parameters van reactietemperatuur, grondstofverhouding en houdtijd een belangrijke rol bij het bepalen van de verkregen materialen, terwijl het onderzoek naar de Li / Nb-verhouding veel groter dan 1:1 bij de bereiding van Li-Nb -O verbindingen zijn niet eerder gerapporteerd.
In dit artikel werden de effecten van de Li/Nb-verhouding op de bereiding van Li-Nb-O-verbindingen door een hydrothermische methode diepgaand bestudeerd. Een reeks analytische technieken werd gebruikt om de kristalliniteit, morfologie en chemische samenstelling van de Li-Nb-O-monsters te karakteriseren, met name de veranderingen voor en na de hydrothermische reactie. Pure LiNb3 O8 en LiNbO3 fotokatalysatoren werden voorbereid en de fotokatalytische prestaties werden bestudeerd met het effect van de Li/Nb-verhouding in grondstoffen.
Methoden
De bereiding van Li-Nb-O-verbindingen werd uitgevoerd door de hydrothermische methode met lithiumhydroxide-monohydraat (LiOH·H2 O; Aladdin, ACS, ≥ 98,0%) en niobiumpentaoxide (Nb2 O5; Aladdin, AR, 99,9%) als uitgangsmaterialen. Ten eerste 3,5 mmol Nb2 O5 werd gedispergeerd in 35 ml gedeïoniseerd water met een bepaalde hoeveelheid LiOH·H2 O onder magnetisch roeren. De molverhoudingen van Li:Nb zijn 1:3, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1 en 8:1; aangezien de resultaten van de monsters die zijn bereid met verhoudingen van 4:1, 5:1, 6:1 en 7:1 vergelijkbaar zijn, worden hieronder alleen de verhoudingen van Li:Nb =4:1 en 7:1 weergegeven. De suspensieoplossingen werden in 50 ml met Teflon beklede autoclaafreactoren voor hydrothermale synthese gedaan en 24 uur op 260 ° C gehouden, daarna op natuurlijke wijze afgekoeld tot kamertemperatuur. De verkregen poeders werden vervolgens meerdere keren gewassen met gedeïoniseerd water en ethanol en gedroogd bij 60°C. Ten slotte werden de producten gedurende 2 uur bij verschillende temperaturen van 500 tot 800 °C gecalcineerd met een snelheid van 5 °C/min.
De röntgendiffractie (XRD) patronen werden geregistreerd met behulp van een Bruker D8 Discover diffractometer met Cu Kα straling (40 kV, 40 mA). De morfologieën van de monsters werden gekarakteriseerd door veldemissie scanning elektronenmicroscoop (FESEM; JSM-6700F). Chemische bindingen werden geanalyseerd met Fourier-getransformeerde infraroodspectroscopie (FTIR) in het bereik van 2000-650 cm −1 . Röntgenfoto-elektronspectroscopie (XPS) -analyse werd uitgevoerd op een Thermo-Fisher Escalab 250Xi-instrument om de chemische component van Li-Nb-O-verbindingen te karakteriseren. Het specifieke oppervlak werd gemeten op een oppervlakteapparaat (Micromeritics ASAP 2460) bij 77 K door N2 adsorptie/desorptiemethode (BET-methode). De fotoluminescentie (PL) spectra werden gedetecteerd met behulp van een F-280 fluorescentie spectrofotometer met een excitatiegolflengte van 320 nm.
Om de fotokatalytische prestaties van Li-Nb-O-verbindingen te evalueren, werd de afbraak van methyleenblauw (MB) waterige oplossing (5 mg/L) uitgevoerd onder bestraling van een 500 W Hg-lamp bij een natuurlijke pH-waarde. Vijftig milligram poeders werd gedispergeerd in 50 ml MB-waterige oplossing. Vóór de bestraling werd de suspensie 1 uur in het donker geroerd om het adsorptie-evenwicht te bereiken. Vervolgens werd de suspensie bestraald door de Hg-lamp. De concentratie van resterende MB werd geanalyseerd met een interval van 30 minuten met behulp van een ultraviolet-zichtbare nabij-infrarood (UV-vis-NIR) spectrofotometer bij 665 nm.
Resultaten en discussie
De XRD-patronen van de producten verkregen na hydrothermische reactie met verschillende Li/Nb-molverhoudingen worden getoond in Fig. 1. Het is duidelijk dat zuivere LiNbO3 fase (JCPDF, nr. 20-0631) wordt verkregen met Li:Nb = 2:1. Voor de verhouding Li/Nb kleiner dan 2:1, zoals 1:1 of 1:3, is de hoofdfase nog steeds LiNbO3 , vergezeld van het residu van Nb2 O5 (JCPDF, nr. 37-1468), wat betekent dat het Li-gehalte niet voldoende is om volledig te reageren met Nb2 O5 om LiNbO3 . te vormen . Wanneer we het Li-gehalte grotendeels verhogen, doet zich een verbazingwekkend fenomeen voor:er is geen LiNbO3 helemaal gevormd na de hydrothermische reactie, zoals duidelijk wordt getoond in Fig. 1. Wanneer de verhouding van Li/Nb 4:1 of groter is, alleen Nb2 O5 fase bestaat in XRD-patronen, geen andere onzuiverheden gedetecteerd. Wordt het Li-ion weggespoeld tijdens het wasproces? Net zoals de vroegere literatuur vermeldde [23].
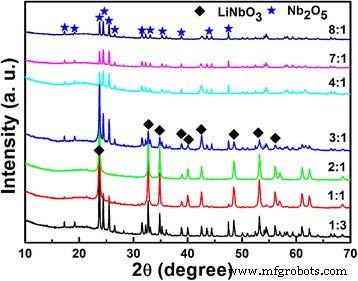
XRD-patronen van de Li-Nb-O-poeders verkregen na hydrothermische reactie met verschillende Li/Nb-molverhoudingen
Om de fase-evolutie te illustreren wanneer de Li/Nb-verhouding groot genoeg is, worden de producten verkregen door de hydrothermische methode, waarbij Li/Nb =8:1 als voorbeeld wordt gebruikt, gecalcineerd bij verschillende temperaturen en de XRD-patronen worden getoond in Fig. 2 Wanneer de producten worden gecalcineerd bij 500 en 600 °C, wordt een nieuwe fase LiNbO3 verschijnt, wat aantoont dat er echt een Li-element bestaat in de producten die net na de hydrothermische reactie zijn verkregen, hoewel niet gedetecteerd door XRD. Ook verschijnt er een diffractiepiek bij 30,26° bij 600 °C, die kan worden geïndexeerd als (410) vlak van monokliene LiNb3 O8 . De reactie kan worden beschreven door de volgende vergelijking. (1) [24]:
$$ {\mathrm{LiNb}\mathrm{O}}_3+{\mathrm{Nb}}_2{\mathrm{O}}_5\to {\mathrm{LiNb}}_3{\mathrm{O}}_8 $ $ (1)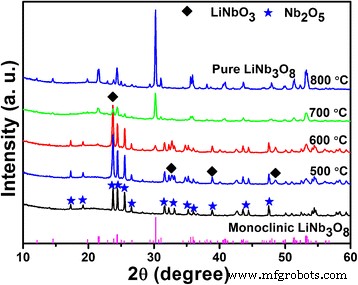
XRD-patronen van de Li-Nb-O-poeders (molverhouding van Li:Nb =8:1) gecalcineerd bij verschillende temperaturen gedurende 2 uur
Bij 700 °C is de monokliene LiNb3 O8 is de overheersende fase met een bijna verwaarloosbare onzuiverheid. De pure fase van LiNb3 O8 wordt verkregen bij 800 °C met alle diffractiepieken geïndexeerd op de monokliene fase (JCPDF, nr. 36-0307), een ruimtegroep van P21/a, die een nieuwe manier biedt om LiNb3 te bereiden O8 verbindingen.
Er wordt ook een FTIR-test uitgevoerd om de fase-evolutie van de producten met Li:Nb = 8:1 te bestuderen, zoals weergegeven in Fig. 3. De grondstof Nb2 O5 wordt getest als referentie. In Fig. 3, de band op 962 cm −1 vanwege de uitrekkende trillingen van Nb = O in Nb2 O5 bestaat tot 700 °C [25]. Na hydrothermische reactie zijn er geen andere banden gedetecteerd in dit bereik, wat betekent dat het enige niobaat nog steeds Nb2 is O5 . Wanneer de calcineringstemperatuur 500 en 600 °C is, een nieuwe band op 891 cm −1 verschijnt, terwijl het verdwijnt bij 700 °C, consistent met de XRD-resultaten van de vorming en reactie van LiNbO3 . Bij 700 en 800 °C, de banden bij 908 en 828 cm −1 komen overeen met de vorming van LiNb3 O8 verbindingen [26, 27]. De FTIR-resultaten komen goed overeen met de XRD-resultaten van Fig. 2.
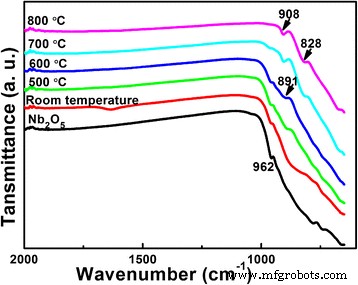
FTIR-spectra van Nb2 O5 grondstoffen en Li-Nb-O-poeders (molverhouding van Li:Nb = 8:1) gecalcineerd bij verschillende temperaturen
Op basis van de resultaten kunnen we concluderen dat de Li/Nb-verhouding een grote invloed heeft op de vorming van LiNbO3; de verhouding kleiner dan 3:1 is gunstig voor de vorming van LiNbO3 , hoewel groter dan 3:1, geen LiNbO3 vormen helemaal niet. Op basis van het diagram is het congruente Li-gehalte 97,2 mol% van het Nb-gehalte voor de bereiding van perfect enkelfasig LiNbO3 , en de overmaat of tekortkoming van het Li-gehalte wordt gecompenseerd door de vorming van Li3 NbO4 of LiNb3 O8 fase [28]. De grote overmaat aan LiOH is gunstig voor de vorming van Li3 NbO4 niet LiNbO3 , terwijl geen Li3 NbO4 fase wordt waargenomen na hydrothermische reactie vanwege de onvoldoende reactieconditie; zelfs als de LiNbO3 plaatselijk gevormd deeltje, wordt het gemakkelijk opgelost in LiOH-oplossing met een sterke alkaliteit [29].
Zoals hierboven besproken, wordt het Li-element niet gedetecteerd na de hydrothermische reactie zonder verdere calcinering, terwijl het echt bestaat in de producten met Li:Nb =8:1. Voor Nb2 O5 , is het nog steeds hetzelfde als de grondstof na de hydrothermische reactie? De XPS-test wordt uitgevoerd om de chemische component van Nb2 . te karakteriseren O5 grondstof en de producten verkregen na hydrothermische reactie, zoals weergegeven in Fig. 4. Het verschil van Nb 3d3/2 en 3d5/2 is de 2,7 eV voor beide samples, wat de Nb 5+ . aangeeft staat in beide monsters zonder andere gereduceerde Nb-oxiden [3]. De bindingsenergieën van Nb 3d verschuiven naar de toestand van lage bindingsenergie na de hydrothermische reactie, ongeveer 0,5 eV verschil. Het betekent dat de chemische omgeving van Nb verandert, terwijl er geen andere verbindingen worden gevormd. De verandering kan te wijten zijn aan het bestaan van Li-ionen in het product; hoewel er geen duidelijke Li-Nb-O-verbinding wordt gevormd, heeft het bestaan van Li-ionen met een grotere iconiteit een sterke aantrekkingskracht van O-ionen rond Nb, wat resulteert in de chemische verschuiving van Nb 3d-bindingsenergie.
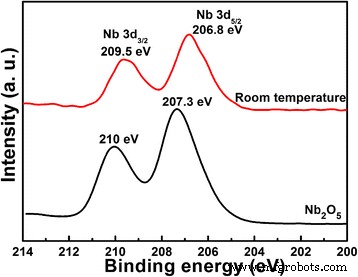
XPS-spectra van Nb2 O5 grondstoffen en de producten (molverhouding van Li:Nb = 8:1) verkregen na hydrothermische methode
De invloed van Li-ionen op Nb2 O5 wordt ook waargenomen in SEM-afbeeldingen, zoals weergegeven in Fig. 5. Afbeelding 5a is de afbeelding van Nb2 O5 grondstof, met onregelmatige vorm, dichte structuur en lengte van enkele micrometers. Na de hydrothermische reactie wordt het grote kristaldeeltje verdeeld in kleine deeltjes met een maximale grootte van ongeveer 200 nm, hoewel de kleine deeltjes nog steeds samenklonteren. Uit de XRD- en XPS-resultaten weten we dat de kleine deeltjes nog steeds Nb2 . zijn O5 . De verandering van de morfologie van Nb2 O5 kan worden toegeschreven aan de hydrothermische toestand en het grote gehalte aan LiOH·H2 O in grondstoffen.

SEM-afbeeldingen van a Nb2 O5 grondstoffen en b de producten (molverhouding van Li:Nb = 8:1) verkregen na hydrothermische methode
De producten die na de hydrothermische reactie worden verkregen, worden gecalcineerd bij 800 °C met verschillende Li/Nb-verhoudingen. Hierna kiezen we drie typische Li/Nb-verhoudingen als voorbeelden:1:3, 2:1 en 8:1. De XRD-patronen van de drie monsters worden getoond in Fig. 6. Van de XRD-resultaten, pure LiNbO3 zijn bereid met Li/Nb = 2:1 en hebben geen verandering laten zien, zelfs niet wanneer ze bij 800 °C worden gecalcineerd. Voor de bereiding van een andere Li-Nb-O-verbinding LiNb3 O8 , het kan worden verkregen met twee absoluut tegenovergestelde Li/Nb-verhoudingen:8:1 en 1:3 (aangeduid als LiNb3 O8 -8:1 en LiNb3 O8 -1:3). Voor andere Li/Nb-verhoudingen die niet zijn weergegeven in Fig. 6, resulteren de producten die bij 800 °C zijn gecalcineerd in de vorming van twee gemengde fasen:LiNb3 O8 en LiNbO3 . Gebaseerd op de XRD-resultaten, pure LiNb3 O8 poeders worden bereid met twee verschillende Li/Nb-verhoudingen, maar zijn er verschillen tussen de twee producten?
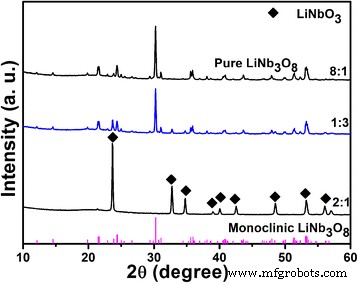
XRD-patronen van drie typische producten met een Li/Nb-verhouding gecalcineerd bij 800 °C gedurende 2 uur
De SEM-afbeeldingen van de twee producten worden weergegeven als respectievelijk Fig. 7b, c. Zoals getoond in Fig. 7, is de morfologie van LiNb3 O8 -1:3 zijn heel anders dan die van LiNb3 O8 -8:1. LiNb3 O8 -8:1 heeft een poreuze en holle structuur gevormd door LiNb3 O8 nanodeeltjes met een lengte van enkele micrometers, vergelijkbaar met die van een honingraat. Het is heel anders met de deeltjesaggregatie van een reactie in vaste toestand, zoals LiNb3 O8 -1:3 getoond. De BET-gebieden van LiNb3 O8 -8:1 en LiNb3 O8 -1:3 zijn 4,46 en 0,96 m 2 /g, respectievelijk, het grotere oppervlak van de eerstgenoemde resulteert uit de poreuze en holle structuur. Het verschil in morfologie kan worden toegeschreven aan de verschillende morfologieën van de reactanten:voor LiNb3 O8 -8:1, de reactant van LiNbO3 wordt gevormd op basis van de calcinaties van de producten na hydrothermische reactie, de morfologie van de producten wordt getoond in Fig. 5b, terwijl voor LiNb3 O8 -1:3, de morfologie van LiNbO3 verkregen direct na de hydrothermische reactie is hexahedron-achtig, zoals weergegeven in figuur 7a [21]. De vorming van de poreuze en holle structuur voor LiNb3 O8 -8:1 kan worden toegeschreven aan de lithiumvervluchtiging tijdens het calcinatieproces, wat gunstig is voor de vorming van nieuw LiNb3 O8 deeltjes en netwerken tussen de deeltjes [11]. Voor LiNbO3 gecalcineerd bij 800 °C (d.w.z. Li/Nb =2:1), de korrelgrootte is ongeveer 200 nm en de vorm lijkt onregelmatig, zoals weergegeven in figuur 7d; het INZET-gebied is ongeveer 3,91 m 2 /g.

SEM-afbeeldingen van drie typische producten met een Li/Nb-verhouding, gecalcineerd bij verschillende temperaturen:a 2:1 bij 500 °C, b 1:3, c 8:1, en d 2:1 bij 800 °C
De fotokatalytische prestaties van LiNb3 O8 en LiNbO3 worden getoond in Fig. 8. Uit de UV-vis-absorptiespectra van MB bij de gevarieerde bestralingstijd (Fig. 8a-d), wordt waargenomen dat de maximale absorptieband (665 nm) zwak wordt met de toename van de bestralingstijd . De afbraaksnelheid van MB is grotendeels verbeterd met de katalysatoren van LiNb3 O8 en LiNbO3 onder UV-licht, speciaal voor LiNb3 O8 -8:1, ongeveer 85% van MB degradeerde na 30 minuten bestraling, zoals weergegeven in Fig. 8e. Aangezien de fotodegradatie van MB met behulp van Li-Nb-O-katalysatoren de pseudo-eerste-orde kinetiek gehoorzaamt, beschreven door de gemodificeerde Langmuir-Hinshelwood kinetiekmodus [30], de constanten van de pseudo-eerste-orde snelheid ( k ) worden berekend, weergegeven in Fig. 8f. De verkregen eerste-orde snelheidsconstanten van MB zonder katalysatoren, LiNb3 O8 -1:3, LiNbO3 , en LiNb3 O8 -8:1 zijn 0,71 × 10 −2 , 1,61 × 10 −2 , 4.18 × 10 −2 , en 6,73 × 10 −2 min −1 , respectievelijk. Hoe hoger de snelheidsconstante van de eerste orde is, des te opmerkelijker zijn de fotokatalytische prestaties. De k van LiNb3 O8 -8:1 is 9,5 keer MB zonder katalysatoren, 4,2 keer LiNb3 O8 -1:3 en 1,6 keer LiNbO3 . Vergeleken met LiNb3 O8 -1:3, de hogere fotokatalytische prestaties van LiNb3 O8 -8:1 kan worden toegeschreven aan de unieke poreuze en holle structuur, die zorgt voor een hoge dichtheid aan actieve plaatsen voor de afbraak van MB [31].
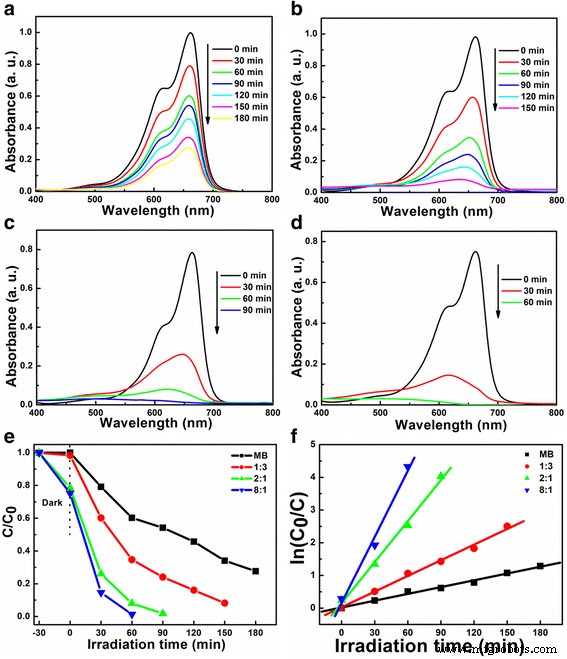
UV-vis absorptiespectra van de afbraak van MB:a zonder katalysator en gekatalyseerd door b LiNb3 O8 -1:3, c LiNbO3 , en d LiNb3 O8 -8:1, respectievelijk. e Fotodegradatie van MB en f kinetische pasvorm met betrekking tot de bestralingstijd met Li-Nb-O-poeders
Vergeleken met LiNbO3 , de verbeterde fotokatalytische prestaties van LiNb3 O8 -8:1, dat bijna hetzelfde absorptievermogen van MB heeft als dat van LiNbO3 , kan worden toegeschreven aan het gelaagde structuurtype met de verminderde symmetrie. De gelaagde structuur kan de scheiding van elektronen en gaten [32] verbeteren, consistent met de PL-spectra, zoals weergegeven in Fig. 9. Tegelijkertijd kan de LiNb3 O8 raamwerk wordt geconstrueerd door drie verschillende niobaat-octaëders en Li-atomen delen gedeeltelijke octaëdrische plaatsen; de hogere niobaat octaëdrische plaats zal naar verwachting meer actieve plaatsen voor fotokatalyse verschaffen. Ten slotte, de kleinere energiebandafstand van LiNb3 O8 (ongeveer 3,9 eV) dan die van LiNbO3 (4.14 eV) betekent dat het meer invallend licht kan gebruiken om deel te nemen aan het fotokatalytische proces [33].
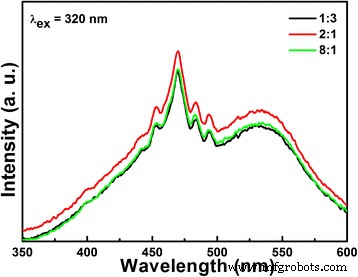
Kamertemperatuur PL-spectra van LiNb3 O8 -1:3, LiNbO3 , en LiNb3 O8 -8:1 katalysatoren
De scheidingsefficiëntie van door foto gegenereerde dragers van Li-Nb-O-katalysator wordt onderzocht met PL-spectra, zoals weergegeven in Fig. 9. Zoals we weten, zijn PL-emissiespectra voornamelijk het resultaat van de recombinatie van vrije dragers. Zoals te zien in Fig. 9, LiNb3 O8 vertoont kleinere emissiepieken rond 470 nm dan LiNbO3 . Het betekent dat LiNb3 O8 heeft een langere levensduur van de ladingsdrager en verbeterde efficiëntie van grensvlakladingsoverdracht, wat kan worden toegeschreven aan de gelaagde structuur met de verminderde symmetrie die de scheiding van elektronen en gaten verbetert.
Conclusies
Uit de bovenstaande resultaten kunnen we concluderen dat de Li/Nb-verhouding een grote invloed heeft op de vorming van LiNbO3; de verhouding kleiner dan 3:1 is gunstig voor de vorming van LiNbO3 , hoewel groter dan 3:1, vormt geen LiNbO3 helemaal niet en de morfologie en chemische binding van Nb2 O5 grondstof zijn totaal gewijzigd door Li ionen. De reden kan worden toegeschreven aan het grote gehalte aan LiOH, wat gunstig is voor de vorming van Li3 NbO4 niet LiNbO3 , en ook, zelfs als de LiNbO3 deeltje vormt zich lokaal, het wordt gemakkelijk opgelost in LiOH-oplossing met een sterke alkaliteit. Pure LiNb3 O8 poeders worden verkregen met twee absoluut tegengestelde Li/Nb-verhoudingen:8:1 en 1:3; de eerste vertoont een unieke poreuze en holle structuur, heel anders met de deeltjesaggregatie (de laatste vertoont). Vergeleken met Li/Nb = 1:3, hogere fotokatalytische prestaties van LiNb3 O8 (Li/Nb = 8:1) worden waargenomen en dit kan worden toegeschreven aan de unieke poreuze en holle structuur, die zorgt voor een hoge dichtheid aan actieve plaatsen voor de afbraak van MB. Vergeleken met LiNbO3 , de verbeterde fotokatalytische prestaties van LiNb3 O8 kan worden toegeschreven aan het gelaagde structuurtype met de verminderde symmetrie die de scheiding van elektronen en gaten verbetert.
Nanomaterialen
- Introductie van de Mark X:prestaties, precisie en presentatie in één
- Hoe IoT Industrie 4.0 en de effecten van IoT op het MKB hervormt
- Voorbereiding van met ICA geladen mPEG-ICA nanodeeltjes en hun toepassing bij de behandeling van door LPS geïnduceerde H9c2-celbeschadiging
- Effecten van dubbellaagse dikte op de morfologische, optische en elektrische eigenschappen van Al2O3/ZnO-nanolaminaten
- De voorbereiding van Au@TiO2 Yolk–Shell Nanostructure en zijn toepassingen voor afbraak en detectie van methyleenblauw
- Voorbereiding en fotokatalytische prestaties van LiNb3O8-fotokatalysatoren met holle structuur
- TiO2-nanobuisarrays:gefabriceerd op basis van een zacht-hard sjabloon en de korrelgrootte-afhankelijkheid van veldemissieprestaties
- De koppelingseffecten van oppervlakteplasmonpolaritons en magnetische dipoolresonanties in metamaterialen
- De brandende effecten van plasma en zuurstof/brandstof
- De nauwkeurigheid en prestaties van uw waterstraalsnijmachine verbeteren
- Grondbeginselen van het scheermes:de effecten van meskwaliteit op de scheerprestaties



