Nec-1 vermindert neurotoxiciteit veroorzaakt door titaniumdioxide-nanomaterialen op Sh-Sy5y-cellen via RIP1
Abstract
Titaniumdioxide-nanomaterialen worden op tal van gebieden toegepast vanwege hun uitstekende fysisch-chemische eigenschappen, die op hun beurt een potentiële bedreiging vormen voor de menselijke gezondheid. Onlangs hebben talrijke in vivo-onderzoeken aangetoond dat nanodeeltjes van titaniumdioxide (TNP's) na blootstelling via verschillende routes in de hersenen van dieren kunnen worden getransporteerd. Geabsorbeerde TNP's kunnen zich ophopen in de hersenen en kunnen neuronale cellen verstoren, wat leidt tot hersendisfunctie. In vitro-onderzoeken bevestigden de neurotoxiciteit van TNP's. De mechanismen die ten grondslag liggen aan de neurotoxiciteit van TNP's blijven onduidelijk. Of necroptose betrokken is bij de neurotoxiciteit van TNP's is onbekend. Daarom voerden we een in vitro onderzoek uit en ontdekten dat TNP's op een dosisafhankelijke manier ontstekingsschade in SH-SY5Y-cellen induceerden, wat werd verzacht door voorbehandeling met necrostatine-1 (Nec-1). Omdat receptor-interacterende proteïne kinase 1 (RIP1) naar verluidt het doelwit van Nec-1 is, hebben we het tot zwijgen gebracht door siRNA. We hebben mutante en wildtype cellen blootgesteld aan TNP's en inflammatoire schade beoordeeld. Het tot zwijgen brengen van RIP1-expressie remde ontstekingsschade veroorzaakt door blootstelling aan TNP's. Alles bij elkaar genomen verbetert Nec-1 de neurotoxiciteit van TNP's via RIP1. Er moeten echter meer onderzoeken worden uitgevoerd om de correlatie tussen de neurotoxiciteit van TNP's en RIP1 volledig te beoordelen.
Inleiding
Vanwege hun uitstekende fysisch-chemische eigenschappen worden nanomaterialen van titaniumdioxide gesynthetiseerd [1] en op grote schaal gebruikt voor verschillende doeleinden, zoals cosmetica [2], industriële gebieden [3, 4] en medische gebieden [5]. Dit wijdverbreide gebruik kan echter een grote bedreiging vormen voor de menselijke gezondheid [6]. Eenmaal blootgesteld, komen de meeste titaniumdioxide-nanodeeltjes (TNP's) het menselijk lichaam binnen via inademing en opname [6]. Het ademhalingssysteem [7], het spijsverteringsstelsel [8] en het cardiovasculaire systeem [9] kunnen allemaal worden onderbroken door geabsorbeerde TNP's. Evenzo kunnen de hersenen, als het belangrijkste onderdeel van het centrale zenuwstelsel, ook worden verstoord, aangezien TNP's in de bloedsomloop de bloed-hersenbarrière kunnen binnendringen en geïnhaleerde NP's via de reukroute naar de hersenen kunnen worden getransporteerd [10] . Zodra TNP's de hersenen binnenkomen, kunnen ze zich daar ophopen en schade aan de hersenen veroorzaken, wat leidt tot disfuncties. Schade aan de hersenen is meestal onomkeerbaar en ernstig, en daarom moet elke mogelijke oorzaak van schade worden onderzocht [11].
Hoewel geen enkele epidemiologische studie de associatie tussen blootstelling aan TNP's en hersenziekten heeft onderzocht, hebben tal van in vivo en in vitro studies de neurotoxiciteit van TNP's bevestigd [12]. Bovendien lag de nadruk vooral op onderzoek om de onderliggende mechanismen bloot te leggen. Voor dit doel hebben we eerder de momenteel bekende moleculaire mechanismen van neurotoxiciteit van TNP's beoordeeld en ontdekten dat processen van geprogrammeerde celdood (PCD), zoals apoptose en autofagie, betrokken waren bij de neurotoxiciteit van TNP's [13].
Necroptose, ook wel gereguleerde necrose genoemd, is een ander type PCD. In tegenstelling tot apoptose die caspase-afhankelijk is, is necroptose een receptor-interacterend proteïnekinase 1/3 (RIP1/RIP3)-afhankelijk. Geactiveerde RIP1 rekruteert RIP3 om een necrosoom te vormen, dat mixed lineage kinase domain-like protein (MLKL) activeert om necroptose te initiëren [14]. Necroptose kan celdood en neuro-inflammatie reguleren [15, 16], die beide betrokken zijn bij de neurotoxiciteit van TNP's. Daarom veronderstelden we dat necroptose betrokken is bij de neurotoxiciteit veroorzaakt door TNP's.
Om onze hypothese te testen, hebben we een in vitro onderzoek uitgevoerd om de rol van necroptose in de neurotoxiciteit van TNP's te onderzoeken. In deze studie werden de levensvatbaarheid van de cellen, LDH-lekkage en inflammatoire cytokines (TNF-α, IL-1β, IL-6 en IL-8) gemeten na blootstelling aan TNP's. Eerst werden SH-SY5Y-cellen gekweekt met verschillende concentraties TNP's. Ten tweede werden cellen blootgesteld aan TNP's met of zonder Nec-1, een krachtige remmer van necroptose. Ten derde werd RIP1-genexpressie, die kan worden onderdrukt door Nec-1, tot zwijgen gebracht met behulp van siRNA, waarna mutante en wildtype cellen werden behandeld met TNP's. Deze studie werpt licht op het uitgebreide begrip van de moleculaire mechanismen die ten grondslag liggen aan neurotoxiciteit van TNP's.
Resultaten
TNP's remmen de levensvatbaarheid van cellen
Om de cytotoxiciteit van TNP's op SH-SY5Y-cellen te verifiëren, hebben we eerst de levensvatbaarheid van de cellen beoordeeld met behulp van de CCK8-assay. Cellen werden 24, 48 en 72 uur gekweekt met TNP-concentraties variërend van 5 tot 160 g / ml. Zoals getoond in Fig. 1 bleef de levensvatbaarheid van de cellen onveranderd in de cellen die werden behandeld met 5, 10, 20 en 40 g/ml na 24 uur blootstelling. Wanneer cellen 48 en 72 uur werden behandeld, bleef de levensvatbaarheid van de cellen alleen onveranderd in de 5 μg/ml-groep (p =0.4507 om 48 uur en p =0,1002 bij 72 uur). Bovendien was de levensvatbaarheid van de cellen dramatisch lager in de cellen die waren behandeld met 80 g/ml TNP's na 48 (p =0.0007) en 72 uur (p =0,0008). Op basis van die resultaten concludeerden we dat TNP's de levensvatbaarheid van cellen op een dosis- en tijdsafhankelijke manier verminderden (gegevens niet getoond), wat aangeeft dat langdurige blootstelling giftiger was.
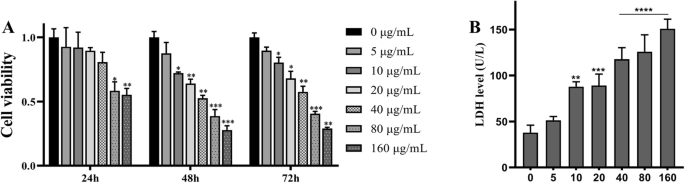
Verschillende concentraties van blootstelling aan TiO2-NP's op cellevensvatbaarheid van SH-SY5Y-cellen na 24, 48 en 72 uur en LDH-lekkage na 72 uur. (Vergeleken met de controlegroep, * p <0,05, ** p <0,01, *** p <0.001, **** p <0,0001)
TNP's beschadigen membraanintegriteit
Nest analyseerden we de toxische effecten van TNP's op de membraanintegriteit na 72 uur blootstelling. Membraanintegriteit werd beoordeeld door LDH-lekkage te meten. Zoals getoond in Fig. 1b, waren de LDH-niveaus significant verhoogd in cellen die werden behandeld met TNP's in doses hoger dan 5 μg / ml. Een verhoogde LDH-productie werd waargenomen in de cellen die werden behandeld met 40, 80 en 160 g/ml (p <0,0001). Deze resultaten suggereerden dat TNP's de LDH-spiegels op een dosisafhankelijke manier verhoogden, wat vergelijkbaar was met de CCK8-assay.
Blootstelling aan TNP's bevordert ontsteking
De ontstekingsreactie na blootstelling aan TNP's werd geanalyseerd met behulp van ELISA. Nadat cellen gedurende 72 uur waren behandeld met verschillende TNP's-concentraties, werden de niveaus van TNF-α, IL-1β, IL-6 en IL-8 gemeten. Zoals getoond in Fig. 2, werd de IL-8-secretie opgereguleerd in alle met TNP's behandelde cellen; de niveaus van TNF-α, IL-1β, IL-6 en IL-8 waren uniform verhoogd in cellen die werden behandeld met doses hoger dan 5 μg/ml (p <0,01). Bovendien was de ontsteking significant hoger in cellen die werden behandeld met doses hoger dan 10 μg/ml groep (p <0,0001). Al met al versterkten TNP's de ontsteking op een dosisafhankelijke manier.
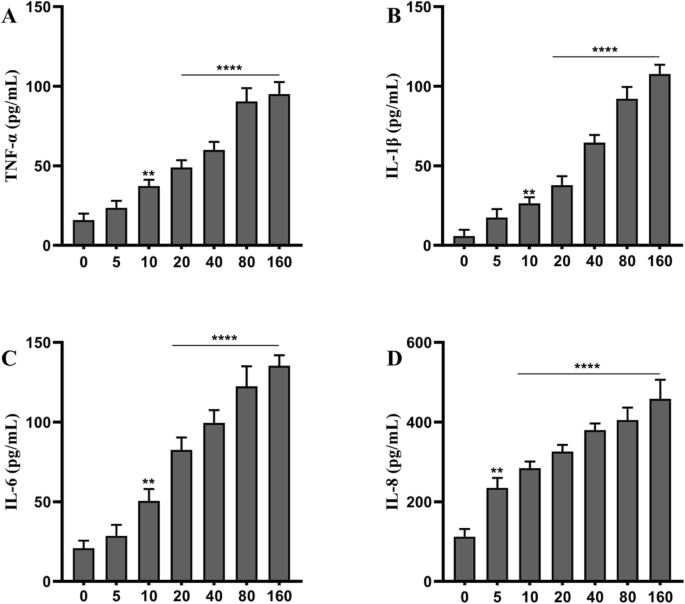
Verschillende concentraties TiO2-NP's (μg/mL) blootstelling aan ontsteking van SH-SY5Y-cellen na 72 uur. (Vergeleken met de controlegroep, **** p <0,0001)
Onze resultaten gaven aan dat TNP's op een dosisafhankelijke manier inflammatoire schade veroorzaakten. We hebben een TNP-concentratie van 80 g/ml en een blootstellingsperiode van 72 uur aangenomen in de volgende experimenten om de rol van necroptose in de neurotoxiciteit van TNP's te onderzoeken.
Nec-1 gelijktijdige behandeling remt neurotoxiciteit van TNP's
Om de rol van necroptose bij ontstekingsletsel te analyseren, hebben we cellen samen behandeld met Nec-1 (een necroptose-remmer) en TNP's. Zoals getoond in Fig. 3a, werden SH-SY5Y-cellen blootgesteld aan TNP's of TNP's + Nec-1 (1, 5, 10, 15 of 20 M), en we ontdekten dat Nec-1 de door TNP's geïnduceerde vermindering van levensvatbaarheid van de cellen (10, 15, 20 M) (p <0,0001). Omdat de levensvatbaarheid van de cellen in de met 15 M en 20 M behandelde groepen niet hoger was dan die in de groepen behandeld met 10 μM (p =0,6643 en p =0,6292), behandelden we cellen samen met 10 μM Nec-1 om het effect op de membraanintegriteit te analyseren.
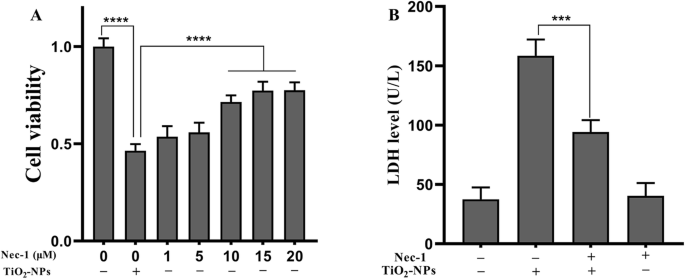
De effecten van Nec-1 op de levensvatbaarheid van cellen en LDH na blootstelling aan TNP's. ( *** p <0.001, **** p <0,0001)
Na het kweken van cellen met TNP's of TNP's + Nec-1, ontdekten we dat LDH-niveaus in de TNP's + Nec-1-groep veel lager waren dan die in de groep met alleen TNP's (p =0,0005). Bovendien verhoogde behandeling met alleen Nec-1 de LDH-lekkage niet (p =0,9878).
Concluderend kon 10 μM Nec-1 de cytotoxiciteit van TNP's effectief remmen en was het niet toxisch voor cellen.
Om het ontstekingsremmende vermogen van Nec-1 te analyseren, werden cellen gekweekt met TNP's of TNP's + Nec-1. Zoals getoond in Fig. 4, is de productie van TNF-α (p =0,003), IL-1β (p =0,0013), IL-6 (p <0,0001), en IL-8 (p =0,0004) was significant lager in de TNPs + Nec-1-groep dan in de TNPs-groep.
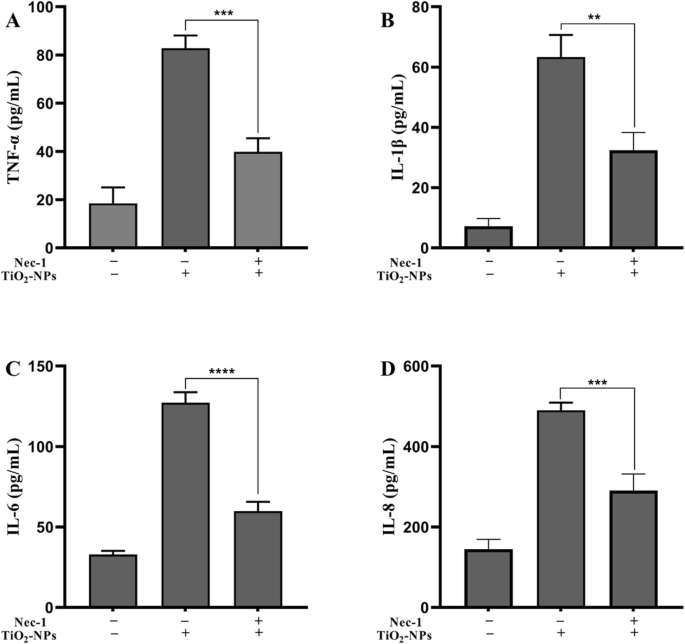
De effecten van Nec-1 op ontstekingen na blootstelling aan TNP's. ( ** p <0,01, *** p <0.001, **** p <0,0001)
Die resultaten impliceren dat Nec-1 ontstekingsreacties veroorzaakt door blootstelling aan TNP's kan verminderen.
Het stilleggen van RIP1 verzacht het door TNP's veroorzaakte ontstekingsletsel
Om te bepalen of Nec-1 ontstekingsschade veroorzaakt door TNP's via RIP1 tenietdeed, hebben we RIP1-expressie van cellen effectief tot zwijgen gebracht met behulp van siRNA (Fig. 5, p <0,0001). Vervolgens werd de ontstekingsbeschadiging na blootstelling aan TNP's op mutante en wildtype cellen gemeten. Figuur 6a laat zien dat de levensvatbaarheid van cellen in de TNPs + si-RIP1-groep opmerkelijk hoger was dan die in de TNPs + si-NC-groep (p =0,0002). LDH-productie (Fig. 6b, p <0,0001) en niveaus van TNF-α (p <0,0001), IL-1β (p =0,0001), IL-6 (p <0,0001), en IL-8 (p =0,0001) (Fig. 7) in de TNP's + si-RIP1-groep waren dramatisch lager dan die in de TNP's + si-NC-groep. Deze resultaten gaven aan dat TNP's ontstekingsschade bevorderden via RIP1.
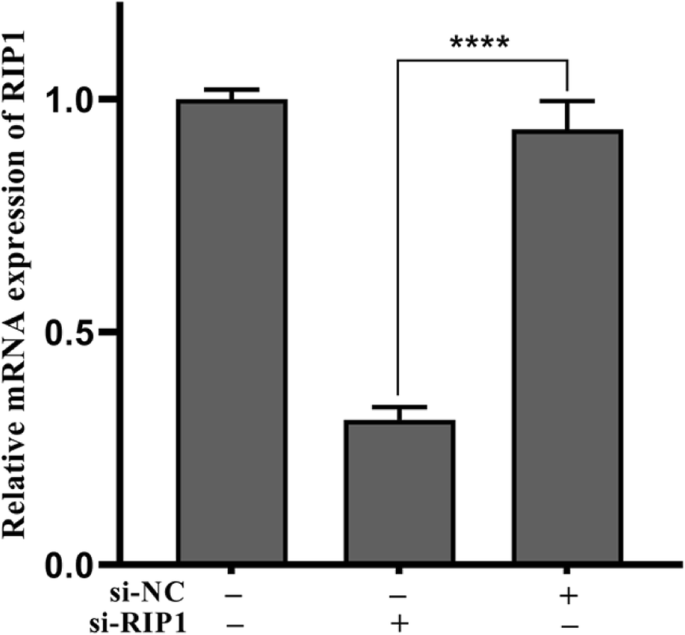
De mRNA-expressie na SH-SY5Y-cellen getransfecteerd met si-RIP1. ( **** p <0,0001)
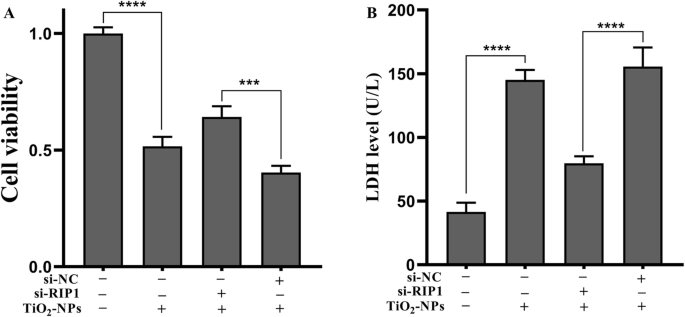
Levensvatbaarheid van de cellen en LDH-lekkage nadat mutante en wildtype cellen werden blootgesteld aan TNP's. ( *** p <0.001, **** p <0,0001)
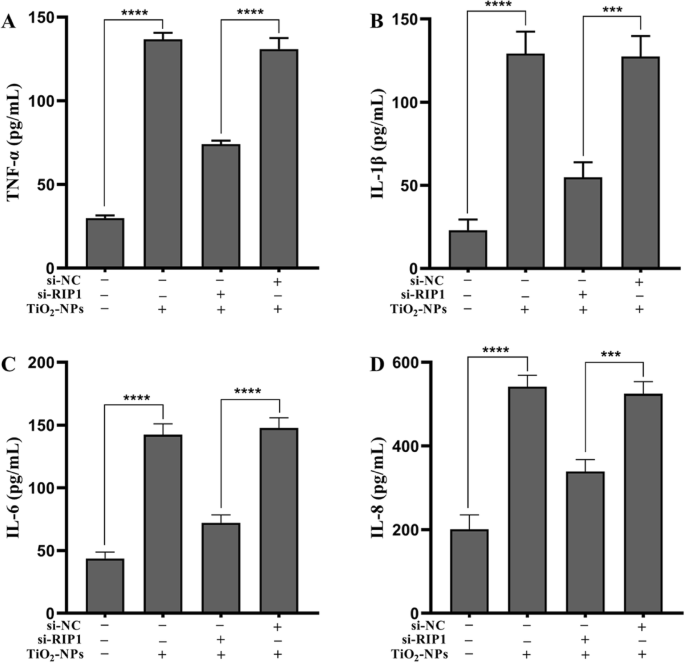
Ontsteking nadat mutante en wildtype cellen werden blootgesteld aan TNP's. ( *** p <0.001, **** p <0,0001)
Discussie
In deze studie ontdekten we dat blootstelling aan TNP's cytotoxiciteit op SH-SY5Y-cellen induceerde op een dosisafhankelijke manier en dat necroptose betrokken was bij de neurotoxiciteit van TNP's. Om de rol van necroptose te onderzoeken, hebben we cellen blootgesteld aan TNP's met of zonder Nec-1 (een krachtige necroptose-remmer) [17, 18], en de levensvatbaarheid van de cellen, LDH-lekkage en de niveaus van inflammatoire cytokines gemeten. Onze gegevens suggereren dat gelijktijdige behandeling met Nec-1 ontstekingsschade veroorzaakt door TNP's kan verminderen. Omdat studies hebben aangetoond dat Nec-1 zijn effecten uitoefent door RIP1-activiteit te onderdrukken, hebben we cellen getransfecteerd met si-RIP1 om te bepalen of RIP1 betrokken was bij de beschermende effecten van Nec-1. Mutante en wildtype cellen werden behandeld met TNP's en de ontstekingsbeschadiging werd beoordeeld. Dit gaf aan dat de levensvatbaarheid van de cellen in de si-RIP1-groep hoger was dan die in de si-NC-groep, en dat de niveaus van LDH-lekkage en inflammatoire cytokines lager waren in de si-RIP1-groep dan die in de si-NC-groep na blootstelling aan TNP's . Concluderend heeft de huidige studie voor het eerst onthuld dat necroptose betrokken is bij de door TNP's geïnduceerde ontstekingsbeschadiging op cellen.
We hebben de neurotoxiciteit van TNP's herbevestigd in ons in vitro onderzoek. Nadat SH-SY5Y-cellen waren blootgesteld aan verschillende concentraties TNP's gedurende verschillende incubatietijden, werd de levensvatbaarheid van de cellen beoordeeld met behulp van de CCK8-assay. Zoals getoond in Fig. la, verminderde blootstelling aan TNP's de levensvatbaarheid van de cellen op een dosisafhankelijke manier; na 48 uur en 72 uur blootstelling was de levensvatbaarheid van de cellen in de 80 en 160 TNPs-groepen drastisch verminderd in vergelijking met de controlegroep (p <0,001). Om de cytotoxiciteit verder te bevestigen, hebben we ook de LDH-lekkage gemeten. De gegevens in Fig. 1b lieten zien dat de LDH-productie dosisafhankelijk toenam na 72 uur blootstelling, en de LDH-spiegels in de 40, 80 en 160 groepen waren opmerkelijk hoger dan die in de controlegroep (p <0,0001). Omdat eerdere studies hebben aangetoond dat neuro-inflammatie kan worden bevorderd door blootstelling aan TNP's [19], werden ook de niveaus van TNF-α, IL-1β, IL-6 en IL-8 gemeten. Figuur 2 illustreert dat de niveaus van die vier inflammatoire cytokines significant opgereguleerd waren in vergelijking met de controlegroep en dramatisch hoger waren in de groepen die werden behandeld met 20 tot 160 g/ml (p <0,0001). Al met al gaven onze resultaten aan dat TNP's op een dosisafhankelijke manier neurotoxiciteit zouden kunnen induceren, wat consistent is met eerdere onderzoeken. TNP's kunnen worden geabsorbeerd door neuronale cellen en remmen de proliferatie [20,21,22]. Bovendien kan blootstelling aan TNP's de levensvatbaarheid van cellen verminderen en LDH-lekkage op een dosisafhankelijke manier bevorderen [23,24,25,26,27].
We behandelden cellen samen met Nec-1 om te verduidelijken of necroptose betrokken was bij de neurotoxiciteit veroorzaakt door TNP's. Nadat cellen waren behandeld met aangegeven concentraties van TNP's met of zonder Nec-1, werden de levensvatbaarheid van de cellen, LDH-lekkage en ontsteking beoordeeld. Figuur 3a laat zien dat de vermindering van de levensvatbaarheid van de cellen na blootstelling aan TNP's significant werd geremd door gelijktijdige behandeling met 10 μM Nec-1. Ondertussen onthulde Fig. 3b dat behandeling met 10 μM Nec-1 de LDH-niveaus niet verhoogde, en de LDH-niveaus in cellen behandeld met TNP's + Nec-1-groep waren dramatisch lager dan die in de groep met alleen TNP's. Vervolgens hebben we de effecten gemeten van gelijktijdige behandeling met Nec-1 op ontsteking veroorzaakt door TNP's. Figuur 4 illustreert dat de niveaus van TNF-a, IL-1β, IL-6 en IL-8 opmerkelijk lager waren in de cellen die waren behandeld met TNP's + Nec-1. Deze resultaten bevestigden opnieuw dat Nec-1 cellen zou kunnen beschermen tegen dood en ontstekingsprocessen [28, 29].
Ten slotte, aangezien RIP1 het doelwit is van Nec-1, hebben we beoordeeld of RIP1 de neurotoxiciteit van TNP's zou kunnen reguleren. We construeerden mutante cellen door RIP1-expressie tot zwijgen te brengen (Fig. 5). Gegevens uit Fig. 6 en Fig. 7 onthulden dat na blootstelling aan TNP's de levensvatbaarheid van de cellen hoger was en dat de LDH-, TNF-α-, IL-1β-, IL-6- en IL-8-niveaus lager waren in de si-RIP1-groep dan die in de si-NC, wat suggereert dat TNP's cytotoxiciteit bevorderen via RIP1. Evenzo hebben verschillende onderzoeken aangetoond dat RIP1 zowel celdood als ontstekingsprocessen kan reguleren [30, 31].
Hoewel we voor het eerst rapporteren dat Nec-1 de neurotoxiciteit van TNP's kan verminderen door de necroptose-signaleringsroute te onderdrukken, heeft onze studie een paar beperkingen. Ten eerste verschilt de cytotoxiciteit van materialen met nano-afmetingen van hun bulkmaterialen en kan grotendeels worden beïnvloed door oppervlakte-eigenschappen [32], wat het tegenovergestelde resultaat van verhoogde levensvatbaarheid van de cellen, gevonden door Sebastián et al., kan verklaren. [33]. Daarom is het essentieel om nanotoxiciteit op onderwerpen uit meerdere aspecten, zoals celproliferatie, membraanintegriteit, oxidatieve stress, ontsteking, mitochondriale functie, celcyclus, cytoskelet en epigenetica, uitgebreid te evalueren. Ten tweede kan RIP1 RIP3 rekruteren om een functioneel necrosoom te vormen, een vitale activator van MLKL, om necroptose te initiëren [34]. We veronderstellen dat RIP3 / MLKL betrokken zou kunnen zijn bij de neurotoxiciteit van TNP's, wat in toekomstig werk zou moeten worden onderzocht. Bovendien moeten de associaties van RIP3/MLKL met de neurotoxiciteit van TNP's ook worden geëvalueerd. Ten derde werd gemeld dat reactieve zuurstofspecies (ROS), als de belangrijkste mechanismen die ten grondslag liggen aan neurotoxiciteit van TNP's [35, 36], het stroomopwaartse signaal van RIP1 zijn [37]. Daarom moet verder worden besproken of ROS de stroomopwaartse van RIP1 zijn in de neurotoxiciteit van TNP's. Ten vierde moeten cellen gedurende een lange periode (meer dan 72 uur) worden blootgesteld aan niet-toxische concentraties (TNP's <5 g/mL) om chronische cytotoxiciteit te beoordelen. Ten vijfde moeten we de rol van necroptose in de neurotoxiciteit van TNP's in meer neuronale cellijnen en primaire menselijke en dierlijke neuronale cellen evalueren.
Conclusies
Onze studie onthulde necroptose als een ander geprogrammeerd celdoodmechanisme dat betrokken is bij de neurotoxiciteit veroorzaakt door TNP's. In deze studie ontdekten we dat TNP's op een dosisafhankelijke manier ontstekingsschade in SH-SY5Y-cellen kunnen veroorzaken en dat gelijktijdige behandeling met Nec-1 (een krachtige remmer van necroptose) die schadelijke effecten zou kunnen verbeteren. RIP1, het doelwit van Nec-1, werd tot zwijgen gebracht door si-RNA, dat ontstekingsschade veroorzaakt door blootstelling aan TNP's effectief verzachtte. Concluderend remde Nec-1 de ontstekingsbeschadiging van SH-SY5Y-cellen veroorzaakt door blootstelling aan TNP's door zich te richten op de RIP1-route. De stroomopwaartse en stroomafwaartse signaalroutes van RIP1 die betrokken zijn bij de neurotoxiciteit van TNP's moeten verder worden beoordeeld.
Materialen en methoden
TNP-voorbereiding en celcultuur
We hebben TNP's eerder gekarakteriseerd en voorbereid volgens onze eerder gepubliceerde procedure [38]. In het kort werden TNP's opgelost in RPMI 1640 tot verschillende concentraties van 5, 10, 20, 40, 80 en 160 g / ml. De TNP-oplossing werd gesteriliseerd en gesoniceerd (300 W, 10 min) bij kamertemperatuur om te voorkomen dat de deeltjes aggregeren vóór de behandeling. Cellen in kweekmedium die niet waren blootgesteld aan TNP's dienden als de controlegroep. SH-SY5Y-cellen, gekocht van de Cell Bank van het Shanghai Institute of Life Sciences, Chinese Academy of Sciences, werden gekweekt in RPMI 1640-medium (HyClone, Logan, UT, VS) aangevuld met 10% foetaal runderserum (Gibco, een product lijn van Thermo Fisher Scientific, Waltham, MA, VS), 100 E/mL penicilline en 100 μg/mL streptomycine bij 37 °C in een bevochtigde incubator met 5% CO2 .
Levensvatbaarheid van cellen en LDH-lektest
De levensvatbaarheid van de cellen werd gemeten met behulp van een celtelkit-8 (CCK8. Dojindo, cat no.CK04). In het kort, 1 × 10 4 SH-SY5Y-cellen werden in een plaat met 96 putjes geplaatst en gekweekt in een incubator bij 37 ° C (5% CO2 ) gedurende 24 uur vóór blootstelling aan TNP's. Cellen werden vervolgens nog 24 uur geïncubeerd met TNP's in verschillende concentraties (0, 1,25, 2,5, 5, 10, 20, 40 en 80 g/ml). Na behandeling werden de cellen nog 2 uur met CCK-8 geïncubeerd. Vervolgens werd de optische dichtheid (OD) gemeten bij 450 nm door de plaat met 96 putjes in een microplaatlezer te plaatsen (BioTek, Winooski, VT, VS). De cellevensvatbaarheid van elke groep, uitgedrukt als een percentage, werd berekend als (ODbehandeld−ODblank)/(ODcontrol−ODblank) × 100%.
Membraanintegriteit werd gemeten met een commerciële kit (Nanjing Jiancheng Bioengineering Institute, China). Nadat SH-SY5Y-cellen 72 uur waren blootgesteld aan verschillende concentraties TNP's, werd de LDH-secretie geanalyseerd volgens de instructies van de fabrikant.
Ontstekingsreactie
ELISA werd toegepast om de niveaus van TNF-a, IL-1β, IL-6 en IL-8 geproduceerd door SH-SY5Y-cellen te meten. In het kort, SH-SY5Y-cellen werden 72 uur blootgesteld aan TNP's en het supernatant werd verzameld voor analyse volgens de instructies van de fabrikant (Elabscience Biotechnology Co., Ltd.).
siRNA-transfectie
Volgens het protocol van de fabrikant werd een concentratie van 100 nM van si-RIP1 of siRNA met negatieve controle (si-NC) in cellen getransfecteerd met behulp van Lipofectamine 2000. De efficiëntie van gen-uitschakeling door siRNA werd geschat met real-time PCR.
Realtime PCR
RNA van cellen blootgesteld aan verschillende concentraties TNP's werd geïsoleerd met behulp van de RNAqueous-kit (Ambion Inc., Austin, TX, VS) op basis van de instructies van de fabrikant. De relatieve expressie van RIP1 werd gemeten door real-time PCR. De relatieve mRNA-niveaus van RIP1 werden genormaliseerd naar β-actine-expressies.
Statistische analyse
SPSS 11.0-software (SPSS Inc., Chicago, IL, VS) werd gebruikt om gegevens te analyseren. Eenrichtingsanalyse van variantie werd gebruikt om de gemiddelden van groepen te vergelijken. p <0,05 werd als statistisch significant beschouwd.
Beschikbaarheid van gegevens en materialen
Beschikbaar uit het manuscript.
Afkortingen
- TNP's:
-
Nanodeeltjes van titaniumdioxide
- Nec-1:
-
Necrostatine-1
- RIP:
-
Receptor interactie proteïne kinase
- MLKL:
-
Mixed lineage kinase domein-achtig eiwit
- ROS:
-
Reactieve zuurstofsoorten
Nanomaterialen
- IBM-wetenschappers meten warmteoverdracht via enkele atomen
- Grafeen zet nanomaterialen op hun plaats
- Nanobomen voor kleurstofgevoelige zonnecellen
- Hoogrendement grafeen zonnecellen
- Nano-heterojuncties voor zonnecellen
- TITANIUMDIOXIDE - TiO2 - Prijs, markt en analyse
- WHITE MASTERBATCH - TITANIUMDIOXIDE MASTERBATCH IN PRODUCTIE
- Op cellen gebaseerde medicijnafgifte voor kankertoepassingen
- Nanotechnieken inactiveren kankerstamcellen
- Een kort voortgangsrapport over hoogrenderende perovskiet-zonnecellen
- Endotheelcellen targeten met multifunctionele GaN/Fe-nanodeeltjes



