Een zeer nanoporeuze, met stikstof gedoteerde koolstofmicrovezel afgeleid van Bioresource als een nieuw soort ORR-elektrokatalysator
Abstract
De synthese van metaalvrije op koolstof gebaseerde elektrokatalysatoren voor zuurstofreductiereactie (ORR) ter vervanging van de conventionele op platina gebaseerde katalysatoren is momenteel een hot topic van onderzoek geworden. Dit werk stelt een activeringsondersteunde carbonisatiestrategie voor voor de fabricage van met stikstof gedoteerde nanoporeuze koolstofmicrovezels (Me-CFZ-900) met een hoog BET-oppervlak (~ 929.4 m 2 g −1 ) door melamine als promotor/stikstofbron en bamboe-koolstof bioafval als koolstofbron te gebruiken met behulp van een zinkchloride-activator. Elektrochemische tests toonden aan dat het Me-CFZ-900-materiaal uitstekende ORR-elektrokatalytische activiteit en stabiliteit op lange termijn vertoonde, en ook een quasi-vier-elektronen ORR-route in alkalische elektrolyt vertoonde. We vinden ook dat het grafiet-N de katalytisch actieve plaats voor de ORR kan zijn, maar de vorming van planair-N kan verder helpen om de ORR-activiteit voor onze katalysatoren te bevorderen. De resultaten openen een nieuwe ruimte en bieden een nieuw idee om waardevolle poreuze nanokoolstofmaterialen te bereiden op basis van koolstofhoudend vast afval voor katalyse van een breed scala aan elektrochemische reacties in de toekomst.
Achtergrond
Geavanceerde elektrochemische energiesystemen, zoals brandstofcellen en metaal-luchtbatterijen, worden beschouwd als veelbelovende alternatieven voor traditionele fossiele brandstoffen [1, 2]. De zuurstofreductiereactie (ORR) is een belangrijke reactie in die energietechnologieën, maar lijdt aan verschillende tekortkomingen, zoals een hoge overpotentiaal, trage ORR-kinetiek en paddiversiteit, waardoor de verbetering van de algemene prestaties en conversie-efficiëntie wordt beperkt [3, 4 ]. Op dit moment zijn de op Pt gebaseerde katalysatoren op grote schaal gebruikt om de ORR in praktische toepassingen te verbeteren, maar hoge kosten en beperkte bronnen van metaal-Pt belemmeren de commercialisering [5,6,7]. De verkenning van goedkope, actieve en stabiele Pt-vrije ORR-katalysatoren is dus belangrijk om snel technologieën voor schone energie te ontwikkelen.
Om te zoeken naar enkele waardevolle vervangers voor metaal-Pt-katalysatoren, wordt de dotering van heteroatomen in koolstofallotropen zoals grafeen [8], graphdiyne [9] en koolstofnanobuisjes [10] in de volksmond bestudeerd vanwege hun onderscheidende fysieke en elektronische structuren. Hoewel er een enorme verbetering is doorgevoerd bij de gecontroleerde fabricage van de gedoteerde koolstofkatalysatoren, is de oorsprong van de katalytische activiteit van ORR nog steeds onduidelijk, wat een technisch knelpunt wordt op dit gebied [11, 12]. Gewoonlijk kan de verbetering van de ORR-activiteit van gedoteerde koolstofkatalysatoren worden toegeschreven aan ladingsmodulatie en gebroken elektroneutraliteit veroorzaakt door de heteroatoomdotering in het koolstofraamwerk [13, 14]. Andere onderzoeken hebben ook aangetoond dat de ORR-activiteit van de op koolstof gebaseerde katalysatoren afkomstig is van een geschikte dopinglocatie en -configuratie [15,16,17]. Bovendien kan het doteren van heteroatomen zoals stikstof de polarisatie van het koolstofoppervlak induceren, wat helpt om nieuwe stikstofbevattende actieve plaatsen te vormen, waardoor de adsorptie van atomen en ionen wordt bevorderd [18]. Het begrijpen van de bijdrage van N-rijke koolstofstructuren is dus belangrijk voor het ophelderen van de ORR katalytisch actieve plaatsen, wat ook een weg kan banen voor gericht ontwerp van ORR-actieve en stabiele gedoteerde koolstofkatalysatoren.
Het gebruik van natuurlijke biomassa (bijv. sojaboon [19], zijdefibroïne [20], kidneyboon [21] en hemoglobine [22]) en dierlijk bioafval (bijv. visschubben [23] en dierlijk bloed [24]) als een directe voorloper of de stikstofbron van katalytisch ORR-actieve plaatsen werd beschouwd als een effectieve route om de gedoteerde koolstofkatalysatoren te fabriceren. Meer recentelijk hebben Li et al. synthetiseerde ook een gedoteerde, op koolstof gebaseerde ORR-katalysator met een driedimensionaal poreus netwerk via het gebruik van hemine-biomateriaal als een voorloper met één bron en met behulp van zelf-geassembleerde natriumchloridekristallen als de sjabloon [25]. Jiang et al. [26] zette het biologische enzym van bloedcentra om in Fe–Nx katalytisch actieve plaatsen voor ORR-elektrokatalyse door de meerstapspyrolyse van biologisch bloedafval. De resulterende elektrokatalysator vertoont superieure ORR-katalytische activiteit, wat aangeeft dat de Fe–Nx structuur van heem in bloedcellen is gunstig bij de vorming van ORR-actieve centra en kan daarom de prestaties van katalysatoren bevorderen. Deze studies kunnen een streven zijn dat een nieuw soort hoogwaardige gedoteerde koolstofkatalysatoren kan worden bereid door pyrolyseprocessen op de juiste manier te beheersen en goedkope biomassamaterialen als voorlopers te kiezen.
Hierin ontwikkelen we, geïnspireerd door goedkope en gemakkelijk verkrijgbare bioafval-afgeleide heteroatoom-gedoteerde koolstof voor superieure ORR-prestaties, een strategie om een N-gedoteerde nanoporeuze koolstofmicrovezel te synthetiseren als een nieuw soort ORR-elektrokatalysator (Me-CFZ-900) door pyrolyse van verspilde bamboe-koolstofweefsels met de activering van zinkchloride, gecombineerd met het gebruik van melamine als promotor/stikstofbron. Voor zover ons bekend zijn er tot nu toe geen rapporten over het ontwerp van poreuze koolstofmicrovezels als ORR-katalysator via gemakkelijke conversie van bamboe-koolstof bioafval. We vinden dat de bereide Me-CFZ-900-katalysator een groot aantal uniforme mesoporiën heeft met een gemiddelde poriediameter van 2,23 nm en een groot oppervlak (~ 929.4 m 2 g −1 ), wat gunstig kan zijn voor het massatransport van O2 elektrokatalytische reductie. Deze studie opent een nieuwe ruimte en biedt een nieuw idee om waardevolle poreuze nanokoolstofmaterialen te bereiden, die kunnen functioneren als de veelbelovende ORR-elektrokatalysatoren door de poriekenmerken en het gehalte aan actieve N-soorten verder te verbeteren.
Methoden
Synthese van op koolstof gebaseerde ORR-katalysatoren
De met stikstof gedoteerde nanoporeuze koolstofmicrovezels werden bereid via een eenvoudige en gemakkelijke pyrolyse in twee stappen van verspilde bamboe-koolstofweefsels (gekocht bij Fujian Hengan Group Co. Ltd., China) met behulp van zinkchloride-activering. Gewoonlijk werden verspilde weefsels versnipperd in een pulper en vervolgens gecarboniseerd bij 350 °C gedurende 1 uur in een buisoven met een verwarmingssnelheid van 20 °C min −1 onder stikstofatmosfeer om wat resterende organische substanties te verwijderen. De verkregen koolstofmicrovezels worden aangeduid als de CF350. Vervolgens werden 0,5 g CF350, 1,0 g melamine en 1,0 g zinkchloride gelijkmatig gemengd door eenvoudige volledig vaste toestand gedurende 0,5 h in een agaatmortel te malen om een nieuwe koolstofhoudende voorloper (Me-CFZ) te verkrijgen. De Me-CFZ-precursor werd verder met warmte behandeld in een buisoven bij 900 °C gedurende 2 h met een verwarmingssnelheid van 10 °C min −1 onder de N2 atmosfeer, resulterend in een succesvolle synthese van Me-CFZ-900. De schematische illustratie voor de synthese van Me-CFZ-900 via een activeringsondersteunde carbonisatiemethode is aangegeven in Fig. 1. Om het effect van de pyrolysetemperaturen op de ORR-prestaties van op koolstof gebaseerde katalysatoren te controleren, hebben we ook andere Me-CFZ gefabriceerd katalysatoren bij verschillende temperaturen, die respectievelijk kunnen worden gemarkeerd als Me-CFZ-700, Me-CFZ-800 en Me-CFZ-1000. Als controle werden CF-900 en CFZ-900 zonder toevoeging van melamine op soortgelijke wijze bereid. Alle monsters werden verder behandeld door ze onder te dompelen in een 0,5 mol l −1 HCl-oplossing gedurende 2 uur voordat ze kunnen worden gebruikt als een ORR-elektrokatalysator. Om de reproduceerbaarheid te garanderen, hebben we alle ORR-katalysatoren drie keer voorbereid en hun fouten kunnen worden gecontroleerd in het bereik van 5,0%.

De schematische illustratie voor de synthese van mesoporeuze stikstof-gedoteerde koolstofmicrovezels voor ORR-elektrokatalyse via de activeringsondersteunde carbonisatie van bamboe-koolstof bioafval
Fysieke karakterisering
Scanning-elektronenmicroscopie met hoge resolutie (SEM) en transmissie-elektronenmicroscopie (TEM) tests werden verkregen door Hitachi UHR S4800 (Japan) en FEI Tecnai-G2 F30-instrument met een versnellingsspanning van respectievelijk 300 kV. Röntgenfoto-elektronspectroscopie (XPS) werd uitgevoerd met behulp van een Kratos XSAM800-spectrometer. Een Micromeritics Analyzer (ASAP 2010) werd toegepast om N2 . te testen -adsorptie/desorptie-isothermen bij 77 K. Röntgendiffractie (XRD) analyse werd uitgevoerd met behulp van een Shimadzu XRD-6000 röntgendiffractometer (Japan) met Cu Ka1 straling (λ =1.54178 Ǻ) bij 4° min
− 1
. Raman-spectroscopiegegevens werden geregistreerd met het Horiba HR800 Raman-systeem met een laserexcitatiegolflengte van 514,5 nm. XR-röntgenfoto is gemaakt met een Shimadzu XRD-6000 (λ = Röntgendiffractometer (Japan) met Cu Ka1 straling  ).
).
Elektrochemische metingen
Elektrokatalytisch gedrag van de op koolstof gebaseerde ORR-katalysator werd geëvalueerd op een CHI760E Bipotentiostat (Shanghai Chenhua Instruments Co. Ltd., China). Een glas-koolstof roterende ring-schijfelektrode (GC-RRDE, Φ = 5 mm, Pine Instrument Co.), een verzadigde calomelelektrode (SCE) en een grafietstaaf (Φ =0,5 cm) werden respectievelijk gebruikt als werkelektrode (WE), referentie-elektrode (RE) en hulpelektrode (AE). De fabricage van WE verwijst naar onze eerdere rapporten [12]. Over het algemeen 10 μl van 10 mg ml −1 dispersie werd op het GC-RRDE-oppervlak gepipetteerd en natuurlijk aan de lucht gedroogd. De massalading van op koolstof gebaseerde katalysatoren en commerciële Pt/C-katalysator (20 wt% Pt, Aladdin Industrial Co. Ltd.) werd gecontroleerd op ~ 600 μg cm −2 . Alle potentialen (vs. SCE) werden omgezet in de potentialen versus de omkeerbare waterstofelektrode (RHE). Verder werden elektrochemische impedantiespectra (EIS) verkregen in aanwezigheid van een 1 mmol l −1 K3 [Fe(CN)6 ]/K4 [Fe(CN)6 ] (molverhouding = 1:1) mengsel als een redox-sonde in 0,1 M KCl-oplossing. Om de volledige peroxide-ontleding die tijdens de test werd geproduceerd voldoende te induceren, werd de ringpotentiaal ingesteld op 0,5 V (vs. SCE) zoals elders vermeld. De %HO2 − opbrengst en aantal elektronenoverdracht (n ) tijdens de ORR werden berekend met behulp van de volgende vergelijkingen [25]:
$$ \%{HO}_2^{-}=100\times \frac{2{I}_{\mathrm{r}}/N}{I_{\mathrm{d}}+\left({I} _{\mathrm{r}}/N\right)} $$ (1) $$ n=4\times \frac{I_{\mathrm{d}}}{I_{\mathrm{d}}+{I }_{\mathrm{r}}/N} $$ (2)waar ik d is de faraday-stroom op de schijf, I r is de faraday-stroom in de ring, en N is de verzamelefficiëntie van ringelektrode (0,38). n werd berekend uit de Koutecky-Levich-vergelijking [27]:
$$ 1/{j}_d=1/{j}_k+1/B{\omega}^{1/2} $$ (3) $$ B=0.62{nFC}_{\mathrm{O}} {D}_{\mathrm{O}}^{2/3}{\nu}^{-1/6}{\omega}^{1/2} $$ (4)waar F is de constante van Faraday, C O is de O2 verzadigingsconcentratie in de elektrolyt, D O is de O2 diffusiecoëfficiënt in de elektrolyt, ν is de kinetische viscositeit van de elektrolyt, en ω is de rotatiesnelheid van de elektrode en 0,62 is een constante wanneer de rotatiesnelheid wordt uitgedrukt in rpm.
Resultaten en discussie
Afbeelding 2 toont de SEM- en TEM-afbeeldingen van de Me-CFZ-900-katalysator. Zoals waargenomen in deze SEM-afbeeldingen, bestaat de Me-CFZ-900-katalysator uit onregelmatige met stikstof gedoteerde koolstofmicrovezels (Fig. 2a, b). Bovendien bevestigen TEM-afbeeldingen van Me-CFZ-900 (Fig. 2c, d) de resultaten van SEM-analyse verder. De vorming van mesoporiën in de Me-CFZ-900-katalysator wordt toegeschreven aan de rol van activering van zinkchloride tijdens pyrolyse bij hoge temperatuur die de snelle dehydratie en katalytische dehydroxylering induceert, wat resulteert in de afgifte van waterstof en zuurstof in de vorm van H2 O damp. Dit activeringsproces kan het gemakkelijker maken om meer mesoporiën te produceren tijdens het stikstofdoteringsproces in de Me-CFZ-900-katalysator. Bovendien kunnen enkele blootgestelde randdefecten ook worden waargenomen dankzij de N-doping, wat gunstig is om de katalytische activiteit van ORR te bevorderen.

De SEM (een , b ) en TEM (c , d ) afbeeldingen van Me-CFZ-900
Stikstofadsorptie/desorptie-isothermen werden gebruikt om het Brunauer-Emmett-Teller (BET) specifieke oppervlak en de kenmerken van de porieverdeling te onderzoeken, zoals weergegeven in figuur 3a en aanvullend bestand 1:figuur S1. Het blijkt dat een groot INZET-oppervlak (~ 929.4 m 2 g −1 ) van Me-CFZ-900 kan worden toegeschreven aan zijn ruwe defectrijke oppervlak en mesoporeuze eigenschappen, wat goed overeenkomt met de resultaten van TEM-metingen. De BJH-poriegrootteverdeling van de Me-CFZ-900-katalysator is aangegeven in de inzet van figuur 3a. Het totale porievolume van Me-CFZ-900 met een gemiddelde poriediameter van 2,3 nm is ~ 0,53 cm 3 g −1 , maar de mesoporiën richten zich vooral op de poriediameter van 3,88 nm. Deze uitstekende eigenschappen kunnen nauw verband houden met de verbetering van de ORR-activiteit. De koolstofstructuren van verschillende op koolstof gebaseerde ORR-katalysatoren werden onderzocht met röntgendiffractiepatronen in figuur 3b. Er kunnen geen kristallijne pieken worden waargenomen, behalve twee koolstofvlakken ((002) en (101)) die zich respectievelijk op ~-24° en ~-43° bevinden, wat de amorfe koolstofstructuur suggereert [19, 20]. De sterke (002) diffractiepiek kan voornamelijk worden toegeschreven aan de roostervlakken van een typische turbostratische koolstof [28]. Er kan echter een hogere 2-theta van (002) piek en een lagere 2-theta van (101) piek voor Me-CFZ-900 vergeleken met die voor CF-900 en CFZ-900 worden verkregen vanwege de lichte vervorming in kristallijn regelmaat langs de a of b richting door dotering van stikstofatomen in de sp 2 koolstof rooster. Ook hebben alle Raman-spectra van de CF-900, CFZ-900 en Me-CFZ-900 (Fig. 3c) twee bordbanden vertoond, gelegen op ~ 1345 en ~ 1590 cm −1 , die zijn toegewezen aan de ongeordende sp 3 koolstof (D-band) en grafiet sp 2 koolstof (G-band), respectievelijk. De intensiteitsverhouding (I D /Ik G ) van de "D" -band tot de "G" -band werd gebruikt om de ongeordende en grafische graden te karakteriseren. De bijbehorende I D /Ik G voor CF-900, CFZ-900 en Me-CFZ-900 zijn respectievelijk ongeveer 0,91, 0,91 en 0,92. Een hogere ik D /Ik G verhouding van Me-CFZ-900 vertegenwoordigt een hogere stikstof-doping-efficiëntie en een meer defecte structuur, waardoor de dichtheid van de actieve plaats kan worden verhoogd en de ORR-elektrokatalytische activiteit kan worden verbeterd. Eerder rapport stelde ook voor dat de elektrische geleidbaarheid van gedoteerde koolstofkatalysatoren kan worden verbeterd door het doteren van meer stikstofatomen [25]. Om deze reden hebben we de elektrische geleidbaarheid (EC) van alle gedoteerde koolstofkatalysatoren verder getest door middel van elektrochemische impedantiespectroscopie (EIS) in 1 mmol l −1 K3 [Fe(CN)6 ]/K4 [Fe(CN)6 ] (molverhouding = 1:1) sondeoplossing, zoals weergegeven in Fig. 3d. De Bode-resultaten bewijzen dat Me-CFZ-900 een veel lagere weerstand biedt voor massatransport, wat een betere algehele geleidbaarheid suggereert in vergelijking met CF-900 en CFZ-900. Bovendien kan een hogere elektrische geleidbaarheid van Me-CFZ-900 helpen om de elektronentransportcapaciteit te bevorderen, wat resulteert in een betere ORR-activiteit in alkalisch medium.
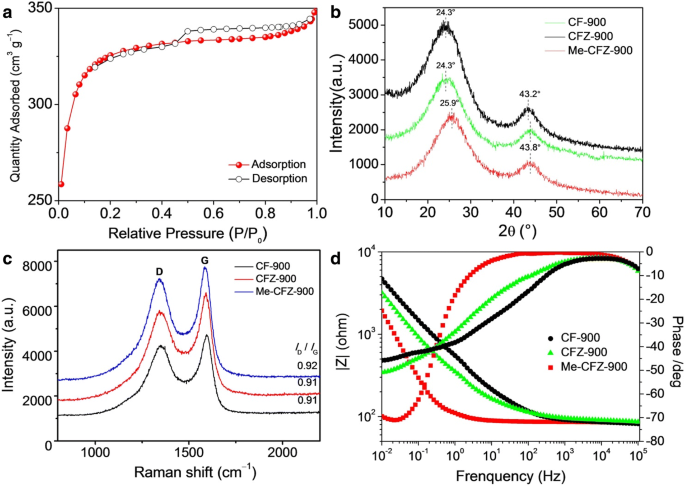
een N2 -sorptie-isothermen van Me-CFZ-900. b XRD-patronen van CF-900, CFZ-900 en Me-CFZ-900. c Raman-spectra van CF-900, CFZ-900 en Me-CFZ-900. d Bode-spectra van CF-900, CFZ-900 en Me-CFZ-900 onder een sinusgolf van 5,0 mV amplitude in het frequentiebereik van 100 kHz tot 10 MHz
De XPS-enquêtegegevens (zie Aanvullend bestand 1:Afbeelding S2) geven aan dat Me-CFZ-900 voornamelijk bestaat uit respectievelijk stikstof, koolstof en zuurstof. Het verschijnen van N1s XPS-piek suggereert de succesvolle dotering van stikstof in de koolstofstructuur, wat voldoende wordt bewezen door analyse van de C1s-piek van Me-CFZ-900. De N1s-piek van CF-900 en CFZ-900 kan echter niet worden waargenomen vanwege het lage stikstofgehalte in het bamboe-koolstof bioafval, zoals weergegeven in aanvullend bestand 1:figuur S1 en tabel S1. Bovendien werd het totale N-gehalte van drie gedoteerde N-katalysatoren bepaald door oppervlakte-XPS-analyse. Het totale N-gehalte van Me-CFZ-900 is 2,71 at.%, maar het totale N-gehalte is respectievelijk slechts 0.91 at.% voor CF-900 en 0.94 at.% voor CFZ-900. We controleren verder N1s XPS-spectra met hoge resolutie van CF-900, CFZ-900 en Me-CFZ-900, zoals weergegeven in figuur 4 (a-c). De N1s XPS-spectra van CF-900 en CFZ-900 kunnen worden gedeconvolueerd tot één piek met een bindingsenergie (BE) van ~-401,5 eV, wat overeenkomt met de grafiet-N-soort. Het N1s XPS-spectrum met hoge resolutie van Me-CFZ-900 geeft echter het bestaan aan van vier soorten stikstofgroepen:pyridine-N bij 398,3 eV, pyrrolic-N bij 398,8 eV, grafiet-N bij 401,2 eV en geoxideerd-N bij 403,4 eV [29,30,31]. De vorming van pyridine-N en pyrrolic-N is afgeleid van de thermische ontleding van melamine tijdens het activeringsproces bij hoge temperaturen. Bovendien kunnen de C1s-spectra met hoge resolutie (afb. 4d en aanvullend bestand 1:figuur S3) van de CF-900, CFZ-900 en Me-CFZ-900 worden gedeconvolueerd in vier pieken op 284,5, 285,9, 287,0 en 293,0 eV, die zijn toegewezen aan grafische sp 2 koolstof (C=C), amorf koolstof (C–C), sp 2 koolstofatomen gebonden aan stikstof (C–N), en sp 2 koolstofatomen gebonden aan zuurstof (C-O) [32], afzonderlijk. Het aandeel C–N-structuur neemt toe van 7,8 at.% voor CF-900 tot 12,2 at. % in Me-CFZ-900, wat verder bewijst dat meer stikstofatomen met succes zijn opgenomen in het koolstofraamwerk van Me-CFZ-900. Bovendien laten deze resultaten zien dat de toevoeging van melamine als promotor en stikstofbron tijdens pyrolyse bij 900 ° C de totale en gedoteerde N-gehalten kan beïnvloeden en vervolgens kan helpen bij de vorming van meer actieve plaatsen in Me-CFZ-900, wat de om de katalytische activiteit van ORR tijdens elektrochemische tests te verbeteren.
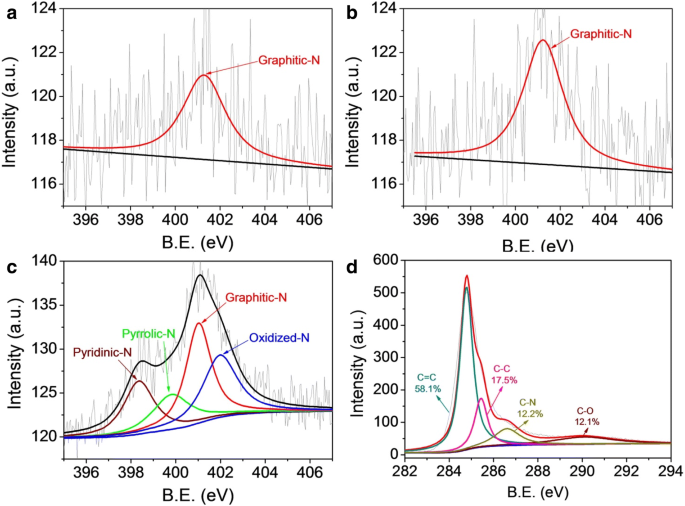
Hoge resolutie N1s XPS-spectra van CF-900 (a ), CFZ-900 (b ), en Me-CFZ-900 (c ). (d ) C1s XPS-spectra met hoge resolutie van Me-CFZ-900 (d )
Om de elektrokatalytische activiteit van ORR te evalueren, werden drie op koolstof gebaseerde ORR-katalysatoren respectievelijk gecoat op het GC-RRDE-oppervlak en verder getest met cyclische voltammetrie (CV) en lineaire sweep-voltammetrie (LSV) in O2 -verzadigd 0,1 mol l −1 KOH-oplossing. De elektrochemische resultaten van de ORR-activiteit zijn aangegeven in figuur 5a. Het blijkt dat alle CV-curven van CF-900, CFZ-900 en Me-CFZ-900 in O2 -verzadigde elektrolyt vertoont duidelijke ORR-pieken met piekpotentialen van respectievelijk 0,69, 0,84 en 0,91 V versus RHE. Er is gevonden dat de ORR-activiteit voor drie koolstofkatalysatoren de volgorde van Me-CFZ-900 > CFZ-900 > CF-900 volgt. Verder LSV-curven (Fig. 5b) opgenomen in O2 -verzadigde KOH-oplossing werden verkregen met een rotatiesnelheid van 1600 rpm om de katalytische activiteiten van CF-900, CFZ-900 en Me-CFZ-900 beter te begrijpen. De CFZ-900-gekatalyseerde elektrode vertoont betere ORR-activiteit met een halve golfpotentiaal (E 1/2 ) van 0,78 V vergeleken met de CF-900-gekatalyseerde elektrode met een E 1/2 van 0,65 V versus RHE. Trouwens, een hogere E 1/2 van ~-0,86 V en een grotere beperkte stroomdichtheid bij gegeven potentialen kan worden verkregen op de Me-CFZ-900-gekatalyseerde elektrode, die vergelijkbaar is met die van de commerciële Pt/C (20 wt%)-katalysator (zie aanvullend bestand 1:Figuur S4) en andere koolstofkatalysatoren vermeld in de literatuur (zie aanvullend bestand 1:tabel S2). Deze resultaten komen goed overeen met de resultaten van CV-metingen, wat verder de uitstekende ORR-activiteit van Me-CFZ-900 aantoont. Er wordt gesuggereerd dat de activering van zinkchloride en de toevoeging van een stikstofbron de katalytische activiteit van ORR kan verbeteren door de vorming van mesoporeuze structuren en de verbetering van de N-dopingefficiëntie tijdens het pyrolyseproces.
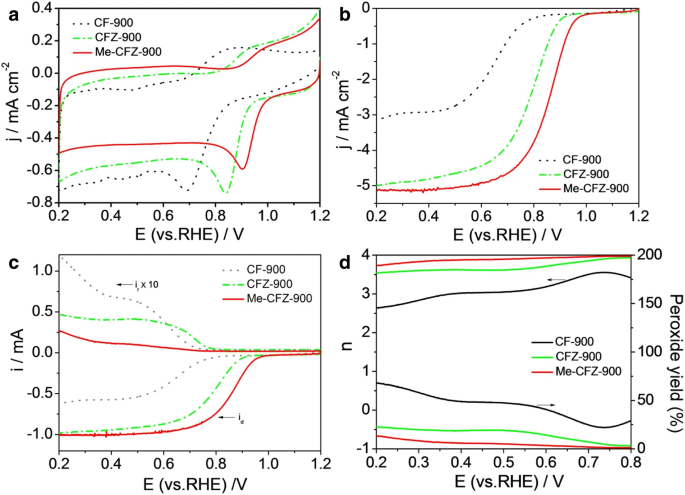
een CV-curven van CF-900, CFZ-900 en Me-CFZ-900 in O2 -verzadigd 0,1 mol l −1 KOH-oplossing. b LSV-curves voor ORR van CF-900, CFZ-900 en Me-CFZ-900 en 20 wt% Pt/C in O2 -verzadigde 0,1 M KOH-oplossing met een rotatiesnelheid van 1600 rpm. c Schijf- en ringstromen verkregen met LSV op RRDE voor CF-900, CFZ-900 en Me-CFZ-900 in O2 -verzadigd 0,1 mol l −1 KOH-oplossing. d Het corresponderende elektronenoverdrachtsnummer en H2 O2 opbrengst van c
RRDE-metingen werden uitgevoerd om inzicht te krijgen in de ORR-kinetiek van op koolstof gebaseerde katalysatoren, zoals weergegeven in figuur 5c. Bovendien, op basis van de RRDE-gegevens, werd het corresponderende elektronennummer overgedragen (n ) en peroxidesoorten (H2 O2 %) geproduceerd tijdens ORR worden berekend met behulp van vergelijkingen. respectievelijk (1) en (2). De berekeningsresultaten worden weergegeven in Fig. 5d. De H2 O2 opbrengst (<-14,0%) en het aantal elektronenoverdracht (3,45-3,95) op Me-CFZ-900 kan worden gevonden in het potentiële bereik van 0,2-0,8 V versus RHE, wat aangeeft dat een quasi-vier-elektronenroute voor het ORR-proces vergelijkbaar is naar de ORR-kinetiek van commerciële Pt/C-katalysatoren (aanvullend bestand 1:figuur S3). Vergeleken met de Me-CFZ-900, hogere H2 O2 opbrengst en een kleiner aantal elektronenoverdracht kunnen worden waargenomen op zowel de CF-900 als de CFZ-900 in hetzelfde potentiaalbereik. Echter, de H2 O2 de opbrengst op CFZ-900 is hoger dan die op Me-CFZ-900, maar het aantal elektronenoverdracht op CFZ-900 is vergelijkbaar met dat op Me-CFZ-900, wat ook een quasi-vier-elektronenroute suggereert voor het ORR-proces. Helaas heeft de CF-900 het laagste aantal elektronenoverdracht (2,64-3,56) en de hoogste H2 O2 opbrengst (22,2-68,2%), wat impliceert dat de ORR die door CF-900 wordt gekatalyseerd, voornamelijk een gemengd pad volgt van processen met twee elektronen en vier elektronen. Deze resultaten bewijzen dat de door de zinkchloride-activering bereide koolstofkatalysatoren een hogere ORR-katalytische efficiëntie en elektrokatalytische prestatie vertoonden met of zonder de toevoeging van melamine. Gecombineerd met XPS-analyse en ORR-activiteitsgegevens, vinden we dat alleen grafiet-N-soorten kunnen voorkomen in CF-900 en CFZ-900, maar ORR-katalytische activiteit vertonen, wat bewijst dat het grafiet-N een van de elektrokatalytisch actieve plaatsen kan zijn die bijdragen aan de ORR elektrokatalyse. Het is opmerkelijk dat de toevoeging van melamine aan de voorloper de vorming van pyridine-N- en pyrrolic-N-soorten met vlakke structuren kan bevorderen, die verantwoordelijk kunnen zijn voor de verbetering van de ORR-activiteit, ondersteund door de eerder gerapporteerde resultaten [29]. Bovendien kunnen de uitstekende ORR-prestaties van Me-CFZ-900 ook worden toegeschreven aan andere aspecten:(1) een hoog INZET-oppervlak en mesoporeuze structuur van Me-CFZ-900 kunnen de adsorptie en het transport van zuurstofmoleculen en de blootstelling van meer vergemakkelijken actieve plaatsen; (2) hogere elektrische geleidbaarheid van Me-CFZ-900 kan het elektronentransport van het ORR-proces effectief stimuleren; en (3) meer N-atomen worden opgenomen in de koolstofstructuur van Me-CFZ-900, wat meer stikstofrijke defecte structuren en actieve plaatsen kan produceren. Daarom is een gecontroleerde synthese van hoge gehalten aan vlakke en grafitische stikstofverbindingen essentieel om de op actieve koolstof gebaseerde katalysatoren voor ORR te produceren, maar verdere verbetering van de elektrische geleidbaarheid, stikstofdopingefficiëntie en mesoporeuze eigenschappen is de belangrijkste kwestie om de katalysator van ORR te verbeteren. activiteit.
Om het effect van de pyrolysetemperaturen op de ORR-activiteit beter te begrijpen, hebben we ook nog drie katalysatoren bereid, zoals Me-CFZ-700, Me-CFZ-800 en Me-CFZ-1000 met dezelfde pyrolyseprocedure. In Fig. 6a hebben alle bereide katalysatoren een duidelijke ORR-piek vertoond, maar Me-CFZ-900 heeft de grootste piekstroom en het meest positieve piekpotentieel. LSV-curven geregistreerd bij een rotatiesnelheid van 1600 tpm suggereren verder dat de Me-CFZ-900 meer positieve aanvangs- en halvegolfpotentialen voor ORR heeft vertoond in vergelijking met andere katalysatoren (figuur 6b). Het is duidelijk dat de ORR-katalytische activiteit van onze bereide katalysatoren sterk afhankelijk is van de pyrolysetemperatuur. De optimale temperatuur is 900 °C voor ons systeem, aangezien hoger of lager nog steeds inferieure ORR elektrokatalytische activiteit zal opleveren. Het kan te wijten zijn aan de dichtheid van actieve plaatsen en poreuze eigenschappen in katalysatoren die worden geregeld door de pyrolysetemperatuur. Om het ORR-kinetiekgedrag van verschillende op koolstof gebaseerde katalysatoren beter te begrijpen, voeren we ook de RRDE-tests uit om de H2 O2 opbrengst en aantal elektronenoverdracht (Fig. 6c, d). Het is te zien dat de ringstroom (i r ) van Me-CFZ-900 is duidelijk lager dan die van andere katalysatoren in het potentiaalbereik van 0,2-0,8 V, wat resulteert in het hoogste aantal elektronenoverdracht en de laagste H2 O2 rendement op Me-CFZ-900 op basis van de RRDE-gegevens. Deze resultaten bevestigen verder dat de beste ORR-activiteit van bereide katalysatoren kan worden verkregen bij 900 °C.
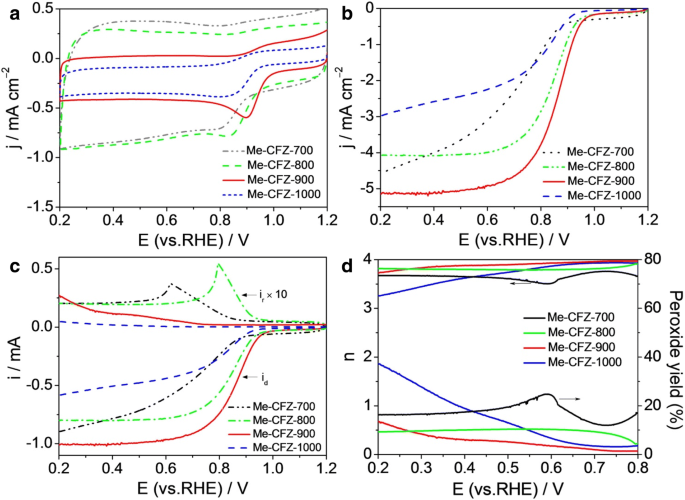
een CV en b LSV-curves van Me-CFZ-700, Me-CFZ-800, Me-CFZ-900 en Me-CFZ-1000 in O2 -verzadigd 0,1 mol l −1 KOH-oplossing. c Schijf- en ringstromen verkregen met LSV's op RRDE voor Me-CFZ-700, Me-CFZ-800, Me-CFZ-900 en Me-CFZ-1000 in O2 -verzadigd 0,1 mol l −1 KOH-oplossing. d Het corresponderende elektronenoverdrachtsnummer en H2 O2 opbrengst van c
Het ORR-katalysegedrag van Me-CFZ-900 werd verder geëvalueerd door de CV-curven en LSV-curven in N2 versus O2 -verzadigd 0,1 mol l −1 KOH-oplossingen (Fig. 7). In N2 -verzadigde elektrolyt, behalve een duidelijke capacitieve CV, kan geen zichtbare piek worden waargenomen in Fig. 7a, wat aangeeft dat deze geen kenmerk heeft. Integendeel, wanneer de CV-test wordt uitgevoerd in O2 -verzadigde elektrolyt, wordt een goed gedefinieerde ORR-piek bij ~ 0.90 V verkregen. Bovenstaande resultaten suggereren kwalitatief een ORR-elektrokatalytische activiteit van Me-CFZ-900 met een ORR-beginpotentieel van ~-1,0 V in de buurt van de commerciële Pt/C-katalysator (aanvullend bestand 1:figuur S4). Om het ORR-proces van Me-CFZ-900 beter te onthullen, werden bovendien RDE-metingen uitgevoerd met een scansnelheid van 5 mV s −1 met verschillende rotatiesnelheden (400-2500 rpm), zoals weergegeven in Fig. 7b. De beperkende diffusiestroomdichtheid neemt toe met toenemende rotatiesnelheid, wat aantoont dat de stroom kinetisch wordt geregeld. De Koutecky-Levich-plots (j −1 versus ω −1/2 ) verkregen bij 0, 2-0, 6 V vertonen een goede lineariteit en bijna parallellisme (of overlap) (Fig. 7a), wat vergelijkbare elektronenoverdrachtsgetallen aangeeft voor ORR bij vijf potentialen (0,2-0,6 V). Het gemiddelde aantal elektronenoverdrachten wordt berekend als ~ 3,84 vanaf de helling van Koutecky-Levich-plots met behulp van vergelijkingen. (3) en (4), wat verder bevestigt dat de ORR op Me-CFZ-900 een reactiepad van vier elektronen volgt, vergelijkbaar met de Pt/C-katalysator [33]. Dit resultaat komt goed overeen met de door RRDE geteste resultaten. Bovendien is de stabiliteit voor ORR-elektrokatalyse een van de grootste zorgen in de huidige alkalische brandstofceltechnologie. Voor dit doel werd de stabiliteit op lange termijn van Me-CFZ-900 gemeten door een versnelde verouderingstest (AAT) in O2 -verzadigde 0,1 M KOH-oplossing. Voordat LSV opnieuw op ORR-katalyse test, heeft de Me-CFZ-900-katalysator last van continue CV-metingen tussen 0,2 en 1,2 V vs. RHE gedurende 5000 cycli met een scansnelheid van 200 mV s −1 . Zoals getoond in Fig. 7d, vertonen LSV-curven van Me-CFZ-900 een negatieve verschuiving van slechts ~ -21 mV in halve-golfpotentiaal en ongeveer 2,0% afname in beperkte diffusiestroomdichtheid, maar er wordt geen merkbare vermindering van ORR-beginpotentieel waargenomen . Onze eerdere rapporten laten zien dat de commerciële Pt/C-katalysator gewoonlijk een negatieve verschuiving van ~ 50-mV in ORR-halvegolfpotentiaal vertoont na CV-test gedurende 5000 cycli. Deze elektrochemische resultaten suggereren een veelbelovende stabiliteit op lange termijn van Me-CFZ-900, die duidelijk superieur is aan de commerciële Pt/C-katalysator (aanvullend bestand 1:figuur S5). Samenvattend kunnen we vaststellen dat de Me-CFZ-900-katalysator die in dit werk is bereid, een veelbelovende kandidaat is voor op Pt gebaseerde ORR-katalysatoren in alkalisch medium.
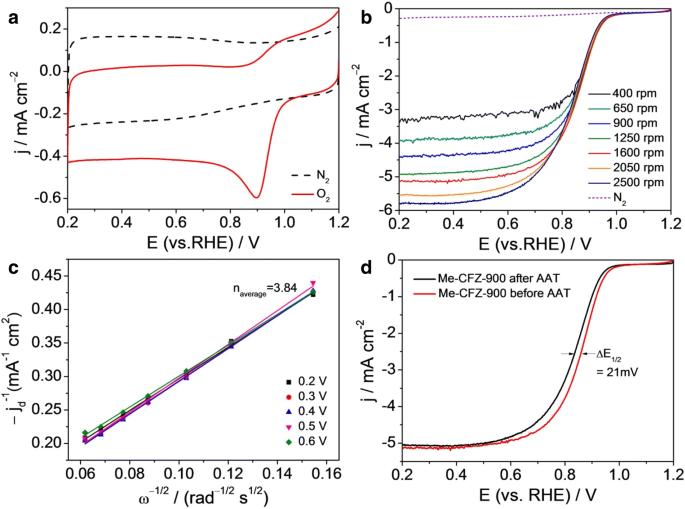
een CV-curven van Me-CFZ-900 in 0,1 mol l −1 KOH-oplossing verzadigd met N2 versus O2 . b LSV-curves van Me-CFZ-900 in O2 -verzadigd 0,1 mol l −1 KOH-oplossing bij verschillende rotatiesnelheden (400-3600 rpm). c Koutecky-Levich plots van j d −1 versus ω −1/2 verkregen van b bij gegeven mogelijkheden. d LSV-curves van Me-CFZ-900 in O2 -verzadigd 0,1 mol l −1 KOH-elektrolyten voor en na AAT-test
Conclusies
Samenvattend ontwikkelen we een nieuwe methode om nanoporeuze N-gedoteerde koolstofmicrovezels (Me-CFZ-900) afgeleid van bamboe-koolstof bioafval te bereiden voor de elektrokatalyse van zuurstofreductiereactie in alkalische media. The as-prepared Me-CFZ-900 catalyst exhibits the ORR electrocatalytic activity with a half-wave potential of ~ 0.86 V and a peak potential of ~ 0.91 V. The peroxide yield less than 14% and the average electron transfer number of 3.84 are obtained on Me-CFZ-900, further showing a quasi-four-electron reaction pathway. An only 21 mV negative shift in half-wave potential and 2.0% decline in the limited current density are observed on Me-CFZ-900 after doing the accelerated aging test. Furthermore, high BET surface area (929.4 m 2 g −1 ) and mesoporous structure of Me-CFZ-900 can facilitate the adsorption and transportation of oxygen molecule. This work can help the researchers to build the high-performance carbon-based ORR electrocatalyst derived from biomass wastes and to understand the origin of the ORR electrocatalytic activity.
Afkortingen
- AAT:
-
Accelerated aging test
- AE:
-
Auxiliary electrode
- BET:
-
Brunauer-Emmett-Teller
- CF:
-
Carbon microfibers
- CV:
-
Cyclic voltammetry
- E 1/2 :
-
Half-wave potential
- E ORR :
-
Onset potential
- E p :
-
Peak potential
- FE-SEM:
-
Field-emission scanning electron microscopy
- GC:
-
Glassy carbon
- HR-TEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- LSV:
-
Linear sweep voltammetry
- Me-CFZ-900:
-
Nitrogen-doped porous carbon microfibers
- ORR:
-
Oxygen reduction reaction
- Pt/C:
-
Platinum/carbon catalyst
- RDE:
-
Rotation disk electrode
- RE:
-
Reference electrode
- RHE:
-
Reversible hydrogen electrode
- RRDE:
-
Rotation ring-disk electrode
- SCE:
-
Saturated calomel electrode
- WE:
-
Working electrode
- XPS:
-
Röntgenfoto-elektronenspectroscopie
Nanomaterialen
- Nieuwe voedings- en doseringsbrochure van Gericke
- Nieuwe doorbraken in FDM van Stratasys
- Een nieuw boek van Dominique Cardon
- Geactiveerde koolstofvezels met hiërarchische nanostructuur afgeleid van afval katoenen handschoenen als hoogwaardige elektroden voor supercondensatoren
- Magnetische koolstofmicrosferen als herbruikbaar adsorbens voor het verwijderen van sulfonamide uit water
- Een eenvoudige aanpak voor het synthetiseren van fluorescerende koolstofkwantumstippen uit tofu-afvalwater
- Zwaar grafiet-stikstof zelfgedoteerde koolstof met hoge porositeit voor de elektrokatalyse van zuurstofreductiereactie
- Synthese en supercondensatorprestaties van met polyaniline/stikstof gedoteerde mesoporeuze koolstofcomposieten
- Zeer actieve en stabiele Fe-N-C-zuurstofreductie-elektrokatalysatoren afgeleid van elektrospinning en in-situ pyrolyse
- Eenvoudige synthese van met stikstof gedoteerde microporeuze koolstofbollen voor hoogwaardige symmetrische supercondensatoren
- Eenvoudige voorbereiding van koolstofnanobuisjes-Cu2O-nanocomposieten als nieuwe katalysatormaterialen voor reductie van P-nitrofenol



