Een hydrothermische synthese van Fe3O4@C hybride nanodeeltjes en magnetische adsorptieprestaties om zware metaalionen in waterige oplossing te verwijderen
Abstract
Geavanceerd materiaal met een kern en een hoog specifiek oppervlak wordt beschouwd als een effectief materiaal om zware metalen uit waterige oplossingen te verwijderen. Een kern-gepelde Fe3 O4 @C hybride nanodeeltjesaggregaten met milieuvriendelijk kanaal in de studie. Bovendien kan de hogere blootstelling van adsorptielocaties worden bereikt voor de speciale configuratie die een hoger Brunauer-Emmet-Teller (BET)-oppervlak bereikt tot 238,18 m 2 g −1 . Zo wordt een efficiëntere verwijdering van zware metaalionen verkregen, Pb (II), Cd (II), Cu (II) en Cr (VI) tot respectievelijk 100, 99,2, 96,6 en 94,8%. Bovendien zijn de producten na adsorptie gemakkelijk te scheiden van de waterige oplossingen, vanwege de relatief grote submicrometergrootte en de versterkte externe magnetische velden die worden geïntroduceerd door de op ijzer gebaseerde kernen. We bieden een ideale modus om zware metaalionen te verwijderen met Fe3 . met kernschil O4 @C onder de waterbehandelingsvoorwaarde. Een nieuwe benadering is verduidelijkt dat kern-schil nano-/microfunctionele materialen goed op grote schaal kunnen worden gesynthetiseerd die op veel gebieden worden gebruikt, zoals milieusanering, katalysatoren en energie.
Achtergrond
Met de stem van milieubescherming is constant en stijgende, er is steeds meer aandacht voor het toxische effect dat verwijst naar de menselijke gezondheid en milieuvervuiling door verontreiniging met zware metalen [1,2,3]. Het verwijderen van zware metalen elementen uit industrieel afvalwater voorafgaand aan lozing wordt cruciaal [4]. Tot op heden werden de afgelopen decennia ionenuitwisseling, coagulatieprecipitatie en een reeks traditionele technologieën toegepast om zware metalen uit afvalwater te verwijderen [5, 6]. Het besef dat conventionele technieken aanzienlijke voordelen voor de mens opleveren, bracht ook nadelen aan het licht die zowel vanuit het management als de technische kant worden gekenmerkt, zoals hoge bedrijfskosten, extra vorming van giftig slib en onvolledige metaalverwijdering [7,8,9]. Aan de andere kant is het beheersen van de deeltjesgrootte, de morfologie van adsorberende materialen, een van de efficiënte en innovatieve oplossingen gebleken om dat soort problemen op te lossen. Holle bollen, nanodraden en nanobuisjes hebben een betere adsorptieprestatie om bij te dragen aan de verwijdering van zware metalen in referenties [10,11,12,13]. Verder zijn onderzoeken gericht op het nieuwe materiaal dat de kern-schaalstructuur bevat met de kern-leegte-schaalfunctie. Het is bewezen vanwege zijn voordelen in vergelijking met dezelfde grootte van vaste tegenhangers, zoals de geldigheid daarvan in de veranderingen van oppervlakten, brekingsindex, lagere dichtheid en accommoderend volume, wat leidt tot een grote bijdrage, zowel vanuit de aspecten van eigenschappen en functies [14, 15]. Deze unieke structuur met afstembare vorm, compositie en interieurarchitectuur is dus een opwindende richting om milieusanering na te streven.
Er is veel literatuur over kern-schaalstructuurmaterialen. Guo [16] had kooibel Ag@TiO2 . gemaakt materialen, en de studie bracht betere fotokatalytische en elektrochemische eigenschappen tot uitdrukking. Liu [17] bereide kern-shell Fe3 O4 polydopamine nanodeeltjes die een mooi potentieel vertoonden op het gebied van medicijnondersteuning, katalysatordrager en koolstofadsorbens. Voor zover wij weten, is de hulp van verwijderbare of opofferingssjablonen (bijv. polymeer silica [18], bollen [19], koolstof [20] en ionische vloeistoffen [21]) van de gewenste omhulsels belangrijk bij de algemene synthese van kern- shell hybride nanodeeltjes structuren. De meest beschikbare materialen met kern-schilstructuur worden echter gesynthetiseerd door processen met meerdere sjablonen die zich voornamelijk richten op de relatief eenvoudige configuraties, zoals één samenstelling in deeltjes met één schil. Bovendien ontbreekt het nog steeds aan een methode voor het verwijderen van zware metaalionen met een algemene benadering, vergezeld van een verdere versterking van de haalbaarheid van de geavanceerde materialen met kern-schaalstructuren, inclusief tijd en kosten in het constructieproces van complexe nanostructuren die werden beperkt door synthesesjablonen en routes met meerdere sjablonen, die zowel technisch als ecologisch een wens zijn geworden.
De synthese van het magnetische functionele nanocomposiet is een effectieve en handige manier om de scheiding tussen het adsorbens en de oplossing voor het uitbreiden van de magnetische scheiding op te lossen [22]. In dit proces worden steeds meer covalent geïmmobiliseerde polymeer, nieuwe moleculen en anorganisch materiaal in het oppervlak van magnetische nanodeeltjes geplaatst; het zijn ook nuttige techniekroutes voor de behandeling van afvalwater met giftige zware metaalionen [23]. Bijvoorbeeld nieuwe gesynthetiseerde chitosan-gemodificeerde magnetische nanocomposieten [24] en monodispers Fe3 O4 @silica core-shell structuur composiet magnetische nanodeeltjes core-shell microsferen [25] worden gerapporteerd. Ondanks dat deze magnetische nanocomposieten gemakkelijk van de oplossing kunnen worden gescheiden door het adsorptieproces op basis van de externe magnetische, moet er nog steeds verder worden nagedacht over de speciale voorwaarden, zoals de toepasbaarheid van sterk zuur afvalwater.
Er zijn de laatste tijd veel onderzoeken gedaan naar op koolstof gebaseerde nanogestructureerde materialen. Wildgoose [26] presenteerde dat dit soort materialen duidelijke voordelen hebben in termen van kosten, alkalicorrosieweerstand, specifiek oppervlak en adsorptiecapaciteit. Uchida [27] wees erop dat de carboxyl-functionele groepen gemakkelijk kunnen worden gegenereerd op het oppervlak van koolstof en vervolgens de adsorptiecapaciteit van zware metaalionen verder vergroten. De fatale tekortkoming van de moeilijkheid om ze uit een oplossing te verwijderen, veroorzaakt door de kleine grootte van koolstofdeeltjes, beperkte echter de toepassing ervan in de behandeling van afvalwater van zware metalen. Aangezien met koolstof gecoat magnetisch nanodeeltje een richting is voor media in afvalwaterzuivering, toonde het geavanceerde effecten op de adsorptiecapaciteit en scheidingseigenschap in het externe magnetische veld. Er is veel meer aandacht toegenomen [28,29,30,31,32,33,34,35]. Zhang [36] bereidde magnetische holle koolstofnanosferen voor die werden gebruikt bij het verwijderen van chroomionen. Om zware metalen te verwijderen, rapporteerden Wang-groepen [37] een case study van Fe-nanodeeltjesmaterialen. Deze eerdere studies gaven aan dat het overeenkomstige toekomstige werk moet verwijzen naar zeer efficiënte adsorbentia voor zware metaalionen met gemakkelijke scheiding en grote adsorptiecapaciteit. Ondertussen moet erop worden gewezen dat er zeldzame studies zijn over Fe3 . met kernschil O4 @C hybride nanodeeltjesaggregaten tot nu toe.
In deze studie hebben we koolstofmicrosferen met magnetische kernen gemaakt. Er werd ook een beknopte strategie voorgesteld om Fe3 . met kernschil te synthetiseren O4 @C hybride nanodeeltjesaggregaten, een geavanceerd materiaal voor het verwijderen van zware metaalionen met de sterkte zuiverheid, oppervlakten en adsorptiecapaciteit. Vergeleken met traditionele productietechnologie van Fe3 O4 materialen, de voordelen zijn duidelijk. Het drukt niet alleen een groter oppervlak en stabiele configuratie uit, maar ook de verwijderingssjabloon die niet wordt beïnvloed door productmorfologie. Ons onderzoek biedt een hogere mate van de actieve sites [38, 39]. Het adsorbens kan gemakkelijk worden gescheiden wanneer de externe magnetische velden worden geïntroduceerd, die worden veroorzaakt door de op ijzer gebaseerde nanodeeltjes [40, 41]. Daarom is de verkregen kern-shelled Fe3 O4 @C hybride nanodeeltjesaggregaten vertonen superieure adsorptiecapaciteit voor zware metaalionen met de route milieuvriendelijk, massaproductie en kostenvoordelen.
Experimenteel
Materialen en synthese
Synthese van Core-Shelled Fe3 O4 Hybride nanodeeltjesaggregaten
In typische synthesestappen wordt 0,72 g Fe(NO3 )3 ·9H2 O, 0,0086 g NH4 H2 PO4 , 0,008 g Na2 SO4 ·10U2 O en 3 g glucose werden respectievelijk opgelost in gedestilleerd water, alles bij elkaar gemengd in een volume van 90 ml, gedestilleerd water aan het mengsel toegevoegd en gedurende 10 minuten continu gemengd met een basische magnetische roerder. Vervolgens verschoof het mengsel in 100 ml met Teflon beklede roestvrijstalen autoclaaf gedurende 180 ° C, 48 uur. Nadat de reactie was voltooid en op natuurlijke wijze tot kamertemperatuur was afgekoeld, werd de zwarte voet verkregen en verschillende keren gewassen met gedeïoniseerd water en absolute ethanol, waarna de zwarte voet de hele nacht bij 65 ° C onder vacuüm werd gedroogd en ten slotte werd verkregen voorlopers door gecalcineerd bij 450 °C met een snelheid van 3 °C min −1 behield vervolgens verwarming met een sequentiële koolmonoxide / argongasstroom (4 uur) en afgekoeld tot de omgevingstemperatuur. De Fe3 O4 @C-monster werd verkregen. Zoals beschreven in Schema 1 de hydrolyse van Fe 3+ leidt tot een Fe-oxidelaag in nanometernauwkeurigheid. Ondertussen wordt sucrose verkoold. Daarna zullen microsferen van Fe-C-O-composietmateriaal in situ ontstaan tijdens de badverwarmingsreactie door middel van calcineringssecties en vervolgens Fe3 met kernomhulsel krijgen O4 @C hybride nanodeeltje.
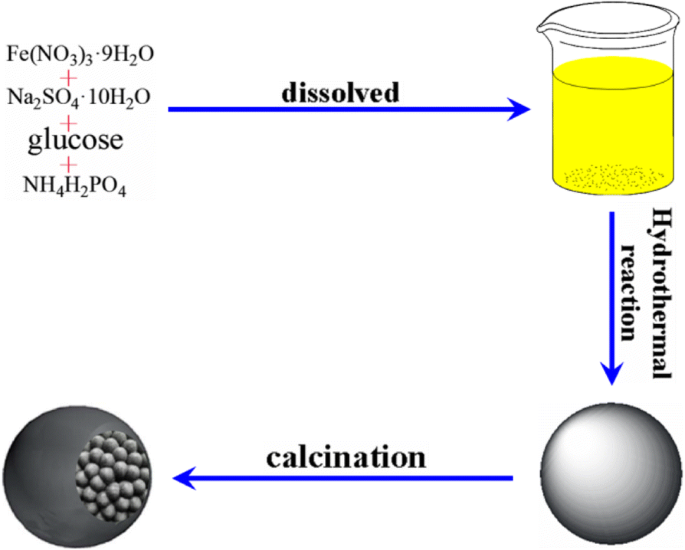
Syntheseroute van de kern-gepelde Fe3 O4 @C hybride nanodeeltje
Karakterisering
De fasesamenstelling van bereid materiaal werd geanalyseerd met röntgendiffractie (XRD), die werd genomen bij 2θ = 20°–90° door Rigaku D/max-A diffractometer met Co Kα-straling. FTIR (Fourier-transformatie-infraroodspectroscopie, Thermo Nicolet AVATARFTIR 360) werd uitgevoerd om de FTIR-tekens van de monsters vast te leggen binnen het bereik van 400–4000 cm −1 ook. AMRAY 1000B SEM (Scanning-elektronenmicroscoop), HR-TEM (High-resolution transmissie-elektronenmicroscoop, JEOL JEM-2100) (200 Kv) en geselecteerde gebiedselektronendiffractie (SAED) werden geïmplementeerd om de morfologie van het monster, de microstructuurfunctie, en de roosterstructuur. Bovendien werd Micromeritics Tristar-apparaat bij 350,15 ° C genomen om de processen van stikstofadsorptie en -desorptie te meten; Brunauer-Emmet-Teller (BET) werd gebruikt om de specifieke oppervlakten te bespreken; kwantitatieve analyse van atoomabsorptiespectroscopie (AAS) zal worden uitgevoerd door de Hitachi Z2000-spectrofotometer, die is uitgerust met holle kathodelampen en een acetyleen-luchtvlam. De magnetische prestatie van geprepareerd materiaal werd gemeten met een vibrerende monstermagnetometer (VSM).
Experimenten voor het verwijderen van zware metaalionen
Bij kamertemperatuur werd overwogen om een reeks experimenten uit te voeren om zware metaalionen te verwijderen. Allereerst worden Pb (II), Cd (II), Cu (II) en Cr (VI) toegevoegd in vier gesloten containers; daarna 0,1 M HCl en 0,1 M NH3 •H2 O worden gebruikt om de pH in te stellen op 3, en vervolgens de adsorptieoplossingen met het uiteindelijke volume van 50 ml en een concentratie van 10 mg L −1 waren verkregen. Vervolgens, onder voortdurend roeren, 20 mg als bereid Fe3 O4 @C-monster werd toegevoegd aan de bovenstaande oplossingen. Tijdens het adsorberende reactieproces werd bijna 1,0 ml van elke bovengenoemde oplossing uitgeloogd over de verschillende perioden (respectievelijk (0, 0,5, 1, 1,5, 2, 4, 6, 10 en 24 uur) door middel van een gebruik van een penbuis die voorzien van membraanfilter, eindelijk gedempt voor toepassing op AAS-maat.
Resultaat en discussie
Fysisch-chemische kenmerken van kerngepeld Fe3 O4 @C Nanosfeer
De XRD-patronen van het gesynthetiseerde Fe3 O4 @C hybride nanodeeltjesaggregaten en zijn voorloper werden getoond in Fig. 1, waaruit duidelijk blijkt dat het productieproces een hogere kristalliniteit heeft dan de voorloper door calcinaties bij 450 ° C. De voorbereide monsters vertoonden composietmaterialen die overeenkomen met kubische (f c c) Fe3 O4 (JCPDS (Joint Committee on Powder Diffraction Standards) kaart nr. 75-0033). De diffractiepiek bij 21,5 °, zoals weergegeven in de patronen, moet worden toegewezen aan het (002) vlak van grafietkoolstof dat ook direct kan worden gevonden door SEM en TEM.
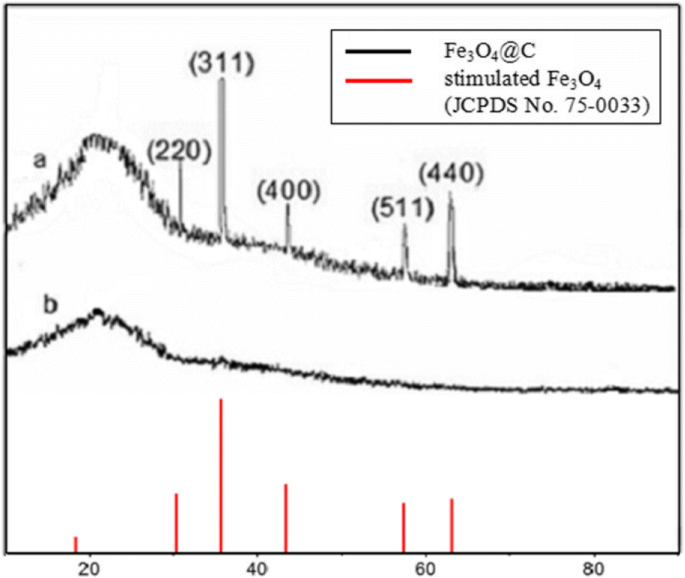
XRD-patronen van Fe3 . met kernschil O4 @C hybride nanodeeltjesaggregaten en zijn voorloper (a—Fe3 O4 @C hybride nanodeeltjesaggregaten; b—de voorloper)
SEM-afbeeldingen van de voorloper en Fe3 . met kernschil O4 @C hybride nanodeeltjessynthese geproduceerd via calcinering bij 450 ° C bij verschillende vergrotingen werden weergegeven in Fig. 2a-c. Het is duidelijk dat, afgezien van een kleine minish in grootte, de gesynthetiseerde Fe3 O4 @C behield de morfologie van de bereide voorloper die microsferen ca. met de grootte van 700 nm uniform. Figuur 2b, c beschreef duidelijk de hybride kern-schaalstructuur van de Fe3 O4 @C; het kan worden bewezen door de mesosferen. Figuur 2c toonde ook aan dat het gesynthetiseerde poeder is gemaakt van de deeltjes van nanogrootte op basis van de resultaten van de deeldeeltjes met een gedeeltelijke breuk. De bovenstaande gespleten microsferen zijn waarschijnlijk afkomstig van het snelle massatransport door de schelpen. Figuur 2d, e beschreef ook de structuur van Fe3 O4 @C. Er is een zichtbare kern-schaal binnenstructuur in figuur 2d, wat duidelijk maakt dat de Fe3 O4 nanodeeltjes zijn uiteraard verdeeld in de amorfe koolstof. Dit komt overeen met het SEM-resultaat. Aan de andere kant komen HRTEM (Fig. 2e) en XRD ook goed overeen, waaruit blijkt dat de roosterafstand (0,297 nm) overeenkomt met (220) vlakafstand van kubische Fe3 O4 . Uit het SAED-resultaat bleek dat de Fe3 O4 nanodeeltjes waren zeer kristallijne eenkristallen. Het unieke hybride kern-schaalmonster kan dus een hogere respons-efficiëntie van de adsorptieplaats op de doeladsorbaten hebben, wat kan worden gebruikt op het gebied van milieubescherming.

SEM-afbeelding van geprepareerde voorloper (a ). SEM-afbeeldingen (b , c ), TEM-afbeelding (d ), HRTEM-microfoto (e ), en elektronendiffractie met geselecteerd gebied (f ) van as-gesynthetiseerde kern-shelled Fe3 O4 @C hybride nanodeeltjesaggregaten verkregen door calcineren bij 450 °C
De magnetische eigenschappen van zoals voorbereid werden geëvalueerd met behulp van VSM, en de resultaten worden getoond in Fig. 3. De magnetische verzadigingswaarde wordt bereikt 53 emu/g vergeleken met kale Fe3 O4 microsferen (67,55 emu/g). De hoge magnetisatiewaarde van het voorbereide materiaal is duidelijk te zien. De inzet in Fig. 3 laat zien wanneer een extern magnetisch veld werd aangelegd, de deeltjes worden aangetrokken door de magneet, waardoor de waterige oplossing helder en transparant blijft.
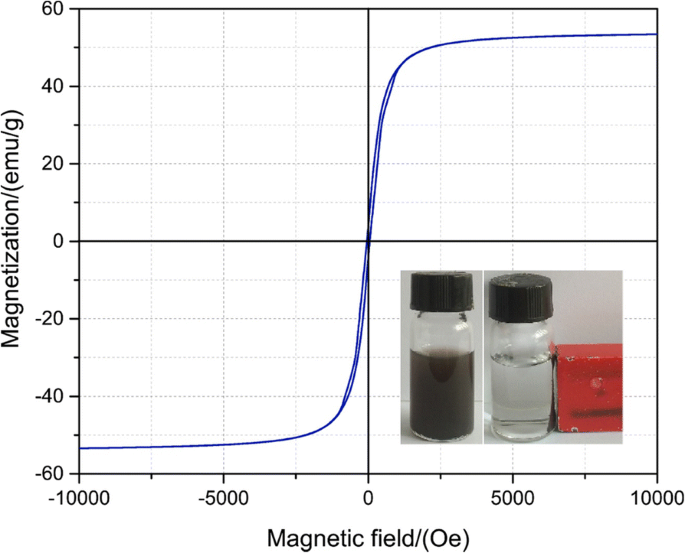
Magnetiseringslusmetingen
Figuur 4a toont de adsorptie- en desorptie-isotherm van de monsters, terwijl figuur 4b de poriegrootteverdeling van de verkregen monsters toont, beide kwamen van respectievelijk voor en na calcinaties. De isotherm is een representatieve isotherm van mesoporeus materiaal op basis van het klassieke type IV. De poriegrootteverdeling door calcinaties toonde duidelijk de gemiddelde poriediameters van 7,5 tot 9,1 nm, kleiner dan de voorloper. Ondertussen nam het BET-oppervlak van het monster aanzienlijk toe van 9,74 tot 238,18 na calcinaties, wat hoger is dan de meeste rapporten [36, 37]. Bovenstaande gaf ook aan dat de zich onthoudende Fe3 O4 @C-monsters waren een materiaal met losse mesoporeuze structuur, wat een voordeel is voor de verbeterde adsorptieprestaties.
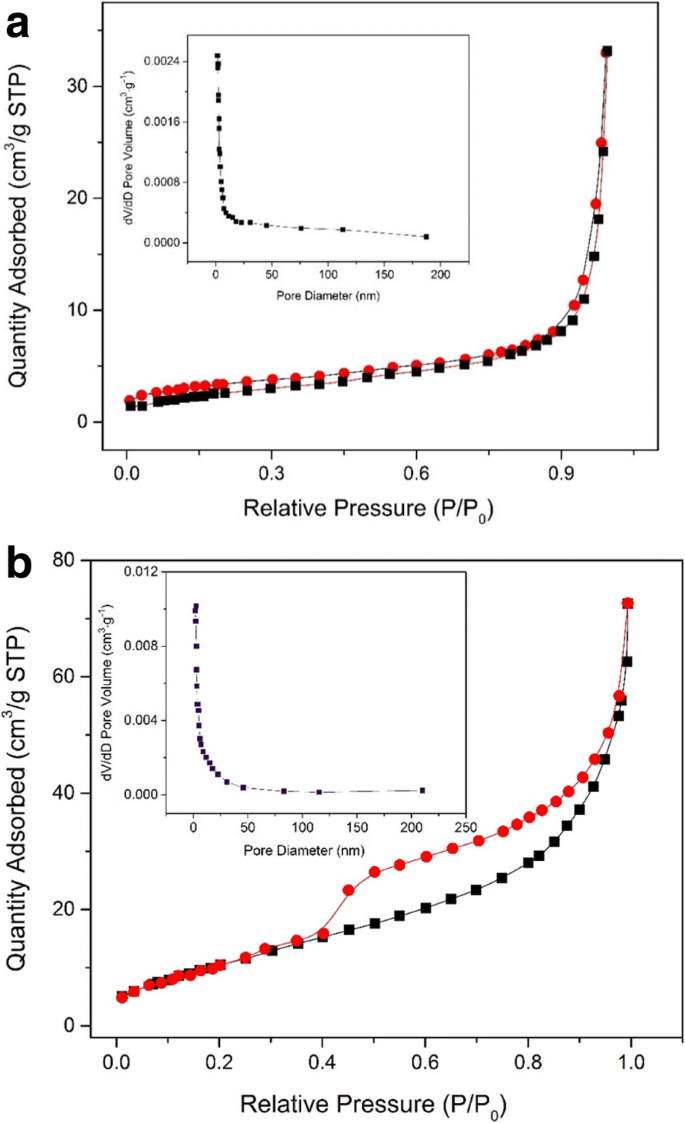
Stikstofadsorptie-desorptie-isotherm en Barrett-Joyner-Halenda (BJH) poriegrootteverdelingsgrafiek (inzet) van het voorbereide monster vóór (a ) en na (b ) calcinaties
Opname van zware metaalionen door Fe3 O4 @C
Pb (II), Cd (II), Cu (II) en Cr (VI) werden gekozen als adsorbaten voor het bestuderen van de absorptiecapaciteit van bereid Fe3 O4 @C, en ze werden bij kamertemperatuur in de pH = 3 geplaatst om kinetische experimenten uit te voeren. Zoals getoond in Fig. 5, werden alle adsorptie-ionen met succes geadsorbeerd door het bereide monster, de efficiëntie bereikte 100% voor Pb (II), 99,2% voor Cd (II), 96,6% voor Cu (II) en 94,8% voor Cr (VI), respectievelijk. Het heeft een bredere toepassing en een hogere verwijderingsefficiëntie dan de vorige studie [42]. Deze hoge opname-efficiëntie kan worden toegeschreven aan de intrinsieke voordelen van hybride kern-schilstructuren met hoge specifieke oppervlakten, die de Fe3 O4 @C-voorbeeld met meer actieve sites voor het verwijderingsproces. Bovendien kan het gemakkelijk worden teruggewonnen na adsorptie vanwege de relatief grote submicrometerdeeltjesstructuren. Het kan ook gemakkelijk worden waargenomen dat de Pb (II) de hoogste snelheid vertoonde die redelijk is vanwege de adsorptie, gewoonlijk door ionenuitwisseling, en er bestaat elektrostatische interactie van de vrije metaalionen en het oppervlak van het adsorbens. Dus, Cd, Cu en Cr zijn lichte en gemakkelijke desorpties na ionenuitwisseling, Pb (II) is het tegenovergestelde [43,44,45,46,47,48,49].
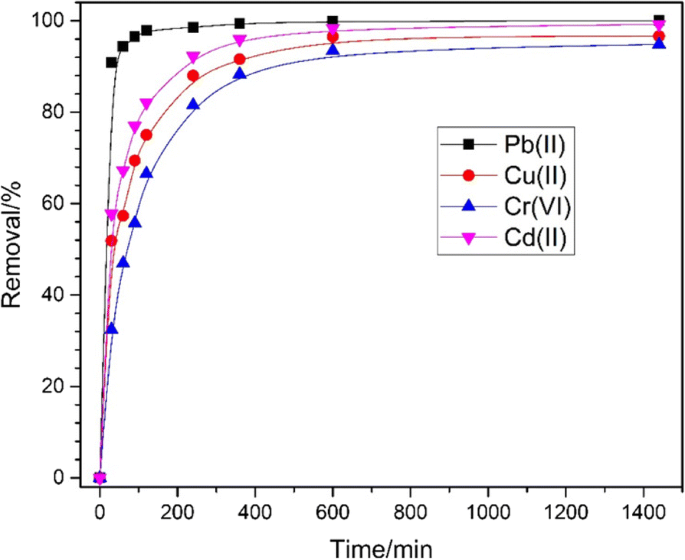
Verband tussen de verwijderingsefficiëntie en tijd voor de adsorptie van Pb (II), Cd (II), Cu (II) en Cr (VI) door Fe3 O4 @C (400 mg L −1 ) monster met initiële concentraties van zware metaalionen als 10 mg L −1 , respectievelijk
FTIR-spectra van het met zware metalen geladen Fe3 O4 @C
Afbeelding 6 toont het voorbeeld met de hoogste Pb 2+ opname aan het begin en einde van de adsorptie, die werd gebruikt in de studie om de interactie tussen Fe3 te achterhalen O4 @C en zware metaalionen. Verder is de voorwaartse en achterwaartse trilling van de −OH-groep van H3 O + via ionenuitwisseling of fysisorptie van watermoleculen, wat leidde tot een brede trillingsband van 3475,26 cm −1 . De piek bij 2304,20 cm −1 wordt toegeschreven aan de vibratie van CO2 , terwijl de piek op ca. 1625 cm −1 werd meestal veroorzaakt door de O-H-curve. De piek op 1605,45 cm −1 was van carboxylgroepen (−C=O−). De belangrijkste bijdrage van de andere pieken in het bereik van 400-1000 cm − 1 werd normaal geassocieerd met O-metaalbindingen. Het verschil van de piekpositie en intensiteit van metaal O in zowel het begin als het einde van de adsorptie van Pb 2+ impliceert dat Pb 2+ wordt geladen op de Fe3 O4 @C monster sterk.
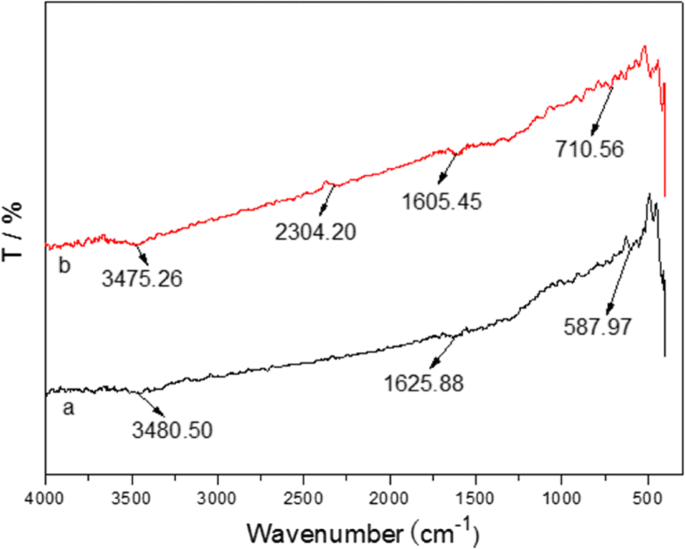
FTIR-spectra van het bereide Fe3 O4 @C voorbeeld voor (a ) en na (b ) adsorptie van Pb (II)
Adsorptiekinetiek
Er werden verschillende teksten opgesteld om het adsorptievermogen en de kinetiek van de Fe3 te bespreken O4 @C hybride nanodeeltjesaggregaten in deze sectie. Pb 2+ werd voorbereid voor verwijderingsexperiment uit de waterige oplossingen bij pH = 3. Bereid daarna het volume van 50 ml van de 10, 30 en 50 mg L −1 initiële oplossingen, 20 mg adsorbentia, toegevoegd aan de Pb 2+ oplossingen in erlenmeyers van 100 ml met een adsorptie van respectievelijk 30 °C. Met de verschillende perioden (0, 7, 14, 21, 28, 35, 60, 180, 480 en 1440 min), werd ongeveer 1 ml uit elke oplossing geëxtraheerd, ze zullen worden gebruikt voor AAS-analyse. vgl. (1) toont het pseudo-tweede-orde kinetische snelheidsmodel [50]:
$$ \frac{t}{q_t}=\frac{1}{k_2{q}_e^2}+\frac{1}{q_e}t $$ (1)waar q e is Pb 2+ geadsorbeerd per massa-eenheid wanneer het adsorbens in evenwicht is, q t (mg g −1 ) betekent de Pb 2+ geadsorbeerd op eenheidsmassa gedurende de tijd t (min); k 2 (g mg −1 min −1 ) is de snelheidsconstante van het kinetische model, dat een pseudo-tweede-orde is. Afbeelding 7a toont de reactietijd van de Fe3 O4 @C-voorbeeld in Pb 2+ verwijdering bij de verschillende beginconcentraties (10, 30 en 50 mg L −1 ), dan is het efficiëntieverschil gemakkelijk te achterhalen. Het resultaat gaf de Fe3 . aan O4 @C-monsters drukten hogere adsorptieprestaties uit, en waren ook gemakkelijk te scheiden. Figuur 7b beschreef de adsorptiesnelheid bij de verschillende concentraties van Pb 2+ (10, 30 en 50 mg L −1 ). De adsorptiesnelheid was negatief gerelateerd aan de initiële concentratie. Deze trend kan als volgt worden onthuld, er is slechts een deel van de oppervlakte-actieve plaats gebruikt tijdens de adsorptie. Namelijk met de concentratie van Pb 2+ Toen de adsorptie toenam, begon de adsorptie eerst op de plaatsen met hoge energie, gevolgd door de verzadiging van de plaatsen met lage energie die uiteindelijk de afname van de adsorptiesnelheid veroorzaakten [51]. Tabel 1 toont de correlatiecoëfficiënt (R 2 ) bereikte 0,999 in deze studie; het geeft duidelijk aan dat het adsorptieproces goed overeenkomt met het pseudo-tweede-ordemodel.
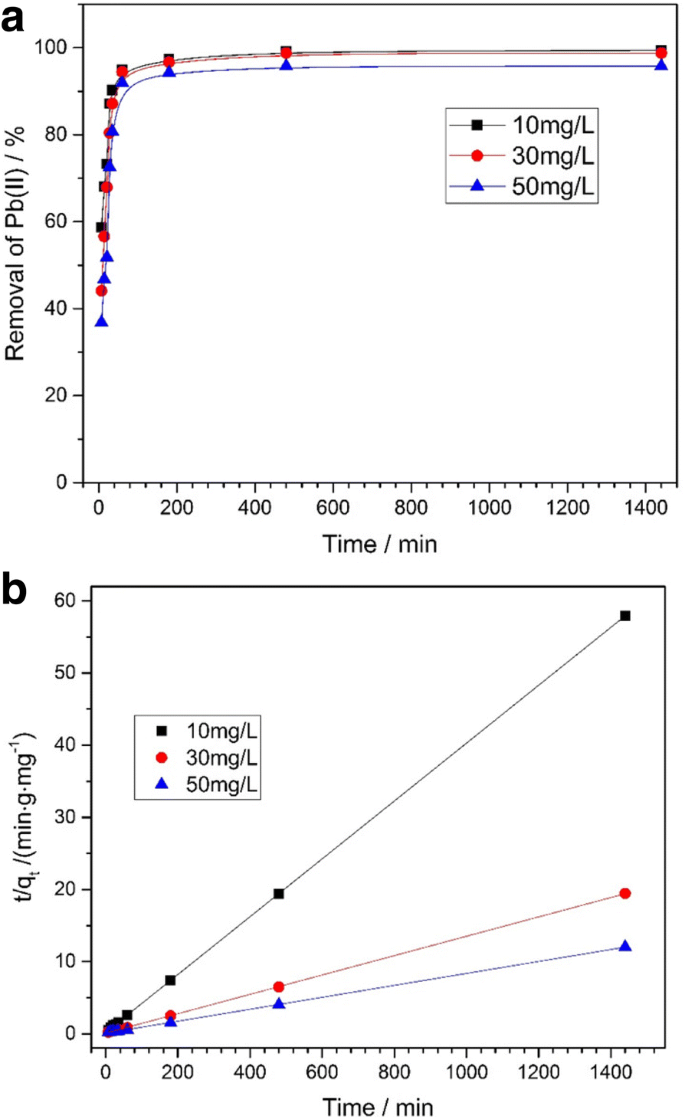
een Relatie tussen de verwijderingsefficiëntie en tijd voor de adsorptie van Pb(II) door Fe3 O4 @C (20 mg) bij initiële Pb2+-concentraties van 10, 30 en 50 mg L −1 , respectievelijk. b Pseudo-tweede-orde kinetiek voor adsorptie van Pb2+ op de Fe3 O4 @C-voorbeeld (T = 30 °C; absorberende dosis =400 mg L −1 ; Pb2+ concentraties:a = 10 mg L −1 , b = 30 mg L −1 , c = 50 mg L −1 )
Adsorptie-isotherm
In dit deel werd 20 mg adsorbens toegevoegd aan de erlenmeyers van 100 ml en Pb 2+ Er werden ook oplossingsmonsters bereid (10–60 mg L −1 , 50 ml, pH = 3). Bij 30 ° C werden de bovenstaande conische kolfmonsters in een afgesloten toestand bewaard en in een thermostatische schudder geplaatst (24 uur, 150 rpm) en daarna door centrifugeren om de bovenstaande vloeistof te verkrijgen, gemeten met AAS. Afbeelding 8a toont de voorbereide Fe3 O4 @C adsorptievermogen voor Pb 2+ . De Langmuir- en Freundlich-isothermen werden geïmplementeerd om het adsorptieverloop in het onderzoek te verklaren. Het proces vond plaats in een gelokaliseerde monolaag, zonder interactie tussen adsorbaatmoleculen [52]. Bovendien is de site voor het adsorbaatmolecuul wie het eerst komt, het eerst maalt, geen verdere adsorptie op dezelfde site. De Langmuir-isotherm wordt als volgt beschreven:
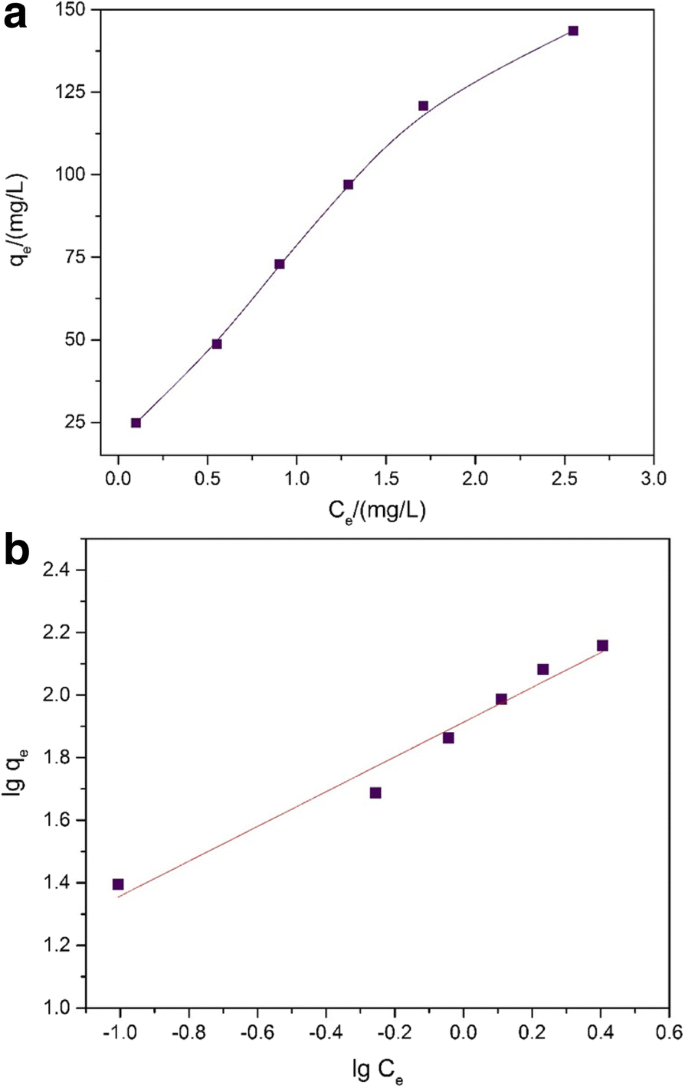
een Adsorptie-isotherm voor Pb2+ op de Fe3 O4 @C-voorbeeld (T = 30 °C; adsorberende dosis =400 mg L −1 ; Pb2+-concentratie =10–60 mg L −1 ). b Freundlich lineaire plots voor adsorptie-isotherm van de Fe3 O4 @Csample over de verwijdering van Pb2+ bij 30 °C
$$ \frac{C_e}{q_e}=\frac{C_e}{q_{\mathrm{max}}}+\frac{1}{k_L{q}_{\mathrm{max}}} $$ (2 )waarbij de theoretische maximale monolaag sorptiecapaciteit wordt weergegeven als q max (mg g −1 ), nemend k L om de constante van Langmuir uit te drukken (L mg −1 ), en C e is de concentratie van Pb (II) aanvankelijk. Terwijl de Langmuir-isothermen niet het ideale gevolg voor onze studie bereiken, betekent dit dat het niet goed geschikt is. Overeenkomend met de lineaire vorm als Vgl. (3) is een ander veelvoorkomend empirisch model als de Freundlich-isotherm, die de hypothese heeft dat, samen met de stijging van de bezettingsgraad van de site, er van tevoren stevigere bindingsplaatsen worden vastgebonden en de intentie ervan dienovereenkomstig afneemt [52].
$$ \lg {q}_e=\lg {k}_F+\frac{1}{n}\lg {C}_e $$ (3)Hier, k F betekent de Freundlich-constante (mg g −1 )(L mg −1 ) 1/n , en 1/n drukt de heterogeniteitsfactor uit. De specifieke inhoud van k F en 1/n , geïdentificeerd met een plot van lg q e versus LG C e , wordt getoond in Fig. 8b. Tabel 2 laat een gunstige adsorptieconditie zien [52, 53]. Het gaf de reden aan dat de Freundlich-exponent n groter is dan 1. Er kan worden geconcludeerd dat het adsorptie-effect van Pb 2+ was afhankelijk van de hybride kern-schilstructuren of heterogeniteit voor de oppervlakken van de Fe3 O4 @C-voorbeeld. In de tussentijd, R 2 , de correlatiecoëfficiënt van het monster, reikt tot 0,9712, wat betekende dat het Freundlich-isothermmodel geschikt was voor de experimentele evenwichtsanalyse.
Thermodynamische analyse
Gezien een geïsoleerd systeem als de relevante aanname, werd de Arrhenius-vergelijking (Vgl. (4)) genomen om de thermodynamische analyse uit te voeren. Onder bepaalde speciale omstandigheden van een thermostatische schudder was die oorspronkelijke concentratie doorgaans 30 mg L −1 en het adsorptievolume was 50 ml, vervolgens werd 20 mg adsorbens in de erlenmeyers met een capaciteit van 100 ml gedaan, evenals Pb 2+ oplossingen bij vijf classificatietemperaturen, waaronder 30, 40, 50, 60 en 70 °C. Tijdens het adsorptieproces werden de waterige monsters bemonsterd na verschillende tijdsbakken; gedurende deze periode zijn de consistente concentraties van Pb 2+ moesten ook worden gemeten op basis van de AAS die werd gebruikt om de adsorptiekinetiek ervan te analyseren volgens de bovengenoemde verschillende temperatuursituaties. Bovendien wordt de in de vorige gegeven vergelijking van Arrhenius gebruikt om de activeringsenergie te evalueren die de voorwaarde was voor het adsorptieonderzoek.
$$ \ln {k}_2=1n\kern0.5em A-\frac{E_a}{RT} $$ (4)Hier, E een is de activeringsenergie van Arrhenius (kJ mol −1 ). A vertegenwoordigt de factor van Arrhenius; de gasconstante (8.314 J mol −1 K −1 ) wordt uitgedrukt met R , en T verwijst naar de absolute temperatuur (K). De bijbehorende helling is −Ea /R , gebaseerd op een plot van lnk 2 tegen 1/T (Fig. 9) om de rechte lijn te krijgen.
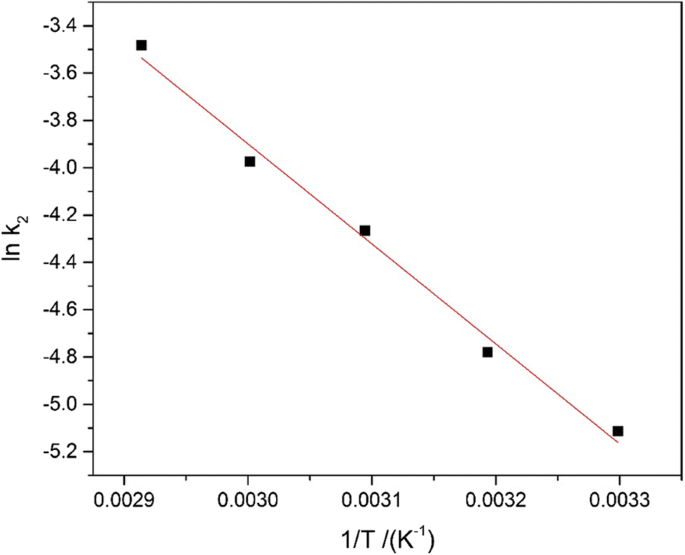
Plot van lnk2versus 1/T voor Pb2+ adsorptie op de Fe3 O4 @C-voorbeeld (TOC)
De afmetingen van activeringsenergie werden genomen om de vorm van adsorptie te bepalen. Meestal met een specifiek bereik (0–40 kJ mol −1 ) voor de activeringsenergie in het proces van fysisorptie [54] was daarentegen een groter bereik nodig in het chemisorptieproces. De activeringsenergie was 34,92 kJ mol −1 hier. Het gaf aan dat het adsorptieproces van Pb 2+ op de Fe3 O4 @C is ingedeeld in fysisorptie.
Conclusies
De verbinding van Fe3 . met kernschil O4 @C hybride nanodeeltjesaggregaten worden bereikt door middel van vreedzame en gematigde milieustappen op basis van de solvothermische synthesemethode en verkregen de calcinaties uiteindelijk bij 450 ° C. Via de op koolstof gebaseerde hybride core-shell nanostructuren kan een grotere mate van blootstellingsefficiëntie van adsorptieplaatsen efficiënt worden gerealiseerd voor het adsorbaat in vergelijking met een vaste, die adsorptie-eigenschappen zal opleveren die beter zijn om de zware metaalionen te elimineren. Bovendien zorgen de op ijzer gebaseerde kernen ervoor dat de adsorbentia gemakkelijk kunnen worden gescheiden van de waterige oplossingen. Onder dit apparaat (goedkoper, minder medeplichtigheid en hogere productiviteit) wordt een nieuwe benadering verduidelijkt dat core-shell nano / microfunctionele materialen goed op grote schaal kunnen worden gesynthetiseerd die op veel gebieden worden gebruikt, zoals milieusanering, katalysator, en energie.
Afkortingen
- AAS:
-
Atoomabsorptiespectroscopie
- BET:
-
Brunauer-Emmet-Teller
- FTIR:
-
Fourier-transformatie infraroodspectroscopie
- HR-TEM:
-
Transmissie-elektronenmicroscoop met hoge resolutie
- JCPDS:
-
Gemengd Comité voor normen voor poederdiffractie
- SAED:
-
Geselecteerd gebied elektronendiffractie
- SEM:
-
Scanning elektronenmicroscoop
- TEM:
-
Transmissie-elektronenmicroscoop
- VSM:
-
Magnetometer met trillingsmonster
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Vodcast:OEE en realtime prestatiebeheer
- Adsorberende verwijdering van koper(II)-ionen uit waterige oplossing met behulp van een magnetiet nano-adsorbens uit afval van walshuid:synthese, karakterisering, adsorptie en kinetische modellering O…
- Nanogestructureerde Silica/Gold-Cellulose-Bonded Amino-POSS Hybrid Composite via Sol-Gel Process en zijn eigenschappen
- Onderzoek naar de sorptie van zware metalen met behulp van nanocomposieten van met ijzer gemodificeerde biochar
- Synthese van elektrisch geleidende silica nanovezel/gouden nanodeeltjescomposiet door laserpulsen en sputtertechniek
- Het effect van contactloos plasma op structurele en magnetische eigenschappen van Mn Х Fe3 − X О4 Spinels
- Hydrothermische synthese van In2O3 nanodeeltjes hybride tweeling hexagonale schijf ZnO heterostructuren voor verbeterde fotokatalytische activiteiten en stabiliteit
- Silica Aerogel-ondersteunde hydrozinkiet en carbonaat-geïntercaleerd hydrotalciet voor zeer efficiënte verwijdering van Pb(II)-ionen door precipitatietransformatiereacties
- Bereiding van palladium(II)-ion-imprinted polymere nanosferen en de verwijdering van palladium(II) uit waterige oplossing
- Synthese en in vitro prestaties van met polypyrrool gecoate ijzer-platina nanodeeltjes voor fotothermische therapie en foto-akoestische beeldvorming
- Synthese en karakterisering van gemodificeerde BiOCl en hun toepassing bij adsorptie van kleurstoffen met een lage concentratie uit een waterige oplossing



