Bereiding van thermoresponsieve polymeer nanogels van oligo(ethyleenglycol) diacrylaat-methacrylzuur en hun eigenschapskarakterisering
Abstract
Op stimulering reagerende polymeren hebben de laatste jaren steeds meer aandacht gekregen vanwege hun brede toepassingen op diverse gebieden. Een nieuw, op stimuli reagerend polymeer, gebaseerd op oligo(ethyleenglycol)diacrylaat (OEGDA) en methacrylzuur (MAA), P(OEGDA-MAA), wordt bereid door precipitatiepolymerisatie en er is aangetoond dat het een LCST-type VPTT (volumefase) heeft. overgangstemperatuur) bij 33 °C in water en een UCST-type VPTT bij 43 °C in ethanol, allemaal in een concentratie van 1 mg/ml. Beide VPTT's zijn sterk concentratie- en pH-afhankelijk, wat een gemakkelijke manier biedt om de faseovergangstemperatuur af te stemmen. Het polymeer wordt gekenmerkt met betrekking tot zijn samenstelling en zijn morfologie in water en in ethanol bij verschillende concentraties. Op basis van de resultaten worden de twee overgangen bestudeerd en geïnterpreteerd. Dit werk biedt een nieuwe manier voor de bereiding van een nieuw type stimuli-responsief polymeer met een groot potentieel voor verschillende toepassingen, met name die in biomedische gebieden, omdat bekend is dat PEG-gebaseerde stimuli-responsieve polymeren niet-toxisch en niet-immunogeen zijn.
Achtergrond
Op prikkels reagerende polymeren zijn in staat te reageren op externe prikkels met aanzienlijke verandering in hun fysisch-chemische eigenschappen [1,2,3]. Dankzij dit reactievermogen is een grote verscheidenheid aan toepassingen ontwikkeld, waaronder actuatoren, medicijnafgifte, genoverdracht en materiaalscheiding [4,5,6,7]. Onder de veel voorkomende externe stimuli, zoals temperatuur, pH, ionsterkte, elektrisch veld en ultrageluid, hebben polymeren die reageren op temperatuurverandering, namelijk thermogevoelige polymeren, al tientallen jaren veel aandacht gekregen [1,2,3,4,5,6, 7,8,9], waarvan de polymeren met een volume-faseovergangstemperatuur (VPTT) of een lagere kritische oplossingstemperatuur (LCST), voor niet-verknoopte oplosbare polymeren, verreweg het meest bestudeerd zijn. Dit geldt met name voor P(N -isopropylacrylamide), PNIPAM, een thermogevoelig polymeer dat uitgebreid is onderzocht op zijn potentiële biomedische toepassingen [2, 9,10,11,12] vanwege zijn VPTT in water van ongeveer 32 °C, dicht bij de menselijke lichaamstemperatuur.
Het is algemeen aanvaard dat op PNIPAM gebaseerde materialen een waarneembare hysterese hebben, sterke waterstofbindingsinteracties met eiwitten hebben en amines met een laag molecuulgewicht produceren tijdens hydrolyse. Al deze eigenschappen hebben hun toepassingen op biotechnologisch gebied beperkt [13]. Onlangs is een nieuwe familie van polymeren (PEG) op basis van oligo(ethyleenglycol) (OEG) met thermoresponsieve eigenschappen ontwikkeld [14,15,16,17]. PEG in water is echter alleen thermoresponsief bij verhoogde temperatuur en onder druk [18], wat PEG voor veel toepassingen ongeschikt maakt. Om de toepassingen als thermoresponsieve materialen te verbreden, is de gebruikelijke praktijk om functionele groepen aan een of beide OEG-terminals te hechten, waardoor een OEG-macromonomeer wordt gemaakt, dat vervolgens wordt gepolymeriseerd door verschillende processen, waaronder bijvoorbeeld anionisch [19], kationisch [20] , groepoverdrachtspolymerisatie [21, 22]; conventionele polymerisatie met vrije radicalen [23]; een verscheidenheid aan op vrije radicalen gebaseerde levende polymerisaties, waaronder ATRP [24], RAFT [25, 26] en NMP [27]; en diverse andere polymerisatieprocessen [28, 29]. Het is nu algemeen bekend dat VPTT of LCST van de op OEG gebaseerde polymeren kunnen worden aangepast door de experimentele omstandigheden van hun syntheses te veranderen, om hun structuren te veranderen, waaronder bijvoorbeeld het molecuulgewicht, de architectuur en de lengte van het EG-segment, de verhouding en de structuur van de comonomeren en de aard van de eindgroepen. Al deze zijn goed gepresenteerd in recente recensies [1, 17].
Het is opmerkelijk dat een absolute meerderheid van de gerapporteerde onderzoeken naar op OEG gebaseerde responsieve polymeren is bereid met één uiteinde van het OEG-monomeer gefunctionaliseerd door (meth)acrylaat, terwijl het andere uiteinde wordt beëindigd door een ether. De aldus bereide polymeren bestaan daarom uit een ruggengraat van de (meth)acrylsegmenten met de OEG-ketens als de hangende groepen, waardoor het OEG-polymeer een kamachtige keten wordt. Een ander gemeenschappelijk kenmerk van de tot nu toe gerapporteerde OEG-gebaseerde polymeren is dat deze polymeren meestal zijn bereid door polymerisatie van één enkel OEG-macromonomeer [19] of copolymerisatie van twee of meer OEG-macromonomeren met verschillende OEG-lengte of -structuur [14,15, 16], in beide gevallen niet verknoopt. Tegen deze achtergrond wordt in dit werk een nieuw type op OEG gebaseerd polymeer, P(OEGDA-MAA), bereid door copolymerisatie van oligo(ethyleenglycol)diacrylaat (OEGDA) met methacrylzuur (MAA), door precipitatiepolymerisatie in water. Het aldus gevormde polymeer is daarom verknoopt vanwege de diacrylaatstructuur en er is aangetoond dat het thermoresponsief is met een VPTT in water, wat vergelijkbaar is met de algemeen gerapporteerde faseovergang van het LCST-type, terwijl dit polymeer in ethanol een VPTT van het UCST-type vertoont. Beide VPTT's zijn sterk afhankelijk van de concentratie. Deze faseovergangen worden gekenmerkt met betrekking tot polymeersamenstelling en morfologie in dispersie bij verschillende concentraties. Dit werk biedt daarom een nieuw type op stimuli reagerend polymeer met een groot potentieel voor verschillende toepassingen, met name in biomedische gebieden.
Methoden
Materialen
Oligo(ethyleenglycol)diacrylaat (OEGDA, Mn = 575) werd gekocht bij Aladdin (Shanghai, China). Methacrylzuur (MAA) was van Tianjin Guangcheng Chemicals (Tianjin, China), met remmers verwijderd door het passeren van basisch Al2 O3 (Sinopharm Chemical Regent Co. Ltd., Shanghai, China). Ammoniumpersulfaat (APS) werd geleverd door Tianjin Hedong Hongyan Chemicals (Tianjin, China). De dialysezakken (MWCO 3500) waren van Union Carbide Corporation (Shanghai, China).
Voorbereiding van P(OEGDA-MAA)
Het copolymeer van OEGDA en MAA, P(OEGDA-MAA), werd bereid door precipitatiepolymerisatie in water. Voor een typisch proces werden MAA (0,1834 g, 2,11 mmol) en OEGDA (0,8166 g, 1,43 mmol, molaire verhouding van OEGDA/MAA = 40/60) toegevoegd aan 500 ml gedeïoniseerd water dat zich vooraf in een glazen kolf van 1 L capaciteit. Na spoelen met stikstof om zuurstof te verwijderen, werd APS-oplossing (10 gew.%, 300 μL) toegevoegd. De kolf werd snel afgesloten en in een waterbad van 70 °C geplaatst om de polymerisatie gewoonlijk gedurende 4 uur te starten. De heldere inhoud in de fles werd na initiatie snel troebel, wat wijst op de precipitatie van het polymeer. Aan het einde van de polymerisatie werd het reactiesysteem afgekoeld tot kamertemperatuur en veranderde het troebele emulsie-achtige mengsel in een heldere polymeerdispersie, waaraan een bepaalde hoeveelheid NaCl-oplossing (2 M) met een pH van 1,0 voorafging. aangepast met zoutzuur, toegevoegd. De toevoeging van NaCl-oplossing veroorzaakte de precipitatie van het polymeer, dat werd verzameld door centrifugatie bij 10.000 tpm, opnieuw gedispergeerd in water en uiteindelijk 72 uur bij kamertemperatuur gedialyseerd tegen gedeïoniseerd water om NaCl te verwijderen.
Karakterisering
1 H NMR-analyse van de polymeren werd uitgevoerd op een 400-MHz NMR-spectrometer (Avance III, Bruker, Zwitserland) met behulp van dimethylsulfoxide-d 6 (DMSO-d 6 ) als oplosmiddel. De morfologie van het gedroogde polymeer werd waargenomen met behulp van een scanning-elektronenmicroscoop (SEM, FEI Quanta Feg-250, VS). Het OEGDA-gehalte van het polymeer werd bepaald met behulp van potentiometrische titratie zoals eerder beschreven [30]. Een dispersie van het polymeer in gedeïoniseerd water (1,0 mg/ml) werd getitreerd tot pH 11,5 met een gekalibreerde NaOH-oplossing van ongeveer 0,1 M. De pH van de dispersie werd gemeten en geregistreerd met een pH-meter (Metrohm 808 Titrandio, Zwitserland). Het equivalentiepunt werd gebruikt om het MAA-gehalte in het copolymeer te bepalen. VPTT van P(OEGDA-MAA) in een maagdispersie (pH = 1.0, 150 mM NaCl) werd gemeten zoals eerder beschreven [30]. VPTT van P (OEGDA-MAA) in zijn ethanoldispersie werd bepaald door de transmissie van de dispersie te volgen door een licht van 565 nm met behulp van een spectrofotometer (UV3101PC, Shimadzu, Japan). De polymeerdispersie werd eerst verwarmd tot 70 °C, boven de overgangstemperatuur, gedurende 5 minuten in evenwicht gebracht en gevolgd door afkoeling van 65 tot 10 °C met een interval van 5 °C met ook een evenwichtstijd van 5 minuten bij elke temperatuur . De transmissie versus temperatuur werd geregistreerd en de temperatuur, waarbij 50% van de maximale transmissie werd bereikt, werd genomen als de VPTT. De grootte en grootteverdeling van P(OEGDA-MAA) hydrogels in ethanol en in water werden gemeten door dynamische lichtverstrooiing (DLS, Nano-ZS, Malvern Instruments, VK).
Resultaten en discussie
Samenstellingsanalyse van P(OEGDA-MAA)
Het is opmerkelijk dat, in de gerapporteerde bereidingen van diverse op OEG gebaseerde thermoresponsieve polymeren, een grote meerderheid van OEG-macromonomeren slechts aan één uiteinde is gefunctionaliseerd, en voor de meeste waarvan methacrylaat wordt gebruikt als de terminale groepen, terwijl voor de comonomeren van laagmoleculaire gewicht worden verschillende (meth)acrylaten en acrylamide gebruikt en wordt MAA zelden gebruikt [3, 13,14,15,16,17]. Om een nieuw type op OEG gebaseerde thermoresponsieve polymeren te bereiden, werd een nieuw type OEG met beide uiteinden gefunctionaliseerd met acrylaat (OEGDA) gecopolymeriseerd in water met MAA, ook een zelden gebruikt monomeer (zie aanvullend bestand 1:figuur S1). De polymerisatie werd uitgevoerd met 40% OEGDA in mol. De samenstelling van de verkregen P(OEGDA-MAA) werd geanalyseerd met 1 H-NMR (afb. 1). De toewijzingen van de pieken zijn uitgevoerd op basis van die van de gebruikte monomeren (zie aanvullend bestand 1:figuur S2) en op de gerapporteerde polymeren met vergelijkbare structuren [31]. De groep van de pieken bij een chemische verschuiving van 1,2 ppm of lager werd toegewezen aan de methylprotonen in MAA-eenheid in het polymeer; de grote en scherpe piek bij 2,0 ppm werd toegewezen aan de protonen in de hoofdketen bestaande uit MAA- en acrylsegmenten, terwijl de groep van de grote pieken van 3,2 tot 3,9 ppm werd toegewezen aan de protonen van het ethyleen van de ruggengraat. De karakteristieke pieken, bij chemische verschuivingen van 12,35 en 4,11 ppm (Fig. 1) toegeschreven aan het carboxyl proton van MAA (Ha) en de oxyethyleen ester protonen (Hb) direct naast de acrylaat eenheden, werden gebruikt om de samenstelling van de copolymeer. OEGDA-gehalte in P(OEGDA-MAA)-copolymeer werd berekend door Vgl. 1:
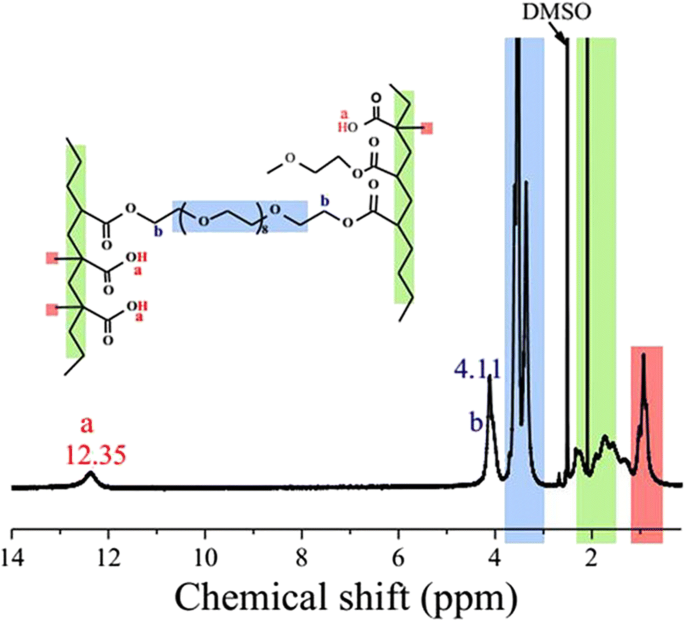
1 H NMR-spectrum van P(OEGDA-MAA)
$$ \left[\mathrm{OEGDA}\right]\ \mathrm{in}\ \mathrm{the}\ \mathrm{copolymeer}\ \left(\mathrm{mol}\%\right)=\left({ S}_{\mathrm{b}}/4\right)/\left({S}_{\mathrm{a}}}+{S}_{\mathrm{b}}/4\right) $$ ( 1)waar S een is het geïntegreerde oppervlak van de piek bij 12,35 ppm die de carboxylprotonen en S vertegenwoordigt b is die van de piek bij 4,11 ppm [30]. Het OEGDA-gehalte in het copolymeer werd aldus verkregen op 40,9 mol%. Ditzelfde OEGDA-gehalte werd ook geschat door potentiometrische titratie (zie aanvullend bestand 1:Afbeelding S3), wat 38,8 mol% opleverde voor OEGDA-gehalte. Vergeleken met de verhouding van de gebruikte monomeren voor de polymeerbereiding (40 mol% OEGDA), kan men concluderen dat de twee monomeren, OEGDA en MAA, volledig gecopolymeriseerd waren.
Morfologie van P(OEGDA-MAA)
Om de waterige dispersie van P(OEGDA-MAA) te bereiden, werd de gedroogde polymeerhydrogel van bekende hoeveelheid gedispergeerd in een bepaalde hoeveelheid water bij kamertemperatuur. werd uitgevoerd onder de VPTT van het polymeer in water, hierna laag-VPTT genoemd. Voor de dispersie van P(OEGDA-MAA) in ethanol werd een bekende hoeveelheid van het polymeer toegevoegd aan ethanol van bekende hoeveelheid in een glazen fles met schroefdop, vooraf geplaatst in een waterbad van 70 °C onder magnetisch roeren. Onder zacht roeren werd binnen 30 min tot 1 uur een quasi-heldere dispersie gevormd, afhankelijk van de polymeerconcentratie. Voor alle dispersies in ethanol met verschillende polymeerconcentraties werden ze gedurende 1 uur op 70 ° C verwarmd om de geëquilibreerde zwelling voor het polymeer te krijgen, gevolgd door afkoeling tot kamertemperatuur, waardoor de quasi-heldere dispersies troebel werden, aangezien deze kamertemperatuur ver onder de VPTT van het polymeer in ethanol lag. De heldere waterige dispersie en de troebele suspensie in ethanol van het polymeer werden eruit gehaald en op de drager van het monster gedruppeld voor de morfologie-waarneming door SEM. Geselecteerde afbeeldingen worden gegeven in Fig. 2. Het is te zien dat hydrogeldeeltjes van nanogrootte, met hun aantalgemiddelde diameter van ongeveer 40 nm, duidelijk werden waargenomen voor het monster bereid uit de waterige dispersie (1,0 mg/ml, Fig. 2a ). Het is opmerkelijk dat de polymerisatie werd uitgevoerd bij 70 ° C, een temperatuur die aanzienlijk hoger is dan de lage VPTT van het polymeer, waarin polymeerdeeltjes werden gevormd. Hoewel het gevormde polymeer niet oplosbaar was in water, moeten ze zeer hydrofiel zijn, wetende dat ze voornamelijk uit ethoxylaat en methacrylzuur bestaan. Hiermee rekening houdend, is het denkbaar dat het polymeer in een later stadium van de polymerisatie zou neerslaan, aangezien werd waargenomen dat de heldere oplossing ongeveer 30 minuten na het begin troebel werd, een veel langere tijd dan bij conventionele precipitatiepolymerisatie [32, 33]. Bovendien was de monomeerconcentratie erg laag (0,2 gew.%) en was het gevormde polymeer, P(OEGDA-MAA), verknoopt. Al deze gecombineerd, de vorming van nanogeldeeltjes van zeer kleine grootte, ongeveer 40 nm in gedroogde toestand, was niet verrassend. Bij kamertemperatuur in water, hetzij door het polymerisatiesysteem aan het einde van de polymerisatie af te koelen, hetzij door het gedroogde polymeer opnieuw in water te dispergeren, wordt aangenomen dat deze hydrogeldeeltjes niet echt op moleculair niveau zijn opgelost omdat het polymeer verknoopt was, maar in plaats daarvan grotendeels gezwollen door water in zo'n grote mate dat het polymerisatiesysteem eruitzag als een echte polymeeroplossing met een transmissie van 100% (Fig. 3). In feite is een hydrodynamische deeltjesgrootte (R u , de straal) van ongeveer 12 nm werd gedetecteerd in dit systeem aan het einde van de polymerisatie door DLS (aanvullend bestand 1:figuur S4). Vergeleken met de grootte (diameter, 40 nm) van de deeltjes in droge toestand (Fig. 2a), was de DLS-grootte van de hydrogeldeeltjes nog kleiner, wat suggereert dat de hydrogeldeeltjes moeten zijn geaggregeerd tijdens waterverdamping in het SEM-monster. Dit is gemakkelijk te begrijpen, aangezien de hydrogeldeeltjes, met 100% doorlaatbaarheid in de waterige dispersie, grotendeels gezwollen moeten zijn, en veel kleinere deeltjes in hun droge toestand dan de DLS-grootte werd verwacht als elk van hen onafhankelijk was gehouden. en vormden vaste deeltjes wanneer het oplosmiddel werd verwijderd. Wetende dat het verknoopte polymeer volledig gezwollen was, met hun hydrofiele ketenuiteinden grotendeels uitgestrekt in de omringende waterfase, zouden hun hydrofiele ketens en uiteinden tot op zekere hoogte moeten worden gepenetreerd. Dit maakte de hele dispersie zeer homogeen. De 100% transmissie van de dispersie was een indicatie van de homogeniteit. Onder deze omstandigheid was enige aggregatie van de hydrogeldeeltjes niet onverwacht bij waterverdamping; het zou eigenlijk onvermijdelijk moeten zijn.

SEM-beelden van P(OEGDA-MAA) verkregen uit hun dispersie bij kamertemperatuur bij verschillende concentraties in water van 1 mg/ml (a ) en in ethanol van 5 mg/ml (b ) en 10 mg/ml (c )
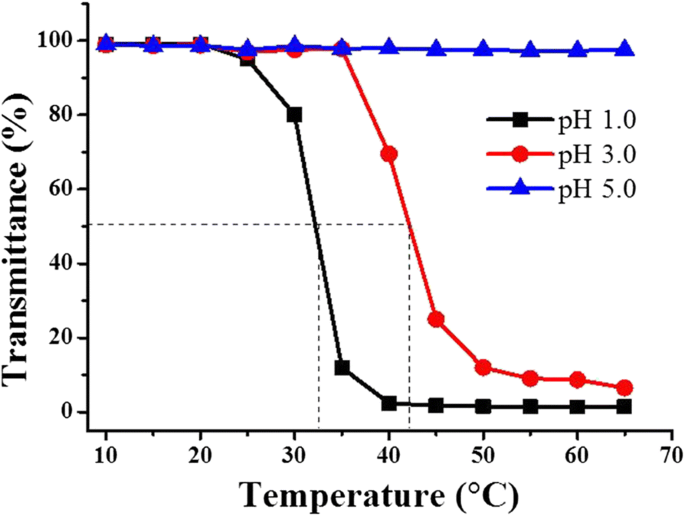
Afhankelijkheid van lichttransmissie van P(OEGDA-MAA)-dispersie (1,0 mg/ml, 150 mM NaCl) van temperatuur bij verschillende pH's
Wat betreft het troebele mengsel van P(OEGDA-MAA) in ethanol bij kamertemperatuur, het monster werd op dezelfde manier bereid door het op de monsterdrager te laten vallen en de morfologie waargenomen onder SEM. Voor het monster met een concentratie van 5 mg / ml bleek dat de nanodeeltjes, waargenomen in water zoals weergegeven in figuur 2a, verdwenen (figuur 2b). In plaats daarvan verschenen geaggregeerde korrels van het hydrogelpolymeer en de grootte van de korrels was significant groter dan die van de deeltjes verkregen uit hun waterdispersie (figuur 2a). Dit is een sterke aanwijzing dat de dezwelling nogal verschillend was voor de twee soorten dispersies.
Het is zeer waarschijnlijk dat de hydrogelpolymeerketens meer doordrongen waren in ethanol boven de hoge VPTT van het UCST-type dan in water onder de lage VPTT van het LCST-type. Dit is zeer waarschijnlijk omdat ethanol qua structuur en hydrofiliciteit meer lijkt op P(OEGDA-MAA). Door af te koelen tot kamertemperatuur, werden de oorspronkelijke nanodeeltjes van de hydrogelpolymeren, gevormd tijdens hun synthese en grotendeels opgezwollen boven deze UCST-type hoge VPTT, aan elkaar geplakt en de korrels of hun aggregatie werden daarom waargenomen. Bij een hogere concentratie (10 mg/ml, afb. 2c) in ethanol, leek het erop dat de hydrogelpolymeerketens verder doordrongen waren, zodat een continue hydrogelfilm werd gevormd, met willekeurig verspreide kleine korrels.
Lage VPTT van P(OEGDA-MAA) hydrogel in water
Dit polymeer, P(OEGDA-MAA), zoals hierboven gesynthetiseerd, was thermoresponsief (figuur 3) en de respons was ook nauw afhankelijk van de pH. Een VPTT van 33 °C werd gedetecteerd in water met een concentratie van 1 mg/ml en pH 1,0, en deze VPTT verschoof naar een hogere temperatuur bij 42 °C bij pH 3, een duidelijke toename met verhoogde pH. Met de pH verder verhoogd tot 5, vertoonde het polymeer geen enkele verandering in de lichttransmissie, d.w.z. de VPTT verdween. Deze waarnemingen suggereren dat de aanwezigheid van waterstofionen noodzakelijk was om het hydrogelpolymeer thermo-responsief te laten zijn, heel anders dan de meeste van de OEG-gebaseerde responsieve materialen bereid met monomeren vrij van carbonzuur, die responsief blijven bij pH = 7 of hoger [34] . Het is bekend dat een responsief polymeer bij kamertemperatuur wordt opgelost of gezwollen indien het wordt verknoopt door verschillende interacties tussen hun ketens en watermoleculen, dwz hun VPTT-gedrag kan worden beschouwd als het gevolg van de competitie tussen hydrofiele polymeer-water-interacties en hydrofobe polymeer-polymeer interacties [1, 2, 7, 16, 35]. Onder deze VPTT hebben de interacties tussen het hydrofiele deel van het polymeer en water de voorkeur, zijn watermoleculen gerangschikt rond de polymeerketens, waardoor waterstofbindingen tot stand worden gebracht met de hydrofiele EG-segmenten, wat leidt tot polymeersolubilisatie indien lineair, en zwelling wanneer verknoopt, terwijl boven VPTT , wordt deze interactie van water-polymeer verminderd, synchroon met verhoogde interacties tussen het hydrofobe polymeer zelf, wat leidt tot dehydratatie van de polymeerketens en hun zelfaggregatie. Voor de meeste op OEG gebaseerde polymeren zonder carboxylgroep is er geen sterke waterstofbrugdonor in hun ketens maar zwakke van der Waals-interacties. De afhankelijkheid van VPTT van pH is relatief matig. De situatie verandert echter drastisch wanneer carboxylgroepen in de polymeerketens worden opgenomen, zoals in het onderhavige geval voor P(OEGDA-MAA). Bij lage temperatuur (< VPTT) gecombineerd met een lage pH, beneden pKa (4,8) van het carbonzuur [1, 3], worden de carboxylgroepen geprotoneerd en kunnen ze de rol spelen van protondonor om de etherzuurstof van het polymeer te vormen waterstofbinding, en een dergelijke complexvorming resulteert in een soort krimp van de hydrogel omdat de interactie van watermoleculen met de polymeerketens op deze manier wordt verminderd, hoewel de polymeerketens gehydrateerd blijven en het polymeer opgelost lijkt met een hoge transmissie. Bij hoge pH worden de carboxylgroepen geïoniseerd, wat leidt tot een elektrostatische afstoting van de negatief geladen polymeerketens. Deze afstoting is veel groter dan alle interacties die kunnen worden bereikt door de niet-elektrolytpolymeerketens onderling of met water, dwz van der Waals en waterstofbinding, en maakt de polymeerketens in hun meest uitgebreide staat mogelijk:een volledige oplossing wordt bereikt voor de polymeren die niet verknoopt zijn, en de ketens worden grotendeels verlengd met het polymeer grotendeels gezwollen voor degenen die chemisch verknoopt zijn [3]. In Fig. 3 bij pH 5 was de verdwijning van VPTT het geval wanneer een groot aantal van de polymeerketens geïoniseerd was, wat als gevolg daarvan een afstoting tussen de polymeerketens veroorzaakte, waardoor ze zelfs bij een hogere temperatuur opgezwollen bleven, zonder dat de ingestorte staat waargenomen. Bij een lagere pH (pH 3 bijvoorbeeld) waren er minder geïoniseerde carboxylgroepen aan eenzelfde polymeerketen, die bij een bepaalde temperatuur minder verlengd was; de interacties van niet-elektrolyt polymeerketens, zoals van der Waals en waterstofbindingen, werden belangrijker, en een vertraagde VPTT werd daarom gedetecteerd bij een hogere temperatuur. Het is duidelijk dat hoe lager de pH is; hoe lager de VPTT, zoals waargenomen in figuur 3. Bovendien geldt dit alleen voor polymeerketens die bij hoge pH negatief worden geladen. Voor de polymeren die kationisch worden bij hoge pH (die met aminegroepen bijvoorbeeld), is het tegenovergestelde waar:VPTT verschijnt bij hogere pH en verdwijnt bij lagere pH [3, 36].
Deze VPTT-overgang werd goed aangetoond door de groottevariatie van de hydrogeldeeltjes, bepaald door DLS bij verschillende temperaturen (Fig. 4) op een waterige dispersie van P(OEGDA-MAA) met een concentratie van 1 mg/ml en pH 1,0. Bij een temperatuur onder de VPTT (33 °C) werden zeer kleine deeltjes gedetecteerd. De grootte nam langzaam en continu toe met temperatuurstijging, van ongeveer 15 nm bij 10 ° C tot ongeveer 20 nm bij 25 ° C. Een abrupte toename van de deeltjesgrootte werd gedetecteerd met de temperatuurstijging over de VPTT, een diameter van de deeltjes van ongeveer 600 nm werd gedetecteerd bij 35 ° C, net boven de VPTT (33 ° C); zodra de temperatuur voorbij de VPTT is, werd een andere langzame en geleidelijke toename in de grootte van de gedispergeerde polymeerhydrogels waargenomen. Het was vrij duidelijk dat de groottes die hier werden gedetecteerd, ongeveer 600 nm bij 35 ° C en 1100 nm bij 60 ° C, die waren van de geaggregeerde hydrogeldeeltjes, in vergelijking met die verkregen onder de VPTT. Figuur 4 onthulde dat de uitdroging van het thermoresponsieve polymeer veel eerder begon vóór de VPTT; het was bij de VPTT of in een temperatuurbereik dat er heel dicht bij lag dat de uitdroging grotendeels werd versneld, waardoor de deeltjes krimpen en aggregeerden als gevolg van uitdroging, en dat een scherpe afname van de transmissie werd gedetecteerd, zoals weergegeven in Fig. 3 De variatie in grootte van de hydrogeldeeltjes gaf ook aan dat de door uitdroging veroorzaakte aggregatie van de hydrogeldeeltjes zich nog steeds aan het ontwikkelen was na de VPTT; het was niet alleen detecteerbaar door lichttransmissie omdat de afname van de transmissie daardoor vrij minimaal was in vergelijking met de hoge opaciteit in deze toestand.
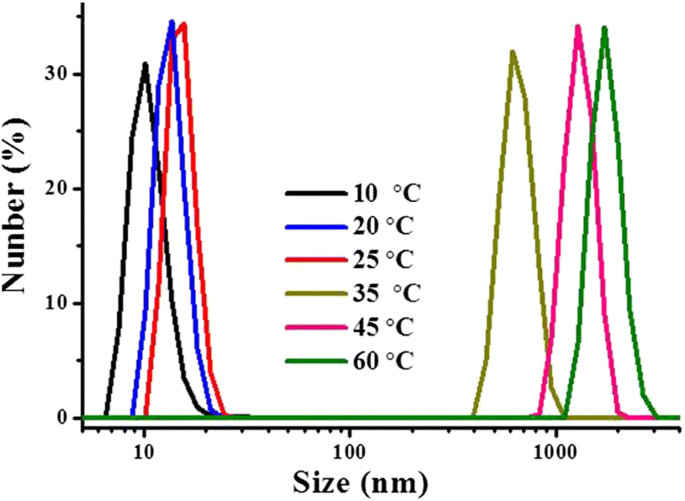
Diameter van thermoresponsieve P(OEGDA-MAA) hydrogel in waterige dispersie (1 mg/ml, pH 1,0) bij verschillende temperaturen
Naast de afhankelijkheid van het reactievermogen van de pH zoals te zien in figuur 3, is het thermoresponsieve gedrag van het materiaal ook nauw gerelateerd aan de ionsterkte, concentratie en de snelheid van verwarming/afkoeling. Verschillende auteurs hebben aangetoond dat VPTT van op OEG gebaseerde polymeren nogal ongevoelig is voor concentratie [14, 37]. Wu et al. meldde in een onderzoek naar een copolymeer van 2-(2-methoxyethoxy)ethylmethacrylaat met oligo(ethyleenglycol)methylethermethacrylaat dat een klein verschil werd waargenomen en vermoedelijk toegeschreven aan een hogere concentratie (10 gew.%) dan in andere onderzoeken [16]. De invloed van de polymeerconcentratie op de VPTT werd kort onderzocht, waarbij de concentratie varieerde van 1,0 tot 5,0 mg/ml (zie Aanvullend bestand 1:Figuur S5). Er werd gevonden dat, in vergelijking met de VPTT waargenomen bij 33 °C voor de hydrogel bij een concentratie van 1,0 mg/ml, de VPTT werd verschoven naar een lagere temperatuur van 29 °C bij een concentratie van 2,0 mg/ml, en naar een verdere lagere temperatuur van ongeveer 27 ° C met de concentratie verhoogd tot 5,0 mg/ml. Dit komt simpelweg door het concentratie-effect van het copolymeer. In het huidige verwarmingsproces, ver beneden de VPTT, waren alle of de meeste polymeerketens onafhankelijk en grotendeels opgezwollen in hun dispersie; rond VPTT begonnen ze te aggregeren, en na VPTT werden alle polymeren geaggregeerd om een heterogene suspensie van de polymeren in het oplosmiddel (water in het onderhavige geval) te vormen, wat leidde tot 0% lichttransmissie. VPTT is de indicatie van het tijdstip waarop de polymeerketens massaal beginnen te aggregeren. Het is gemakkelijk voor te stellen dat de polymeerketens gemakkelijk met elkaar in contact kunnen komen om te aggregeren in een dispersie met een hogere concentratie, en dat er een kortere tijd nodig is om een vermindering van de transmissie te hebben die gelijk is aan die in een verdunde dispersie.
VPTT van P(OEGDA-MAA) Hydrogel in Ethanol
In tegenstelling tot LCST-type VPTT zijn studies naar de polymeren met UCST of UCST-type VPTT in veel mindere mate gerapporteerd [38]. Polysulfobetaïne [39] en poly(N -acrylolyglyciamide) [40,41,42] zijn de polymeren naar verluidt met UCST in water, terwijl polyacrylamide [43] en poly(acetoacetoxyethylmethacrylaat) [44] UCST vertonen in een binair ethanol/wateroplosmiddelmengsel. Roth et al. toonde aan dat poly[oligo(ethyleenglycol)methylethermethacrylaat], (POEGMA), UCST vertoonde in een grote verscheidenheid aan alifatische alcoholen en dat de UCST-faseovergangstemperatuur afhankelijk was van de structuur, het molecuulgewicht en de concentratie van POEGMA, zoals evenals het oplosmiddel, co-oplosmiddelen [45]. Van P(NIPAM) werd ook gemeld dat het UCST-gedrag vertoonde in een ethanol/watermengsel [46].
In tegenstelling tot de test op het LCST-type VPTT in water, werd het onderzoek naar UCST-type VPTT van dit materiaal uitgevoerd in ethanol. De transmissie werd geregistreerd van 70 ° C tot 15 ° C met een evenwichtstijd van 5 minuten bij elke temperatuur (Fig. 5). Wanneer de temperatuur 70 °C of hoger was, was de hydrogel-ethanoldispersie homogeen en transparant, met een transmissie van 100% voor alle monsters, behalve die met de hoogste concentratie van 30 mg/ml, waarvan de transmissie ongeveer 95%. Wij zijn van mening dat een transmissie van 100% zou worden bereikt met een langere evenwichtstijd. Deze hoge transmissie was een indicatie dat het hydrogelpolymeer grotendeels was opgezwollen en dat de dispersie eruitzag als een authentieke oplossing. Bij afnemende temperatuur werd voor alle monsters een afname van de transmissie waargenomen en deze was duidelijk concentratiegerelateerd. Bij een temperatuurdaling tot 60 °C bleef de transmissie op 100% voor de twee monsters met een lagere concentratie (1 en 2 mg/ml), en een waarneembare afname van de transmissie werd alleen waargenomen wanneer de temperatuur onder de 60 °C daalde, terwijl voor de drie monsters met een hogere concentratie (5, 10 en 30 mg/ml), werd een duidelijke afname van de transmissie gedetecteerd vanaf 70 °C, en de afname was significanter voor het monster met een hogere concentratie. Bij 60 ° C daalde de transmissie van de monsters tot respectievelijk 87, 80 en 70%, strikt in volgorde van hun concentratie van laag naar hoog. Dit was precies hetzelfde als wat werd waargenomen bij de lage VPTT in water, en gemakkelijk te begrijpen door het concentratie-effect. Het enige verschil was dat het hier om ethanol ging in plaats van om water, en door de temperatuur te verlagen werden de intra- en intermoleculaire interacties van de hydrogelpolymeren belangrijker, deze interacties overtroffen die tussen het polymeer en ethanol. Ethanolmoleculen geassocieerd met polymeerketens boven de VPTT werden geleidelijk losgekoppeld wanneer de temperatuur werd verlaagd, en de polymeerketens begonnen zichzelf te aggregeren wanneer de temperatuur dicht bij de VPTT was, wat leidde tot de afname van de lichttransmissie zoals weergegeven in figuur 5.
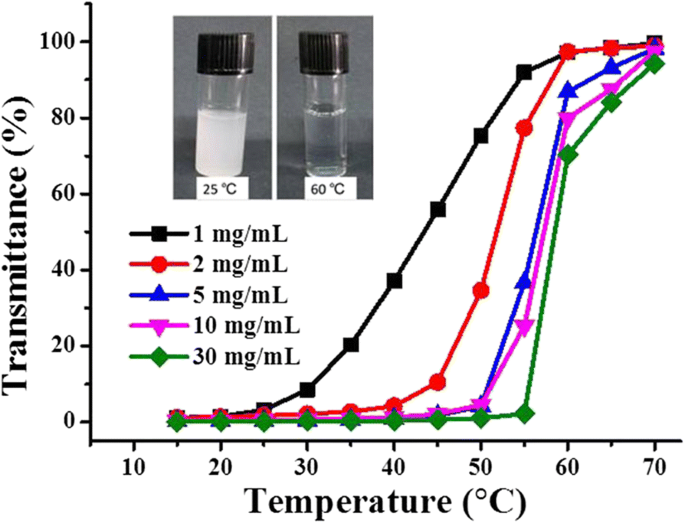
Doorlaatbaarheid van P(OEGDA-MAA) in ethanol met verschillende concentraties. De inzetstukken zijn de optische afbeeldingen van de hydrogels in ethanol (1 mg/ml) bij respectievelijk 25 en 60 °C
Faseovergangsmechanisme
Om het mechanisme van dit UCST-type VPTT beter te begrijpen, werd de grootte van de hydrogeldeeltjes bij een concentratie van 1 mg/ml gemeten in het koelproces bij verschillende temperaturen (tijd) met behulp van DLS, precies zoals gedaan voor het LCST-type VPTT. De resultaten zijn weergegeven in Fig. 6. Een zeer kleine deeltjesgrootte, met een straal van ongeveer 8 nm (R u ), werd verkregen bij 60 ° C, hoewel het monster er homogeen en transparant uitzag. De kleine grootte van de hydrogeldeeltjes was in overeenstemming met de grootte van de nanogel in water onder die lage VPTT bij 10 ° C (diameter van 15 nm, Fig. 4), wat een aanwijzing kan zijn dat de verknoopte hydrogel grotendeels was opgezwollen tot een toestand alsof ze afzonderlijk op moleculair niveau bij zo'n lage concentratie zijn opgelost, en de hydrofiele ketenuiteinden (voornamelijk carboxylgroepen) zich volledig uitstrekken naar het omringende oplosmiddel; het hele systeem was inderdaad homogeen en leek volledig transparant. Gezien de gebruikte hoeveelheid MAA (60 mol%) en de hoge oplosbaarheid ervan in water, is het niet uitgesloten dat sommige ketensegmenten, en met name ketenuiteinden die alleen uit MAA bestaan, goed aanwezig waren in de polymeren. Deze ketenuiteinden zouden het meest worden blootgesteld aan het omringende oplosmiddel in hun volledig gezwollen toestand, d.w.z. aan water onder het LCST-type VPTT en aan ethanol boven het UCST-type VPTT. Owing to the limited number of the hydrophilic chain ends and their high hydration, the size of the hydrogel particles detected might be only the size of the crosslinked core, as shown by the encircled area in Fig. 7. In fact, hydrogel particles with their R h around 10 nm, determined by DLS, were often reported. Diverse examples are available, such as polyacrylamide above its UCST in aqueous alcohol solutions [43] and 4-propoxyazobenzene-terminated PNIPAM in aqueous solution below its LCST [47]. And R h as small as 2 to 3 nm was reported for an OEG-based responsive polymer below its LCST [48]. For the present polymer, by decreasing the temperature from 60 to 45 °C, very close to the VPTT, the R h of the hydrogel particle size slightly increased to about 7 nm. This increase might be caused by the collapse of the hydrophilic chain ends, which were extended into ethanol at temperature above the UCST-type VPTT as discussed above. At this stage, the crosslinked core of the hydrogel particles was largely shrunk because the ethanol molecules were squeezed out of the polymer inner, owing to a decrease in the interaction of the polymer chains with ethanol molecules by decreasing the temperature, accompanied by an increase in the interaction of the polymer chains between themselves. By further decreasing the temperature to 40 °C just across the UCST (43 °C), the radius of the hydrogel particles abruptly increased to a significantly large size of 150 nm, very similarly to what observed for the aqueous dispersion shown in Fig. 4 when the temperature was increased across the LCST-type VPTT. This size here is no more that of a single crosslinked nanogel as above but rather that of the aggregate of the nanogel particles, as illustrated in Fig. 7. The radius of the particle aggregates further grew to 270 nm with the temperature further decreased to 25 °C. This suggests that, before reaching the UCST-type VPTT, the transmittance decrease was due to mainly the change in polymer chain conformation, i.e., the hydrophilic chains (ethylene oxide segments, and particularly carboxylic groups) were changed from their full extension in the solvent to coils on the surface of the individual hydrogel polymer particles with a crosslinked core for each, whereas the transmittance decrease around the VPTT was caused by self-aggregation of the nanogel particles (unimers), in accordance with further disassociation of ethanol molecules from the polymer chains. This has been named as a two-step process including dehydration of the particles (unimers) and their aggregation [16, 35, 37, 49]. In characterization of LCST or VPTT by varying temperature, the disassociation of the hydrophilic chains from the solvent molecules leads to the formation of a core-shell structure, with the hydrophobic polymer chains as the core and the dehydrated chains as the shell, this mechanism is also described as formation of core-shell micelles followed by their aggregation [16, 37]. A schematic illustration is given in Fig. 7 for this mechanism.
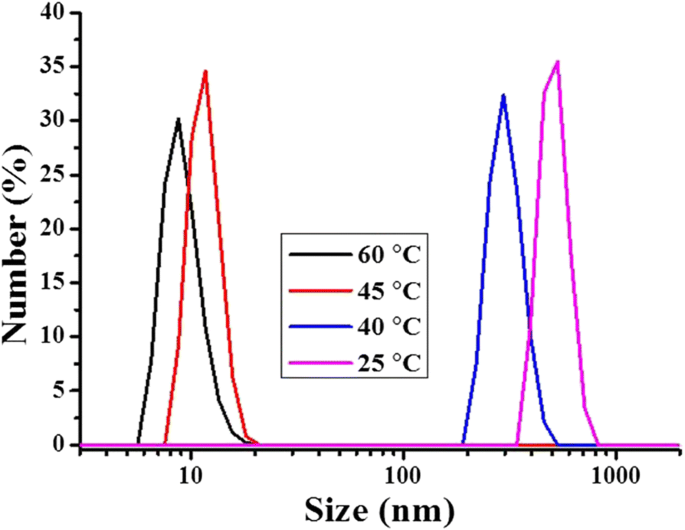
Diameter of P(OEGDA-MAA) hydrogels in ethanol (1 mg/mL) at different temperature
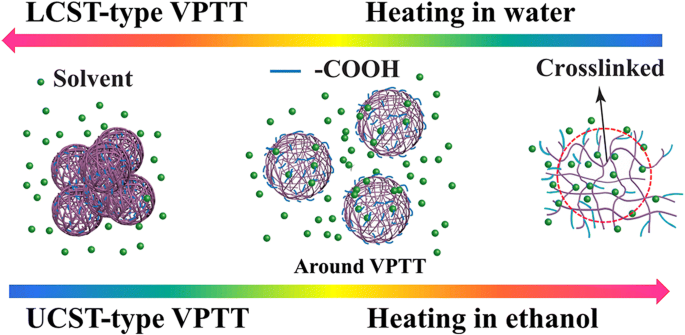
Schematic illustration of the VPTT mechanism for the UCST-type VPTT of P(OEGDA-MAA) in ethanol
Conclusies
A novel responsive polymer based on OEG, P(OEGDA-MAA), is prepared through precipitation copolymerization of OEGDA with MAA. The polymer prepared with 40 mol% of OEGDA was chemically crosslinked and showed a distinct LCST-type VPTT of 33 °C in water at pH 1.0 and concentration of 1.0 mg/mL. This VPTT was closely concentration and pH dependent. It shifted towards lower temperature with increased concentration, whereas a shift towards higher temperature was observed with increased pH, and the VPTT completely disappeared at pH 5. This same polymer exhibited also a UCST-type VPTT in ethanol at 43 °C, which was equally concentration dependent. The size evolution of the hydrogel particles versus temperature was measured for the two types of dispersions across their VPTT. For the LCST-type VPTT in water, a slight size increase was detected with increased temperature as long as the temperature was below this VPTT; and a dramatic size increase was observed once the temperature was increased to above this LCST-type VPTT. For the UCST-type VPTT in ethanol, the opposite was observed, i.e., a slight size increase with decreased temperature as long as the temperature was above this VPTT, and a dramatic size increase once the temperature was lowered below the UCST-type VPTT. These results suggest that the responsiveness of the polymer follows a two-step process, including a transition of polymer chain conformation from extended status to coil-form due to the dehydration of the hydrophilic chains from the largely swelled state, followed by an aggregation of the individual particles. This work provides therefore a novel type of candidate materials for potential applications in biomedical fields.
Afkortingen
- APS:
-
Ammonium persulfate
- ATRP:
-
Atom transfer radical polymerization
- DLS:
-
Dynamische lichtverstrooiing
- EG:
-
Ethylene glycol
- LCST:
-
Lower critical solution temperature
- MAA:
-
Methacrylic acid
- OEG:
-
Oligo(ethylene glycol)
- OEGDA:
-
Oligo(ethylene glycol) diacrylate
- P(OEGDA-MAA):
-
Poly(oligo(ethylene glycol) diacrylate-methacrylic acid)
- PEG:
-
Poly(ethylene glycol)
- PNIPAM:
-
P(N -isopropylacrylamide)
- POEGMA:
-
Poly[(oligo(ethylene glycol) methyl ether methacrylate]
- RAFT:
-
Reversible addition-fragmentation chain transfer polymerization
- R h :
-
Hydrodynamic particle radius
- UCST:
-
Upper critical solution temperature
- VPTT:
-
Volume phase transition temperature
Nanomaterialen
- Preparatie en magnetische eigenschappen van kobalt-gedoteerde FeMn2O4-spinel-nanodeeltjes
- Voorbereiding van met ICA geladen mPEG-ICA nanodeeltjes en hun toepassing bij de behandeling van door LPS geïnduceerde H9c2-celbeschadiging
- Op weg naar TiO2-nanovloeistoffen:deel 1:voorbereiding en eigenschappen
- Grafeen- en polymeercomposieten voor toepassingen met supercondensatoren:een recensie
- Paramagnetische eigenschappen van van fullereen afgeleide nanomaterialen en hun polymeercomposieten:drastisch uitpompeffect
- Synthese van ZnO-nanokristallen en toepassing in omgekeerde polymeerzonnecellen
- Voorbereiding en fotokatalytische prestaties van LiNb3O8-fotokatalysatoren met holle structuur
- Voorbereiding van PPy-Coated MnO2 hybride micromaterialen en hun verbeterde cyclische prestaties als anode voor lithium-ionbatterijen
- Synthese en karakterisering van gemodificeerde BiOCl en hun toepassing bij adsorptie van kleurstoffen met een lage concentratie uit een waterige oplossing
- Vervaardiging en karakterisering van ZnO-nanoclips door het door polyol gemedieerde proces
- Afhankelijkheid van de toxiciteit van nanodeeltjes van hun fysische en chemische eigenschappen



