Identificatie van karakteristieke macromoleculen van Escherichia coli genotypen door Atomic Force Microscope mechanische kartering op nanoschaal
Abstract
De categorisering van microbiële stammen is conventioneel gebaseerd op de moleculaire methode, en zelden zijn de morfologische kenmerken in de bestudeerde bacteriestammen. In dit onderzoek hebben we de macromoleculaire structuren van het bacteriële oppervlak onthuld via mechanische AFM-mapping, waarvan de resolutie niet alleen werd bepaald door de tipgrootte op nanoschaal, maar ook door de mechanische eigenschappen van het monster. Deze techniek maakte de nanoschaalstudie van vliezige structuren van microbiële stammen mogelijk met eenvoudige monstervoorbereiding en flexibele werkomgevingen, die de meerdere beperkingen in elektronenmicroscopie en label-enable biochemische analytische methoden overwon. De karakteristieke macromoleculen die zich tussen het cellulaire oppervlak bevinden, werden beschouwd als eiwitten van de oppervlaktelaag en bleken specifiek te zijn voor de Escherichia coli genotypen, waarvan de gemiddelde molecuulgroottes werden gekarakteriseerd met diameters van 38 tot 66 nm, en de moleculaire vormen waren nierachtig of rond. Samenvattend hebben de macromoleculaire structuren aan het oppervlak unieke kenmerken die verband houden met de E. coli genotype, wat suggereert dat de genomische effecten op cellulaire morfologieën snel kunnen worden geïdentificeerd met behulp van mechanische AFM-mapping.
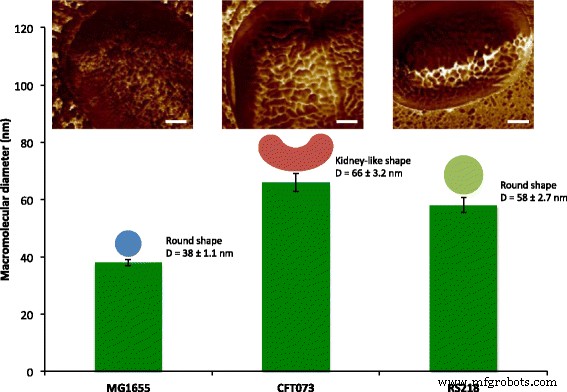
Kwantificering van oppervlaktemacromoleculen van E. coli cellen met behulp van AFM mechanische mapping. Oppervlaktemacromoleculen van cellulair oppervlak van drie E. coli genotypen, MG1655, CFT073 en RS218, werden gekarakteriseerd met maten variërend van 38 tot 66 nm en met ronde of nierachtige vormen. De topografische afbeeldingen zijn gekleurd met adhesiekaarten met de schaalbalken = 200 nm.
Achtergrond
Vanwege de inferieure resolutie van optische microscopie en de beperkte werkomgeving van elektronenmicroscopie, overwegen onderzoekers in het microbiële veld zelden het uiterlijk van bacteriële cellen te gebruiken, maar passen ze in plaats daarvan moleculaire of chemische analytische methoden toe voor de identificatie van genomische fragmenten, expressie van eiwitten, enz. Het is niet verrassend dat deze methoden een aantal nadelen hebben, waaronder arbeidsintensief en tijdrovend zijn, en daarom zijn meer ongecompliceerde, efficiënte en flexibele benaderingen nodig. Uitgevonden in 1982 door Binnig et al., is de atomic force microscope (AFM) ontworpen om een sonde op nanoschaal te gebruiken die wordt bewaakt door een laserstraal voor de observatie van het oppervlak van een specimen met nanoscopische of zelfs atomaire resolutie [1]. Door de morfologie af te beelden via een fysieke sondepunt, overwint deze techniek de resolutielimiet en omgevingsbeperkingen van zowel optische als elektronenmicroscopie en heeft een aantal voordelen, zoals eenvoudige monstervoorbereiding en flexibele werkomgevingen in de lucht of vloeistofomstandigheden [2, 3]. Wat microbiële studies betreft, hebben de huidige toepassingen van AFM voornamelijk betrekking op het kwalitatief in beeld brengen van de statische of dynamische morfologieën van bacteriële cellen of de expressie van flagella en pili [4,5,6], terwijl weinig studies zich hebben gericht op de oppervlakte-ultrastructuur van microbiële cellen en de kwantitatieve analyse van cellulaire eigenschappen.
In dit onderzoek is AFM geselecteerd voor het oppervlakteonderzoek van Escherichia coli (E. coli ) cellen, en de vormen en afmetingen van de individuele bacterie werden waargenomen door de AFM-topografie en fasebeelden. Bovendien bleek gelijktijdige mechanische mapping aanvullende biomechanische informatie over de oppervlaktecomponenten te onthullen, waarbij kleine verschillen in de adhesieve eigenschappen tussen de macromoleculen en de omringende matrix konden worden gedetecteerd tijdens elk fysiek contact tussen de tip en het monster. Door dergelijke geavanceerde technieken toe te passen op de microbiële velden, hebben we drie E. coli genotypen die één laboratoriumstam en twee humane pathogene stammen bevatten voor de identificatie van oppervlaktemacromoleculen. De resultaten toonden aan dat de techniek een beeldresolutie zou kunnen bieden die de schaal van de AFM-tip overschrijdt door de mechanische verdeling van het monster te detecteren. Concluderend stellen we voor dat een dergelijke ontwikkeling in de oppervlaktewetenschap niet alleen onderzoekers die in microbiële velden werken details van het cellulaire uiterlijk zou verschaffen, maar ook zou bijdragen aan onze kennis van de oppervlaktekenmerken van andere bio- of nanomateriaalsystemen.
Methoden
Microbiële monsters
De drie E. coli stammen die in dit onderzoek werden getest, werden klinisch geïsoleerd en geleverd door het laboratorium van prof. Ching-Hao Teng aan het Institute of Molecular Medicine, National Cheng Kung University. MG1655 is de intestinale en de wildtype laboratoriumstam van E. coli K-12 en de twee andere stammen zijn menselijke pathogenen:CFT073, de belangrijkste oorzaak van urineweginfecties, en RS218, geassocieerd met neonatale meningitis bij zuigelingen [7].
Gefunctionaliseerd substraat
Er werden twee stappen van oppervlaktemodificaties toegepast voor de covalente binding tussen het vaste oppervlak en microbiële cellen. Eerst werd een 3-aminopropyltriethoxysilaan (APTES, Sigma-Aldrich Co. LLC, VS) oplossing gebruikt om een initiële NH2 te vormen. -gefunctionaliseerde laag op het oppervlak, waar de stabiele APTES-coating werd bijgedragen aan de stabiele Si-O-bindingen - Si geleverd door APTES en O van het geoxideerde oppervlak. Met twee COOH-functies combineert glutaaraldehyde tot de NH2 functie van APTES met één COOH en werkt met de NH2 op bacterieel oppervlak met de andere COOH.
De schone substraten werden gedurende een uur ondergedompeld in APTES-oplossing met een mengsel van 5% APTES in ethanol en gespoeld met ethanol en ddH2 O. De objectglaasjes werden gedroogd met behulp van een stikstofstroom en vervolgens gedurende een nacht in glutaaraldehyde-oplossing, 2% in PBS, geplaatst en met PBS gewassen.
Voorbereiding van monsters
Enkele kolonies van de E. coli stammen werden gekozen uit de lysogeny bouillon (LB) agarplaten en geïncubeerd in LB bouillon. Na de kweektijden van 12 uur werd de bacteriële oplossing vervolgens 1:100 verdund in verse, vooraf geëquilibreerde LB-bouillon. Na nog eens 12 uur voor microbiële kweek, werd de bacteriële oplossing onderworpen aan centrifugeren bij 1500×g (4000 tpm) gedurende 3 minuten en opnieuw gesuspendeerd in LB-bouillon, waarbij dit proces tweemaal wordt herhaald. Tweehonderd microliter van de bacteriële oplossing werd op het gefunctionaliseerde substraat gedruppeld en 30 minuten met rust gelaten. Het monster werd vervolgens tweemaal ondergedompeld in gedestilleerd water om de losse cellen te verwijderen en onmiddellijk afgebeeld onder AFM in omgevingslucht.
AFM-karakterisering
Een AFM-instrument (Bruker Nano, Santa Barbara, CA, VS) en een siliciumnitride-sonde met de gekalibreerde veerconstante van 0,7 N/m en een puntstraal van 10 nm werden geselecteerd voor het oppervlakteonderzoek van microbiële monsters. De AFM-scansnelheid en lijnpixels waren respectievelijk 0,5 Hz en 256 lijnen voor de scangrootte van 10 m voor de eerste detectie van topografie, en de parameters werden vervolgens ingesteld op 0,3 Hz en 512 lijnen voor de scangrootte van 2 μm voor de gedetailleerde observatie. De PeakForce kwantitatieve nanomechanische (QNM) -modus werd gebruikt voor de nanomechanische mapping, waarbij de adhesieve eigenschappen van het oppervlak werden berekend op basis van de maximale aantrekkingskracht onder de terugtrekkingskracht-afstandcurven.
Onze eerdere studie over Streptococcus mutans toonde de mechanische evolutie op het bacteriële oppervlak gedurende 2 uur, gevolgd door continue AFM-mechanische mapping, en de microbiële monsters werden geverifieerd om binnen een dergelijke duur in leven te blijven [8,9,10]. Om de levensvatbaarheid van de E. coli monsters die in dit werk werden gebruikt, werden de voorstudies op de bacteriële monsters uitgevoerd en de continue verandering in oppervlakteadhesie gedurende 4 uur impliceerde dat de cellen na monstervoorbereiding ten minste 4 uur in leven blijven (getoond in aanvullend bestand 1). Bijgevolg werden de microbiële monsters die in dit werk werden getest, binnen 2 uur na de voorbereiding van het monster door AFM gemeten. Alle E. coli genotypen werden afzonderlijk en op verschillende tijdstippen gekweekt en de AFM-metingen werden onmiddellijk na de voorbereiding van het monster uitgevoerd. Met andere woorden, de bacteriemonsters stonden niet in een rij te wachten op het onderzoek, dus de effecten van de wachttijd op de verschillen tussen E. coli stammen werden geminimaliseerd. De kwantitatieve gegevens voor elke E. coli stam werden verzameld uit de metingen die in dit onderzoek binnen 2 uur zijn gedaan.
Statistische analyse
Prism (GraphPad Software, VS) werd gebruikt voor de statistische analyse in dit werk. Cellulaire lengtes en macromoleculaire afmetingen werden gepresenteerd als gemiddelde waarden samen met de standaardfout van het gemiddelde (SEM). De meervoudige vergelijkingen tussen E. coli genotypen werden verwerkt met behulp van gewone eenrichtingsanalyse van variantie (ANOVA). Het betrouwbaarheidsniveau van 95% (p <-0,05) werd geselecteerd en de asterisken geven de mate van significant verschil aan dat werd gevonden. Monsternummer n van elke stam was> 40.
Resultaten en discussie
Surface Ultrastructure door Multiple Mapping
Bij het scannen met AFM op een observatieschaal van 10 μm op een bacterieel monster, worden verschillende enkele E. coli MG1655-cellen konden worden gezien en de cellulaire vorm in drie dimensies kon worden waargenomen vanaf het topografische beeld (figuur 1a); de duidelijke contouren van de cellen die in twee dimensies worden getoond, werden verkregen door het beeld van de afbuigingsfout (figuur 1b), en er konden verschillende tubuli naast de bacteriecellen worden gevonden. De golfachtige filamenten (figuur 1c) kwamen overeen met het verschijnen van microbiële flagella gerapporteerd in een ander werk, dat een dergelijke bevinding als flagella bevestigde, en de kortere en haarachtige pili kon ook worden gezien [11]. Bij het verkleinen van het waarnemingsgebied van de sonde voor de gedetailleerde studie van afzonderlijke microbiële cellen, vertoonde de topografie een klein verschil in de verticale richting tussen cellulaire oppervlakken, zoals weergegeven in figuur 1d, en het beeld van de doorbuigingsfout leek meer morfologische informatie te bieden, terwijl het verzamelde omgevingsgeluid was te veel om de ultrastructuur van het celoppervlak te onderzoeken (figuur 1e). Toen de gelijktijdige biomechanische eigenschappen van het monster werden gemeten tijdens het contact tussen de tip en het geteste object, bleek dat het bacteriële oppervlak eigenlijk bestond uit een enorme hoeveelheid macromoleculen met een specifieke vorm en grootte, zoals bleek uit de adhesieve krachtmapping ( Afb. 1f); zo werd de morfologische resolutie in topografische en doorbuigingsfoutbeelden verder verbeterd met biomechanische informatie.
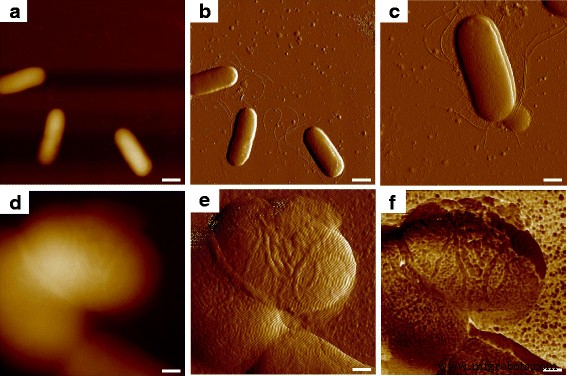
Oppervlakte-ultrastructuur van E. coli MG1655 met behulp van AFM multiple mapping. een en b waren de topografische en doorbuigingsfoutbeelden, en c was het gedetailleerde beeld van de doorbuigingsfout van de bacteriële cel met de expressie van flagella en pili. Een enkele cel werd vervolgens gefocust, waar d en e waren de topografische en doorbuigingsfoutbeelden, en f was de overeenkomstige adhesiekartering. De schaalbalken = 1 μm in a en b , 500 nm in c , en 200 nm in d –f
In figuur 2a is de uitdrukking van flagella door E. coli MG1655 was duidelijk te zien, waar de grootte van de filamenten vergelijkbaar was met die in figuur 1b, met de adhesie-eigenschappen relatief lager dan die van het substraat. Bovendien bleek het bacteriële oppervlak te zijn samengesteld uit cirkelvormige componenten die werden gekenmerkt als minder hechtend in vergelijking met de omringende matrix. Deze waarneming is vergelijkbaar met onze eerdere bevindingen over de weefsellagen van de huid van muizen, en de terugkerende en vergelijkbare korrels werden beschouwd als macromoleculen, waarvan de structuur dichter en consistenter is dan die in het intermoleculaire gebied, zodat de verschillen in adhesieprestaties konden gemakkelijk worden waargenomen [12]. De buitenste laag van de cellulaire envelop in Gram-negatieve bacteriën is een laag van zelf-assemblerende eiwitten, zoals geïllustreerd in figuur 2b, die bekend staat als een oppervlaktelaag (S-laag) eiwit [13]. S-laagstructuren werden traditioneel gemeten met elektronenmicroscopie, terwijl de vereisten van vacuümomgevingen en geleidende coating de oorspronkelijke en realtime informatie over de eiwitten verloren. Hoewel sommige onderzoeken de S-laag-eiwitten extraheren en opnieuw in elkaar zetten op mica-substraat voor de AFM-scanning, ontbraken de resultaten voor de in situ en realtime prestaties van de S-laagstructuur [14, 15]. Op basis van de cellulaire architectuur en enkele eerdere afbeeldingen van het microbiële oppervlak door elektronenmicroscopie, beschouwden we de waargenomen macromoleculen als S-laageiwitten [16].
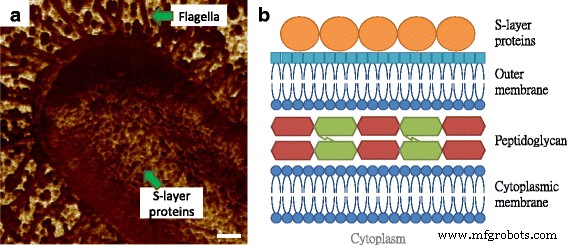
Illustratie van verticale en oppervlaktestructuren van E. coli cellen. een De oppervlaktemacromoleculen op E. coli MG1655-cel afgebeeld door AFM-adhesiemapping. b De moleculaire architectuur van celenvelop in Gram-negatieve microben, die bestaat uit cytoplasmatisch membraan, peptidoglycaan, buitenmembraan en S-laag. De schaalbalk = 200 nm
Door de AFM- en transmissie-elektronenmicroscopie (TEM) -metingen te vergelijken, heeft de eerste verschillende voordelen ten opzichte van de laatste, zoals eenvoudigere monstervoorbereiding, minder beperkte experimentele vereisten en meer biologisch-vriendelijke beeldvormingstoepassingen. De selectie van TEM op biologisch gebied wordt over het algemeen geselecteerd vanwege het vermogen om de intercellulaire organellen te zien en de ultraresolutie (meestal nanometer of sub-nanometer) beeldvorming die kan worden verkregen. De AFM-adhesiemapping in het huidige werk verbeterde de kenmerkresolutie en presenteerde de rangschikkingen van oppervlaktemacromoleculen op een manier die niet afhing van de tipgrootte, maar in plaats daarvan van de intrinsieke structuur van het monster zelf. Bovendien maakt deze benadering resolutie op nanoschaal van microbiële oppervlakken mogelijk over een gebied van tientallen micrometers.
Genomisch manipulerende verschillen in morfologische kenmerken
Na het observeren van de oppervlakte-ultrastructuur van E. coli MG1655-cellen, is een kwestie van belang hoe de macromoleculen in andere stammen zijn gerangschikt. De menselijke pathogenen E. coli CFT073 en RS218 werden dus onderzocht door AFM met dezelfde experimentele parameters, en er waren geen significante verschillen in cellulaire vormen en afmetingen tussen deze drie genotypen bij de kenmerkgrootte van 10 m, te zien in Fig. 3a-c. Het in kaart brengen van de adhesieve kracht werd gebruikt om de S-laag-eiwitten te identificeren, en er werden ongelijke structuren met verschillende vormen en maten gedetecteerd tussen de verschillende E. coli stammen, zoals getoond in Fig. 3d-f. Voor het gemak van vergelijking zijn de gedetailleerde adhesiekaarten van de E. coli stammen werden weergegeven in Fig. 3g-i. De oppervlaktemacromoleculen werden gekarakteriseerd als een ronde vorm in MG1655- en RS218-cellen, hoewel verschillende moleculaire diameters, die 38 ± 1.1 nm waren (n = 80) voor MG1655 en 58 ± 2.7 nm (n = 46) voor RS218. Aan de andere kant bezaten de CFT073-cellen een unieke vorm van S-laag-eiwitten, die nierachtig waren met een lengteverschil tussen twee eindpunten van 66 ± 3.2 nm (n = 44). Na analyse van de grootte van de S-laag-eiwitten van deze drie genotypen voor meerdere vergelijkingen, toonden de resultaten de significante verschillen tussen deze stammen aan (Fig. 4).
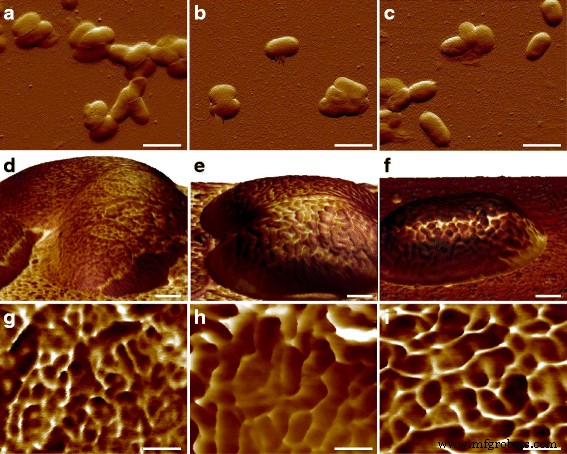
Morfologische kenmerken van de E. coli genotypen. De bovenste rij toonde de doorbuigingsfoutafbeeldingen van a MG1655, b CFT073 en c RS218. De middelste rij toonde de 3D-topografieën gekleurd met adhesiekaarten op d MG1655, e CFT073 en f RS218-cellen. De onderste rij was de gedetailleerde hechtingskaart op g MG1655, h CFT073, en i RS218. Bij het in kaart brengen van hechting verwees de donkerdere kleur naar minder hechtingsprestaties en vice versa. De schaalbalken waren 2 μm voor a –c , 200 nm voor d –f , en 100 nm voor g –ik
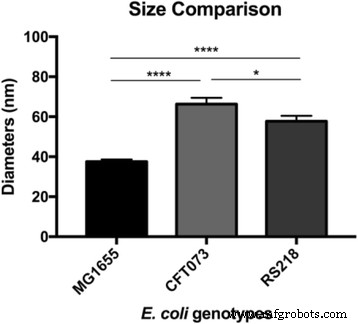
Moleculaire grootten van E. coli genotypen. De diameters van oppervlakte-eiwitten werden gedetecteerd door AFM en verwerkt via eenrichtings-ANOVA voor de meerdere vergelijkingen. ****p < 0.001 en *p < 0.05
Microbiële S-lagen spelen naar verluidt een belangrijke rol in veel functies, die cellen beschermen tegen ernstige omgevingen, aanvallen van fagocytose en roofzuchtige bacteriën. Bovendien dienen S-lagen ook als adhesine dat de effectieve kolonisatie mogelijk maakt [17]. De S-laagstructuren zijn goed bestudeerd door TEM en zijn onderverdeeld in verschillende roostertypes met een ruimte tussen hart op hart in het bereik van 4-35 nm [16]. De variatie tussen onze AFM-resultaten en TEM-rapporten uit de literatuur werd beschouwd als de verschillende beeldvormingsmethodologieën, waarbij TEM de 2D-morfologie van de S-laagstructuur geeft en AFM de 3D-topografie vastlegt die de meerdere invloeden omvat die worden bijgedragen door cellulaire radiaal en ruwheid en de geometrie van AFM-sonde.
Oorspronkelijk werd gedacht dat verschillende soorten S-laagstructuren mogelijk waren om hun verschillende taxonomische kenmerken te gebruiken om onderscheid te maken tussen bacteriesoorten, hoewel toen werd ontdekt dat zelfs voor enkele soorten de microbiële vlekken verschillende roosters van eiwitten konden hebben [13, 16, 18, 19]. Hoewel sommige studies de rol van de S-laag bij de vorming van filamenten, de soorten eiwitten op celmembranen en de genomische diversiteit in grootte tussen E. coli genotypen zijn de verschillen in S-laag-eiwitten zelden opgemerkt [20,21,22]. De resultaten van de huidige studie onthulden de verschillen in morfologische kenmerken tussen E. coli MG1655, CFT073 en RS218 en suggereren dat het uiterlijk van de oppervlaktemacromoleculen waarschijnlijk specifiek was voor individuele E. coli genotype.
Conclusies
In dit werk werd genomisch-specifieke nanostructurele informatie over het bacteriële oppervlak gedetecteerd door AFM mechanische mapping, die de adhesieve verschillen tussen de macromoleculen en de omringende matrix onderscheidde. De oppervlakte-macromoleculen van de microbiële cellen werden beschouwd als de eiwitten van de oppervlaktelaag, volgens de moleculaire architectuur van Gram-negatieve microben. De rangschikkingen en afmetingen van die macromoleculen bleken specifiek te zijn voor de geteste E. coli genotypen met verschillende vormen en maten, waarbij deze verschillen significant blijken te zijn door statistische analyse. Concluderend zijn we van mening dat de bacteriële S-laagstructuur genoomafhankelijk is en de potentiële methode kan zijn voor de snelle diagnose van microbe-geassocieerde ziekten of microbiële stammen. Om de praktische toepassing van de S-laagkarakteristiek te implementeren, is het onderzoek naar meer bacteriële genotypen vereist voor de complementcatalogus. We zijn momenteel bezig met het opzetten van de database die bacteriële morfologische kenmerken en de fysiologische/pathologische prestaties met elkaar verbindt en geloven dat dit een veelbelovende vooruitgang zal zijn voor de praktische toepassing van AFM-onderzoek.
Afkortingen
- AFM:
-
Atoomkrachtmicroscoop
- ANOVA:
-
Eenrichtingsanalyse van variantie
- APTES:
-
3-Aminopropyltriethoxysilaan
- LB:
-
Lysogeny-bouillon
- QNM:
-
Kwantitatief nanomechanisch
- S-laag:
-
Oppervlaktelaag
- TEM:
-
Transmissie-elektronenmicroscopie
Nanomaterialen
- IBM-wetenschappers vinden een thermometer uit voor de nanoschaal
- AFM-pioniers erkend met Kavli-prijs
- De volgende gusher van Big Oil is op nanoschaal
- Niet-geleiders geleiden stroom op nanoschaal
- Biogene synthese, karakterisering en antibacteriële potentiële evaluatie van koperoxide-nanodeeltjes tegen Escherichia coli
- Oppervlakte-effect op olietransport in Nanochannel:een onderzoek naar moleculaire dynamiek
- Kleine hoekverstrooiing van vetfractalen op nanoschaal
- Afhankelijkheid van gelokaliseerde oppervlakteplasmonresonantie van verkeerd uitgelijnd afgeknot Ag-nanoprismadimeer
- High-throughput fabricage van hoogwaardige nanovezels met behulp van een gemodificeerd vrij oppervlak elektrospinning
- Vervaardiging van putten op nanoschaal met hoge doorvoer op dunne polymeerfilm met behulp van AFM-tipgebaseerde dynamische ploeglithografie
- Defecten op het oppervlak van Ti-gedoteerde MgAl2O4-nanofosfor



