Antibacteriële activiteit van in situ bereide oplossing van chitosan/zilver nanodeeltjes tegen methicilline-resistente stammen van Staphylococcus aureus
Abstract
Achtergrond
Onderzoek naar nieuwe effectieve geneesmiddelen tegen de methicilline-resistente stammen van Staphylococcus aureus (MRSA) is een urgent probleem van de moderne geneeskunde. Antiseptica als alternatief voor antibiotica zijn sterke, duurzame en actieve preparaten tegen resistente stammen en schenden de microbiocenose niet.
Materialen en methoden
De activiteit van in situ bereide chitosan-Ag nanodeeltjes (Ag NP's) oplossing met verschillende componentverhoudingen werd getest tegen MRSA geïsoleerd uit patiënten. Ag NP's werden gesynthetiseerd via een chemische reductiemethode met behulp van een groene chemiebenadering. Om de antimicrobiële activiteit en dispergeerbaarheid van Ag NP's te verbeteren, werd oppervlaktemodificatie van Ag NP's door cetrimoniumbromide (CTAB) uitgevoerd.
Ag NP's en chitosan-Ag NP's-oplossing werden gekarakteriseerd met behulp van röntgendiffractie, transmissie-elektronenmicroscopie, infraroodspectroscopie en spectrofotometrische metingen.
Resultaten en conclusies
De resultaten van XRD-, FTIR-, UV-Vis- en TEM-metingen bevestigden de chemische samenstelling van chitosan en Ag NP's en hun hoge zuiverheid.
Chitosan-AgNPs-oplossingen hebben hun superieure antimicrobiële werkzaamheid aangetoond in vergelijking met de zuivere vormen. Tegelijkertijd was in situ bereiding van chitosan-Ag NP's-oplossing (chitosanpoeder 6,0 μg / ml, Ag / CTAB NP's) niet mogelijk vanwege de precipitatie van de componenten. Dit resultaat is veelbelovend en kan worden beschouwd als een effectieve oplossing in de strijd tegen resistente bacteriën.
Achtergrond
Infecties blijven wereldwijd een belangrijke oorzaak van morbiditeit en mortaliteit, ondanks de aanwezigheid van een aanzienlijk aantal antibiotica en antiseptica. Bij matige en ernstige infecties wordt de antibiotische therapie gewoonlijk empirisch gestart voordat de resultaten van bacteriologisch onderzoek worden verkregen. Constant gebruik van antibiotica schiep gunstige voorwaarden voor de selectie en vermeerdering van antibioticaresistente micro-organismen [22]. Een hoge prevalentie van multidrugresistentie tegen agentia van alle infectieuze processen is tegenwoordig gedocumenteerd [6]. De meest beruchte multiresistente bacterie is methicilline-resistente Staphylococcus aureus (MRSA) [9]. De ziekteverwekker is verantwoordelijk voor een breed spectrum van ziekten bij mens en dier, variërend van huidinfecties tot ernstige aandoeningen als longontsteking, endocarditis en bloedvergiftiging, en deze infecties kunnen gevolgen hebben voor de menselijke gezondheid [32]. Analyse van etiologische oorzaken van infecties bij patiënten met inadequate therapie onthulde dat de therapie ontoereikend was in 32,6% gevallen van op MRSA gebaseerde infecties [12] en geassocieerd was met 3-4 miljard US dollar aan jaarlijkse kosten voor gezondheidszorg [32].
Onderzoek naar nieuwe effectieve medicijnen tegen de MRSA is een urgente kwestie van de moderne geneeskunde. Antiseptica als alternatief voor antibiotica zijn sterke, duurzame en actieve preparaten tegen resistente stammen en schenden de microbiocenose niet. Het overwinnen van deze problemen vereist nieuwe en innovatieve voorbereidingen. De benadering van het combineren van verschillende mechanismen van antibacteriële werking door hybride nanomaterialen te ontwerpen, biedt een nieuw paradigma in de strijd tegen resistente bacteriën [18]. Metalen, zoals koper en zilver, zijn in uitzonderlijk lage concentraties extreem giftig voor bacteriën. Vanwege de biocidale activiteit zijn metalen op grote schaal gebruikt als antimicrobiële middelen in een groot aantal toepassingen die verband houden met de landbouw, de gezondheidszorg en de industrie in het algemeen. In tegenstelling tot andere antimicrobiële middelen zijn metalen stabiel onder de huidige omstandigheden in de industrie, waardoor ze als additieven kunnen worden gebruikt [19].
De antimicrobiële eigenschappen van zilver zijn al sinds de oudheid bekend, en toenemende antibioticaresistentie van bacteriën en de ineffectiviteit van synthetische antibiotica tegen sommige bacteriestammen hebben geleid tot de hernieuwde belangstelling voor zilver, zilverzouten, zilververbindingen en nanokristallijn zilver als antibacteriële middelen. Zilveren nanodeeltjes (Ag NP's) hebben een significant antibacterieel en schimmeldodend effect [26]. Ag NP's vertonen synergisme met andere antibiotica en antiseptica (ceftazidim, streptomycine, kanamycine, polymyxine) [25, 38]. Maar J. Jains toonde aan dat chlooramfenicol het antibacteriële effect van Ag NPs-oplossing vermindert [16].
De belangrijkste nadelen die het gebruik van Ag NP's beperken, zijn hun gemakkelijke aggregatie, de ongecontroleerde afgifte van zilverionen en hun cytotoxiciteitspotentieel [40]. Combinatie van Ag NP's met natuurlijke middelen, zoals chitosan, propolis, klei of zeolieten [33, 35], zorgt voor extra effecten. De combinatie van polymeren en nanozilver kan hun antimicrobiële effecten synergetisch verbeteren, en het gebruik van in situ synthesemethoden maakt opname in de polymeermatrix mogelijk, waardoor uniforme verdelingen worden bereikt en aggregatie wordt vermeden [28].
In de afgelopen jaren is de efficiëntie van groene chemiemethoden voor de synthese van metallische NP's aanzienlijk toegenomen [1]. Plantenextracten worden vaak gebruikt als reducerende, stabiliserende en afdekkende middelen [23] die kosteneffectieve en milieuvriendelijke methoden bieden voor de synthese van NP's. Onder plantenextracten is gemberextract van groot wetenschappelijk belang dankzij zijn chemische en biologische eigenschappen [8]. Bladextract van gember is al gebruikt voor de synthese van zilveren NP's [37]; de geproduceerde deeltjes hadden echter een vrij brede deeltjesgrootteverdeling (10-100 nm). Gemberwortelstok wordt veel gebruikt als specerij en als volksgeneesmiddel; het extract bevat specifieke fenolische verbindingen:gingerol en zijn derivaten, een aantal bioactieve fenolische en niet-fenolische bestanddelen [31]. Deze verbindingen vertonen een breed spectrum aan activiteiten, waaronder antimicrobiële, antischimmel- en antivirale. Wortelwortelextract lijkt een veelbelovend substraat voor de ontwikkeling van bioactieve en biocompatibele nanodeeltjes, omdat het ook antioxiderende en ontstekingsremmende eigenschappen vertoont.
Chitine en chitosan zijn veelbelovende materialen voor medische toepassingen vanwege hun bacteriostatische/bactericide eigenschappen en biocompatibiliteit met menselijke weefsels [20]. Chitosan is een derivaat van chitine, dat kan worden verkregen door deacetylering van chitine. Beide bevatten dezelfde monomeren, N -acetyl-2-amino-2-deoxy-D-glucopyranose en 2-amino-2-deoxy-D-glucopyranose, die verschillen in de verhouding van geacetyleerde en gedeacetyleerde monomeren. Chitosan is een veelbelovend materiaal voor het vormen van composieten met verschillende stoffen, waaronder metalen nanodeeltjes zoals Ag en Cu [33]. Aan de andere kant kan сetrimoniumbromide (CTAB) nanodeeltjes in oplossing stabiliseren en de toxiciteit van sommige nanodeeltjes, zoals ZnO, TiO2 en Ni [17] verminderen. Maar de gegevens over antibacteriële activiteiten van het CTAB-NPs-complex zijn beperkt [7].
Het doel van dit onderzoek is het vinden van een optimale verhouding van chitosan en Ag NP's, gemodificeerd door CTAB voor de samenstelling van de oplossing (chitosan/Ag) die actief zou zijn tegen klinische MRSA-stammen.
Methoden
Materialen
Zilvernitraat, L-ascorbinezuur en cetrimoniumbromide (C16 H33 )N(CH3 )3 Br (CTAB) werden gekocht van Sigma-Aldrich en gebruikt zoals ontvangen. Gember (Zingiber officinale , Zingiber acae ) wortelstok werd gekocht in een plaatselijke supermarkt (Poznan, Polen). Chitosan 200 kDa, deacetyleringsgraad 82% werd gekocht bij CJSC "Bioprogress" (Rusland, Moskou) en zonder verdere zuivering gebruikt. Ultrapuur water (weerstand> 17 MΩcm − 1 ) van een GZY-P10 watersysteem werd tijdens de experimenten gebruikt. Alle media en schijven met antibiotica zijn gekocht bij Hi Media (India).
In situ voorbereiding van Chitosan/Ag NPs-oplossingen
Om de chitosan/Ag-oplossingen in situ te bereiden, werden eerst Ag NP's gesynthetiseerd en gemodificeerd.
Synthese van Ag NP's
Ag NP's werden gesynthetiseerd via een chemische reductiemethode met behulp van een groene chemiebenadering. Volgens deze aanpak gebruikten we gember (Zingiber officinale ) extract als oppervlakteactieve stof en ascorbinezuur (vitamine C) als reductiemiddel. Om gemberwortelstokextract te bereiden, werd 250 g wortelstok grondig gewassen met gedestilleerd water en vervolgens in kleine stukjes gesneden. Gehakte gemberwortelstok werd gedurende 5 dagen (bij kamertemperatuur, op een donkere plaats) in een water-ethanoloplossing (250 ml, 1:1-verhouding) bewaard. Vervolgens werd het supernatant vacuüm gefiltreerd (door een Whatman-filterpapier) en bewaard (bij 4 ° C). Om Ag NP's te synthetiseren, werd zilvernitraat (840 mg) opgelost in water (20 ml) en werd gemberwortelextract (20 ml) toegevoegd. Vervolgens werd een mengsel van een oplossing van L-ascorbinezuur (10%, 10 ml) en gemberextract (20 ml) onder magnetische besturing druppelsgewijs aan de zilvernitraatoplossing toegevoegd. Het reactiemengsel werd donker. Daarna werd het onder terugvloeikoeling verwarmd (60°C, 1,5 uur). Vervolgens werden vers gesynthetiseerde Ag NP's gewassen met water totdat de pH 7 bereikte, met behulp van centrifugatie (4000 tpm, 30 min).
Om de antimicrobiële activiteit en dispergeerbaarheid van Ag NP's te verbeteren, werd oppervlaktemodificatie van Ag NP's door CTAB uitgevoerd, wat bekend is vanwege zijn oppervlakteactieve en antiseptische eigenschappen [17]. Typisch werd de dispersie van Ag NP's (3 ml, 76,4 mg/ml) gemengd met CTAB-oplossing (20 ml, 6,7 mg/ml) en gesoniceerd (3 uur). Vervolgens werd supernatant verzameld voor UV-Vis-metingen en werden Ag NP's driemaal gewassen met water, met behulp van centrifugatie (4000 tpm, 30 min). Het gehalte aan CTAB in het supernatant werd bepaald met behulp van de spectrofotometrische techniek (UV-Vis) door de intensiteit van de 190 nm-piek te volgen. De adsorptie van Ag NP's (in mg/g) ten opzichte van CTAB werd berekend uit het verschil tussen het aanvankelijke CTAB-gehalte in de oplossing en het gehalte in het supernatant na interactie met het monster. Het adsorptievermogen en de CTAB-laadinhoud werden berekend met de volgende vergelijkingen:
Adsorptievermogen (mg/g) = (gewicht van CTAB in oplossing, gewicht van CTAB in supernatant)/(gewicht van Ag NP's),
CTAB-ladingsgehalte (%) = (1 − (gewicht van Ag NP's)/(gewicht van CTAB geladen Ag NP's)) × 100%.
In situ voorbereiding van Chitosan/Ag NP-oplossingen
Om chitosan/Ag NPs-oplossingen te verkrijgen, werd chitosan van 200 kDa (1 g) gedurende 24 uur bij kamertemperatuur opgelost in 2% azijnzuur (100 ml) om een 1% chitosan-oplossing te vormen. In experimenten werden twee monsters van Ag NP's gebruikt:pure Ag NP's en Ag NP's-CTAB.
Fysicochemische karakterisering van Ag NP's en chitosan
Poederröntgendiffractieonderzoeken (XRD) werden uitgevoerd op een Empyrean-diffractometer (PANalytical), met behulp van Cu Kα-straling (1,54 ), een reflectietransmissie-spinner (monsterstadium) en PIXcel 3D-detector, werkend in de Bragg-Brentano-geometrie . De 2Theta-scans zijn opgenomen bij kamertemperatuur onder hoeken variërend van 10° tot 95° met een stapgrootte van 0,007°, in continue scanmodus.
Transmissie-elektronenmicroscopie (TEM)-metingen werden uitgevoerd met behulp van een JEM-ARM-200F transmissie-elektronenmicroscoop die werkte bij een versnellingsspanning van 200 kV.
De infraroodspectra werden verkregen met behulp van een Tensor 27 (Bruker Optics) spectrometer uitgerust met een globale bron en MCT-detector. Monsters werden bereid met kaliumbromide als matrixmateriaal en werden gemengd in verhoudingen van 1 mg monster tot 200 mg KBr. Pellets werden bereid met de standaardtechniek onder een druk van 10 ton/cm 2 met een loop van 16 mm in diameter. De metingen zijn uitgevoerd bij kamertemperatuur. Voor elk spectrum 512 scans in het spectrale bereik van 4000–400 cm − 1 zijn gemaakt met een resolutie van 4 cm − 1. De gegevens zijn verwerkt met behulp van het Opus-softwarepakket.
Spectrofotometrische metingen (UV–Vis) werden uitgevoerd met behulp van UV/VIS/NIR-spectrometer Lambda 950 (Perkin Elmer) bij golflengten van 200-800 nm met water als oplossing.
Microbiologische tests
Bacteriële cultuur
Bacterieculturen werden verzameld uit het gebied van de middelste neusgang en uit de keel van de 70 opgenomen patiënten met behulp van steriele wattenstaafjes met wattenstaafjes. De monsters werden onmiddellijk in transportmedia naar het laboratorium getransporteerd en vervolgens geënt op bloedagar. Bacterieculturen werden morfologisch en biochemisch geïdentificeerd door standaard laboratoriumprocedures volgens de Manual of Methods for General Bacteriology in het bacteriologische laboratorium van Sumy State University. We hebben 50 Staphylococcus aureus . geïsoleerd stammen. Elke kweek onderging Gram-kleuring en werd getest op productie van katalase, vrij coagulase, geel pigment, mannitolfermentatie, groei bij hoge zoutconcentratie en lipaseproductie op eigeel-agarmedium (Hi Media, Mumbai).
Antimicrobiële gevoeligheidstesten
Antibioticagevoeligheidstests werden uitgevoerd op alle S . aureus isolaten om hun antibioticaresistentieprofielen te bepalen. De schijfdiffusiemethode van Kirby-Bauer werd gebruikt om de antibioticagevoeligheid van de isolaten te beoordelen. Antimicrobiële gevoeligheidstesten werden uitgevoerd op Muller-Hinton-agar tegen azithromycine, levofloxacine, claritromycine, ciprofloxacine en methicilline (Nationaal Comité voor klinische laboratoriumnormen, 1999). Verse overnachtkweken werden bereid en in tests gebruikt. Standaard stam van S . aureus ATCC 25923 werd gebruikt als controle. Een aliquot (100 L) van elke isolaatsuspensie werd uitgespreid op Mueller Hinton-agar. Antibiotische schijven werden voorzichtig op de geïnoculeerde Mueller Hinton-agar gedrukt om intiem contact met het oppervlak te verzekeren, en de platen werden aëroob 18-24 uur bij 37 ° C geïncubeerd. De diameters van de remzones werden gemeten. Klinische stammen werden gecategoriseerd als vatbaar en resistent volgens evaluatiecriteria die zijn ontwikkeld door de richtlijnen van het Clinical and Laboratory Standards Institute (CLSI) [24]. De stammen van Staphylococcus aureus die resistent bleken te zijn tegen methicilline, werden gescreend als MRSA.
Bepaling van minimale remmende concentraties van Chitosan-Ag NP's-oplossingen
Antimicrobiële activiteiten van chitosan-oplossing, Ag NP's en chitosan-Ag NP's-oplossingen werden bepaald volgens de aanbevelingen van NCCLS (1999) door het gebruik van een bouillon-macrodilutiemethode. We bepaalden de minimale remmende concentratie (MIC) voor testoplossingen tegen elke meticilline-resistente Staphylococcus aureus (in totaal 10 MRSA-stammen). De buis met de laagste concentratie die de visuele groei van bacteriën volledig remt (geen troebelheid) werd beschouwd als de MIC.
In het kort, aan het begin werden zeven concentraties pure Ag NP's en Ag / CTAB NP's bereid met behulp van voedingsbouillon met de 2-voudige seriële verdunningsmethode. Er waren drie identieke rijen van elk type Ag NP-verdunning. Vervolgens voegden we in elke buis van elke rij 1, 2 of 3 ml 1% chitosan-oplossing toe. De uiteindelijke concentratie van chitosan en Ag NP's in geteste buisjes wordt weergegeven in tabel 1.
Testbacteriestammen werden gekweekt in een geschikte bouillon, eenmaal gewassen in steriele zoutoplossing en verdund in gedestilleerd water. De bacteriële concentratie werd gestandaardiseerd op een optische dichtheid van 0,08 bij 600 nm (ongeveer 1,5 × 10 8 UFC/mL) met behulp van de McFarland-schaal. Dan 100 μl S . aureus suspensie werd geïnoculeerd in buizen met Ag NP's, chitosan-oplossing en Ag NPs-chitosan-oplossing. Buisjes die groeimedium bevatten en geteste monsters zonder inoculums werden als controles gebruikt. Alle buizen werden 24 uur aëroob bij 37 ° C geïncubeerd. Alle maatregelen waren in drievoud.
Resultaten
Karakterisatie van Ag NP's en chitosan gebruikt voor het in situ bereiden van oplossingen
Een deel van gesynthetiseerde Ag NP's werd gemodificeerd door CTAB (Ag/CTAB NP's) (om de biologische activiteit en stabiliteit van Ag NP's-dispersies te verbeteren). Het adsorptievermogen van Ag NP's voor CTAB bleek 70,0 mg/g te zijn, wat overeenkomt met het CTAB-gehalte in het monster van ongeveer 6,54%.
De resultaten van XRD-metingen van Ag NP's toonden de aanwezigheid van vier scherpe pieken op 38,15, 44,33, 64,48, 77,47 en 81,54 ° 2Theta (figuur 1a). Volgens de American Mineralogist Crystal Structure Database (AMCSD) [5] werden deze pieken toegeschreven aan het zilver. De brede piek binnen 12.00–21.06 °2Theta kan worden toegeschreven aan organische verbindingen die zijn ontstaan uit de synthese (L-ascorbinezuur en gember). Het XRD-patroon van chitosan (Fig. 1a, inzet) vertoont diffractiepieken bij ongeveer 9 en 20 ° 2Theta, wat typische vingerafdrukken zijn van semikristallijn chitosan [5]. Kristalliniteit van chitosan wordt gegenereerd uit waterstofbruggen tussen overeenkomstige hydroxyl en N -acetylgroepen. Elke kristallijne piek kenmerkt de kristallografische structuur, die wordt gegenereerd door parallelle en antiparallelle uitlijningen van polymere ketens of vellen. Semikristallijn chitosan heeft amorfe en kristallijne gebieden.
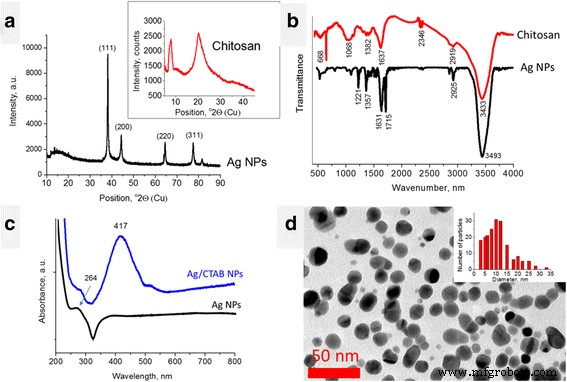
Karakterisering van Ag NP's en chitosan. een XRD-patronen, b FTIR-spectra, c UV–Vis absorptiespectrum van Ag NP's (water), d TEM-beeld van Ag NP's
FTIR-spectra van chitosan en Ag NP's worden getoond in figuur 1b. Het spectrum van chitosan vertoont brede en intensieve banden bij 3450-3200 cm − 1 (waterstofgebonden OH-rektrillingen) overlapt met NH-rekbanden, CH-rekband op 2783 cm − 1 , en de band voor amide I op 1652 cm − 1 (Fig. 1b). Buigtrillingen van methyleen- en methylgroepen zijn ook zichtbaar bij ν = 1375 cm − 1 en ν = 1426 cm − 1 , respectievelijk. Absorptie in het bereik van 1160 tot 1000 cm − 1 is toegeschreven aan trillingen van de CO-groep. De band in de buurt van ν = 1150 cm − 1 is gerelateerd aan asymmetrische trillingen van CO in de zuurstofbrug als gevolg van deacetylering van chitosan. De banden in de buurt van 1080–1025 cm − 1 worden toegeschreven aan ν CO van de ring COH, COC en CH2 OH. De kleine piek bij ~ 890 cm − 1 komt overeen met het kwispelen van de sacharidestructuur van chitosan [11, 13].
Het FTIR-spectrum van Ag NP's onthulde verschillende intensieve pieken bij 1226, 1366, 1636, 1714, 2851, 2924 en 3438 cm − 1 . Deze laatste werden toegeschreven aan de H-gebonden OH-groepen. De pieken van 1226 en 1366 cm − 1 zijn te wijten aan CO- en CH-buigtrillingen; dubbele piek bij 1636 en 1714 cm − 1 wijzen op de aanwezigheid van C=C- en C=O-groepen (rektrillingen). De pieken op 2851 en 2924 cm − 1 zijn gerelateerd aan CH-rektrillingen [13]. De aanwezigheid van organische groepen op het Ag NP-oppervlak is te wijten aan organische verbindingen die worden gebruikt voor hun synthese, L-ascorbinezuur en gember, waarvan FTIR-spectra bekend zijn [10]. Als we de spectra van de laatste vergelijken met die van Ag NP's, valt op dat de dubbele piek bij 1636 en 1714 cm − 1 is inherent aan het spectrum van L-ascorbinezuur en blauw verschoven. De meest intensieve gemberpieken binnen 1000–1200 cm − 1 (COC-trillingen) worden niet intensief uitgedrukt in het Ag NP-spectrum. Daarom speelt L-ascorbinezuur de overheersende rol bij de reductie van zilverionen, de overdracht van twee elektronen en de transformatie in dehydroascorbinezuur [29]. De blauwverschuiving van de piekpositie van L-ascorbinezuur geeft een bewijs voor de chemische binding van dit molecuul op het Ag NP's-oppervlak.
Het UV-Vis-absorptiespectrum van de Ag NP's gedispergeerd in water (figuur 1c) onthulde de asymmetrische piek bij ongeveer 387 nm. De piek binnen 387-420 nm staat bekend als de karakteristieke piek voor Ag NP's en wordt meestal toegeschreven aan het oppervlakte-plasmonresonantie-effect [30]. De asymmetrie van deze piek (plateau) kan worden toegeschreven aan snelle precipitatie van Ag NP's. De piek bij ongeveer 264 nm is ook bekend voor Ag NP's en is meestal gerelateerd aan de overgang van elektronen naar hogere energietoestanden in Ag NP's [38]. Aan de andere kant onthulde het UV-Vis-spectrum van L-ascorbinezuur ook een piek bij 255 nm [4]. Daarom kan de piek bij 264 nm in het Ag NP-spectrum worden beschouwd als een roodverschoven piek van L-ascorbinezuur, wat de aanwezigheid van deze chemisch gebonden moleculen op het oppervlak van Ag NP's bevestigt.
Het is interessant dat het UV-Vis-spectrum van Ag / CTAB NP's (figuur 1c, blauwe lijn) een symmetrische piek onthulde bij 417 nm. Dit bevestigde dat de stabiliteit van Ag NP's in water was verbeterd door oppervlaktemodificatie door CTAB-moleculen.
TEM-metingen onthulden dat Ag NP's een ronde vorm hebben en dat de meeste 10-12 nm groot zijn (figuur 1d).
Antibacteriële activiteiten van de in situ bereide chitosan/Ag NP's-oplossingen tegen methicilline-resistente stammen van Staphylococcus aureus
MIC van zuivere Ag NP's en Ag/CTAB NP's tegen 100% MRSA was 9,6 g/ml. De laagste concentraties hebben minder activiteiten laten zien (tabel 2). Chitosan-oplossing vertoont antibacteriële werking met MIC 6 g/ml tegen 100% klinische MRSA-stammen. Onder hen had 60% van de stammen MIC 3,3 en 5 μg/ml chitosan-oplossing.
Het remmende effect van de chitosan-Ag NP-oplossing tegen MRSA wordt weergegeven in figuur 2a. Er werd gevonden dat de chitosan-Ag NP-oplossing een superieure antimicrobiële werkzaamheid vertoonde in vergelijking met zijn zuivere vormen. Tegelijkertijd was in situ bereiding van chitosan-Ag NP's/CTAB-oplossing (chitosan 6,0 μg/ml, Ag/CTAB NP's) niet mogelijk vanwege de precipitatie van de componenten:vorming van grijszwarte ringagglutinatie en scheiding van de componenten in twee fasen. In dit geval kon de antibacteriële activiteit niet worden geëvalueerd. Rekening houdend met het onverwachte resultaat van het mengen van chitosan en CTAB en de laagste antibacteriële activiteit van Ag NPs-CTAB (zie figuur 2b), concludeerden we dat Ag NPs-oppervlaktemodificatie door CTAB niet veelbelovend is. De aanwezigheid van CTAB-moleculen op het oppervlak van Ag NP's verbeterde de stabiliteit van waterdispersies, maar verminderde de antimicrobiële activiteit aanzienlijk en veroorzaakte neerslag in de oplossing.
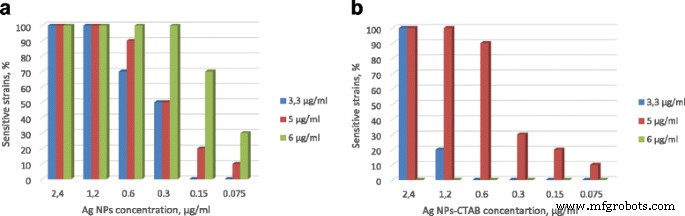
Het percentage gevoelige MRSA-stammen na behandeling. Chitosan-Ag NPs-oplossing (a ) en chitosan-AgNPs-CTAB-oplossing (b ). 3,3, 5 en 6 μg/ml - dit zijn de concentraties chitosan in oplossing
Discussie
Toxiciteit verwijst naar alle schadelijke effecten op een organisme tijdens blootstelling aan nanodeeltjes en hun zouten. Als het doel is om een specifiek organisme te steriliseren of te desinfecteren, kan toxiciteit worden geïnterpreteerd als een positief resultaat (antibacterieel, antiviraal) [15]. De huidige fundamentele behoefte in nanotechnologie is de ontwikkeling van milieuvriendelijke en betrouwbare methoden voor de synthese van metallische nanodeeltjes. We hebben het gebruik bevestigd van biologische reductiemiddelen die natuurlijke, goedkope en milieuvriendelijke materialen zijn voor het produceren van zilveren nanodeeltjes, om de aanwezigheid van risicovolle en giftige oplosmiddelen te voorkomen [37]. Het gebruik van Ag NP's als therapeutische middelen is beperkt vanwege hun cytotoxiciteit tegen zoogdiercellen. Verschillende factoren kunnen van invloed zijn op het effect van Ag NP's op micro-organismen, zoals grootte, vorm, stabiliteit en concentratie van Ag NP's [4].
In ons onderzoek hebben we Ag NP's verkregen met een grootte van 5-18 nm. Het is een van de meest fundamentele parameters die de optische [39], antimicrobiële [27] en antivirale eigenschappen van Ag NP's [21] beïnvloeden. Kleinere deeltjes vertonen een grotere antibacteriële activiteit. Sommige onderzoeken hebben aangetoond dat de NP's groter dan 10 nm zich ophopen op het celoppervlak en de cellulaire permeabiliteit in gevaar brengen; NP's kleiner dan 10 nm dringen echter door in de bacteriën, waardoor het DNA en de enzymen worden aangetast, wat leidt tot celdood [14]. Het is interessant om op te merken dat hoewel de meeste resultaten aantoonden dat de hypothese van toxiciteit toeneemt met een kleinere deeltjesgrootte, er ook experimentele gegevens zijn die aantonen dat kleinere NP's ofwel minder toxisch waren of geen grootteafhankelijke toxiciteit hadden [15]. Er zijn veel onderzoeken die de antimicrobiële activiteit van de Ag NP's hebben aangetoond, met een bereik van 3 tot 100 nm [19].
Zoals eerder vermeld, werden de effecten van chitosan op de stabiliteit en antimicrobiële eigenschappen van de gesynthetiseerde Ag NP's geëvalueerd. Voorafgaand aan de gevoeligheidstesten werden de gesynthetiseerde nanodeeltjes onderworpen aan verschillende karakteriseringsmethoden om hun zuiverheid te bepalen. Ons onderzoek toonde aan dat Ag NP's in een concentratie van 9,6 μg/ml effectief zijn tegen 100% van de MRSA-stammen en dat CTAB de effectiviteit van Ag NP's niet verhoogde.
Het is bekend dat chitosan een significante antibacteriële activiteit heeft tegen een breed spectrum aan bacteriën [2]. Desondanks geven sommige rapporten aan dat pure chitosan ernstige infecties niet voorkomt [3]. Er zijn verschillende publicaties geweest die verschillende combinaties van chitosan en zilver met verbeterde antimicrobiële eigenschappen hebben gerapporteerd [11]. Zilver-chitosan nanocomposieten werden voorgesteld als coatings voor biomedische technologie en voedselverpakkingstoepassingen en wondverbandtoepassingen [2, 3]. Maar er zijn beperkte gegevens over het antibacteriële effect van chitosan-Ag NPs-oplossing tegen MRSA [34]. Onze gegevens tonen aan dat eenvoudig mengen van Ag NP's in chitosan-oplossing de antibacteriële activiteit van beide componenten kan verbeteren. We krijgen een toename van alle onderzochte antibacteriële activiteiten van de stof. MIC van chitosan was 3,3 g/ml en zuivere Ag NP's MIC en Ag NP's met CTAB MIC waren respectievelijk 1,2 en 2,4 μg/ml. Kaur et al. (2013) rapporteerden ook antibacteriële activiteit van zilver/chitosan nanocomposieten tegen S . aureus , waarin ze vergelijkbare resultaten lieten zien [36], maar ze bepaalden de MIC niet. Deze bevinding toont de effectiviteit van chitosan-Ag NP's-oplossing aan, maar we zagen geen voordelen van CTAB als antibacterieel middel. Integendeel, een andere studie toonde aan dat Ag NP's gestabiliseerd met CTAB een uitgesproken antibacterieel effect hebben tegen S . aureus en Escherichia coli . Waarschijnlijk linkt chitosan in ons experiment met CTAB dat het Ag NP-effect voor bacteriële cellen vermindert.
Conclusies
In deze studie werd de activiteit van in situ bereide chitosan-Ag NP's-oplossingen met verschillende componentverhoudingen getest tegen MRSA geïsoleerd uit patiënten. Onze resultaten toonden aan dat eenvoudig mengen van de chitosan-oplossing en Ag NP's de minimale remmingsconcentratie van de stoffen in respectievelijk 2- en 4-voudig (3,3 en 1,2 g/ml) vermindert. Dit resultaat is veelbelovend en kan worden beschouwd als een effectieve oplossing in de strijd tegen resistente bacteriën. Het is ook een vooruitgang in de richting van gepersonaliseerde geneeskunde. Toekomstig cytotoxiciteitsonderzoek van chitosan-Ag NP's-oplossing zou een antwoord geven over doses die geschikt zijn voor klinisch gebruik.
Afkortingen
- Ag NP's:
-
Zilveren nanodeeltjes
- ARI:
-
Acute luchtweginfecties
- CTAB:
-
Cetrimoniumbromide
- FTIR:
-
Fourier-transformatie infraroodspectroscopie
- MRSA:
-
M ethicilline-resistente stammen van Staphylococcus aureus
- TEM:
-
Transmissie-elektronenmicroscopie
- UV–Vis:
-
Ultraviolet-zichtbare spectroscopie
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Biocompatibele FePO4-nanodeeltjes:medicijnafgifte, RNA-stabilisatie en functionele activiteit
- Biogene synthese, karakterisering en antibacteriële potentiële evaluatie van koperoxide-nanodeeltjes tegen Escherichia coli
- Voorbereiding en verbeterde katalytische hydrogeneringsactiviteit van Sb/Palygorskite (PAL) nanodeeltjes
- synergetische effecten van Ag-nanodeeltjes/BiV1-xMoxO4 met verbeterde fotokatalytische activiteit
- Bepaling van de katalytische activiteit van met overgangsmetaal gedoteerde TiO2-nanodeeltjes met behulp van oppervlaktespectroscopische analyse
- Recente ontwikkelingen in synthetische methoden en toepassingen van zilveren nanostructuren
- Op grafeenoxide gebaseerde nanocomposieten versierd met zilveren nanodeeltjes als antibacterieel middel
- Eigenschappen van zinkoxide-nanodeeltjes en hun activiteit tegen microben
- In situ synthese van bimetaal wolfraam-koper nanodeeltjes via reactief radiofrequent (RF) thermisch plasma
- Poly (γ-glutaminezuur) bevordert verbeterde dechlorering van p-chloorfenol door Fe-Pd-nanodeeltjes
- Invloed van Mg-doping op ZnO-nanodeeltjes voor verbeterde fotokatalytische evaluatie en antibacteriële analyse



