Verkenning van Zr–Metal–Organic Framework als efficiënte fotokatalysator voor waterstofproductie
Abstract
De toepassing van metaal-organisch raamwerk (MOF) op het gebied van fotokatalyse is beperkt vanwege de onstabiele chemische eigenschappen en het niet reageren in zichtbaar licht. Hierin werden de Pd/MOF-katalysatoren bereid door impregnatiereductie. Het is belangrijk dat we het kleurstofgevoelige systeem van Pd/MOF redelijk hebben geconstrueerd en de toepassing van MOF met succes hebben uitgebreid tot het zichtbare bereik. Het vertoonde maximale fotokatalytische activiteit (9,43 mmol/g) onder bestraling met zichtbaar licht (λ ≥ 420 nm) met eosine Y als fotosensitizer, die tweemaal zo groot was als de pure MOF (0,03 mmol/g). Het activeringsproces met een uitwisselbaar gastoplosmiddel produceerde de Zr-MOF met het grote oppervlak en de hoge stabiliteit, die een grote elektronische transmissiecapaciteit bieden. De Pd-nanodeeltjes zorgen voor een elektronische uitlaat en de kleurstof verbreedt het spectrale absorptiebereik. Het synergetische effect van de verschillende componenten draagt bij aan de hoge waterstofproductieactiviteit. Dit werk biedt een referentie voor de toepassing van MOF op het gebied van fotokatalyse.
Achtergrond
Energiecrisis en milieuvervuilingsprobleem kregen steeds meer aandacht door inefficiënt gebruik van enorme fossiele brandstoffen [1]. Daarom is het zoeken naar alternatieven voor hernieuwbare energie voor fossiele brandstoffen een zeer belangrijke maar uitdagende opdracht [2,3,4]. Fotokatalytische waterstofproductie door watersplitsing met behulp van zonne-energie werd beschouwd als een alternatieve, milieuvriendelijke manier, maar het is beperkt tot de ontwikkeling van zeer actieve en stabiele fotokatalysatoren tegen lage kosten. Tot nu toe zijn er verschillende fotokatalysatoren ontwikkeld voor H2 productie, bijvoorbeeld metaaloxide (TiO2 [5,6,7], NiO [8], CuO [9]), metaalsulfide (CdS [10], CuS [11], NiS [12], MoS [13, 14]), en nitridehalfgeleiders (C 3 N4 ) [15,16,17,18,19,20,21,22]. Onlangs hebben Yu en collega's een systematische analyse gemaakt van de heterojunctie-fotokatalysatoren, wat een belangrijke referentie vormt voor het daaropvolgende fotokatalytische onderzoek [23]. Verder is wat fosfor zoals CoP [24, 25], Ni2 P [26], Cu3 P [27] en MoP [28] zijn gebruikt voor H2 productie. Vooral metaal-organische raamwerken (MOF's) met uitstekende eigenschappen hebben de afgelopen jaren enorme aandacht getrokken als katalysatoren of katalysatordragers voor fotokatalytische watersplitsing [29,30,31]. Hoewel er nog steeds enkele beperkingen zijn, zijn de mogelijkheden voor MOF's als heterogene katalysatoren zeer bemoedigend [32,33,34,35] omdat MOF's als een nieuwe klasse van poreus materiaal opwindende eigenschappen hebben, zoals grote oppervlakten, kristallijne open structuren, afstembare poriegrootte en functionaliteit. In het bijzonder kan het hoge specifieke oppervlak van MOF's meer bevestigingspunten opleveren voor een co-katalysator, waarin het actievere plaatsen zou kunnen creëren en beter contact zou kunnen maken met reactanten. Aan de andere kant kunnen de poreuze structuren van MOF's ook extra paden bieden voor de migratie van foto-geïnduceerde elektronen en de scheiding van de ladingsdrager vergemakkelijken [36, 37]. Om al deze redenen konden MOF's als een zeer efficiënte fotokatalysator worden verwacht. Wat nog belangrijker is, er zijn enkele fotoactieve MOF's gemeld; specifiek, NH2 -MIL-125(Ti) zou fotokatalytisch CO2 . kunnen verminderen formiaat vormen onder zichtbaar licht volgens Sun et al. [38]. Metaal-organisch raamwerk en metaalmolecuul worden toegepast op ruimtelijke ladingsscheiding voor het verbeteren van H2 evolutie onder zichtbaar licht [39].
Horiuchi et al. synthetiseerde de amino-gefunctionaliseerde Ti-MOF-NH2 , die een efficiënte fotokatalyse vertoonde voor waterstofproductiereactie met triethanolamine (TEOA) als een opofferingselektronendonor onder bestralingsconditie van zichtbaar licht [40]. Jiang et al. gestructureerde elektronenvaltoestanden in een metaal-organisch raamwerk om de scheiding van het elektron-gat te verbeteren, waarbij zichtbaar licht fotoreductie van CO2 werd toegepast [41].
Bovendien werden de palladium-nanodeeltjes met succes ingekapseld in UiO-66-materiaal door Dong et al., die een efficiënte katalytische activiteit vertoonden voor de Suzuki-Miyaura-koppelingsreacties bij milde toestand [42].
Lillerud et al. eerste gesynthetiseerde Zr-gebaseerde MOF's, die ze aanduiden als UiO-66 [43]. Er werd gemeld dat UiO-66 een hoge chemische en thermische stabiliteit (500 ° C) vertoonde vanwege de hoge affiniteit van zirkonium voor zuurstofliganden en de compacte structuur [44]. In 2010 gebruikten Garcia en collega's UiO-66 voor watersplitsing onder bestraling met UV-licht, wat de deur opende voor MOF's naar fotokatalytische watersplitsing [45]. De UiO-66 kan echter niet effectief zijn voor fotokatalyse omdat ze niet effectief op zichtbaar licht kunnen reageren. Het is algemeen bekend dat met kleurstof gesensibiliseerde fotokatalysatoren de rand en intensiteit van de absorptieband kunnen vergroten, typisch een metaalcomplex fotosensibilisator. In 2014 beschreven He en collega's de toepassing van UiO-66 en Pt@UiO-66, waarbij rhodamine B als fotosensibilisator werd gebruikt, in deze systemen, en de katalytische activiteiten waren 33 en 116 μmol g −1 h −1 , respectievelijk [46]. Dit werk breidde met succes het bereik van UiO-66-absorptie uit tot zichtbaar licht, maar de activiteit van waterstofproductie van het systeem was nog steeds laag. In 2015 beschreven Yuan en collega's een heel eenvoudig systeem waarbij erythrosine B-kleurstof werd gebruikt om UiO-66 en de hoogste H2 te sensibiliseren. productiesnelheid van 4,6 μmol h −1 [47]. In 2016 beschreven Xiao en collega's een Pt@UI-66-NH2 katalytisch systeem met een zeer hoge waterstofproductie-activiteit (257,38 μmol g −1 h −1 ) [48]. De synergie van metaal-organische raamwerken en metalen nanodeeltjes voor verbeterde katalyse wordt systematisch beoordeeld in het werk van Jiang [49, 50].
UiO-66 met een absorptiebandrand van 335 nm in het UV-gebied kan worden toegeschreven aan de π − π * -overgang in organische liganden. UiO-66 vertoont fotokatalytische activiteit vanwege zijn vermogen om te werken als een halfgeleider [45]. Hoewel UiO-66 op grote schaal is bestudeerd op het gebied van fotokatalyse, is de fotokatalytische efficiëntie ervan nog steeds erg laag. Daarom is er nog een lange weg te gaan om de juiste cokatalysator te vinden en een redelijk fotokatalytisch systeem te bouwen om de fotokatalytische activiteit van UiO-66 en de toepassing van fotokatalyse te verbeteren.
In dit werk hebben we een kleurstofgevoelig fotokatalysereactiesysteem ontworpen en gebouwd, waarbij we TEOA gebruiken als offerdonor onder bestraling met zichtbaar licht (λ ≥ 420 nm) en introduceerde eosine Y (EY) als fotosensibilisator. Een Zr-metaal-organisch raamwerk van nanogrootte (Zr-MOF, UiO-66) werd solvotherm gesynthetiseerd en de Pd / MOF-katalysatoren werden ook bereid door impregnatiereductie. De Pd-geladen Zr-MOF werd getest op efficiënte fotokatalytische waterstofproductie. Het vertoonde maximale fotokatalytische activiteit (2,28 mmol h −1 g −1 ) onder bestraling met zichtbaar licht (λ ≥ 420 nm) met EY als fotosensibilisator.
Methoden
Voorbereiding van UiO-66
Alle chemicaliën waren van analytische kwaliteit en werden direct zonder verdere zuivering gebruikt.
UiO-66 werd gesynthetiseerd via een solvotherme route. In een typische synthese, ZrCl4 (1,89 g) en tereftaalzuur (2,79 g) werden opgelost in 48,7 ml N ,N -dimethylformamide (DMF) met 1,43 ml zoutzuur (HCl) en vervolgens werd de oplossing overgebracht naar een met teflon beklede roestvrijstalen autoclaaf van 100 ml. De autoclaaf werd afgesloten en gedurende 20 uur in een oven op 220 °C verwarmd. Na natuurlijk afkoelen werd het product verzameld door centrifugeren en driemaal gewassen met DMF en vervolgens meerdere keren achtereenvolgens gezuiverd in methanol om er zeker van te zijn dat de verstopte DMF-moleculen werden verwijderd. Ten slotte volgde het drogen onder vacuüm (90 ° C, 6 uur) voordat de monsters voor de fotokatalytische reacties werden gebruikt.
Synthetisch van Pd/MOF composiet fotokatalysatoren
De Pd/MOF-composietfotokatalysatoren werden bereid door impregnatiereductie [42, 50]. De hierboven bereide UiO-66-poeders (0,2 g) werden in een schone beker gedaan, die 200 ml gedeïoniseerd water bevatte en gemengd met de juiste hoeveelheid H2 PdCl4 oplossing en werden nog 1 uur krachtig geroerd om ze volledig te dispergeren. Dan de NaBH4 (vers bereid) werd druppelsgewijs toegevoegd aan de oplossing onder continu magnetisch roeren; de reactieoplossing werd gedurende 3 uur geroerd om de reductiereactie te voltooien (n (H2PdCl4) :n (NaBH4) = 1:3). De verkregen zwarte korrels werden gewassen met gedeïoniseerd water en 6 uur in een vacuümoven bij 70°C gedroogd. H2 PdCl4 werd toegevoegd in een hoeveelheid van 1, 3 en 5% van de massa van UiO-66, en de resulterende monsters werden respectievelijk Pd/MOF 1%, Pd/MOF 3% en Pd/MOF 5% genoemd.
Karakterisering
Morfologie van het monster werd gekarakteriseerd door een veldemissie scanning elektronenmicroscoop (JSM-6701F.JEOL) bij een versnellende spanning van 5 kV. Transmissie-elektronenmicroscopie (TEM) -metingen werden uitgevoerd met behulp van een FEI Tecnai TF20-microscoop bij 200 kV. De kristallijne structuur van de producten werd geïdentificeerd door röntgendiffractie-analyse (XRD, Rigaku RINT-2000) met behulp van Cu Kα-straling bij 40 keV en 40 mA. De XRD-patronen werden geregistreerd van 10° tot 90° met een scansnelheid van 0,067°s −1 . UV-vis diffuse reflectiespectra werden genomen op een UV-2550 (Shimadzu) spectrometer met behulp van BaSO4 als referentie. De elementsamenstelling werd gedetecteerd door röntgenfoto-elektronenspectroscoop (XPS, ESCALAB 250Xi). De stikstofadsorptie-desorptie-isothermen van monsters werden gemeten bij 77 K met een ASAP 2020M-instrument en geanalyseerd met de Brunauer-Emmett-Teller (BET) -vergelijking. De poriegrootteverdelingsgrafieken werden verkregen door het Barret-Joyner-Halenda (BJH) -model.
Fotokatalytische H2 Evolutie-experimenten
Fotokatalytische experimenten werden uitgevoerd in een kwartsglasreactor ca. 62 cm 3 en de opening van de reactor werd afgesloten met een septum van siliconenrubber. In een typisch fotokatalytisch experiment werd 10 mg katalysator gesuspendeerd in 30 ml 15% (v /v ) TEOA waterige oplossing met 20 mg kleurstof EY en gedispergeerd door middel van ultrasone trillingen gedurende ongeveer 15 minuten. Het systeem is ontgast door N2 . te borrelen gas om de reactantmengsels onder anaërobe omstandigheden te verzekeren. Het systeem werd bestraald met een lichtgevende diodelamp van 5 W (420 nm) voor H2 evolutie onder magnetische roerconditie.
De hoeveelheid waterstofontwikkeling werd gemeten met behulp van gaschromatografie (Tianmei GC7900, TCD, 13 X kolommen, N2 als drager).
Foto-elektrochemische metingen
Voorbereiding van werkende elektrode
Het met fluor gedoteerde tinoxide (FTO) (1 × 5 cm 2 ) substraat wordt gewassen met reinigingsmiddel, acetonoplossing, isopropylalcohol, ethanol en water onder ultrasone verwerking gedurende ongeveer 30 minuten. De katalysator (10 mg) werd toegevoegd in 500 L watervrije ethanol (met 50 L 5% Nafion-oplossing) en ultrasone behandeling om suspensievloeistof te vormen. Vervolgens wordt 0,2 ml van de bovenstaande suspensie gelijkmatig aangebracht op de voorbehandelde FTO met een druppelcoating en wordt het coatinggebied gecontroleerd op ongeveer 1 cm 2 . De geverfde elektrode wordt in een natuurlijke omgeving gedroogd en de werkelektrode wordt verkregen.
Alle PEC-metingen werden voltooid op een elektrochemisch werkstation (VersaStat4-400, Advanced Measurement Technology, Inc.) in een systeem met drie elektroden met behulp van de voorbereide fotoanode als werkelektrode, een Pt-plaat als tegenelektrode en een verzadigde calomel elektrode (SCE) als referentie-elektrode. Een 300 W xenonlamp uitgerust met een filter (λ ≥ 420) werd gebruikt als stralingsbron. 0,2 M Na2 SO4 waterige en waterstofproducerende systeemoplossing (met TEOA en kleurstof EY) was werkgever als elektrolyt. De fotostroomresponstest van de fotoanodes met aan en uit cycli werd uitgevoerd met een vaste voorspanning van 0,4 V vs. SCE.
Resultaten en discussie
Morfologie en structuur
De typische scanning-elektronenmicroscopie (SEM) beeldvorming van de UiO-66 en Pd/MOF is weergegeven in Fig. 1. De originele UiO-66 werd bereid met een eenvoudige en milde solvothermische methode. De SEM-afbeeldingen (Fig. 1a) lieten duidelijk zien dat de kale UiO-66 een uniforme grootte en een glad oppervlak heeft. Pd-nanodeeltjes werden verkregen door reductie van H2 PdCl4 bij kamertemperatuur met natriumboorhydride (NaBH4 ). Figuur 1b is het SEM-beeld van de Pd/MOF-composietfotokatalysatoren, waaruit bleek dat het oorspronkelijke gladde UiO-66-oppervlak veel fijnstof bevatte. Het kan worden bewezen dat deze kleine deeltjes elementair palladium zijn door de daaropvolgende XPS-resultaten. Het glanzende oppervlak kan extra paden bieden voor fotogegenereerde ladingen, en Pd-nanodeeltjes op het oppervlak van UiO-66 kunnen actieve plaatsen bieden voor H2 evolutie. De door foto gegenereerde ladingen kunnen snel worden overgedragen van geëxciteerde kleurstof naar UiO-66, en de verrijkte elektronen op de UiO-66 kunnen worden overgebracht naar de Pd-nanodeeltjes en gecombineerd met de protonen in de oplossing om waterstofmoleculen te vormen. Het is gunstig voor de scheiding van fotogegenereerde elektron-gaten en voor de verbetering van de fotokatalytische waterstofproductieactiviteit. Daarom werd de zeer efficiënte waterstofproductie door watersplitsing met zichtbaar licht verwacht.

De typische scanning elektronenmicroscopie (SEM) patronen van a UiO-66 en b Pd/MOF
Voor verdere studie van de morfologie van het Pd / MOF-monster en de Pd-nanodeeltjes van het UiO-66-oppervlak, werden het typische TEM-beeld en de TEM (HRTEM) -beeldpatronen met hoge resolutie getoond in Fig. 2. Zoals getoond in Fig. 2a, sommige van de Pd-nanodeeltjes worden blootgesteld aan de buitenkant van de UiO-66, wat bevorderlijk is voor de binding van elektronen en protonen in de oplossing. Bovendien is te zien dat de Pd-nanodeeltjes goed verspreid zijn op het oppervlak van UiO-66 en dat de diameter ongeveer 6 nm is. Het HRTEM-beeld (figuur 1b) laat duidelijk zien dat de roosterafstand van de kwantumgrote Pd-nanodeeltjes ca. 0,223 nm, wat consistent is met de roosterafstand van het (111) vlak van metalen Pd [48]. Het is duidelijk te zien dat de Pd-nanodeeltjes uniform waren verdeeld over het oppervlak van UiO-66 (Fig. 2c) en de grootte van de Pd-nanodeeltjes ligt tussen 4 en 9 nm (Fig. 2d). In het bijzonder is de grootte van de Pd-nanodeeltjes voornamelijk geconcentreerd bij 6 nm.
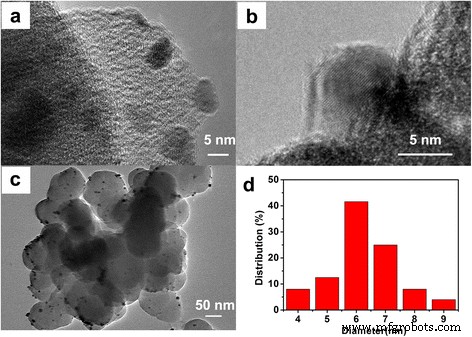
een De TEM-patronen en b de HRTEM-patronen van het Pd/MOF-monster van 3%. c , d De grootteverdeling voor Pd NP's van Pd/MOF 3% steekproef
De röntgendiffractie (XRD) patronen van de pure UiO-66 en Pd/MOF worden getoond in Fig. 3. Het is duidelijk aangetoond dat diffractiepieken goed geïndexeerd zijn met andere werken, wat aangaf dat de MOF met succes werd gesynthetiseerd [43] . Bovendien is gemeld dat het UiO-66-raamwerk stabiel is in water, benzeen, ethanol en DMF, evenals in een sterk zure (HCl) -oplossing en een sterke base (NaOH) -oplossing waar het nog steeds een aanzienlijke mate behoudt van kristalliniteit [43]. De patronen in Fig. 3 toonden aan dat de kristalliniteit van UiO-66 niet veranderde na toevoeging van de Pd-nanodeeltjes, wat aantoonde dat de Pd-nanodeeltjes de chemische structuur van het raamwerk niet hebben vernietigd. Daarom is de UiO-66 als fotokatalysatordrager haalbaar en kan de stabiele productie van waterstof worden verwacht door watersplitsing met behulp van zonne-energie in de TEOA-waterige oplossing. Bovendien werden de diffractiepieken van Pd niet waargenomen in patronen vanwege de lage belasting, kwantumgrootte en goede dispersie.
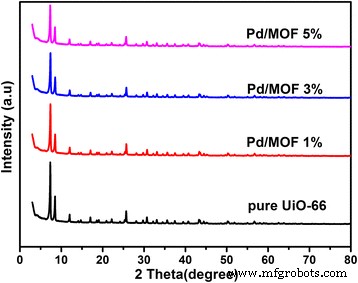
De röntgendiffractie (XRD) patronen van pure UiO-66, Pd/MOF 1%, Pd/MOF 3% en Pd/MOF 5%
De Fourier-transformatie-infraroodspectra (FTIR) van monsters worden getoond in Fig. 4. De haaienpieken verschenen op 1585 en 1400 cm −1 worden toegeschreven aan de in- en uit-fase rekwijzen van de carboxylaatgroep. Concreet, de piek op 1585 cm −1 is geassocieerd met C–C in de aromatische verbinding van de organische linker, en de piek bij 1400 cm −1 is te wijten aan C-O wortel in C-OH van carbonzuur. De piek op 659 en 746 cm −1 worden geassocieerd met respectievelijk de OH-buiging en Zr-O-modi. Bovendien is de piek bij 552 cm −1 die wordt geassocieerd met Zr–(OC) symmetrische rek en de piek bij 546 cm −1 wat geassocieerd is met Zr-(OC) asymmetrisch rekken verscheen bij lagere frequenties. Bovendien waren de posities van elke piek in alle monsters niet veranderd, wat aangeeft dat de introductie van Pd-nanodeeltjes de chemische structuur van UiO-66 [51] niet vernietigde.
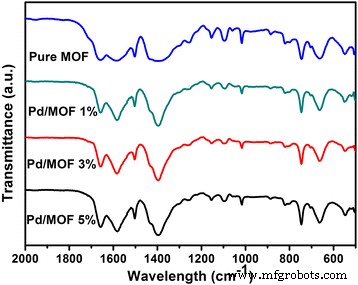
De Fourier-transformatie infraroodspectra (FTIR) van pure UiO-66, Pd/MOF 1%, Pd/MOF 3% en Pd/MOF 5%
Het BET-specifieke oppervlak (S BET ) en de poriegrootteverdelingen voor monsters werden berekend door stikstofadsorptie-desorptie-isothermmetingen (figuur 5). De poriegrootteverdelingen werden verkregen door gebruik te maken van desorptiegegevens volgens de BJH-methode. Zoals weergegeven in tabel 1 laat het zien dat de S BET van pure UiO-66 is 791.6141 m 2 /G. Na de introductie van Pd-nanodeeltjes, de S BET van de samengestelde katalysatoren neemt in verschillende mate toe. De steekproef van Pd/MOF 3% toont de grootste S BET , die bijdraagt aan de adsorptie van het kleurstofmolecuul. In het bijzonder de S BET neemt af wanneer de Pd-nanodeeltjes blijven toenemen (Pd/MOF 5%, 838,9649 m 2 /g).
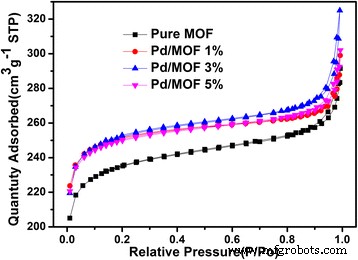
De N2 adsorptie-desorptie-isothermen van pure MOF, Pd/MOF 1%, Pd/MOF 3% en Pd/MOF 5%
Röntgenfoto-elektronspectroscopiepatronen van Pd/MOF 3%
Om de chemische samenstelling te bepalen en de chemische toestand van de elementen in het monster te identificeren, worden XPS-spectra ook weergegeven in Fig. 6. In het bijzonder kunnen alle pieken die overeenkomen met de Zr-, Pd-, O- en C-elementen worden gedetecteerd in Afb. 6a. Bovendien vertoont het spectrum met hoge resolutie van het monster twee pieken bij 333,7 en 347,2 eV, die kunnen worden toegeschreven aan Pd 3d en Zr 3p van metalen Pd. Die resultaten toonden aan dat metallisch Pd met succes is afgezet op het UiO-66-raamwerk door reductiemiddel van NaHP4 , wat in overeenstemming was met de vorige resultaten.
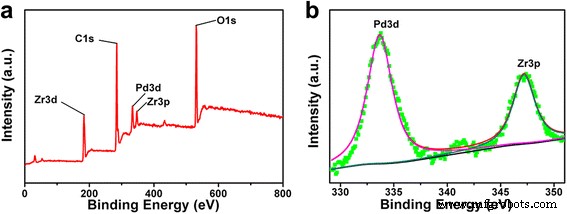
een , b Röntgenfoto-elektronspectroscopie (XPS) patronen van Pd/MOF 3%
De UV-Vis-absorptiespectra
Er werd al gemeld dat de geleidingsband van UiO-66 −0,6 V was ten opzichte van de normale waterstofelektrode (NHE), en dit is negatiever dan de redoxpotentiaal van H + /H2 (−0,4 V vs. NHE, pH =7). Het bewees dat de originele UiO-66 het potentieel heeft om waterstof te produceren door watersplitsing [42]. Fig. 7 toonde echter aan dat de pure UiO-66 een wit poeder is met een absorptiebandrand van slechts 300 nm en dat de Pd/MOF-bandrand van optische absorptie duidelijke veranderingen vertoont na toevoeging van metallisch Pd, waardoor alle kale MOF en Pd/MOf konden geen waterstof produceren door watersplitsing in het zichtbaar-lichtgebied. Om dit probleem op te lossen, werd EY ingezet voor het vergroten van het absorptiegebied. Het is bekend dat EY een fotosensitizer is, die zichtbaar licht zou kunnen absorberen. Daarom is fotokatalytische watersplitsing voor waterstofproductie met zichtbaar licht heel goed mogelijk.
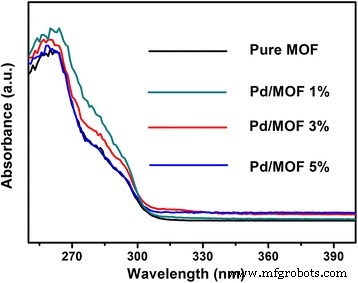
De UV-vis absorptiespectra van pure UiO-66, Pd/MOF 1%, Pd/MOF 3% en Pd/MOF 5%
De fotokatalytische activiteiten van verschillende katalysatoren voor waterstofevolutie
Het proces van fotokatalytische activiteiten voor waterstofontwikkeling is ontworpen en geïmplementeerd, waarbij TEOA (pH 10) als offerdonor werd gebruikt onder bestraling met zichtbaar licht (λ ≥ 420 nm) en introduceerde EY als fotosensitizer. De tijdvakken van H2 evolutie over verschillende katalysatoren gaf aan dat slechts sporen van H2 werd gedetecteerd (slechts 0,03 mmol na bestraling van 4 uur) in de pure UiO-66, wat te wijten is aan het elektron van aangeslagen EY dat niet ronduit kon reageren met H + bij afwezigheid van metallisch palladium. Met de toevoeging van verschillende hoeveelheden Pd-nanodeeltjes nam de fotokatalytische waterstofproductie in verschillende mate toe. 3,24 mmol H2 werd geproduceerd na 4 uur bestraling met 1% Pd geladen op MOF. Het suggereerde dat Pd een actieve soort was voor H2 productie. Bovendien, wanneer 3% Pd werd geladen naar MOF, 9,43 mmol H2 evolutie geëvolueerd, die toeschrijft aan meer actieve sites verkregen. Echter, 6,06 mmol H2 evolutie werd geproduceerd na het laden van 5% Pd, waarbij omdat overtollige Pd-nanodeeltjes het oppervlak van UiO-66 bedekten, de absorptie van kleurstofmoleculen op UiO-66 werd belemmerd. We hebben de adsorptie van verschillende kleurstoffen op de katalysator getest. De experimentele resultaten waren consistent met de BET-testgegevens. Het monster van Pd/MOF 3% vertoonde de maximale kleurstofadsorptie (39,7 μmol/g) (tabel 2). De affiniteit van metaal Pd en UiO-66 voor kleurstofmoleculen is anders, dus overmatige Pd-lading op het oppervlak van UiO-66 voorkomt adsorptie van het kleurstofmolecuul. Aan de andere kant vertoonde het monster Pd/MOF 5% een verminderde S BET , wat ook kan leiden tot een afname van de hoeveelheid geadsorbeerde kleurstof.
Effect van de pH op de fotokatalytische activiteit Pd/MOF 3% van (10 mg) voor waterstofevolutie (reactietijd 5 uur)
De pH van de oplossing had een significante invloed op de fotokatalytische activiteit (Fig. 8 en 9) [52]. Verschillende pH-waarden van de oplossing werden bestudeerd van 5 tot 11. Het is duidelijk te zien dat de snelheid van waterstofontwikkeling maximaal was bij pH 7 (18,10 mmol), terwijl de snelheid van H2 evolutie was verminderd onder zowel meer zure als meer alkalische TEOA waterige oplossingen. De snelheid van waterstofontwikkeling was slechts 0,78 mmol bij pH 5 vanwege de protonering van TEOA bij zure pH, wat resulteerde in een kortere levensduur en efficiëntie van aangeslagen EY, en de snelheid van waterstofontwikkeling was afgenomen. De activiteit van de fotokatalysator vertoonde echter een afname na toename van de basiciteit. Dit komt omdat de sterk alkalische omstandigheden de concentratie van H + . verminderen en leiden tot een afname van de kinetiek van waterstofproductie.
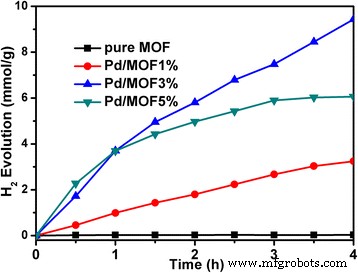
De fotokatalytische activiteiten van pure MOF, Pd/MOF 1%, Pd/MOF 3% en Pd/MOF 5% voor waterstofontwikkeling
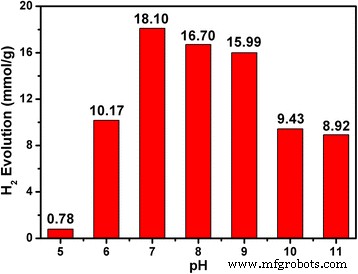
Effect van de pH op de fotokatalytische activiteit van Pd/MOF 3% (10 mg) voor waterstofontwikkeling (reactietijd 5 uur, EY 20 mg)
De stabiliteitstest voor het monster van Pd/MOF 3% in het kleurstofgevoelige fotokatalytische systeem
Om de stabiliteit van het systeem te verifiëren, is een stabiliteitstest uitgevoerd. Het stabiliteitsexperiment werd uitgevoerd in TEOA waterige oplossing met toevoeging van EY als sensibilisator. Zoals weergegeven in figuur 10, werd het experiment in vier fasen uitgevoerd. In de eerste cyclus nam de waterstofproductiesnelheid aanhoudend toe in 5 uur, wat komt omdat de kleurstof een sleutelrol heeft gespeeld in de eerste reactiecyclus. In de tweede cyclus, de N2 wordt gebruikt om het gas in het reactiesysteem te vervangen zonder extra kleurstoffen. In dit stadium wordt de waterstofproductie verminderd, wat te wijten is aan de kleurstof die werd afgebroken terwijl de reactietijd toenam. In de derde fase, de N2 als tweede trap wordt vervangend gas gebruikt en er wordt geen kleurstof toegevoegd. In dit stadium nam de waterstofproductie continu af, en dit was voornamelijk te wijten aan de toevoeging van afgebroken kleurstoffen. In de vierde fase werd het gas in het reactiesysteem vervangen door N2 en toegevoegd aan EY (20 mg). In dit stadium wordt de opbrengst aan waterstof duidelijk teruggewonnen in vergelijking met de derde fase, die te danken is aan het toegevoegde eosine. De bovenstaande resultaten laten zien dat de bereide Pd/MOF 3%-katalysator uitstekende eigenschappen heeft en dat de stabiliteit van het kleurstofgesensibiliseerde systeem moet worden verbeterd, wat ook de focus is van de volgende stap.
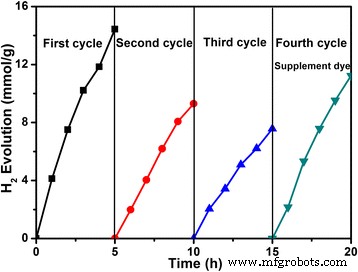
De stabiliteitstesten voor het monster van Pd/MOF 3% in het kleurstofgevoelige fotokatalytische systeem
Fotoluminescentie (PL) Analyse
Om de overdracht van door foto gegenereerde elektronen te onderzoeken, werd de fotoluminescentie-uitdoving van EY onderzocht. Zoals weergegeven in figuur 11, vertoonde de kleurstof EY een maximale emissiegolflengte van 537 nm wanneer de excitatiegolflengte 460 nm was. Na de toevoeging van UiO-66 veranderde de intensiteit van de maximale excitatiegolflengte niet duidelijk, maar de fluorescentie-intensiteit van de maximale emissiegolflengte werd in verschillende mate verminderd na toevoeging van verschillende Pd/MOF-monsters. Dit geeft aan dat Pd-deeltjes een sleutelrol spelen in de elektronenoverdracht van het systeem. Toen de Pd/MOF 3% werd toegevoegd, was de fluorescentie-intensiteit het laagst, wat het beste scheidingseffect van een door foto gegenereerd elektrongat bewees. Dit resultaat was in overeenstemming met het tijdsverloop van waterstofontwikkeling door verschillende katalysatoren. Wanneer Pd-nanodeeltjes zijn geïntroduceerd, kunnen de door foto gegenereerde elektronen in UiO-66 snel worden overgedragen naar Pd. Ze vertoonden dus een scherpe afname van de emissie-intensiteit van EY.
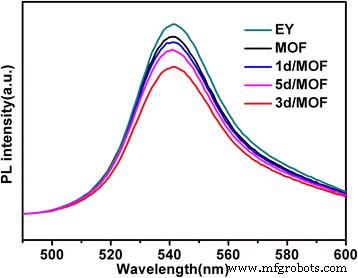
Fluorescentiespectra van de EY-gesensibiliseerde MOF-, Pd/MOF 1%-, Pd/MOF 3%- en Pd/MOF 5%-monsters in 15% (v /v ) TEOA waterige oplossing bij pH 10
De foto-elektrische prestatietest
Om het proces van elektronenoverdracht in het systeem verder te bestuderen, werd ook de foto-elektrische eigenschap van het met kleurstof gesensibiliseerde fotokatalytische waterstofproductiesysteem getest. Afbeelding 12a zijn de momentane fotostroom-tijdcurves voor monsters van pure MOF, Pd/MOF 1%, Pd/MOF 3% en Pd/MOF 5%. Het laat zien dat de fotostroomdichtheid van pure MOF het laagst is onder zichtbaar licht. Toen de Pd-nanodeeltjes op MOF werden geladen, nam de fotostroomdichtheid aanzienlijk toe en toen de 3% Pd werd geïntroduceerd, bereikte de fotostroomdichtheid het maximum. Het superieure specifieke oppervlak van MOF-materiaal is gunstig voor de adsorptie van een groot aantal kleurstofmoleculen. Onder bestraling met zichtbaar licht wordt kleurstof EY geëxciteerd om een aangeslagen toestand te vormen en vervolgens wordt het aangeslagen toestand EY-molecuul geblust door TEOA om een sterk reducerende EY te vormen − ·. EY − · kan snel elektronen afleveren aan de MOF en vervolgens deelnemen aan de reacties. Elektronen kunnen echter niet snel bij het overdrachtsproces worden betrokken, waardoor een groot aantal elektronen verloren gaat. Een enkele MOF vertoont dus zeer lage fotostroomdichtheden en waterstofproductieactiviteit. Pd-nanodeeltjes dienen als een elektronenuitgang, waardoor grote hoeveelheden elektronen snel naar het MOF-oppervlak kunnen worden overgebracht en daardoor de fotostroomdichtheid en waterstofproductie worden verbeterd. De foto-elektrische testresultaten komen goed overeen met de kinetiek van waterstofproductie, en het bewees dat de Pd-nanodeeltjes inderdaad de fotokatalytische activiteit van MOF kunnen verbeteren.
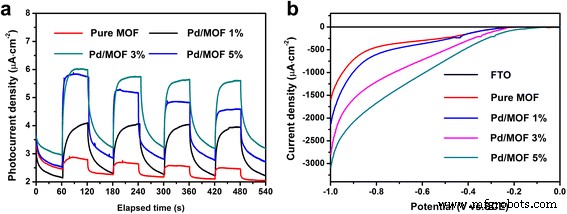
een Transient photocurrent responses for samples of MOF, Pd/MOF 1%, Pd/MOF 3%, and Pd/MOF 5% in 0.2 M Na2 SO4 aqueous solution under visible-light irradiation (λ ≥ 420 nm) at 0.4 V vs. SCE. b Linear sweep voltammograms of MOF, Pd/MOF 1%, Pd/MOF 3%, and Pd/MOF 5% in 0.2 M Na2 SO4 aqueous solution under visible-light irradiation (λ ≥ 420 nm)
Figure 12b is a linear voltammetric scan for the samples. As can be seen from the diagram, a weak current response is found on the FTO at the lower voltage, which is due to the cathodic current produced by the reduction of H + to H2 under severe negative pressure. At the same voltage, the sample adding Pd showed a higher current response than the pure MOF. Especially after 3% of the Pd was added to MOF, the sample Pd/MOF 3% showed the most prominent current response. These results are in good agreement with the above test results. It proved that Pd nanoparticles can significantly enhance the hydrogen production activity of MOF in dye-sensitized photocatalytic system.
Speculation on the Mechanism for H2 Evolution
Based on the above results, the possible mechanism of photocatalytic hydrogen evolution in EY-sensitized system can be explained in Scheme 1. The large specific surface area of UiO-66 is beneficial to the adsorption of dye molecules. Firstly, a large number of EY molecules were adsorbed onto the surface of UiO-66 by physical adsorption. Then, the ground state of EY absorbs light photo to form singlet excited state EY 1* under visible-light irradiation. Singlet excited EY 1* rapidly produces the lowest lying triplet excited state EY 3* via an efficient intersystem crossing (ISC). In the case of existing TEOA as a sacrificial donor, EY 3* can be reductively quenched and can produce EY −· . Subsequent electron transfer can be obtained by comparing the energy levels. It has been reported that the reductive potential of EY −· is −0.8 V vs. NHE, and the conduction band of UiO-66 is −0.6 V vs. NHE. Therefore, the electrons can actively transmit from EY −· to UiO-66. The accumulated electrons on UiO-66 frameworks will transfer to the Pd nanoparticles, and finally, H + obtains electrons from Pd to form hydrogen. UiO-66 can function as an excellent electron acceptor and transporter to efficiently prolong the lifetime of charge carriers. Consequently, it improves the charge separation efficiency and the catalytic H2 evolution activity of the Pd/MOF. The UiO-66 has extremely large surface area and well-order porous structures and channels and is conducive to the electron transfer.
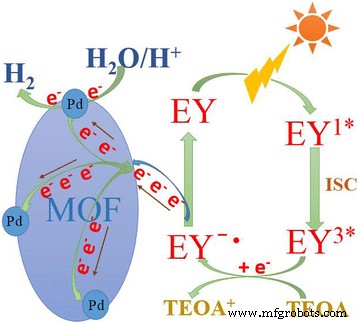
Possible mechanism of photocatalytic hydrogen evolution in EY-sensitized system
Conclusions
The Pd/MOF catalysts were prepared by impregnation reduction. It is important that we have reasonably constructed the dye-sensitized system of Pd/MOF and successfully extended the application of MOF to the visible range. The Pd-loaded Zr-MOF was tested for efficient photocatalytic hydrogen production and exhibited maximal photocatalytic activity (9.1 mmol/g) under visible-light irradiation (λ ≥ 420 nm) with EY as a photosensitizer. The remarkable enhanced properties of which was carefully studied by means of XRD, TEM, HRTEM, XPS, UV-vis diffuse reflectance, and photocatalytic hydrogen production. The results are consistent with each other. The activities of photocatalytic hydrogen production was enhanced twice order of magnitude compared with the pure MOF (0.09 mmol/g). The promotion of photocatalytic hydrogen evolution activity should be attributed to the utilization of the longer wavelength visible light and a great electronic transmission capacity of MOF. The synergistic effect between Pd and Zr-MOF is corroborated by photo-luminescence spectra and electro-chemical and photo-electro-chemical experiments, which demonstrated that the charge separation and the electron transfer are more efficient with the aid of Pd. The possible mechanism had been presented. The EY was employed for increasing absorb band gap of irradiation. UiO-66 could accept and transport electron and contribute to prolong the lifetime of charge carriers. Pd as an active species significantly enhanced the photocatalytic activity for hydrogen evolution.
Nanomaterialen
- Schaeffler ontwikkelt nieuwe technologieën voor de industrialisatie van waterstofproductie
- MoS2 met gecontroleerde dikte voor elektrokatalytische waterstofevolutie
- S, N co-gedoteerde grafeen Quantum Dot/TiO2-composieten voor efficiënte fotokatalytische waterstofgeneratie
- Koolstofnanodots als dual-mode nanosensoren voor selectieve detectie van waterstofperoxide
- Hiërarchische heterostructuur van ZnO@TiO2 holle bollen voor zeer efficiënte fotokatalytische waterstofevolutie
- PtNi-legering Cocatalyst-modificatie van eosine Y-gesensibiliseerde g-C3N4/GO-hybride voor efficiënte zichtbaar-licht fotokatalytische waterstofevolutie
- S-gedopeerd Sb2O3-nanokristal:een efficiënte zichtbaar-lichtkatalysator voor organische afbraak
- Efficiënte productie van hoogwaardig grafeen met weinig lagen met behulp van een eenvoudige hydrodynamisch ondersteunde exfoliatiemethode
- Een ternair magnetisch recyclebaar ZnO/Fe3O4/g-C3N4 composiet fotokatalysator voor efficiënte fotodegradatie van monoazo kleurstof
- 5 Kwaliteitscontroles uw fabrieksbehoeften voor efficiënte productie
- Traceerbaarheidspraktijken voor castingproductie



