Structurele eigenaardigheden van ion-geleidende organisch-anorganische polymeercomposieten op basis van alifatische epoxyhars en zout van lithiumperchloraat
Abstract
Het artikel heeft betrekking op hybride amorfe polymeren die zijn gesynthetiseerd op basis van epoxyoligomeer van diglycide-alifatische ester van polyethyleenglycol, dat werd uitgehard met polyethyleenpolyamine en lithiumperchloraatzout. Structurele eigenaardigheden van organisch-anorganische polymeercomposieten werden bestudeerd door differentiële scanningcalorimetrie, groothoekröntgenspectra, infraroodspectroscopische, scanning-elektronenmicroscopie, elementanalyse en transmissie- en reflectieve optische microscopie. Enerzijds lieten de resultaten zien dat de introductie van LiClO4 zout in epoxypolymeer leidt tot de vorming van de coördinerende metaal-polymeercomplexen van het donor-acceptortype tussen centrale Li + ion en ligand. Aan de andere kant werd ook het verschijnen van amorfe micro-insluitingen gevonden, waarschijnlijk van anorganische aard.
Achtergrond
Vloeibare elektrolyten worden vaak gebruikt in lithium- of lithium-ionbatterijen bij kamertemperatuur met een ionische geleidbaarheid van 10 −3 tot 10 −2 S/cm [1, 2].
Het zou handig zijn als de accu's bij hogere temperaturen zouden kunnen werken, omdat er dan geen apart koelcircuit op systeemniveau nodig is of de behoefte aanzienlijk wordt verminderd [3]. Hoge temperaturen veroorzaken echter problemen vanwege de snelle afbraak van vloeibare elektrolyten [3]. Daarnaast zijn er twee hoofdproblemen die de ontwikkeling van vloeibare elektrolyten belemmeren. Ten eerste leidt de vorming van lithiumdendrieten op elektroden tot ernstig gevaar vanwege de mogelijke mogelijkheid van interne kortsluitingen. Ten tweede veroorzaakt de elektrochemische instabiliteit van de lithiumelektroden een onbeduidende levenscyclus van batterijen tijdens herhaalde laad-/ontlaadprocessen [4].
Bovendien hebben de eerste generatie batterijprototypes, die vloeibare elektrolyten gebruikten, een hoog risico op lekken die de betrouwbaarheid van een apparaat aantasten [1]. Veiligheid is een van de meest urgente kwesties in verband met de verdere vooruitgang in de ontwikkeling van de volgende generatie batterijen. Dat maakt vaste elektrolyten een van de meest veelbelovende kandidaten voor de vervanging van ontvlambare en potentieel gevaarlijke vloeibare elektrolyten [5].
Vaste polymeerelektrolyten (SPE) zijn in verschillende toepassingen gebruikt als ionengeleiders in verschillende elektrochemische apparaten zoals lithiumbatterijen, ultracondensatoren, brandstofcellen en zonnecellen [6]. Oplaadbare lithium- en lithium-ionbatterijen spelen een belangrijke rol op de markt van elektrochemische energieopslagapparaten, aangezien ze veel worden gebruikt voor het opladen van draagbare elektronische apparaten en voor autonome besturingsapparaten [2]. Daarom was recentelijk de ontwikkeling van nieuwe vaste polymeerelektrolyten een belangrijk doel, aangezien een optimale balans tussen hoge ionische geleidbaarheid en technologische materiaalcondities nog steeds niet is bereikt [7, 8]. SPE hebben eigenschappen als goede compatibiliteit met elektroden, lage zelfontladingssnelheid, gemakkelijke verwerking voor verschillende vormen en maten, gebrek aan lekkage, flexibiliteit en zelfvoorziening voor vormveranderingen tijdens laad-ontlaadcycli [7,8,9,10 ].
Polyethyleenoxide (PEO) [11, 12] is een van de meest bestudeerde oligomeren, die worden gebruikt voor het maken van SPE vanwege de effectieve coördinatie van metaalionen daarin vanwege de optimale afstand en oriëntatie van etherzuurstofatomen in zijn moleculaire ketens [ 12]. Het nadeel van PEO is de amorf-kristallijne structuur [4, 13, 14] die leidt tot de geleidbaarheid door het amorfe gebied van een polymeer alleen [11, 15] boven de glasovergangstemperatuur T g [6, 12, 16], en als gevolg daarvan heeft PEO een lage ionische geleidbaarheid bij kamertemperatuur vanwege de aanwezigheid van een hoge kristallijne fase [4, 14, 17].
Tegenwoordig omvatten vaste polymeerelektrolyten in de regel anorganische zouten die oplossen in oligomeren die op hun beurt een vaste matrix vormen met de ionische geleidbaarheid [10, 12, 18, 19]. Toegevoegd zout dient als een bron van ionen en draagt bij aan hun beweging langs de polymeerketens, zodat het een cruciale rol speelt bij het ionentransport in polymeerelektrolyten [16]. Hierbij zijn concentratie en mobiliteit van ionen belangrijke parameters die de geleidbaarheid in polymeerelektrolyten beïnvloeden [14, 17]. Het begrijpen van het mechanisme van het ionentransport in een polymeer vereist de studie van ion-ion- en ion-polymeer-interacties, wat van groot belang is [10, 14]. Er zijn veel onderzoeken naar ionentransport in polymeerelektrolyten uitgevoerd met verschillende soorten kationen zoals Na + , Li + , Ag + , en Mg + [20]. De composieten op basis van lithiumzouten worden echter bij voorkeur bestudeerd, omdat de Li + kationen zijn de kleinste en kunnen gemakkelijk in een polymeermatrix bewegen [17, 20]. Een ander belangrijk kenmerk is de thermische stabiliteit van ionen en hun inertie ten opzichte van de celcomponenten [21].
Hoge ionische geleidbaarheid kan worden bereikt door de zoutconcentratie in polymeer te verhogen [6]; de auteurs [9] hebben echter aangetoond dat de geleidbaarheid van de composieten op basis van PEO wordt beperkt door een bepaalde waarde van een zoutconcentratie. Bij hogere zoutconcentratie neemt de geleidbaarheid af door vorming van de ionencomplexen, wat op zijn beurt leidt tot een afname van de ionenmobiliteit en het aantal ladingsdragers [10].
Voor toepassing als elektrolyten moeten polymeren bepaalde eigenschappen hebben, zoals amorfheid, de aanwezigheid van etherzuurstof in hun structuur, lage glasovergangstemperatuur, hoge dimensionele stabiliteit, mechanische sterkte en het vermogen om dunne films te vormen [9, 18]. Een van de geschikte materialen die aan deze eisen voldoet, is alifatisch epoxyoligomeer, namelijk de diglycide alifatische ester van polyethyleenglycol. Het heeft een identieke ketenstructuur als polyethyleenoxide, maar is amorf en kan de hoge concentratie lithiumperchloraatzout op dezelfde manier oplossen als PEO.
Daarom is het doel van dit werk de synthese van vaste amorfe polymeercomposieten op basis van alifatische epoxyoligomeer en de studie van de invloed van lithiumperchloraatzouten op hun structuur.
Methoden
Materialen en synthese
Het epoxy-oligomeer (diglycide alifatische ester van polyethyleenglycol (DEG-1)) en lithiumperchloraat (LiClO4 ) zout werden gebruikt voor de synthese van ionengeleidende epoxypolymeercomposieten. Deze componenten zijn vooraf 24 uur onder vacuüm bij 80 °C voorgedroogd. Na drogen werd het zout opgelost in het DEG-1-oligomeer. Oplossingen van DEG-1-LiClO4 werden bereid met LiClO4 inhoud van 0 tot 50 phr van DEG-1. 10 phr polyethyleen polyamine (PEPA) verharder is gebruikt als verharder voor de synthese van de composieten.
Thermische eigenschappen werden bestudeerd door differentiële scanning calorimetrie (DSC) met TA Instruments DSC Q2000 in het temperatuurbereik van -70 tot +150 °C met een verwarmingssnelheid van 10 °C/min. Glasovergangstemperatuur (T g ) werd bepaald uit de DSC-curven bij de tweede verwarming. De experimentele fout bij het bepalen van de glasovergangstemperaturen was ±1 °C.
De elektrische en diëlektrische eigenschappen werden onderzocht door de breedband diëlektrische analysator "Novocontrol Alpha" met Novocontrol Quatro Cryosystem (Novocontrol Technologies, Montabaur, Duitsland) die was uitgerust met een circuit met twee elektroden, in het frequentiebereik van 10 −1 tot 10 7 Hz en het temperatuurbereik van -60 tot +200 °C. De spanning die op een monster werd aangelegd was gelijk aan 0,5 V. De testmonsters hadden een diameter van 20 mm en een dikte van 0,5 mm en waren vooraf onder vacuüm gecoat met een aluminiumlaag. De verkregen gegevens werden geanalyseerd met behulp van de software "Novocontrol WinDeta 3.8."
Structurele organisatie en kenmerken van macromoleculaire ordening van de gesynthetiseerde polymeersystemen werden onderzocht met behulp van groothoekröntgenspectra (WAXS) met behulp van de röntgendiffractometer DRON-4.7. Optisch röntgenschema werd uitgevoerd door de Debye-Scherer-methode bij het passeren van de primaire straal door het polymeermonsterpolymeer met behulp van CuK α emissie (λ =-1,54 Å) die monochromatisch is gemaakt door Ni-filter. De onderzoeken werden uitgevoerd door automatische stapscanning in het bereik van verstrooiingshoeken (2θ ) van 2,6° tot 40°, en de belichtingstijd was 5 s.
Infrarood (IR) spectroscopische onderzoeken zijn uitgevoerd met een spectrometer met Fourier-transformatie "Tensor-37" van Bruker Corp. in het golfbereik van 600°–3800° cm −1 . Volgens het paspoort van het apparaat is de relatieve meetfout <2%.
De morfologische kenmerken van de gesynthetiseerde composieten werden bestudeerd met behulp van de methode van de reflecterende optische microscopie (ROM) door Unicorn NJF 120A polarisatiemicroscoop bij polarisatiehoeken 0 ° -90 °. Microfoto-analyse werd uitgevoerd met behulp van Carl Zeiss Imaging Solutions AxioVision V4.7.1-software.
Structurele kenmerken van de gesynthetiseerde composieten zijn bestudeerd met behulp van methoden van de elektronenmicroscopie (SEM) door JEOL 100-CX II transmissie-elektronenmicroscoop, uitgerust met een scansysteem. Elementaire analyse van insluitsels werd uitgevoerd met behulp van een analytisch complex bestaande uit een scanning-elektronenmicroscoop JEOL JSM-35CF en röntgenspectrometer met dispersieve in energie-röntgenquanta (model INCA Energy-350 van "Oxford Instruments"). Een belangrijk kenmerk van een dergelijke elektronenmicrosonde-analyse is de plaats:de maximale grootte van het excitatiegebied is 2 m. Volgens de morfologische kenmerken en de chemische samenstelling op basis van de energiedispersieve spectrale analyse, is de automatische scheiding van insluitsels op typen (elementaire samenstelling) en het meten van hun grootte uitgevoerd. De resultaten zijn geanalyseerd met behulp van een speciaal programma voor kwantitatieve faseverdeling en inclusieonderzoek. Alle resultaten worden weergegeven in gewichtspercentages. De experimentele fout was 0,1%.
WAXS-, IR-, ROM- en SEM-onderzoeken en elementanalyse werden uitgevoerd bij de temperatuur T = 20 ± 2 °C.
Resultaten en discussie
Analyse van de DSC-onderzoeken en van het diëlektrische en elektrische onderzoek van de gesynthetiseerde composieten met een lithiumperchloraatzoutgehalte van 0 tot 20 phr werd eerder gepresenteerd in ons artikel [22]. Verdere verbreding van LiClO4 inhoud (van 0 tot 50 phr) handhaaft lineaire toename van glasovergangstemperatuur T g van -10 tot 64 °C (afb. 1a). Dat kan een gevolg zijn van elektrostatische interacties tussen lithiumkationen Li + en de macromoleculaire keten van DEG-1 met vorming van coördinatieve complexen, die gepaard gaan met verplaatsing van de elektronendichtheid van de zuurstofatomen en hun gedeeltelijke polarisatie. Het wordt weerspiegeld in een substantiële vermindering van de segmentale mobiliteit van DEG-1-ketens binnen de gevormde complexen die wordt weergegeven in de toename van de glasovergangstemperatuur van de polymeermatrix.
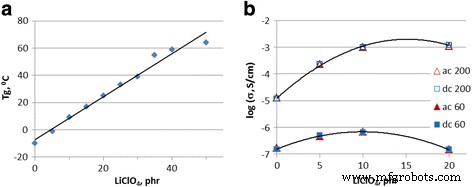
Thermische en elektrische eigenschappen van composieten. een Afhankelijkheid van glasovergangstemperatuur T g (een ) en geleidbaarheid σ bij 60 en 200 °C (b ) op LiClO4 zoutgehalte
Afbeelding 1b toont de verandering van geleidbaarheid σ met groei van LiClO4 inhoud in composiet. Bij lage temperatuur (60 °C) is de maximale waarde van σ wordt bereikt bij 10 phr zout en de σ waarde van composiet met 20 phr LiClO4 is gelijk aan die in zuivere DEG-1. Bij hoge temperatuur (200 °C) zal de σ waarden zijn drie ordes van grootte hoger met een maximum bij 15 phr van LiClO4 . Een dergelijk karakter van geleidbaarheidsafhankelijkheid van LiClO4 inhoud kan worden verklaard door het bestaan van twee tegengestelde concurrerende processen. Ten eerste geeft de groei van het zoutgehalte in composiet de toename van het aantal dragers en de toename van de geleidbaarheid. Ten tweede, groei van T g weerspiegelt de beperking van DEG-1 moleculaire bewegingen die de mobiliteit van de dragers vermindert. Bij hogere temperaturen compenseert de verhoging van moleculaire bewegingen dit mechanisme en wordt de geleidbaarheid aanzienlijk hoger.
Analyse van de groothoek röntgendiffractiepatronen van de systemen heeft aangetoond dat ze allemaal amorf zijn (figuur 2). De gemiddelde waarde van de periode (d ) van een moleculaire ordening op korte afstand van DEG-1/PEPA internodale moleculaire segmenten die zich in het polymeervolume bevinden, kan worden berekend met behulp van de Bragg-vergelijking:
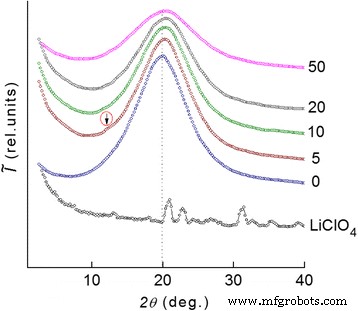
De WAXS-onderzoeken van de DEG-1/LiClO4 systemen. De groothoek röntgendiffractiepatronen van een lithiumperchloraatzout LiClO4 en systemen met het verschillende zoutgehalte (getoond in de buurt van curven)
$$ d=l{\left(2 \sin {\theta}_m\right)}^{-1} $$waar λ is de golflengte van de karakteristieke röntgenstraling (λ = 1.54 Å voor CuK α emissie) en is gelijk aan 4,44 .
Echter, de introductie van LiClO4 zout met een kristallijne structuur in de epoxyhars gaat gepaard met veranderingen in het diffractiepatroon. Dat blijkt uit de aanwezigheid van subtiele diffractiepieken van het diffuse type op 2θ m -12,2° op de achtergrond van de amorfe halo, die vergelijkbaar is met de hoekpositie van de DEG-1 op 2θ m ≈ 20,0° (d ≈ 4.39 ). Deze diffractiepiek kenmerkt het bestaan van metaal-polymeercomplexen van het donor-acceptortype, in ons geval tussen centrale ionen (Li + ) en etherzuurstof van de epoxyketens in het intermoleculaire volume van de epoxyhars, en dit bevestigt de veronderstellingen gemaakt door de analyse van DSC-gegevens. Gebaseerd op de hoekpositie van deze diffractiepiek in composiet met 50 phr LiClO4 , de gemiddelde Bragg-afstand d tussen de moleculaire ketens gecoördineerd door kationen Li + is 4.30 .
De structuur van de polymeercomposieten is onderzocht door middel van infraroodspectroscopie. De belangrijkste absorptiebanden van LiClO4 , DEG-1 en PEPA met relevante groepen worden weergegeven in tabel 1. Deze absorptiebanden werden respectievelijk geïnterpreteerd in overeenstemming met [23,24,25].
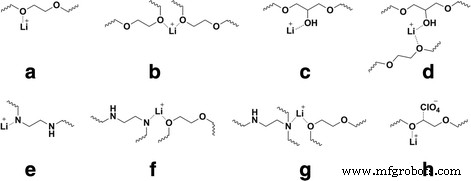
Zoals men kan zien, zijn de karakteristieke absorptiebanden van de ring van epoxy's afwezig in de spectra (Fig. 3, 0 phr LiClO4 inhoud) die de volledige uitharding van de epoxycomponent aangeeft. Deze absorptiebanden zijn ook afwezig in de IR-spectra (Fig. 3, 5-50 phr) van de uitgeharde composieten. De absorptiebanden in het bereik van golfnummers 1300–1520 en 1000–1190 cm −1 , die respectievelijk overeenkomen met fluctuaties van –CH2 – en (C–O–C en C–NC) groepen, uitbreiden en verschuiven naar het laagfrequente gebied met LiClO4 inhoud toenemen. Het is bekend dat dit kan worden geassocieerd met de vorming van coördinatiebindingen tussen Li + kationen en ClO4 − anionen en polymeerketens [26, 27]. Het is algemeen aanvaard dat Li + kationen kunnen gemakkelijk complexen vormen met polyethyleenetherbindingen [23, 24, 27,28,29,30] en ook met polyaminen [31]. De absorptieband bij 1637 cm −1 in het IR-spectrum van LiClO4 geeft de niet-gedissocieerde staat aan (tabel 1) [23, 24]. Opgemerkt moet worden dat deze band in de IR-spectra van 5-50 monsters afwezig is. Dit geeft aan dat de zuivere (niet-gedissocieerde) vorm van LiClO4 in de composieten is niet opgenomen. In overeenstemming hiermee zijn in Fig. 4 de mogelijke ion-dipoolinteracties van Li + ion met de etherbinding van polyethyleenoxidefragment en OH-groep van de onthulde epoxyring van DEG-1 (Fig. 4a-d) en met secundaire aminegroep van PEPA (Fig. 4e), met secundaire of tertiaire aminegroep en etherbinding gelijktijdig (Fig. 4e-g), worden weergegeven. Als voorbeeld van gecoördineerde ClO4 − ion, Fig. 4h geeft het schema weer van deze anion-interactie met een positief geladen koolstofatoom dat zich in de buurt van het elektronegatieve zuurstofatoom bevindt.
De IR-spectra van de composieten. De infraroodspectroscopie van de systemen met de verschillende lithiumperchloraatzoutgehaltes (de getallen in de buurt van curven)

een –u Regelingen van complexen. Complexen die mogelijk voorkomen in de systemen LiClO4 /DEG-1/PEPA
Opgemerkt moet worden dat in het monster met toevoeging van 5 phr lithiumperchloraat en na stollen een nieuwe absorptieband bij 864 cm −1 verschijnt in zijn IR-spectrum, dat in de monsters met een zoutgehalte van 10-50 phr behouden blijft. Aangezien de meeste absorptiebanden van metaalcomplexen zich in het laagfrequente gebied [32] bevinden, is het duidelijk dat deze absorptieband geassocieerd is met complexen waarbij LiClO4 betrokken is. . De interactie van PEO en LiClO4 wordt veel bestudeerd in de literatuur en in gepresenteerde materialen is de absorptieband rond 860 cm −1 is afwezig [23, 24, 27,28,29,30]. Waarschijnlijk verwijst deze band naar de vorming van lithium-aminocomplex, welke aanwezigheid de fluctuaties van in de buurt gelegen methyleengroepen beïnvloedt. Dat wordt bevestigd door het verschijnen van een nieuwe absorptieband in het IR-spectrum van composiet met 5 phr LiClO4 op 1525 cm −1 (Fig. 3), die wordt verschoven naar het laagfrequente gebied met een verhoging van het zoutgehalte tot 50 phr. Volgens [26] is dit te wijten aan het toenemende aantal coördinatieobligaties. Belangrijk om op te merken dat wanneer filmmonsters met 5-50 phr LiClO4 werden vermalen tot een poeder en gegoten in de KBr-tabletten, de beschreven absorptiebanden bij ≤1525 en 860-864 cm −1 verdwenen, aangezien verplettering leidt tot vernietiging van de zwakke coördinatiebindingen. Dat bevestigt ook het coördinerende karakter van deze banden. Als voorbeeld toont Fig. 5 de IR-spectra van de monsters met 5 en 30 phr LiClO4 inhoud.
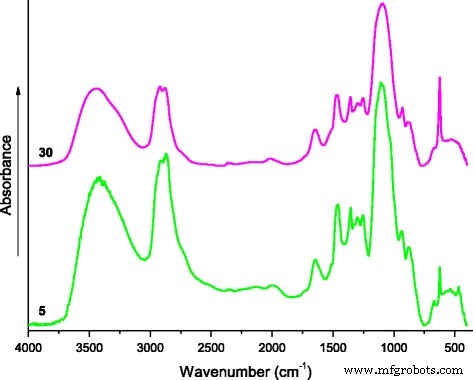
De IR-spectra (in tabletten van KBr). De IR-spectra van de composieten met verschillende LiClO4 inhoud (gemarkeerd door cijfers in de buurt van curven)
Over het algemeen is de toenemende hoeveelheid LiClO4 leidt tot de toename van de coördinatiebindingen, die de mobiliteit van macromoleculaire ketens verminderen [28]. Afbeelding 3 toont een geleidelijke afname van de intensiteit van de absorptiebanden geassocieerd met valentiefluctuaties van OH–, NH– en –CH2 – groepen. Bij de vernietiging van coördinatiebindingen in de monsters gevormd in de KBr-tabletten, komen deze valentiebindingen duidelijk tot uiting (Fig. 5).
Naast de coördinatiebindingen moeten andere belangrijke factoren die van invloed zijn op de structuur van de verkregen composieten worden aangegeven. Dus de reactie tussen DEG-1 en PEPA in aanwezigheid van LiClO4 komt blijkbaar vollediger voor (tot een bepaalde zoutlimiet), aangezien bekend is dat LiClO4 is een effectieve aminolysekatalysator van oxiranenring [33]. Een andere structuurvormende factor kan worden gerealiseerd als een net van waterstofbruggen, inclusief die met de deelname van ClO4 − ionen [30].
In ons geval zijn de complexen van Li + ionen met maximaal coördinatiegetal 2 worden weergegeven in figuur 4, maar het coördinatiegetal van ionen kan 8 bereiken [31]. Vanwege de kleine straal (0,6 A) is de Li + ionen zijn zeer mobiel, dus ze kunnen de complexen gemakkelijk maken en vernietigen [29, 31], en daarom is het moeilijk om een complexe structuur te definiëren met lithiumperchloraatzout dat werd gevormd tijdens de uithardingsreactie.
Figuur 6 toont de microfoto's van reflecterende optische microscopen van de gesynthetiseerde composieten met verschillende inhoud van lithiumperchloraatzout. De vorming van geordende structuren in de composieten met toevoeging van het zout aan het systeem werd waargenomen. In dit geval onthulde de reflecterende optische microscopie die werd gebruikt in gepolariseerde modus de aanwezigheid van de gedistribueerde insluitsels, waarschijnlijk van anorganische aard met afmetingen variërend van 2 tot 20 m. Om de aanwezigheid van insluitsels in de composieten te bevestigen, werd het structurele onderzoek uitgevoerd met behulp van scanning-elektronenmicroscopie. De resultaten worden weergegeven in Fig. 7. Men kan de aanwezigheid van de insluitsels zien die worden waargenomen door ROM (voor de monsters met wat LiClO4 inhoud) en de toename van hun aantal en grootte met de toename van LiClO4 inhoud in de composieten. Om de aard van gevonden insluitsels te bepalen, de elementanalyse van negen verschillende oppervlaktegebieden van de composiet met 50 phr LiClO4 is voldaan (Fig. 8). Genormaliseerde massaverdeling van elementen in de microgebieden getoond in Fig. 8 worden weergegeven in Tabel 2. Het is duidelijk dat de inhoud van elementen in spectra anders is. Het is belangrijk dat de insluitsels geïdentificeerd door ROM (Fig. 6) en SEM (Fig. 7) worden gekenmerkt door het verminderde gehalte aan koolstof en het verhoogde gehalte aan zuurstof en chloor, die in de samenstelling van LiClO4

Reflecterende optische microscopie resultaten. ROM van het epoxypolymeer met a 0, b 10, c 20, en d 50 phr LiClO4 zout
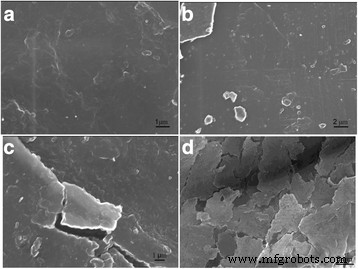
Scanning elektronenmicroscopie resultaten. SEM van de composieten met a 0, b 10, c 20, en d 50 phr LiClO4 zout

SEM met elementanalyse. SEM van het composiet met 50 phr LiClO4 oppervlak met de benoeming van spectra voor elementanalyse
De elementaire samenstelling van het initiële lithiumperchloraatzout werd ook bepaald. Er werd gevonden dat het chloorgehalte in zout 41,61%wt . is en zuurstof is 58,39%gew . Lithiumgehalte kon niet worden bepaald.
Samenvattende elementaire kaart (Fig. 9d) van de composiet met 20 phr LiClO4 werd geconstrueerd uit elementaire kaarten van individuele elementen (koolstof-Fig. 9a; zuurstof-Fig. 9, b; chloor-Fig. 9c) voor het bepalen van de verdeling van elementen op het oppervlak. De berekeningen hebben aangetoond dat de inhoud van de elementen op het oppervlak van de composiet als volgt is:koolstof is 51,57 gew.%, zuurstof is 43,79 gew.% en chloor is 4,64 gew.%, terwijl hun verdeling samenvalt met de volgorde van insluitsels geïdentificeerd door de middelen van optische en elektronenmicroscopie. Dit laat toe te concluderen dat de aard van deze insluitsels met zuurstof- en chloorverzadiging anorganisch is.
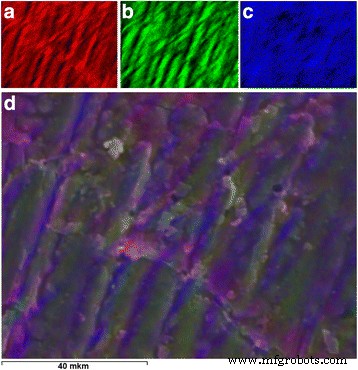
De resultaten van de elementanalyse. De elementaire kaart van het oppervlak van de composiet met 20 phr LiClO4 :een C, b O, c Cl en de d gecombineerde kaart
Conclusies
De uitgebreide studie van composieten op basis van alifatische epoxyoligomeer (DEG-1) met verschillende hoeveelheden LiClO4 zout (0–50 phr) onthulde het ontstaan van interacties tussen lithiumkationen Li + en de macromoleculaire keten van DEG-1 met vorming van coördinatieve complexen. Het wordt weerspiegeld in een aanzienlijke vermindering van de segmentale mobiliteit van DEG-1-ketens binnen de gevormde complexen die de glasovergangstemperatuur lineair verhogen T g van polymeermatrix met het zoutgehalte.
Het bleek dat bij hogere temperatuur (200 versus 60 °C), de geleidbaarheidswaarden σ zijn drie orden van grootte hoger met een maximum van 15 phr van LiClO4 . Dergelijk geleidbaarheidsgedrag wordt verklaard door het bestaan van twee tegengestelde concurrerende processen, namelijk de groei van het zoutgehalte in composiet geeft de toename van het dragergetal en de toename van de geleidbaarheid. Aan de andere kant vermindert de beperking van moleculaire bewegingen van DEG-1 vanwege de vorming van de coördinatieve complexen de mobiliteit van de drager. Bij hogere temperaturen compenseert de verhoging van moleculaire bewegingen dit mechanisme en wordt de geleidbaarheid aanzienlijk hoger.
Gedetailleerd IR-spectroscopieonderzoek toegestaan, wat het schema van LiClO4 . suggereert interactie met polymeerketens, namelijk de mogelijke ion-dipool interacties van Li + ion met de etherbinding van polyethyleenoxidefragment en OH-groep van de beschreven epoxyring van DEG-1, met secundaire aminegroep of tertiaire aminegroep van PEPA en etherbinding tegelijkertijd.
De resultaten van morfologische en structurele studies door middel van optische en elektronenmicroscopen evenals door elementanalyse hebben de aanwezigheid van insluitsels met afmetingen van nanometers tot ~20 μm, waarschijnlijk van anorganische aard, verdeeld in de polymeermatrix aan het licht gebracht.
Afkortingen
- DEG-1:
-
Epoxy-oligomeer van diglycide alifatische ester van polyethyleenglycol
- DSC:
-
Differentiële scanningcalorimetrie
- IR:
-
Infrarood
- LiClO4 :
-
Lithiumperchloraatzout
- PEO:
-
Polyethyleenoxide
- PEPA:
-
Polyethyleen polyamine
- ROM:
-
Reflecterende optische microscopie
- SEM:
-
Scanning elektronenmicroscopie
- SPE:
-
Vaste polymeerelektrolyten
- T g :
-
Glasovergangstemperatuur
- TOM:
-
Transmissie optische microscopie
- WAXS:
-
Groothoek röntgenspectroscopie
Nanomaterialen
- De eigenschappen van hars- en vezelcomposieten en waarom ze nuttig zijn
- De geschiedenis van epoxyhars
- Houtbewerking en epoxyhars
- Epoxyhars als hobby
- Maak indruk op vrienden en familie met epoxyharsprojecten
- Nano- en batterijanode:een recensie
- PES-additief verhoogt de weerstand tegen breuk en microscheurtjes in epoxycomposieten
- Sino Polymer ontwikkelt hoogwaardige prepreg van epoxyhars
- Structurele epoxyhars T26 (EP-UD-tape)
- Structurele epoxyhars T26 (EP-PCF)
- Structurele epoxyhars T26 (EP-CF)



