Het effect van sulfaatanionen op de ultrafijne Titania-kiemvorming
Abstract
Het fenomenologische model van het effect van sulfaatanionen op de nanogedispergeerde titaniasynthese tijdens hydrolyse van titaniumtetrachloride werd bestudeerd. Er werd voorgesteld dat zowel chelerende als overbruggende bidentaatcomplexen vormen tussen sulfaatanionen en octaëdrisch gecoördineerde [Ti(OH)h (OH2 )6−u ] (4−u)+ mononers is de bepalende factor voor nucleatie in de anatasefase.
Achtergrond
Ultrafijne TiO2 heeft een breed scala aan veelbelovende toepassingen op veel verschillende gebieden - van het milieugerichte fotokatalytische systeem, zoals de afbraak van gevaarlijke organische verbindingen [1], afvalwaterzuivering [2], directe ontleding van NO x , SO x en luchtzuivering [3] tot nieuwe industriegebieden:sensormaterialen [4] en zonnecellen [5]. Fasesamenstelling, deeltjesgrootte en oppervlaktetoestand zijn de belangrijkste kenmerken die de katalytische reactiviteit, lichtgevoeligheid en adsorptie-eigenschappen van TiO2 bepalen . De afname van de deeltjesgrootte van titania leidt bijvoorbeeld tot een snelle toename van de katalytische activiteit [6]. Tegelijkertijd zijn de fotokatalytische eigenschappen van titania erg gevoelig voor de fasesamenstelling van TiO2 polymorfen zoals anatase, brookiet en rutiel [7].
De keuze van de titania-synthesemethode met de controle van de fysische en chemische parameters zijn van cruciaal belang determinanten van de resulterende composities. De bereiding van TiO2 . op nanoschaal is mogelijk door sol-gel [8], chemische precipitatie [9], micro-emulsie [8] en hydrothermische [10] methoden. De sol-gel-methode is de meest flexibele techniek voor de bereiding van oxide op nanoschaal. De variaties van primaire voorlopertypen, hydrolyseomstandigheden, temperatuur en pH van het reactiemedium maken de controle van de nucleatie en groei van nanodeeltjes mogelijk. De verkregen sol-gelmethode van titaniumoxide is typisch gebaseerd op de reacties van titaniumalkoxiden Ti(OR)n hydrolyse. De verandering van deze dure chemicaliën naar de goedkopere voorloper zoals TiCl4 is veelbelovend voor een grootschalige productie van TiO2 . op nanoschaal . Een veelbelovend voordeel van TiCl4 toepassing is de mogelijkheid van polycondensatiereacties die worden gecontroleerd door additieve ionen met behulp van de voorspelde kiemvorming van de gespecificeerde fase van titania.
Het doel van dit artikel was om de effecten van SO4 . te onderzoeken 2− anionen op de oligomeerpolycondensatie en oxidenetwerkvorming tijdens titaankiemvorming voor het sol-gelproces op basis van TiCl4 hydrolyse.
Methoden
Titaantetrachloride TiCl4 (Merck, 99,9%; soortelijke dichtheid 1,73 g/cm 3 bij 20°C) werd afgekoeld tot 0°C en zoutzuur (36,0% waterige oplossing) werd toegevoegd onder verdere verdamping van waterstofchloride. De TiCl4 tot zoutzuurverhouding was 2:1. Een waterige oplossing van natriumkoolwaterstof werd druppelsgewijs toegevoegd aan de sol van titaniumoxychloride TiOCl2 om onder krachtig roeren een pH van 5,0-5,5 te krijgen. Gelvorming werd waargenomen tijdens alle pH-verhogende processen. De suspensie van nanodeeltjes werd 3 uur op 80 °C gehouden en daarna gewassen met gedestilleerd water om Na + te verwijderen. en Cl − ionen. Neergeslagen TiO2 werd gedroogd bij 150°C en de verkregen xerogel werd gemarkeerd als S1. Het S2-materiaalsyntheseproces werd op dezelfde manier uitgevoerd, maar kristallijn gedroogd Na2 SO4 werd direct toegevoegd aan titaniumtetrachloride op het podium van TiCl4 hydrolyse.
Diffractiepatronen werden verkregen met de diffractometer DRON-4-07 uitgerust met een röntgenbuis BSV28 (Cu Kα straling, 40 kV, 30 mA), een Bragg-Brentano-geometrietype en een Ni Kβ -filter. Er is een kwalitatieve analyse uitgevoerd met behulp van ICSD-structuurmodellen. De structurele modellen voor anatase en rutiel waren gebaseerd op respectievelijk de ICSD #92363 en ICSD #24780. Koperpoeder gegloeid in vacuüm (850-900 ° C gedurende 4 uur) met een gemiddelde korrelgrootte van ongeveer 50 μm werd gebruikt als referentiemonster om instrumentele piekverbreding te bepalen. De volledige breedte bij half maximum (FWHM) voor een diffractiepiek van dit referentiemonster bij de 2θ = 43,38° was 0,129°; daarom maakte het het mogelijk om anatase- en brookietfasen te onderscheiden. De grootte van de coherent verstrooiende domeinen werd berekend met de Scherrer-vergelijking:\( D=\frac{K\lambda}{\beta cos\theta} \), met K is de constante van Scherrer (K = 0.9), λ is de golflengte (0,154 nm), β de FWHM (in radialen), en θ is de piek hoekpositie. We gebruikten de combinatie van Gauss en Cauchy (gedomineerde) functies als profielvorm.
Infraroodspectra werden opgenomen met de Thermo-Nicolet Nexus 670 FTIR-spectrometer in de 4000-400 cm −1 regio. De TiO2 /KBr-mengsel werd na vibrerend malen tot korrels geperst en gemeten in de transmissiemodus.
De morfologie van monsterpoeders werd bestudeerd door transmissie-elektronenmicroscopie (TEM) met een 100 kV-microscoop JEOL JEM-100CX II. Het microscopisch kleine koperen rooster bedekt met een dunne transparante koolstoffilm werd gebruikt als specimendrager voor TEM-onderzoeken.
Resultaten en discussie
De aanwezigheid van natriumsulfaat in het reactiemedium had een significante invloed op de fasesamenstelling van de verkregen materialen (Fig. 1). Het materiaal gesynthetiseerd in afwezigheid van Na2 SO4 additief (S1) was een mengsel van anatase en rutiel met de relatieve fase-inhoud van respectievelijk 65 ± 4 en 35 ± 5 gew.%. De gemiddelde grootte van de coherent verstrooiende domeinen (CSD) was ongeveer 14 nm voor anatase en 9 nm voor rutiel, dus beide fasen zijn goed gekristalliseerd. Ondertussen bevindt het deel van het materiaal zich dicht bij de amorfe toestand, zoals de aanwezigheid van de halo op het XRD-patroon voor 2θ = 16–32 o Is voor de hand liggend. Volgens de synthesevoorwaarden is het onwaarschijnlijk dat de vorming van een niet-titaniafase plaatsvindt. Hierdoor bestaat het materiaal uit gescheiden gebieden met verschillende kristalliniteitsgraden. Het specifieke oppervlak van het S1-monster was ongeveer 152 m 2 g −1 . Het materiaal S2 was dicht bij amorf ultrafijn titania met duidelijke structurele kenmerken van anatase. Het halo op XRD-patroon wordt in dit geval ook waargenomen, maar het is relatief versmald en verschoven naar grotere 2θ-waarden. De gemiddelde grootte van CSD was ongeveer 4-5 nm (de analyse wordt gecompliceerd door de lage kristalliniteit van het materiaal). Het specifieke oppervlak voor S2-monster is vergroot tot 328 m 2 g −1 .
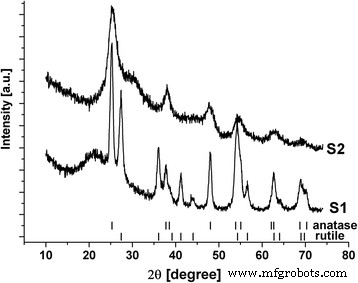
XRD-patronen van S1- en S2-materialen
TEM-afbeeldingen van S1-monster (Fig. 2a) laten geen duidelijke conclusies toe over de morfologie ervan, maar de waargenomen agglomeraten bestonden uit de lamellaire-achtige primaire deeltjes met de grootte van 10-15 nm. Verder is er geen bewijs van kristallijne gebiedsgrenzen (figuur 2b). Het S2-monster had een belachtige morfologie van de agglomeraten (figuur 2c, d). HR TEM vertoonde een hoge kristalliniteit van sommige korrels van dit materiaal (figuur 3) met de interplanaire afstanden van 0,34-0,37 nm. De verkregen interplanaire afstand komt overeen met het (101) vlak van anatase (0,352 nm). Dit geeft aan dat de groeirichting van CSD (kristallieten) die de voorkeur heeft, de [010]-kristallografie-as is. Dit resultaat leidde tot de conclusie dat de anataas-nanokristallen met geoxygeneerde oppervlakken facetten hebben ontwikkeld in de 010〉-richting [11].

TEM-afbeeldingen van de monsters S1 (a , b ) en S2 (c , d )

HR TEM-afbeeldingen van S2-materiaal met de randen van {101} vliegtuigen
Meer informatie over gesynthetiseerde materialen werd verkregen door FTIR-spectroscopie. Het brede absorptiegebied rond 3400 cm −1 geeft de aanwezigheid aan van chemisch gesorbeerde OH-groepen op het oppervlak van titaniadeeltjes (ν-OH-modi) (Fig. 4) [12]. De verschuiving van de ν-OH-banden van typisch 3700-3600 naar ongeveer 3400 cm −1 kan worden veroorzaakt door de aanwezigheid van waterstofbruggen [13]. De band rond 1600 cm −1 toont de aanwezigheid van moleculair geadsorbeerd water aan (δ-H2 O-standen) [14]. De hogere kristalliniteitsgraad voor S1-monsters veroorzaakt de vorming van relatief meer verschillende absorptiebanden in het titania-karakteristieke gebied (400-700 cm −1 ) [15].
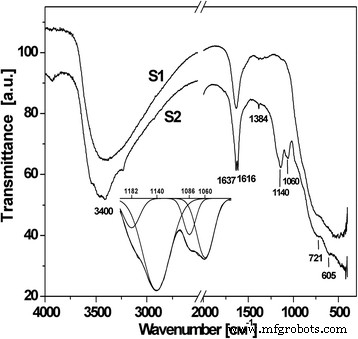
FTIR-spectra van S1- en S2-materialen
De extra absorptieband op de FTIR-patronen voor S2-materialen op 1139 en 1060 cm −1 komt overeen met chemisch gesorbeerd SO4 2− ionen [16]. Een scherpe band met lage intensiteit 1384 cm −1 is typerend voor de metaaloxiden die zijn gemodificeerd door sulfaationenbanden en toegewezen aan de S=O-strekfrequentie. Ondertussen is S=O–H-coördinatie onwaarschijnlijk omdat de absorptieband zal verschuiven in het laagfrequente gebied tot 1325 cm −1 in dit geval. Er zijn twee verschillende varianten van SO4 2− immobilisatie op het titania-oppervlak - een chelerende vorming van een tweetandig complex met coördinatie tot één metaalion door twee zuurstofatomen of een gebrugde vorming van een tweetandig complex met behulp van binding door twee metaalionen; beide complexen behoren tot de C2v-puntgroep. Overbrugd tweetand SO4 2− anionen gecoördineerd met Ti 4+ hebben karakteristieke rekfrequenties in de 930–1200 cm −1 bereik en grote absorptiepiek bij 1148 cm −1 wordt toegeschreven aan asymmetrische rektrillingen [17]. De banden in de 1300–900 cm −1 regio werden waargenomen voor SO4 2− /TiO2 systeem, en de pieken op 1217, 1134, 1044 en 980 cm −1 werden in [18] geïdentificeerd als karakteristieke frequenties van een tweetandige brug SO4 2− afgestemd op metalen. Volgens [19] heeft een gebrugd tweetandig complex vier absorptiebanden bij 1195-1160, 1110-1105, 1035-1030 en 990-960 cm −1 , die zijn toegewezen aan de asymmetrische en symmetrische rekfrequenties van de S=O- en S-O-bindingen.
De conclusie over energetische gunstigheid van chelerende complexvorming waarbij SO4 2− anionen worden gecoördineerd tot Ti-atomen door middel van twee zuurstof werd gemaakt op basis van gesulfateerd titania-onderzoek met behulp van DFT-berekening [20]. De vorming van een chelaatsulfaatcomplex komt overeen met de skeletale FTIR-band bij 1201 cm −1 [21] aangezien chelerend bidentaatcomplex vier banden heeft op 1240-1230, 1125-1090, 1035-995 en 960-940 cm −1 die zijn toegewezen aan de asymmetrische en symmetrische rekfrequenties van S=O- en S-O-banden [19].
Deconvolutie van de 1200–1000 cm −1 gebied van S2-materiaal FTIR-spectra onthulden de aanwezigheid van vier banden op 1182, 1140, 1086 en 1060 cm −1 . De absorptieband bij 1086 cm −1 ligt vrij dicht bij die van het chelerende bidentaatcomplex. Twee banden van chelerende en overbruggende bidentaatcomplexen overlappen elkaar, dus band op 1182 cm −1 kan overeenkomen met beide typen complexen. De banden op 1060 en 1140 cm −1 impliceren dat een gebrugd bidentaatcomplex wordt gevormd op het oppervlak van het S2-monster.
We kunnen het volgende model van SO4 . voorstellen 2− impact op titania-kiemvorming in het stadium van olatie-interactie tussen primaire hydrocomplexen, rekening houdend met de resultaten getoond in [22]. De hydrolyse van TiCl4 leidt tot [Ti(OH2 )6 ] 4+ formatie waar Ti 4+ ionen bevinden zich in de octaëdrische coördinatie met de volgende transformatie naar [Ti(OH)h (OH2 )6−u ] (4−u)+ monomeren als gevolg van deprotonering. De hydrolyseverhouding h is een functie van de pH en wordt bepaald door de partiële ladingstheorie [23]. In deze monomeren is OH − groepen hebben thermodynamische voordelen van de locatie in de octaëder equatoriale vlakken, en H2 O-moleculen nemen voornamelijk de "vertex" -positie in [24]. De producten van hydrolyse zijn [Ti(OH)(OH2 )5 ] 3+ en [Ti(OH)2 (OH2 )4 ] 2+ monomeren wanneer de pH van het reactiemedium dicht bij 1 ligt. Bij pH = 3, de [Ti(OH)2 (OH2 )4 ] 2+ en [Ti(OH)3 (OH2 )3 ] + complexen bestaan naast elkaar in oplossing. Bij pH = 4 leidt de hydrolyse tot de vorming van de [Ti(OH)3 (OH2 )3 ] + complexen, en in het bereik van pH = 6–8, de [Ti(OH)4 (OH2 )2 ] 0 monomeren worden gevormd. De mogelijkheid van de vorming van titania-polymorfen wordt bepaald door de ruimtelijke organisatie van [Ti(OH)h (OH2 )6−u ] (4−u)+ primaire monomeren. [Ti(OH)4 (OH2 )2 ] 0 monomeren (waarin OH-groepen octaëder equatoriale vlakken bezetten en H2 O-moleculen bevinden zich in de hoekpunten) in neutrale of alkalische media [20, 25]. Dimeren worden gevormd als gevolg van een olatiereactie tussen twee primaire monomeren waarvoor de octaëdercoördinatie een gemeenschappelijke rand heeft buiten het equatoriale vlak van de octaëder. Na verdere polycondensatie, de zigzag-achtige of spiraalvormige ketting van [Tin (OH)4n (OH2 )2 ] 0 er worden veelvlakken gevormd en de voorwaarden voor de nucleatie in de anatasefase worden gecreëerd. De [Timn Omn (OH)2mn (OH2 )2m ] 0 polymeer wordt gevormd als gevolg van m lineaire structuren van [Tin (OH)4n (OH2 )2 ] 0 olatie interactie. De nucleatie van de anatasefase is het resultaat van octaëdrische fusie door laterale vlakken van vlakken [26]. Tegelijkertijd interageren de hydroniumionen van het reactiemedium met hydroxylgroepen in het equatoriale octaëdervlak. Als de hydroniumionconcentratie in het reactiemedium toeneemt, [Ti(OH)h (OH2 )6−u ] (4−u)+ monomeren vormen zich onder h < 2 voorwaarde. Olation-interactie daartussen leidt tot de vorming van polymeerketens waarbij monomeren zijn verbonden door gezamenlijke randen in equatoriale octaëders, waardoor de voorwaarde voor nucleatie in de rutielfase wordt gedefinieerd [25].
De aanwezigheid van SO4 2− ionen in het reactiemedium bij een pH van ongeveer 5,5 veroorzaken zowel Ti(SO4 )(OH)2 (H2 O)2 chelaatvormer en Ti2 (SO4 )(OH)6 (OH2 )2 overbruggende vorming van bidentate complexen (Fig. 5). Er zijn twee verschillende routes van olatie-interactie tussen deze complexen. Twee monomeren verbinden zich met elkaar of door het delen van apicale randen (invloed van chelerende complexen) of in equatoriaal vlak (invloed van overbruggende tweetandige complexen) met het dehydrateren van watermolecuul. In de volgende fase vindt in beide gevallen de vorming van scheve zigzag-achtige tetranucleaire titaniumcomplexen plaats met dehydratatie van twee watermoleculen en begint de nucleatie van de anataasstructuur.
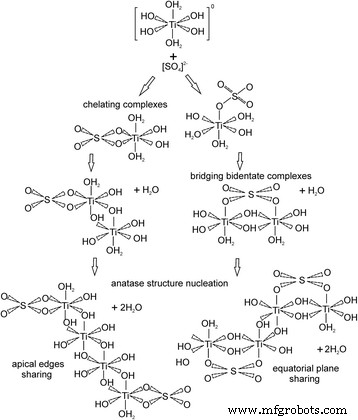
Voorgestelde mechanismen van nucleatie in de anatasefase met de vorming van chelerend en overbruggend bidentaat SO4 2− complexen
Conclusies
Het effect van SO4 2− anionen op de titaankiemvorming tijdens hydrolyse van titaantetrachloride werden bestudeerd. We concludeerden dat het kiemvormingsproces voornamelijk wordt gecontroleerd door de pH van het reactiemedium en SO4 2− anion aanwezigheid. Sulfaatanionen vormen beide chelerende Ti(SO4 )(OH)2 (H2 O)2 en overbruggende tweetand Ti2 (SO4 )(OH)6 (OH2 )2 complexen in het stadium van titaantetrachloridehydrolyse. We stelden het model voor met twee routes van olatie-interactie tussen titaniumsulfaatcomplexen wanneer SO4 2- liganden stimuleren de vorming van schroefpolymeerketens en de nucleatie van TiO2 anataasfase.
Nanomaterialen
- De Pentode
- Wat is het huideffect?
- De geschiedenis van NASCAR:hoe het allemaal begon
- Het verleden, het heden en de toekomst van LPWAN
- Onderwaterdrone:het verhaal van de waanzin
- De 10-seconden maatregel voor de effectiviteit van onderhoud
- Onderhoud Wereldwonderen:CN Tower Onderhoud
- Het geval van een luidruchtige versnellingsbak
- Het echte internet der dingen?
- Geautomatiseerd vanaf het begin
- De geschiedenis van robotica in de maakindustrie



