Polyaniline Nanoskein:synthetische methode, karakterisering en Redox-detectie
Abstract
Polyaniline nanoskein (PANS), die polyaniline nanovezels hebben, werd ontwikkeld. PANS werd geformuleerd via opeenvolgende extractie-, verwarmings- en zwelprocessen. De samenstellingen van PANS zijn geanalyseerd met behulp van röntgenfoto-elektronspectroscopie, Fourier-transformatie-infraroodspectroscopie, thermogravimetrische analyse en Brunauer-Emmett-Teller-analyse, en de resultaten hiervan geven aan dat PANS uitsluitend uit organische materialen bestaat. Bovendien heeft PANS converteerbare absorptiekenmerken getoond volgens de omringende zure omgevingen, en met behulp van deze kenmerken wordt de mogelijkheid van PANS voor het waarnemen van omringende redoxtoestandsveranderingen gepresenteerd.
Inleiding
Bloemvormige anorganische structuren zijn gebruikt voor verschillende toepassingen zoals katalyse [1, 2], biosensoren [3, 4] en theragnostische middelen [5]. Er zijn enkele synthetische strategieën voor het genereren van deze complexe structuren. De synthese met behulp van sjabloon is de eerste benadering, liposoom is bijvoorbeeld gebruikt als een zachte sjabloon om de vorming van dendritische Pt-vellen te begeleiden [6, 7]. De tweede benadering is gebaseerd op het fenomeen van georiënteerde aanhechting van primaire nanodeeltjes wanneer oppervlakken met vergelijkbare atomaire rangschikkingen elkaar naderen. De synthese van dendritische PtRu-nanodeeltjes vormt gefacetteerde PtRu-primaire nanodeeltjes, die op dit principe was gebaseerd [8]. De derde benadering is gebaseerd op het gebruik van specifieke afdekmiddelen of oppervlakteactieve stoffen om anisotrope groei van anorganische materialen te induceren. De syntheses van Pt- en Au-multipods in aanwezigheid van poly(vinylpyrrolidon) of cetyltrimethylammoniumbromide zijn zulke voorbeelden [9, 10]. Bovendien, na de eerste benadering van Ge et al. [2] zijn organisch-anorganische hybride bloemvormige structuren intensief bestudeerd. In het proces van synthese voor hybride bloemvormige structuren, de combinaties van verschillende eiwitten (bijv. enzymen [11] en DNA [12]) en metaalionen (bijv. Cu [13], Ca [14, 15] en Mn [16]) zijn gebruikt. De afgelopen jaren waren er studies dat de synthese van bloemvormige structuren was gebaseerd op polyaniline (PAni) met behulp van sterk zure doping [17] en polyurethaan nanovezel [18]. Daarnaast waren er verschillende rapporten over bloemvormige structuren samengesteld uit organische materialen, zoals stikstof-gedoteerde koolstofmaterialen [19, 20] en polyacrylonitril [21].
In deze studie rapporteren we een methode voor het formuleren van organische bloemvormige structuren, die voornamelijk bestaat uit PAni, en zijn materiaaleigenschappen. PAni, een representatief geleidend polymeer, werd in deze studie als een organische component gebruikt. PAni staat bekend om zijn converteerbare optische eigenschappen vanwege zijn unieke doping-/dedoping- of oxidatie-/reductieprocessen [22]. Met behulp van dit fenomeen heeft onze onderzoeksgroep gerapporteerd dat PAni-gemedieerde nanostructuren kunnen worden gebruikt als fotothermische middelen [23] en redox-detectiesondes [24, 25] voor biomedische toepassingen. In het bijzonder kan de elektronische bandgap voor PAni worden gecontroleerd door doping/dedoping-toestanden [26]. Het verschil tussen doping- en dedopingtoestanden beïnvloedt veranderingen van optische spectra van PAni in het zichtbare bereik [24]. Deze doterings- en dedoperingstoestanden van PAni kunnen worden aangepast door verschillende doteermiddelen, zoals sterke zuren, Lewis-zuren, overgangsmetalen en alkali-ionen [23].
We noemden bloemvormige PAni-deeltjes als PAni nanoskein (PANS) omdat de vorm van PANS lijkt op een bol garen, die is samengesteld uit PAni-nanovezels. Bovendien lijkt gesynthetiseerde PAni intrinsiek een fibrillaire en lineaire moleculaire structuur zoals draad te vormen. PANS werd gesynthetiseerd toen we benzylether (BE) toevoegden aan N-methyl-2-pyrrolidon (NMP) -oplossing die PAni bevat, en dit mengsel werd door verwarmings- en zuiveringsprocessen geleid (figuur 1a). En vervolgens werden veranderingen van omringende redoxtoestanden gemeten op basis van kleurverandering van PANS, waarbij optische eigenschappen werden omgezet (figuur 1b). Veel eerder gepubliceerde rapporten hebben echter glucose gedetecteerd met behulp van fluorescentieratiometrische methoden via verschillende detectiemechanismen [27,28,29]. Voor zover wij weten, waren up-to-date onderzoeken voor de detectie van glucose met behulp van converteerbare optische eigenschappen van PAni ontoereikend.
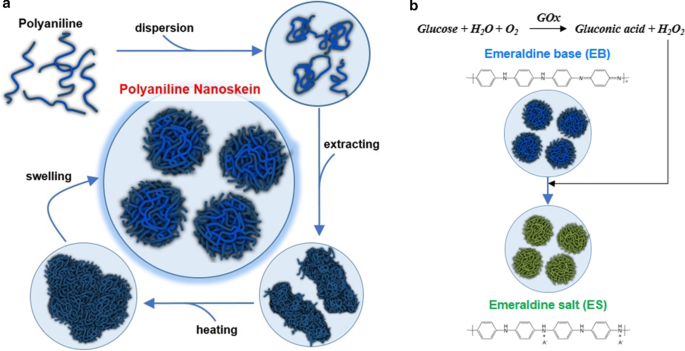
een Het synthetische proces van polyaniline nanoskein (PANS). b Glucosedetectieproces met PANS
Materialen en methoden
Materialen
Polyaniline (PAni) Mw ~ 5000, benzylether (BE), glucose-oxidase (GOx, van Aspergillus Niger, 145.200 eenheden/g) en D-( +)-glucose werden gekocht bij Sigma-Aldrich (St. Louis, MO, VS). N-methyl-2-pyrrolidon (NMP) en ethanol (EtOH) werden gekocht bij Dae-jung, Korea. Dulbecco's fosfaatgebufferde zoutoplossing (DPBS) werd gekocht bij Welgene, Korea, en bufferoplossing (pH 4) werd gekocht bij Samchun, Korea. Alle andere chemicaliën en reagentia waren van analytische kwaliteit. Voor alle synthetische processen werd ultrapuur gedeïoniseerd water (DW) gebruikt.
Synthese van Polyaniline Nanoskein (PANS)
Het syntheseproces van het onberispelijke product was als volgt:PAni (250 mg) werd opgelost in NMP (20 ml) en vervolgens werd BE (40 ml) toegevoegd. Het mengsel werd 1 uur voorverwarmd tot 200°C en 30 minuten verwarmd tot 300°C. De reactant werd 3 uur op kamertemperatuur afgekoeld. De resulterende oplossing werd gewassen met EtOH en het neerslagmiddel afgescheiden door 10 minuten te centrifugeren bij 3000 rpm. Vervolgens werd de oplossing opnieuw gedispergeerd in EtOH. Vervolgens werd de in EtOH opgeloste oplossing 24 uur gedialyseerd met behulp van dialysemembraan (MWCO:3.500 Spectra / Por® 6, SPECTRUM® LABORATORIES, Rancho Dominguez, CA, VS). Na dialyse werd de oplossing gedurende 30 minuten bij 15.000 rpm gecentrifugeerd. Het neerslagmiddel werd opnieuw opgelost in 30 ml DW. De uiteindelijke PANS-concentratie werd berekend als 8,33 mg/ml.
Karakterisering van PANS
De morfologie van PANS werd geëvalueerd met transmissie-elektronenmicroscopische (TEM, JEM-1011, JEOL Ltd, Japan) en scanning-elektronenmicroscopische (SEM, JSM-6701F, JEOL Ltd, Japan) beeldvorming. Röntgenfoto-elektronenspectra werden opgenomen met behulp van een K-alpha-systeem (Thermo Fisher Scientific, Waltham, MA, VS). Fourier-transformatie infraroodspectra (FT-IR Spectrum Two, PerkinElmer, Waltham, MA, VS) analyse werd uitgevoerd om de karakteristieke banden van de gesynthetiseerde PANS te bevestigen, en de grootteverdeling van de PANS werd geanalyseerd door een dynamische lichtverstrooiing (ELS-Z , Otsuka electronics, Japan) methode. Verder werden het oppervlak en het porievolume van PANS gemeten met een Brunauer-Emmett-Teller-analysator (Autosorb-iQ 2ST/MP, Quantachrome Instruments, Boyton Beach, FL, VS), en werd de gewichtshoeveelheid van PANS geanalyseerd met een thermogravimetrische analysator (SDT-Q600, TA-instrument, New Castle, DE, VS). Bovendien werd de absorptie van PANS geanalyseerd met behulp van een UV-Vis-spectrofotometer (Optizen 2120UV, MECASYS Co., Korea).
Glucosedetectie met PANS
Allereerst werd de concentratie van GOx aangepast tot 15 mg / ml met behulp van DPBS en werd glucose verdund met pH 4-bufferoplossing. De resulterende glucoseconcentraties werden respectievelijk ingesteld op 40, 20, 10, 5 en 1 mg/ml. En vervolgens werd 1 ml PANS (1,67 mg/ml) gemengd met 20 L GOx (15 mg/ml) en 80 μL glucose (respectievelijk 40, 20, 10, 5 en 1 mg/ml). De uiteindelijke glucoseconcentraties in gemengde oplossingen werden berekend als respectievelijk 2,91, 1,45, 0,73, 0,36 en 0,07 mg/ml. De absorptie van PANS met GOx en glucose werd geanalyseerd met behulp van de UV-Vis-spectrofotometer.
Resultaten en discussie
De morfologie van PANS werd bevestigd door transmissie-elektronenmicroscopische (TEM) en scanning-elektronenmicroscopische (SEM) afbeeldingen zoals weergegeven in figuur 2. PANS vertoonde een bolvorm met hiërarchische structuren. In het syntheseproces van PANS werd PAni eerst opgelost in NMP en vervolgens werd BE toegevoegd aan de PAni/NMP-oplossing. Vanwege het oplosbaarheidsverschil voor PAni tussen NMP en BE, werd PAni in het mengsel geëxtraheerd, dus dit proces werd het 'extractieproces' genoemd. nabijheid tussen PAni-moleculen (de eerste rij in Fig. 2 en zie ook Aanvullend bestand 1:Fig. S1). Daarna werd het mengsel achtereenvolgens een uur verwarmd op 200 °C en 30 minuten op 300 °C ('opwarmproces'). Het NMP heeft een kookpunt van ongeveer 203 °C, dus PAni bestond in BE na het verhittingsproces. Na het verhittingsproces was PAni meer genucleëerd dan in het extractieproces, en de vorm van PANS werd rondachtig. Bovendien begon het oppervlak van PANS te rimpelen, maar veel PANS-deeltjes waren geaggregeerd (de tweede rij in Fig. 2 en zie ook Aanvullend bestand 1:Fig. S1). Vervolgens werd PANS zowel gewassen als opgezwollen met ethanol (EtOH) (de derde rij in Fig. 2 en zie ook Aanvullend bestand 1:Fig. S1). Na het zwelproces zou EtOH tussen PAni-moleculen worden ingevoegd, dus de intermoleculaire afstand zou ook worden vergroot. Dienovereenkomstig bestond PANS op afzonderlijke deeltjes en had het ook een hiërarchische structuur. Om de ideale conditie van formulering van PNAS te bevestigen, werd de concentratie van PAni ook gecontroleerd (aanvullend bestand 1:Fig. S2). TEM-beeldanalyse volgens de voedingshoeveelheid PAni bij elk synthetisch proces (dwz extractie-, verwarmings- en zwelproces) werd ook uitgevoerd, en naarmate de voedingshoeveelheid PAni werd verlaagd (van 50,0 mg/ml naar 12,5 mg/ml), PANS was veel schaarser geformuleerd. Bovendien werd de hiërarchische structuur van PANS zeker bevestigd via een 90 ° gekanteld SEM-beeld bij een voedingshoeveelheid PAni van 50 mg / ml (aanvullend bestand 1:Fig. S3). Voor de gedetailleerde studies van het formuleren van het mechanisme van PANS, werd bij voorkeur een oplosbaarheidstest van PAni uitgevoerd (aanvullend bestand 1:Fig. S4). PAni stond bekend als hydrofoob en werd opgelost in een met water mengbaar polair aprotisch oplosmiddel zoals NMP [24]. De fibrillaire vorm van PAni werd waargenomen wanneer PAni werd opgelost in NMP. Aan de andere kant had PAni in BE en EtOH meer geaggregeerd en groter formaat dan in NMP; bovendien kan PAni in EtOH weinig interactie hebben met elke PAni-molecule. De oplosbaarheidstests van PAni met behulp van metingen van absorptiespectra werden ook uitgevoerd; EtOH bleek de beste oplosbaarheid onder de EtOH, BE en gedeïoniseerd water (DW). De kale PAni-moleculen losten nauwelijks op in DW. Bovendien werden experimenten met een andere conditie uitgevoerd volgens het molecuulgewicht (Mw) van PAni (aanvullend bestand 1:Fig. S5). In het geval van Mw 5 kDa vertoonden PANS meer strengachtige structuren dan andere omstandigheden (d.w.z. Mw 10 kDa en 50 kDa). In andere gevallen kiemde PAni niet zoals Mw 5 kDa, en dit fenomeen kan oplosbaarheidsverschillen zijn met NMP voor PAni. Met andere woorden, naarmate het Mw van PAni wordt verhoogd, heeft PAni de neiging onoplosbaar te zijn in NMP, en daardoor zou PAni geen PAni-nanovezels in NMP voorkomen. Als gevolg hiervan waren er niet voldoende PAni-nanovezels, dus strengachtige structuren van PANS zouden ook niet worden geformuleerd. Op basis van deze resultaten wordt de formulering van PANS als volgt verondersteld:(1) kale PAni lost helemaal niet op in DW; (2) PAni heeft de beste oplosbaarheid in NMP; (3) PAni in NMP werd geëxtraheerd door toevoeging van BE via oplosbaarheidsverschil; (4) het NMP werd verdampt door een verwarmingsproces uit PAni/(NMP en BE) mengsel; (5) de resulterende oplossing wordt gewassen met EtOH en de EtOH wordt tussen PAni-moleculen ingevoegd; (6) PANS-deeltjes zijn gezwollen en goed verspreid in DW.

Morfologie van PANS via transmissie-elektronenmicroscopische (TEM, links) en scanning elektronenmicroscopische (SEM, rechts) beeldvorming. Alfabetische tekens vertegenwoordigen opeenvolgende synthetische processen van PANS; (E):extraheren van de reactant met BE, (H):achtereenvolgens verhitten van de reactant op 200 °C en 300 °C, en (S):het opzwellen van de reactant met EtOH. Merk op dat (X):geen behandeling. Schaalbalken zijn 500 nm
Om de kenmerken van PANS te bestuderen, werd allereerst TEM (HRTEM) beeldvormingsanalyse met hoge resolutie uitgevoerd (figuur 3a). PANS had morfologie voor een bol garen, die was samengesteld uit vele PAni-nanovezels. Om de moleculaire structuur van PANS te verifiëren, werd röntgenfoto-elektronspectroscopische (XPS) analyse voor kale PAni (bPAni) en PANS uitgevoerd (Fig. 3b en zie ook Aanvullend bestand 1:Fig. S6). De spectra van het C1s-kernniveau kunnen worden gedeconvolueerd in vier pieken:C=O/C–O bij 286,7 eV (1), C=N + /C-Cl bij 285,8 eV (2), CN/C=N bij 285,0 eV ( 3) en C-C/C-H bij respectievelijk 284,4 eV (4). Deconvolutie van C1's was gebaseerd op gegevens die eerder werden gerapporteerd door Golczak et al. [30]. Met name de veranderingen in de verdelingen voor (3) en (4) waren opmerkelijk, en deze resultaten betekenen dat het stikstofaandeel in PANS was verhoogd. Dit fenomeen kan worden toegeschreven aan het bestaan van NMP in PANS-structuren, en dit NMP-molecuul beïnvloedt interacties tussen PAni-moleculen voor de formulering van PANS. Om de moleculaire structuur van PANS verder te onderzoeken, werden Fourier-transformatie-infraroodspectra (FTIR) voor bPAni en PANS ook geanalyseerd (Fig. 3c en zie ook Aanvullend bestand 1:Fig. S7). De pieken op 1290 cm −1 (aromatische C–N-strekking), 1490 cm −1 (C=C en C=N rekken van benzenoïde ring), en 1590 cm −1 (C=C en C=N rekken van chinoïde ring) werden in beide gevallen bevestigd voor bPAni en PANS. De specifieke pieken van PANS op 1670 cm −1 (sterretje in figuur 3c) kan worden toegeschreven aan tertiair amine in NMP, en deze piek werd ook waargenomen in het FTIR-spectrum van NMP (aanvullend bestand 1:figuur S7). Thermogravimetrische analyse (TGA) resultaten van bPAni en PANS onthullen dat PANS niet alleen uit PAni maar ook uit andere moleculen bestond (figuur 3d). De afbraak van bPAni werd waargenomen bij ongeveer 350 ° C; het afbraakpunt van PANS werd echter waargenomen bij ongeveer 200 ° C, wat samenvalt met het kookpunt van NMP. Van XPS tot TGA-resultaten, blijkt uit figuur 3b-d dat PANS niet alleen uit pure PAni bestond, maar ook uit PAni en andere organische verbindingen zoals NMP. Bovendien werden het oppervlak en het porievolume van PANS bepaald door Brunauer-Emmett-Teller (BET) analyse (Fig. 3e), en PANS had 9,486 ± 0,728 m 2 /g oppervlakte en 0,044 ± 0,004 cm 3 /g porievolume. (vgl. 6,358 ± 0,682 m 2 /g oppervlakte en 0,019 ± 0,001 cm 3 /g porievolume voor respectievelijk bPAni.) Deze resultaten betekenen dat PANS poreuzer is met een hoge oppervlakte-tot-volumeverhouding dan kale PAni. De verdeling van de hydrodynamische diameter van PANS vertoonde 799 ± 85 nm in een waterige oplossing (figuur 3f). Deze resultaten in figuur 3 laten zien dat PANS uitsluitend bestaat uit organische verbindingen (PAni en NMP) met hiërarchische structuren.
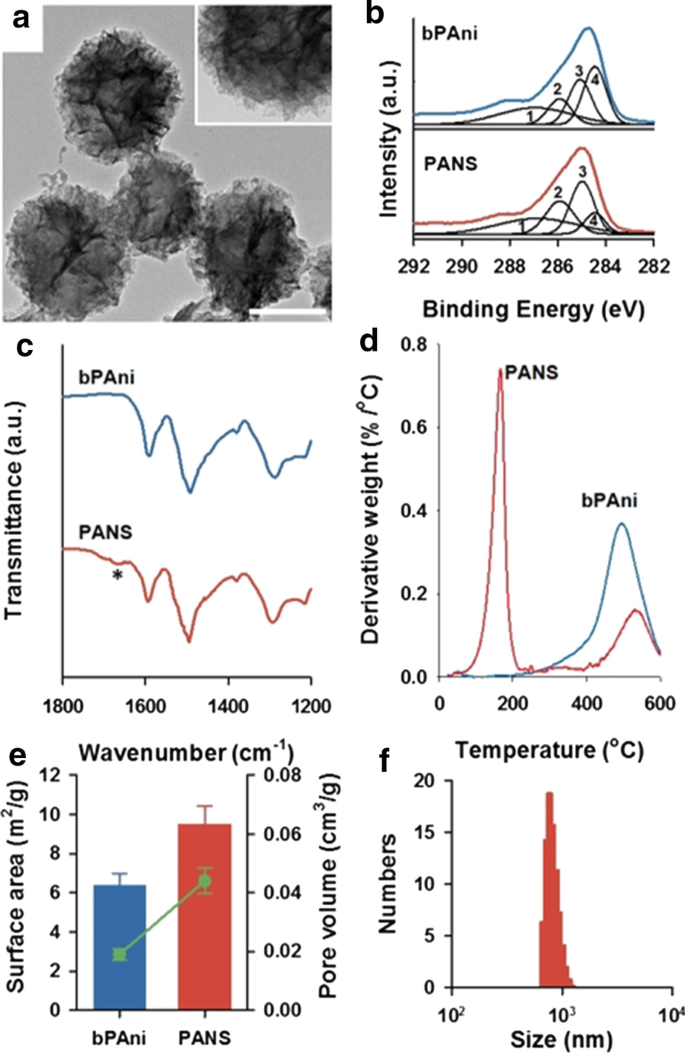
een Hoge resolutie transmissie-elektronenmicroscopische (HRTEM) beelden van PANS. De schaalbalk is 100 nm en de inzet is een afbeelding met een hoge vergroting. b XPS C1s-spectra van kale polyaniline (bPAni) (boven) en PANS (onder). 1:C=O/C–O, 2:C–N + /C=N + , 3:C–N/C = N, 4:C–C/C–H. c FTIR-spectra van bPAni (boven) en PANS (onder). Een asterisk vertegenwoordigt een interessante piek die in meer detail in de tekst wordt beschreven. d Thermogravimetrische analyse (TGA) van bPAni (boven) en PANS (onder). e Oppervlakte (bar) en porievolume (lijn en verstrooiing) van bPAni en PANS met behulp van Brunauer-Emmett-Teller (BET) -analyse. v Grootteverdeling van PANS via dynamische lichtverstrooiing (DLS)-methode
Om de mogelijkheid van PANS als converteerbare optische sondes te onderzoeken, werden kleurveranderingen van PANS geanalyseerd met behulp van absorptiespectra. De veranderingen van de absorptie-eigenschappen van PAni-structuren, zoals nanodeeltjes, films en vellen, staan erom bekend dat ze de doterings- / dedopingtoestanden variëren. De doterings-/dedoperingstoestanden van PAni kunnen worden aangepast door verschillende doteermiddelen, zoals sterke zuren, Lewis-zuren, overgangsmetalen en alkali-ionen [31, 32]. PANS vertoonde die eigenschappen ook volgens veranderingen van de omringende pH-waarden (Fig. 4). Bij lage pH-waarden (< pH 2) ging PANS over in een toestand van smaragdzout (ES, groene kleur), zoals aangegeven door de aanwezigheid van de π–π*-overgang van de benzenoïde ringen en polaronbandovergangen bij ongeveer 480 en 800-900 nm, respectievelijk [33]. Bij toenemende pH-waarden nemen de pieken bij 480 en 800-900 nm geleidelijk af in absorptie en wordt een sterke absorptiepiek bij ongeveer 680 nm waargenomen. De absorptiepiek bij 680 nm wordt toegeschreven aan excitatie van de hoogst bezette moleculaire orbitaal van het benzenoïde deel met drie ringen van de PAni naar de laagste onbezette moleculaire orbitaal van de gelokaliseerde chinoïdering en de twee omringende iminestikstoffen in de smaragdgroene base (EB) toestand van de PAni [34]. Om nauwkeuriger onderscheid te maken tussen de ES- en EB-toestand van PANS, wordt de absorptieverhouding (λ 680 /λ 480 ), werd berekend op representatieve golflengteposities van pieken bij respectievelijk EB- en ES-toestanden van PANS (figuur 4c). Toen de pH-waarde daalde van 10 naar 4, bleef de absorptieverhouding op bijna 1,06, en deze daalde dramatisch tot bijna 0,88 bij pH-waarden van 4 tot 1. Deze resultaten geven aan dat spectrale veranderingen van PANS kunnen worden gebruikt om de specifieke veranderingen van redox-toestand door veranderingen in de omgeving.
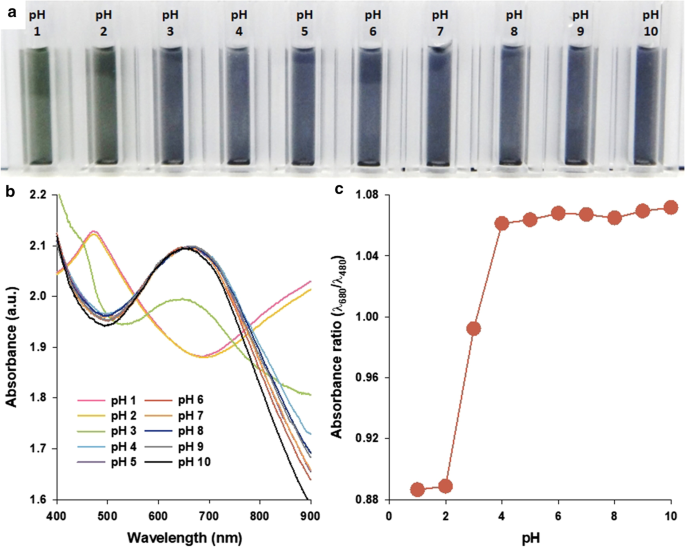
een Een foto, b absorptiespectra, en c absorptieverhouding voor representatieve golflengten voor EB (bij 680 nm) en ES (bij 480 nm) toestanden van PANS-oplossingen in aangegeven pH-omstandigheden
Om het detectievermogen van PANS voor specifieke veranderingen van de redoxtoestand van de veranderingen van de omringende omgevingen te onderzoeken, werden glucose en GOx geselecteerd als representatieve kandidaten. Bij het verhogen van de glucoseconcentraties van 0,00 tot 2,91 mg/ml, veranderde de kleur van PANS-oplossingen van blauw in groen (Fig. 5a). De absorptiespectra van PANS werden ook geanalyseerd (Fig. 5b), maar vormveranderingen in spectra waren minder dan die in experimenten met pH-veranderingen zoals getoond in Fig. 4. Dit fenomeen kan worden verklaard door de volgende vergelijkingen:
$${\text{Glucose}} + {\text{H}}_{2} {\text{O}} + {\text{O}}_{2} \mathop{\longrightarrow}\limits^{ {\text{GOx}}}{\text{Gluconic}}\,{\text{acid}} + {\text{H}}_{2} {\text{O}}_{2}$$ ( 1) $${\text{H}}_{2} {\text{O}}_{2} + {\text{PANS}}\,({\text{EB}}) \to 2{\ text{e}}^{ - } + {\text{O}}_{2} + {\text{PANS}}\,({\text{ES}})$$ (2)In verg. (1) wordt glucose geoxideerd door GOx, wat resulteert in gluconzuur en waterstofperoxide. Bovendien, zoals getoond in Vgl. (2), het resulterende waterstofperoxide wordt gereduceerd tot de PANS in EB-toestand tot ES-toestand. De waarden van de absorptieverhouding (λ 680 /λ 480 ) werden gevormd tussen 0,98 en 0,86, en dit resultaat geeft aan dat PANS bestond in een tussentoestand (λ 680 /λ 480 = 0.98) en ES-status (λ 680 /λ 480 =0,86), zoals weergegeven in figuur 5c. De reactie tussen glucose en GOx is een representatieve redoxreactie en deze reactie staat erom bekend waterstofperoxide te produceren, wat resulteert in waterstofionen en elektronen. Deze resultaten geven aan dat PANS kan worden gedoteerd met waterstofionen en elektronen. Dientengevolge wordt de π-π * -overgang van de benzenoïde ring waargenomen in absorptiespectra door de vorming van schouder bij 480 nm. Gezamenlijk geeft dit resultaat aan dat PANS kan worden gebruikt om enzymen zoals glucose te detecteren. Men denkt dat PANS ook kan worden gebruikt om de activiteit van andere enzymen te detecteren en om de redox-activiteit in het biologische systeem te bevestigen.
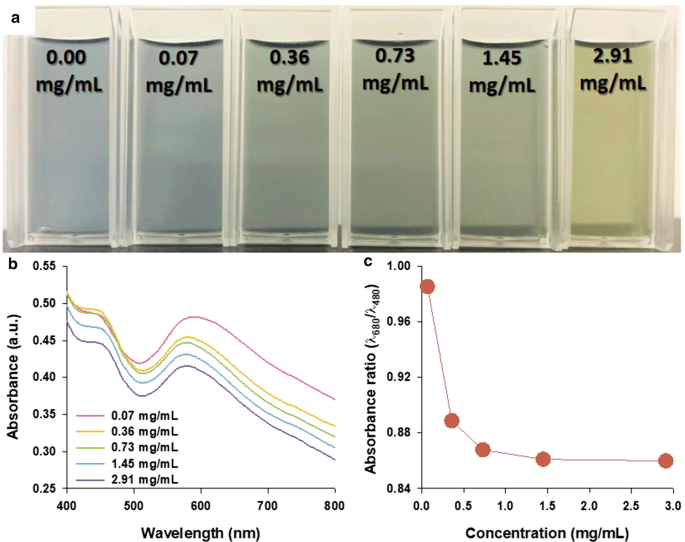
een Een foto, b absorptiespectra, en c absorptieverhouding voor representatieve golflengten voor EB (bij 680 nm) en ES (bij 480 nm) toestanden van PANS-oplossingen met aangegeven glucoseconcentraties
Conclusie
Samenvattend, de formulering van strengvormige PANS, die is samengesteld uit PAni-vezels, is bereikt en het formuleringsmechanisme is ook voorgesteld. Het synthetische proces van PANS omvat opeenvolgende extractie-, verwarmings- en zwelprocessen. De samenstellingen van PANS zijn geanalyseerd, die uitsluitend uit organische materialen bestaan. Bovendien werden de mogelijkheden van PANS als converteerbare optische sondes voor het waarnemen van veranderingen in de omringende redoxtoestanden bevestigd via de verandering van pH-waarden en combinatie van glucose en GOx. De huidige studie werpt licht op de synthese van nieuwe klasse van 3D-vormige nanostructuren en nanobiosensoren voor het waarnemen van omringende redoxtoestandsveranderingen.
Beschikbaarheid van gegevens en materialen
Alle gegevens die tijdens dit onderzoek zijn gegenereerd of geanalyseerd, zijn opgenomen in dit gepubliceerde artikel.
Nanomaterialen
- Mesh huidige methode en analyse
- C# abstracte klasse en methode
- C# Gedeeltelijke klasse en gedeeltelijke methode
- C# verzegelde klasse en methode
- Eenvoudige fabricage van multi-hiërarchische poreuze polyaniline-composiet als druksensor en gassensor met instelbare gevoeligheid
- Ontwerpen van nette en samengestelde koolstofnanobuisjes door middel van porosimetrische karakterisering
- Vervaardiging en karakterisering van nieuwe composiet Tio2 koolstof nanovezel anodische katalysatorondersteuning voor directe methanolbrandstofcel via elektrospinmethode
- Vervaardiging, karakterisering en biologische activiteit van avermectine nano-afgiftesystemen met verschillende deeltjesgroottes
- Recente ontwikkelingen in synthetische methoden en toepassingen van zilveren nanostructuren
- Vervaardiging en karakterisering van ZnO-nanoclips door het door polyol gemedieerde proces
- Dikte-afhankelijke magnetische en microgolfresonantiekarakterisering van gecombineerde FeCoBSi-films met streeppatroon



