Vormingsmechanisme van huid-kern chemische structuur binnen gestabiliseerde polyacrylonitrilmonofilamenten
Abstract
Hoewel het een halve eeuw geleden is dat op polyacrylonitril (PAN) gebaseerde koolstofvezels voor het eerst werden ontwikkeld, was het exacte vormingsmechanisme van de huid-kernstructuur van op PAN gebaseerde koolstofvezels, met name de gestabiliseerde PAN-vezels, nog steeds niet goed opgehelderd vanuit het gezichtspunt van de chemische structuur. Om deze bovengenoemde uitdaging aan te gaan, werd een krachtig hulpmiddel met een resolutie op nanoschaal genaamd foto-geïnduceerde krachtmicroscopie toegepast om de chemische groepsverdeling in de dwarsdoorsnede van gestabiliseerde PAN-vezels in kaart te brengen en het evolutiemechanisme van de huid-kernstructuur door de hele stabilisatie te onthullen werkwijze. De resultaten gaven aan dat de vorming van de huid-kernstructuur van gestabiliseerde PAN-vezel werd toegeschreven aan de complexe en overlappende chemische reacties veroorzaakt door de zuurstofgradiënt langs radiale richting en de vorming van een dichte kristallaag op het grensvlak tussen de huid en het kerndeel. Ten slotte werd de kristallaag vernietigd en hadden de monofilamenten de neiging om homogeen te zijn bij verdere oxidatie.
Inleiding
Op PAN gebaseerde koolstofvezel (CF) is een grensverleggend materiaal met een hoge treksterkte en Young's modulus, evenals een uitstekende hittebestendigheid. Vanwege zijn superieure eigenschappen is het breed toegepast als het versterkte structurele materiaal in de luchtvaart, ruimtevaart en andere nieuwe industriële gebieden [1,2,3]. Momenteel hebben de sterkste commercieel verkrijgbare koolstofvezels een treksterkte van ~ 7 GPa. Echter, op basis van –C–C bindingssterkteberekeningen met een ideaal grafietmodel, ligt de theoretische sterkte van koolstofvezels rond de 180 GPa [4]. De enorme kloof tussen echte en theoretische treksterkte wordt voornamelijk toegeschreven aan de heterogene huid-kernstructuur van koolstofvezel. Deze structurele heterogeniteit resulteert in een ongelijke spanningsverdeling binnen monofilament van koolstofvezel. Vernietiging vindt meestal plaats in het gebied, dat aan hogere stress lijdt, wat leidt tot het breken van koolstofvezel [5,6,7]. Daarom is het van groot belang om het vormingsmechanisme van dit structurele defect te achterhalen en het effect ervan op de eigenschappen van de resulterende koolstofvezels te minimaliseren.
De vervaardiging van koolstofvezels omvat drie stappen, waaronder het spinnen van PAN-precursoren, thermische stabilisatie en carbonisatie. Hiervan is thermische stabilisatie de meest complexe stap die reacties omvat zoals cyclisatie, dehydrogenering en oxidatie. Cyclisatiereactie leidt tot het genereren van gecycliseerde structuren en de omzetting van –C≡N naar –C=N. Dehydrogeneringsreactie wordt geassocieerd met de vorming van -C=C. Carbonylgroepen worden geïntroduceerd nadat de voorlopervezels een oxidatiereactie ondergaan [2, 8]. Het stabilisatieproces draagt bij aan de transformatie van lineaire PAN-ketens naar onsmeltbare en hittebestendige ladderstructuur, die nodig is voor het carbonisatieproces [9,10,11]. De bereiding van op PAN gebaseerde koolstofvezel is een continu proces, om het anders te zeggen, en de uiteindelijke heterogene huid-kernstructuur in koolstofvezel wordt voornamelijk geërfd van de gestabiliseerde PAN-vezel. Daarom is het onthullen van het vormingsmechanisme van de huid-kernstructuur van gestabiliseerd PAN-monofilament, met name de chemische structurele distributie, gunstig om de structurele heterogeniteit in koolstofvezel te minimaliseren.
Er zijn talloze onderzoeken gedaan naar de stabilisatie van PAN-vezels. Het onderzoek naar de huid-kernstructuur van gestabiliseerde PAN-vezels is echter zeer beperkt. Lv et al. [12] rapporteerde dat de heterogene zuurstofdiffusie van huid naar kern resulteert in de vorming van een dicht huidgebied, dat verdere diffusie van zuurstof vertraagt en leidt tot de vorming van huid-kernstructuur. Nunna et al. [13] gebruikte Raman-spectroscopie en elementanalyse om de huid-kernstructuur van gestabiliseerde vezels te onthullen. Deze elegante werken hebben in hoge mate bijgedragen aan de studie van de huid-kernstructuur van de gestabiliseerde PAN-vezels. Ze richten zich echter voornamelijk op de radiale mechanische eigenschap van stabiliserende PAN-vezels in plaats van op de chemische structuur, de gedetailleerde structurele informatie is nog steeds niet erg duidelijk. Daarom is apparatuur met een hoge ruimtelijke resolutie nodig voor de studie van de huid-kern chemische structuur van gestabiliseerde PAN-vezels in verschillende stadia van het stabilisatieproces.
In deze studie werd foto-geïnduceerde krachtmicroscopie (PiFM) toegepast om het vormingsmechanisme van de huid-kern chemische structuur in gestabiliseerde PAN-monofilamenten bij verschillende temperaturen te analyseren. Zoals weergegeven in Fig. 1 is PiFM een geavanceerde scanningsondemicroscopietechniek die een atomaire krachtmicroscopie (AFM) tip combineert met een afstembare infraroodlaser om een dipool voor chemische beeldvorming te induceren. Het kan een laterale resolutie van ~ 10 nm bieden. Er is een puls op f m = f 1 − f 0 , waar f 0 en f 1 zijn de eerste en tweede mechanische eigenmode resonanties van cantilever. Topografie en PiFM-signaal van het monster worden gelijktijdig opgenomen door het AFM-feedbacksysteem op f 1 en f 0 , respectievelijk [14].
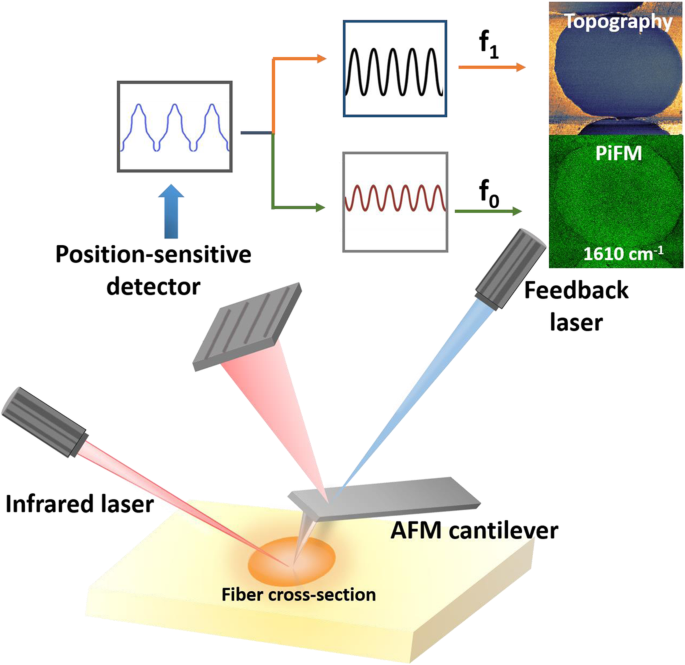
Vereenvoudigd schema van de foto-geïnduceerde krachtmicroscopie (PiFM) setup
Methoden
Voorbereiding van monsters
Er werden monsters verzameld van verschillende stabilisatiestadia onder verschillende omgevingstemperaturen. De PAN-vezels die in deze studie worden gebruikt, zijn de 6 K-precursorvezels van HENGSHEN T700 (HENGSHEN Co. Jiangsu, CHINA). De voorlopervezels gingen continu door vijf ovens met geleidelijk stijgende temperaturen (210 °C, 220 °C, 230 °C, 240 °C, 250 °C). De monsters werden achtereenvolgens aangeduid als 01-05. De stabilisatietijd in elke oven was 8 min en de loopsnelheid van de sleep was 30 m/h.
De procedure voor het voorbereiden van monsters voor PiFM-metingen is als volgt:Ten eerste wordt een vezelkabel recht op de bodem van het model bevestigd om ervoor te zorgen dat de vezelas evenwijdig is en dicht bij het epoxyblokoppervlak en vervolgens wordt ingebed in epoxyhars. Om de dwarsdoorsnede te verkrijgen, werd het oppervlak loodrecht op de vezelas mechanisch geslepen en gepolijst door een polijstmachine (Struers Inc.).
Karakterisering
PiFM-metingen (Molcular Vista, VS) werden uitgevoerd om de veranderingen van functionele groepen in verschillende radiale posities van het monofilament tijdens de stabilisatie te onderzoeken en werden in contactloos uitgevoerd om schade aan de zachtste monsters te voorkomen en een hogere ruimtelijke resolutie te bereiken dan AFM-topografie.
Raman-spectroscopie werd uitgevoerd met een objectief van × 100 met behulp van de 532 nm-laser van confocale Raman-spectroscopie (RM2000, Renishaw, VK).
Resultaten en discussies
Afbeelding 2b geeft de typische PiFM-spectra weer in 1400–1900 cm −1 regio op verschillende posities langs radiale richting. De absorptieband rond 1580 cm −1 is te wijten aan combinatietrillingen van –C=C en –C=N strekmodi [15]. De absorptieband rond 1720 cm −1 is toegewezen aan de ν C=O . Er kon worden waargenomen dat de intensiteit van deze twee banden veranderde met posities. Dit fenomeen was te wijten aan de verschillende chemische structuren gevormd door de verschillende reacties langs radiale richting tijdens stabilisatie. De evolutie van de chemische huid-kernstructuur in de monofilamenten kon echter niet visueel worden onthuld. Daarom werd PiFM-mapping uitgevoerd in beide vibratiemodi met specificiteit op nanoschaal.
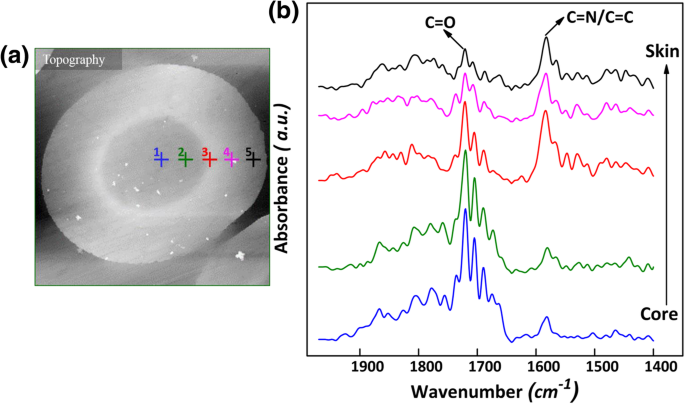
een Topografiebeeld van monster 03; b De spectra in 1400-1900 cm −1 van verschillende punten langs radiale richting
Afbeelding 3 toont de topografie en de PiFM-toewijzing van de absorptie-intensiteit bij 1600 en 1730 cm −1 van monsters 01-05. De intensiteit van ν –C=C en ν –C=N op 1600 cm −1 van de kern was duidelijk kleiner dan die van de huid. Dit werd toegeschreven aan de verschillende chemische reacties veroorzaakt door de verdeling van de zuurstofconcentratiegradiënt in de dwarsdoorsnede. Voorgestelde chemische reactieschema's van warmtebehandelde PAN worden geïllustreerd in Schema 1, de dehydrogenering wordt voornamelijk aangedreven door zuurstof, terwijl anoxische toestand meer geleidend is voor het optreden van cyclisatie [16]. In het beginstadium was er meer zuurstof geconcentreerd in het huiddeel, dus dit deel gebeurde meestal door dehydrogeneringsreactie en genereerde meer onverzadigde bindingen. De onverzadigde bindingen die in het huidgedeelte werden gevormd, versterkten de algehele intensiteit bij 1600 cm −1 . Verder verscheen er een heldere ring op het grensvlak tussen de huid en de kern van monsters 02 en 03, wat kan worden toegeschreven aan de vorming van een kristallaag op het grensvlak. Nunna et al. [17] hebben bewezen dat de mechanische eigenschappen van de huid en de kern verschillend zijn en dat de verminderde modulus van de huid hoger is dan die van de kern. Hoewel de huid en de kern dezelfde spanning ervoeren als een functie van de rekkracht tijdens stabilisatie, was het vervormingsweerstandsvermogen van moleculaire ketens in de huid hoger dan de kern vanwege een hogere modulus. Daarom ontstond er een schuifkracht op het grensvlak tussen de huid en het kerndeel. In dit geval zouden moleculaire ketens in het grensvlakgebied efficiënter en regelmatiger worden gestapeld onder afschuifkracht, waardoor een hogere dichtheid van functionele groepen -C=N en -C=C wordt gegenereerd. Volgens de wet van Lambert-Beer moet de intensiteit van de infraroodabsorptie worden verbeterd, wat resulteert in het verschijnen van de heldere ring. Bovendien vertraagde de dunne en dichte kristallaag de diffusie van zuurstof naar de kern verder. Daarom werd het huid-kernverschil van monster 03 verder vergroot. Naarmate het stabilisatieproces vorderde, verdween de heldere ring echter geleidelijk en hadden de monofilamenten de neiging homogeen te zijn, zoals weergegeven in Fig. 3 04-05. Het was omdat de verdere oxidatie leidt tot de vernietiging van de kristalbarrièrelaag, wat gunstig was voor verdere zuurstofdiffusie en dehydrogenering in het kerndeel. Dit komt ook goed overeen met het fenomeen dat de kristalliniteit van gestabiliseerde PAN-vezel aanvankelijk toeneemt en vervolgens een continue afname vertoont met toenemende temperatuur [18].

Topografie van monsters 01-05; PiFM-toewijzing van de absorptie-intensiteit bij 1600 en 1730 \( {\mathsf{cm}}^{-\mathsf{1}} \) voor monsters 01–05
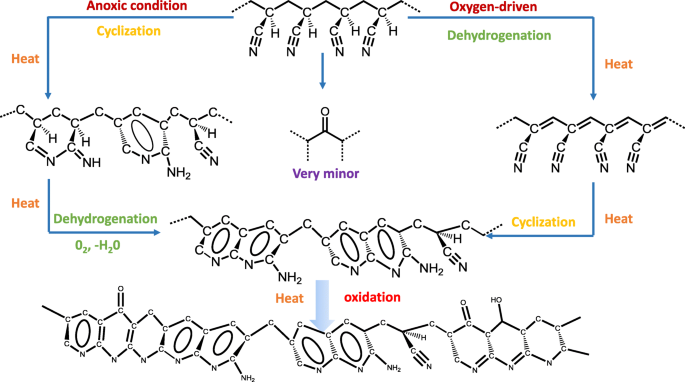
Voorgestelde structurele veranderingen tijdens stabilisatie
Aan de andere kant, hoewel de algehele intensiteit op 1730 cm −1 vertoonde bijna geen toename tot monster 04, er werd een duidelijk huid-kernverschil waargenomen in monsters 02 en 03. Dit komt omdat de PAN werd verkregen door de copolymerisatie van acrylonitril en itaconzuur dat een carbonylgroep bevat. In het beginstadium vond de dehydrogeneringsreactie meestal plaats in het huidgedeelte, dus werd de carbonylgroep geëlimineerd in de vorm van H2 O. Daarom heeft het kerndeel een hogere concentratie carbonylgroep. Met de verdere stabilisatie bevorderden de hogere temperatuur en de verbeterde uniformiteit van het zuurstofgehalte in radiale richting gelijktijdig de oxidatie in de huid en dehydrogenering in de kern in monsters 04 en 05. De oxidatie omvatte niet alleen de vorming van –C=O-bindingen, maar verbeterde ook de dehydrogenering door waterstof in de vorm van H2 . te elimineren O [19]. Zoals getoond in Fig. 3, is het duidelijk waar te nemen dat de geconjugeerde en de geoxideerde structuren de neiging hebben om homogeen te zijn in de monsters 04 en 05 in termen van de absorptie-intensiteiten bij 1600 en 1730 cm −1 .
Zoals te zien is in figuur 3, waren de monsters voornamelijk rijk aan –C=O in het kerngebied en rijk aan –C=N/−C=C in het huidgebied. Afbeelding 4 toont PiFM-toewijzing van monsters 01-03. Voor kwantificering, de verhouding van I–C=O /I–C=N/−C=C werd berekend en weergegeven in tabel 1, die werd beschouwd als de verhouding van geoxideerde structuur tot geconjugeerde structuur. Er was een duidelijke afname van monsters 01 tot 03, wat aantoont dat de hogere concentratie van koolstof-koolstof dubbele bindingen werd gegenereerd na een verdere dehydrogeneringsreactie in het huidgebied.
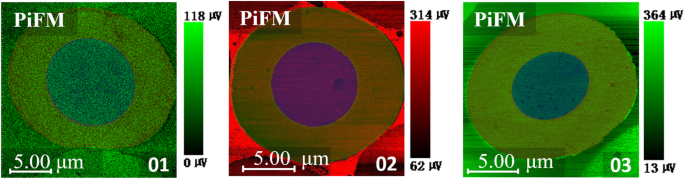
Microgebiedanalyse op de afbeelding
Raman-metingen voor de dwarsdoorsnede van vezels werden uitgevoerd om verder te bewijzen dat dehydrogeneringsreactiedomeinen in het huidgebied. De integrale oppervlakteverhouding van D tot G-band A D /A G waarde wordt beschouwd als de sp 2 /sp 3 –C-verhouding [20]. Afbeelding 5 toont de A D /A G waarde in de huid en kerngebieden van vezels met betrekking tot de behandelingstemperatuur van 220 ° C tot 250 ° C (Er was bijna geen D- en G-bandsignaal van monster 01, wat te wijten is aan een lage mate van dehydrogeneringsreactie en een sterk fluorescentie-effect veroorzaakt door organische stof). Er was een significant verschil tussen de huid en de kern, het huidgedeelte had een hogere concentratie sp 2 hybride koolstofatomen. Dit werd toegeschreven aan een hogere mate van dehydrogeneringsreactie in het huidgedeelte, wat leidt tot de vorming van –C=C. Naarmate het stabilisatieproces vorderde, werd de A D /A G waarde licht gedaald, wat wijst op de hogere mate van grafitisering. Dit komt goed overeen met de resultaten van PiFM-mapping.
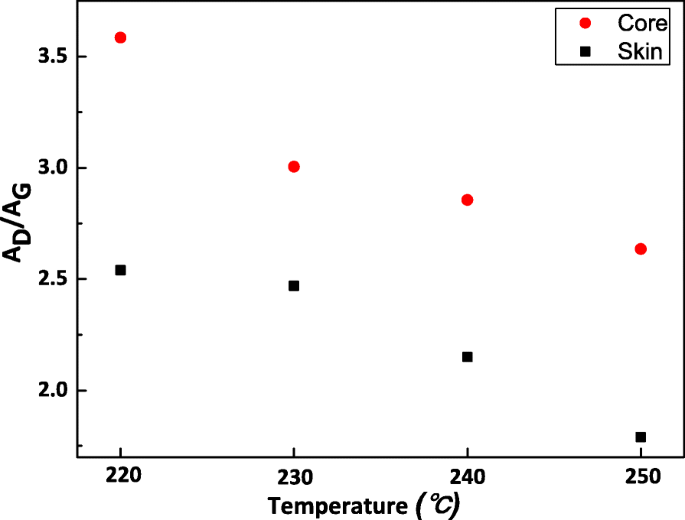
De A D /A G waarde in huid en kerngebieden van vezels met betrekking tot behandelingstemperatuur van 220 °C tot 250 °C
Om de vorming van de huid-kern chemische structuur van PAN-gestabiliseerde vezels schematisch te beschrijven, is een algemeen diagram van het meest waarschijnlijke vormingsmechanisme getekend in Fig. 6. De verschillende reacties zijn gelabeld met de overeenkomstige kleur, blauw staat voor dehydrogenering, geel staat voor cyclisatie, en rood markeert de oxidatie. De vorming van de huid-kern chemische structuur werd veroorzaakt door het cyclisatiedomein in het kerngebied, terwijl het huiddeel het door zuurstof aangedreven dehydrogeneringsdomein onderging. Dit kan worden toegeschreven aan de heterogene zuurstofverdeling in de huid en het kerndeel. Bovendien werd de structurele heterogeniteit ook vergroot door de kristallaag gevormd op het grensvlak tussen de huid en de kern. Terwijl het stabilisatieproces zich ontwikkelde, werd de kristallaag vernietigd door oxidatie. Achtereenvolgens zou de verhoogde mate van oxidatie in het hele monofilament ervoor kunnen zorgen dat de vezel schijnbaar homogeen is.
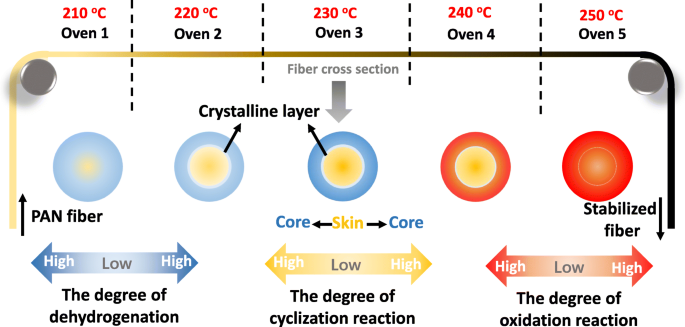
Vormingsmechanisme van de huid-kernstructuur van gestabiliseerde PAN-vezels
Conclusies
Deze studie toont aan dat de huid-kernstructuur van gestabiliseerde PAN-vezels die aanvankelijk gevormd werden door cyclisatie, optrad in een kerngebied, terwijl het huiddeel het door zuurstof aangedreven dehydrogeneringsdomein onderging. Dan, met de hogere mate van oxidatie, zouden de filamenten de neiging kunnen hebben homogeen te zijn.
Afkortingen
- AFM:
-
Atoomkrachtmicroscopie
- PAN:
-
Polyacrylonitril
- PiFM:
-
Foto-geïnduceerde krachtmicroscopie
Nanomaterialen
- Vilt
- Spandex
- Garen
- Touw
- Vormingsmechanisme van goed geordende, dicht opeengepakte superroosters van nanodeeltjes afgezet vanuit de gasfase op sjabloonvrije oppervlakken
- Onthulling van de atomaire en elektronische structuur van gestapelde koolstof nanovezels
- Structuur en elektronische eigenschappen van met overgangsmetaal gedoteerde kaoliniet nanoklei
- Invloed van omstandigheden van vorming van Pd/SnO2 nanomateriaal op eigenschappen van waterstofsensoren
- Au-Capped GaAs-nanopillar-arrays gefabriceerd door metaalondersteunde chemische etsing
- Effecten van micro-omgevings-pH van liposoom op chemische stabiliteit van geladen geneesmiddel
- C - Programmastructuur



