Bi2Se3-gevoelige TiO2-nanobuisfilms voor fotogegenereerde kathodische bescherming van 304 roestvrij staal onder zichtbaar licht
Abstract
Titaandioxide (TiO2 ) arrays van nanobuisjes gekoppeld aan een halfgeleider met smalle opening - bismutselenide (Bi2 Se3 ) - vertoonde een opmerkelijke verbetering in de fotokathodische beschermingseigenschap voor 304 roestvrij staal onder zichtbaar licht. Bi2 Se3 /TiO2 nanocomposieten werden met succes gesynthetiseerd met behulp van een eenvoudige tweestapsmethode, waaronder een elektrochemische anodisatiemethode voor het bereiden van pure TiO2 en een chemische badafzettingsmethode voor het synthetiseren van Bi2 Se3 nanobloemen. De morfologie en structuur van de composietfilms werden bestudeerd door middel van scanning-elektronenmicroscopie, energiedispersiespectroscopie, röntgenfoto-elektronenspectroscopie en röntgendiffractie. Bovendien is de invloed van de Bi2 Se3 De inhoud van de foto-elektrochemische en fotokathodische beschermingseigenschappen van de composietfilms werd ook bestudeerd. De fotostroomdichtheid van de Bi2 Se3 /TiO2 nanocomposieten was significant hoger dan die van pure TiO2 onder zichtbaar licht. De sensibilisator Bi2 Se3 verbeterde de efficiënte scheiding van de fotogegenereerde elektron-gatparen en de fotokathodische beschermingseigenschappen van TiO2 . Onder zichtbaar licht, Bi2 Se3 /TiO2 nanocomposieten gesynthetiseerd door de chemische baddepositiemethode met Bi 3+ (0,5 mmol/L) vertoonde de optimale fotogegenereerde kathodische beschermingsprestaties voor 304 roestvrij staal.
Achtergrond
Als belangrijke technische materialen is roestvast staal op grote schaal toegepast bij belangrijke projecten op tal van gebieden vanwege hun uitstekende corrosieweerstand. Roestvast staal kan echter ernstige corrosie ondergaan wanneer het wordt gebruikt in specifieke agressieve omgevingen, zoals zure omgevingen, evenals onder chloridehoudende of hoge temperaturen [1,2,3,4]. Uitgebreid onderzoek en toepassingen van de traditionele anticorrosiemethode, waaronder coatings [5, 6], gebruik van een opofferingsanode [7] en opgedrukte huidige kathodische bescherming [8, 9], zijn de afgelopen decennia ontwikkeld. Milieuvriendelijke en duurzame roestwerende technologie blijft echter een belangrijke doelstelling. Als een nieuwe anticorrosietechnologie werd fotokathodische bescherming voor het eerst voorgesteld door Yuan en Tsujikawa in 1995 [10] voordat ze aandacht kregen van corrosieonderzoekers [11,12,13,14].
Titaandioxide (TiO2 ) is een belangrijk foto-elektrisch materiaal met goede foto-elektrische conversie en fotokatalyse-eigenschappen en wordt veel gebruikt in katalysatoren [15], zonnecellen [16] en gassensoren [17] vanwege de lage kosten, niet-toxiciteit en stabiele chemische eigenschappen. TiO2 en TiO2 composieten op basis van foto's worden gebruikt voor kathodische bescherming door foto's:een veelbelovende techniek voor corrosiepreventie die de laatste jaren een snelle ontwikkeling heeft doorgemaakt [18,19,20,21,22,23]. De bandgap (3,2 eV) van TiO2 beperkt de fotorespons tot alleen het ultraviolette gebied, wat de gebruiksverhouding van zonne-energie aanzienlijk verlaagt. Bovendien, foto-geïnduceerde ladingsdragers in kale TiO2 nanodeeltjes hebben een zeer korte levensduur vanwege de snelle recombinatie van foto-geëxciteerde elektron-gatparen, wat het fotokathodische beschermingseffect van pure TiO2 vermindert films. Dus, hoe de bovenstaande tekortkomingen van TiO2 . te verhelpen is een veelbesproken onderwerp geworden. Er zijn veel onderzoeken gedaan naar de bereiding van TiO2 met niet-metalen elementen (F, N en S) [12, 24, 25], metaalatomen (Fe, Co, Cu en Ce) [26,27,28,29] en enkele nano-halfgeleiders met smalle bandgap (Ag2 O, ZnSe, WO3 , CdS, Ag2 S, CdSe en Bi2 S3 ) [30,31,32,33,34,35,36] om de dragerscheiding en lichtgebruik van TiO2 te verbeteren .
Bismutselenide (Bi2 Se3 ) is een gelaagde halfgeleider met directe bandgap en een belangrijk lid van de V2 VI3 samengestelde familie. Het heeft een hoge absorptiecoëfficiënt in de zichtbare en nabij-infrarode lichtgebieden met een smalle bandgap (0,35 eV) [37]. Als een belangrijk n-type chalcogenide, Bi2 Se3 bezit veel belangrijke eigenschappen, zoals een hoge elektrische geleidbaarheid [38], aanzienlijke thermo-elektrische eigenschap [39], lichtgevoeligheid [40], elektrochemische eigenschap [41] en fotogeleiding [42]. Bovendien, Bi2 Se3 is een populaire topologische isolator [43,44,45] en heeft de unieke eigenschap van geleidende oppervlaktetoestanden en geïsoleerde bulktoestanden. Bi2 . van hoge kwaliteit Se3 nanostructuren zijn bereid met behulp van een fysische depositiemethode in hoog vacuüm, chemische dampafzetting, atomaire laagafzetting, gepulseerde laserdepositie en een damp-vloeistof-vaste stoftechniek bij hoge temperatuur [44,45,46,47,48,49]. Deze synthetische methoden voor Bi2 Se3 vereisen een moeilijke fabricage, wat leidt tot hoge productiekosten. In dit artikel worden de bovenstaande problemen overwonnen door gebruik te maken van een goedkope en eenvoudige methode voor depositie in een chemisch bad voor Bi2 Se3 nanoflower-afzetting op TiO2 . De combinatie van een n-Bi2 Se3 /n-TiO2 heterojunctie als een efficiënte fotoanode werd voor het eerst toegepast op de fotogegenereerde kathodische bescherming van 304ss. De morfologie, structuur en optische absorptie-eigenschap van Bi2 Se3 /TiO2 nanocomposieten werden bestudeerd door middel van scanning elektronenmicroscopie (SEM), röntgendiffractie (XRD), energiedispersieve röntgenspectroscopie (EDS), röntgenfoto-elektronspectroscopie (XPS) en UV-zichtbare (UV-Vis) diffuse reflectiespectra , respectievelijk.
Methoden
Alle chemicaliën die in dit onderzoek werden gebruikt, waren van analytische kwaliteit en werden zonder verdere zuivering gebruikt zoals ze waren ontvangen. Alle waterige oplossingen werden bereid met gedeïoniseerd water.
Voorbereiding van TiO2 Filmpje
Ti-folies (20 mm × 10 mm × 0,3 mm;> 99,9% zuiverheid) werden gepolijst met een mengsel dat NH4 bevatte. F (2,25 g), H2 O (12,5 ml), H2 O2 (30 gew.%, 30 mL) en HNO3 (68 gew.%, 30 ml), en vervolgens werden Ti-stukken gereinigd met gedeïoniseerd water en ethanol. TiO2 film werd bereid op Ti-folie met de anodische oxidatiemethode die in de literatuur wordt vermeld [50]. De Pt-plaat werd gekozen als de kathode en de Ti-folie was de anode bij 20 V gedurende 1 uur in een ethyleenglycoloplossing die NH4 bevatte F (0,22 g), H2 O (4 ml) en ethyleenglycol (40 ml) bij kamertemperatuur. Daarna werden de monsters gespoeld met gedeïoniseerd water en ethanol. Ten slotte werden de monsters gedurende 2 uur bij 450 °C gegloeid en in omgevingslucht gekoeld om TiO2 te verkrijgen. film.
Synthese van Bi2 Se3 op de TiO2 Filmpje
De Bi2 Se3 werd bereid door de chemische baddepositiemethode. In de experimentele procedure werd 8 mmol nitrilotriazijnzuur (H3 NTA) en 0,4 mmol Bi(NO3 )3 ·5H2 O werden toegevoegd aan gedeïoniseerd water (400 ml) om het bismutchelaat te vormen, met een Bi 3+ concentratie van 1,0 mmol/L in de gemengde oplossing. Twee millimol ascorbinezuur als reducerend reagens werd aan de bovenstaande oplossing toegevoegd en vervolgens werd ammoniumhydroxide voorzichtig druppelsgewijs toegevoegd totdat de pH van het mengsel was ingesteld op ongeveer 8,6-8,9 en de gemengde oplossing kleurloos en transparant leek. Eindelijk, Na2 SeSO3 (20 ml, 30 mmol/L) werd in de bovenstaande oplossing geïnjecteerd. Bij alle bovenstaande experimenten werden de waterige oplossingen grondig geroerd met een magnetische roerder om een homogene oplossing te verkrijgen. Dan een TiO2 substraat werd ondergedompeld in de uiteindelijke oplossing (40 ml) in een bekerglas (100 ml). Het bekerglas bedekt met huishoudfolie werd vervolgens gedurende 200 minuten overgebracht naar een oven die werd verwarmd tot een temperatuur van 80 °C om de Bi2 te verkrijgen. Se3 nanoflower op de TiO2 substraat. Ten slotte werd het monster uit de beker gehaald en verschillende keren gewassen met gedeïoniseerd water en ethanol en daarna in omgevingslucht gedroogd. Op deze manier, Bi2 Se3 -gesensibiliseerde TiO2 films werden verkregen en gelabeld met Bi2 Se3 /TiO2 -1,0. Voor de eenvoud, verschillende hoeveelheden Bi2 Se3 op TiO2 substraten worden aangeduid als Bi2 Se3 /TiO2 -γ in dit artikel, waarbij γ de concentratie van Bi 3+ . aangeeft in de H3 NTA en Bi (NO3 )3 ·5H2 O oplossing. Met de hoeveelheden van de andere reagentia constant gehouden, Bi2 Se3 /TiO2 -0,5 en Bi2 Se3 /TiO2 -0,25 werden verkregen voor Bi 3+ concentraties van respectievelijk 0,5 mmol/L en 0,25 mmol/L. De invloed van verschillende hoeveelheden Bi2 Se3 over de foto-elektrochemische en fotokathodische beschermingseigenschappen van de composietfilms werd in dit artikel onderzocht.
Morfologie en samenstellingsanalyse
Scanning-elektronenmicroscopie (SEM, Hitachi S-4800, Japan) werd gebruikt om de morfologieën van de bereide films te onderzoeken. Energie-dispersieve röntgenspectroscopie (EDS, Oxford Energy 350 röntgenenergiespectrumanalyser) en röntgenfoto-elektronspectroscopie (XPS, Thermo Scientific ESCALAB 250Xi) werden gebruikt om de chemische samenstelling van de Bi2 te bepalen. sub> Se3 /TiO2 nanocomposieten. UV-Vis DRS (Japan Hitachi UH4150) werd gebruikt om de lichtabsorptie van de monsters te bepalen. De samenstelling van de kristallijne fase van de monsters werd gekarakteriseerd door een röntgendiffractometer (XRD, Duitsland Bruker AXSD8) met behulp van Cu Kα straling (γ = 1.54056 Å) van 10° tot 80°.
Foto-elektrochemische metingen
Zoals getoond in Fig. 1 werd een koppelingssysteem bestaande uit fotolyse en elektrolytische cellen gebruikt voor de foto-elektrochemische metingen, en een protonenuitwisselingsmembraan werd gebruikt om de twee cellen aan elkaar te koppelen. De fotolysecel bevatte een 0,1 mol/L Na2 S en 0,2 mol/L NaOH gemengde oplossing, die de rol speelde van een opofferingsmiddel voor het bevorderen van de scheiding van elektronen en gaten [33, 51], terwijl een 0,5 mol/L NaCl-oplossing werd gebruikt als elektrolyt voor de elektrolytische cel. In de elektrolytische cel werd een systeem met drie elektroden aangenomen met een Pt-folie als de tegenelektrode (CE), een verzadigde calomelelektrode als de referentie-elektrode (RE) en 304ss als de werkelektrode (WE). Bi2 Se3 /TiO2 nanocomposietmonsters die in de fotolysecel werden geplaatst, werden door een koperdraad verbonden met een 304ss-elektrode die in de elektrolytische cel was ondergedompeld. De lichtbron in het zichtbare lichtbereik werd bestraald door een hogedruk xenonlamp (PLS-SXE 300 C, Beijing Perfectlight Company, China). De veranderingen in de nullastpotentiaal (OCP) en fotostroomcurves werden gemeten met behulp van een Gamry-potentiostaat/galvanostaat/ZRA-systeem (GAMRY 3000, Gamry Instruments, VS) voor en tijdens bestraling met licht.
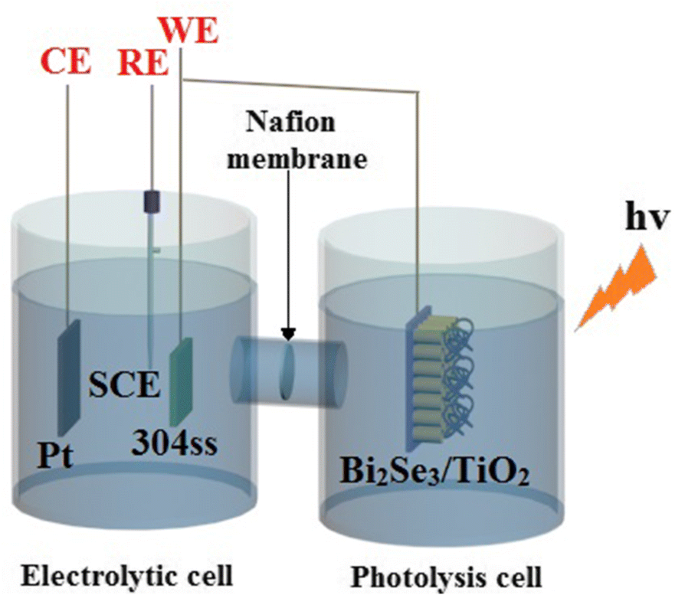
Schematische schetsen van de experimentele opstelling gebruikt voor foto-elektrochemische analyse
Resultaten en discussie
Karakterisering van Pure TiO2 en Bi2Se3/TiO2
Afbeelding 2a toont typisch bovenaanzicht en topografieën in dwarsdoorsnede voor TiO2 films bereid onder de anodisatiemethode. De TiO2 nanobuisarrays tonen een nanoporeuze structuur die is samengesteld uit goed geordende nanobuisjes met een hoge dichtheid met een gemiddelde binnendiameter en lengte van respectievelijk ongeveer 55 nm en 680 nm. Zoals weergegeven in Fig. 2b–d, is de TiO2 nanobuisoppervlakken zijn met succes gewijzigd door Bi2 Se3 via de chemische baddepositiemethode voor verschillende concentraties Bi 3+ . Voor Bi2 Se3 /TiO2 -0,25, de Bi2 Se3 nanovlokken werden sporadisch verdeeld en ongelijkmatig geaggregeerd over de TiO2 nanobuisjes (Fig. 2b). Wanneer de concentratie van Bi 3+ was 0,5 mmol/L, Bi2 Se3 was bijna volledig samengesteld uit bloemachtige patronen van plooibare ultradunne nanovlokken met een diameter van ongeveer 800 nm, zonder het mondstuk van de TiO2 te blokkeren nanobuisjes of ze beschadigen (Fig. 2c). Bi2 Se3 nanobloemen waarvan werd waargenomen dat ze gelijkmatig verdeeld waren over het oppervlak van de TiO2 toonde een interne verknoopte structuur voor de ultradunne nanovlokken, die effectief de aggregatie van lamellen voorkwam en een langdurige levensduur van de architecturen handhaafde, zoals weergegeven in figuur 2c. Na de concentratie van Bi 3+ werd verhoogd tot 1,0 mmol/L, de hoeveelheid en diameter van de Bi2 Se3 nanoflowers namen aanzienlijk toe en de agglomeratie van nanoflowers blokkeerde de nanobuisjes, zoals weergegeven in figuur 2d. Het corresponderende EDS-spectrum van de Bi2 Se3 /TiO2 -0,5 films getoond in Fig. 2e onthulden dat de karakteristieke pieken voor Ti, O, Bi en Se waren gemarkeerd met atoompercentages van Bi en Se van respectievelijk 0,9% en 1,3%. Het is algemeen bekend dat de meetfout van de EDS-test toeneemt met de afname van de inhoud van het testelement. Het is dus acceptabel dat de atoomverhouding van Bi en Se dicht bij 2:3 ligt.

SEM-afbeeldingen voor a pure TiO2 , b Bi2 Se3 /TiO2 -0,25, c Bi2 Se3 /TiO2 -0,5 en d Bi2 Se3 /TiO2 -1,0; e EDS-spectrum voor Bi2 Se3 /TiO2 -0,5 films
Afbeelding 3a toont de XRD-spectra voor pure TiO2 (kromme a) en Bi2 Se3 /TiO2 -1,0 nanocomposieten (curve b). Afgezien van de Ti-substraatpieken, kwamen de diffractiepieken bij 25,38°, 38,03°, 48,01°, 54,05°, 55,17°, 62,71° en 70,44° goed overeen met de roostervlakken (101), (004), (200), (105), (211), (204) en (220) van anatase TiO2 , respectievelijk (JCPDS 21-1272). Behalve de TiO2 pieken, werden de kenmerkende diffractiepieken bij 29,35 ° en 74,90 ° geïndexeerd met de roostervlakken (015) en (0216) van het rhomboëdrische kristal Bi2 Se3 (JCPDS 33-0214). Er is echter geen duidelijke piek van Bi2 Se3 /TiO2 -1,0 vanwege lage inhoud Bi2 Se3 gedeponeerd op TiO2 en de XRD-spectra kwamen overeen met de SEM- en EDS-resultaten. Röntgenfoto-elektronspectroscopie (XPS) werd gebruikt om de chemische samenstelling en toestanden van de Bi2 verder te bepalen. Se3 /TiO2 nanocomposieten. Zoals weergegeven in figuur 3b, onthulde XPS het bestaan van Bi-, Se-, Ti- en O-componenten naast C-verontreinigingen als gevolg van onvoorziene koolwaterstofverontreiniging. Afbeelding 3c toont de piekposities voor Ti 2p bij 458,7 en 464,5 eV, wat aangeeft dat de titaniumoxiden voornamelijk bestonden uit TiO2 [52]. Zoals geïllustreerd in figuur 3d, kwamen de O 1s-semaforen overeen met twee Gauss-pieken:het maximum bij de lagere bindingsenergie (530,0 eV) werd toegeschreven aan de roosterzuurstof (OL ) in Bi2 Se3 /TiO2 nanocomposieten en de tweede bij de hogere bindingsenergie (531,5 eV) was afgeleid van de geadsorbeerde zuurstof (OA ), inclusief zwak bindende zuurstof- of hydroxylgroepen. Het bestaan van OA was te wijten aan het ontstaan van zuurstofvacatures op het oppervlak van de nanocomposieten, wat de foto-elektrische conversie-eigenschappen van Bi2 zou kunnen verbeteren Se3 /TiO2 nanocomposieten in fotokathodische bescherming [53]. Afbeelding 3e laat zien dat de 4f7/2 asymmetrische piek voor Bi opgelost in twee pieken (157,5 en 159,4 eV), met de Bi 4f5/2 spectrum op dezelfde manier verdeeld in twee banden bij respectievelijk 162,8 en 164,7 eV. De posities van de lagere pieken (157,5 eV en 162,8 eV) kwamen goed overeen met die in Bi2 Se3 , waarbij de hogere pieken overeenkomen met bismutoxide bij 159,4 eV en 164,7 eV [54, 55]. Geconcludeerd kan worden dat een handvol bismutmetaal is geoxideerd tijdens het syntheseproces met Bi2 Se3 pure TiO2 . wijzigen . Zoals weergegeven in Fig. 3f, werden de twee pieken toegewezen aan de 3d3/2 en 3d5/2 kernniveaus van Se bij respectievelijk 55,1 en 54,2 eV, wat aangeeft dat Se bestond in de vorm van Se 2- [56].
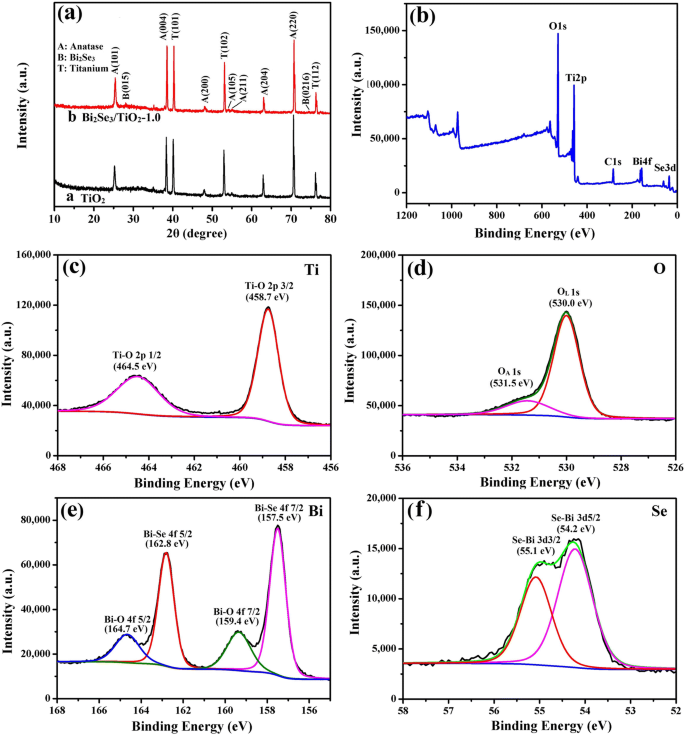
een XRD-patronen voor pure TiO2 en Bi2 Se3 /TiO2 -1,0 nanocomposieten; b het totale onderzoeksspectrum, c Ti 2p, d O 1s, e Bi 4f en f Se 3d XPS-spectra voor Bi2 Se3 /TiO2 -1,0 nanocomposieten
Afbeelding 4 toont het lichtabsorptievermogen van pure TiO2 en Bi2 Se3 /TiO2 -1,0 nanocomposieten. De karakteristieke absorptierand voor pure TiO2 was ongeveer 380 nm binnen het UV-gebied vanwege de bandgap-energie van anatase TiO2 (3,2 eV) (curve a). Uitgesproken adsorptie werd waargenomen voor Bi2 Se3 /TiO2 nanocomposieten in het gebied van zichtbaar licht (350-800 nm) (curve b), met een absorptievermogen voor zichtbaar licht dat hoger is dan dat van pure TiO2 vanwege de integratie van de Bi2 Se3 nanobloem. Dit fenomeen kan worden toegeschreven aan het feit dat Bi2 Se3 wordt geëxciteerd onder zichtbaar licht vanwege de smalle bandgap (0,35 eV), met elektronen en gaten geproduceerd in de geleidingsband (CB) en valentieband (VB). Daarom is de toevoeging van Bi2 Se3 verhoogt effectief het absorptievermogen van zichtbaar licht van Bi2 Se3 /TiO2 nanocomposieten.
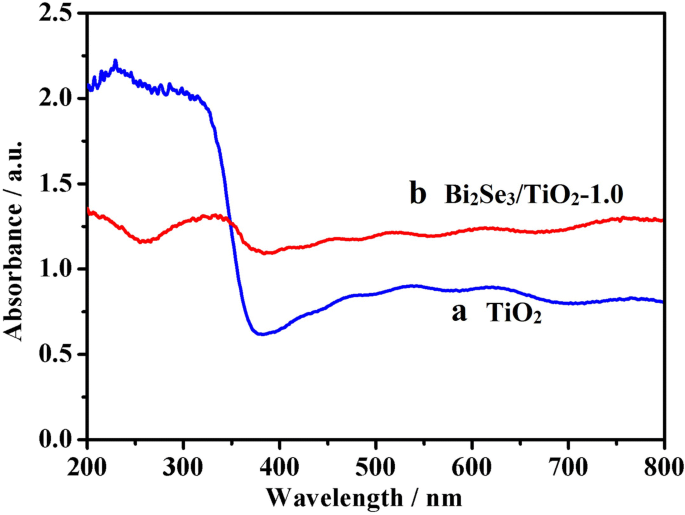
UV-zichtbare absorptiespectra voor TiO2 (a) en Bi2 Se3 /TiO2 -1,0 (b)
Fotokathodische beschermingsprestaties van pure TiO2 en Bi2Se3/TiO2
Zoals weergegeven in Fig. 5, zijn de OCP-curven voor 304ss gekoppeld aan pure TiO2 en Bi2 Se3 /TiO2 nanocomposietfotoanodes werden gemeten onder intermitterend zichtbaar licht, waarbij de OCP-respons op verlichting werd gevraagd en verschoven naar een negatief potentieel voor alle gekoppelde elektroden. In de beginfase van het licht aan vertoonde de OCP voor alle gekoppelde elektroden een negatieve verschuiving gedurende een korte tijd, wat te wijten was aan de overdracht van de aangeslagen foto-elektronen van het zuivere TiO2 en Bi2 Se3 /TiO2 nanocomposiet naar de 304ss-elektrode [1, 57]. Vervolgens kunnen de relatief stabiele OCP-waarden worden toegeschreven aan de balanceringssnelheid tussen de creatie en recombinatie van fotogegenereerde elektronen [32]. Na het uitschakelen van de bestraling worden de OCP-waarden voor de Bi2 Se3 /TiO2 nanocomposieten keerden met een lagere snelheid terug naar hun oorspronkelijke waarden in vergelijking met pure TiO2 . Dit fenomeen kan worden toegeschreven aan het elektronenpooleffect van Bi2 Se3 /TiO2 nanocomposieten, die fotogeïnduceerde elektronen kunnen opslaan onder lichtbestraling en deze elektronen langzaam vrijgeven zonder lichtbestraling. Bij bestraling met zichtbaar licht was de OCP-waarde voor 304ss ongeveer − 450 mV in combinatie met TiO2 (curve a), en de OCP-waarden voor 304ss gekoppeld aan Bi2 Se3 /TiO2 -0,25 (curve b), Bi2 Se3 /TiO2 -0,5 (curve d) en Bi2 Se3 /TiO2 -1,0 (curve c) bereikte respectievelijk -905 mV, -996 mV en -958 mV. Deze resultaten gaven aan dat 304ss kathodisch gepolariseerd was eenmaal gekoppeld aan Bi2 Se3 /TiO2 nanocomposieten en dat de Bi2 een goede kathodische bescherming voor 304ss zou kunnen bieden Se3 /TiO2 fotoanoden. Zoals weergegeven in Fig. 5 d, is de 304ss gekoppeld aan Bi2 Se3 /TiO2 -0,5 bezat het meeste negatieve potentieel, wat aangaf dat de beste fotokathodische beschermingsprestaties voor 304ss. Dit resultaat kan zijn omdat de actieve sites en lichte oogst toenam met de toenemende Bi2 Se3 inhoud. Echter, een overmatige hoeveelheid Bi2 Se3 deeltjes dienden als recombinatieplaatsen voor elektronen en gaten, wat de ladingsoverdracht van de Bi2 belemmerde Se3 /TiO2 nanocomposieten naar 304ss.
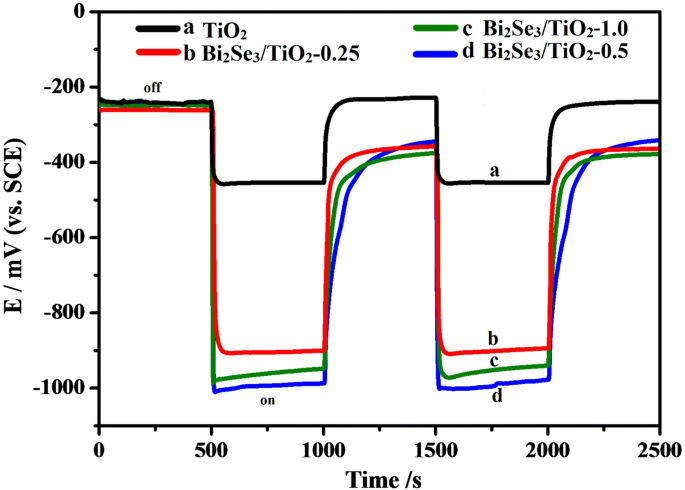
OCP voor 304ss gekoppeld aan pure TiO2 en Bi2 Se3 /TiO2 nanocomposieten in een 0,5 mol NaCl-oplossing
Zoals getoond in Fig. 6, de fotostroomdichtheid vs. tijdcurves voor TiO2 en Bi2 Se3 /TiO2 nanocomposieten vertoonden een snelle en reproduceerbare fotorespons onder intermitterende verlichting van zichtbaar licht, wat de foto-elektrische conversieprestaties van de materialen weerspiegelde. De door foto gegenereerde stroom was relatief klein onder zichtbaar licht vanwege de zwakke absorptie van zichtbaar licht (kromme a). De door foto gegenereerde stroom nam echter opmerkelijk toe onder belichting met zichtbaar licht na sensibilisatie van TiO2 door de Bi2 Se3 nanoflower (krommen b tot d). De gegevens impliceerden dat de Bi2 Se3 /TiO2 nanocomposieten in staat waren zichtbaar licht te gebruiken en dat de heterojunctie tussen TiO2 en Bi2 Se3 bevorderde de scheiding van door foto gegenereerde elektronen en gaten [58]. Verder zijn de foto-elektronen geproduceerd in de geleidingsband van de Bi2 Se3 nanoflower kan gemakkelijk worden overgebracht naar de meer positieve geleidingsband van de TiO2 nanobuisjes onder zichtbaar licht. Na drie bestralingsintervallen behield de fotostroom een relatief stabiele waarde en werd er geen fotostroomdegradatie gedetecteerd, wat de goede fotochemische stabiliteit van de Bi2 illustreert. Se3 /TiO2 nanocomposietfilms. Voor verschillende concentraties Bi 3+ , de Bi2 Se3 /TiO2 nanocomposieten vertoonden verschillende intensiteiten voor de fotostroomrespons. In het bijzonder de tijdelijke fotostroomdichtheid voor Bi2 Se3 /TiO2 -0,5 (415 μA/cm 2 ) was hoger dan die voor Bi2 Se3 /TiO2 -0,25 (85 A/cm 2 ) en Bi2 Se3 /TiO2 -1,0 (160 μA/cm 2 ), wat aangeeft dat Bi2 Se3 /TiO2 -0,5 bezat een ideale scheidingsefficiëntie voor de door foto gegenereerde elektron-gatparen. De actieve sites en lichte oogst waren verminderd vanwege het tekort aan Bi2 Se3 nanoflowers op de Bi2 Se3 /TiO2 nanocomposietfilms, terwijl recombinatieplaatsen voor elektronen en gaten toenamen in de aanwezigheid van een overmatige hoeveelheid Bi2 Se3 nanobloemen. Onder zichtbaar licht, de grootste foto-geïnduceerde stroomdichtheid van de Bi2 Se3 /TiO2 -0,5 fotoanode was consistent met de grootste foto-geïnduceerde potentiële dalingen geïllustreerd in Fig. 5, wat de optimale fotokathodische beschermingsprestaties van Bi2 verder bevestigt Se3 /TiO2 -0,5 voor 304ss.
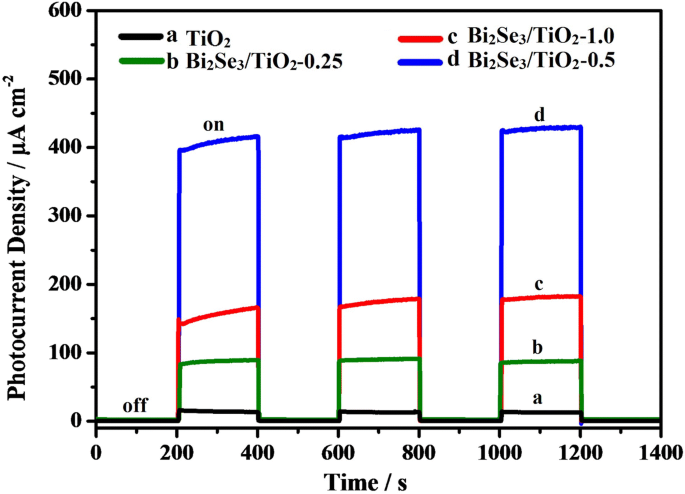
Fotostroomdichtheid vs. tijdkrommen voor zuivere TiO2 en Bi2 Se3 /TiO2 nanocomposieten in 0,1 mol/l Na2 S en 0,2 mol/L NaOH gemengde oplossing
Afbeelding 7 toont de foto-elektrische conversie- en transportprocessen voor de Bi2 Se3 /TiO2 nanocomposieten. Onder zichtbaar licht, Bi2 Se3 nanoflowers kunnen gemakkelijk fotonen absorberen omdat ze geadsorbeerde zuurstof bevatten (OA ) en hebben een smalle bandbreedte (0,35 eV). Wanneer de fotonen worden geabsorbeerd door de Bi2 Se3 nanoflowers, zullen foto-aangeslagen elektronen worden gegenereerd door excitatie van de valentieband (VB) van Bi2 Se3 naar de geleidingsband (CB) van Bi2 Se3 . De foto-aangeslagen elektronen in het CB van Bi2 Se3 worden verschoven naar de CB van TiO2 , terwijl de fotogegenereerde gaten in de VB van TiO2 worden overgedragen aan de VB van Bi2 Se3 , en worden vervolgens vastgelegd door S 2− in de elektrolyt om te veranderen in S op het oppervlak van fotoanodefilm. Wanneer de foto-geëxciteerde elektronen de fotoanode verlaten en overgaan naar 304ss, zullen ze reageren met het zuurstofgas en water om OH − om te zetten. . Verder, Na + wordt door een protonenuitwisselingsmembraan van elektrolysecel naar fotolysecel getransporteerd, zodat het koppelingssysteem als geheel elektrisch neutraal is. Als gevolg hiervan worden de fotogegenereerde ladingen effectief gescheiden en wordt de recombinatiewaarschijnlijkheid voor fotogegenereerde elektron-gatparen verminderd. Zodra 304ss foto-aangeslagen elektronen ontvangt van de Bi2 Se3 /TiO2 nanocomposiet door de draad, de potentiaal van 304ss verschuift negatief. Onder zichtbaar licht verlicht de Bi2 Se3 /TiO2 nanocomposieten kunnen de corrosiesnelheid van 304ss verminderen. Daarom is de efficiënte scheiding van foto-geëxciteerde elektron-gatparen in Bi2 Se3 /TiO2 nanocomposieten versnellen de redoxreactie en genereren effectieve fotokathodische bescherming voor 304ss.
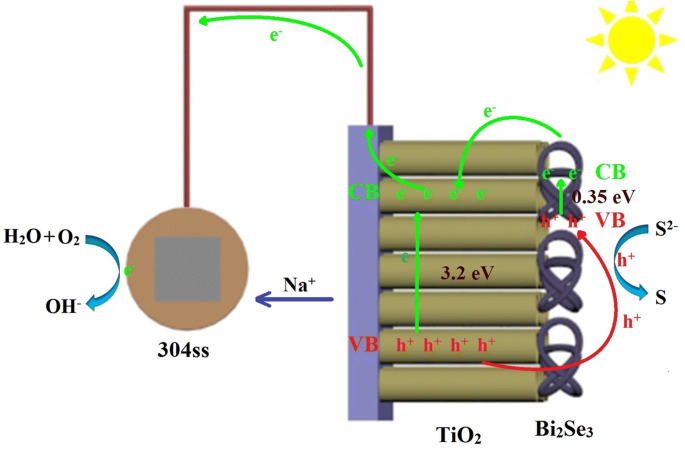
Schematische weergave van de elektronenoverdrachtsprocessen in Bi2 Se3 /TiO2
Conclusies
In dit artikel, TiO2 nanobuisarrays werden bereid door de anodisatiemethode en Bi2 Se3 nanoflowers werden gekweekt op TiO2 nanobuisjes door afzetting in een chemisch bad. De Bi2 Se3 /TiO2 nanocomposieten vertoonden een homogene verdeling en geordende kenmerken. Elektrochemische tests voor de nanocomposieten en pure TiO2 in combinatie met 304ss toonde aan dat de fotogegenereerde kathodische beschermingsprestaties van de Bi2 Se3 /TiO2 nanocomposieten was superieur vergeleken met die voor pure TiO2 . De OCP-waarde voor 304ss in combinatie met Bi2 Se3 /TiO2 -0,5 vertoonde een negatieve verschuiving naar − 996 mV onder belichting met zichtbaar licht als gevolg van de actieve plaatsen en lichtopname van TiO2 gesensibiliseerd door Bi2 Se3 . Door de resultaten van de elektrochemische tests voor drie Bi2 Se3 /TiO2 nanocomposieten, het nanocomposiet bereid met 0,5 mmol/L Bi 3+ in de elektrolyt vertoonden optimale prestaties.
Afkortingen
- 304ss:
-
304 roestvrij staal
- CB:
-
Geleidingsband
- CE:
-
De tegenelektrode
- EDS:
-
Energie-dispersieve röntgenspectroscopie
- H3 NTA:
-
Nitrilotriazijnzuur
- OA:
-
Geadsorbeerde zuurstof
- OCP:
-
Open circuit potentieel
- OL:
-
Roosterzuurstof
- RE:
-
De referentie-elektrode
- SCE:
-
Verzadigde calomelelektrode
- SEM:
-
Scanning elektronenmicroscopie
- UV-Vis:
-
UV-zichtbare diffuse reflectiespectra
- VB:
-
Valentieband
- WIJ:
-
De werkende elektrode
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Roestvrij staal plukken voor toepassingen bij hoge temperaturen
- Onderscheidend 304 en 316 roestvrij staal
- Fotokatalytische activiteiten verbeterd door Au-plasmonische nanodeeltjes op TiO2-nanobuisjesfoto-elektrode gecoat met MoO3
- Structurele en zichtbare infrarood optische eigenschappen van Cr-gedoteerde TiO2 voor gekleurde koele pigmenten
- Een gemakkelijke methode voor het laden van CeO2-nanodeeltjes op anodische TiO2-nanobuisarrays
- Goed uitgelijnde TiO2-nanobuisjes met Ag-nanodeeltjes voor zeer efficiënte detectie van Fe3+-ionen
- Cu2−xSe-modificatie op Monoclinic BiVO4 voor verbeterde fotokatalytische activiteit onder zichtbaar licht
- TiO2-nanomembranen vervaardigd door atomaire laagafzetting voor supercondensatorelektrode met verbeterde capaciteit
- Passivering voor roestvrijstalen onderdelen en behuizingen
- Meest voorkomende toepassingen voor roestvrij staal
- Precisiemetalen voor makers



