Hoge methanolgasdetectieprestaties van Sm2O3/ZnO/SmFeO3-microsferen gesynthetiseerd via een hydrothermische methode
Abstract
In dit werk hebben we Sm2 . gesynthetiseerd O3 /ZnO/SmFeO3 microsferen door een hydrothermische methode gecombineerd met microgolfondersteuning om te dienen als een methanolgassensor. We onderzochten het effect op de microstructuur op verschillende hydrothermische tijden (12 h, 18 h, 24 h en 30 h), en de BET- en XPS-resultaten lieten zien dat het specifieke oppervlak en de geadsorbeerde zuurstofspecies consistent waren met een microstructuur die een significante invloed heeft op de detectieprestaties. De gaseigenschappen van de Sm2 O3 -gedoteerde ZnO/SmFeO3 microsferen werden ook onderzocht. Met een hydrothermische tijd van 24 h vertoonde de gassensor uitstekende detectieprestaties voor methanolgas. Voor 5 ppm methanolgas bij 195 °C bereikte de respons 119,8 met uitstekende herhaalbaarheid en stabiliteit op lange termijn in een test van 30 dagen in een relatief hoge vochtigheidsatmosfeer (55-75% RV). Zelfs bij 1 ppm methanolgas was de respons ook hoger dan 20. Dus de Sm2 O3 -gedoteerde ZnO/SmFeO3 microsferen kunnen worden beschouwd als potentiële materialen voor methanolgassensoren.
Inleiding
Methanol is een belangrijke stof in de industrie en het dagelijks leven. Het is ook een belangrijke grondstof voor veel producten zoals formaldehyde, kleurstoffen en antivries. Directe methanolbrandstofcellen (DMFC) worden beschouwd als belangrijke alternatieve brandstoffen voor autofabrikanten die milieuvriendelijk zijn [1]. Methanol kan echter leiden tot totale blindheid bij een inname van 10 ml via de voeding, en wanneer de hoeveelheid methanol hoger is dan 30 ml, kan dit dodelijke ziekten veroorzaken [2]. Het is dus noodzakelijk om snel lage concentraties methanolgas te detecteren bij lagere bedrijfstemperaturen. Eerder onderzoek naar methanolgassensoren [3, 4] was echter niet bevredigend vanwege de hoge detectielimiet (> 50 ppm) en de hoge bedrijfstemperatuur (> 275 °C). Bovendien hebben weinig onderzoeken gerapporteerd over het probleem van de vochtigheidsstabiliteit van gassensoren.
Metaaloxidehalfgeleiders (MOS) spelen een belangrijke rol in gassensoren vanwege hun uitstekende elektrische eigenschappen. Om de gasdetectieprestaties te verbeteren, hebben sommige onderzoekers halfgeleidermetaaloxiden gesynthetiseerd die zijn gemodificeerd met edelmetalen [5, 6]. De hoge kosten en schaarste van edele metalen belemmeren echter hun praktische toepassing op grote schaal aanzienlijk [7]. In de afgelopen jaren hebben veel onderzoekers zich gericht op het construeren van heterojuncties, waaronder p-p [8], n-n [9, 10] en p-n heterojuncties. Vanwege de chemisch verschillende componenten vertonen heterostructuren superieure detectie-eigenschappen in vergelijking met enkelvoudige oxiden. Met name de pn heterojunctie is de meest voorkomende. Li. et al. [11] synthetiseerde een SnO2 -SnO p-n heterojunctie als een NO2 gassensor. Het antwoord op 50 ppm NEE2 gas bij 50 °C door SnO2 -SnO was acht keer hoger dan die van pure SnO2 . Ju et al. [12] bereid NiO/SnO2 als een triëthylamine gassensor, en de respons was 48,6, terwijl het 14,5 was voor pure SnO2 bij 10 ppm bij 220 °C. Qu et al. [7] synthetiseerde een ZnO/ZnCo2 O4 holle kernschaal als xyleengassensor. De reactie van ZnO/ZnCo2 O4 tot 100 ppm xyleengas was 34,26, terwijl de respons lager was dan 5 voor zuiver ZnO.
ZnO is een typisch n-type halfgeleidend metaaloxide dat in veel onderzoeken op het gebied van gassensoren is gerapporteerd vanwege de gemakkelijke synthesemethode, lage kosten en controleerbare grootte [13]. In het bijzonder heeft ZnO een uitstekende selectiviteit voor alcoholverbindingen [14,15,16]. In de afgelopen jaren hebben onderzoekers zich gericht op p-type (bijvoorbeeld LaFeO3 ) halfgeleidende metaaloxiden in gasgevoelige materialen vanwege de hoge respons en goede stabiliteit [17,18,19]. In eerdere onderzoeken heeft SmFeO3 , wat een typisch p-type halfgeleidermetaaloxide is, vertoonde goede detectie, maar de gevoeligheid en stabiliteit zijn nog steeds onvoldoende [20, 21].
In dit werk, Sm2 O3 /ZnO/SmFeO3 microsferen werden bereid met een hydrothermische methode als een methanolgassensor en het effect van verschillende hydrothermische tijden werd bestudeerd (figuur 1). De gasdetectieresultaten van de Sm2 O3 /ZnO/SmFeO3 microsferen gaven uitstekende detectieprestaties aan voor methanolgas bij een relatief lage concentratie (5 ppm), bij een lage bedrijfstemperatuur (195 °C), korte responstijd (46 s) en hersteltijd (24 s) en bij een hoge relatieve vochtigheid ( 75% RV) met een hoge respons (119,8). De sensor vertoont ook een goede herhaalbaarheid en stabiliteit op lange termijn. Deze uitstekende detectieprestaties geven aan dat Sm2 O3 /ZnO/SmFeO3 is een veelbelovende kandidaat voor het detecteren van methanolgasmaterialen in de toekomst.
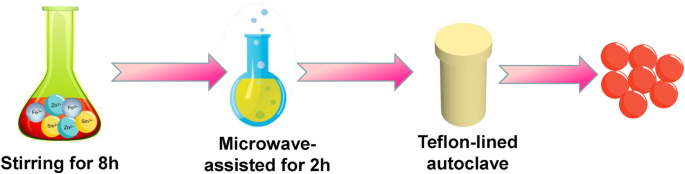
Schema van de voortgang van de voorbereiding van microsferen
Methodesectie
Materialen
Alle chemicaliën die in dit onderzoek werden gebruikt, waren analytisch van zuivere kwaliteit.
Synthese van Sm2 O3 /ZnO/SmFeO3 Microsferen
Het composiet werd gesynthetiseerd door middel van een door microgolven ondersteunde hydrothermische reactie. Eerst 4,44 g samariumnitraathexahydraat (Sm(NO3 )3 ·6H2 O), 4,04 g ijzernitraat-nonahydraat (Fe(NO3 )3 ·9H2 O), 0,09 g zinknitraat (Zn(NO3 )2 ·6H2 O) en 4,80 g citraat werden opgelost in 100 ml gedestilleerd water en geroerd totdat de oplossing helder werd. Vervolgens werd 2 g polyethyleenglycol (PEG) toegevoegd. Identieke oplossingen werden in viervoud bereid. De gemengde oplossing werd gedurende 8 uur krachtig geroerd bij 80 ° C en de suspensie werd gedurende 2 uur in een chemisch microgolfapparaat (CEM, VS) bij 75 ° C geplaatst. Vervolgens werd de oplossing in een met Teflon beklede autoclaaf gebracht en verwarmd van 25°C tot 180°C en 12 uur, 18 uur, 24 uur en 30 uur op 180°C gehouden. Om de organische stoffen te verwijderen, werd het verkregen ijzerrode precipitaat verschillende keren gewassen met gedeïoniseerd water via centrifugeren, en vervolgens werd het 72 uur gedroogd bij 60°C en 2 uur gecalcineerd bij 700°C. De producten, S1 (12 h), S2 (18 h), S3 (24 h) en S4 (30 h), werden uiteindelijk bereid.
Karakterisering
De structuren van de monsters werden gekarakteriseerd met behulp van XRD (D/max-2300, Cu Kα1, λ = 1.54056 Å, 35 kV). De monsters werden gescand van 10 tot 90° (2θ). De morfologie en deeltjesgrootte werden onderzocht met veldemissie scanning elektronenmicroscopie (FESEM). De microstructuren van de monsters werden onderzocht met transmissie-elektronenmicroscopie (TEM) en transmissie-elektronenmicroscopie met hoge resolutie (HRTEM) via een JEM-2100-microscoop die werkte bij 200 kV. Energiedispersieve röntgenspectroscopie (EDS) werd verkregen met behulp van de TEM-bevestiging. Röntgenfoto-elektronspectroscopie (XPS) werd gemeten op een XPS van Thermo Fisher Scientific Co. Ltd. bij 1486,6 eV. De specifieke oppervlakten werden berekend door de Brunauer-Emmett-Teller (BET) vergelijking op basis van de stikstofadsorptie-desorptie-isotherm opgenomen met een Quadrasorb evo-instrument (Quantachrome Co. Ltd.) bij 77 K (oppervlakte en porositeitssysteem).
Vervaardiging en meting van gassensoren
Gassensoren zijn vervaardigd volgens de literatuur [22]. In het algemeen werden as-gesynthetiseerde monsters grondig gedispergeerd in gedeïoniseerd water om een homogene pasta te vormen en vervolgens gecoat op het oppervlak van een keramische buis. Een spoelverwarmer van een Ni-Cr-legering werd als verwarming in de keramische buis gestoken om de bedrijfstemperatuur te regelen door de verwarmingsspanning aan te passen. De gassensoren werden gedurende 1 week in de lucht gerijpt bij 150°C om de stabiliteit en herhaalbaarheid van de sensoren te verbeteren. De gasdetectieprestaties van de sensoren werden gemeten door een WS-30A gassensormeetsysteem. Metingen van de gasdetectieprestaties werden uitgevoerd in een statisch systeem onder laboratoriumomstandigheden.
De parameters van de gassensor omvatten de respons, selectiviteit, respons- en hersteltijd en de optimale werktemperatuur. De gasrespons van een p-type gassensor wordt beschreven als:
$$ S={R}_{\mathrm{g}}/{R}_{\mathrm{a}} $$ (1)waar R g vertegenwoordigt de weerstand in doelgassen en R een vertegenwoordigt dat in de lucht. Onder dezelfde omstandigheden werden ook andere gassen getest om de selectiviteit van de gassensor te onderzoeken. De respons- en hersteltijd werden gedefinieerd als de tijd die de sensor nodig heeft om 90% van de totale weerstandsverandering te bereiken in het geval van respectievelijk adsorptie en desorptie. Gasadsorptie-/desorptieprocessen aan het oppervlak worden grotendeels beïnvloed door de werktemperatuur en de hoogste respons wordt vertoond bij de optimale werktemperatuur.
De gasconcentratie die wordt verkregen met de statische distributiemethode voor vloeibaar gas wordt bepaald door het volgende te berekenen:
$$ C=\frac{22.4\times \phi \times \rho \times {V}_1}{M\times {V}_2}\times 1000 $$ (2)Resultaten
Structurele en morfologische kenmerken
Het röntgendiffractiepatroon van gesynthetiseerd S1, S2, S3 en S4 wordt weergegeven in figuur 2a en de overeenkomstige EDS-elementaire mapping van S3 wordt getoond in figuur 2b. De belangrijkste diffractiepieken van de monsters verkregen met verschillende hydrothermische tijden worden toegewezen aan SmFeO3 (PDF#74-1474) met een hoge kristalliniteit. Drie andere diffractiepieken zijn aanwezig bij 2θ = 28,254°, 32,741° en 55,739°, die respectievelijk kunnen worden toegewezen aan (222, 400) en (622); deze resultaten komen overeen met de standaard XRD-patronen van Sm2 O3 (PDF#42-1461). Er is geen piek voor ZnO waargenomen in de XRD-spectra vanwege de lage concentratie ZnO; in Fig. 2b wordt echter duidelijk elementair Zn waargenomen naast de elementen van Sm, Fe en O, die ook worden getoond in de EDS-toewijzing. Er werden geen andere diffractiepieken waargenomen die overeenkomen met onzuiverheden, wat erop wees dat het monster een mengsel was van Sm2 O3 en SmFeO3 met hoge zuiverheid.
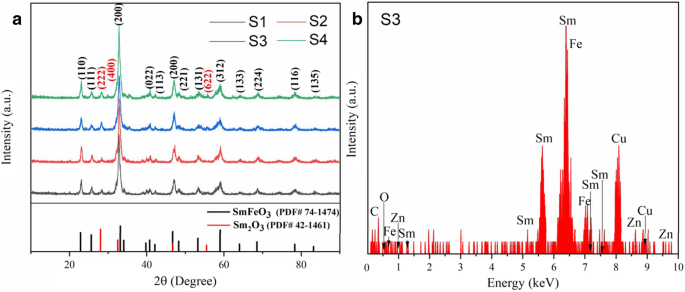
een XRD-patroon van S1, S2, S3 en S4. b EDS-spectrum van S3
SEM-afbeeldingen met een lage vergroting worden getoond in Fig. 3 (a1-d1), die een panorama vertonen van respectievelijk de verkregen S1, S2, S3 en S4. Zoals te zien is in de vier afbeeldingen, zijn de diameters van de verkregen Sm2 O3 /ZnO/SmFeO3 microsferen waren ongeveer 2-3 m en geen andere morfologische kenmerken duidden op perfecte uniformiteit of dispergeerbaarheid van de monsters. Afbeelding 3(b1-b4) toont vergrote SEM-afbeeldingen van de monsters. Naarmate de hydrothermische tijd toenam, nam het contactoppervlak van de microsfeer toe, wat leidde tot de vermindering van speciale plaatsen op het oppervlak.

Verschillende resolutie SEM-afbeeldingen van S1 (a1 –a3 ), S2 (b1 –b3 ), S3 (c1 –c3 ), en S4 (d1 –d3 ). e Schematisch diagram van het vormingsproces van S1 tot S4
Bovendien worden vergrote SEM-afbeeldingen van de oppervlakken van S1, S2, S3 en S4 getoond in Fig. 3 (c1-c4). De oppervlakken van de vier monsters waren ruw met een groot aantal nanodeeltjes. De ruimte tussen aangrenzende nanodeeltjes was duidelijk zichtbaar, vooral in figuur 3(c3) en figuur 3(d3). Dit fenomeen geeft aan dat de ruwheid toenam naarmate de tijd van de hydrothermische behandeling toenam, wat zou kunnen resulteren in een toename van het specifieke oppervlak (figuur 3e). Het ruwe oppervlak met poriën verbeterde het specifieke oppervlak aanzienlijk, wat de respons effectief verbeterde vanwege het toegenomen aantal actieve sites. Gecombineerd met de conclusie van Fig. 3b en Fig. 3d, was BET nodig om te bepalen welk monster het grootste oppervlak had.
Het specifieke oppervlak en het poriënvolume zijn belangrijke factoren voor gasdetectieprestaties. Dus de N2 adsorptie-desorptie-isothermen werden ook gemeten, zoals weergegeven in Fig. 4. Zoals waargenomen, de N2 adsorptie-desorptie-isothermen van de vier monsters werden geïndexeerd op de P/P0 as, die een typische type III-isotherm vertegenwoordigt met een H3-hysteresislus [23]. N2 adsorptie nam sterk toe wanneer de relatieve druk P . was /P 0 = 0,8. De twee isothermen waren bijna lineair bij lage druk (0,2-0,8), wat aangeeft dat alle monsters macroporeuze adsorptie hadden. De typische omkeerbare isothermen geven aan dat alle monsters spleetvormige poriën vertonen. Volgens de poriegrootteverdelingen werd de gemiddelde poriegrootte berekend op 31,077 nm voor S1, 31,046 nm voor S2, 26,398 nm voor S3 en 32,339 nm voor S4 (tabel 1.). Het oppervlak werd sterk beïnvloed door de hydrothermale tijd; het oppervlak van S3 was 27,579 m 2 /g, wat duidelijk hoger was dan die van andere monsters (oppervlakken van S1, S2 en S4 waren 21,159 m 2 /g, 26.150 m 2 /g, en 20.714 m 2 /g, respectievelijk). De INZET-resultaten zijn consistent met de detectie-eigenschappen. Een groot oppervlak kan zorgen voor meer actieve plaatsen en een groot porievolume, waardoor de gasdiffusie wordt verbeterd. Als gevolg hiervan zijn de gasprestaties aanzienlijk verbeterd.
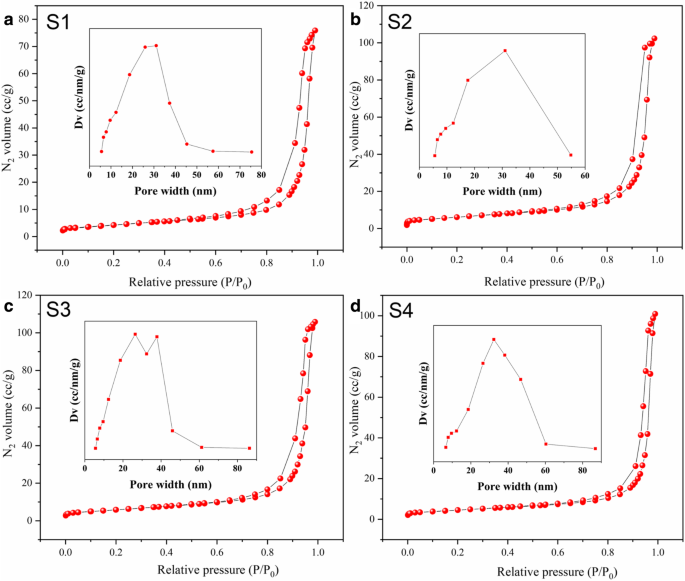
Stikstofadsorptie-desorptie-isothermen en bijbehorende poriegrootteverdelingscurven van S1 (a ), S2 (b ), S3 (c ), en S4 (d )
Voor de verdere karakterisering is gekozen voor S3 omdat deze het grootste oppervlak heeft. Het TEM-beeld toont de structuur van S3, die bestaat uit nanodeeltjes met een grootte van ongeveer 26 nm (figuur 5b); dit geeft aan dat de microsferen zelf-geassembleerd waren door nanodeeltjes. Het HRTEM-onderzoek gaf meer inzicht in de structurele kenmerken van de S3-microsfeer, die wordt getoond in figuur 5c. De interplanaire afstanden werden geschat op 0,276 nm, 0,260 nm en 0,321 nm, wat overeenkomt met het (200) vlak van SmFeO3 , het (002) vlak van Sm2 O3 , en het (222) vlak van ZnO, respectievelijk (Fig. 5c inzet). De elementtoewijzing in Fig. 5d, e, f en g geeft de uniforme verdeling van respectievelijk Sm, Fe, Zn en O weer. Het is duidelijk dat de hoeveelheid Zn relatief minder was dan die van andere elementen.

een , b TEM-afbeeldingen en c HRTEM-beelden van S3. STEM-elementtoewijzing van S3 voor Sm (d ), Fe (e ), Zn (f ), en O (g )
De XPS-analyse van S3 wordt getoond in Fig. 6. Zoals getoond in Fig. 6a, komen twee pieken in 1082,9 eV en 1109.9 eV overeen met Sm 3+ 3d5/2 en 3d3/2 , respectievelijk. Afbeelding 6b geeft het XPS-spectrum van Fe 2p weer met pieken bij 724,1 eV en 710,2 eV die Fe 3+ vertegenwoordigen 2p1/2 en Fe 3+ 2p3/2 , respectievelijk. De pieken bij 1044,4 eV en 1021,3 eV worden toegewezen aan Zn 2+ 2p1/2 en Zn 2+ 2p3/2 , die respectievelijk het bestaan van Zn 2+ . bevestigen in de composiet; dit bevestigde verder de TEM-resultaten. De splitsing van de 2p was 23,1 eV, wat in overeenstemming is met de energiesplitsing die is gerapporteerd voor ZnO en overeenkomt met de 2p-bindingsenergie van Zn (II). De geabsorbeerde zuurstofsoort speelt een belangrijke rol in halfgeleiders in het gasdetectieproces [24]. XPS-analyses kunnen de verhouding van geadsorbeerde zuurstofsoorten bevestigen; dus XPS met hoge resolutie van O 1 s voor de monsters werd onderzocht en de resultaten worden getoond in Fig. 6d. Zoals weergegeven in figuur 6d, zijn er twee pieken toegeschreven aan O 1s. De piek bij 531,4 eV komt overeen met \( {\mathrm{O}}_2^{-} \) in vier monsters, wat staat voor geabsorbeerde zuurstof (\( {\mathrm{O}}_2^{-} \)) op de oppervlak van materialen. Bovendien komen de chemische bindingsenergieën bij 529,3 eV, 529,2 eV, 529,0 eV en 529,2 eV overeen met roosterzuurstof (O 2− ) in respectievelijk S1, S2, S3 en S4. Het is duidelijk dat de spectra van O 1 laten zien dat het gehalte aan geadsorbeerde zuurstof van S3 hoger is dan dat van S1, S2 en S4, wat voornamelijk werd toegeschreven aan het grote oppervlak en verschillende hydrothermische tijden. Verschillende tijden voor de hydrothermische reactie hebben enorme effecten op de hoeveelheid m-O (m = Sm, Fe en Zn). Een hogere verhouding van \( {\mathrm{O}}_2^{-} \)/\( {\mathrm{O}}^{2^{-}} \) kan de gasdetectieprestaties aanzienlijk verbeteren [25 ]. In theorie is een sensor op basis van S3 een potentieel kandidaatmateriaal voor een gassensor.
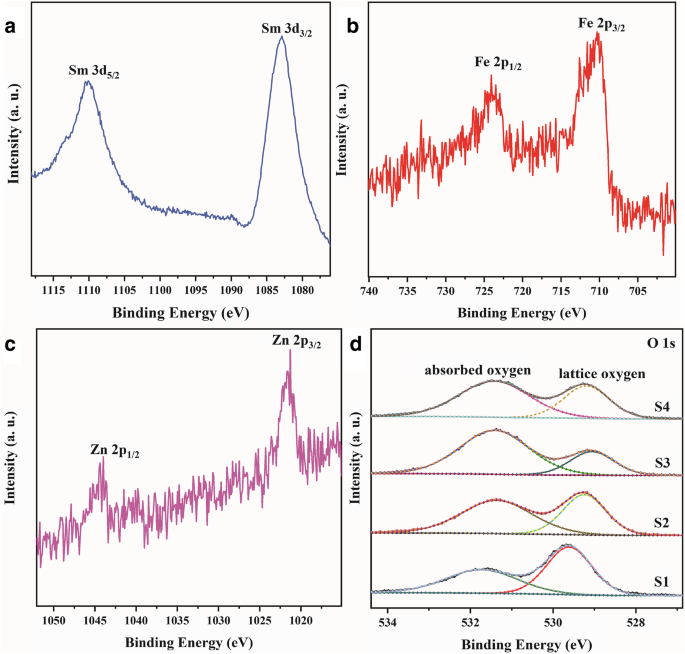
XPS-spectra met hoge resolutie van Sm (a ), Fe (b ), Zn van S3 (c ), en O 1 s van S1, S2, S3 en S4 (d )
Resultaten en discussie
Sm2 O3 /ZnO/SmFeO3 microsferen werden gesynthetiseerd als een potentieel detectiemateriaal voor gas en de gasdetectieprestaties van S1, S2, S3 en S4 werden onderzocht. Over het algemeen worden de reacties van sensoren sterk beïnvloed door de temperatuur, en Fig. 7 toont de reacties van S1, S2, S3 en S4 tot 5 ppm methanol gemeten bij verschillende bedrijfstemperaturen (variërend van 125 tot 295 °C). De maximale responswaarden van S1, S2, S3 en S4 waren respectievelijk 22,0, 54,3, 119,8 en 19,9 bij 195 °C. De respons van S3 was 5,4 keer hoger dan die van S1, 2,2 keer hoger dan die van S2 en 5,9 keer hoger dan die van S4 bij dezelfde temperatuur. Daarom werd 195 °C gekozen als de optimale bedrijfstemperatuur van de sensoren voor de volgende gasdetectietests. Bij een bedrijfstemperatuur onder de 195 °C nam de respons aanzienlijk toe. Daarentegen nam de respons af naarmate de bedrijfstemperatuur verder steeg. De reacties van de sensoren namen aanvankelijk sterk toe met de bedrijfstemperatuur, wat te wijten was aan twee redenen. Ten eerste veranderde de soort geadsorbeerde zuurstof met de bedrijfstemperatuur op het oppervlak van het materiaal. Ten tweede, naarmate de temperatuur toenam, kon het gasmolecuul de activeringsenergiebarrière van de oppervlaktereactie overwinnen [26]. Daarna nam de respons af met toenemende bedrijfstemperatuur. De reden voor dit fenomeen kan te wijten zijn aan de daling van het aantal actieve plaatsen voor methanoladsorptie met de toenemende temperatuur. De andere reden kan zijn dat het adsorptievermogen lager is dan dat van de desorptie van methanolmoleculen, wat leidt tot inferieure prestaties van het meetmateriaal bij hoge temperatuur. De S3-sensor vertoonde een superhoge respons op methanolgas, wat aangeeft dat Sm2 O3 /ZnO/SmFeO3 microsferen die een hydrothermische tijd van 24 uur ondergaan, kunnen een potentieel methanolgasdetectiemateriaal zijn.
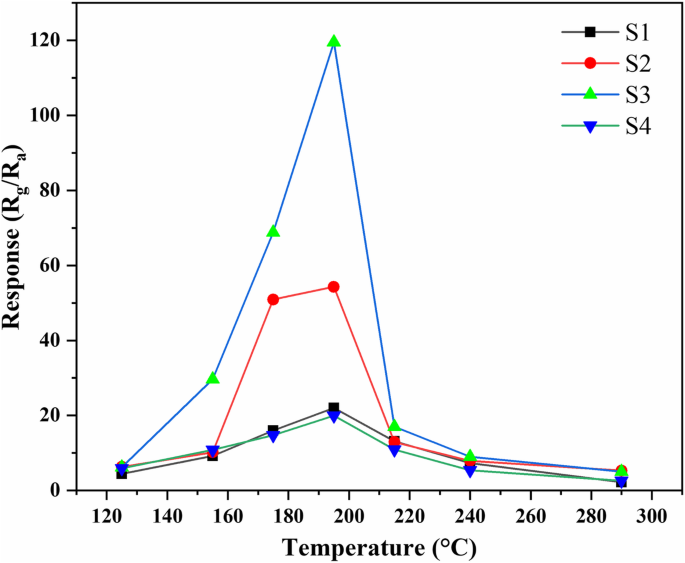
Relatie tussen respons en bedrijfstemperatuur tot 5 ppm methanol op basis van S1, S2, S3 en S4
Om methanolgas beter te onderscheiden van andere gassen, werd de respons op verschillende gassen bij 5 ppm, waaronder aceton, formaldehyde, ammoniak, benzine en benzeen bij 195 °C gemeten om de selectiviteit van S1, S2, S3 en S4 te onderzoeken. in Fig. 8a, b, c en d. Er kan worden waargenomen dat de respons op 5 ppm methanol 119,8 is, terwijl de respons op aceton, formaldehyde, ammoniak, benzine en benzeen respectievelijk 64,1, 17,2, 15,9, 23,0 en 24,8 is. De responskloof tussen methanol en aceton reikt tot 55,7, het is hoog genoeg om andere gassen te onderscheiden voor een methanolgassensor.
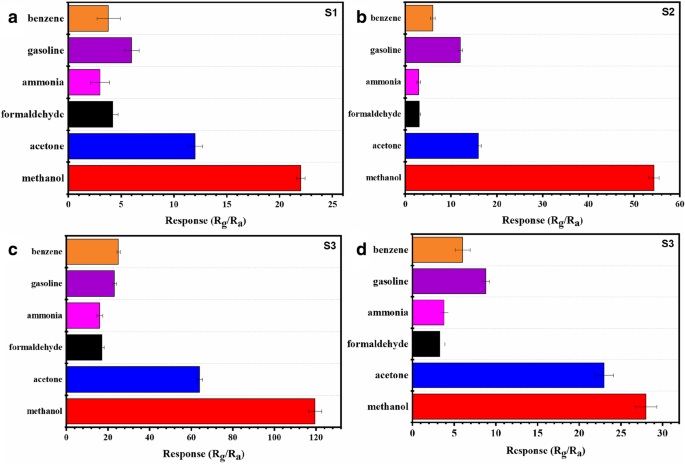
Selectiviteit van microbolletjes op verschillende hydrothermische tijden op basis van S1 (a ), S2 (b ), S3 (c ), en S4 (d ) op verschillende gassen met een concentratie van 5 ppm bij 195 °C
Dynamische responstransiënten van S1, S2, S3 en S4 op verschillende methanolgasconcentraties worden weergegeven in figuur 9a. Zoals getoond, waren de responsen van S3 ongeveer 19,8, 40,6, 85,2, 101,3 en 119,8 voor methanolgas bij respectievelijk 1, 2, 3, 4 en 5 ppm. Bovendien vertoonden de andere drie sensoren ook respons- en herstelkenmerken op verschillende concentraties methanolgas, variërend van 1 tot 5 ppm. Er is een verband tussen de respons en de concentratie van de vier sensoren op methanolgas, zoals weergegeven in figuur 9b. De respons van alle sensoren nam toe met toenemende methanolgasconcentratie van 1 tot 5 ppm; in het bijzonder nam de respons van S3 sterk toe met een toename van de concentratie. Het is duidelijk dat de respons significant verbeterde voor S3, zelfs bij lage concentraties methanol (de respons was 19,8 zelfs bij 1 ppm methanol). De theoretische detectielimiet wordt berekend via de kleinste-kwadratenmethode [34]. Volgens het resultaat van het passen in het lineaire regime, is de helling 25,24 en een passende kwaliteit R 2 = 0,972. Honderddertig gegevens werden opnieuw geplot op de basislijn van de sensor in de lucht; dus met behulp van de wortel-gemiddelde-kwadraatdeviatie (RMSD) (1) kan de sensorruis worden berekend.
$$ {\mathrm{RMS}}_{\mathrm{noise}}=\sqrt{\frac{S^2}{N}}=0.0219 $$ (3)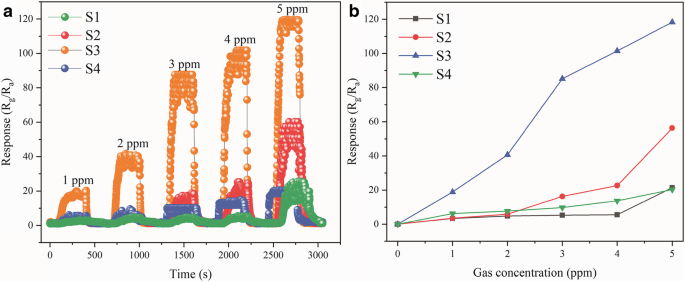
een Dynamische responstransiënten van S1, S2, S3 en S4 op methanolgas bij lage concentratie bij 195 °C. b Verband tussen respons en concentratie van S1, S2, S3 en S4 tot verschillende methanolgasconcentraties (1 ppm, 2 ppm, 3 ppm, 4 ppm en 5 ppm) bij 195 °C
De sensorruis is 0,0219 van de vergelijking. De punten werden gemiddeld en een standaarddeviatie (S) werd verzameld als 0,062.
De theoretische detectielimiet is ongeveer 7,37 ppb van Vgl. (4):
$$ \mathrm{DL}=3\frac{{\mathrm{RMS}}_{\mathrm{noise}}}{S\mathrm{lope}}=7.37\ \mathrm{ppb} $$ (4)Het grote oppervlak van S3 biedt voldoende actieve sites om tot een snelle respons te leiden. Wanneer de sensor werd blootgesteld aan lucht, daalde de respons onmiddellijk naar de oorspronkelijke staat. De tijd die nodig was voor dit proces was slechts 24 s, wat kwam door de desorptie van methanolgasmoleculen en zuurstof geabsorbeerd op het oppervlak van het materiaal. De omkeerbare cycli en respons (voor 4 cycli) van S3 tot 5 ppm methanolgas bij 195 ° C werden onderzocht, wat wordt weergegeven in Fig. 10b. De responsen van S3 waren 121,40, 122,10, 124,80 en 121,40 onder dezelfde omstandigheden, wat de superieure reproduceerbaarheid van S3 aantoont. Om de invloed van vochtigheid te bestuderen, werd de S3-respons op 5 ppm methanolgas bij 195 °C bij een hoge luchtvochtigheid onderzocht, zoals weergegeven in Fig. 10c. De reacties van S3 op 5 ppm methanolgas in 55% (RH), 60% (RH), 65% (RH) en 70% (RH) waren respectievelijk 124, 118, 112, 109 en 107. De afwijking in de respons was slechts 17 in het bereik van 55 tot 70% RV. De S3-gassensor vertoonde een goede stabiliteit, zelfs onder een zeer vochtige atmosfeer, wat duidt op vochtigheidsonafhankelijke gasdetectie voor S3. De langetermijnstabiliteit van S3 tot 5 ppm methanolgas bij 195 ° C werd gemeten (figuur 10d). De reactie van de S3-sensor op 5 ppm methanol bij 195 °C in de 30-dagentest kon worden genegeerd. De uitstekende stabiliteit op de lange termijn was een aanvullend bewijs voor de toepassing ervan in de industrie.
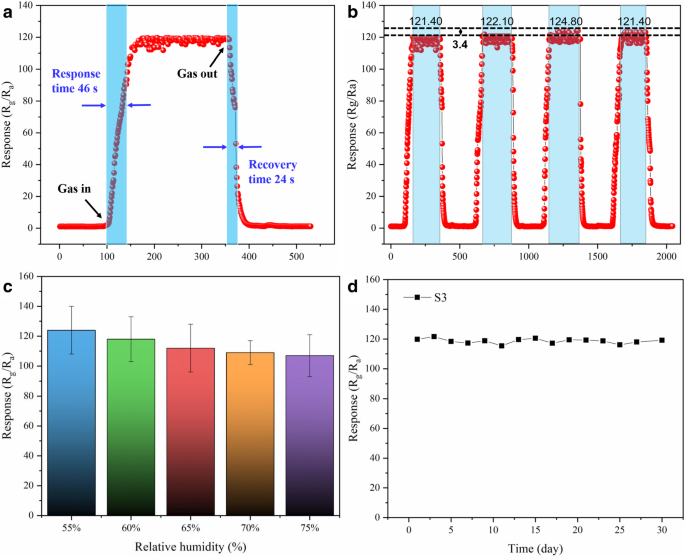
een Respons- en herstelcurve van het S3 tot 5 ppm methanolgas bij 195 °C. b Omkeerbaarheid van S3 tot 5 ppm methanolgas bij 195 °C onder 4 cycli. c De relatie tussen respons en relatieve vochtigheid op 5 ppm methanolgas van S3. d Stabiliteit van S3 tegen 5 ppm methanolgas gedurende 30 dagen bij 195 °C
Vochtigheidsinterferentie is een belangrijke parameter voor gasdetectieprestaties, omdat de adsorptie van watermoleculen kan leiden tot minder chemisorptie van zuurstofsoorten op het oppervlak [31]. Sm2 O3 nanodeeltjes spelen een vitale rol bij het opruimen van hydroxylgroepen (OH) op het oppervlak, waarbij een waarneembare reactie wordt gehandhaafd door de zuurstofionen-opname te ondersteunen [35].
Het is bekend dat de capaciteiten van geadsorbeerde zuurstofsoorten nauw samenhangen met de gasdetectie-eigenschappen van halfgeleidende oxiden (tabel 2). Wanneer de gassensor in omgevingslucht werkt, absorberen zuurstofmoleculen aan het oppervlak (\( {\mathrm{O}}_2^{-} \), O − , en \( {\mathrm{O}}^{2^{-}} \)) van materialen en vangt elektronen op, waardoor de elektronenconcentratie afneemt en de gatenaccumulatielaag van het oppervlaktemateriaal toeneemt; dit veroorzaakt een daling van de sensorweerstand. Als een typische p-type halfgeleider die wordt blootgesteld aan een oxiderend gas, zoals O2 , de verschillende soorten zuurstofsoorten zijn verschillend bij verschillende temperaturen. De relatie tussen temperatuur en zuurstofsoort is als volgt [36]:
$$ {\mathrm{O}}_{2\left(\mathrm{g}\right)}\leftrightarrow {\mathrm{O}}_{2\left(\mathrm{ads}\right)} $$ (5) $$ {\mathrm{O}}_{2\left(\mathrm{ads}\right)}+{e}^{-}\to {\mathrm{O}}_{2\left( \mathrm{ads}\right)}^{-}\left(<100{{}^{\circ}\mathrm{C}}\right) $$ (6) $$ {O}_{2\left (\mathrm{ads}\right)}^{-}+{e}^{-}\to 2{O}_{\left(\mathrm{ads}\right)}^{-}\left(100 {{}^{\circ}\mathrm{C}}-300{{}^{\circ}\mathrm{C}}\right) $$ (7) $$ {O}_{\left(\mathrm {ads}\right)}^{-}+{e}^{-}\to {O}_{\left(\mathrm{ads}\right)}^{2-}\left(>300{{ }^{\circ}\mathrm{C}}\right) $$ (8)Terwijl de sensor wordt blootgesteld aan een reducerend gas (zoals methanolgas), reageren de methanolgasmoleculen met de geabsorbeerde zuurstof op het materiaaloppervlak, en dit zal ertoe leiden dat elektronen van geadsorbeerde zuurstofsoorten terug naar de halfgeleider worden afgegeven, wat resulteert in een afname van de geleidbaarheid. De reactie tussen methanolgasmoleculen en geadsorbeerde zuurstof kan worden beschreven als (9):
$$ {\mathrm{CH}}_3{\mathrm{O}\mathrm{H}}_{\left(\mathrm{gas}\right)}+3{\mathrm{O}}_{\left( \mathrm{ads}\right)}^{n-}\to {\mathrm{CO}}_2+{\mathrm{H}}_2\mathrm{O}+3{ne}^{-} $$ (9 )Volgens de bovenstaande resultaten vertoonde de S3-sensor uitstekende gasdetectieprestaties voor 5 ppm methanolgas. Een schematisch diagram van de Sm2 O3 /ZnO/SmFeO3 pn heterojunctie wordt getoond in figuur 11. De vorming van een pn heterojunctie is een reden voor de verbeterde detectie-eigenschappen. ZnO is een n-type halfgeleider en SmFeO3 is een p-type halfgeleider, en bij het combineren van ZnO en SmFeO3 , wordt een pn-heterojunctie gevormd tussen het oppervlak van de twee soorten metaaloxiden. De elektronen gaan van ZnO naar SmFeO3 , terwijl de gaten overgaan in de tegenovergestelde richting vanwege de verschillende Fermi-niveaus totdat een evenwicht in het Fermi-niveau en de elektronendepletielaag ontstaat op het grensvlak van de heterojunctie [37].
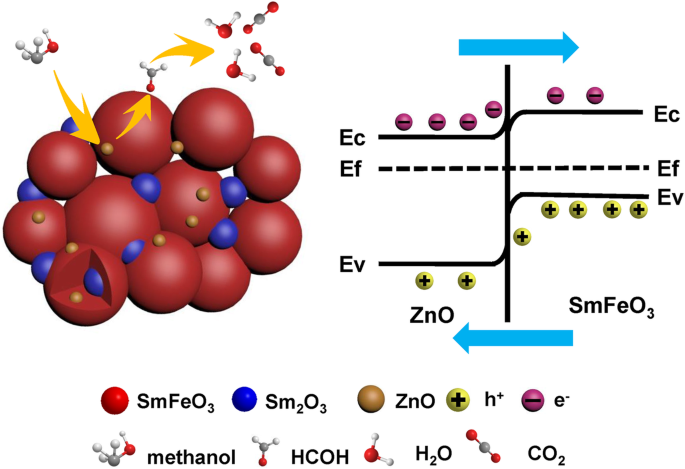
Het schematische diagram van Sm2 O3 /ZnO/SmFeO3 p-n heterojunctie
Het doelgas (methanol) reageert met de geadsorbeerde zuurstof op het oppervlak van ZnO, waardoor elektronen terugkeren. De reacties op het grensvlak van de heterojunctie worden getoond in (10-11) [38]:
$$ {\mathrm{CH}}_3\mathrm{OH}+{\mathrm{O}}^{-}\left({\mathrm{O}}^{2^{-}}/{\mathrm{ O}}_2^{-}\right)\to \mathrm{HCHO}+{\mathrm{H}}_2\mathrm{O}+{e}^{-} $$ (10) $$ \mathrm{ HCHO}+{\mathrm{O}}^{-}\left({\mathrm{O}}^{2-}/{\mathrm{O}}_2^{-}\right)\to {\mathrm {CO}}_2+{\mathrm{H}}_2\mathrm{O}+{e}^{-} $$ (11)Bovendien, het methanolgas met het gat in SmFeO3 produceert het tussenproduct HCHO en reageert verder met geadsorbeerde zuurstof op het oppervlak van p-type SmFeO3 op het grensvlak tussen de heterojunctie (11–12):
$$ {\mathrm{CH}}_3\mathrm{OH}+{h}^{+}+{\mathrm{O}}^{-}\left({\mathrm{O}}^{2-} /{\mathrm{O}}_2^{-}\right)\to \mathrm{HCHO}+{\mathrm{H}}_2\mathrm{O} $$ (11) $$ \mathrm{HCHO}+ {h}^{+}+{\mathrm{O}}^{-}\left({\mathrm{O}}^{2-}/{\mathrm{O}}_2^{-}\right) \naar {\mathrm{CO}}_2+{\mathrm{H}}_2\mathrm{O}+{e}^{-} $$ (12)Daarom trekt het pn-heterojunctie-interface tussen de twee soorten metaaloxiden gemakkelijk reductieve en oxidatieve gassen aan. Er wordt een diepere elektronenuitputtingslaag gevormd, wat leidt tot verbeterde waarnemingsprestaties.
Naast de vorming van een p-n heterojunctie, werd ook het grote specifieke oppervlak en de hoge hoeveelheid geadsorbeerde zuurstof toegeschreven aan het verbeteren van de detectieprestaties. De volgorde van het specifieke oppervlak was S3 > S2 > S1 > S4, en de waarnemingsreacties van de vier sensoren waren in dezelfde volgorde. This indicates that a large specific surface area is beneficial for sensing response, which provides more active sites for both the target gas and oxygen molecules and favors the surface catalytic reaction. S3 exhibits a higher ratio of \( {\mathrm{O}}_2^{-} \)/O 2− than S1, S2, and S4, and the results indicated that S3 had the highest ability for adsorbing ionized oxygen species, which may contribute to increasing the sensing performance [39].
Conclusion
In this report, Sm2 O3 /ZnO/SmFeO3 microspheres were successfully synthesized as a methanol gas sensor, and we investigated the effect of different hydrothermal reaction times on the microstructure. The BET and XPS results reveal that different hydrothermal reaction times significantly influence the specific surface area and adsorbed oxygen species, which have a huge effect on the gas-sensing performance. The p-n heterojunction is another important reason for the enhanced performance. When the hydrothermal reaction time was 24 h, the sensor exhibited the highest performance for methanol gas. The response of the Sm2 O3 /ZnO/SmFeO3 microsphere reached 119.8 for 5 ppm of methanol gas at 195 °C in a relatively high humidity atmosphere, and the response was higher than 20 even at 1 ppm of methanol gas. In addition, the sensor also shows excellent repeatability and long-term stability only with a small deviation in the 30-day test. Therefore, a sensor based on Sm2 O3 /ZnO/SmFeO3 microspheres is a good choice for the detection of methanol gas.
Afkortingen
- BET:
-
Brunauer-Emmett-Teller
- DMFC:
-
Direct methanol fuel cells
- EDS:
-
Energiedispersieve röntgenspectroscopie
- FESEM:
-
Veldemissie scanning elektronenmicroscopie
- HRTEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- MOS:
-
Metal oxide semiconductors
- PEG:
-
Polyethyleenglycol
- RH:
-
Relative humidity
- TEM:
-
Transmissie-elektronenmicroscopie
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Hoogwaardige kunststoffen in de halfgeleiderindustrie
- Hoge fotokatalytische prestaties van twee soorten grafeen-gemodificeerde TiO2-composietfotokatalysatoren
- Zichtbare, door licht aangedreven fotokatalytische prestaties van N-gedoteerde ZnO/g-C3N4-nanocomposieten
- Vervaardiging en karakterisering van nieuwe composiet Tio2 koolstof nanovezel anodische katalysatorondersteuning voor directe methanolbrandstofcel via elektrospinmethode
- Synthese van sferisch zilver-gecoat Li4Ti5O12 anodemateriaal door een Sol-Gel-ondersteunde hydrothermische methode
- Na4Mn9O18/Carbon Nanotube-composiet als materiaal met hoge elektrochemische prestaties voor waterige natrium-ionbatterijen
- Hoge prestaties van PEDOT:PSS/n-Si-zonnecellen op basis van een gestructureerd oppervlak met AgNWs-elektroden
- Hydrothermisch gesynthetiseerd van CoMoO4-microsferen als uitstekend elektrodemateriaal voor supercondensator
- Verbetering van de prestaties van a-IGZO TFT-apparaten met behulp van een schoon interfaceproces via Etch-Stopper nanolagen
- Humaat-geassisteerde synthese van MoS2/C-nanocomposieten via co-precipitatie/calcineringsroute voor hoogwaardige lithium-ionbatterijen
- Draaien met hoge prestaties



