Titania nanobuisjes bereid door snelle afbraak anodisatie voor fotokatalytische ontkleuring van organische kleurstoffen onder UV en natuurlijk zonlicht
Abstract
Titania nanobuis (TNT) poeder werd bereid door snelle afbraak anodisatie (RBA) in een perchloorzuurelektrolyt. De fotokatalytische efficiëntie van de bereide en poeders gegloeid bij temperaturen tussen 250 en 550 ° C werd getest onder UV en natuurlijk zonlicht door ontkleuring van zowel anionische als kationische organische kleurstoffen, dwz methyloranje (MO) en rhodamine B (RhB) , als modelverontreinigende stoffen. De buisvormige structuur van de nanobuisjes bleef behouden tot 250 °C, terwijl bij 350 °C en hoger de nanobuisjes transformeerden in nanostaafjes en nanodeeltjes. Afhankelijk van de gloeitemperatuur bestaan de TNT's uit anatase-, gemengde anatase/brookiet- of anatase/rutielfasen. De bandgap van de voorbereide nanobuisjes is 3,04 eV en verschuift bij uitgloeien naar het zichtbare lichtgebied. De resultaten van röntgenfoto-elektronspectroscopie (XPS) tonen de aanwezigheid van titania en onzuiverheden, waaronder chloor, op het oppervlak van de TNT's. De atomaire verhouding van Ti/O blijft ongewijzigd voor de gegloeide TNT's, maar de chloorconcentratie neemt af met de temperatuur. De fotoluminescentie (PL) duidt op een hoge elektron-gat-recombinatie voor de bereide TNT's, waarschijnlijk vanwege de resterende onzuiverheden, lage kristalliniteit en vacatures in de structuur, terwijl de hoogste fotostroom werd waargenomen voor het TNT-monster dat was gegloeid bij 450 ° C. De TNT's veroorzaken een kleine afbraak van de kleurstoffen onder UV-licht; in tegenstelling tot eerdere rapporten wordt echter volledige ontkleuring van kleurstoffen waargenomen onder zonlicht. Alle TNT-monsters vertoonden hogere ontkleuringssnelheden onder bestraling met zonlicht dan onder UV-licht. De hoogste reactiesnelheid voor de TNT-monsters werd verkregen voor het als voorbereide TNT-poedermonster onder zonlicht met behulp van RhB (κ 1 = 1,29 u −1 ). Dit wordt toegeschreven aan de bandgap, het specifieke oppervlak en de kristalstructuur van de nanobuisjes. De zoals voorbereide TNT's presteerden het meest efficiënt voor ontkleuring van RhB en presteerden beter dan het referentie-anatasepoeder onder bestraling met zonlicht. Dit kan worden toegeschreven aan de overvloed aan reactieve plaatsen, een hoger specifiek oppervlak en het afbraakmechanisme van RhB. Deze RBA TNT-fotokatalysatorpoeders laten een efficiënter gebruik van het zonlichtspectrum zien, waardoor ze geschikt zijn voor milieusanering.
Achtergrond
Eendimensionale titanium nanobuisjes (TNT) hebben de afgelopen tien jaar veel aandacht gekregen. Ze zijn bestudeerd voor een aantal prospectieve toepassingen, vanwege hun veelbelovende elektrische en optische eigenschappen en hoge specifieke oppervlakte [1]. Het meest veelbelovende onderzoek naar TNT is gedaan voor gasdetectie, fotokatalyse, kleurstofgevoelige zonnecellen, elektrochrome apparaten en biomedische toepassingen [2]. TNT's kunnen worden gesynthetiseerd met verschillende methoden, waaronder elektrochemische anodisatie, hydrothermische verwerking, chemische verwerking, sjabloonondersteunde en sol-gelmethoden [1,2,3,4]. In sjabloonvrije methoden, Zwilling et al. [5] introduceerde de bereiding van TNT-arrays door elektrochemische anodisatie van titaniumfolie in 1999. Het onderzoek naar anodisatie van titanium is de morfologie en afmetingen van TNT-arrays blijven beheersen door parameters zoals elektrolyten, elektrolyt-pH, temperatuur, toegepaste potentiaal, stroomdichtheid en anodisatietijd [6, 7]. Het is echter tijdrovend om grotere batches TNT-arrays te maken om de arrays verder van het Ti-substraat af te pellen om poeders te verkrijgen [8]. Daarom werd een snellere methode ontwikkeld, snelle afbraak-anodisatie (RBA) genaamd, waarbij gebruik wordt gemaakt van chloride- en perchloraationen in een elektrolyt [7, 9]. In RBA wordt metallisch titanium binnen enkele seconden na het aanleggen van spanning omgezet in metaaloxide-nanobuisjes. Wanneer de spanning wordt aangelegd, groeit een dunne laag oxide op het oorspronkelijke oxide van het metaaloppervlak, dat snel wordt aangevallen door halogenide-ionen om de gelokaliseerde putjes op het metaaloppervlak te vormen [10]. Het putvormingsproces wordt beïnvloed door de aangelegde spanning, temperatuur en halogenideconcentratie [10]. Na pitting vormt zich de oxidelaag in de pits door de binnenwaartse migratie van O 2− ionen van de elektrolyt naar het metaaloppervlak [11]. De geoxideerde metaalionen (Ti 4+ ) migreren naar buiten, en de gevormde TiO2 laag wordt geëtst door de chloride-ionen om in water oplosbaar [TiCl6 . te vormen ] 2− ionen [9]. Nanobuisjes worden gevormd wanneer het evenwicht wordt gehandhaafd in de oxidegroei en het chemisch etsen van oxide [9, 11]. De bundels nanobuisjes groeien binnen enkele seconden in willekeurige richting rond de kuilen. Na verloop van tijd vallen de nanobuisjesbundels in de elektrolyt door hoge spanning tussen het metaal en de oxide nanobuisjes [9]. Het nanobuisjepoeder wordt vervolgens uit de elektrolyt verzameld [11]. TNT-poeders bereid door RBA zijn onderzocht voor een aantal potentiële toepassingen, zoals DSSC [12, 13], waterstofgeneratie [14,15,16,17,18,19], fotokatalytische afbraak van verontreinigende stoffen onder bestraling met UV-licht [20 ,21,22] en biomedische implantaten [23, 24].
Titaandioxide is gebruikt voor het verwijderen van organische verontreinigende stoffen uit de waterstroom, omdat het niet-toxisch, thermisch stabiel, goedkoop en gemakkelijk verkrijgbaar materiaal is [25]. TNT's zijn bestudeerd voor de fotokatalytische afbraak van organische verontreinigende stoffen in het water met behulp van verschillende kleurstoffen als modelverontreinigende stoffen [25,26,27]. TNT's hebben een hoog specifiek oppervlak en hebben een amorfe of kristallijne structuur, afhankelijk van het syntheseproces. De kristalstructuur kan worden gewijzigd door annealing waarbij tegelijkertijd de morfologie, bandgap, samenstelling en specifiek oppervlak van de nanobuisjes worden beïnvloed [3, 11]. De bandgap van de TNT's ligt naar verluidt in het bereik van 3,0-3,2 eV [2], afhankelijk van de kristalstructuur van de nanobuisjes. De kristalstructuur van de nanobuisjes is afhankelijk van de syntheseomstandigheden en kan worden aangepast aan de drie polymorfen van TiO2 , d.w.z. anataas, rutiel en brookiet. Anatase heeft een indirecte bandgap en heeft een langere elektron-gat-levensduur in vergelijking met de directe bandgap van de rutiel- en brookietfase [28]. Nanobuisjes zullen naar verwachting een verbeterde fotokatalytische efficiëntie hebben vanwege hun buisvormige morfologie, groter specifiek oppervlak en bredere bandgap [29] onder bestraling met UV-licht. Bijgevolg rapporteren een aantal onderzoeken de werkzaamheid van TNT-arrays voor de afbraak van organische kleurstoffen door bestraling met UV-licht [25,26,27]. Aangezien UV-licht slechts een klein deel van het zonlichtspectrum uitmaakt, vereist een efficiënter gebruik van zonne-energie voor milieusanering ook het gebruik van het zichtbare lichtbereik. TNT's zijn echter inefficiënte fotokatalysatoren onder bestraling met zichtbaar licht [29]. Om de fotokatalytische efficiëntie van TNT's in het zichtbare lichtbereik te verbeteren, worden hun elektronische eigenschappen meestal gewijzigd door anionische (niet-metaalionen) of kationische (metaalionen) dotering [27, 30,31,32].
In de huidige studie werden niet-gedoteerde TNT-poeders bereid door RBA en gedurende 3 uur aan de lucht onderworpen aan gloeien van 250 tot 550 ° C. De resulterende TNT-poeders worden onderzocht als fotokatalysatoren onder UV- en natuurlijke zonlichtbestraling door hun efficiëntie te bepalen door ontkleuring van Rhodamine B (RhB) en methyloranje (MO) kleurstoffen. De kleurstoffen zijn stabiel met unieke kleuren en zijn gebruikt in de papier-, textiel-, cosmetica- en fotografische industrie [20]. Er is een aantal fotokatalytische onderzoeken gedaan naar TNT-arrays [32]; er zijn echter slechts enkele rapporten gepresenteerd voor de fotokatalytische afbraak van organische verontreinigende stoffen door TNT-poeders bereid door RBA [20, 21, 33]. Voor zover wij weten, zijn er echter geen kleurstofafbraakonderzoeken uitgevoerd onder natuurlijk zonlicht voor TNT's die zijn bereid door RBA. In deze studie ontdekten we dat ongedoteerde TNT's bereid door RBA efficiënter zijn onder natuurlijk zonlicht dan onder UV-licht, en volledige ontkleuring van organische kleurstoffen wordt verkregen onder natuurlijke bestraling met zonlicht. Dit suggereert een efficiënt gebruik van het zonnespectrum voor milieusanering, zoals de zuivering van industrieel afvalwater.
Methoden/experimenteel
Voorbereiding van de TNT's
TNT-poeder werd bereid met 0,1 M HClO4 elektrolyt (Sigma-Aldrich, 70%) en een aangelegde spanning van 20 V zoals eerder beschreven [11]. De bereide en gegloeide poeders (250-550 °C, 3 uur) werden gekarakteriseerd om de morfologie, samenstelling, kristalstructuur en het specifieke oppervlak van de nanobuisjes te onderzoeken.
Karakterisatiemethoden
De morfologie werd onderzocht met transmissie-elektronenmicroscopie (TEM; Tecnai F-20G2 FEG S-twin GIF) bij een bedrijfsspanning van 200 kV. Röntgendiffractie (XRD) karakterisering werd uitgevoerd om de kristalstructuur van de TNT's te bestuderen met behulp van een PANalytical X'pert Pro diffractometer, en de metingen werden gedaan in twee theta-bereik van 20°-110° bij een bedrijfsspanning van 40 kV en stroom van 40 mA, door gebruik te maken van Co-Kα-straling met een golflengte van 0,179 nm. Raman-spectroscopie werd verkregen met behulp van een Labram HR Raman-spectrometer van Horiba Jobin-Yvon, uitgerust met argonlaseropwinding van 514 nm bij 50 mW. De meting werd uitgevoerd op de TNT-poeders met een objectief van × 50 (Olympus BX41). UV /Vis/NIR-spectroscopie werd gebruikt om de absorptiespectra te verkrijgen voor de berekening van de bandgap-energieën. Diffuse reflectiespectroscopie (DRS) metingen werden uitgevoerd met behulp van een Agilent Cary 5000-apparatuur met een integrerende bol. De meting werd uitgevoerd in het bereik van 200-800 nm en een gekalibreerd monster van Spectralon werd gebruikt voor de basislijncorrectie. Fourier-transformatie-infraroodspectroscopie (FTIR) is uitgevoerd in de modus voor verzwakte totale reflectie (ATR) in het spectrale bereik van 525–4000 cm −1 , met een resolutie van 4 cm −1 , met een Nicolet 380 FTIR. Röntgenfoto-elektronspectroscopie (XPS) werd gebruikt om de chemische samenstelling van het oppervlak te analyseren. De metingen zijn gedaan met behulp van het Kratos Analytical AXIS Ultra-systeem, uitgerust met een monochromatische Al Kα (1486,6 eV) röntgenbron en C 1s (284,8 eV) werd gebruikt als de bindingsenergiereferentie. Fotoluminescentiespectroscopie (PL) van de TNT-poeders werd uitgevoerd met behulp van een Perkin Elmer LS 50B luminescentiespectrometer uitgerust met een 20 W Xenon-lamp met een excitatie van 330 nm.
Voor fotostroomkarakterisering werden elektroden bereid door afzetting van TNT-film op met fluor gedoteerd tinoxide (FTO) glas. De films werden bereid door druppelgieten met behulp van een suspensie van de TNT-poeders in ethanol op het FTO-glas, gevolgd door 20 minuten drogen in een oven bij 70 ° C in de lucht. Enkele druppels Nafion (Sigma-Aldrich; 5 gew.% in lagere alifatische alcoholen en water) werden op de film toegevoegd en het monster werd opnieuw 20 minuten in een oven bij 70 ° C aan de lucht gedroogd. De karakterisering van de fotostroom werd gedaan bij een spanning van 500 mV met behulp van Jaissle IMP83 PC-T-BC-potentiostaat. De metingen werden uitgevoerd met behulp van een opstelling met drie elektroden met behulp van een Ag / AgCl-referentie-elektrode, Pt als een tegenelektrode en de TNT-film afgezet op FTO-glas als een werkelektrode. 0,1M Na2 SO4 (Sigma-Aldrich; -99,0%) werd als elektrolyt gebruikt. De monsters werden bestraald met een Oriel 6365 150 W Xe-lamp in het bereik van 250-600 nm, waarbij de invallende golflengte werd gekozen met behulp van een Oriel Cornerstone 130 1/8 m monochromator. Elektrochemische impedantiespectroscopie (EIS) werd uitgevoerd met behulp van een Gamry Referece 600+ potentiostaat (Gamry Instruments). Bij de metingen werd een opstelling met drie elektroden met een Ag/AgCl-referentie-elektrode (+-0,199 V vs RHE, radiometer analytisch), TNT-werkelektrode en een Pt-draadtegenelektrode gebruikt. EIS werd gebruikt om elektronenoverdracht te bestuderen met de buitenste bol redox-sonde Ru(NH3 )6 2 +/3 + (5 mM in 1 M KCl). EIS werd uitgevoerd van 200 kHz tot 100 mHz met een AC-signaal van 15 mV. De formele potentiaal zoals bepaald met cyclische voltammetrie werd gebruikt als DC-potentiaal in de metingen. Alle metingen zijn uitgevoerd bij kamertemperatuur.
Fotokatalyse van TNT's
De fotokatalytische efficiëntie van de TNT-poeders werd onderzocht door ontkleuring van waterige oplossingen van anionische methyloranje (MO, Fluka, Reag. Ph. Eur) en kationische rhodamine B (RhB, Sigma, ~ 95%) kleurstoffen als modelverontreinigingen onder UV en zonlicht bestraling. De schematische illustratie van de fotokatalytische ontkleuring van de MO- en RhB-kleurstoffen met behulp van TNT's als katalysatoren wordt getoond in Fig. 1. De UV-experimenten werden uitgevoerd in een in-house gebouwde reactor uitgerust met twee Philips PL-S 11W/10/2P UV-lampen. De UV-lampen hebben een golflengte van 350-400 nm en een intensiteit van 1 mW cm −2 . Suspensies voor de fotokatalytische experimenten werden bereid door 100 mg TNT-poeder toe te voegen aan 100 ml 10 mg L −1 MO of RhB waterige oplossingen. Om het adsorptievermogen van de katalysatoren te controleren, werden de dispersies 3 uur onder donkere omstandigheden bewaard. De dispersies werden vervolgens gedurende 3 uur bestraald met UV of natuurlijk zonlicht om de fotokatalytische activiteit te testen. Anatase TiO2 poeder (Sigma-Aldrich, 99,8%) werd als referentiemateriaal gebruikt. Er werden ook blanco tests uitgevoerd om de fotolyse van MO en RhB onder zowel UV als zonlicht te meten. De beginconcentratie (C0 ) van de suspensies werden gemeten voorafgaand aan bestraling bij t = 0, d.w.z. na 3 uur donkere adsorptie. De concentratie (C) van de monsters werd op bepaalde tijdsintervallen gemeten door de katalysator van de kleurstofoplossingen te scheiden door gebruik te maken van 0,45 m nylon spuitfilters en indien nodig te centrifugeren. De verandering in concentratie (C/C0 ) is evenredig met de verandering in absorptie (A/A0 ), waarbij A 0 is de initiële absorptie bij t = 0. De verandering in MO (λ max = 465 nm) en RhB (λ max = 554 nm) wordt de concentratie bestudeerd door de absorptie te registreren met een Hitachi U-5100 UV /Vis-spectrofotometer. De minimale detectielimiet is 1,0 mg L −1 voor MO en 0,1 mg L −1 voor RhB. De experimenten met natuurlijk zonlicht werden uitgevoerd in Espoo, Finland (60°11′01.3″ N 24°49′32.2″ E) op volledig zonnige dagen rond het middaguur in juni-juli 2017.
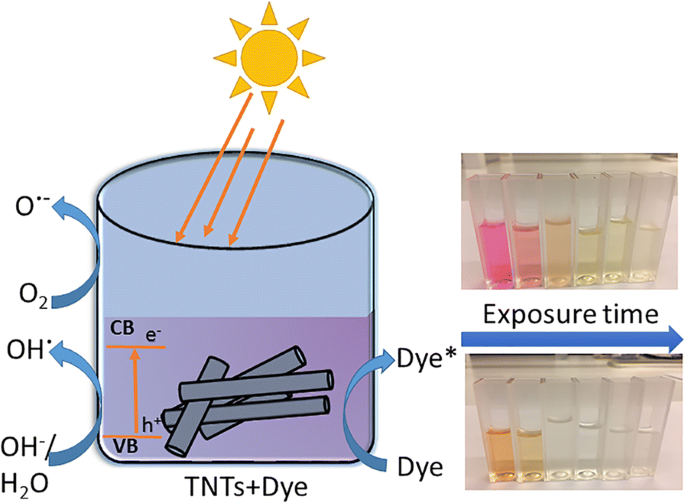
Schematische illustratie van ontkleuring van organische kleurstoffen onder natuurlijke zonnestraling door ongedoteerde TNT's
Resultaten en discussie
Morfologie en structuur
De enkelwandige TNT-bundels worden binnen enkele seconden na het aanleggen van de spanning in het RBA-proces verkregen. Nanobuisjes met een open bovenkant en een gesloten onderkant, de poriegrootte van 11-18 nm en een bundellengte in het bereik van 18-35 μm worden gevormd [11]. Wanneer de nanobuisjes gedurende 3 uur worden uitgegloeid bij 250, 350, 450 en 550 ° C, treden veranderingen in hun morfologie en kristalstructuur op. Deze wijzigingen worden in detail besproken in ref. [11]. In het kort kunnen ze als volgt worden samengevat:wanneer ze worden uitgegloeid, behouden de nanobuisjes hun morfologie tot 250 ° C. Bij hogere temperaturen transformeren de nanobuisjes in nanostaafjes en nanodeeltjes, zoals weergegeven in Fig. 2a-d. Deze transformatie resulteert in de schijnbare afname van het specifieke oppervlak tijdens uitgloeien bij 350 ° C en bij hogere temperaturen, zoals vermeld in tabel 2. De nanostaafmorfologie verkregen bij hogere temperaturen, dwz 350-550 ° C wordt ook getoond in aanvullend bestand 1:Afbeelding S1a–c.

TEM-afbeeldingen van TNT's. een Zoals voorbereide TNT's met één uiteinde open en andere gesloten zoals weergegeven in inzet (figuur inzet schaalbalk = 10 nm), TNT's uitgegloeid bij b 250 °C, c 350 °C (nanorod-transformatie), en d 450 °C
Afbeelding 3 toont de XRD-gegevens van de voorbereide en gegloeide TNT's. De bereide TNT's zijn kristallijn en vertonen diffractiepieken van de anatasefase. Deze resultaten komen goed overeen met de eerdere bevindingen [11, 18, 34]. De anatasefase wordt ook gevonden voor monsters die zijn gegloeid bij 250, 350 en 450 ° C. Bovendien vertonen TNT 450 en TNT 250 ook pieken uit de brookietfase, zoals weergegeven in de inzet van figuur 3. De brookietpiek verdwijnt wanneer het monster wordt uitgegloeid bij 550 °C. TNT 550 vertoont pieken van de anataas- en rutielfase, vergelijkbaar met eerdere bevindingen [11]. Opgemerkt moet worden dat er geen brookietpieken werden gevonden na annealing in een eerdere studie [34], maar Preethi et al. [17] rapporteerde een brookiet/anatase-fasemengsel voor hun bereide TNT's. De aanwezigheid van brookietfase samen met anatase in TNT 450 werd ook bevestigd door de Raman-spectra die worden getoond in aanvullend bestand 1:figuur S2. Raman-gegevens tonen de aanwezigheid van anatasefase in bereide TNT, TNT 250 en TNT 350, vergelijkbaar met eerdere bevindingen [11]. TNT 550 toont de pieken van de rutielfase, die de XRD-resultaten ondersteunt (aanvullend bestand 1:figuur S2). De gewichtspercentages van elke polymorf werden benaderd door de empirische vergelijking voorgesteld door Zhang en Banfield [35]. De voorgestelde formules worden getoond in Vgl. 1a–c onder [16, 35, 36].
$$ {W}_A=\frac{K_A{A}_A}{K_A{A}_A+{A}_R+{K}_B{A}_B} $$ (1a) $$ {W}_R=\frac{ A_R}{K_A{A}_A+{A}_R+{K}_B{A}_B} $$ (1b) $$ {W}_B=\frac{K_B{A}_B}{K_A{A}_A+{A }_R+{K}_B{A}_B}, $$ (1c)waar W A , W B , en W R vertegenwoordigen de gewichtsfracties van anatase, brookiet en rutiel. A A is de intensiteit van de (101) piek van de anatasefase, A B vertegenwoordigt de intensiteit van de brookiet (121), A R vertegenwoordigt de (110) piekintensiteit van de rutielfase, en K A en K B zijn de correctiecoëfficiënten (K A = 0.886 en K B =-2,721) [35, 36]. De resultaten suggereren 64% van de anatasefase en 36% van de brookietfase voor TNT 450 en 34% van de anatase en 66% van de rutielfase voor TNT 550.
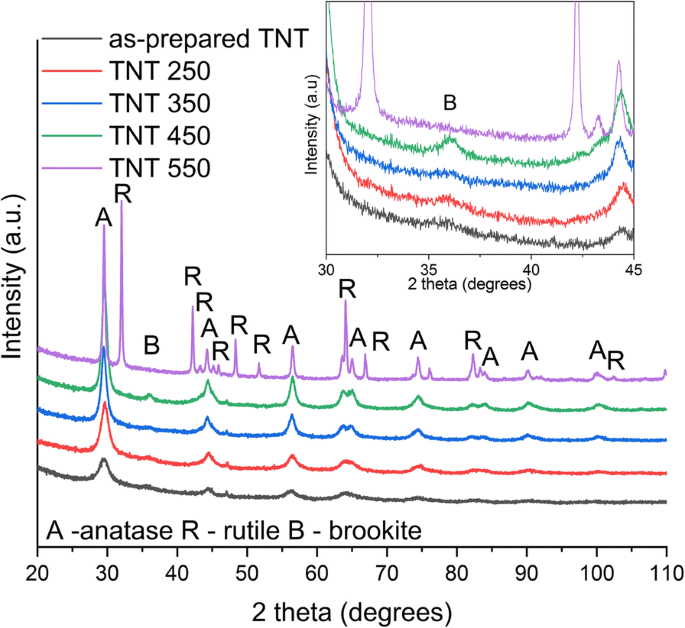
XRD van bereide en gegloeide TNT's met behulp van Co K-alpha-straling
De diffuse reflectie-absorptiespectra van de TNT-monsters worden getoond in figuur 4a. De diffuse reflectiespectra worden gebruikt voor de berekening van bandgap-energie door de Kubelka-Munk-methode toe te passen (figuur 4b). De bandgap van de voorbereide nanobuisjes is ongeveer 3,04 eV (tabel 2). Vergelijkbare bandgap-afmetingen worden gevonden voor de nanobuisjes die zijn gegloeid tot 350 ° C. TNT 450 en TNT 550 hebben een bandgap-energie van 3,14 en 2,88 eV. Een vergelijkbare roodverschuiving naar zichtbaar licht is ook waargenomen voor titanaat-nanobuisjes bij uitgloeien [3]. Deze verschuiving naar het zichtbare lichtbereik wordt toegeschreven aan de verandering in de kristalstructuur van de nanobuisjes bij het uitgloeien, aangezien naast de anataasfase ook de rutielfase werd waargenomen bij 550 °C [11]. De eerder gerapporteerde waarde voor de bandgap van het rutiel is 3,00 eV [2], en de experimentele bevindingen voor de bandgap van de brookietfase liggen in het bereik van 3,1-3,4 eV [37], wat goed overeenkomt met onze resultaten. De bandgap van de zoals voorbereide TNT's en de vernauwing van de bandgap-energieën bij uitgloeien komen ook goed overeen met eerder gepubliceerde resultaten [9, 34]. De bandgap-energie van het referentie-anatasepoeder is 3,18 eV, wat goed overeenkomt met die van bulk-anatase (3,23 eV) [37].
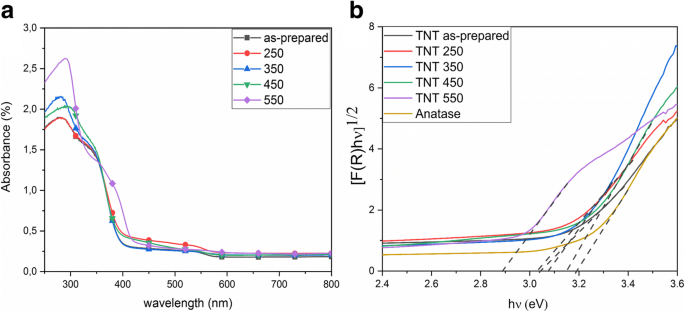
UV /Vis diffuse reflectie a absorptiespectra van bereid en uitgegloeid TNT b Kubelka-Munk-functie voor schatting van de bandgap
De FTIR van de nanobuisjes en het referentie-anatasepoeder wordt getoond in Fig. 5. De prominente O-H-buiging (1620-1640 cm −1 ) en rekbare trillingen (3000-3500 cm −1 ) worden waargenomen voor de voorbereide TNT's, vergelijkbaar met eerdere waarnemingen [11]. De O-H-trillingen worden ook waargenomen voor de gegloeide TNT's, waarvan de intensiteit afneemt met de uitgloeitemperatuur. Voor het referentie-anatasepoeder worden geen hydroxyltrillingen waargenomen. De afname van hydroxylgroepen bij annealing is vergelijkbaar met eerdere resultaten [3, 11]. Opgemerkt moet worden dat de trillingen van 2000 tot 2500 cm − 1 zijn te wijten aan een artefact van de apparatuur.
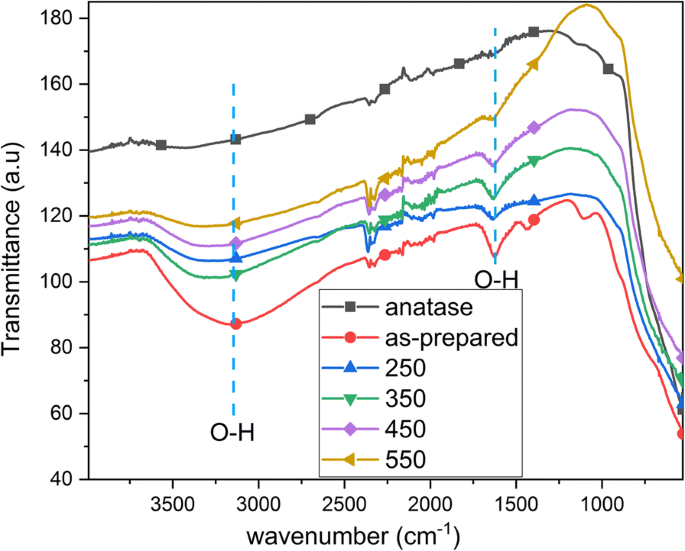
FTIR van bereide TNT's, gegloeide TNT's (250, 350, 450 en 550 °C) en referentie-anatasepoeder
Afbeelding 6 toont de XPS-spectra die zijn verkregen van het TNT-oppervlak. De onderzoeksspectra (Fig. 6a) werden gebruikt om de atomaire percentages van de elementen in het oppervlaktegebied weergegeven in Tabel 1 te berekenen. De relatieve hoeveelheid C wordt niet getoond in Tabel 1. Ti2p-spectra getoond in Fig. 6b tonen de karakteristieke pieken bij 458,9 eV (Ti2p3/2 ) en 464,6 eV (Ti2p1/2 ) van de TNT's die overeenkomen met TiO2 [31, 38,39,40]. De fitting werd verkregen met behulp van 40% Gauss-pieken. Deze pieken worden gevonden voor de TNT's, maar de bindingsenergie op de 2p3/2 piek verschuift geleidelijk 0,4 eV naar beneden wanneer de gloeitemperatuur stijgt. Dit is in overeenstemming met de faseovergang van anatase naar rutiel, aangezien de laatste een iets lagere Ti2p-bindingsenergie heeft [41]. Figuur 6c toont de O1s-spectra van alle monsters met de deconvolutie gemaakt tot het gegloeide monster van 550 ° C met Gaussiaanse / Lorentziaanse (GL) componenten bij de bindingsenergie van 529,8 eV geassocieerd met O-Ti-binding [31, 38, 39, 42 ] en bij 530,9 eV wat gerelateerd is aan de aanwezigheid van een hydroxylgroep met Ti (OH-Ti) [39, 42]. XPS vertoont een sterke aanwezigheid van chloor op het voorbereide TNT-oppervlak. Het spectrum in figuur 6d heeft twee Cl2p-doubletten, één van 198,6 eV (Cl2p3/2 ) en nog een bij 200,1 eV (Cl2p1/2 ) [43,44,45]. Deze pieken zijn ook aanwezig in alle andere monsters, zoals weergegeven in figuur 6d. Chloor is een residu van de elektrolyt en de hoeveelheid neemt af bij uitgloeien. Yang et al. [38] rapporteerde ook de afname van de atomaire concentratie van fluoride-ionen met gloeien voor TNT-arrays bereid in een fluoride-elektrolyt. As-prepared TNT, TNT 250 en TNT 350 hebben een piek bij een bindingsenergie van 208,5 eV (Cl2p3/2 ), gerelateerd aan de ClO4 − ionbinding op het oppervlak van nanobuisjes [46]. De hoge bindingsenergiepieken verdwijnen voor monsters die bij hogere temperaturen zijn gegloeid, zoals in het geval van TNT 450 en TNT 550 (figuur 6d). Tabel 1 toont het atoompercentage van elementen van TNT-oppervlakken en reductie van Cl − van 2,3 tot 0,3% bij gloeien. De verhouding van Ti/O blijft hetzelfde, in tegenstelling tot een eerder rapport [38].
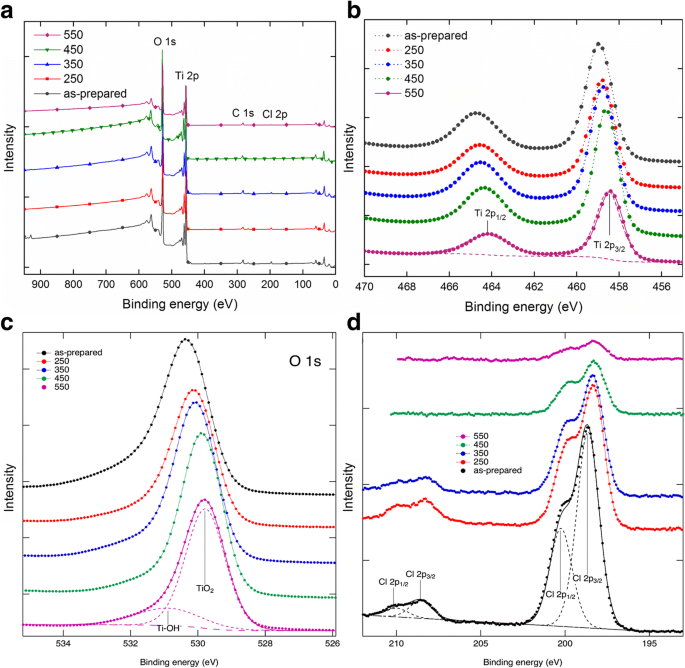
XPS-spectra van TNT a onderzoeksspectra en scans met hoge resolutie van b Ti2p, c O1s en d Cl2p
PL wordt veel gebruikt om de door foto gegenereerde elektronen in fotokatalysatoren te onderzoeken. Afbeelding 7 toont de PL-spectra van de TNT-poedermonsters. Alle TNT-samples, behalve TNT 550, hebben een emissieband gecentreerd op 399 nm (3,11 eV). Alle monsters delen echter het maximale emissiebereik van ongeveer 419 nm (2,96 eV). Deze twee emissiebanden ondersteunen de bandgap-waarden die zijn verkregen uit diffuse reflectiespectra zoals weergegeven in figuur 4. De verschuiving in bandgap wordt ook ondersteund door de kristalstructuurverandering die plaatsvindt in de TNT-monsters, aangezien TNT 550 een gemengde anatase / rutielstructuur heeft, en alle andere TNT-monsters hebben kristalstructuren van ofwel anatase ofwel anatase/brookiet. Antonius et al. vonden een vergelijkbare roodverschuiving in de bandgap voor hun gemengde anataas/rutiel TNT's [34]. De PL-intensiteiten van de band bij ca. 419 nm kunnen in afnemende volgorde worden gezet van TNT > TNT 350 > TNT 250 ≈ TNT 450 > TNT 550. De as-prepared TNT's vertonen een hogere recombinatie in vergelijking met de andere TNT-monsters , waarschijnlijk als gevolg van meer defecten en lagere kristalliniteit van de nanobuisjes. De lagere PL-intensiteit van TNT 250 en TNT 450 in vergelijking met TNT 350 wordt toegeschreven aan de gemengde anatase/brookietstructuur, wat de elektronenoverdracht van anatase naar brookiet bevordert [47]. De intensiteit van TNT 550 suggereert ook een verhoogde ladingsscheiding en een langere levensduur van de elektron-gatparen in vergelijking met de andere TNT-monsters. Antonius et al. [34] rapporteerde ook de laagste PL-intensiteiten voor rutiel/anatase-TNT's. De levensduur van de fotogeïnduceerde ladingsdrager is echter sterk afhankelijk van de verhouding tussen rutiel en anatase [48]. De emissiebanden tussen 468 en 700 nm worden toegeschreven aan de oppervlaktedefecten van TiO2 [17]. De typische defecten in de voorbereide TNT's zijn Ti 3+ locaties, zuurstofvacatures en de gedeeltelijke coördinatie van Ti 4+ [49, 50]. De gedeeltelijke coördinatie van Ti 4+ kan ontstaan door anionische onzuiverheden (Cl − ) afkomstig uit het bereidingsproces [51]. De resultaten verkregen met XPS (Fig. 6) tonen chloorverontreiniging in alle TNT-monsters; de concentratie van de onzuiverheid neemt echter af bij uitgloeien. Deze onzuiverheden dragen ook bij aan de kristaldefecten die recombinatie bevorderen [51]. De emissiebandmaxima rond 445 nm (2,79 eV) en 484 nm (2,56 eV) kunnen worden toegeschreven aan de oppervlaktetoestanden (O-Ti-OH) op het vervormde octaëdrische TiO6 [34]. De emissiebanden rond 539 nm (2,30 eV) [17] en 527 nm (2,36 eV) [52] worden geassocieerd met zuurstofvacatures in de titania-structuur. De emissieband rond 517 nm (2,40 eV) wordt geassocieerd met de Ti 4+ ionen nabij de zuurstofvacatures [53].
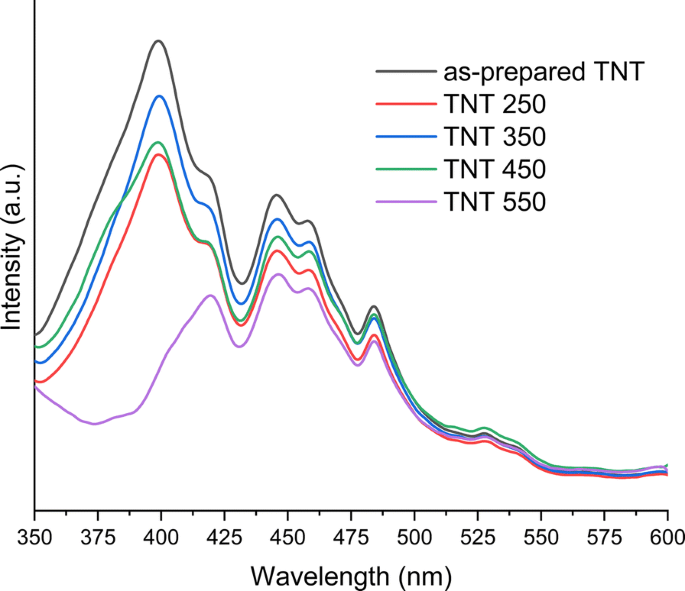
De fotoluminescentie-emissiespectra van bereide en gegloeide TNT's
Figuur 8b toont de karakterisering van het invallende foton naar stroomrendement (IPCE) van de TNT-elektroden bij bestralingsgolflengten van 300-400 nm. De IPCE-waarden worden berekend met de volgende vergelijking
$$ \mathrm{IPCE}\%=\frac{1240\times {J}_{\mathrm{ph}}}{\lambda \times {I}_{\mathrm{light}}} $$ (2)waar J ph is de gemeten fotostroomdichtheid (mA cm −2 ), λ is de invallende bestraalde golflengte en I licht is de intensiteit van de lichtbron (mW cm −2 ) bij een specifieke golflengte (nm). De fotostroom wordt verkregen voor TNT 350, TNT 450 en TNT 550 bij bestraling. De hoogste fotostroom- en IPCE-waarden worden verkregen voor de TNT 450 in het geval van een gemengde anatase/brookietstructuur. Brookiet heeft een 0,14 eV meer negatieve geleidingsband dan anatase, wat bijdraagt aan de elektronenoverdracht van brookiet naar anatase [47, 54]. De IPCE-waarde van TNT 450 (anatase/brookiet) is 1,37 keer hoger dan TNT 350 (anatase) en 3,95 keer hoger dan TNT 550 (anatase/rutiel). TNT 550 (anatase/rutiel) heeft de kleinere fotostroom in vergelijking met TNT 350 (anatase), wat goed overeenkomt met eerdere bevindingen [49, 55]. Eerdere studies tonen aan dat een hoog rutiel/anatase-fasegehalte de fotostroomefficiëntie [56] en fotokatalytische activiteit [57] vermindert. Dit komt goed overeen met onze bevindingen aangezien TNT 550 uit duidelijk meer rutiel dan anataas bestaat. Er kon echter geen fotostroom worden verkregen voor de voorbereide en TNT 250-monsters. De fotostroom wordt beperkt door de in het monster aanwezige trap-toestanden [49,50,51]. Eerdere studies hebben het verschijnen van fotostroom in TNT's gegloeid bij 450 ° C [2, 55, 58] of slechts een kleine fotostroom van de voorbereide TNT-arrays [55] gemeld. In die gevallen waren de voorbereide TNT-arrays echter amorf. Hierin wordt een fotostroom verkregen voor de TNT-monsters die zijn gegloeid bij temperaturen van of boven 350 ° C. De efficiëntie van de fotostroom is over het algemeen lager voor RBA TNT's in vergelijking met goed uitgelijnde TNT-arrays, vanwege de inhomogene verdeling van nanobuisbundels [59]. Het verschil kan het gevolg zijn van de voorbereiding van de elektrode, waardoor mogelijk ethanolresten in de TNT's achterblijven of het gevolg zijn van het gebruik van Nafion om de poeders aan het FTO-glas te hechten. De TNT-elektroden werden gebruikt voor elektrochemische impedantiespectroscopie (EIS), en de resultaten en analyse zijn te vinden in het aanvullende bestand 1:Afbeelding S3.
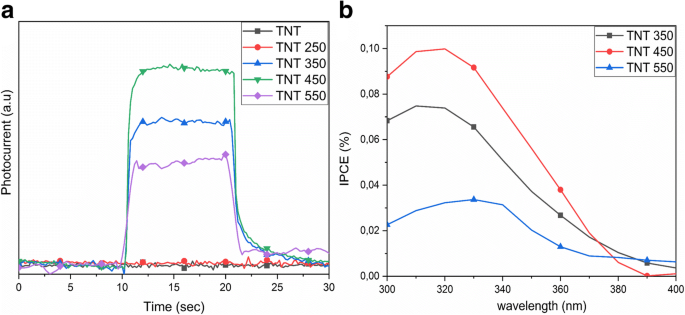
een De fotostroom verkregen bij de stralingsgolflengte van 320 nm. b De IPCE-waarden van de TNT 350, 450 en 550
Fotokatalytische ontkleuring van TNT's
De adsorptie en fotokatalytische prestaties van de TNT-poeders werden geëvalueerd door fotokatalytische ontkleuring van de anionische MO- en kationische RhB-kleurstoffen in waterige oplossing onder UV-licht en natuurlijk zonlicht. Het basismechanisme van fotokatalytische afbraak omvat fotogeneratie van het elektron-gatpaar onder bestraling. Als de bestralingsgolflengte groter is dan de bandgap van het materiaal, worden de elektronen bevorderd van de valentieband naar de geleidingsband, waardoor een elektron-gatpaar ontstaat [26]. Het fotogegenereerde elektron-gatpaar reageert met water om reactieve hydroxyl (OH·) en superoxide radicalen (O· − te vormen) ), die een interactie aangaan met de organische verbinding om ze te ontleden tot CO2 en water [25]. De schematische weergave van het degradatiemechanisme voor een enkele fase wordt voorgesteld in aanvullend bestand 1:figuur S4. The mixed crystal structure of anatase/brookite (TNT 450) and anatase/rutile (TNT 550) with a phase-junction allows the mobility of electrons to flow from brookite to anatase [54] and from rutile to anatase [57]. This allows low electron-hole recombination upon excitation, and a schematic illustration is provided in Additional file 1:Figure S5. The adsorption capacity of the samples was examined prior to irradiation by keeping the samples under dark conditions until adsorption-desorption equilibrium was reached, i.e., within 3 h. The adsorption is shown in Fig. 9 as the time before irradiation begun. The largest adsorption of ca 28% was found for MO on the as-prepared TNT powder. All other samples adsorbed 15% or less of dye for both MO and RhB (Fig. 9).
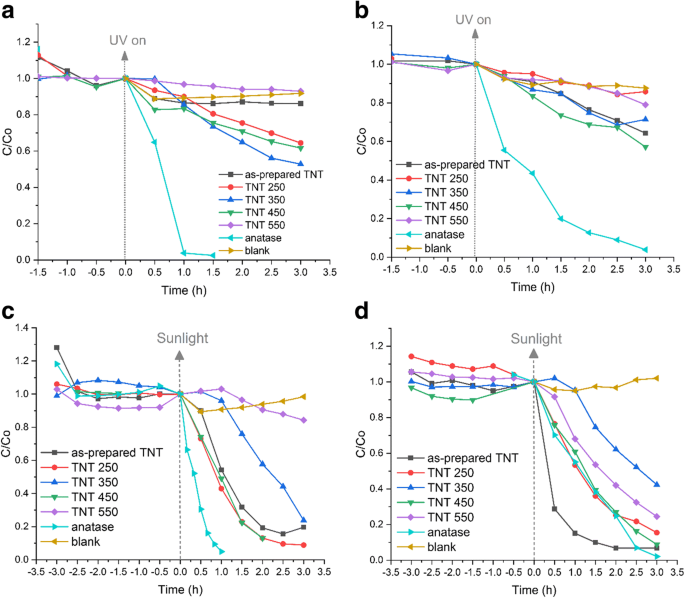
Photocatalytic decolorization of a MO and b RhB under UV light irradiation and c MO, and d RhB under sunlight irradiation for 3 h using the TNT powders
Control experiments (blank tests) were performed for both dyes without a catalyst under UV light and sunlight irradiation. They showed a slight decrease in dye concentration under UV light:RhB concentration decreased by 14% and MO by 8%. The blank tests under sunlight displayed a 2% variation in concentration, which is within the margin of error of the measurement.
Figure 9a–b displays the decolorization of MO and RhB under UV light irradiation. The anatase reference powder decolorized both dye solutions within 3 h, whereas the best TNT powder for MO under UV light was TNT 350 with 47% of MO decolorized. TNT 250 and TNT 450 performed quite similarly with 36 and 38% of MO decolorized, respectively. For RhB, TNT 450 performed most effectively of the TNT powders with 43% of RhB decolorized within 3 h, while the as-prepared TNT powder was next with 36% of RhB decolorized.
The decolorization of MO and RhB under natural sunlight using RBA TNT catalysts are presented in Fig. 9c–d. It is notable that MO was completely decolorized by the as-prepared TNT, TNT 250, and the reference anatase powder within the detection limit of 1.0 mg L −1 . TNT 450 decolorized MO up to 87% in 2 h. The fastest decolorization of RhB was observed using the as-prepared TNT, whereas the decolorization using TNT 250, TNT 450, and anatase reference powder was approximately equal. It is clear that the TNT powders perform significantly better under natural sunlight as compared to UV light.
The data were fitted to the pseudo-first-order kinetic equation, which is expressed as ln(C/C0 ) = −κ 1 t , where κ 1 is the first-order rate constant. By plotting ln(C/C0 ) against time (t ), a straight line of which the slope equals the rate constant is obtained. All the determined rate constants and correlation factors (R 2 ) are given in Table 2, and the fitting is shown in Fig. 10. The highest rate constants are found for the anatase reference powder under UV light, i.e., 2.78 h −1 for MO and 1.05 h −1 for RhB. For the TNT powders, the highest κ 1 is found for TNT 350 (0.24 h −1 ) in MO and for TNT 450 (0.18 h −1 ) in RhB under UV light. The anatase reference powder displayed the highest rate constant at 3.02 h −1 in MO under sunlight, while TNT 450 yielded a κ 1 of 1.05 h −1 under the same conditions. However, the as-prepared TNT in RhB performed better (rate constant of 1.29 h −1 ; R 2 = 0.93) than the reference anatase powder (rate constant of 1.22 h −1 ; R 2 = 0.89). The high photocatalytic activity of reference anatase powder in sunlight is ascribed to the UV light in the natural sunlight spectrum since the results are analogous under both UV and sunlight. The as-prepared TNT and TNT 450 have the two highest decolorization rates of the TNT powders for RhB; TNT 450 has the highest rate under UV light although the difference between the as-prepared TNT (0.15 h −1 ) and TNT 450 (0.18 h −1 ) is negligible. The as-prepared TNTs are the most efficient catalyst for RhB under sunlight.
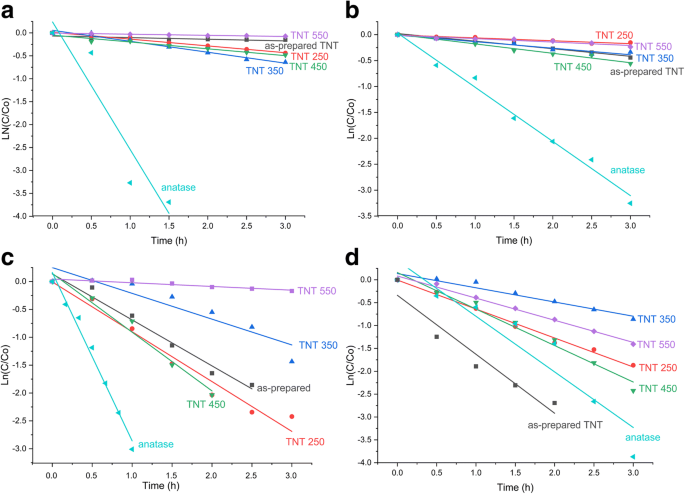
Pseudo-first-order plots of the decolorization of a MO and b RhB under UV light irradiation, and c MO and d RhB under natural sunlight irradiation
The main differences between the as-prepared TNT and TNT 450 powders are in their structure, specific surface area, the atomic concentration of chloride impurity, and electron-hole lifetime. The as-prepared TNTs are tubular consisting of anatase phase with the high specific surface area of 179 m 2 g −1 , while the TNT 450 are rods consisting of anatase and brookite phases with a specific surface area of 70 m 2 g −1 . The PL and IPCE results suggest better conductivity of TNT 450 as compared to as-prepared TNTs. The absorption spectra in Fig. 11 show that there is a clear difference in the photocatalytic mechanism between the as-prepared TNTs under sunlight (Fig. 11a) and UV light irradiation (Fig. 11b). Also, the degradation processes of RhB for TNT 450 (Fig. 11c) are clearly different from as-prepared TNTs. No peak shift (λ max = 554 nm) is observed under UV light, only a decrease in absorbance for the RhB peak. Two types of changes are observed under sunlight:First, the absorbance for RhB decreases, and second, the peak shifts to 498 nm. The peak at 498 nm is identified as Rhodamine, which is an N-de-ethylation product of RhB [60, 61]. N-de-ethylation only takes place under visible light, in this case, the visible light spectrum from the solar light irradiation, due to the excited RhB molecules [62]. The adsorbed and excited RhB molecules then transfer the excited electron to the conduction band of the TNT powder. This step also confirms the degradation of RhB to Rhodamine by N-de-ethylation and further to smaller components [62,63,64]. No other catalyst displayed Rhodamine as an intermediate product during decolorization of RhB. The N-de-ethylation reaction is dependent on the formation of OOH · and OH · , which is suggested to be more prominent in the reaction of the as-prepared TNTs with RhB. The as-prepared TNT carries more –OH functional groups on its surface (Fig. 5) and results in excellent dispersion of the as-prepared powder in the aqueous solution [62]. The N-de-ethylation only takes place on as-prepared TNTs in our case, similar to the study by Guo et al. [65], where they only observed N-de-ethylation on their titanate nanotubes. The justification for this phenomenon may be that nanorods have a lower adsorption capacity associated with the reduction of the specific surface area upon annealing [65]. The decolorization reaction of RhB using TiO2 materials under UV light is different and requires the formation of RhB +· and the presence of air [65]. The mechanism has been widely studied elsewhere [65].
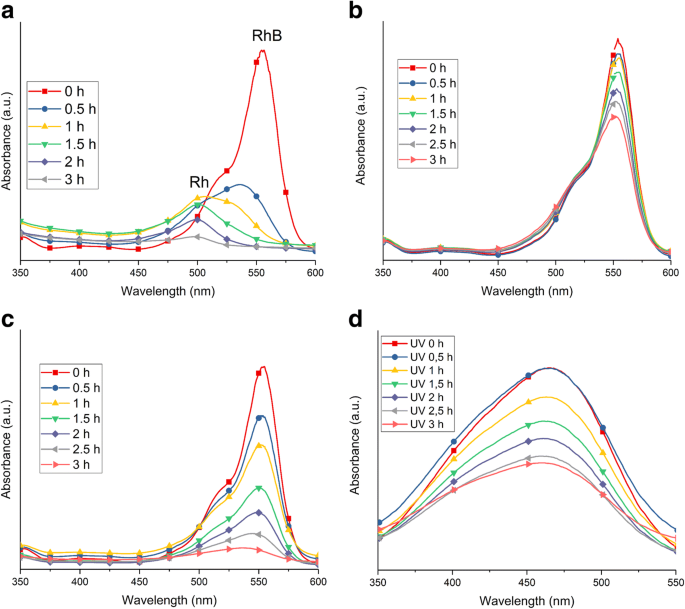
UV-Vis absorbance spectra of the decolorization of RhB using a the as-prepared TNT powder under sunlight, b the as-prepared TNT powder under UV light, c the TNT 450 powder under sunlight and the decolorization of MO by d TNT 350
The photocatalytic decolorization of MO using the TNT powders presents a different trend between the samples of which one has an increased decolorization effect. Under UV light, TNT 350 presented the most prominent kinetic rate of 0.24 h −1 , whereas for sunlight, the most prominent rate was found for TNT 450 with 1.05 h −1 ; however, the TiO2 anatase reference powder was superior in both cases. Despite the comparatively small specific surface area, TNT 450 with the mixed crystal structure (anatase/brookite) exhibited the best photocatalytic efficiency of the prepared TNTs. This is attributed to the improved electron-hole separation, apparent from high photocurrent obtained from TNT 450 in Fig. 8. This result is consistent with published reports [37, 47]. The adsorption spectra from the MO show only the decrease in absorbance with irradiation time (Fig. 11d). No blueshift is observed for the decolorization of MO for any TNT catalyst, suggesting the damage to the conjugated system made up of azo groups and aryl rings of MO dye [65].
Titanate nanotubes with different morphology and crystal structure have been tested under simulated solar light and have reached almost complete degradation of MO and RhB [65]. RBA TNT powders as photocatalysts have been investigated under UV light using MO [20] and acid orange 7 (AO7) dye [21]. Liao et al. [20] reported a reaction rate of 0.082 min −1 (4.92 h −1 ) which is significantly higher than the rates obtained in this study under UV light. However, it is noteworthy that the post-treatment destroyed the tubular structure of the TNTs into particles (Liao et al. [20]). Hahn et al. [21] reported decolorization rates for doped TNT layers up to 0.469 h −1 (undoped TiO2 0.385 h −1 ) using AO7 as a model dye under UV light irradiation. It is crucial to use a catalyst that can utilize the extended sunlight spectrum for efficient degradation of pollutants. RBA TNT powders prepared under different washing conditions and annealed at 500 °C, with a pure rutile phase have been reported as an efficient photocatalyst for RhB degradation under visible light illumination [33]. In the present report, the study of photocatalytic properties of TNT powders prepared by RBA is extended from UV to visible light range under sunlight irradiation, contrary to the general perception of titania only being active under UV light.
Conclusies
The TNT powders were prepared by rapid breakdown anodization. By annealing the TNT powders at 250–550 °C, the bandgap narrowed from 3.04 eV down to 2.88 eV, and the tubes transformed from anatase phase to anatase/brookite and further to anatase/rutile phase mixtures. The tubes transformed to nanorods at 350 °C, reducing the specific surface area from 179 to 35 m 2 g −1 . The XPS results show the characteristic peaks of Ti2p and O1s and Cl2p in all TNTs; however, the atomic concentration of chlorine decreases upon annealing. The PL results for TNT 250 and TNT 450 suggest lower electron-hole recombination as compared to as-prepared TNT and TNT 350. The higher recombination in the as-prepared TNTs is attributed to the low crystallinity and the number of surface defects. The photocatalytic activity of the TNT powders was investigated by decolorization of MO and RhB dyes under UV and natural sunlight. The photocatalytic decolorization of both dyes improved under natural sunlight, contradicting the general perception of titania nanotubes being inefficient photocatalysts under visible light irradiation. The as-prepared TNTs, TNT 250, and TNT 450 performed the best of the TNT powder samples under natural sunlight using RhB and MO as model pollutants, whereas the as-prepared TNT powder outperformed the reference TiO2 anatase powder when using RhB as a model pollutant. This could be attributed to the higher specific surface area and different photocatalytic degradation mechanism of RhB on the as-prepared TNT. TNT 250 and TNT 450 displayed similar activity under sunlight irradiation, which is ascribed to the large surface area and reaction sites for TNT 250. The specific surface area is reduced for TNT 450, and the better photocatalytic activity is attributed to a favorable crystal structure and less electron-hole recombination. In addition, the highest IPCE values are obtained for TNT 450. These RBA TNTs may intensify the use of the natural sunlight spectrum for removal of organic contaminants from polluted waters.
Afkortingen
- DRS:
-
Diffuse reflectance spectroscopy
- EIS:
-
Elektrochemische impedantiespectroscopie
- FTIR:
-
Fourier-transformatie infraroodspectroscopie
- FTO:
-
Met fluor gedoteerd tinoxide
- IPCE:
-
Incident photon to current efficiency
- MO:
-
Methylsinaasappel
- PL:
-
Fotoluminescentie
- RBA:
-
Rapid breakdown anodization
- RhB:
-
Rhodamine B
- SEM:
-
Scanning elektronenmicroscopie
- TEM:
-
Transmissie-elektronenmicroscopie
- TNTs:
-
Titania nanotubes
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- XRD:
-
Röntgendiffractie
Nanomaterialen
- Nano-heterojuncties voor zonnecellen
- Demonstratie van een flexibele op grafeen gebaseerde biosensor voor gevoelige en snelle detectie van eierstokkankercellen
- Vergelijking van metallische elektroden van het nanogat-type en nanopillar-type die zijn opgenomen in organische zonnecellen
- Een efficiënt en effectief ontwerp van InP-nanodraden voor maximale oogst van zonne-energie
- Fotokatalytische activiteit van attapulgiet–TiO2–Ag3PO4 ternair nanocomposiet voor afbraak van Rhodamine B onder gesimuleerde zonnestraling
- Effect van morfologie en kristalstructuur op de thermische geleidbaarheid van Titania-nanobuisjes
- Ontwerpprincipes voor nanodeeltjesplasmon-versterkte organische zonnecellen
- Effectieve lichtabsorptie met behulp van de dubbelzijdige piramideroosters voor dunne-film silicium zonnecel
- Een recensie over de elektrochemisch zelfgeorganiseerde Titania nanobuisarrays:synthese, modificaties en biomedische toepassingen
- Invloed van Mg-doping op ZnO-nanodeeltjes voor verbeterde fotokatalytische evaluatie en antibacteriële analyse
- Een nieuwe nanocone-clustermicrostructuur met antireflectie en superhydrofobe eigenschappen voor fotovoltaïsche apparaten



