Vervaardiging en karakterisering van nieuwe composiet Tio2 koolstof nanovezel anodische katalysatorondersteuning voor directe methanolbrandstofcel via elektrospinmethode
Abstract
Platina (Pt) is de gebruikelijke katalysator die wordt gebruikt in een directe methanolbrandstofcel (DMFC). Pt kan echter leiden tot katalysatorvergiftiging door koolstofhoudende soorten, waardoor de prestatie van DMFC wordt verminderd. Deze studie richt zich dus op de fabricage van een nieuwe composiet TiO2 koolstof nanovezel anodische katalysatorondersteuning voor directe methanolbrandstofcellen (DMFC's) via elektrospintechniek. De afstand tussen de punt en de collector (DTC) en de stroomsnelheid werden onderzocht als beïnvloedende parameters in de elektrospintechniek. Om ervoor te zorgen dat het beste katalytische materiaal wordt vervaardigd, onderging de nanovezel verschillende karakteriseringen en elektrochemische tests, waaronder FTIR, XRD, FESEM, TEM en cyclische voltammetrie. De resultaten laten zien dat D18, vervaardigd met een stroomsnelheid van 0,1 mLhr −1 en DTC van 18 cm, is een ultrafijne nanovezel met de kleinste gemiddelde diameter, 136,73 ± 39,56 nm. Het presenteerde de hoogste katalysatoractiviteit en elektrochemische actieve oppervlaktewaarde als 274,72 mAmg −1 en 226,75 m 2 g −1 PtRu , respectievelijk, vergeleken met de andere monsters.
Achtergrond
Directe methanol brandstofcel (DMFC) is een van de toekomstige hernieuwbare energieopwekkingssystemen en zeer milieuvriendelijk. Het systeem wekt direct elektrische energie op met behulp van een vloeibare brandstof (methanol) zonder extra apparaten of verbrandingsprocessen. De voordelen van DMFC's zijn hun eenvoud, hoge specifieke energie, lage bedrijfstemperatuur en eenvoudig opstarten met direct bijtanken [1]. DMFC-systemen hebben echter nog steeds te kampen met verschillende beperkingen, zoals katalysatorvergiftiging en langzame reactiekinetiek, wat ertoe leidt dat het systeem lage prestaties en een laag vermogen heeft [2]. Beide beperkingen zijn te wijten aan de katalysator en het materiaal dat in dit systeem wordt gebruikt.
Platina (Pt) is de gebruikelijke katalysator die wordt gebruikt in DMFC. Pt kan echter leiden tot katalysatorvergiftiging door koolstofhoudende soorten, waardoor de prestatie van DMFC wordt verminderd. Later wordt platina-ruthenium (PtRu) geïntroduceerd om de reactiesnelheid te verhogen, maar de kinetische parameter van de katalysator is nog steeds een van de grootste problemen bij DMFC. Daarom begint de verandering naar deze bimetaalkatalysator op het gebied van DMFC-katalysator te worden geplaatst. Een van de meest aantrekkelijke benaderingen onder onderzoekers is de introductie van metaaloxide en nanomaterialen als de zijkatalysatorcomponent. Titaandioxide (TiO2 ) is een metaaloxide dat veel aandacht krijgt van onderzoeksontwikkelaars. TiO2 heeft verschillende gunstige eigenschappen, die niet-toxisch, niet-ontvlambaar en zeer goed bestand zijn tegen corrosie [1], de elektrochemische en thermische stabiliteit [3] kunnen verhogen en de elektronische eigenschappen en het bifunctionele mechanisme van composietkatalysatoren kunnen beïnvloeden [4]. Ito et al. [5] ontwikkelde PtRu/TiO2 -embedded koolstof nanovezel (CNF) (PtRu/TECNF), en Ercelik et al. [6] presenteerde de PtRu/C-TiO2 als elektrokatalysator in DMFC-toepassingen, en het resultaat toont aan dat de prestaties van deze nieuwe samengestelde elektrokatalysator hoger zijn dan die van PtRu-katalysator.
Nanomateriaal is een van de nanotechnologieën die fascineerde in een breed scala aan toepassingen, waaronder energieconversie. Er zijn talloze soorten nanomaterialen op het gebied van energieconversie, namelijk nanovezels, nanobuisjes, nanodraden, nanostaafjes en andere. Dit materiaal wordt de belangrijkste attractie in onderzoek naar energiemateriaal vanwege de dimensionale reductie tot op nanometerschaal die veel elementaire stappen kan beïnvloeden, waaronder ladingsoverdracht en moleculaire herschikking, evenals de oppervlakte-eigenschappen om hoge grensvlakvolumefracties en verbeterde reactiesnelheden te bieden [ 7]. Deze studie richt zich op nanovezelstructuren voor beide materialen, TiO2 metaaloxide en koolstof. Dit komt door de speciale eigenschappen van nanovezels die hoge oppervlakte/volume- en aspectverhoudingen [7], hoge elektrische geleidbaarheid, goede mechanische sterkte en uniforme dispersie van katalysator kunnen bieden, wat de elektrokatalytische activiteit kan verhogen [8].
Nanovezels kunnen worden geproduceerd door verschillende processen, waaronder smeltblazen, grensvlakpolymerisatie, elektrospinning en door anti-oplosmiddel geïnduceerde polymeerprecipitatie [9]. Onlangs is elektrospinnen de belangrijkste keuze van onderzoekers vanwege het grote voordeel van het produceren van ultrafijne nanovezelstructuren. Electrospinning is een uniek proces voor de vorming van vezels met submicron-schaal diameters (in het nanometer tot micrometer bereik) met behulp van op polymeer gebaseerde oplossingen of smelten door elektrostatische krachten [10]. Er zijn drie hoofdcomponenten voor electrospinning:een hoogspanningsvoeding (enkele tientallen kV's), de spindop (spuit met een naald) en een geaarde collector (bijvoorbeeld plaat of roterende collector) [11, 12]. Afbeelding 1 illustreert het algehele proces en de instelling voor het elektrospinproces. Daarom is elektrospinnen populair vanwege de eenvoudige procedure, veelzijdigheid, hoge opbrengst, effectief en met een zuiniger proces [7, 13].
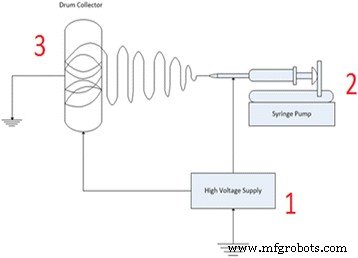
Electrospinning ingesteld voor alle hoofdcomponenten
Dit proces heeft verschillende parameters die kunnen worden afgestemd om de optimale nanovezelstructuren te verkrijgen, hetzij voor diameter of oppervlaktemorfologie, en de beïnvloedende parameters zijn voor elk materiaal verschillend. De parameters kunnen worden onderverdeeld in drie hoofdcategorieën:oplossings-, omgevings- en procesparameters. Deze studie is gericht op procesparameters en de stroomsnelheid van de oplossing en de afstand tussen de naaldpunt en de collector (DTC) werden gekozen als de belangrijkste beïnvloedende parameters om de kleinste diameter te verkrijgen. Dit komt door de kleine hoeveelheid onderzoek die op deze parameters is gericht [14], hoewel ze zijn beschouwd als de belangrijkste variabelen voor het verkrijgen van ultrafijne nanovezels [15,16,17,18].
Deze studie presenteert dus de samengestelde TiO2 koolstof nanovezel als katalysatordrager op de anode-elektrode. Deze combinatie van het composiet zal naar verwachting de elektrokatalytische activiteit verhogen en de katalysatorvergiftiging verlagen om de algehele prestaties van DMFC te verbeteren. De belangrijkste doelstellingen van deze studie zijn om de kleinst mogelijke nanovezeldiameter te fabriceren om het oppervlak te vergroten en een actievere plek te bieden voor katalytische reactie en de DMFC-prestaties te verbeteren. De fabricage van nanovezels omvat verschillende stappen, waaronder sol-gel-, elektrospinning-, stabilisatie- en carbonisatieprocessen. Om de nanovezels met de kleinste diameter te verkrijgen, worden de elektrospinparameters van stroomsnelheid en DTC als de belangrijkste variabelen in deze studie genomen. De bereide nanovezels worden gekenmerkt door Fourier-transformatie-infraroodspectroscopie (FTIR), röntgendiffractie (XRD) en scanning-elektronenmicroscopie (FESEM). Alle katalysatordragers met verschillende elektrospinparameters worden afgezet op PtRu (PtRu/TiO2 -CNF) en geëvalueerd door elektrochemische actieve oppervlakte (ECSA) analyse en cyclische voltammetrie (CV) om de prestaties te evalueren en hun potentieel als katalysatordragers in DMFC's te bepalen. De experimentele resultaten tonen het effect van de elektrospinning-parameters op de diameter van de nanovezels, evenals hun potentieel in DMFC-toepassingen.
Methoden/experimenteel
Materialen
Poly(vinylacetaat) (PVAc, Mw = 500.000), dimethylformamide (DMF, 99,8%), titaniumisopropoxide (TiPP, 97% inhoud), azijnzuur (99,7%) en Ru-precursor (45-55% inhoud) werden verkregen van Sigma-Aldrich Co., Ltd., terwijl Pt-precursor (40% gehalte) en ethanol (99,8%) werden ontvangen van respectievelijk Merck, Duitsland en R&M Chemical Reagents. Alle chemicaliën werden gebruikt zonder enige verdere zuivering. Het belangrijkste apparaat, de elektrospinmachine, is gemerkt met Nfiber N1000, Progene Link Sdn. Bhd., en ultrasone celbreker INS-650Y is van INS Equipments Trading Co., Ltd., China.
Voorbereiding van TiO2 -CNF-nanovezels
De sol-gel-methode begint met de bereiding van een polymeeroplossing, waarbij PVAc (11,5 gew.%) als koolstofbron werd opgelost in het oplosmiddel, DMF. De polymeeroplossing werd 1 uur bij 60°C geroerd en daarna een nacht bij kamertemperatuur geroerd. De TiO2 voorloper, TiPP en polymeeroplossing werden gemengd in een verhouding van 1:1 en een kleine hoeveelheid azijnzuur en ethanol werd aan de polymeeroplossing toegevoegd. Het mengsel werd gedurende 60 s gehomogeniseerd door een ultrasone celbreker. Vervolgens werd de oplossing overgebracht naar een injectiespuit voor injectie in een elektrospin-eenheid van nanovezels. De aangelegde spanning was 16 kV, terwijl de stroomsnelheid en DTC werden gemanipuleerd in het bereik van 0,1–0,9 mLh −1 en 14-18 cm. De stroomsnelheid was ingesteld op 0,1, 0,5 , en 0,9 mLh −1 , respectievelijk aangeduid met F0.1, F0.5 en F0.9. De monsters met DTC-waarden van 14, 16 en 18 cm worden respectievelijk aangeduid met D14, D16 en D18. De gefabriceerde nanovezel werd 5 uur bij kamertemperatuur laten rusten voordat hij 8 uur bij 130 ° C werd gestabiliseerd. De gestabiliseerde nanovezel werd gedurende 2 uur onder een stikstofatmosfeer gecarboniseerd bij 600 ° C met behulp van een buisoven en vervolgens gedurende 5 minuten met een mortier en een stamper verpletterd voor verder gebruik in dit onderzoek. De massalading voor alle monsters is hetzelfde, namelijk 6,67 mgs −1 .
Depositie van katalysator
De TiO2 -CNF-nanovezels werden toegevoegd aan een mengsel van isopropylalcohol (IPA) en gedeïoniseerd water (DI-water) en gedurende 20 minuten in een ultrasoon bad gesoniceerd. De voorloper van de platina- en rutheniumkatalysator (20 gew.% met een verhouding van 1:1) werd in de oplossing gemengd en 20 minuten geroerd. Vervolgens werd de pH van de gemengde oplossing aangepast met NaOH-oplossing tot pH 8 werd bereikt. De temperatuur werd verhoogd tot 80 °C en 25 ml 0,2 M NaBH4 werd druppelsgewijs toegevoegd aan de gemengde oplossing. De oplossing werd nog 1 uur geroerd. Het mengsel werd vervolgens afgekoeld, gefiltreerd en herhaaldelijk gewassen. Het katalysatorpoeder werd 3 uur bij 120 °C gedroogd en tenslotte verpulverd met een vijzel en stamper om een fijn katalysatorpoeder te verkrijgen dat klaar was voor gebruik in de prestatietests.
Karakterisering van de katalysator
De chemische verbinding in de katalysatordrager werd geïdentificeerd met behulp van Fourier-transformatie-infraroodspectroscopie (FTIR, PerkinElmer) en röntgendiffractie (XRD, D8 Advance / Bruker AXS, Duitsland) werd gebruikt om het patroon en de kristalstructuur van de monsters te analyseren. De morfologie en grootteverdeling van de monsters werden geanalyseerd met veldemissie scanning elektronenmicroscopie (FESEM, SUPRA 55VP). Transmissie-elektronenmicroscopie (TEM, Tecnai G2 F20 X-Twin) werd gebruikt om de gedetailleerde structuur en elementaire verdeling van de nanovezels te observeren.
Evaluatie van de elektrochemische meting
De prestatie werd gemeten voor alle katalysatoren die met verschillende parameters waren vervaardigd. De PtRu-katalysator werd afgezet op de TiO2 -CNF-katalysatorondersteuning voor evaluatie door elektrochemische metingen. Deze metingen werden verkregen met behulp van een celsysteem met drie elektroden, dat cyclische voltammetrie (CV) gebruikt om de katalysatoractiviteit in de methanoloxidatiereactie (MOR) te onderzoeken met behulp van een elektrochemisch werkstation van Autolab. Het celsysteem met drie elektroden werd bij kamertemperatuur gebruikt en omvatte een Pt, zilver / zilverchloride (Ag / AgCl) en glasachtige koolstofelektrode (GCE, 3 mm diameter) als de tegen-, referentie- en werkelektrode. Voordat de meting werd gestart, werd de GCE schoongemaakt met aluminiumoxide en polijstpapier, waarbij meerdere keren een afgerond patroon werd gevolgd dat leek op het cijfer "acht". Vervolgens werd de GCE vóór gebruik gespoeld met DI-water en gedurende 30 seconden gesoniceerd. De katalysatorinkt voor de GCE werd bereid door 15 mg katalysator te dispergeren in een mengsel van 400 μl DI-water, 400 μl IPA en 125 μl Nafion-oplossing (5 gew.%) gedurende 30 minuten. Vervolgens werd 2,5 μl katalysatorinkt met een micropipet op de GCE gecoat en gedurende 1 uur bij kamertemperatuur gedroogd voordat het nog eens 30 minuten op 80 ° C werd verwarmd. De elektrolyt was een oplossing van 0,5 M H2 SO4 in 2 M methanol, en er werd gedurende 20 minuten met stikstofgas geborreld om alle zuurstof te verwijderen. De CV-meting werd uitgevoerd over een potentieel bereik van − 0,1–1,1 V vs. Ag/AgCl bij een scansnelheid van 50 mVs −1 .
Resultaten en discussie
Structurele karakterisering
Effect van stroomsnelheid
FTIR-spectroscopie werd uitgevoerd op de TiO2 -CNF-monsters om de aanwezige chemische verbindingen te identificeren. De IR-spectra van de monsters geproduceerd met verschillende stroomsnelheden worden getoond in Fig. 2. De spectra onthulden chemische bindingssignalen die representatief zijn voor TiO2 en koolstof. De gemiddelde en brede pieken bij 3200-3600 cm −1 vertegenwoordigen OH-functionele groepen, terwijl de scherpe en sterke C=O-absorptieband zich in het gebied van 1550-1850 cm −1 bevond [19]. Pieken voor alkanen (C-H-groepen) zijn zwak en breed en bevinden zich in de regio's van 1300-1450 cm −1 . C-C-groepen verschijnen echter zogenaamd bij zeer lage golfgetallen, lager dan 500 cm −1 [19] en bestaan niet in de spectra vanwege het kleine bereik van het golfgetal (4000 cm −1 < wavenumber > 50 cm −1 ) produceren door het spectrum. De middelgrote en scherpe banden in het gebied van 650-900 cm −1 behoren tot Ti-O-groepen, zoals gesuggereerd door Ding et al. [20]. De IR-spectra bevatten alle functionele groepen in de TiO2 -CNF-monsters. Alle monsters hebben vergelijkbare golfgetallen en pieken, wat aangeeft dat de stroomsnelheid van de polymeeroplossing tijdens elektrospinnen geen invloed heeft op de chemische verbindingen in het monster.
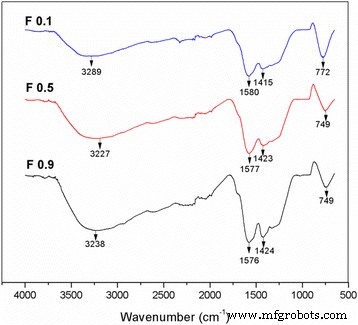
De IR-spectra voor de TiO2 -CNF-monster met verschillende stroomsnelheidsparameters in het bereik van 650 tot 4000 cm −1 golfnummer
De TiO2 -CNF-monsters vervaardigd met stroomsnelheden van 0,1, 0,5 , en 0,9 mlh −1 worden respectievelijk aangeduid met F0.1, F0.5 en F0.9. Afbeelding 3 toont de XRD-patronen van de TiO2 -CNF-katalysatordragers vervaardigd met verschillende stroomsnelheden. Figuur 3a is een individueel monster voor de katalysatordrager, een F0.1-monster, om het close-up XRD-patroon te bekijken met al het piekmateriaal in TiO2 -CNF, terwijl Fig. 3b het volledige monster van de stroomsnelheid is. Het bestaan van TiO2 en koolstof in het monster is te zien. De TiO2 bestaat uit twee structuren, anatase en rutiel, omdat de carbonisatietemperatuur een kleine hoeveelheid anatase TiO2 omzet in rutiel TiO2 . De diffractiepieken voor anatase TiO2 zijn 25° (101), 38° (112), 48° (200), 53,9° (105), 62° (213) en 68° (116), terwijl die voor rutiel, TiO2 zijn 27° (110), 36° (101), 41° (111) en 54° (211). De koolstofbron wordt aangegeven door verschillende diffractiepieken, waaronder die bij 30° (110) en 55° (211). De anataas en rutiel TiO2 vormde een tetragonale structuur, terwijl koolstof zich in de vlakgecentreerde kubische kristallografische structuur bevond.
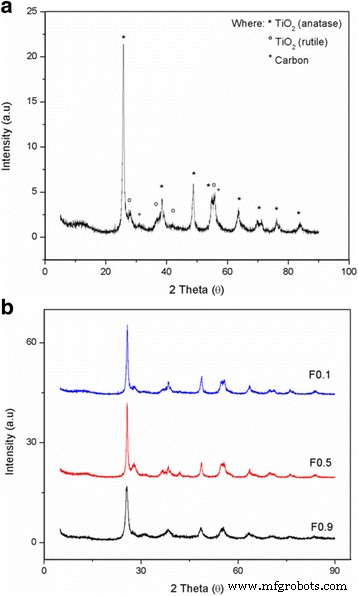
Röntgendiffractiepatronen van a individuele TiO2 -CNF-voorbeeld en b ander debiet monster
De stroomsnelheid in de elektrospintechniek bleek de nanovezeldiameter te beïnvloeden, die werd berekend met behulp van FESEM-analyse. Het FESEM-beeld wordt weergegeven in figuur 4, terwijl de resultaten van de grootteverdeling en diameter worden getoond in figuur 5 en tabel 1. Het beeld bevestigt dat de nanovezelstructuur werd gevormd bij alle bestudeerde stroomsnelheden. De F0.1-nanovezels vertoonden een gladde morfologie vanwege de langzamere stroomsnelheid, die voldoende tijd geeft voor het oplosmiddel om te verdampen, wat helpt om de gladde structuur te produceren. De gemiddelde nanovezeldiameter van 100 metingen is 161,18 ± 26,08 nm, wat de kleinste diameter is van de monsters die met verschillende stroomsnelheden zijn geproduceerd. Het FESEM-beeld van F0.5 toont echter de vorming van platte linten op de nanovezels vanwege het gebrek aan verdamping van de kern, dwz het oplosmiddel wordt in de kern opgesloten en diffundeert naar de omgevingsatmosfeer om de platte lintstructuur te veroorzaken [ 21]. F0.9 toont meer ruwe nanovezels met niet-uniforme diameters en verschillende kralen gevormd op de nanovezelmorfologie. Dit gebeurt wanneer het debiet veel hoger is dan de optimale waarde, waardoor de droogtijd voordat de vezel de collector bereikt, wordt verkort. De gemiddelde nanovezeldiameters van F0.5 en F0.9 waren hoger dan die van F0.1, die respectievelijk 220,28 ± 38,01 en 286,33 ± 50,83 nm waren. Het FESEM-beeld laat zien dat de diameter van de nanovezels toeneemt naarmate de stroomsnelheid toeneemt tijdens elektrospinnen. F0.1, met een stroomsnelheid van 0,1 mLhr −1 , werd gebruikt voor verdere analyse van het effect van DTC op de nanovezeldiameter.

FESEM-afbeelding van a TiO2 -CNF (F0.1), b TiO2 -CNF (F0.5), en c TiO2 -CNF (F0.9) bij × 30.000 vergroting
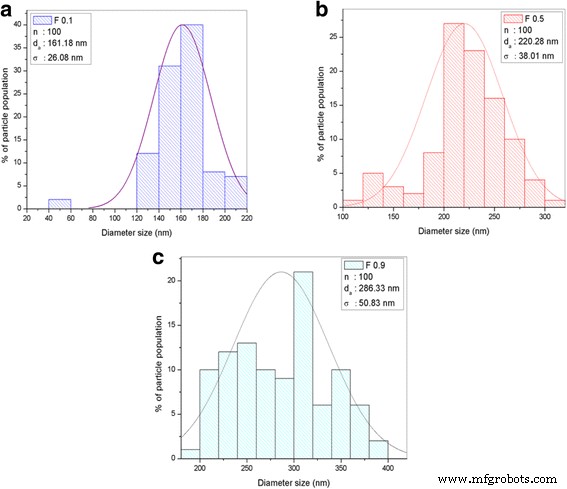
Histogramgegevens van diametergrootteverdeling met de parameter n, da , en . een TiO2 -CNF (F0.1). b TiO2 -CNF (F0.5). c TiO2 -CNF (F0.9)
Effect van de afstand tussen de punt en de collector
De gesynthetiseerde TiO2 -CNF-katalysatordragers werden geanalyseerd door FTIR om de chemische binding in de monsters te evalueren, en de IR-spectra van de monsters zijn geïllustreerd in Fig. 6. De IR-spectra tonen drie monsters met verschillende DTC-parameters na het carbonisatieproces. Alle gesynthetiseerde monsters tonen het bestaan van O-Ti-O- en carbonaationbindingen, waarbij de pieken en golfgetallen in de spectra in hetzelfde bereik lagen als die in de F0.1-, F0.5- en F0.9-monsters in de vorige paragraaf. De golfgetallen lagen dicht genoeg bij elkaar om de gelijkenis van de monsters aan te geven, inclusief de monsters geproduceerd bij verschillende stroomsnelheden in Fig. 2. Monster D14 vertoont echter een bestaan van een nieuwe piek rond 2300-2400 cm −1 , die de N-H strektrillingen aangeven. Deze piek kan worden gecategoriseerd als een piek van tertiaire aminezouten, waar de NH-binding zwak is en geen praktische waarde heeft die kan worden verwaarloosd [19]. De aanwezigheid van deze binding kan te wijten zijn aan de onvolledige verwijdering van de oplosmiddelverbinding tijdens het carbonisatieproces. Deze waarneming laat zien dat de elektrospinparameters van stroomsnelheid en DTC de chemische binding in de monsters niet beïnvloeden.
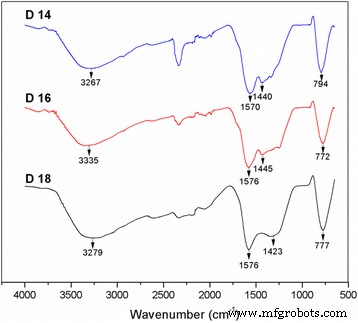
Het IR-spectrum voor de TiO2 -CNF-monster met verschillende DTC-parameter in het bereik van 650 tot 4000 cm −1 golfnummer
De kristalliniteit van de TiO2 -CNF-katalysatordragers werden geanalyseerd. De XRD-patronen worden getoond in Fig. 7a voor individuele monsters en Fig. 7b voor DTC. Het individuele monster in Fig. 7a geeft het close-up XRD-patroon voor DTC 18 aan om de bestaanspiek voor al het betrokken materiaal te zien. De materialen die betrokken zijn bij de katalysatordrager, TiO2 en koolstof, blijken in elk monster aanwezig te zijn. De diffractiepieken werden onderzocht over een bereik van 2θ van 5° tot 90°, en de pieken bij 31° (110) en 55° (211) geven aan dat koolstof met een FCC-kristallografische structuur aanwezig is in de katalysatordrager. De scherpe diffractiepiek bij 25° (101) werd toegeschreven aan TiO2 in anatasevorm, en er zijn verschillende andere pieken voor anatase TiO2 , inclusief die op 38° (004), 48° (200), 53° (105), 55° (211), 63° (204) en 69° (116). De andere vier diffractiepieken bij 27° (110), 36° (101), 41° (111) en 54° (211) behoren tot rutiel TiO2 . Zowel anataas als rutiel TiO2 een tetragonale kristallografische structuur hebben.
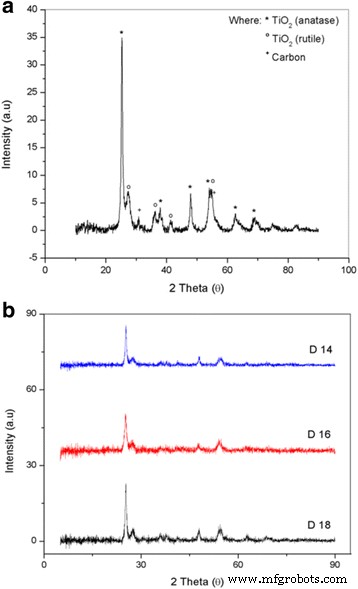
Röntgendiffractiepatronen van a individuele TiO2 -CNF-voorbeeld en b ander DTC-voorbeeld
TiO2 -CNF-nanovezels werden vervaardigd via elektrospinning met verschillende DTC-waarden, aangeduid als D14, D16 en D18. De DTC werd gevarieerd naar 14, 16 en 18 cm. De diameter van de nanovezel werd berekend met behulp van FESEM-analyse. Afbeelding 8 toont de FESEM-afbeeldingen van de monsters met verschillende DTC-waarden bij een vergroting van × 30.000. Het effect van de variatie in DTC op de diameter van de nanovezels werd geschat met behulp van de deeltjesgrootteverdeling (diameter), zoals geïllustreerd in Fig. 9, en de waarden zijn getabelleerd in Tabel 2. De diameterverdeling omvat verschillende parameters, n (nanodeeltjes bevolking), da (rekenkundig gemiddelde deeltjesgrootte), en σ (standaarddeviatie) [22].

FESEM-afbeelding van a TiO2 -CNF (D14), b TiO2 -CNF (D16), en c TiO2 -CNF (D18) bij een vergroting van × 30.000
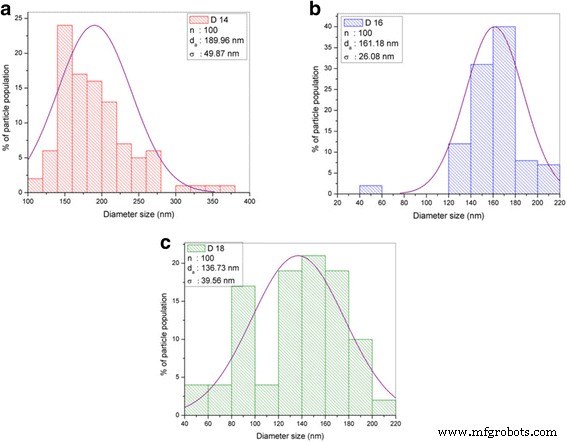
Histogramgegevens van diametergrootteverdeling met de parameter n, da , en . een TiO2 -CNF (D14). b TiO2 -CNF (D16). c TiO2 -CNF (D18)
De kleinste gemiddelde diameter was 136,73 ± 39,56 nm (90-170 nm), behorend tot D18, gevolgd door D16 en D14 met diameters van respectievelijk 161,18 ± 26,08 en 189,96 ± 49,87 nm. Hoe langer de afstand tussen de punt en de collector, hoe kleiner de diameter van de nanovezels. Dit gedrag is te wijten aan de afzettingstijd en het instabiliteitsinterval van de zweep tijdens het elektrospinproces. De langere afstand zorgt voor een langere depositietijd en gedurende die periode treedt het fenomeen zweepinstabiliteit op, ook bekend als het uitdunnings- en splijtmechanisme. Dit fenomeen treedt op als gevolg van interacties tussen geladen ionen en het elektrische veld [17]. Wanneer de elektrische kracht die op de punt van het mondstuk wordt uitgeoefend een kritieke waarde bereikt, splitsen de sterk geladen dichtheid en de visco-elastische kracht de jets in kleinere jets, waardoor een buigend, kronkelend en spiraalvormig pad naar de collector ontstaat. Wanneer de DTC langer is, treedt herhaaldelijk straalsplitsing op, wat resulteert in ultrafijne vezels met een kleinere diameter. Daarom behoort de kleinste diameter tot monster D18 met een stroomsnelheid van 0,1 mlh −1 en DTC van 18.
De diameter van gefabriceerde nanovezels, TiO2 -CNF, wordt vergeleken met de vorige studie van de diameter van nanovezels voor TiO2 -gebaseerde nanovezels, en deze vergelijking wordt weergegeven in Tabel 3. De resultaten laten zien dat de TiO2 -CNF heeft de kleinste nanovezeldiameter met 136,73 ± 39,56 nm. Dit komt door de optimale parameter die wordt gebruikt tijdens de elektrospinmethode; die laag is in stroomsnelheid en hoge waarde van DTC. Dus, met een kleinere stroomsnelheid en een hogere DTC-waarde, wordt de kleinere diameter van een nanovezel geproduceerd. Dit toont aan dat de elektrospinparameters het grootste effect hebben op de diameter van nanovezel. Hoewel een langere DTC en een kleiner debiet de voorkeur hebben, zijn er optimale waarden voor deze parameters, omdat deze parameters kunnen leiden tot gewichtsverlies. Dit gebeurt door oververdamping, waarbij de nanovezel zich vormt voordat deze de collector bereikt, waardoor de nanovezel vrijelijk naar ongewenste gebieden kan reizen.
Het D18-monster met een stroomsnelheid van 0,1 mlh −1 en DTC van 18 werd geselecteerd voor TEM-analyse om de morfologie te onderzoeken en de diametergrootte te verkrijgen. Het TEM-beeld en elementaire mapping van de TiO2 -CNF-katalysatorondersteuning wordt getoond in Fig. 10. De TEM-afbeelding laat zien dat TiO2 -CNF resulteert in gladde en zijdeachtige nanovezels met een diameter van 135,38 nm. De diameter ligt in hetzelfde bereik (90-170 nm) als die verkregen uit FESEM-analyse. Mapping wordt gebruikt om de distributie van TiO2 . te onderzoeken en koolstof op nanovezel. De resultaten weerspiegelen dat TiO2 en koolstof uniform gevormd in de nanovezelstructuur, dankzij de homogene verdeling van de polymeeroplossing en de TiO2 voorloper tijdens de sol-gel methode. Deze mapping toont ook de locatie van de materialen, waarin TiO2 en koolstof bevinden zich langs het gehele nanovezeloppervlak, wat de vorming van actieve reactiegebieden tijdens katalyse ten goede komt. De andere nanovezelmonsters hebben naar verwachting dezelfde gelijkmatige verdeling van TiO2 en koolstof. De deeltjesgrootte van TiO2 en koolstof in de nanovezelmonsters en hun effect op MOR wordt besproken in de volgende sectie.

TiO2 -CNF-katalysatorondersteuning a TEM-afbeelding (schaal 100 nm), b TEM-afbeelding voor TiO2 en C nanovezel mapping, c mapping voor C nanovezel, en d mapping voor TiO2 nanovezel
Elektrochemische karakterisering van de methanoloxidatiereactie
Elektrochemische karakterisering omvat drie hoofdstappen, namelijk karakterisering van de elektrochemische activiteit, de elektrokatalytische prestatie en de stabiliteit en duurzaamheid op lange termijn. De elektrochemische activiteit en elektrokatalytische prestaties werden geanalyseerd door CV met behulp van een systeem met drie elektroden om kwalitatieve en kwantitatieve informatie over de betrokken reactie te verkrijgen [23]. Afbeelding 11a, b toont het TEM-beeld van de PtRu-katalysator die is afgezet op het oppervlak van de F0.1 en D18 TiO2 -CNF ondersteunt, respectievelijk. De PtRu-katalysator was gelijkmatig verdeeld over het oppervlak van nanovezels in zowel F0.1 als D18. Afbeelding 11c toont het XRD-patroon van D18 PtRu/TiO2 -CNF, terwijl Tabel 4 de gegevens geeft voor de nanovezeldiameter, verkregen uit FESEM, en kristallietgrootte van de deeltjes in de monsters, verkregen uit XRD. Tabel 4 laat zien dat de monsters uit de F-serie (F0.1, F0.5 en F0.9) met toegevoegde katalysator een TiO2 hebben (anatase) kristallietgrootte van ongeveer 20 tot 22 nm. De verandering in nanovezeldiameter heeft weinig effect op de kristallietgrootte van TiO2 , terwijl de kristallietgrootte van koolstof verandert naarmate de diameter van de nanovezel toeneemt van 15,9 nm in F0.1 tot 25,8 nm in F0.9. De kristallietgrootte van Pt heeft ook de neiging toe te nemen met de koolstofkristallietgrootte. De kristallietgrootte van Pt ondersteund op F0.1, F0.5 en F0.9 is respectievelijk 5,67, 8,04 en 9,75 nm. De veranderingen in de grootte van het Pt-kristalliet zijn te wijten aan de oppervlakte-eigenschappen van de nanovezel. Tabel 4 toont ook de kristallietgrootte van PtRu die wordt ondersteund op monsters uit de D-serie. De diameter van de nanovezel neemt in waarde af van D14 naar D16 naar D18. In tegenstelling tot de monsters uit de F-serie, is de kristallietgrootte van TiO2 (anatase) in de monsters van de D-serie neemt af naarmate de diameter van de nanovezels afneemt. De TiO2 kristallietgrootte is 23,40, 21,50 en 18,60 nm voor respectievelijk D14, D16 en D18. De kristallietgrootte van koolstof en Pt neemt ook af met een afname van de diameter van de nanovezel. De grootte van het koolstofkristalliet neemt af van 17,3 nm in D14 tot 14,4 nm in D18, terwijl de grootte van het Pt-kristalliet op D14, D16 en D18 respectievelijk 5,44, 5,67 en 4,64 nm is. Uit deze gegevens blijkt dat de veranderingen in de kristallietgroottes van TiO2 en koolstof in de nanovezel leiden tot veranderingen in de oppervlakte-eigenschappen van de nanovezel, wat leidt tot de veranderingen in de kristallietgrootte van de Pt-deeltjes die op het oppervlak van de nanovezel worden afgezet.
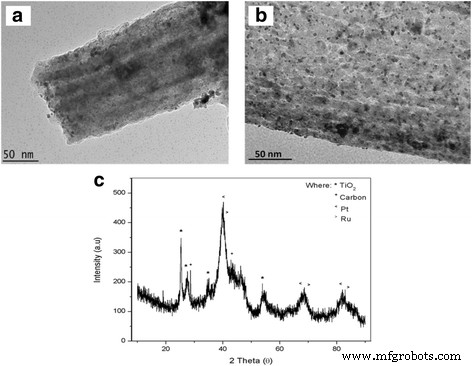
Afbeelding van PtRu gedeponeerd op TiO2 -CNF a TEM-afbeelding van PtRu/TiO2 -CNF in F0.1, b TEM-afbeelding van PtRu/TiO2 -CNF in D18, en c XRD-patroon van PtRu/TiO2 -CNF van D18
Afbeelding 12 toont de CV-profielen van de PtRu/TiO2 -CNF-elektrokatalysatoren met verschillende katalysatordragers in 0,5 M H2 SO4 oplossing. De CV-curve voor F0.1, F0.5 en F0.9 worden getoond in Fig. 12a, terwijl D14, D16 en D18 worden getoond in Fig. 12b. Waterstofadsorptie-desorptie door Pt vindt plaats rond -0,2 tot 0,1 V vs. Ag/AgCl. De massabelasting voor alle elektrokatalysatoren in dit profiel is gelijk aan 0,57 mgcm −2 . De PtRu/TiO2 -CNF supported on D18 exhibits a steep current peak for hydrogen adsorption in comparison in the other D series samples, while F0.1 has a steep peak in comparison with the F series samples. The peak indicates that the active surface area on the PtRu/TiO2 -CNF electrocatalyst and the ECSA can be calculated from the equation:ECSA = Q /(Γ .W Pt ). Where, Q is the integral of the hydrogen adsorption area, Γ is the constant for the charge required to reduce the proton monolayer on the Pt (2.1 CmPt −2 ), and W Pt is the mass loading of Pt. Table 5 shows the ECSA of all the catalyst samples in units of m 2 g −1 with mass loadings according to the mass of PtRu. From Table 5, the ECSA for PtRu supported on F0.1, F0.5, and F0.9 is 131.29, 65.05, and 25.03 m 2 g −1 , respectievelijk. The ECSA value decreases with increasing Pt crystallite size in the catalyst samples. The catalyst supported on D14, D16, and D18 has an ECSA value of 21.48, 131.29, and 226.75 m 2 g −1 , respectievelijk. As shown previously, the value of the Pt crystallite size in the D series samples decreases from D14 to D18, and thus, the ECSA increases according to Pt crystallite size. Smaller size particles lead to an increase in the active surface area of the catalyst. Overall, the electrospinning parameters clearly show big influence towards the diameter and surface properties (surface morphology) of nanofibers.
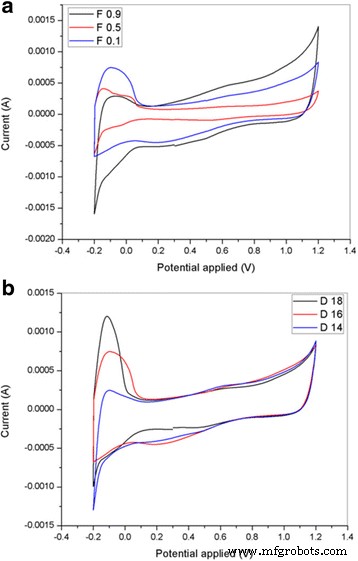
Cyclic voltammetry profiles of the PtRu/TiO2 -CNF with a different flow rate, F0.1, F0.5, F0.9, and b different DTC, D14, D16, and D18, in 0.5 M H2 SO4 solution at the scan rate of 50 mVs −1
The electrocatalytic performance of PtRu supported on the different F and D series nanofibers is tabulated and plotted in Table 5 and Fig. 13. The CV curve was measured in 2 M methanol and 0.5 M H2 SO4 solution saturated with N2 gas at room temperature. The mass loading for all the electrocatalyst is the same which is 0.57 mgcm −2 . Figure 13 shows multiple CV curves over a potential range of − 0.1 to 1.1 V vs. Ag/AgCl. Figure 13a shows the CV graphs for PtRu supported on the F series nanofiber samples. As the diameter of the nanofiber decreases from sample F0.9 to F0.1, the current density in MOR increases, and the oxidation peak and onset potential of MOR shift towards positive values. On the other hand, in the D series nanofiber samples, the oxidation peak potential of the catalyst supported on D14, D16, and D18 is 0.754, 0.771, and 0.732 V (vs. Ag/AgCl), respectively. There is no pattern in the oxidation peak potential in the D series samples, and the onset potential is almost the same for each sample, at 0.36 V vs. Ag/AgCl. However, the peak current density at the oxidation peak potential of MOR increases in accordance to the catalyst support on D14, D16, and D18. The peak current density for D14, D16, and D18 is 201.45, 249.58, and 274.72 mAmg −1 PtRu , respectievelijk. It can be clearly seen that the increase in the current density matches the patterns in the diameter, from FESEM analysis, and ECSA value. This shows that a smaller diameter size produces high surface area and increases the number of active sites on the electrocatalyst surface. The higher peak current for the composite electrocatalyst may result from the supporting material (TiO2 -CNF), where changes in the structure and the combination of materials can be very effective in producing positive effects on the metal-support interaction [5, 24].
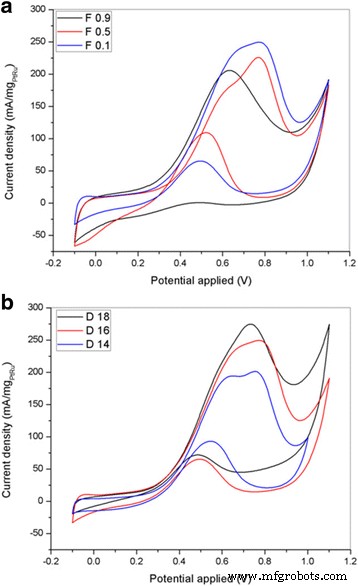
Cyclic voltammograms for PtRu/TiO2 -CNF with different a flow rate and b DTC of the catalyst support in 2 M methanol and 0.5 M H2 SO4 at the scan rate of 50 mVs −1
The reverse scan in the CV curve shows a small oxidation peak at a potential of approximately 0.49–0.55 V vs. Ag/AgCl. This second oxidation peak appeared due to the incomplete removal of oxidized carbonaceous species in the forward scan [25]. However, the ratio between the forward (If ) and reversed (Ib ) oxidation peak for PtRu/TiO2 -CNF (D18) exceeded 3.8, which means that the electrocatalyst has high tolerance towards carbonaceous species, reducing the potential for catalyst poisoning. This result shows that the combination of metal oxide and carbon nanofibers has a good potential for use in fuel cell applications.
Conclusion
TiO2 -CNF nanofibers can be fabricated via electrospinning, which is the main technique, and several other methods. The nanofibers are influenced by the flow rate and the DTC, which were examined as electrospinning process parameters, with three different samples for each parameter, denoted F0.1, F0.5, F0.9, D14, D16, and D18. The results showed that the TiO2 -CNF (D18) sample produced the smallest average diameter of 136.73 ± 39.56 nm. TiO2 -CNF was mixed with PtRu to form the composite catalyst, and its CV performance was examined. The current density of the PtRu/TiO2 -CNF (D18) sample is 1.4 times higher than that of PtRu/TiO2 -CNF (D14), while the ECSA of PtRu/TiO2 -CNF (D18) is 10 times higher than that of the other samples. Thus, the flow rate and DTC highly affect the diameter, morphology, and performance of the nanofibers. The nanofiber performance increased with decreasing nanofiber diameter, which shows the capability of the composite nanofiber catalyst to be an upcoming anode catalyst for DMFCs.
Nanomaterialen
- Vervaardigingsmethode voor kunstmatige moleculen wint prijs voor beste poster
- Grafeen- en polymeercomposieten voor toepassingen met supercondensatoren:een recensie
- Ontwerpen van nette en samengestelde koolstofnanobuisjes door middel van porosimetrische karakterisering
- Verbeterde prestaties van een nieuwe anodische PdAu/VGCNF-katalysator voor elektro-oxidatie in een glycerolbrandstofcel
- Vervaardiging, karakterisering en cytotoxiciteit van sferisch gevormde geconjugeerde van goudkokkelschil afgeleide calciumcarbonaat nanodeeltjes voor biomedische toepassingen
- Polyaniline-gecoate actieve kool aerogel/zwavelcomposiet voor hoogwaardige lithium-zwavelbatterij
- Vervaardiging en karakterisering van ZnO-nanoclips door het door polyol gemedieerde proces
- Nieuwe Anodic Catalyst Support voor Direct Methanol Fuel Cell:Karakteriseringen en Single-Cell Performances
- Een gemakkelijke methode voor het laden van CeO2-nanodeeltjes op anodische TiO2-nanobuisarrays
- Platinum-gebaseerde katalysatoren op verschillende koolstofdragers en geleidende polymeren voor directe methanol-brandstofceltoepassingen:een overzicht
- Nanogestructureerde Pd-gebaseerde elektrokatalysator en membraanelektrode-assemblagegedrag in een passieve directe glycerol-brandstofcel



